Aeromonas hydrophila, Streptococcus agalactiae
DAN JAMUR Saprolegnia sp.
SKRIPSI
DEWI ROMA WIDYA 090302025
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
Aeromonas hydrophila, Streptococcus agalactiae
DAN JAMUR Saprolegnia sp.
SKRIPSI
DEWI ROMA WIDYA
Skripsi sebagai satu diantara beberapa syarat untuk dapat memperoleh gelar Sarjana Perikanan di Program Studi Manajemen Sumberdaya Perairan
Fakultas Pertanian Universitas Sumatera Utara
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
pubescens L) Terhadap Bakteri Aeromonas hydrophila, Streptococcus agalactiae dan Jamur
Saprolegnia sp.
Nama : Dewi Roma Widya
Nim : 090302025
Program Studi : Manajemen Sumberdaya Perairan
Disetujui Oleh
Komisi Pembimbing
Prof. Dr. Dwi Suryanto, M. Sc Desrita, S.Pi, M.Si
Ketua Anggota
Mengetahui
Dr. Ir. Yunasfi, M. Si
Ketua Program Studi Manajemen Sumberdaya Perairan
Dengan ini saya menyatakan bahwa skripsi yang berjudul:
Aktivitas Antimikroba Ekstrak Biji Teratai (Nymphaea pubescens L.) Terhadap Bakteri Aeromonas hydrophila, Streptococcus agalactiae dan Jamur Saprolegnia sp.
Adalah benar merupakan hasil karya saya sendiri dan belum diajukan dalam
bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan
informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak
diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam
Daftar Pustaka di bagian akhir skripsi ini.
Medan, Desesmber 2013
ABSTRAK
DEWI ROMA WIDYA. Aktivitas Antimikroba Biji Teratai (Nymphaea pubescens L.) Terhadap Bakteri Aeromonas hydrophila, Streptococcus agalactiae
dan Jamur Saprolegnia sp. Dibimbing oleh DWI SURYANTO dan DESRITA.
Penanggulangan penyakit pada ikan yang biasanya menggunakan zat kimia atau antibiotik dapat menimbulkan resistensi. Penanggulangan secara alami dengan memanfaatkan ekstrak tanaman merupakan salah satu alternatif. Penelitian ini
bertujuan untuk menguji aktivitas antimikroba ekstrak biji teratai (Nymphaea pubescens L.) terhadap bakteri dan jamur penyebab penyakit pada
ikan. Biji teratai diekstrak dengan pelarut yang berbeda yaitu n-heksana, etil asetat dan metanol. Pengujian aktivitas antimikroba dilakukan dengan metode difusi cakram, untuk mengetahui senyawa yang terkandung di dalam ekstrak dilakukan uji fitokimia. Untuk mengetahui tingkat toksisitas ekstrak menggunakan metode
Brine Shrimp Lethality Test. Ekstrak biji teratai dapat menghambat pertumbuhan bakteri Aeromonas hydrophila, Streptococcus agalactiae dan jamur Saprolegnia
sp. dengan besar zona hambat yang berbeda. Zona hambat pertumbuhan mikroba terbesar terdapat pada bakteri S. agalactiae sebesar 10,72 mm. Ekstrak yang memiliki aktivitas antimikroba optimal dihasilkan dengan menggunakan pelarut n-heksana. Ekstrak biji teratai memiliki toksisitas dengan nilai LC50<1000 µg/ml. Analisis senyawa kimia menunjukkan dalam ekstrak biji teratai mengandung alkaloid, fenolik, glikosida, saponin dan steroid/terpenoid.
Kata kunci: Aktivitas antimikroba, mikroba patogen, Nymphaea pubescens L.
DEWI ROMA WIDYA. Activity of Lotus Seeds (Nymphaea pubescens L.) on
Aeromonas hydrophila, Streptococcus agalactiae Bacteria and Saprolegnia sp. Fungi. Under the Supervision of DWI SURYANTO and DESRITA.
Disease prevention in fish using chemicals or antibiotics lead to microbial resistance. One of alternative to control the fish disease is to use plant extract. The aim of this study was to investigate the antimicrobial activity of lotus seeds (Nymphaea pubescens L.) on pathogenic bacteria and fungi in fish. The lotus seed was extracted with several solvent, such as n-hexsana, etil asetat and methanol. Testing of antimicrobial activity carried out by disc diffusion method, to determine the compounds contained in the extract phytochemical test. To determine the level of toxicity of the extract using the Brine Shrimp Lethality Test. The extracts inhibitated the growth of Aeromonas hydrophila, Streptococcus agalactiae bacteria and Saprolegnia sp. fungi to some extent. Largest microbial growth inhibition zone of bacteria present in S. agalactiae by 10.72 mm.The optimal antimicrobial activity was obtained from n-heksana. The extract showed cytotoxic activity with LC50<1000 µg/ml. The chemical compound analysis showed that extract of lotus seed contains alkaloid, fenolik, glikosida, saponin and steroid/terpenoid.
Penulis lahir di kota Padang Sidimpuan, Provinsi
Sumatera Utara pada tanggal 26 September 1991 dari
ayahanda Drs. H. Torkis Harahap, MM dan Ibunda Hj.
Daimmah Nasution. Penulis merupakan anak ketiga dari
enam bersaudara.
Penulis menyelesaikan pendidikan di SMA
Negeri 1 Padang Sidimpuan dengan jurusan IPA tahun
2009. Penulis melanjutkan pendidikan di Program Studi Manajemen Sumberdaya
Perairan, Fakultas Pertanian, Universitas Sumatra Utara melalui jalur ujian tertulis
Seleksi Penerimaan Mahasiswa Baru Program Studi Baru.
Penulis melaksanakan magang di Unit Pelayanan Teknis (UPT) Budidaya
Ikan, Dinas Perikanan dan Kelautan Kota Medan dan Praktek Kerja Lapangan
(PKL) di PT. Pantai Samudra Indonesia, Kabupaten Tapanuli Tengah, Provinsi
Sumatera Utara.
Selain mengikuti perkuliahan penulis juga menjadi asisten laboratorium
Dasar Ilmu Perairan tahun 2011-2012, Biologi Perairan tahun 2010-2011, Sistem
Informasi Sumberdaya Perairan tahun 2011 dan Hama dan Penyakit Ikan tahun
Puji syukur penulis ucapkan kehadirat Allah SWT karena atas rahmat,
hidayah, serta karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang
berjudul ”Aktivitas Antimikroba Ekstrak Biji Teratai (Nymphaea pubescens L.) Terhadap Bakteri Aeromonas hydrophila, Streptococcus agalactiae dan Jamur
Saprolegnia sp.”
Penulis mengucapkan terima kasih yang sebesar-besarnya dan
penghargaan yang setinggi-tingginya kepada ayahanda Drs. H. Torkis Harahap,
MM dan Ibunda Hj. Daimmah Nasution yang selalu memberi motivasi dan
dukungan sehingga penulis dapat menyelesaikan skripsi ini. Penulis juga
mengucapkan terimakasih kepada kakanda Afriani Melda Dewi, ST., Afreri,
Purnama Dewi SP. dan adinda Marito Aisyah Dewi, Iqbal Rajamin dan Hasna
Dewi.
Ucapan terimakasih juga penulis sampaikan kepada Bapak Prof. Dr. Dwi
Suryanto, M.Sc selaku Ketua Komisi Pembimbing dan kepada Ibu Desrita, S.Pi,
M.Si selaku anggota Komisi Pembimbing, yang telah banyak memberikan arahan
dan masukan dalam penyelesaian skripsi ini.
Penulis juga mengucapkan terimakasih kepada Bapak Dr. Ir. Yunasfi,
M. Si dan Pindi Patana, S.Hut, M.Sc selaku Ketua dan Sekretaris Program Studi
Manajemen Sumberdaya Perairan. Seluruf staf pengajar dan pegawai di Program
Studi Manajemen Sumberdaya Perairan. Bapak Lamek Marpaung, M.Phil, Ph.D
kepala Laboratorium Kimia Bahan Alam Hayati Fakultas MIPA Universitas
(UPT) Budidaya Ikan, Dinas Perikanan dan Kelautan Kota Medan. Ibu Ied
Parinduri S.Si dan seluruh staf pegawai di Stasiun Karantina Ikan Pengendalian
Mutu dan Keamanan Hasil Perikanan Kelas I Medan II.
Terimakasih kepada Muhammad Rizky, Rahmad Hidayat, Ghanang Dhika
Aria, Wan Nita Ulfani Barus S.Pi, Arief Baizuri Majid, Aznia Marlina Sima,
Dedi Pradana, Deliana Dongoran, Sharah Dina, Fathul Khoiri, Fitria Ismy, Hapiz
Fahrezi, Hafiz Muhammad, Nanda Muthia Hardianti, Nina Safriyanti, Popy
Aprilia, Reza Alnanda S.Pi., Rika Wirani, Rina Sari Lubis S.Pi., Yudha Perdana
Putra, dan seluruh teman-teman seperjuangan di angkatan 2009 Program Studi
Manajemen Sumberdaya Perairan yang telah banyak membantu penulis dalam
menyelesaikan skripsi ini.
Penulis berharap semoga skripsi ini bermanfaat dalam pengembangan ilmu
pengetahuan khususnya dalam bidang manajemen sumberdaya perairan.
Halaman
Kerangka Pemikiran Penelitian ... 3
Tujuan Penelitian ... 4
Manfaat Penelitian ... 4
Hipotesis Penelitian ... 5
TINJAUAN PUSTAKA Teratai (Nymphaea pubescens L.) ... 6
Bakteri Aeromonas hydrophila ... 7
Bakteri Streptococcus sp. ... 9
Jamur Saprolegnia sp. ... 10
Senyawa Antimikroba ... 12
Senyawa Fitokomia ... 13
Ekstraksi ... 16
Uji Brine Shrimp Lathality ... 17
Kemampuan Beberapa Tanaman Sebagai Antimikroba ... 18
METODE PENELEITIAN Waktu dan Tempat ... 20
Alat dan Bahan ... 20
Pelaksanaan Penelitian Pembuatan Ekstrak Biji Teratai ... 21
Uji Fitokimia ... 22
Uji Toksisitas ... 25
HASIL DAN PEMBAHASAN
Hasil Penelitian
Ekstraksi Biji Teratai... 30
Uji Fitokimia Biji Teratai ... 30
Uji Toksisitas Biji Teratai ... 31
Uji Antimikroba Ekstrak Biji Teratai ... 32
Pembahasan Ekstraksi Biji Teratai... 34
Uji Fitokimia Biji Teratai ... 34
Uji Toksisitas Biji Teratai ... 36
Uji Antimikroba Ekstrak Biji Teratai ... 41
KESIMPULAN DAN SARAN Kesimpulan ... 48
Saran ... 48
No. Halaman
1. Bagan Alur Penelitian ... ... 4
2. Teratai (Nymphaea pubescens L.) ... ... 6
3. Aeromonas hydrophila... ... 8
4. Streptococcus agalactiae ... 10
5. Saprolegnia sp... ... 11
6. Pola Media Uji... ... 26
7. Perhitungan Zona Hambat... 27
8. Zona Hambat Bakteri Aeromonas hydrophila ... 31
9. Zona Hambat Bakteri Streptococcus agalactiae ... 32
No. Halaman
1. Komposisi Kimia Tepung Biji Teratai ... ... 7
2. Hasil Ekstrak Pekat Biji Teratai ... 29
3. Hasil Uji Fitokimia Ekstrak Biji Teratai ... 29
4. Hasil Pengukuran LC50 dengan Metode BSLT ... 30
No. Halaman
1. Sterilisasi Alat dan Bahan ... 55
2. Pembuatan Ekstrak Biji Teratai ... 56
3. Proses Pengujian Toksisitas A. salina ... 57
4. Pembuatan Konsentrasi Larutan Uji ... 59
5. Pembuatan Media Bakteri dan Jamur ... 60
6. Analisis Kriteria Bakteri Aeromonas hydrophila... ... 61
7. Analisis Kriteria Bakteri Streptococcus agalactiae... ... 62
8. Analisis Kriteria Jamur Saprolegnia sp. ... 63
9. Pembuatan Larutan Baku McFarland ... 64
10.Proses Pengujian Antimikroba ... 65
11.Hasil Skrining Fitokimia Biji Teratai ... 69
12.Data Awal Kematian A. salina pada Berbagai Konsentrasi ... 72
13.Contoh Perhitungan Penentuan LC50 Ekstrak Biji Teratai ... 73
14.Data Awal Zona Hambat Ekstrak Biji Teratai ... 79
15.Tabel Probit ... 81
ABSTRAK
DEWI ROMA WIDYA. Aktivitas Antimikroba Biji Teratai (Nymphaea pubescens L.) Terhadap Bakteri Aeromonas hydrophila, Streptococcus agalactiae
dan Jamur Saprolegnia sp. Dibimbing oleh DWI SURYANTO dan DESRITA.
Penanggulangan penyakit pada ikan yang biasanya menggunakan zat kimia atau antibiotik dapat menimbulkan resistensi. Penanggulangan secara alami dengan memanfaatkan ekstrak tanaman merupakan salah satu alternatif. Penelitian ini
bertujuan untuk menguji aktivitas antimikroba ekstrak biji teratai (Nymphaea pubescens L.) terhadap bakteri dan jamur penyebab penyakit pada
ikan. Biji teratai diekstrak dengan pelarut yang berbeda yaitu n-heksana, etil asetat dan metanol. Pengujian aktivitas antimikroba dilakukan dengan metode difusi cakram, untuk mengetahui senyawa yang terkandung di dalam ekstrak dilakukan uji fitokimia. Untuk mengetahui tingkat toksisitas ekstrak menggunakan metode
Brine Shrimp Lethality Test. Ekstrak biji teratai dapat menghambat pertumbuhan bakteri Aeromonas hydrophila, Streptococcus agalactiae dan jamur Saprolegnia
sp. dengan besar zona hambat yang berbeda. Zona hambat pertumbuhan mikroba terbesar terdapat pada bakteri S. agalactiae sebesar 10,72 mm. Ekstrak yang memiliki aktivitas antimikroba optimal dihasilkan dengan menggunakan pelarut n-heksana. Ekstrak biji teratai memiliki toksisitas dengan nilai LC50<1000 µg/ml. Analisis senyawa kimia menunjukkan dalam ekstrak biji teratai mengandung alkaloid, fenolik, glikosida, saponin dan steroid/terpenoid.
Kata kunci: Aktivitas antimikroba, mikroba patogen, Nymphaea pubescens L.
DEWI ROMA WIDYA. Activity of Lotus Seeds (Nymphaea pubescens L.) on
Aeromonas hydrophila, Streptococcus agalactiae Bacteria and Saprolegnia sp. Fungi. Under the Supervision of DWI SURYANTO and DESRITA.
Disease prevention in fish using chemicals or antibiotics lead to microbial resistance. One of alternative to control the fish disease is to use plant extract. The aim of this study was to investigate the antimicrobial activity of lotus seeds (Nymphaea pubescens L.) on pathogenic bacteria and fungi in fish. The lotus seed was extracted with several solvent, such as n-hexsana, etil asetat and methanol. Testing of antimicrobial activity carried out by disc diffusion method, to determine the compounds contained in the extract phytochemical test. To determine the level of toxicity of the extract using the Brine Shrimp Lethality Test. The extracts inhibitated the growth of Aeromonas hydrophila, Streptococcus agalactiae bacteria and Saprolegnia sp. fungi to some extent. Largest microbial growth inhibition zone of bacteria present in S. agalactiae by 10.72 mm.The optimal antimicrobial activity was obtained from n-heksana. The extract showed cytotoxic activity with LC50<1000 µg/ml. The chemical compound analysis showed that extract of lotus seed contains alkaloid, fenolik, glikosida, saponin and steroid/terpenoid.
Latar Belakang
Permintaan produk perikanan untuk kebutuhan domestik maupun ekspor
semakin meningkat. Untuk memenuhi kebutuhan dilakukan pengembangan
budidaya perikanan dengan intensif (Gardenia dkk., 2010), sehingga produksi
meningkat. Salah satu contoh produksi ikan lele di Indonesia sebagai ikan
konsumsi mengalami peningkatan dari tahun 2007 hingga 2011 yaitu 91,735 ton,
114,371 ton, 144,755 ton, 242,811 ton dan 340,674 ton dengan kenaikan rata-rata
39,82% (Kementerian Kelautan dan Perikanan, 2011). Sayangnya, intensifikasi
budidaya tersebut sering menyebabkan menurunnya kualitas lingkungan yang
pada akhirnya menimbulkan masalah seperti timbulnya penyakit.
Timbulnya penyakit dapat disebabkan karena kurang baiknya kondisi
perairan, kualitas pakan, maupun kualitas induk. Selain itu, penggunaan teknik
budidaya yang kurang tepat dan kontaminasi dari alat-alat budidaya maupun
pekerjanya juga dapat menyebabkan timbulnya penyakit (Hatmanti, 2003).
Penyakit pada ikan dapat disebabkan oleh bakteri, jamur, virus dan parasit
yang terdapat di perairan. Penyakit yang disebabkan oleh bakteri, selain dapat
menyebabkan kematian masal juga menganggu kualitas ikan dengan menurunkan
mutu daging ikan yang terinfeksi sehingga tidak disukai oleh konsumen
(Gardenia dkk., 2010). Salah satu penyakit bakterial pada ikan disebabkan oleh
bakteri Aeromonas hydrophila dan Streptococcus agalactiae. Genus Aeromonas
terdiri atas tiga spesies utama, yaitu Aeromonas punctata, A. hydrophila dan
menimbulkan kematian puluhan ton ikan di Indonesia pernah terjadi di Jawa Barat
pada bulan Oktober 1980 (Ghufran dan Kordi, 2004).
Disamping bakteri beberapa jamur dapat menimbulkan penyakit infeksi
pada ikan budidaya, baik ikan air tawar maupun ikan laut atau payau, ikan
konsumsi ataupun ikan hias. Salah satunya adalah jamur Saprolegnia sp., ikan yang terserang penyakit ini dipenuhi benang-benang putih seperti kapas yang
tumbuh pada kulit, sirip, insang mata dan telur ikan. Serangan jamur ini
menyebabkan kematian pada ikan yang dapat merugikan.
Penanggulangan penyakit pada ikan biasanya menggunakan zat kimia atau
antibiotik. Penggunaan antibiotik dapat menimbulkan resistensi terhadap bakteri,
jamur, virus dan parasit. Selain itu juga membutuhkan biaya yang cukup besar
serta dapat mencemari lingkungan. Pengobatan dengan cara ini biasanya
dilakukan dengan mencampurnya ke dalam pakan ikan, sehingga dapat
terakumulasi dalam tubuh ikan tersebut.
Penanggulangan secara alami dengan memanfaatkan tanaman merupakan
salah satu alternatif. Beberapa tanaman mengandung senyawa yang bersifat
antimikroba yang dapat dimanfaatkan untuk menghambat pertumbuhan dan
membunuh agen penyebab penyakit, salah satunya adalah biji teratai
(Nymphaea pubescens L.). Penelitian yang dilakukan Nuraini (2007) menunjukkan bahwa ekstrak biji teratai (Nymphaea pubescens Willd) mentah mampu menghambat pertumbuhan Escherichia coli, Bacillus cereus,
Ekstrak tumbuhan dapat mempunyai tingkat toksisitas tertentu, sehingga
perlu dilakukan uji toksisitas untuk mendukung hasil uji antimikroba. Metode
penelusuran untuk menentukan toksisitas ekstrak ataupun senyawa dilakukan
terhadap larva udang dari A. salina.
Pemanfaatan ekstrak biji teratai untuk pengendalian penyakit pada ikan
belum pernah dilakukan, oleh sebab itu perlu dilakukan penelitian pengaruh
ekstrak biji teratai (Nymphaea pubescens L.) dalam menghambat pertumbuhan
bakteri Aeromonas hydrophila, Streptococcus agalactiae dan jamur
Saprolegnia sp. yang merupakan penyebab penyakit pada ikan.
Perumusan Masalah
Teratai merupakan salah satu jenis tumbuhan air. Penelitian terdahulu oleh
Nuraini (2007) diketahui bahwa biji teratai (Nymphaea pubescens Willd) dapat menghambat pertumbuhan beberapa jenis bakteri Escherichia coli, Bacillus cereus,
Staphylococcus aureus dan Pseudomonas aeruginosa. Adapun perumusan masalah
dalam penelitian ini adalah
1. Apakah kandungan senyawa kimia yang terdapat dalam biji teratai?
2. Apakah ekstrak biji teratai dapat menghambat pertumbuhan bakteri dan jamur
patogen pada ikan?
3. Apakah ekstrak biji teratai toksik terhadap Artemia salina Leach?
Kerangka Pemikiran Penelitian
Intensifikasi budidaya menyebabkan menurunnya kualitas lingkungan
yang dapat menimbulkan penyakit pada ikan. Penanggulangan penyakit dilakukan
Penanggulangan secara alami perlu dilakukan, salah satunya dengan
mengekstraksi biji teratai (Nymphaea pubescens L.). Kerangka pemikiran ditampilkan pada Gambar 1.
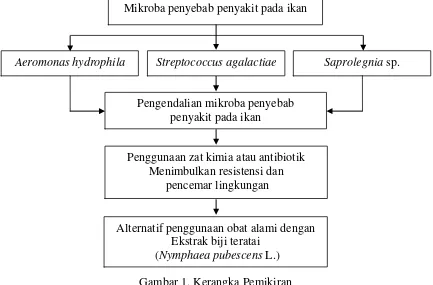
Gambar 1. Kerangka Pemikiran
Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Mengidentifikasi senyawa kimia yang terkandung dalam ekstrak biji teratai.
2. Mengetahui daya antimikroba ekstrak biji teratai terhadap bakteri uji
Aeromonas hydrophila, Streptococcus agalactiae dan jamur Saprolegnia sp. secara in vitro.
3. Mengetahui daya toksisitas ekstrak biji teratai terhadap Artemia salina Leach. Mikroba penyebab penyakit pada ikan
Aeromonas hydrophila Streptococcusagalactiae Saprolegnia sp.
Pengendalian mikroba penyebab penyakit pada ikan
Alternatif penggunaan obat alami dengan Ekstrak biji teratai
(Nymphaea pubescens L.) Penggunaan zat kimia atau antibiotik
Manfaat Penelitian
Penelitian ini bermanfaat memberikan informasi penggunaan biji teratai
sebagai sumber daya alami untuk mengendalikan penyakit ikan sehingga
mempunyai nilai ekonomis dalam mengobati penyakit yang disebabkan oleh
Aeromonas hydrophila, Streptococcus agalactiae dan jamur Saprolegnia sp. untuk meningkatkan produksi sektor perikanan di Indonesia.
Hipotesis Penelitian
Hipotesis penelitian ini adalah:
1. Biji teratai mengandung senyawa kimia terpenoid, steroid, saponin, alkaloid,
fenolik dan glikosida.
2. Ekstrak biji teratai dapat menghambat dan membunuh bakteri Aeromonas
hydropila, Streptococcus agalactiae dan jamur Saprolegnia sp. karena mengandung senyawa antimikroba.
Teratai (Nymphaea pubescens L.)
Teratai merupakan tumbuhan air yang tumbuh di daerah bersuhu 20˗30°C.
Teratai tumbuh di perairan tenang dan lembab, memerlukan banyak sinar
matahari. Teratai (Gambar 2) memiliki akar yang kuat, panjang dan berumbi.
Daunnya mengapung di atas air, bagian atas daun berwarna hijau tua, sedangkan
bagian bawahnya berwarna ungu kemerahan. Bentuk daun bundar dengan
diameter antara 9˗ 12cm, bagian tepi daun melipat dan daunnya mempunyai
tangkai (Nuraini, 2007). Adapun sistematika dan klasifikasi teratai adalah sebagai
berikut:
Kingdom : Plantae
Divisio : Spermathophyta
Kelas : Dicotyledoneae
Ordo : Nymphaeales
Famili : Nymphaeaceae
Genus : Nymphaea
Spesies : Nymphaea pubescens L.
Gambar 2. Teratai (Nymphaea pubescens L.)
Teratai menghasilkan buah dengan diameter sekitar 4–12 cm, di dalam
buah terdapat biji yang berwarna hijau setelah tua akan berwarna coklat gelap.
Biji teratai umumnya dikenal dengan sebutan ghol, biji ini memiliki beberapa manfaat terutama sebagai bahan makanan dan obat. Biji teratai di Cina
dijadikan bubur yang baik untuk orang-orang yang dalam proses penyembuhan
penyakit karena mempunyai sifat mendinginkan. Menurut Fitrial (2009),
komposisi biji teratai bervariasi tergantung pada spesiesnya, tempat tumbuh serta
musim. Berdasarkan hasil penelitian terdahulu kandungan gizi tepung biji teratai
dapat dilihat pada Tabel 1.
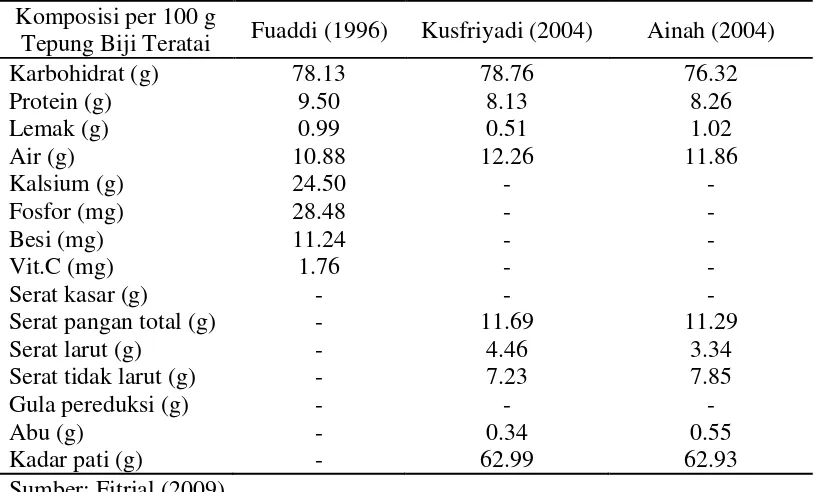
Tabel 1. Komposisi kimia tepung biji teratai Komposisi per 100 g
Tepung Biji Teratai Fuaddi (1996) Kusfriyadi (2004) Ainah (2004) Karbohidrat (g)
Serat pangan total (g) Serat larut (g)
Serat tidak larut (g) Gula pereduksi (g)
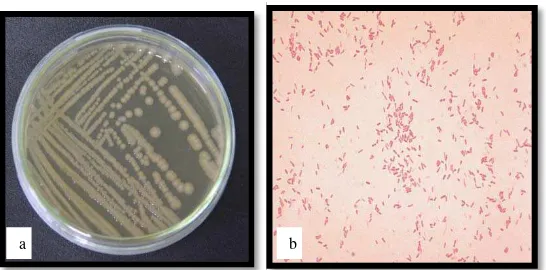
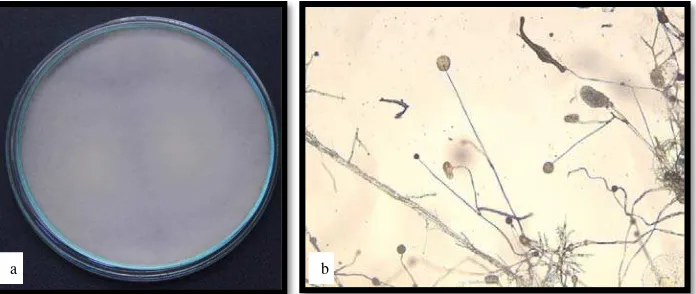
Ciri utama bakteri Aeromonas (Gambar 3) adalah bentuknya seperti batang, ukurannya 1–4,4 x 0,4–1μm, bersifat gram negatif, fakultatif anaerob
(dapat hidup dengan atau tanpa oksigen), tidak berspora, bersifat motil (bergerak
aktif) karena mempunyai satu flagel (Monotrichous flagella) yang keluar dari
salah satu kutubnya, senang hidup di lingkungan bersuhu 15–300C dan pH 5,5–9
Gambar 3. Aeromonas hydrophila (a) Makroskopis (b) Mikroskopis
Aeromonas hydrophila dapat ditemukan dalam makanan dan lingkungan perairan di seluruh dunia. Bakteri ini adalah anggota dari famili Aeromonadaceae
yang dikenal sebagai patogen pada hewan. Bakteri ini dapat menyebabkan infeksi
usus manusia dan beberapa penyakit yang berakibat fatal. Karena sering
ditemukan di lingkungan perairan A. hydrophila dapat menyebabkan penyakit serius pada ikan (Belal dkk., 2009).
Bakteri A. hidrophyla dapat hidup di berbagai perairan di dunia seperti air sungai, estuaria, air laut dan dikenal sebagai penyebab penyakit Motil Aeromonas Septicaemia (MAS) lalu bakteri tersebut memproduksi berbagai produk protein ekstraseluler, termasuk toksin, haemolysin dan enzim protease yang diduga
sebagai penyebab virulensi bakteri tersebut terhadap inangnya
(Muslim dkk., 2009). Penularan bakteri ini melalui air, kontak badan, pemakaian
alat yang telah tercemar atau karena alat digunakan untuk pemindahan ikan yang
telah terserang bakteri A. hidrophyla.
Kerugian yang ditimbulkannya sangat besar, sebab dalam waktu relatif
singkat puluhan ton ikan mati secara masal, baik ukuran benih maupun induk.
Serangan bakteri ini bersifat laten (berkepanjangan), jadi tidak memperlihatkan
gejala penyakit meskipun telah dijumpai pada tubuh ikan. Serangan bakteri ini b
baru terlihat apabila ketahanan tubuh ikan menurun akibat stres yang disebabkan
oleh penurunan kualitas air, kekurangan pakan atau penanganan ikan yang kurang
baik (Ghufran dan Khordi, 2004).
Ikan yang terserang bakteri A. hidrophyla menujukkan perubahan warna tubuh menjadi gelap, berenang tidak beraturan, mata ikan rusak, sisik seperti akan
lepas, sirip rusak, insang berwarna pucat, ikan berenang ke permukaan seperti
kekurangan oksigen, insang rusak sehingga sulit bernapas, kulit ikan menjadi
kasat dan timbul pendarahan dengan luka-luka borok, perut menjadi besar (dropsi)
dan apabila dibedah akan terlihat pendarahan pada hati, ginjal dan limpa.
Bakteri Streptococcus agalactiae
Streptococcus merupakan bakteri gram positif yang berbentuk bulat. Bakteri ini termasuk kelompok bakteri asam laktat yang tumbuh berantai atau
berpasangan.
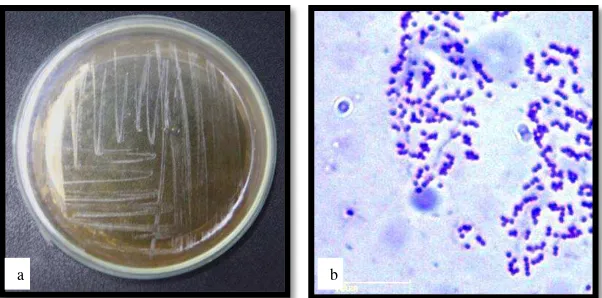
Streptococcus agalactiae (Gambar 4) termasuk dalam genus Streptococcus
golongan B. Bakteri ini secara khas merupakan β hemolitik dan membentuk
daerah hemolisis yang hanya sedikit lebih besar dari koloni
(bergaris tengah 1˗ 2 mm). Streptococcus golongan B menghidrolisis natrium hipurat dan memberi respons positif pada tes Christie, Atkins, Munch-Peterson
Gambar 4. Streptococcus agalactiae (a) Makroskopis (b) Mikroskopis
Streptococcus agalactiae mempengaruhi banyak spesies ikan liar dan ikan budidaya di seluruh dunia dan menyebabkan penyakit yang melibatkan
Septicaemia dan kolonisasi berbagai organ. Tanda-tanda klinis infeksi
S. agalactiae ikan terlihat lesu, tidak mau makan tubuh berbentuk huruf C, berenang tidak beraturan dan berputar-putar, operculum berwarna cerah, tulang
belakang melengkung dan menyebabkan kematian. Ikan nila
(Oreochromis niloticus) rentan terkena infeksi S. agalactiae (Pasnik dkk., 2009). Bakteri ini menyerang tubuh yang telah mengalami luka atau sebagai
serangan lanjutan dari parasit. Bakteri ini menyebabkan penyakit streptococcis
pada ikan nila. Bakteri ini agak sulit untuk dikendalikan karena tahan terhadap
sejumlah antibiotik yang sering digunakan dalam penanggulangan penyakit.
Jamur Saprolegnia sp.
Saprolegnia sp. (Gambar 5) adalah jenis jamur yang hidup di perairan tawar. Jamur ini memperbanyak keturunannya dengan cara seksual (dengan alat
kelamin) dan dengan cara aseksual (tanpa alat kelamin). Memperbanyak
keturunan secara aseksual dilakukan dengan spora yang mempunyai dua buah
rambut getar (biflagellata) (Ghufran dan Khordi, 2004).
Gambar 5. Saprolegnia sp. (a) Makroskopis (b) Mikroskopis
Saprolegnia sp. menyebabkan penyakit saprolegniasis pada ikan air tawar seperti ikan mas, tawes, gabus, gurami dan nila. Ikan yang terserang
saprolegniasis biasanya diawali serangan dari bakteri dan parasit serta penanganan yang tidak baik setelah terserang bakteri tersebut. Jamur ini biasanya
menyerang ikan dan telur ikan. Pada ikan dewasa biasanya yang diserang bagian
kulit yang telah terluka. Sedangkan telur ikan yang terserang akan terlihat seperti
dilapisi kapur.
Ikan dan telur ikan yang terserang jamur ini dapat diketahui dengan
mudah, sebab terlihat bagian organ ikan (biasanya bagian luar) atau telur yang
terserang, ditumbuhi oleh sekumpulan miselium jamur yang menyerupai
gumpalan benang-benang halus (hypa) yang tampak seperti kapas. Kumpulan benang ini biasanya terlihat di bagian kepala, tutup insang atau di sekitar sirip
(Ghufran dan Khordi, 2004).
Diameter hypa kira-kira 20μm. Di dalam kantong sporangianya dijumpai ribuan zoospora yang mempunyai rambut getar (flagella). Zoospore yang sudah
matang akan keluar dari kantongnya (sporangia) dan kondisi inilah yang setiap
saat selalu mengancam keselamatan ikan dan telur ikan
(Ghufran dan Khordi, 2004).
Senyawa Antimikroba
Senyawa antimikroba merupakan senyawa biologis atau kimia yang
memiliki kemampuan untuk menghambat atau bahkan membunuh pertumbuhan
dan aktivitas mikroba. Pengertian antimikroba secara umum adalah zat yang dapat
menghambat pertumbuhan mikroba dan digunakan untuk kepentingan pengobatan
infeksi pada manusia dan hewan. Antibakteri termasuk dalam antimikroba yang
digunakan untuk menghambat pertumbuhan bakteri (Fitrial, 2009).
Berdasarkan cara kerjanya, antibakteri dibedakan menjadi bakteriostatik
dan bakterisidal. Antibakteri bakteriostatik bekerja dengan cara menghambat
pertumbuhan bakteri, sedangkan antibakteri bakterisidal bekerja dengan cara
mematikan bakteri secara langsung. Bakteriostatik dapat bertindak sebagai
bakterisidal dalam konsentrasi tinggi (Pelczar dan Chan, 2005).
Antimikroba yang sangat toksik yang membahayakan inangnya bukan
merupakan antibiotik yang baik dan dianggap beracun. Antimikroba yang baik
adalah antimikroba yang mampu menyembuhkan penyakit tanpa menimbulkan
efek samping terhadap inangnya dan juga harus memiliki sifat toksisitas selektif
yang tinggi.
Zat antimikroba dalam melakukan efeknya harus dapat mempengaruhi
bagian-bagian vital sel seperti membran sel, enzim-enzim dan protein struktural.
Menurut Pelczar dan Chan (2005) cara kerja senyawa antimikroba dalam
melakukan efeknya terhadap mikroorganisme adalah dengan merusak dinding sel,
mengubah permeabilitas membran sel, kerusakan sitoplasma, menghambat kerja
Senyawa antimikroba yang berasal dari tanaman, sebagian besar diketahui
merupakan metabolit sekunder tanaman, terutama golongan fenolik dan terpenoid
dalam minyak atsiri. Beberapa senyawa yang bersifat antimikroba alami berasal
dari tanaman diantaranya adalah fitoleksin, asam organik, minyak esensial (atsiri),
fenolik dan beberapa kelompok pigmen tanaman atau senyawa sejenis
(Mawaddah, 2008).
Senyawa Fitokimia
Alkaloid merupakan salah satu metabolit sekunder yang banyak
ditemukan di alam dan mempunyai keaktifan fisiologis tertentu. Alkaloid ada
yang sangat beracun tetapi ada pula yang sangat berguna dalam pengobatan
misalnya kuinin, morfin dan striknin (Maryati, 2006). Alkaloid bersifat basa yang
mengandung satu atau lebih atom nitrogen, umumnya tidak berwarna dan
berwarna jika mempunyai struktur kompleks dan bercincin aromatik. Alkaloid
bersifat optis aktif dan dalam proses ekstraksi dapat mengakibat isomerisasi
sehingga alkaloid yang diperoleh berupa campuran resemik (Simbala, 2009).
Flavonoid diturunkan dari unit C6 – C3 (fenil-propana) yang bersumber
dari asam sikimat (via fenilalanin) dan unit C6 yang diturunkan dari jalur
poliketida. Makanan yang kaya flavanoid dianggap penting untuk mengobati
penyakit-penyakit seperti kanker dan penyakit jantung (yang dapat memburuk
akibat oksidasi lipoprotein densitas-rendah). Kuarsetin merupakan suatu flavanoid
yang banyak terdapat dalam berbagai makanan dan antioksidan kuat
(Heinrich dkk., 2010).
Steroid banyak ditemukan di alam sebagai fraksi lipid dari tanaman atau
pada tumbuhan dibentuk oleh senyawa sterol dan banyak terdapat dalam jaringan
tumbuhan sehingga sering dikenal dengan fitosterol. Senyawa steroid dapat
menghambat pertumbuhan bakteri gram positif (Ayuningtyas, 2008). Steroid
merupakan senyawa bioaktif yang memiliki fungsi sebagai antijamur. Senyawa
senyawa ini dapat menghambat pertumbuhan jamur, baik melalui membran
sitoplasma maupun mengganggu pertumbuhan dan perkembangan spora jamur
(Lutfiyanti dkk., 2012).
Saponin merupakan senyawa yang diduga sebagai senyawa antibakteri
karena memiliki kemampuan dalam menghambat fungsi membran sel sehingga
merusak permeabilitas membran yang mengakibatkan dinding sel rusak atau
hancur. Keberadaan saponin dalam tumbuhan dapat juga dimanfaatkan sebagai
obat bagi manusia. Menurut Nopianti dkk. (2008), saponin merupakan golongan
senyawa triterpenoid yang dapat juga digunakan sebagai insektisida. Saponin
terdapat pada tanaman yang kemudian dikonsumsi serangga, mempunyai
mekanisme kerja dapat menurunkan aktivitas enzim pencernaan dan penyerapan
makanan, sehingga saponin bersifat sebagai racun perut.
Tanin merupakan komponen zat organik derivat polimer glikosida yang
terdapat dalam bermacam-macam tumbuhan, terutama tumbuhan berkeping dua
(dikotil). Monomer tanin adalah digallic acid dan D-glukosa. Ekstrak tanin terdiri
dari campuran senyawa polifenol yang sangat kompleks dan biasanya tergabung
dengan karbohidrat rendah. Oleh karena adanya gugus fenol, maka tanin akan
dapat berkondensasi dengan formaldehida. Tanin terkondensasi sangat reaktif
terhadap formaldehida dan mampu membentuk produk kondensasi, berguna untuk
mensubsitusi gugus fenol dari resin fenol formaldehid guna mengurangi
pemakaian fenol sebagai sumberdaya alam tak terbaharukan
(Linggawati dkk., 2002).
Fenol (asam karboksilat) digunakan secara luas sebagai desinfektan dan
antiseptik. Golongan fenol diketahui memiliki aktivitas antimikroba yang bersifat
bakterisidal namun tidak bersifat sporisidal. Fenol sebagai disinfektan cair tidak
dipengaruhi oleh bahan organik, aktivitasnya rendah terhadap endospora bakteri,
efektif pada konsentrasi 2˗5% dengan mendenaturasi protein dan merusak
membran sel bakteri serta aktif pada pH asam. Aktivitas antimikroba senyawa
fenolik adalah dengan merusak lipid pada membran plasma mikroorganisme,
sehingga menyebabkan isi sel keluar. Dinding sel Mycobacterium penyebab tuberculosis dan lepra kaya dengan lipid sehingga Mycobacterium sangat peka terhadap senyawa fenolik (Pratiwi, 2008).
Triterpen adalah terpenoid turunan –C30 yang terdistribusi sangat luas,
termasuk pada manusia, tanaman, fungi, bakteri, karang lunak dan amfibi.
Triterpen juga merupakan resin dan eksudat resin dari tanaman. Resin ini lazim
ditemui pada tanaman dari famili Burseraceae dan diproduksi jika pohon menjadi rusak sebagai pelindung fisik terhadap serangan oleh fungi dan bakteri. Selain itu
banyak komponen terpenoid resin ini memiliki aktivitas antimikroba yang tinggi,
baik membunuh mikroba yang berpotensi menyerang maupun memperlambat
pertumbuhannya hingga pohon dapat memperbaiki kerusakannya
Ekstraksi
Ekstraksi merupakan suatu metode untuk memisahkan senyawa penting
dari bahan tertentu agar senyawa tersebut dapat lebih baik dalam pemanfaatannya.
Ekstraksi yang sering digunakan adalah dengan menggunakan pelarut karna lebih
ekonomis walaupun membutuhkan waktu yang lama.
Umumnya ekstraksi dikerjakan untuk simplisia yang mengandung zat-zat
yang berkhasiat atau zat-zat lain untuk keperluan tertentu, simplisia
(hewan/tumbuhan) mengandung bermacam-macam zat atau senyawa tunggal,
sebagian mengandung khasiat pengobatan, misalnya bermacam-macam alkaloid,
glukosa, damar, oleoresin, minyak atsiri, lemak dan sebagainya. Disamping itu
terdapat juga jenis-jenis gula, zat pati, zat lendir, albumin, protein, peptin, selulosa
dan lain-lainnya. Umumnya mempunyai daya larut dalam cairan pelarut tertentu
dan sifat-sifat kelarutan ini dimanfaatkan dalam ektraksi (Syamsuni, 2006).
Beberapa metode ekstraksi seperti maserasi (maserer), perkolasi (perkoler),
decotct dan digerasi (digerer).
Proses ekstraksi dapat berjalan dengan baik bila pelarut ideal memenuhi
syarat-syarat yaitu selektivitasnya tinggi, memiliki perbedaan titik didih dengan
solute cukup besar, bersifat inert, perbedaan densiti cukup besar, tidak beracun,
tidak bereaksi secara kimia dengan solute maupun diluen, viskositasnya kecil,
tidak bersifat korosif, tidak mudah terbakar, murah dan mudah didapat
(Yasita dan Intan, 2009). Beberapa faktor yang berpengaruh dalam proses
ekstraksi adalah temperatur, waktu kontak, perbandingan solute, faktor ukuran
Teknik ekstraksi yang digunakan pada penelitian ini adalah ekstraksi
maserasi (maserer). Maserasi adalah cara penarikan simplisia dengan merendam
simplisia tersebut dalam cairan penyari pada suhu biasa ataupun memakai
pemanas (Syamsuni, 2006). Pada penelitian ini, pelarut yang digunakan dalam
proses ekstraksi adalah heksana, etil asetat dan metanol yang ketiganya
berturut-turut merupakan senyawa nonpolar, semi polar, dan polar.
Heksana merupakan pelarut yang bersifat nonpolar dan berfungsi
melarutkan lemak. Heksana terdiri dari hidrokarbon alkana dengan rumus molekul
C6H14. Heksana yang digunakan sebagai pelarut berupa cairan tak berwarna dan
memiliki titik didih 69°C serta larut dalam air. Sedangkan etil asetat merupakan
komponen organik semi polar dengan rumus molekul C4H8O2. Etil asetat bersifat
volatil, nontoksik, dan tidak higroskopis (Nuraini, 2007).
Uji Brine Shrimp Lethality Test
Uji bioaktivitas menggunakan larva udang A. salania dikenal dengan istilah Brine Shrimp Lethality Test (BSLT). BSLT adalah suatu metode penelusuran untuk menentukan toksisitas ekstrak ataupun senyawa terhadap larva
udang dari A. salina (Darmawan, 2011). Uji toksisitas dengan metode BSLT ini merupakan uji toksisitas akut dimana efek toksik dari suatu senyawa ditentukan
dalam waktu singkat setelah pemberian dosis uji. Metode BSLT dapat dipercaya
untuk menguji aktivitas toksikologi dari bahan-bahan alami (Ramadhani, 2009).
Brine Shrimp Lethality Test (BSLT) merupakan salah satu metode untuk menguji bahan-bahan yang bersifat toksik. Uji toksisitas dengan metode BSLT ini
merupakan uji toksisitas akut dimana efek toksik dari suatu senyawa ditentukan
uji. Suatu ekstrak dikatakan toksik berdasarkan metode BSLT jika harga
LC50 < 1000 μg/ ml. BSLT digunakan untuk pengujian sitotoksik sederhana pada
dosis yang rendah dan sebagian besar senyawa antitumor. Aktivitas yang luas dari
senyawa aktif terhadap udang, akan tetapi prosedur yang sederhana, biaya yang
rendah dan korelasinya terhadap pengujian sitotoksitas dan pengujian antitumor
membuat pengujian ini sebagai uji pendahuluan yang sesuai dan dapat dilakukan
secara rutin di laboratorium dengan fasilitas sederhana (Aras, 2013).
Hasil uji toksisitas dengan metode BSLT dapat diketahui dari jumlah
kematian larva udang Artemia salina Leach karena pengaruh ekstrak atau senyawa bahan alam tumbuhan tertentu dari dosis yang telah ditentukan. Tingkat
toksisitas dari ekstrak tumbuhan dapat ditentukan dengan melihat nilai LC50
(lethal concentration). Apabila nilai LC50 kurang dari 1000 mg/ml, ekstrak tumbuhan tersebut dikatakan toksik. Tingkat toksisitas tersebut akan memberi
makna terhadap potensi aktivitasnya sebagai anti bakteri
(Indiastuti dan Yuani, 2008).
Kemampuan Beberapa Tanaman Sebagai Antimikroba
Aktivitas antimikroba ekstrak herba meniran terhadap bakteri patogen
S. aureus menunjukkan bahwa hambatan pada ekstrak metanol konsentrasi 10% yaitu dengan diameter zona hambat sebesar 21,29 mm, diikuti dengan ekstrak
metanol konsentrasi 5% yaitu dengan diameter zona hambat sebesar 17,32 mm
dan kemudian ekstrak metanol konsentrasi 1% yaitu dengan diameter zona
hambat sebesar 15,30 mm. aktivitas antimikroba ekstrak herba meniran terhadap
metanol konsentrasi 5% yaitu dengan diameter zona hambat sebesar 14,63 mm,
dan ekstrak metanol konsentrasi 1% yaitu dengan diameter zona hambat sebesar
13,01 mm. Aktivitas antimikroba ekstrak herba meniran terhadap khamir patogen
C. albicans menunjukkan bahwa ekstrak metanol konsentrasi 10% yaitu dengan diameter zona hambat sebesar 17,63 mm (Desfita, 2011).
Uji sensitivitas antibakteri ekstrak Sargassum sp. terhadap bakteri
E. coli pada konsentrasi 80% cukup peka, zona hambat 13 mm, 12,5 mm, 13,5 mm, rata-rata 13 mm. Konsentrasi 90% sangat peka, zona hambat 17 mm, 15
mm, 15 mm, rata-rata 15,7 mm. Konsentrasi 100% sangat peka, zona hambat 19
mm, 19 mm,18 mm, rata-rata 18,6 mm (Bacthiar dkk., 2012)
Ekstrak kulit kayu manis (Cinnamomum burmanii) terhadap bakteri
Salmonella sp., Shigella sp., Streptococcus mutan dan Staphylococcus aureus
diperoleh bahwa ekstrak n-heksana memiliki zona hambat bakteri yang paling
kuat sebesar 5,415 mm daripada ekstrak etil asetat sebesar 1,25 mm dan metanol
sebesar 0,88 mm. Penelitian yang dilakukan Marliani (2011) dari ekstrak buah
labu air (Lagenari siceraria (Molina) Standl) terhadap bakteri gram positif
Bacillus cereus lebih kuat sebesar 9,0023 mm dibandingkan bakteri gram negatif
Waktu dan Tempat Penelitian
Penelitian dilaksanakan dari bulan Mei-September 2013. Pembuatan
ekstrak dan pengujian fitokimia biji teratai di Laboratorium Kimia Bahan Alam,
Fakultas Matematika dan Ilmu Pengetahuan Alam dan Laboratorium Fitokimia
Fakultas Farmasi, Universitas Sumatera Utara. Pengujian Brine Shrimp dilakukan di Unit Pelayanan Teknis (UPT) Budidaya Ikan, Dinas Perikanan dan Kelautan
Kota Medan. Pengujian efektivitas antimikroba di Stasiun Karantina Ikan
Pengendalian Mutu dan Keamanan Hasil Perikanan Kelas I Medan II.
Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah Mikroskop, mortar,
ayakan mesh 32, labu Erlenmeyer, spatula, blender, pipet tetes, rak tabung, objek
glass, cover glass, tabung reaksi, timbangan analitik, corong, rotary evaporator,
water bath, corong pemisah, kaki tiga, wadah penetasan, aerasi, sendok teh, tanggok, gelas ukur, botol vial, jarum suntik, cawan Petri, oven, hot plate, stirer,
autoclave, Laminar air flow, jarum ose, bunsen, inkubator, beaker glass, pinset,
micropipet, vortex, jangka sorong dan kertas saring.
Bahan yang digunakan dalam penelitian ini adalah biji teratai (Nymphaea pubescens L.), isolat murni bakteri Aeromonas hydrophila diperoleh dari Balai Karantina Ikan Pengendalian Mutu dan Keamanan Hasil Perikanan Kelas I Medan
Laboratorium Mikrobiologi, Fakultas MIPA Universitas Sumatera Utara, Thin Layer Cromatography (TLC), air, garam non-yodium, kista Artemia salina
(Mackay Marine), pelarut n-Heksana, Etil asetat, Metanol, Dimethyl sulfoxide
(DMSO), asam asetat anhidrat, H2SO4 pekat, air laut, HCl 2 N, Pb asetat,
kloroform isopropanol, FeCl3 1%, metanol, NaOH 10%, petroleum bensin,
pereaksi Dragendrauf, pereaksi Bauchardat, pereaksi Mayer, pereaksi Wagner,
Trypticase soy agar (TSA), Potato Dextrose Agar (PDA), Brain-Heart Infusion Agar (BHIA), akuades, alkohol 70%, NaCl 0,9%, kertas cakram, disk kloramfenikol, disk nistatin, kapas, kertas label, aluminium foil. Alat dan bahan
yang digunakan terlebih dahulu dilakukan sterilisasi, tahapan sterilisasi dapat
dilihat pada Lampiran 1.
Metode Penelitian
Pembuatan Ekstrak Biji Teratai
Tanaman teratai diperoleh dari kolam Fakultas Pertanian, kolam
Perpustakaan Universitas Sumatera Utara dan di sekitar kota Medan. Buah yang
sudah tua dipanen, kemudian diambil bijinya. Biji dikeringkan pada suhu ruangan
tanpa terkena sinar matahari langsung selama ± 1 minggu. Biji yang kering akan
berwarna kecoklatan atau hitam dan kulitnya keras. Kulit biji dibuang kemudian
isi biji ditumbuk dengan mortar dan diblender sehingga menjadi serbuk
(simplisia). Selanjutnya simplisia ditimbang sebanyak 300 gram dan dimasukkan
ke dalam labu Erlenmeyer yang berisi 1 liter pelarut n-Heksana. Perendaman
(maserasi) dilakukan pada suhu kamar dan tidak boleh terkena sinar matahari,
Setelah ± 24 jam, sampel disaring sehingga diperoleh filtrat dan ampas,
kemudian filtrat dievaporasi dengan rotary evaporator untuk memisahkan pelarut dengan ekstrak biji teratai. Ekstrak dimasukkan ke dalam botol vial dan dilakukan
pemekatan ekstrak dengan penangas air (water bath) sampai seluruh pelarutnya habis menguap dan diperoleh ekstrak pekat. Perlakuan yang sama juga dilakukan
terhadap pelarut etil asetat dan metanol secara berturut-turut dengan pengenceran
tunggal. Pembuatan ekstrak biji teratai dapat dilihat pada Lampiran 2.
Uji Fitokimia Biji Teratai
Uji fitokimia biji teratai merupakan uji yang dilakukan untuk mengetahui
senyawa-senyawa kimia yang terdapat di dalamnya. Tahapan pengujian saponin,
steroid/terpenoid, alkaloid dan fenolik dilakukan berdasarkan metode Harborne
(1998) dan pengujian glikosida berdasarkan metode Materi Medika Indonesia
tahun 1995.
Simplisia sebanyak 10 gram dimasukkan ke dalam labu Erlemeyer yang
telah berisi pelarut n-Heksana 100 ml kemudian diaduk dan direndam selama 24
jam. Perlakuan yang sama juga dilakukan terhadap pelarut etil asetat dan metanol
secara berturut-turut dengan pengenceran tunggal.
a. Pengujian golongan alkaloid
Ekstrak sampel diambil 4 ml dimasukkan masing-masing 1 ml kedalam 4
tabung reaksi. Tabung pertama ditambahkan 2 tetes pereaksi Bouchardat, apabila
terbentuk endapan berwarna cokelat sampai hitam maka sample positif alkaloid.
Tabung kedua ditambahkan 2 tetes pereaksi Dragendroff, apabila terbentuk
ditambahkan 2 tetes pereaksi Mayer, apabila terbentuk endapan berwarna
putih/kuning maka sampel positif alkaloid. Tabung keempat ditambahkan 2 tetes
pereaksi Wagner, apabila terbentuk endapan berwarna cokelat maka sampel
positif alkaloid.
b. Pengujian golongan fenolik
Ekstrak sampel diambil 1 ml dimasukkan ke dalam tabung reaksi kemudian
ditambahkan FeCl3 1% jika terjadi perubahan warna menjadi hitam maka positif
terdapat senyawa senyawa fenolik.
c. Pengujian golongan glikosida
Simplisia ditimbang 3 gram kemudian dimasukkan ke dalam labu Erlenmeyer,
ditambahkan 30 ml campuran etanol 96% - air (7:3), ditambahkan asam sulfat
pekat hingga diperoleh pH larutan 2, kemudian direfluks dengan memakai
pendingin bola selama 10 menit, kemudian didinginkan lalu disaring.
Filtrat diambil 20 ml ditambahkan 25 ml timbal (II) asetat 0,4 M, dikocok
lalu didiamkan selama 5 menit, kemudian disaring. Filtrat diekstraksi 3 kali,
masing-masing dengan 20 ml campuran pelarut kloroform-isopropanol (3:2)
kemudian akan diperoleh dua lapisan, kumpulkan masing-masing sari (sari air dan
sari pelarut organik). Pada kumpulan sari pelarut organik ditambahkan natrium
sulfat anhidrat, kemudian disaring lalu filtrat diuapkan pada suhu tidak lebih dari
500C. Sisa penguapan dilarutkan dengan 2 ml metanol.
Uji Gula
Filtrat dimasukkan dalam tabung reaksi, diuapkan diatas penangas air. Sisa
terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya ikatan
gula.
Uji Non-gula
Filtrat diuapkan di atas penangas air, sisa filtart dilarutkan dengan 5 tetes
asam asetat anhidrat, ditambahkan 10 tetes asam sulfat pekat, jika terbentuk warna
biru hijau, menunjukkan adanya glikosida (reaksi Liebermann Burchard)
d. Pengujian golongan terpenoid /steroid
Ekstrak diambil sebanyak 2 ml dimasukkan ke dalam tabung reaksi,
kemudian ditambahkan 2 tetes perekasi Liebermann-Bouchard. Apabila terbentuk
warna biru ungu/biru hijau menunjukkan adanya terpenoid/steroid.
Pengujian dengan CeSO4 dilakukan dengan metode Thin Layer Cromatography (TLC) dengan cara ekstrak sampel diteteskan ke plat TLC kemudian disemprot dengan pereaksi CeSO4 dan dipanaskan di atas hot plate. Perubahan warna yang terjadi di plat diamati dan dibandingkan dengan standar
triterpenoid dan β-sitosterol yang terbentuk.
e. Pengujian golongan saponin
Setelah 24 jam ampas dari proses maserasi diambil dengan spatula
sebanyak 0,5 gram dan dimasukkan ke dalam tabung reaksi kemudian
ditambahkan 10 ml akuades. Tabung reaksi dikocok hingga muncul buih. Ekstrak
diberi 1 tetes HCl 2 N, bila buih terbentuk ± 10 menit maka terdapat senyawa
Uji Toksisitas Biji Teratai
Pengujian ini dilakukan dengan metode Brine Shrimp Lethality Test
(BSLT). Kista A. salina ditetaskan dalam bejana yang sudah berisi air dengan salinitas 83 ppt dan dilengkapi dengan alat aerasi. Selanjutnya dibiarkan selama
48 jam hingga kista menetas dan tumbuh dewasa (naupli).
Larutan induk ekstrak biji teratai untuk setiap uji dibuat dengan
melarutkan 20 mg dalam 2 ml pelarut DMSO. Larutan uji 1000 ppm dibuat
dengan memipet larutan induk sebanyak 500 μl, sedangkan larutan uji 100 ppm
dengan memipet 50 μl dan 10 ppm dibuat 5 μl dari larutan induk. Masing-masing
larutan uji dimasukkan ke dalam vial dan ditambahkan air dengan salinitas 83 ppt
(250 gram garam laut + 3 liter akuades) hingga volumenya 5000 μl. Sebanyak 10
ekor larva udang A. salina dimasukkan ke dalam vial. Masing-masing konsentrasi dibuat ulang sebanyak 5 kali (5 vial) dan 1 vial untuk kontrol. Kematian A. salina
diamati setelah 24 jam. Proses pengujian toksisitas A. salina dapat dilihat pada Lampiran 3.
Pembuatan Konsentrasi Larutan Uji
Konsentrasi yang akan digunakan yaitu 0% (Kontrol negatif); 50%; 60%;
70%; 80%; dibuat dengan cara menimbang ekstrak biji teratai sebanyak 0,8 gram
dan dilarutkan dalam 1 ml larutan DMSO. Selanjutnya dilakukan pengenceran
hingga diperoleh konsentrasi 50%; 60%; 70% (Lampiran 4). Uji antibiotik
(kontrol positif) untuk jamur menggunakan disk nistatin 20,6 µg dan bakteri disk
Penyiapan Bakteri dan Jamur Uji
Pembuatan media tumbuh bakteri dan jamur dapat dilihat pada
Lampiran 5. Bakteri Aeromonas hydropila diinokulasi ke media TSA dan
Streptococcus agalactiae ke media BHIA sedangkan jamur Saprolegnia sp. diinokulasikan ke media PDA. Analisis bakteri Aeromonas hydropila,
Streptococcus agalactiae dan jamur Saprolegnia sp. (Lampiran 6, Lampiran 7 dan Lampiran 8). Inokulum selanjutnya diinkubasi pada suhu 28˗350C selama 24 jam
untuk bakteri Aeromonas hydropila, 48 jam untuk bakteri Streptococcus agalactiae dan 7 hari untuk jamur Saprolegnia sp. Stok kultur bakteri yang ada diambil biakannya dengan jarum ose steril dan suspensikan ke dalam tabung yang
berisi 3 ml larutan NaCl fisiologis 0,9%. Kemudian dihomogenkan dengan vortex
hingga diperoleh kekeruhan suspensi sebanding dengan kekeruhan larutan
Mc Farland sama dengan 0,5 x 108 CFU/ml. Pembuatan larutan Mc Farland dapat
dilihat pada Lampiran 9. Jamur dipotong 0,5 x 0,5 cm dengan menggunakan pisau
steril kemudian diletakkan ke media PDA baru.
Pengujian Ekstrak Biji Teratai Terhadap Bakteri dan Jamur
Pengujian ekstrak biji teratai dilakukan dengan metode difusi disk
menggunakan kertas cakram berdiamter 6 mm. Cakram dimasukkan ke dalam
botol vial yang telah berisi larutan ekstrak dengan konsentrasi 50%; 60%; 70%;
80%, ditunggu ± 1 jam hingga larutan ekstrak meresap ke dalam cakram.
Sebanyak 10 ml PDA, TSA dan BHIA masing-masing dituangkan ke
dalam cawan petri steril dan dibiarkan memadat. Pada suspensi bakteri dicelupkan
lidi kapas steril dan diusapkan perlahan-lahan pada permukaan media secara
ditetesi ekstrak dengan konsentrasi berbeda dan antibiotik diletakkan secara
teratur pada permukaan media uji dengan menggunakan pinset steril
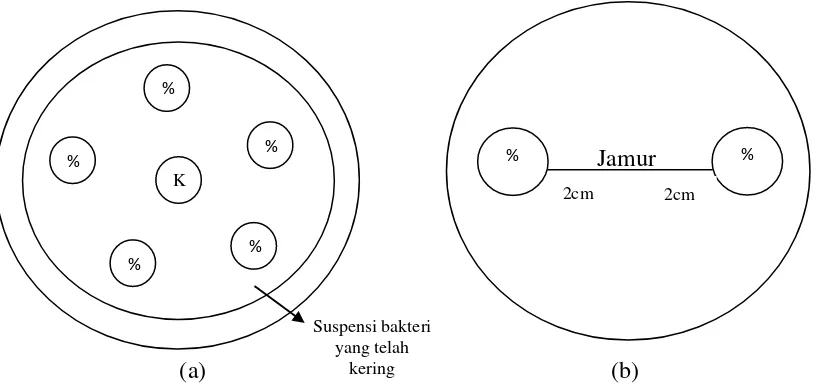
(Gambar 6a).
Pada media tumbuh jamur yang berumur 2 hari diletakkan cakram yang
telah ditetesi ekstrak dengan konsentrasi berbeda dan antibiotik secara teratur
dengan menggunakan pinset steril dan diinkubasi selama 7 hari (Gambar 6b).
Proses pengujian mikroba dapat dilihat pada Lampiran 10.
(a) (b)
Gambar 6. Pola Media Uji; a. Bakteri, b. Jamur
Pengamatan Zona Hambat Pertumbuhan Bakteri dan Jamur
Pengamatan untuk bakteri dilakukan setelah masa inkubasi yaitu dengan
melihat adanya zona hambatan (daerah bening) di sekitar cakram. Diameter zona
hambat diukur dengan jangka sorong. Diameter zona hambat diukur dengan
mengurangkan diameter zona hambat (b) dengan diameter kertas cakram (a)
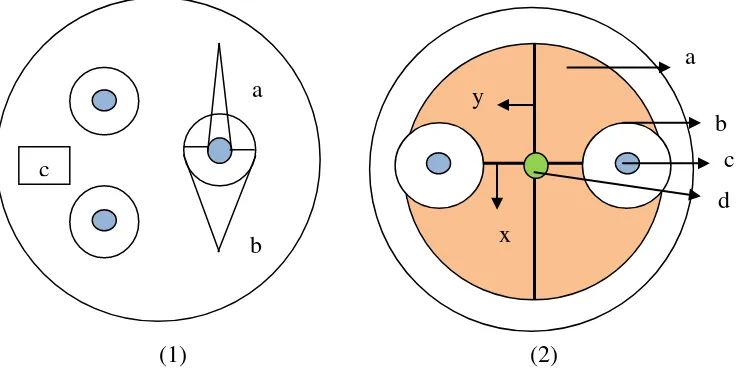
(Gambar 7).
Suspensi bakteri yang telah
kering %
% % Jamur
2cm 2cm
%
K
% %
(1) (2)
Gambar 7. Perhitungan zona hambat; (1) bakteri a: diameter cakram, b: diameter daerah yang tidak ditumbuhi bakteri, c: Daerah yang ditumbuhi bakteri. (2) jamur a: koloni jamur, b: zona hambat, c: cakram, d: titik tengah jamur, x: diameter koloni jamur yang terhambat pertumbuhannya, y: diameter koloni jamur normal.
Pengamatan untuk jamur dilakukan selama 7 hari masa inkubasi yaitu
dengan cara mengukur batas akhir pertumbuhan dari jamur pada sumbu x dan
batas akhir pertumbuhan jamur normal pada sumbu y, kemudian mengurangkan
�−�
2 (Suryanto dkk., 2011)
Analisis Data
Pengujian Fitokimia
Pengujian ini dilakukan untuk mengetahui senyawa-senyawa kimia yang
terdapat di dalam biji teratai. Pengamatan dilakukan langsung setelah pemberian
bahan-bahan sesuai dengan senyawa fitokimia yang akan diuji. a
b c
a
b
c
d y
Pengujian Brine Shrimp
Perlakuan yang diberikan yaitu P0 0% (kontrol), P1 10 ppm, P2 100 ppm
dan P3 1000 ppm. Perlakuan dilakukan sebanyak 5 kali ulangan untuk setiap
konsentrasi. Pengamatan A. salina dilakukan setelah 24 jam. Analisis data menggunakan analisis probit untuk menentukan LC50.
Pengujian Daya Antimikroba
Perlakuan yang diberikan yaitu ekstrak biji teratai yang berbeda yaitu
perlakuan P0 0% (DMSO), P1 50%, P2 60%, P3 70%, P4 80% dan P5 antibiotik
untuk uji antimikroba. Perlakuan dilakukan sebanyak 5 kali ulangan untuk setiap
Hasil Penelitian
Ekstraksi Biji Teratai (Nymphaea pubenscens L.)
Ekstraksi biji teratai dilakukan dengan menggunakan pelarut n-heksana,
etil asetat dan metanol. Hasil ekstraksi biji teratai dapat dilihat pada Tabel 2.
Tabel 2. Hasil ekstraksi pekat biji teratai
n-heksana
Ekstrak pekat 5,5969 4,1706 10,1379
Warna Kuning Hijau kekuningan Merah bata
Uji Fitokimia Biji Teratai
Ekstrak metanol mengandung senyawa alkaloid, fenolik, glikosida,
saponin dan terpenoid/steroid. Ekstrak etil asetat mengandung senyawa alkaloid,
glikosida dan terpenoid/steroid. Ekstrak n-heksana mengandung senyawa
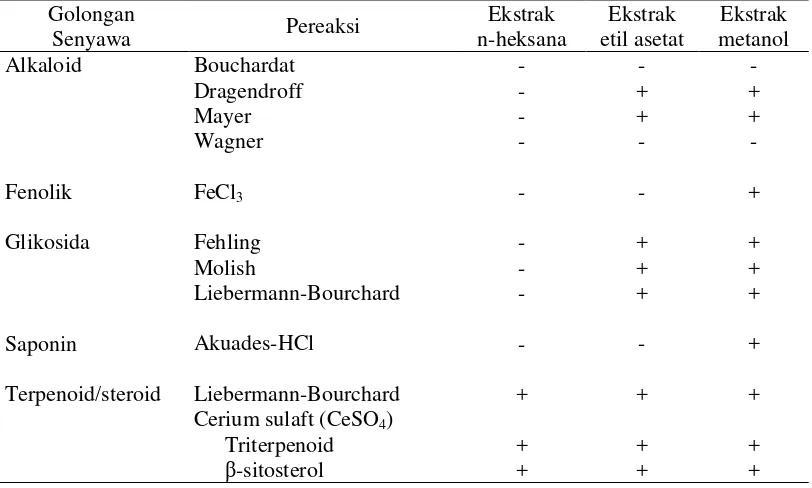
terpenoid/steroid. Hasil pengujian fitokimia biji teratai dapat dilihat pada Tabel 3.
Tabel 3. Hasil uji fitokimia masing-masing ekstrak biji teratai
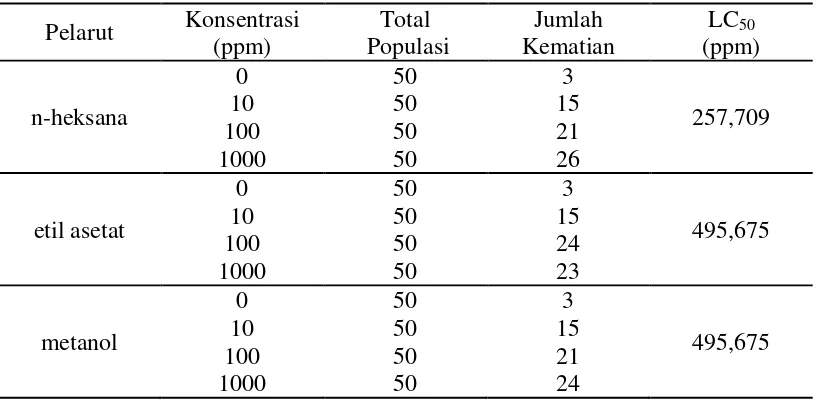
Uji Toksisitas Biji Teratai
Hasil pengujian ekstrak biji teratai terhadap larva A. salina menunjukkan bahwa ekstrak biji teratai bersifat toksik dengan kisaran LC50 antara
250˗500µg/ml dapat dilihat pada Tabel 4.
Tabel 4. Hasil pengamatan LC50 dengan metode BSLT
Pelarut Konsentrasi
Uji Antimikroba Ekstrak Biji Teratai Terhadap Mikroba
Ekstrak biji teratai menunjukkan adanya zona hambat pada ketiga mikroba
uji. Zona hambat terlihat pada bakteri A. hydrophila setelah pengamatan 24 jam
hanya pada pelarut n-heksana. Zona hambat yang terlihat pada bakteri
Table 5. Hasil pengamatan antimikroba dengan metode difusi
Mikroba Konsentrasi Diameter Zona Hambat (mm)
n-heksana etil asetat metanol
A. hydrophila 0
A. hydrophila menunjukkan adanya zona hambat pada ekstrak n-heksana. Besarnya zona hambat yang dihasilkan oleh ekstrak terlihat dengan adanya zona
hambat di sekitar cakram (Gambar 8).
(1) (2) (3)
Gambar 8. Zona hambat ekstrak biji teratai dengan pelarut (1) n-heksana (2) etil asetat (3) metanol terhadap pertumbuhan bakteri A. hydrophila
Hasil pengujian ekstrak biji teratai terhadap pertumbuhan bakteri
zona hambat yang dihasilkan oleh ekstrak terlihat dengan adanya zona hambat di
sekitar cakram (Gambar 9).
(1) (2) (3)
Gambar 9. Zona hambat ekstrak biji teratai dengan pelarut (1) n-heksana (2) etil asetat (3) metanol terhadap pertumbuhan bakteri S. agalactiae
Hasil pengujian ekstrak biji teratai terhadap pertumbuhan jamur
Saprolegnia sp. menunjukkan adanya zona hambat pada setiap ekstrak. Besarnya zona hambat yang dihasilkan oleh ekstrak terlihat dengan terhambatnya
pertumbuhan jamur (Gambar 10).
(1) (2)
(3) (4)
Gambar 10. Zona hambat ekstrak biji teratai dengan pelarut (1) n-heksana (2) etil asetat (3) metanol terhadap pertumbuhan jamur Saprolegnia sp. (4)
kontrol positif dan negatif
Pembahasan
Ekstraksi Biji Teratai (Nymphaea pubenscens L.)
Ekstraksi biji teratai dengan menggunakan pelarut n-heksana, etil asetat
dan metanol diperoleh secara berturut-turut adalah 5,5969 gram, 4,1706 gram dan
10,1379 gram. Hasil penelitian menunjukkan bahwa komponen-komponen
senyawa yang terkandung pada biji teratai lebih banyak terekstrak atau larut pada
pelarut yang bersifat polar. Menurut Sari (2008) pelarut metanol adalah pelarut
yang dapat melarutkan seluruh kandungan kimia dari sampel yang bersifat polar
maupun non polar, karena komponen-komponen tersebut saling terkait satu
dengan lainnya melalui gugus fungsional sehingga komponen kimia yang ada
pada sampel tanaman obat dapat tersari secara sempurna.
Uji Fitokimia Biji Teratai
Hasil uji fitokimia alkaloid menunjukkan hasil negatif pada ekstrak
n-heksana. Ekstrak etil asetat dan metanol negatif pada pereaksi Bouchardat dan
Wagner serta positif pada perekasi Mayer dan Dragendroff ditandai dengan
adanya endapan putih seperti yang terlihat pada Lampiran 11. Menurut Inayah
dkk. (2012) endapan putih yang terbentuk diduga adalah kalium alkaloid. Pada
pembuatan Pereaksi Dragendroff bismuth nitrat dilarutkan dalam HNO3 pekat
agar tidak terjadi reaksi hidrolisis karena garam-garam bismuth mudah
terhidrolisis. Menurut Harborne (1998) uji alkaloid dilakukan berdasarkan reaksi
warna dengan pereaksi Dragendrof dan terbentuk endapan putih dengan pereaksi
Mayer, Hasil positif alkaloid pada uji Wagner ditandai dengan terbentuknya
endapan coklat sampai kuning, diperkirakan endapan tersebut adalah kalium
Hasil uji fitokimia fenolik menunjukkan hasil negatif pada pelarut
n-heksana dan etil asetat serta positif pada pelarut metanol ditandai dengan
terjadinya perubahan warna menjadi biru hitam setelah diberi FeCl3 seperti yang
terlihat pada Lampiran 10. Menurut Sukarja (1992) ciri khas fenolik adalah
terbentuk warna biru atau biru ungu dengan besi (III) klorida. Warna yang
terbentuk diduga berupa besi (III) heksa fenolat sehingga uji ini memberikan
indikasi gugus OH aromatik.
Hasil uji fitokimia glikosida menunjukkan hasil negatif pada pelarut
n-heksana. Hasil positif pada pelarut etil asetat dan metanol ditandai dengan
adanya endapan merah ketika diberi pereaksi Fehling, terbentuk lapisan cincin
ungu ketika diberi pereaksi Molisch dan berwarna ungu ketika diberi pereaksi
Liebermann-Bouchard seperti telihat pada Lampiran 11.
Hasil uji fitokimia saponin menunjukkan hasil negatif pada pelarut
n-heksana dan etil asetat serta positif pada pelarut metanol ditandai dengan
munculnya buih setelah diberi akuades kemudian dikocok dan diberi HCl 2 N
1 tetes selama ± 10 menit seperti yang terlihat pada Lampiran 11. Menurut
Suparjo (2008) saponin merupakan metabolit sekunder yang mengandung gugus
gula terutama glukosa, galaktosa, xylosa, rhamnosa atau methilpetosa yang
berikatan dengan suatu aglikon hidrofobik (sapognin) berupa terpenoid, steroid
alkaloid. Sehingga saponin bersifat polar dan dapat larut dalam air. Saponin juga
bersifat non polar karena memiliki gugus hidrofob yaitu aglikon. Oleh karena
itulah dapat terbentuk busa karena saponin terdirpersi diantara senyawa polar dan
Berdasarkan hasil skrining fitokimia biji teratai dari masing-masing
ekstrak menunjukkan bahwa setiap ekstrak mengandung steroid/terpenoid. Hal ini
ditandai dengan adanya perubahan warna biru kehijauan pada pereaksi
Liebermann-Boucard. Pengujian menggunakan TLC menunjukkan hasil positif
pada pelarut n-heksana, etil asetat dan metanol ditandai dengan adanya perubahan
warna yang sama antara sampel dengan triterpenoida dan β-sitosterol setelah
dipanaskan di atas hot plate dapat dilihat pada Lampiran 11.
Uji Toksisitas Biji Teratai
Uji toksisitas dilakukan untuk mendukung hasil uji antimikroba pada
ekstrak biji teratai. Metode yang digunakan adalah Brine Shrimp Lethality Test
(BSLT) dengan menggunakan A. salina. Uji ini merupakan uji yang paling sederhana sebagai langkah awal untuk menentukan sifat toksisitas dari bahan
alami.
Uji toksisitas dalam penelitian ini dilakukan dengan 10 ekor larva
A .salina yang ditetaskan selama 48 jam. Larva A. salina dimasukkan ke dalam
botol vial yang telah berisi ekstrak dengan konsentrasi 10 ppm, 100 ppm dan
1000 ppm dan ditambah air dengan kadar salinatas 83 ppt sampai 5 ml. Sebagai
kontrol digunakan air dengan kadar salinitas 83 ppt tanpa pemberian ekstrak.
Menurut Meyer dkk. (1982) kategori toksisitas suatu bahan berdasarkan nilai LC50
terbagi menjadi 3 kategori, yaitu sangat toksik bila LC50< 30 µg/ml, toksik bila
LC50 30-1000 µg/ml dan tidak toksik bila LC50>1000 µg/ml. Data awal kematian
A. salina pada berbagai konsentrasi dapat dilihat pada Lampiran 12.
Pengujian ekstrak biji teratai dengan pelarut n-heksana, etil asetat dan
tingkat toksisitas lebih tinggi dengan nilai LC50 257,709 µg/ml dibandingkan
dengan ekstrak etil asetat dan metanol dengan nilai LC50 keduanya
495,675 µg/ml. Menurut Lisdawati dkk. (2006) golongan metabolit sekunder
alkaloid, terpenoid, saponin dan senyawa polifenol yang terdapat di dalam daun
dan buah tanaman mahkota dewa memiliki aktivitas antikanker. Data hasil
perhitungan LC50 dapat dilihat pada Lampiran 13.
Pengujian ekstrak biji teratai terhadap A. salina dengan pelarut n-heksana pada konsentrasi 10 µg/ml tingkat kematian 30% dengan nilai probit 4,61,
konsentrasi 100 µg/ml tingkat kematian 42% dengan nilai probit 4,87 dan
konsentrasi 1000 µg/ml tingkat kematian 52% dengan nilai probit 5,13. Grafik
Log konsentrasi ekstrak biji teratai dengan pelarut n-heksana dapat dilihat pada
Lampiran 13. Aktivitas sitotoksik yang dimiliki ekstrak n-heksana dari beberapa
tanaman seperti tanaman srikaya (Annona squamosa) yang memiliki LC50 sebesar 0,587 µg/ml (Tripiana dkk., 2013), ekstrak n-heksana tumbuhan akar PKI
(Mikania micrantha) yang memiliki LC50 sebesar 2,19 µg/ml (Susanti dkk., 2011), ekstrak n-heksana rimpang temu putih (Curcuma zedoaria (Berg.) Rosc) yang memiliki LC50 sebesar 33,10 µg/ml (Widorini dkk., 2002) dan ekstrak n-heksana
kulit batang kecapi (Sandoricum koetjape Merr) yang memiliki LC50 sebesar 32,44 µg/ml (Utama dkk., 2013).
Pengujian ekstrak biji teratai terhadap A. salina dengan pelarut etil asetat pada konsentrasi 10 µg/ml tingkat kematian 30% dengan nilai probit 4,61,
konsentrasi 100 µg/ml tingkat kematian 48% dengan nilai probit 4,87 dan
konsentrasi 1000 µg/ml tingkat kematian 46% dengan nilai probit 4,87. Grafik
Lampiran 13. Aktivitas sitotoksik yang dimiliki ekstrak n-heksana dari beberapa
tanaman seperti daun pandan wangi (Pandanus amaryllifoliur Roxb) yang memiliki LC50 sebesar 288,4 µg/ml (Sukandar dkk., 2008), ekstrak etil asetat
tumbuhan akar PKI (Mikania micrantha) yang memiliki LC50 sebesar 13,49 µg/ml (Susanti dkk., 2011), ekstrak etil asetat tumbuhan paku (Christella arida) yang memiliki LC50 sebesar 13,301 µg/ml (Aprealia and Suyatno, 2013) dan ekstrak
etil asetat kulit batang kecapi (Sandoricum koetjape Merr) yang memiliki LC50 sebesar 179,43 µg/ml (Utamadkk., 2013).
Pengujian ekstrak biji teratai terhadap A. salina dengan pelarut metanol pada konsentrasi 10 µg/ml tingkat kematian 30% dengan nilai probit 4,61,
konsentrasi 100 µg/ml tingkat kematian 46% dengan nilai probit 4,87 dan
konsentrasi 1000 µg/ml tingkat kematian 48% dengan nilai probit 4,87. Grafik
Log konsentrasi ekstrak biji teratai dengan pelarut etil asetat dapat dilihat pada
Lampiran 13. Aktivitas sitotoksik yang dimiliki ekstrak n-heksana dari beberapa
tanaman seperti tanaman srikaya (Annona squamosa) yang memiliki LC50 sebesar 0,857 µg/ml (Tripianadkk., 2013), ekstrak metanol tumbuhan akar PKI (Mikania micrantha) yang memiliki LC50 sebesar 2,19 µg/ml (Susanti, 2011) dan ekstrak
metanol daging buah pare (Momordica charantia L.) yang memiliki LC50 sebesar 74,99 µg/ml (Bawa, 2009).
Hasil penelitian menunjukkan semakin tinggi konsentrasi ekstrak yang
diberikan semakin besar jumlah A. salina yang mati. Kematian larva A. salina
terbesar terdapat pada ekstrak n-heksana konsentrasi 1000 ppm yang
yang sama menyebabkan kematian larva 46% dan ekstrak metanol menyebabkan
kematian larva 48%.
Kematian larva disebabkan oleh senyawa-senyawa yang terkandung di
dalam ekstrak biji teratai yang dapat mengganggu proses pencernaan A. salina, Cahyadi (2009) menyatakan cara kerja senyawa-senyawa yang terkandung dalam
ekstrak adalah dengan bertindak sebagai stomach poisoning atau racun perut. Oleh karena itu bila senyawa-senyawa ini masuk ke dalam tubuh larva, alat
pencernaannya akan terganggu. Selain itu senyawa ini menghambat reseptor
perasa pada daerah mulut larva. Hal ini mengakibatkan larva gagal mendapatkan
stimulus rasa sehingga tidak mampu mengenali makanannya sehingga larva mati
kelaparan.
Ekstrak yang dihasilkan dengan pelarut n-heksana mengandung senyawa
non polar yang mudah untuk masuk ke dalam membran sel melalui proses difusi
yang menyebabkan sel lebih cepat mengalami kerusakan atau mati. Ekstrak yang
dihasilkan dengan pelarut etil asetat dan metanol mengandung senyawa semi polar
dan polar. Senyawa semi polar dan polar tidak mudah berdifusi memasuki dinding
sel atau membran, hal ini mengakibatkan senyawa semi polar dan polar lebih sulit
untuk masuk ke dalam dinding sel sehingga nilai ketoksikan senyawa semi polar
dan polar lebih rendah.
Menurut Mukti dkk (2012), proses difusi pada sel terjadi akibat
kecenderungan dari substansi yang bergerak dari daerah dengan konsentrasi tinggi
ke daerah dengan konsentrasi yang rendah. Pelarut non polar hanya dapat
melarutkan senyawa-senyawa non polar sehingga pelarut semi polar tidak dapat