SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa tesis yang berjudul :"Efektivitas Suplementasi Selenium (Se) Organik dan Vitamin E dalam Ransum Komersial terhadap Reproduksi Puyuh" adalah benar hasil karya saya sendiri dengan arahan dari komisi pembimbing dan belum pernah dipublikasikan kepada jurnal ilmiah manapun. Sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan daiam teks dan dicantumkan dalam Dafiar Pustaka di bagian akhir tesis ini.
Bogor, April 2007
Filri Nova Liya Lztbis
EFEKTIVITAS SWLEMENTASI SELENIUM ORGANIK DAN VITAMIN E DALAM RANSUM KOMERSIAL
TERHADAP REPRODUKSI PUYUH'
(Effect of Supplementation Organic Selenium
and Vitamin E in Commercial Diets on Reproduction of Quails)
This study was aimed to determine the effect of supplementation of Se organic and vitamin E in commercial diets on consumption, egg production, fertility, hatchability and progeny performances. The treatments were supplementation of Se organic (SI = 0.5 ppm and S2 = 1 ppm) and vitamin E (El = 50 ppm dan E2 = 100 ppm) in different commercial diets (P and G). Four hundred twenty female and male quails (ratio 1 : 1) aged 3 weeks old were divided into 10 treatment groups with 3 replicates. Each replicate consisted of 14 quails
.
Two groups as control consisted of two kinds of commercial diets (P and G) without supplementation of Se organic and vitamin E. The eight remaining groups were the groups given the combinations of Se organic and vitamin E at different levels in P and G diets. The results showed that the level of Se organic and vitamin E at 0.5 ppm Se and 100 ppm vitamin E in the two commercial diets significantly (p<0.05) improved the egg production as compared to the control groups. Meanwhile, all the treatments increased the Se and vitamin E content in egg and blood and increased the GSH-Px activities in blood and liver. The Supplementation of Se organic and vitamin E at 1 ppm Se and 100 vitamin E in the two commercial diets significantly (p<0.05) improved fertility, hatchability, hatched weight, mortality, body weight gain and feed conversion of progeny. From this study it was concluded that the supplementations of Se organic and vitamin E in the diets improved reproduction of the quails which were reflected on fertility, hatchability, hatched weight and decreased the mortality number of the progeny. The supplementations of Se organic and vitamin E in the diets improved egg quality, it showed with the bigger egg, higher Se and vitamin E content in the egg.8 Hak cipta milik Institut Pertanian Bogor, tahun 2007 Hak cipta dilindungi
Dilarang mengutip dun menzperbanyak tanpa izin tertzrlis dari
EFEKTIVITAS SUPLEMENTASI SELENIUM ORGANIK
DAN VITAMIN E DALAM RANSUM KOMERSIAL
TERHADAPREPRODUKSIPUYUH
FITRI NOVA LIYA LUBIS
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Ternak
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Efektivitas Suplementasi Selenium Organik dan Vitamin E dalam Ransum Komersial terhadap Reproduksi Puyuh
Nama : Fitri Nova Liya Lubis
NRP : D 051034021
Program Studi : Ilmu Ternak
Disetujui
Komisi Pembimbing
,1..
-
-0Prof. Dr. Ir. Wiranda G ~ilia%. M.Sc. Dr. drh. Tutv Laswardi Yusuf. M.S.
Ketua Anggota
Ketua Program Studi
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas segala rahmat dan karunia-Nya, sehingga k a y a ilmiah ini berhasil diselesaikan. Tema yang
dipilih dalam peneiitian ini adalah : Efektivitas Suplementasi Selenium (Se) Organik dan Vitamin E dalam Ransum Komersial terhadap Reproduksi Puyuh
Ucapan terima kasih penulis sampaikan kepada Ibu Prof. Dr. Ir. Wiranda
G Piliang, M.Sc. dan Ibu Dr. drh. Tuty Laswardi Yusuf, M.S. sebagai komisi
pembimhing yang telah dengan sabar memberikan bimbingan dan saran-saran
sejak awal penelitian hingga karya ilmiah ini selesai, serta kepada Bapak Dr. Ir.
Asep Sudarman M. Rur.Sc sebagai penguji luar komisi.
Terima kasih yang setinggi-tingginya penulis sampaikan kepada Ayahanda
Amrin Lubis dan Ihunda Susyatini tercinta, terkasih dan tersayang atas semua
pengorhanan, kesabaran, doa juga kasih sayangnya. Terima kasih kepada kakakku
Ika, adikku Popo, Dedi, Rizki, Mas Syahrir serta semua keluarga yang telah
memberikan motivasi dan doanya. Kepada teman-teman terbaikku Ratna, Ibu
Lanjarsih, Pak Amir, Ika, Diah, Kemala, Daud, Pak Rusdin, Eni, Reni, Mbak Messi dan Rahmi. Teman-teman PTK 2003 dan PTK 2004 serta semua pihak
yang telah banyak membantu penulis selama penelitian.
Terima kasih juga penulis sampaikan kepada Bapak Isra Noor, D.V.M
dari PT Alltech dan Bapak Suredi dari PT BASF yang telah memberikan bantuan
selenium organik dan vitamin E sehingga penelitian ini dapat terselesaikan.
Terima Kasih.
Semoga karya ilmiah ini bermanfaat untuk perkembangan ilmu
pengetahuan.
Bogor, April 2007
RIWAYAT HIDUP
Penulis dilahirkan di Kisaran pada tanggal 5 Desember 1980 dari
Ayahanda Amrin Lubis dan lbunda Susyatini sebagai anak ke dua dari lima
bersaudara
Penulis lulus sebagai Sarjana Peternakan, Program Studi Produksi Ternak
di Universitas Andalas, Padang, Sumatera Barat pada Oktober 2002. Pendidikan lanjutan ditempuh pada Sekolah Pascasarjana di Institut Pertanian Bogor, Program
DAFTAR
IS1
Halaman
PRAKATA
..
DAFTAR TABEL
...
11...
DAFTAR GAMBAR...
111DAFTAR LAMPIRAN
...
ivPENDAHULUAN
...
1Latar Belakang
. .
...
1Tujuan Penel~t~an
. .
...
3...
Manfaat Penel~t~an 3...
TINJAUAN PUSTAKA 4 Burung Puyuh. .
...
4Fert~l~tas dan Daya Tetas
...
6Peranan Nutrisi Selenium dan Vitamin E
...
6Selenium Organik dan Inorganik
...
9Metabolisme Selenium Organik dan Inorganik
...
12Vitamin E
...
14Metabolisme Vitamin E
...
15Selenium dan Vitamin E sebagai Antioksidan
...
15Peranan Selenium dan Vitamin E pada Embrio
...
20MATERI DAN METODE PENELITIAN
...
22. .
Tempat dan Waktu Peneht~an.
.
...
22Materi Penelit~an
.
...
24.
Metode Penel~t~an.
...
.
24Rancangan Penel~t~an
...
25Peubah yang Diukur
...
26HASIL DAN PEMBAHASAN
...
32Umur mulai bertelur
...
32Konsumsi ransum
...
33Produksi telur
...
35Konversi
...
38Panjang saluran reproduksi
...
40...
Berat hati 41 Berat otak...
42Selenium otak
...
43Selenium darah
...
45Selenium hati
...
46Vitamin E darah
...
48...
Vitamin E telur 49 Aktivitas enzim glutathione darah...
51Aktivitas enzim glutathione hati
. .
...
52Fert~htas
...
53Daya tetas
...
55Bobot tetas
...
57Mortalitas
...
58Konsumsi anak
...
61Pertambahan bobot badan anak
...
62Konversi
...
64PEMBAHASAN UMUM
...
65SIMPULAN
...
67DAFTAR PUSTAKA
...
69DAFTAR TABEL
Nomor Halaman
1
.
Kandungan nutrisi telur puyuh...
5. .
. .
2
.
Komposisi nutrisi ransurn kontrol...
24...
3
.
Perlakuan suplementasi selenium dan vitamin E 25. .
. .
4
.
Komposisi nutrisi ransum anak...
30...
DAFTAR GAMBAR
Halaman
1
.
Keseimbangan antioksidan dan prooksidan pada organisme...
72
.
Mekanisme transportasi dan absorbsi selenium...
123
.
Metabolisme selenium di dalam tubuh...
134
.
Level pertahanan antioksidan di dalam sel...
185 Hubungan antara selenium dan vitamin E pada proses embriogenesis
...
21. .
6.
Alur penelltlan...
237
.
Umur mulai bertelur dengan suplementasi Se dan vitamin E...
328
.
Konsumsi (glekor) dengan suplementasi Se dan vitamin E...
349
.
Produksi telur Hen Day (%) dengan suplementasi Se dan vitamin E...
3510
.
Produksi telur (gram) dengan suplementasi Se dan vitamin E...
381 1
.
Konversi ransum dengan suplementasi Se dan vitamin E...
3912
.
Panjang oviduct (cm) dengan suplementasi Se dan vitamin E...
4013
.
Berat hati (gram) dengan suplementasi Sedan vitamin E...
42...
14.
Berat otak (gram) dengan Suplementasi Se dan vitamin E 43 15.
Kadar Se otak dengan suplementasi Se dan vitamin E...
4416
.
Kadar Se darah dengan suplementasi Se dan vitamin E...
45...
17.
Kadar Se hati dengan suplementasi Se dan vitamin E 46...
18.
Kadar Se telur dengan suplementasi Se dan vitamin E 47 19.
Kadar vitamin E darah dengan suplementasi Se dan vitamin E...
49...
20.
Kadar vitamin E telur dengan suplementasi Se dan vitamin E 50 21.
Aktivitas GSH-Px darah dengan suplementasi Se dan vitamin E...
5122
.
Aktivitas GSH-Px Hati dengan suplementasi Se. .
dan vltamln E...
5225
.
Bobot tetas DOQ dengan suplementasi Se dan vitamin E...
5726
.
Mortalitas anak selama I minggu...
27
.
Konsumsi anak (gram/ekor/4minggu)...
6128
.
Pertambahan Bobot Badan (gr/ekor/4minggu)...
63DAFTAR LAMPIRAN
1. Analisa ragam dan uji lanjut Duncan pada umur mulai bertelur
...
782. Analisa ragam dan uji lanjut Duncan pada konsumsi
produksi telur dan konversi
...
803. Analisa ragam dan ilji lanjut Duncan pada panjang
saluran reproduksi, berat hati dan berat otak
...
85 4. Analisa ragam dan uji lanjut Duncan pada fertilitas,daya tetas dan bobot tetas
...
885. Analisa ragam dan uji lanjut Duncan pada
mortalitas selama 2 minggu
...
946 . Analisa ragam dan uji ianjut Duncan pada konsumsi
PENDANULUAN
Kebutuhan akan protein hewani yang semakin meningkat maka
dibutuhkan usaha-usaha untuk meningkatkan produksi ternak. Puyuh merupakan
salah satu komoditi ternak yang diandalkan untuk memenuhi kebutuhan protein
hewani tersebut. Hal ini disebabkan karena puyuh menghasilkan telur konsumsi
yang mempunyai nilai gizi yang tinggi, tidak kalah dengan telur unggas lainnya,
telur puyuh mengandung protein 13.1% dan lemak 11.1%, dengan kandungan protein yang tinggi dan kadar lemak rendah tersebut maka telur puyuh sangat baik
dikonsumsi oleh orang-orang yang sedang diet kolestrol. Daging puyuh juga dapat
dikonsumsi dengan kandungan protein 21.10% dan lelnak hanya 7.7%. Dipandang dari segi ekonomi, di setiap umur puyuh mempunyai nilai jual yang
cukup tinggi, dari telur konsumsi, telur tetas, hingga bibit dan afiirannya.
Disamping itu puyuh cepat menghasilkan telur dengan produksi yang cukup
tinggi, di mana puyuh betina sudah mampu menghasilkan telur pada umur 41 hari
dengan produksi 250-300 butir telur pertahun. Keunggulan lainnya adalah cara
pemeliharaannya mudah. Karena itu perlu dilakukan upaya untuk meningkatkan
populasi puyuh melalui peningkatan reproduksi.
Peningkatan fertilitas dan daya tetas merupakan peningkatan reproduksi
puyuh dalam upaya mempekahankan dan meningkatkan populasi puyuh. Beberapa faktor mempengaruhi upaya ini, yailu faktor genetik dan faktor
lingkungan. Salah satu faktor lingkungan yang sangat berpengaruh terhadap
reproduksi adalah faktor makanan, selain itu penggunaan pejantan yang seimbang
dalam sekelompok induk juga ikut berpengaruh.
Kehidupan embrio puyuh berada di luar tubuh induk dan sangat
bergantung pada kondisi telur karena kebutuhan embrio akan makanan
bergantung pada ketersediaan zat-zat makanan dalam telur yang merupakan
sumber makanan embrio. Oleh karena itu komposisi nutrisi telur tetas yang baik
akan mendukung perkembangan embrio. Kandungan zat gizi telur sangat tergantung pada kandungan zat gizi dalam pakan yang dimakan oleh induk,
sehingga pemberian pakan induk yang baik akan menghasilkan
merupakan komponen zat gizi pakan yang sangat dibutuhkan dan berpengaruh terhadap reproduksi puyuh dan komposisi yang sesuai
dengan kebutuhan ternak akan dapat meningkatkan reproduksi ternak.
Selenium merupakan kelompok trace mineral, yang penting untuk pertumbuhan dan reproduksi. Se berinteraksi dengan vitamin E sebagai nutrisi
antioksidan yang berperan meningkatkan fertilitas, perkembangan embrio dan
daya tetas telur serta meningkatkan daya tahan bidup anak yang baru menetas,
sehingga menurunkan kematian. Selenium dibedakan dalam dua bentuk yaitu
organik dan inorganik. Se organik memiliki potensi biologis 50% lebih besar dari
Se inorganik karena konsentrasi Se organik pada jaringan dideposit lebih besar
dibandingkan dengan Se inorganik (McDowell 1992). Transfer Se organik dari
makanan induk ke telur dan jaringan embrio lebih efisien dibandingkan Se
inorganik dan berperan memperbaiki pertahanan antioksidan anak yang baru
menetas sehingga akan meningkatkan daya tahan hidup anak. Disamping itu Se
organik dapat memperbaiki kualitas telur dan tidak toksik (Surai 2003). Namun
demikian Se kalau diberikan terlalu banyak atau sebaliknya terlalu sedikit akan
menimbulkan kerugian produksi peternakan karena itu dibutuhkan level optimum
yang mendukung peningkatan reproduksi. Rekomendasi National Research
Council (NRC) (1994) ternak puyuh bibit membutuhkan selenium 0.2 mg/kg
ransum.
Berdasarkan hal-ha1 di atas maka dilaksanakanlah penelitian tentang
reproduksi puyuh yang diberi suplementasi mineral selenium organik dan vitamin
E dalam ransum. Suplementasi Se organik dan vitamin E sampai level tertentu
diharapkan akan meningkatkan reproduksi bempa fertilitas dan daya tetas telur
Tujuan Penetitian
Penelitian ini bertujuan untuk membuktikan efektivitas suplementasi
selenium organik dan vitamin E terhadap: (1) umur mulai bertelur, produksi telur,
fertilitas dan daya tetas. (2) Kandungan selenium hati, otak, darah dan telur. (3)
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat menyumbangkan tambahan informasi
dalam pengembangan ilmu petemakan terutama tentang reproduksi ternak puyuh
yang diberi pakan dengan suplementasi mineral selenium organik dan vitamin E
Hipotesis Penelitian
Suplementasi selenium organik dan vitamin E dalam ransum dapat meningkatkan:
1. Produksi telur, fertilitas dan daya tetas.
2. Kandungan selenium dan vitamin E telur
TINJAUAN PUSTAKA
Burung Puyuh
Bangsa burung puyuh hampir terdapat diseluruh belahan dunia yaitu benua
Amerika, Eropa, Afrika, Asia sampai Australia (Woodard et al. 1973). Dikatakan pula bahwa burung puyuh termasuk genus Cotzrrnix dari family Phasianidae. Di
Indonesia burung puyuh yang biasa dipelihara adalah Coturnix-coturnix japonica.
Wilson et al. (1961) mengatakan bahwa burung puyuh betina mulai
bertelur pada umur 35 hari (rata-rata 40 hari) dan berproduksi penuh pada umur
50 hari. Dalam lingkungan yang sesuai puyuh berproduksi dalam periode yang
lama, menghasilkan telur rata-rata 250 butir pertahun. Puyuh mampu
menghasilkan 3 sampai 4 generasi dalam satu tahun. Menurut Yuwanta (1998)
produksi telur ditentukan oleh produksi ovum, dan produksi ovum ditentukan oleh
jumlah pakan yang dikonsumi. Produksi telur yang tinggi sampai akhir produksi dapat dicapai dengan memberikan makanan yang berkualitas baik yang sesuai
dengan kebutuhan. Sedangkan Woodard et al. (1973) mengemukakan bahwa
waktu untuk pertama kali bertelur pada burung puyuh dicapai pada umur sekitar
42 hari, dimana dewasa kelamin lebih cepat dicapai oleh puyuh betina namun
dewasa tubuh lebih cepat oleh puyuh jantan. Kemudian dikatakan bahwa
kematangan seksual puyuh dicapai pada pakan yang mengandung 25% protein sedangkan pada level 20% protein diperoleh produksi, fertilitas dan daya tetas
telur yang optimal, disamping itu puyuh juga membutuhkan beberapa trace
element seperti zinc, selenium dan magnesium.
Fertilitas optimum diperoleh dari perkawinan rasio I jantan dengan 1 atau
2 betina, fertilitas yang rendab dengan rasio perkawinan yang tinggi disebabkan
oleh preferensi tingkah laku kawin (Woodard dan Abplanalp, 1967). Selama
penyimpanan daya tetas telur menurun secara konstan sekitar 3% perhari.
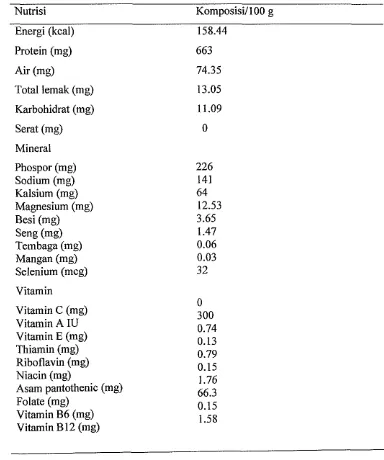
Tabel 1 Kandungan nutrisi telur puyuh (Riana 2000)
Nutrisi Komposisi/100 g
Energi (kcal) 158.44
Protein (mg) 663
Air (mg) 74.35
Total lemak (mg) 13.05
Karbohidrat (mg) 11.09
Serat (mg) 0
Mineral
Phospor (mg) 226
Sodium (mg) 141
Kalsium (mg) 64
Magnesium (mg) 12.53
Besi (mg) 3.65
Seng (mg) 1.47
Tembaga (mg) 0.06
Mangan (mg) 0.03
Selenium (mcg) 32
Vitamin
Vitamin C (mg) 0
Vitamin A IU 300 0.74
Vitamin E (mg) 0.13
Thiamin (mg) 0.79
Riboflavin (mg) 0.15
Niacin (mg) 1.76
Asam pantothenic (mg) 66.3
Folate (mg) 0.15
Vitamin B6 (mg) 1.58
Vitamin B12 (mg)
Umur induk berpengaruh terhadap daya tetas, dimana daya tetas telur
maksimum terjadi pada umur induk 8-24 minggu (Woodard ef al. 1973). Selanjutnya dijelaskan bahwa kematian sebagian besar embrio puyuh terjadi
selama 3 hari pertama inkubasi dan sesaat sebelum menetas. Puncak kematian
umumnya disebabkan ketidakmampuan embrio berkembang membentuk organ
meliputi: pertukaran posisi embrio sebelum pipping (pemecahan kerahang),
pemanfaatan sisa albumen dan penyerapan kantong kuning telur.
Woodard dan Wilson (1963) menyebutkan bahwa Telur puyuh
mempunyai karakteristik pola warna yang bervariasi mulai dari coklat gelap, putih kekuningan dengan corak wama hitam, coklat atau bim. Telur puyuh pertama
lebih kecil dibandingkan dengan telur puyuh berikutnya. Kemudian Mohmond
dan Coleman (1967) melaporkan bahwa proporsi relatif dari telur puyuh adalah
47.4% albumen, 31.9% kuning telur, 20.7% memhran dan kerabang telur,
sedangkan ketebalan kerabang dan membran adalah 0.197 dan 0.063 mm. Berat
rata-rata telur puyuh 10 gram (sekitar 8% dari bemt tubuh betina).
Fertilitas dan Daya tetas
Fertilitas telur dipengaruhi oleh banyak faktor antara lain adalah kualitas
sperma, kualitas ransum dan umur induk (North dan Bell 1990; Funk dan Irwin
1955). Fertilitas akan menurun apabila induk dan pejantan puyuh telah berusia
lebih dari enam bulan (Woodard dan Abplanalp 1967)
North dan Bell (1990) mengemukakan bahwa ada 2 pengertian daya tetas,
yang pertama adalah persentase telur yang menetas dari sejumlah telur yang
ditetaskan. Kedua adalah persentase telur yang menetas dari telur yang fertil.
Banyak faktor yang dapat mempengaruhi daya tetas, diautaranya adalah umur
telur atau lamanya penyimpanan telur (Fasenko et al. 1992), dan ukuran telur
(Tullet dan Burton 1982). Imbangan antara jantan dan induk juga akan
mempengaruhi daya tetas (McDaniel et al. 1981), kualitas jantan ikut berperan
dalam daya Letas. Inovasi dalam manajemen penetasan dan teknologi penetasan
berkaitan erat dengan mortalitas embrio (Roque dan Soares 1994).
Peranan Selenium (Se) dan Vitamin E
Bowie and O'Neill (2000) menyatakan bahwa keseimbangan antioksidan
dan prooksidan merupakan unsur penting dalam pembentukan gen. Selanjutnya dikatakan bahwa keseimbangan antioksidan merupakan salah satu jalan untuk
memelihara efisiensi produksi dan reproduksi pada temak. Gambar 1 menjelaskan
keseimbangan antioksidan-prooksidan di mana selenium dan vitamin E sebagai
Pertahanan Antioksidan Kondisi Stres
Antioksidan dalam pakan Se ,Mn Faktor
(Vitamin A, E, C, Carotenoid, Zn, Cu nutrisi Toksik, PUFA tinggi Flavonoid
1
1
Defistensi vitamin E Se, Mn, Zn,kelebihan Fe Pakan optimum7
Kondisi Lingkungan Optimun
I
Pencegahan penyakit dan pengobatan dengan antibotik dan obat-obatan lain
I
Lingkungan
r
Temperature,Kelembaban, radiasi ultraviolet etc
Internal Penyakit, bakteri, virus, alergi
Vitamin A,E,C, Carotenoid, Glutathione, transpor elehon, phagosit,
asam urea, Enzim antioksidan (SOD,GSH- oksidasi xantin Px, Catalase)
I
I
Kerusakan membran+
.
C
Penurunan kualitas hidup
Kemunduran cita rasa susu Peroksidasi lemak,
9
1
+--- kerusakan lemak Penurunan absorsi Sistem antioksidan organisme
Ketidakmampuan
J
DNAnutrisi
sistem kekebalan
1
Ketidakseimbangan nutrisi
I
Pembentukan radikal
C
Merugikan terhadap pembuluh
4
darah, hati,otak,syaraf dan sistem
----.-
Produksi dan Performance [image:21.559.87.493.57.556.2]otot reproduksi buruk.
Gambar 1 Keseimbangan antioksidan-prooksidan pada organisme (Surai 2003)
Jaeschke (1995) menyebutkan bahwa kondisi stres berhubungan dengan
produksi radikal bebas yang menyebabkan stres oksidasi, dan keseimbangan
prooksidan-antioksidan berpotensi mengakibatkan kerusakan jaringan.
Selanjutnya Dalton et al. (1999) menerangkan bahwa berbagai kondisi stres merangsang pembentukkan radikal bebas yang disebabkan penurunan rangkaian
kerusakan elektron dan produksi radikal superoksida yang berlebihan. Kondisi stres secara umum dibagi kedalam tiga kategori utama. Kategori terpenting adalah
stres nutrisi meliputi level tinggi asam lemak polyunsaturated pada pakan, defisiensi vitamin E, Selenium, Zinc atau mangan, kelebihan besi, hipervitaminosis A dan kehadiran bemacam-macam racun serta komponen- komponen racun. Kelompok kedua adalah stres kondisi lingkungan seperti
peningkatan temperatur, kelembapan, radiasi dan lain-lain. Kategori ketiga yaitu
stres internal yang disebabkan oleh bermacam-macam bakteri atau virus
penyebab penyakit. Selain itu penetasan, anak yang berada pada inkubator sesaat
setelah menetas, pengangkutan dari inkubator ke kandang serta vaksinasi dapat
meningkatkan stres.
Produksi radikal bebas melebihi kapasitas sistem antioksidan untuk
menetralkan peroksida lemak mengakibatkan kerusakan lemak tak jenuh pada sel membran, asam amino pada protein dan nukleotida pada DNA. Sebagai basilnya
keutuban sel dan membran terganggu (Surai 1999). Kerusakan membran dapat
mengakibatkan penurunan efisiensi absorbi nutrisi (meliputi vitamin larut dalam
air) dan menimbulkan ketidakseimbangan vitamin, asam amino dan Inorganik.
Keadaan ini mengakibatkan penurunan produksi dan penampilan reproduksi, kondisi ini semakin memburuk dengan penurunan kekebalan dan perubahan pada
Cardiovascular, otak, saraf dan otot disebabkan peningkatan peroksida lemak.
Surai (2003) mengatakan bahwa konsumsi nutrisi antioksidan pada pakan
dapat memelihara status antioksidan alami ternak. Selanjutnya dijelaskan bahwa penyediaan optimal selenium organik (Se) dengan kombinasi vitamin E
memperbaiki stres dan daya tahan terhadap penyakit sebagai hasilnya performa
produksi dan reproduksi meningkat. Kerja Se berhubungan erat dengan antioksidan lainnya terutama vitamin E, manfaat selenium pada dasmya
terbentuk dari interaksi dengan vitamin E. Menurut Wilson (1997), dalam
perkembangan embrio vitamin E dan selenium saling berinteraksi. Selanjutnya
MacPherson (1994) menyatakan bahwa aktivitas Se dan vitamin E bekeja secara
sinergis sebagai antioksidan utama menghilangkan radikal lemak, radial bebas
oksigen atau metabolit reactive oksigen yang merupakan bagian yang penting dari
penyakit bila pola mekanisme pertahanannya berlebihan. Sitompul (2003)
menjelaskan bahwa peran antioksidan diartikan sebagai suatu fungsi homeostatis
dari organisme untuk menanggulangi akibat kerusakkan sel, jaringan dan organ
akibat pengaruh radikal bebas.
Selenium dapat menghemat atau mengurangi kebutuhan vitamin E dengan
liga cara: (1) menjaga fungsi pankreas, yang membuat pencemaan lemak normal
sehingga penyerapan vitamin E lebih baik; (2) menurunkan jumlah vitamin E
yang dibutuhkan untuk menjaga keutuhan membran lemak melalui GSH-Px; (3)
membantu retensi vitamin E dalam plasma darah (Scott et al. 1982). Selanjutnya dikatakan bahwa vitamin E dapat mengurangi kebutuhan selenium dengan cara:
(1) mencegah hilangnya selenium dari tubuh dengan jalan mempertahankan
selenium dalam tubuh dalam bentuk aktif; (2) mencegah terjadinya rantai oto-
oksidasi yang reaktif dalam membran sehingga menghambat produksi
hidroperoksida.
Selenium Organik dan Inorganik
Selenium suatu unsur semilogam (metalloid) yang mempunyai sifat-sifat
kimia mirip dengan sulfur. Selenium mempunyai nomor atom 34 dan berat atom 78.96. (McDowell 1992). Dalam beberapa nomor senyawa, Se menggantikan S
atau Se ditemukan sebagai kompleks dengan S melalui ikatan kovalen koordinat
(Scott et al. 1982). Mineral Se dapat direduksi menjadi bentuk oksidasi -2
(selenida) atau dioksidasi menjadi bentuk reduksi +4 (selenit) atau +6 (selenat)
(McDowell 1992). Se mempunyai dua bentuk asam yaitu selenious (HzSe03) dan
selenic (H2Se04), dimana dalam bentuk garamnya berturut-turut adalah selenit
dan selenat (Georgievskii 1982). Tanaman dan mikroorganisma dapat mengganti
S dalam sistein dan methionine dengan Se dengan demikian menghasilkan
selenosistein dan selenomethionin (Scott et al. 1982).
Selenium secara kimiawi mempunyai 2 bentuk, organik dan inorganik.
Selenium inorganik dapat ditemukan dalam bentuk logam selenit, selenat dan
selenide. Sebaliknya dalam unsur sayuran selenium merupakan bagian dari asam-
asam amino meliputi methionine dan sisteine yang menggantikan sulfur. Di alam
ternak menerima selenium terutama dalam bentuk organik (Surai 1999).
sumber utamanya terdapat pada selenium tumbuhan (Levander 1986). Total
selenium di dalam tumbuhan dan biji-bijian 50-80% merupakan selenoaminoacid
yang terikat didalam protein sebagai Selenomethionin dan selenosistine (Butler
dan Peterson 1967).
Keterbatasan penggunaan selenium inorganik adalah dapat bersifat racun,
penyimpanan rendah, efisiensi transfer ke susu dan daging rendah dan
kemampuan untuk mempertahankan cadangan selenium tubuh rendah, sehingga
sebagian besar dari selenium yang dikonsumsi akan diekskresikan (Surai 1999).
Selenomethionin tidak dapat disintesis dari selenit atau selenat pada temak, tetapi selenosistein dapat ditemukan pada tubuh ternak yang mengkonsumsi selenium
inorganik seperti selenit dan selenat, ha1 ini disebabkan karena selenosistein
tergabung didalamnya sintesis glutathione dan selenoprotein lainnya (Sunde
1990). Unggas tidak dapat mensintesis sistein sehingga Selenomethionin
dibutuhkan untuk konversi Selenomethionin menjadi selenosistein.
Selenomethionin berubah menjadi selenosistein melalui enzim sistothionase
(Esaki et al. 1981). Lebih lanjut Sunde (1990) memaparkan, selenosistein dapat
menggantikan sistein pada banyak protein, agar selenosistein dapat bergabung
kedalam selenoprotein maka dibutuhkan reaksi selenosistein-P-lyase. Arthur (1997) mengatakan bahwa selenium organik harus berubah dari bentuk dasar
organik kedalam bentuk inorganik dan kemudian kembali lagi kedalam bentuk
organik untuk memenuhi fungsi biologisnya dalam sintesis selenoprotein.
Kemudian Hawks et al. (1985) menambahkan bahwa 30-80% dari selenium
didalam tubuh adalah selenosistein. Selenosistein adalah asam amino yang sangat
penting dalam sintesis sitosolik glutathione peroksidase (Rotruck et al. 1973).
Pada umumnya deposit Se dalam jaringan mempunyai konsentrasi lebih tinggi
bila Se tersedia dalam bentuk organik dibandingkan dalam bentuk inorganik
(McDowell 1992).
Kelebihan selenium organik dibandingkan dengan selenium inorganik
menurut Surai (2003) adalah dapat berakumulasi pada jaringan dalam
menyediakan cadangan selenium. Cadangan selenoarninoacid akan digunakan
pada kondisi shes untuk sintesis selenoprotein dan mengatasi pengaruh buruk
embrio dapat memperbaiki pertahanan antioksidan anak yang baru menetas dan
meningkatkan resistensi terhadap penyakit serta memperbaiki daya tahan hidup
anak. Transfer Se ketelur dan daging lebih efektif sehingga menghasilkan produk
ternak yang dapat dikonsumsi kaya kandungan Se. Se organik memiliki sifat antioksidan sedangkan Se inorganik bersifat prooksidan dapat memicu
pembentukan superoksida dan stres oksidasi melalui reaksi reduksi dengan
glutathion. Selenomethionin (Selenomethionin) relatif tidak toksik, tidak katalitik
dan tidak menghasilkan superoksida (Steward et al. 1999). Selenomethionin menyebabkan respon perbaikan DNA dan melindungi fibroblast dari kerusakan
DNA (Seo et al. 2002). Sementara itu selenit dan selenat meningkatkan oksidasi
elektron dan pernutusan rantai DNA (Sugiyama et al. 1987; Snyder 1988; Milligan et al. 2002). Selenomethionin dipertimbangkan sebagai antioksidan yang sangat kuat melindungi kerusakan sel dari pengaruh peroksinitrit.
Selenoaminoacid ini secara langsung terlibat dalam garis ketiga dari pertahanan
antioksidan (Sies et a1 1998.
Groof dan Sareen (1999) mengemukakan bahwa duodenum merupakan
tempat utama penyerapan selenium, sedangkan pada jejenum maupun ileum
penyerapan terjadi sangat sedikit. Se inorganik merupakan mineral jarang yang diabsorbsi secara pasif. Selama absorbsi Se inorganik direduksi membentuk
selenid dan untuk memudahkan absorbsi perlu oksidasi tinggi, selanjutnya Se
berikatan dengan protein plasma yang kemudian ditranspor ke hati untuk menjadi
bagian dari cadangan Se dalam pembentukan selenoprotein. Selenoaminoacid
diabsorbsi secara aktif melalui mekanisme transpor asam amino dan langsung
Inenyebar diseluruh tubuh melalui darah dan ditranspor ke hati, selanjutnya
berubah kedalam bentuk aktif selenoprotein atau langsung ke jaringan untuk
bergabung kedalam protein jaringan. Masuknya Se organik kedalam sintesis
protein jaringan akan meningkatkan penyimpanan selenium, sehingga kandungan
selenium jaringan meningkat. Pada tingkat seluler, daur ulang protein tubuh
berlangsung terus menerus, perombakan protein terjadi pada proteosom dan
sintesis kembali di dalam ribosom (Combs dan Combs 1986).
Selenomethionin diabsorbsi lebih efektif dibandingkan dengan selenit,
dengan absorbsi selenosistein. Sedangkan absorbsi selenit antara 44-70%, selenat
diabsorbsi lebih baik dibandingkan selenit. Faktor-faktor yang meningkatkan
absorbsi selenium termasuk Vitamin C, A dan E (Groof dan Sareen 1999).
[image:26.556.93.467.139.496.2]Mekanisme transporlasi dan absorbsi selenium dalam tubuh diilustrasikan pada
Gambar 2.
Selenit
E l
Absorbsi pasif
m
Se-amino acidI)
Sistem Gastrointestinal
+
Absorbsi aktifReduksi
+
Ekskresi Empedu Urine Se a A T I
Gambar 2 Mekanisme transportasi dan absorbsi Se (Groof dan Sareen 1999)
Metabolisme Selenium Organik dan Inorganik
Menurut Groof dan Sareen (1999), Se organik merupakan rangkaian yang
khas untuk metabolisme karena bermanfaat untuk cadangan nutrisi yang akan
digunakan untuk sintesis protein dalam otot, reproduksi, dan jaringan lain. Sebaliknya sebagian besar Se inorganik tidak dimanfaatkan dalam pembentukkan
Di dalam jaringan hati, selenomethionin yang diperoleh dari makanan
kemungkinan akan disimpan di dalam kelompok asam amino, atau digunakan
untuk sintesis protein khususnya asam amino methionine atau dikatabolisme
menjadi Se-Adenosylmethionin (SeAm) yang akhimya menghasilkan
selenosistein dan selenosistin. Selenosistein yang diperoleh dari makanan atau
hasil dari metabolisme selenomethionin akan didegradasi oleh selenosistein
P-
lyase untuk menghasilkan selenium bebas. Selenium bebas tersebut kemudianmenempel pada transfer RNA yang berisi serin dan akhimya bergabung ke dalam
kelompok enzim-enzim selenium. Selenium yang tidak digunakan sebagai
kofaktor enzim kemungkinan disimpan untuk pemanfaatan berikutnya atau diubah
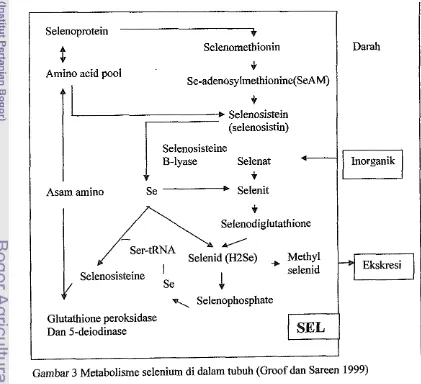
[image:27.559.75.496.301.685.2]menjadi selenid (H2Se) dan.selenit, atau diekskresikan (Groof dan Sareen 1999). Metabolisme selenium organik dan inorganik secara skematis tersaji pada
Gambar 3.
Selenoprotein
t
C Selenomethionin
I
Darah+
Amino acid pool
+
Se-adenosylmethionine(SeAM)
Selenosistein
7
(selenosistin)lL
+
I
SelenosisteineB-lyase Selenat
+
Asam amino Se
-
SelenitEkskresi
I
SelenodiglutathioneMethyl selenid Selenosisteine
u, Selenophosphate
Gambar 3 Metabolisme selenium di dalam tubuh (Groof dan Sareen 1999) Glutathione peroksidase
Selenat di dalam tubuh diubah menjadi selenit kemudian dimetabolisme
menjadi selenodigluthatione yang kemudian diubah menjadi selenide, selanjutnya
selenide didegradasi menjadi selenophosphat atau methylselenide yang akan
diekskresikan. Selenophosphat dimetabolisme dan kemudian menempel pada
tRNA untuk sintesis 5-deiodinase atau gluthatione peroksidase.
Vitamin E
Vitamin E baru ditemukan sekitar tahun 1922 oleh Herbert Evans (Sell
1993). Kemudian Piliang (2004) menambahkan bahwa nama vitamin E dibuat
oleh Evan (1925) yang kemudian peneliti lain yaitu Emerson mencoba memurnikan faktor tersebut dan menamakannya tocopherol yang berasal dari
bahasa Yunani (tokos = kelahiran bayi dan kata kerja pherein = membawa atau
menyebabkan). Penambahan akhiran ol pada akhir kata menunjukkan bahwa
vitamin tersebut termasuk golongan alkohol.
Vitamin E meliputi 8 komponen yang disintesis oleh tumbuh-tumbuhan.
Komponen ini dibagi menjadi 2 kelas yaitu: tocols yang mempunyai rangkaian
jenuh (saturated) dan tocotrienols (trienol) yang mempunyai rangkaian tak jenuh
(unsaturated). Masing-masing kelas tersusun dari 4 vitamer yaitu a,
P,
y, dan 6yang memiliki karakteristik dan aktivitas biologis. Komponen yang paling aktif
adalah a-tocopherol kemudian $-tocopherol yang lebih aktif dari y dan 6
tocopherol. Sedangkan untuk tocotrienols, hanya P-tocohienols yang mempunyai
aktivitas sedikit lebih tinggi dari a-tocotrienols, sementara aktivitas y dan 6
tocotrienol tidak diketahui. Komponen lain dari vitamin E adalah a-tocopheryl
acetat (Groff dan Sareen 1994). Ekstraksi tocopherol dari minyak tumbuh-
tumbuhan menghasilkan dl-a-tocopheryl acetat. dl-a-tocopheryl acetat merupakan
sumber vitamin E terbesar untuk suplementasi (McDowel2000)
Farrel dan Robert (1994) mengemukakan bahwa secara umum vitamin E
berfungsi sebagai antioksidan biologis yang melindungi membran seluler dari
kerusakan oksidatif dan membersihkan (scavenger) membran dari radikal-radikal
bebas. Vitamin E berpengaruh terhadap aktivitas enzim pada plasma, juga
berperan dalam pengaturan sintesis asam nukleat, ekspresi gen dan kontrol daur
hidup beberapa protozoa tertentu. Selanjutnya dikatakan, phospolipid pada sel dan
mengalami peroksidasi karena itu vitamin E sebagai antioksidan yang larut dalam
lemak melindungi asam-asam lemak tersebut dengan jalan memecahkan radikal
bebas yang dapat mengakibatkan kerusakan membran. Groff dan Sareen (1994)
menambahkan bahwa fungsi vitamin E memelihara integritas sel tubuh, mencegah
peroksidasi asam-asam lemak tak jenuh yang berada pada phospolipid membran
seluler, membran mitokondria dan endoplasmik retikulum.
Metabolisme Vitamin E
Absorbsi vitamin E herhubungan dengan pencemaan lemak, dipermudah
dengan adanya empedu dan lipase pankreas. Usus halus merupakan tempat utama
absorbsi vitamin E dalam bentuk alkohol bebas maupun ester, sebagian besar
vitamin E diabsorbsi sebagai alkohol. AIkohol rnemasuki usus dan ditranspor ke
seluruh sirkulasi darah melalui kelenjar getah bening. Aktivitas terbesar vitamin E
pada plasma dan jaringan hewan dalam bentuk a-tocopherol. Tocopherol masuk
ke dalam sistem sirkulasi, menyebar keseluruh tubuh dan penyimpanan terbesar
berada pada jaringan lemak. Vitamin E disimpan di dalam seluruh jaringan bbuh,
terutama disimpan dijaringan adiposa, hati dan otot, penyimpanan terbesar berada
pada hati. Sejumlah kecil vitamin
E
akan tersimpan di dalam tubuh dalam waktuyang lama. Jalur ekskresi utama dari absorbsi vitamin E adalah empedu. Biasanya
kurang dari 1% konsumsi vitamin E akan diekskresikan melalui urine (McDowel
2000).
Selenium dan Vitamin E sebagai Antioksidan
MacPherson (1994) menjelaskan bahwa Se merupakan mineral jarang
(trace mineral) yang sangat efektif sebagai antioksidan yang penting untuk temak. Peranan Se yang sangat penting bagi temak adalah fungsinya dalam aktivitas
selenoenzim (Gluthation peroksidase (GSH-Px)), GSH-Px bersama dengan
katalase, melindungi sel dari kerusakan yang disebabkan oleh radikal bebas,
peroksida dan oksidasi asam-asam lemak tak jenuh yang mengakibatkan
kerusakan sel lemak serta menghancurkan peroksida sebelum peroksida dapat
merusak membran seluler. Berbagai reaksi dan fungsi GSH-Px dalam tubuh
meliputi detoksifikasi mencegah berakumulasinya hidrogen peroksida
(HOOH)
tereduksi, sintesis hormon-hormon tertentu yang berasal dari asam lemak
arakhidonat, dan metabolisme senyawa-senyawa asing. Disamping itu glutathione
sebagai kofaktor dalam metabolisme aldehida tertentu (methylglyoxal dan
formaldehid), kemungkinan juga sebagai transport asam amino dalam ginjal.
Lebih lanjut Brody (1994) menjelaskan, reabsorpsi asam amino yang terdapat
dalam filtrat glomerulus menggunakan bermacam-macam sistem transport, salah
satu sistem transport ini melibatkan glutathione. Sistem yang melibatkan
glutathione erat hubungannya dengan enzim batas luar membran yaitu y-
glutamyltranspeptidase, enzim ini membatasi sel-sel epitel yang menempel pada
lumen tubulus ginjal. Subtrat asam amino yang dikenali oleh enzim ini adalah
sistein, glutamin, methionin, alanin dan serin, juga beberapa substrat dipeptida.
Produk reaksi ini dipindahkan ke dalam sel epitel, dan kemudian dipecah kedalam
asam amino sel. Selain itu Brigelius-Flohe (1999) menyebutkan bahwa fungsi utama dari GSH-Px adalah mengatur keseimbangan reaksi redoks. GSH-Px
mengkatalisis pelepasan H202 menurut sepasang reaksi dibawah ini (Underwood
1977).
Glutatson Peroksidaso
2GSH
+
Hz02-
GSSG+
Hz0Glutat~on perolrsndm
GSSG
+
NADPH-
2GSH+
NADP'Selenium merupakan komponen penting sejumlah selenoprotein yang
terlibat dalam aktivitas antioksidan. Selenoprotein P, selenoprotein W dan ke
empat tipe GSH-Px berperan dalam menetralkan hidroperoksida dan radikal-
radikal bebas oksigen pada berbagai jaringan. Selenoprotein terbaik adalah tipe
GSH-Px. Empat tipe GSH-Px yaitu classical GSH-Px (Rotruck et al. 1973; Flohe
et al. 1973). Kemudian Ursini et al. (1982) menemukan selenoperoksida kedua adalah phospholipid hidroperoksida GSH-Px (PH-GSH-Px). Maddipati dan
Mamett (1987) menyebutkan selenoperoksida tipe ketiga adalah plasma GSH-Px
(PGSH-Px). Selenoperoksida keempat adalah gastrointestinal GSH-Px (GI-GSH-
Px) (Chu et al. 1993). Enzim-enzim ini berbeda pada spesifik jaringan dan fungsi
utamanya adalah memusnahkan dan detoksifikasi hidrogen peroksida dan
MacPherson (1994) menyebutkan bahwa distribusi masing-masing tipe
gluthatione peroksidase berbeda-beda tiap jaringan dan species, sehingga
kebutuhan dan gejala defisiensi tiap species juga berbeda. Cytosolic GSH-Px merupakan selenoprotein yang termasuk ke dalam salah satu enzim antioksidan
yang meliputi katalase, glutathion transferase dan superoksida dismutase. Enzim-
enzim ini menetralkan radikal-radikal oksigen dan hidrogen peroksida yang
dihasilkan didalam sel. Bersama-sama enzim-enzim tersebut mengurangi
persediaan superoksida dan peroksida sehingga mengurangi kemungkinan
kerusakan isi sel dan membran sel (Combs dan Combs 1986). Phospholipid hidroperoksida GSH-Px, erat kaitannya dengan membran sel, pada tipe GSH-Px
ini terjadi interaksi antara selenium dan vitamin E, enzim ini dapat menetralkan
peroksidasi lemak dan secara langsung melindungi membran. PH-GSH-Px kurang
sensitif dibandingkan dengan cytosolic GSH-Px (McPherson 1994). Selanjutnya
dikatakan bahwa plasma GSH-Px (PGSH-Px) adalah antioksidan ekstraseluler
yang bersumber dari ginjal, berperan melindungi sel endothelial lapisan darah dan
pembuluh getah bening. Sedangkan gastrointestinal GSH-Px (GI-GSH-Px)
merupakan bentuk enzim dalam sel sistem gastrointestinal.
Selenoprotein P memiliki peranan antioksidan, di dalam fraksi protein plasma darah mengandung 60-80% Se. Selenoprotein W merupakan antioksidan
yang berada di dalam hati dan jaringan otot, dan kemungkinan jumlahnya didalam
jaringan tersebut sama dengan jumlah GSH-Px. Konsentrasi selenoprotein
jaringan tergantung pada konsumsi selenium (Chen et al. 1990; Persson-Moschos
et al. 1998).
Vitamin E melindungi hati dari peroksidasi lemak dan kerusakan
membran sel (Whitehead et al. 1998). Kemudian Halliwell dan Gutteridge (1989) mengemukakan bahwa vitamin E dikenal sebagai komponen hiologi membran
dan dipertimbangkan sebagai rantai antioksidan dalam peroksidasi lemak Vitamin
E terutama ditemukan pada hidrokarbon membran lemak sebagai alat penghubung
membran dan erat kaitannya dengan oksidasi enzim yang mengakibatkan
produksi radikal bebas, vitamin E melindungi sel dan jaringan dari kerusakan
oksidasi oleh radikal bebas (Gallo-Toress 1980). Selanjutnya disebutkan bahwa
untuk fungsi normal dari pankreas. Defisiensi selenium dan tocopherol
mengakibatkan kerusakan jaringan dan kematian sel yang disebabkan karena
oksidasi membran sel lemak dan hidroperoksida lemak. Peroksidasi lemak dapat
rnenghancurkan keutuhan smtktur sel dan menyebabkan kekacauan metabolisme
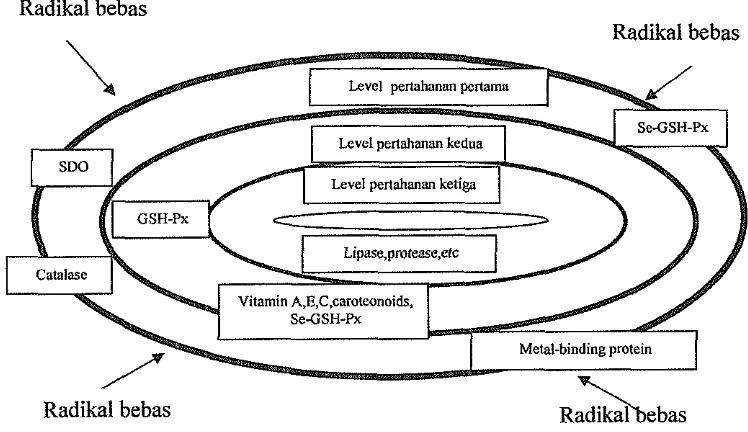
(McDowell 1992; Brody 1994). Gambar 4 menyajikan tiga level pertahanan
antioksidan di dalam sel.
Radikal bebas
Radikal bebas
[image:32.559.110.484.180.396.2]Radikal bebas Radikal 3' ebas
Gambar 4 Level pertahanan antioksidan didalam sel (Surai 2000)
Surai (1999) mengemukakan bahwa sistem antioksidan pada sel hidup
meliputi tiga level pertahanan utama, level pertahanan pertama bertanggung jawab
mencegah pembentukan radikal bebas yang dilakukan oleh tiga enzim
antioksidan, superoksida dismutase (SOD), glutathione peroksidase (GSH-Px) dan
katalase bersama metal-binding protein. Halliwell dan Gutteridge (1999)
menjelaskan bahwa Radikal superoksida adalah radikal bebas utama yang
dihasilkan oleh sel hidup. Aktivitas penting dalam pertahahan antioksidan
disediakan oleh GSI-I-Px dan katalase. Lebih lanjut Yu (1994) mengatakan bahwa
GSH-Px ditemukan pada bagian-bagian yang berbeda pada sel, sedangkan
katalase lokasi utamanya pada peroksisom. Pemusnahan hidrogen peroksida dari
Selenium merupakan bagian integral dari enzim antioksidan GSH-Px,
berada pada level pertama pertahanan antioksidan. Garis pertama dari pertahanan
antioksidan sel tidak mempunyai kekuatan yang cukup untuk mencegah
pembentukan dan perkembangan radikal bebas secara sempuma. Selanjutnya
berperan pertahanan antioksidan level kedua yang meliputi glutathione, vitamin
larut dalam lemak (A, E, carotenoid, ubiquinon) dan vitamin larut dalam air (asam
askorbat, asam urea dll). Antioksidan ini merupakan komponen rantai pemecah
yang potensial mencegah pembentukan dan perkembangan rantai radikal bebas.
Hidroperoksida dapat terbentuk selama reaksi radikal bebas dengan antioksidan,
ROO*
+
Toc = Toc*+
ROOHDimana: ROO* adalah radikal peroksil; Toc adalah tocoperol; Toc* adalah
radikal tocoperoksil, ROOH adalah hidroperoksida. Hidroperoksida bersifat
toksik dan jika tidak dihilangkan akan merusak struktur dan fungsi membran
(Gutteridge dan Halliwell 1990). Kemudian Diplock (1994) menambahkan bahwa
hidroperoksida lemak tidak stabil dan dengan kehadiran ion-ion logam transisi
dapat terurai membentuk radikal-radikal bebas baru dan aldehid sitotoksik.
Hidroperoksida harus dikeluarkan dari dalam sel dengan jalan yang sama
seperti H202, tetapi enzim katalase tidak dapat bereaksi dengan komponen- komponen ini, hanya cytosolic GSH-Px yang dapat mengubah radikal-radikal ini
menjadi produk yang tidak reaktif Se sebagai bagian integral dari GSH-Px, yang juga termasuk kedalam level kedua pertahanan antioksidan tidak mampu untuk
mencegah peroksidasi lemak sehingga beberapa molekul biologis mengalami
kerusakan. Pada level ketiga pertahanan antioksidan, enzim-enzim spesifik seperti
protease, lipase dan beberapa enzim lainnya berperan melakukan perbaikan terhadap molekul-molekul yang rusak. Selanjutnya seluruh element-element
sistem antioksidan berinteraksi membentuk pertahanan antioksidan yang efisien.
Interaksi ini dimulai pada saat absorbsi nutrisi dan berianjut selama metabolisme
nutrisi (Brigelius-Flohe 1999).
Selenium dianggap penting dalam nutrisi temak karena kedua level
pertahanan antioksidan (pertahanan pertama dan kedua) dalam sel tergantung pada
molekul biologis sehingga mengakibatkan kematian sel (Halliwell dan Guteridge
1999).
Peranan Selenium dan Vitamin E pada Embrio
Sistem antioksidan embrio terdiri dari antioksidan alami dan kofaktor
enzim yang diperoleh dari makanan induk, serta enzim antioksidan yang disintesis
dalam jaringan. Kekuatan sistem pertahanan antioksidan sebagian besar
tergantung pada komposisi makanan induk (Surai 1999). Persediaan antioksidan
makanan yang baik seperti Vitamin E, vitamin C, selenium organik memberikan
perlindungan pada embrio, meningkatkan daya tahan hidupnya. Meningkatkan
satu antioksidan akan berpengamh terhadap peningkatan antioksidan lainnya.
Sebagai contoh suplementasi selenium organik pada makanan memperlihatkan
peningkatan level antioksidan lain (Vitamin A, E dan Carotenoid) dalam telur
(Surai dan Sparks 2001).
Surai (2003) memaparkan bahwa selama embriogenesis, asam lemak tak
jenuh terakumulasi di dalam jaringan, di mana pada kondisi ini meningkatkan
resiko shes oksidasi. Proses ini berawal dari shes defisiensi oksigen dan semakin
memburuk selama dan sesaat setelah menetas. Selain itu pernafasan normal dan metabolisme oksidatif pada perkembangan embrio selama periode inkubasi
khususnya beberapa hari sebelum menetas menghasilkan radikal bebas dan
peroksidasi lemak, khususnya asam-asam lemak tak jenub. Peroksidasi lemak
juga disebabkan karena rendahnya kandungan selenium dalam pakan sehingga sintesis selenoprotein terganggu dan aktivitas GSH-Px rendah dan perlindungan
antioksidan tidak efektif. Peroksidasi lemak akan mengakibatkan kemsakan
jaringan membran, enzim non aktif, level hormon dan sintesis enzim terganggu.
Peroksidasi lemak juga mengakibatkan pertumbuhan dan perkembangan embrio
terganggu serta penurunan daya tahan hidup awal anak setelah menetas. Aktivitas
GSH-Px rendah juga akan mengakibatkan akumulasi hidroperoksida (ROOH)
yang mengakibatkan toksik pada sel. Karena itu proses penetasan meningkatkan
kebutuhan sistem antioksidan yang efisien (Surai 2000). Mekanisme pertahanan
antioksidan embrio terdiri dari dua level, di mana level pertahanan pertama adalah
tiga kelompok enzim yaitu superoksida dismutase, glutathion peroksidase dan
menjadi alkohol yang kurang berbahaya (Ursini et al. 1997). Level pertahanan
kedua adalah antoksidan alami vitamin E, carotenoids, asam askorbat, dan
glutathion yang melindungi perkembangan anak. Pada kondisi oksidasi tinggi
diakhir inkubasi dan sehari setelah menetas antioksidan sangat berpengaruh (Surai
1999).
Hubungan antara selenium dan vitamin E pada proses embriogenesis
diilushasikan pada Gambar 5.
selama perkembangan embrio
Aktivitas GSH-Px rendah mengakibatkan peroksidasi Lemak meningkat melalui pembentukkan OH* dari Hz02
t
Stres penetasan
Produksi radikal bebas dan peroksidasi lemak
I
Garis kedua pertahanan antioksidan ( antioksidan pemecah rantai) ROO*
+
A 0 (Vit E) = ROOH (Toksik) ROOH+
GSHPx = ROH (nontoksik) [image:35.559.79.492.186.615.2]I I
Gambar 5 Hubungan Se dan vitamin E pada proses embriogenesis (Surai 2003) Biosintesis Selenoprotein dan stabilisasi mRNA nya
1
Garis pertama pertahanan antioksidan (antioksidan
pencegah) 0 2
+
SOD = Hz02 (Toksik)-
MATERI
DAN
METODE
Tempat dan Waktu Penelitian
Percobaan dilakukan selama 22 minggu dari bulan September 2005 -
Maret 2006. Percobaan dilaksanakan di Laboratorium Kimia Terpadu,
Laboratorium Kimia Makanan, Pusat Penelitian dan Pengembangan Gizi Bogor, Laboratorium Fisiologi dan Farmakologi FKH
-
IPB Bogor, Laboratorium Balai Besar Pasca Panen dan Kandang C Nutrisi dan Makanan Ternak IPBTahapan Penelitian
Peneiitian ini terdiri atas dua tahap percobaan:
Tahap I : Tahap pemeliharaan puyuh. Tahap ini dimulai dari puyuh berumur 3 minggu sampai berumur 25 minggu. Puyuh diberi ransum dengan suplementasi
Se dan vitamin E. Tahap ini bertujuan untuk mengetahui efektivitas Se organik dan vitamin E terhadap:
1. Umur mulai bertelur, konsumsi pakan, produksi telur dan konversi.
2. Kandungan Selenium dalam hati, otak, darah dan telur
3. Kandungan vitamin E dalam darah dan telur
4. Aktivitas glutathione peroksidase darah dan hati.
Tahap I1 : Tahap penetasan telur dan pemeliharaan anak puyuh. Telur mulai
ditetaskan saat puyuh berumur 10, 12, 14, 16 dan 18 minggu dan dilanjutkan
dengan pemeliharaan anak puyuh selama 4 minggu. Ransum yang diberikan pada
anak puyuh selama pemeliharaan tanpa suplementasi Se dan vitamin E. Tahap ini
bertujuan untuk mengetahui efektivitas Se organik dan vitamin E pada ransum induk terhadap:
1. Fertilitas dan daya tetas telur.
2. Bobot tetas dan mortalitas anak.
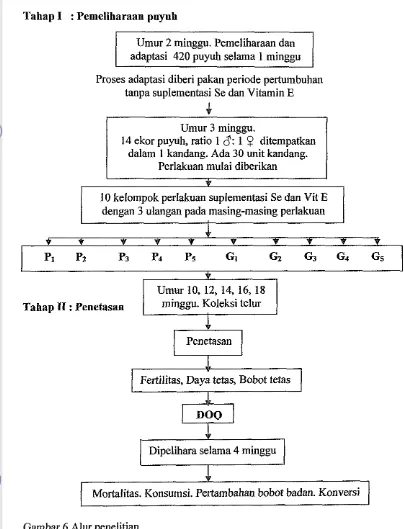
Tahapan Penelitian
Tahap I : Pemeliharaan puyuh
Umur 2 minggu. Pemeliharaan dan adaptasi 420 puyuh selama 1 minggu
Proses adaptasi diberi pakan periode pertumbuhan tanpa suplementasi Se dan Vitamin E
14 ekor puyuh, ratio 1
8:
19
ditempatkandalam 1 kandang. Ada 30 unit kandang. Perlakuan mulai diberikan
v
10 kelompok perlakuan suplementasi Se dan Vit E
dengan 3 ulangan pada masing-masing perlakuan
Umur 10, 12, 14, 16, 18
Tahap I1 : Penetasao minggu. Koleksi telur
Penetasan
0
Fertilitas, Daya tetas, Bobot tetas
I
4
Dipelihara selama 4 minggu
[image:37.559.82.486.67.596.2]I
Mortalitas. Konsumsi. Pertambahanbobot
badan. Konversi1
Gambar 6 Alur penelitian
Keterangan:
P, & G, : Ransum tanpa suplementasi Sedan vitamin E
P2 & G2 : Ransum dengan suplementasi Se 0.5 ppm +vitamin E 50 ppm
P, & G, : Ransum dengan suplementasi Se 0.5 ppm
+
vitamin E 100 ppm P, & G4 : Ransum dengan suplementasi Se 1 ppm + vitamin E 50 ppmTahap I : Pemeliharaan Puyuh
Materi Penelitian
Penelitian ini menggunakan 210 ekor puyuh betina dan 210 ekor puyuh
jantan berumur 3 minggu. Puyuh dibagi ke dalam 10 kelompok perlakuan dengan
3 ulangan, masing-masing terdiri dari 14 ekor puyuh dengan perbandingan jantan
dan betina 1:I. Puyuh ditempatkan pada 30 unit kandang percobaan yang
merupakan kandang baterai dengan ukuran 42x60~20 cm. Sebelum diisi kandang
disanitasi terlebih dahulu dengan kapur dan tempat makan dan minum disanitasi
dengan antisep.
Suplementasi selenium organik (Se) dan vitamin E (dL-a- tocopheryl
acetat) ke dalam ransum sebagai perlakuan, diberikan selama pemeliharaan
puyuh. Selama penelitian menggunakan dua merk ransum komersial yaitu P dan
G untuk periode pertumbuhan dan bertelur. Pemberian ransum pada umur 2-3
minggu adalah ransum periode pertumbuhan, sedangkan pada umur 4 minggu
sampai akhir penelitian pakan diganti dengan ransum periode bertelur yang
diberikan ad libitum. Kandungan nutrisi ransum kontrol dapat dilihat pada Tabel 2
Tabel 2 Komposisi nutrisi ransum kontrol
No Uraian Ransum
Starter Layer
(P) (G) (P) (G)
I Protein (%) 21.50 22.00 20.00 20.00
2 Lemak(%) 6.09 6.00 4.78 4.25
3 Serat kasar (%) 2.82 3.50 4.34 4.50
4 Abu(%) 5.34 6.45 10.69 11.0
5 Kalsium (%) 0.89 0.90 3.24 3.25
6 Phospor (%) 0.70 0.70 0.72 0.70
7 Vitamin E (ppm) 50.0 50.0 43.50 43.00
8 Selenium (ppm) 0.21 0.35 0.46 0.40
Hasil analisa Laboratorium Kimia Terpadu
Metode Penelitian
Penelitian ini terdiri dari 10 kelompok di mana 8 kelompok merupakan
kombinasi perlakuan suplementasi 2 level Se dan 2 level vitamin E pada 2 jenis
vitamin E adalah 50 ppm dan 100 ppm. Dua kelompok sebagai kontrol terdiri
dari ransum P dan G tanpa suplementasi Se dan vitamin E. Masing-masing
perlakuan dan kontrol terdiri dari 3 ulangan, tiap unit ulangan terdiri dari 14 ekor puyuh dengan perbandingan 7 ekor jantan dan 7 ekor betina. Puyuh-puyuh
ditempatkan ke dalam 30 unit kandang. Perlakuan suplementasi Se organik dan
vitamin E disajikan pada Tabel 3.
Tabel 3 Perlakuan suplementasi selenium dan vitamin E
Perlakuan Selenium organik (ppm) Vitamin E (ppm) Suplementasi Total dalam Suplementasi Total dalam
- -
2. P2 0.5 0.96 50 93.50
3. P3 0.5 0.96 100 143.50
4. P4 1 1.46 50 93.50
5. P5 1 1.46 100 143.50
6. GI
-
0.43*-
43*
7. G2 0.5 0.93 50 93
8. G3 0.5 0.93 100 143
9. G4 1 1.43 50 93
10. G5 1 1.43 100 143
a Kandungan di dalam ransum kontrol
Ketcrangan:
P, & G, : Ransum tanpa suplementasi Sedan vitamin E
P2 & G2 : Ransum dengan suplementasi Se 0.5 ppm + vitamin E SO ppm
P3 & G3 : Ransum dengan suplementasi Se 0.5 ppm + vitamin E 100 ppm
P4 & G4 : Ransum dengan suplementasi Se 1 ppm + vitamin E 50 ppm
Ps & Gs : Ransum dengan suplementasi Se 1 ppm + vitamin E 100 ppm Rancangan Penelitian
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL) pola
faktorial terdiri dari 3 faktor, faktor pertama yaitu 2 jenis ransum (P dan G), faktor
kedua adalah suplementasi 2 level Se organik (0.5 ppm dan 1 ppm) dan faktor ketiga yaitu suplementasi 2 level vitamin E (50 dan 100 ppm) sehingga ada 8
kombinasi perlakuan suplementasi Se dan vitamin E dan sebagai kontrol adalah 2
jenis ransum (P dan G) tanpa suplementasi Se maupun vitamin E. Masing-masing
perlakuan dan kontrol terdiri dari 3 ulangan.
Model matematika rancangan penelitian ini adalah :
Keterangan :
Yijk = Nilai Pengamatan.
P = Nilai Tengah Pengamatan
a i
= Pengaruh Aditif Vitamin E ke- iP
j = Pengaruh Aditif Mineral Se ke- j( a
p ) i j = Pengaruh Interaksieijk = Pengaruh Galat Percobaan
Data perlakuan yang diperoleh dari percobaan dianalisa dengan menggunakan analisa ragam (analyses of variance/ANOVA) RAL faktorial dan jika data yang dihasilkan berbeda nyata maka dilanjutkan dengan Uji Duncan.
Perlakuan terbaik akan dibandingkan dengan kontrol dengan Uji-T (Steel dan
Torrie 1993).
Parameter yang diamati adalah :
1. Umur mulai bertelur (dewasa kelamin)
Umur mulai bertelur dihitung hari pertama puyuh bertelur.
2. Produksi telur
J u -& m ~
-
.
.
Produksi hen day (%) = x 100%
Jumiah puyuh
x
jumlah hari selama penelitianProduksi telur (gram) adalah total herat telur yang dihasilkan tiap perlakuan
selama pemeliharaan. Penimbangan telur dilakukan setiap hari perunit
ulangan, di mulai dari puyuh dewasa kelamin sampai berumur 23 minggu. 4. Konsumsi Ransum
Konsumsi ransum adalah jumlah ransum yang dimakan oleh puyuh selama
pemeliharaan. Ransum yang dikonsumsi ditimhang setiap minggu.
Konsumsi = Jumlah ransum yang diberikan - jumlah ransum yang tersisa
5. Konversi Ransum
Konversi ransum diperoleh dengan cara membagi jumlah ransum yang dikonsumsi dengan produksi telur (total berat telur) yang diperoleh selama
penelitian dikali 100%
Konversi = Total konsumsi (gram) ~100%
6. Berat Hati
Setelah temak puyuh dideterminasi, lalu dikeluarkan hatinya dan dilakukan
penimbangan.
7. Berat Otak
Setelah temak puyuh dideterminasi, lalu dikeluarkan otaknya dan dilakukan
penimbangan.
8. Panjang Saluran Reproduksi
Panjang saluran reproduksi yang diukur adalah saluran reproduksi betina.
Saluran reproduksi yang diukur dari infundibulum, magnum, istmus, uterus,
vagina sampai kloaka. Pengukuran dilakukan setelah puyuh diditerminasi, dan
saluran reproduksi dikeluarkan untuk diukur panjangnya.
9. Kandungan selenium telur.
Telur yang dijadikan sampel uji kandungan selenium diambil secara acak
sebanyak 2 butir tiap unit ulangan dari masing-masing perlakuan. Selenium
telur adalah gabungan antara putih dan kuning telur. Prosedur pengukurau selenium dengan menggunakan Hydride Fapour Generator Merhad AAS
sebagai berikut (1) Telur ditimbang sebanyak 0.5 gram-1 gram contoh ke
dalam labu dekstruksi, lalu ditambahan 10 ml asam nitrat pekat panaskan pada
kompor listrik dengan suhu yang tidak terlalu panas ?C 80-90'~ dan dipanaskan
sampai dengan jemih (6 jam). (2). Kemudian ditimbang sebanyak 0.5 gram-1
gram blanko (larutan baku standar Se (1000 ppm)) dengan cara pengeceran :
40, 80, 100, 200, 400ppb. (3). Larutan pereduksi 20 ml ditambahkan kedalam standar dan contoh, ditepatkan sampai dengan 100 ml dengan Aquades. (5).
Contoh siap di baca di AAS dan siap untuk dianalisis.
Kadar Se: mcg - - Abs cth x (konsentrasi std)
x
VO'ume x fp100 gr Abs std Bobot contoh
10. Kandungan vitamin E telur.
Telur yang dijadikan sampel uji kandungan vitamin E diambil secara acak
sebanyak 2 butir tiap unit ulangan dari masing-masing perlakuan. Kandungan
vitamin E telur adalah gabungan antara putih dan kuning telur. Proses analisis
Selanjutnya ditambahkan enzim makatase 40 mg dan 2 ml amonia 0.02%. (3)
Campuran dimasukkan ke dalam ultrasonik selama 20 menit pada suhu 65°C.
Lalu campuran didinginkan pada suhu ruang dan tambahkan etanol 10 ml. (4)
Dimasukkan kembali ke dalam ultrasonik selama 10 menit. (5) Selanjutnya
ditambahkan etanol hingga volumenya 20 ml dan dikocok kembali. (6)
Larutan disentrifuse dan 5 ml supernatan diambil dan dimasukkan ke dalam
labu ukur 5 ml. (7) Larutan siap untuk diinjeksikan ke alat HPLC.
Perhitungan:
Kadar vitamin E: Luas area sampel x 25 ppm x 10
Luas area standar
-
0.5Keterangan:
25 : Konsentrasi standar
10 : Volume akhir (ml)
0.5 : Volume sampel yang diinjeksikan (ml)
1 1. Kandungan selenium darah
12. Kandungan vitamin E darah.
Pengambilan darah dilakukan pada akhir penelitian dengan menggunakan syringe 1 cclml. Semua puyuh betina tiap unit percobaan diambil darahnya
meialui sayap dan kemudian dimasukkan ke dalam tabung yang sudah diberi
heparin kemudian disentrifuse dan diambil plasmanya. Masing-masing sample plasma dimasukkan ke effendorf: Untuk analisa selenium dan vitamin E,
plasma masing-masing perlakuan dikomposit dengan jalan tiap plasma pada tiap effendorf diambil sebanyak 0.5 ml dan digabung dalam 1 tabung
effendorf:
13. Kandungan selenium hati dan otak.
Pengambilan sampel hati dan otak diambil pada akhir penelitian dari ternak
induk yang sudah dipotong.
14. Aktivitas enzim giutathione peroksidase (GSH-Px) Hati.
Pembuatan sampel adalah 100 p1 homogen hati ditambah dengan 200 pI
buffer phosfat pH 7.0, kemudian di kocok dengan vortek. Larutan disentrifuse
pada 3000 rpm selama 5 menit dalam kondisi dingin. Supematan digunakan
untuk mengukur aktivitas glutathion peroksidase (GSH-Px). 200 pl buffer
pI sampel. 200 p1 glutathion tereduksi (GSH) 10 nM dan 200 p1 enzim
glutation reduktase 2.4 unit kemudian di inkubasi selama 10 menit pada suhu
3 7 ' ~ . Tambahan 200 p1 NADPH 1.5 nM ke dalam larutan, diinkubasi lagi pada suhu yang sama selama 3 menit. Tambahan 200 p1 H202 1.5 nM.
Serapan dibaca pada spektrofotometer diantara waktu 1-2 menit pada panjang
gelombang 340 nm.
Perhitungan:
munit GSH-PX = Mhsorban x Vt x 2 x 1000 1
6.22 x Vs mg protein
Keterangan
AAbs = Pembahan absorban Vt = Volume total dalam ml
6,22 = Koefisien ekstrensik dari NADPH
2 = 2 mol GSH yang setara dengan 1 mol NADPH
1000 = Perubahan menjadi milliunit
Vs = Volume sampel dalam ml
15. Aktivitas GSH-Px dalam darah
Aktivitas enzim GSH-Px yang diukur adalah GSH-Px dalam darah ternak puyuh induk. Pengambilan darah bersamaan dengan untuk analisa selenium
dan vitamin E. Prosedur kerja analisa sama dengan prosedur analisa GSH-Px
pada darah.
Tahap I1 : Penetasan Telur
Percobaan pada tahap ini dilakukan penetasan telur. Penetasan dilakukan
sebanyak 5 kali. Telur untuk penetasan pertama diambil ketika puyuh induk
bemmur 10 minggu, penetasan ke 2 saat induk berumur 12 minggu, penetasan
selanjutnya pada umur induk 14, 16 dan 18 minggu. Telur dikumpulkan selama 5
hari berturut-turut untuk sekali penetasan dengan jumlah telur berkisar 700- 900
butir tiap penetasan. Semua telur yang dihasilkan tiap unit ulangan terlebih
dahulu ditimbang satu persatu untuk mengetahui herat telur dan kemudian
dimasukkan ke dalam mesin tetas. Berat telur yang ditetaskan berkisar 11-12
tumpul dan ujung runcing telur dibalik hergantian. Telur menetas pada hari ke
16 dan 17 setelah di~nasukkan ke dalam mesin tetas. Pemecahan kerabang telur
dilakukan pada hari ke 18 pada telur yang tidak menetas untuk memastikan
penyehah tidak menetas, karena tidak fertil atau penyebab lainnya.
Setelah telur menetas maka anak puyuh dipelihara selama empat minggu,
guna mengetahui mortalitas dan performa anak. Anak puyuh diberi pakan
periode pertumbuhan tanpa suplementasi Se dan vitamin E. Komposisi nutrisi
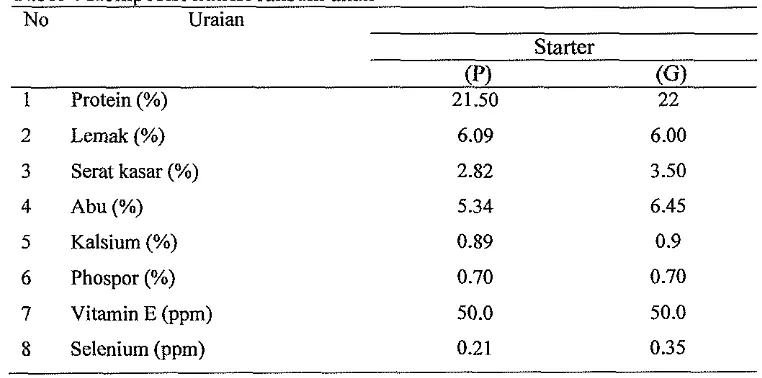
[image:44.559.98.479.228.417.2]ransum anak selama 4 minggu disajikan pada Tabel 4.
Tabel 4 Komposisi nutrisi ransum anak
No Uraian
Starter
(PI (G)
1 Protein (Oh) 2 1.50 22
2 Lemak(%) 6.09 6.00
3 Serat kasar (%) 2.82 3.50
4 Abu(%) 5.34 6.45
5 Kalsium (%) 0.89 0.9
6 Phospor (%) 0.70 0.70
7 Vitamin E (ppm) 50.0 50.0
8 Selenium (ppm) 0.21 0.35
s Hasil analisa Laboratorium Kimia Terpadu
Rancangan Penelitian
Rancangan penelitian yang digunakan adalah RAL faktorial in Time.
Apabila data yang dihasilkan herheda nyata maka dilanjutkan dengan Uji Duncan
(Mattjik dan I Made, 2002). Data terhaik akan dibandingkan pada kontrol dengan
Uji-T. Model matematikanya adalah:
YijkL= p
+
ai+
pj+ a h +
6ijk+
mI+ykl+ a d + pmjl+ apmijl+ ~ i j k lDimana :
Yijk~ = Nilai respon pada faktor A taraf ke-i, faktor B taraf ke-j, ulangan ke-k dan waktu pengamatan ke-1
p = Nilai tengah umum
aPij = Pengaruh interaksi faktor A dengan faktor B 6ijk = Komponen acak perlakuan
o l = Pengaruh waktu ke-I
ykl = Komponen acak waktu pengamatan awil = Pengaruh interaksi waktu dengan faktor A
pwjl = Pengaruh interaksi waktu dengan faktor B
apoijl= Pengaruh interaksi faktor A, faktor B dengan waktu
~ i j k i = Komponen acak dari interaksi waktu dengan perlakuan.
Parameter pada penelitian tahap ini terdiri atas:
1. Fertilitas yaitu persentase telur yang fertil dari telur yang dieramkan.
2. Daya tetas yaitu persentase telur puyuh yang menetas dari jumlah telur yang
fertil. Telur-telur yang tidak menetas akan dipecah dan selanjutnya diperiksa
untuk memastikan penyebab tidak menetasnya.
3. Berat tetas. Semua anak yang menetas ditimbang sesaat setelah dikeluarkan dari mesin tetas.
4. Mortalitas anak dihitung berdasarkan persentase anak yang mati selama 2
minggu pemeliharaan.
5. Konsumsi ransum
6. Pertambahan bobot badan
HASIL DAN PEMBAHASAN
Tahap I : Pemeliharaan puyuh
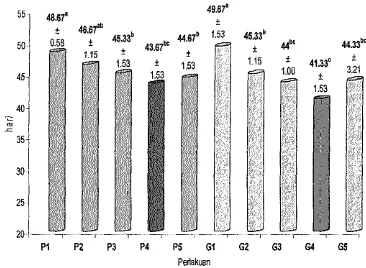
Umur Mulai Bertelur
Pengaruh suplementasi Se dan vitamin E terhadap umur mulai bertelur
[image:46.564.1