PENGARUH KONSENTRASI N-METHYL-2-PYRROLIDONE (NMP) DI MEDIA GELATINISASI PADA PERFORMA MEMBRAN
POLYETHERSULFONE (PES) MOLECULAR WEIGHT 5200
TUGAS AKHIR
Diajukan Guna Memenuhi Persyaratan Untuk Mencapai Derajat Strata-1 Pada Program Studi Teknik Mesin Fakultas Teknik
Universitas Muhammadiyah Yogyakarta
Disusun Oleh: SULISTYO PUJIONO
20120130175
PROGRAM STUDI S-1 TEKNIK MESIN FAKULTAS TEKNIK UNIVERSITAS MUHAMMADIYAH
iv
“Dengan nama Allah Yang Maha Pengasih dan Maha Penyayang”
“Hai orang-orang yang beriman ! Apabila dikatakan kepadamu : “Berlapang
-lapanglah dalam majelis,” maka -lapanglah, niscaya Allah akan memberi
kelapangan untukmu. Dan apabila dikatakan : Berdirilah kamu, maka berdirilah, niscaya Allah akan meninggikan orang-orang yang beriman diantaramu dan orang-orang yang diberi ilmu pengetahuan beberapa derajat.
Dan Allah Maha Mengetahui apa yang kamu kerjakan.” (Surat Al -Mujaadalah, ayat ; 11)
Dari Anas RA katanya ; Rasullullah SAW bersabda : Barang siapa yang keluar dari rumah sebab mencari Ilmu, maka ia (dianggap) yang menegakkan agama
Allah sehingga ia pulang. (HR. Turmudzi)
“Lulus Muda. Tua Kaya. Mati Masuk Surga.”
(Penulis)
v
Puji syukur senantiasa penulis panjatkan ke hadirat Allah SWT atas rahmat, barokah dan ridho-Nya Kemudian, shalawat serta salam-Nya, mudah – mudahan terlimah curah ke pangkuan baginda Rasulullah SAW, beserta keluarganya, sahabatnya, dan umatnya yang masih turut dengan ajarannya. Aamiin. Berkat rahmat dan karunia-Nya, penulis dapat menyelesaikan penelitian untuk Tugas Akhir yang berjudul “Pengaruh Konsentrasi N-Methyl-2-Pyrrolidone
(NMP) Di Media Gelatinisasi Pada Performa Membran Polyethersulfone (PES) Molecular Weight 5200” sebagai salah satu syarat untuk mendapatkan gelar
Sarjana di Program Studi S1 Teknik Mesin, Universitas Muhammadiyah Yogyakarta.
Dalam kelancaran proses penulisan tugas akhir ini tidak lepas berkat bimbingan, arahan, dan petunjuk serta kerjasama dari berbagai pihak, baik pada tahap persiapan, penyusunan hingga terselesaikannya tugas akhir ini. Oleh karena itu dalam kesempatan ini penulis ingin menyampaikan ucapan terima kasih dan penghargaan yang setinggi-tingginya khususnya kepada yang terhormat :
1. Bapak Novi Caroko, S.T., M.Eng., selaku Ketua Jurusan Teknik Mesin, Universitas Muhammadiyah Yogyakarta.
2. Bapak Gunawan Setia Prihandana, S.T., M.Eng., Ph.D., selaku dosen pembimbing I Tugas Akhir yang telah memberikan pengarahan, motivasi, dan bimbingannya selama proses persiapan sampai dengan penyelesaian Tugas Akhir ini.
vi
Toray Project dari Universitas Gadjah Mada yang telah memberikan
pengarahan, motivasi dan bimbingan serta pendanaan dalam penelitian yang ditujukan sebagai Tugas akhir ini.
6. Wahyudi, S.T., M.T., selaku Dosen Pembimbing Akademik
7. Semua Bapak dan Ibu dosen Jurusan Teknik Mesin yang telah memberikan bekal ilmu bagi penulis selama mengikuti kuliah di Program Studi Teknik Mesin selama kurang lebih 4 tahun
8. Seluruh karyawan dan karyawati Pelayanan Mahasiswa Jurusan Teknik Mesin di Universitas Muhammadiyah Yogyakarta yang telah membantu pengarahan dan pengurusan birokrasi selama proses penyelesaian Tugas akhir ini.
9. Warsino dan Sri Lestari selaku kedua orang tua yang penulis cintai, senantiasa memberikan dukungan baik moril maupun materil sampai selesainya studi.
10.Adik – adik kandung tercinta anistia widyawati dan willy nugroho saputro yang selalu memberikan semangat dalam penyelesaian Tugas Akhir ini. 11.Seluruh anggota Toray Project yang telah memberikan dukungan dan
semangat dalam penyelesain penelitian Tugas Akhir ini.
12.Seluruh rekan seperjuangan Program Studi Teknik Mesin Angkatan 2012 Universitas Muhammadiyah Yogyakarta.
13.Rekan – rekan dari Program Studi Pendidikan Bahasa Inggris yang telah bersedia memberikan masukan dan dorongan serta motivasi dalam penyelesaian Tugas Akhir ini.
vii membacanya. Aamiin.
Waalaikum’salam Wr. Wb.
Yogyakarta, 30 Agustus 2016
viii
HALAMAN PENGESAHAN ... ii
HALAMAN PERNYATAAN ... iii
HALAMAN MOTO ... iv
KATA PENGANTAR ... v
DAFTAR ISI ... viii
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xvi
DAFTAR RUMUS ATAU PERSAMAAN ... xviii
DAFTAR NOTASI ATAU SINGKATAN ... xix
DAFTAR LAMPIRAN ... xxi
INTISARI ... xxii
ABSTRACT ... xxiii
BAB I PENDAHULUAN 1.1.Latar Belakang Masalah ... 1
1.2.Rumusan Masalah ... 3
1.3.Batasan Masalah ... 4
1.4.Tujuan Penelitian ... 4
ix
2.2.1. Definisi Membran……… ... 8
2.2.2. Klasifikasi Membran ... 9
2.2.3. Sistem Desain Filtrasi Pada Membran ... 13
2.2.4. Membran Ultrafiltrasi ... 15
2.2.5. Metode Pembuatan Membran ... 17
2.2.6. Material Membran Ultrafiltrasi... 18
2.2.7. Polyethersulfone (PES) ... 20
2.2.8. Polyethylene Glycol (PEG) ... 21
2.2.9. N,N-Dimethylacetamide (DMAc) ... 23
2.2.10. Proses Pembuatan Membran ... 25
2.2.11. Media Gelatinisasi ... 28
2.2.12. Pengujian Performa Membran ... 31
2.2.13. Karakterisasi Membran ... 34
BAB III METODE PENELITIAN 3.1.Bahan Penelitian ... 41
3.2.Alat Penelitian ... 45
3.3.Diagram Alir Penelitian ... 51
3.4.Diagram Alir Proses Pembuatan Membran ... 53
3.5.Tahap Persiapan ... 54
3.6.Proses Pembuatan Casting Solution PES ... 54
x
3.11.Prosedur Pembuatan Mikrofilter ... 58
3.12.Proses Pembuatan Larutan NaCl ... 59
3.13.Proses Tes Difusi ... 59
3.14.Prosedur Tes Difusi ... 63
3.15.Pengamatan Nilai Konduktivitas Larutan Dialisat Setelah Tes Difusi ... 67
3.16.Karakterisasi Permukaan Membran Menggunakan Scanning Electron Microscopy (SEM) ... 68
3.17.Prosedur Pengujian SEM... 68
3.18.Pengamatan Water Contact Angle (WCA) ... 70
BAB IV HASIL DAN PEMBAHASAN 4.1. Fabrikasi Membran PES ... 72
4.2. Ketebalan Membran PES ... 73
4.3. Tes Difusi ... 75
4.4. Pengambilan Data dan Perhitungan Larutan NaCl yang Terserap... 75
4.5. Perhitungan Koefisien Difusi ... 78
4.6. Morfologi Karakteristik Permukaan Membran PES ... 81
4.7. Efek Penambahan NMP Pada Morfologi Permukaan Membran PES ... 83
4.8. Efek Konsentrasi NMP Media gelatinisasi Pada Morfologi Permukaan Membran PES ... 86
xi
xii
Gambar 2.2. Proses kerja membran ... 8
Gambar 2.3. Penggolongan membran asimetris ... 9
Gambar 2.4. Penggolongan membran simetris ... 10
Gambar 2.5. Membran tak berpori ... 11
Gambar 2.6. Membran berpori ... 11
Gambar 2.7. Sistem desain filtrasi membran dead-end ... 14
Gambar 2.8. Sistem desain filtrasi membran cross-flow ... 14
Gambar 2.9. Proses filtrasi menggunakan membran berpori pada hemodialisis 16 Gambar 2.10. Struktur molekul PES yang Tersedia Secara Komersial ... 20
Gambar 2.11. Tes difusi dengan metode yang berbeda ... 32
Gambar 2.12. Prinsip kerja SEM ... 35
Gambar 2.13. Hasil pengujian SEM ... 36
Gambar 2.14. Ilustrasi WCA pada membran ... 38
Gambar 2.15. Profil tetes air dan WCA pada permukaan membran dengan hidrofilisitas berbeda ... 38
Gambar 2.16. Gambar WCA dari material ... 40
Gambar 3.1. PES MW 5200 Powder ... 41
Gambar 3.2. PEG MW 1000 ... 42
Gambar 3.3. DMAc ... 42
Gambar 3.4. NMP ... 43
Gambar 3.5. PDMS ... 43
xiii
Gambar 3.10. HMS-79 Magnetic heated stirrer ... 47
Gambar 3.11. Syringe pump SK-500II ... 47
Gambar 3.12. Dino – Lite AM4515 Digital Microscope ... 49
Gambar 3.13. ECTester 11 OAKTON ... 49
Gambar 3.14. Mikrometer Sylvac ... 50
Gambar 3.15. Diagram alir penelitian ... 51
Gambar 3.15. Diagram alir penelitian (lanjutan) ... 52
Gambar 3.16. Diagram alir pembuatan membran PES ... 53
Gambar 3.17. Media gelatinisasi dengan variasi NMP 0 %, 1%, 3%, 5%, 7% .... 55
Gambar 3.18. Kaca sebagai media glass slide ... 56
Gambar 3.19. Metode pembuatan membran ... 56
Gambar 3.20. Proses pengukuran ketebalan membran PES ... 57
Gambar 3.21. Desain structural mengadopsi maze-shaped ... 58
Gambar 3.22. Desain structural layer Gu ... 58
Gambar 3.23. Skema perakitan mikrofilter ... 58
Gambar 3.24. Pembuatan Larutan NaCl ... 59
Gambar 3.25. Skema tes difusi untuk menentukan koefisien difusi ... 61
Gambar 3.26. Skema tes difusi untuk menentukan water flux ... 62
Gambar 3.27. Mengatur flow rate pada syringe pump ... 63
Gambar 3.28. Panel tombol syringe pump ... 64
Gambar 3.29. Skema tes difusi untuk mencari koefisien difusi ... 64
xiv
Gambar 3.34. SEM JSM-7500F ... 68
Gambar 3.35. Diagram Alir Pengujian SEM JSM-7500F ... 69
Gambar 3.36. Skema Percobaan WCA ... 71
Gambar 4.1. Pengukuran ketebalan (mm) memban PES pada masing – masing media gelatinisasi ... 73
Gambar 4.2. Grafik hubungan pengaruh media gelatinisasi terhadap ketebalan membran PES ... 74
Gambar 4.3. Grafik hubungan media gelatinisasi terhadap water flux membran PES ... 77
Gambar 4.4. Grafik hubungan media gelatinisasi terhadap koefisien difusi membran PES ... 79
Gambar 4.5. Hasil SEM membran PES 7 (NMP 7%) bagian lapisan permukaan atas ... 82
Gambar 4.6. Hasil SEM membran PES 7 (NMP 7 %) bagian lapisan bawah ... 82
Gambar 4.7. Hasil SEM membran PES 0 (NMP 0%)... 84
Gambar 4.8. Hasil SEM membran PES 1 (NMP 1%)... 84
Gambar 4.9. Hasil SEM membran PES 3 (NMP 3%)... 85
Gambar 4.10. Hasil SEM membran PES 5 (NMP 5%)... 85
Gambar 4.11. Hasil SEM membran PES 7 (NMP 7%)... 86
Gambar 4.12. Pengamatan Water Contact Angle pada media gelatinisasi NMP 0 % ... 87
Gambar 4.13. Pengamatan Water Contact Angle pada media gelatinisasi NMP 1 % ... 88
xv
xvi
dipisahkan oleh beberapa jenis membran ... 13
Tabel 2.2. Penggolongan nilai fluks dan tekanan pada masing fungsi membran . 13 Tabel 2.3. Karakteristik tiap –tiap modul ... 15
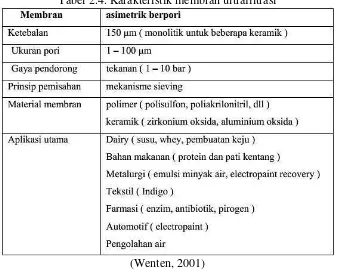
Tabel 2.4 Karakteristik membran ultrafiltrasi ... 16
Tabel 2.5. Material Membran ... 19
Tabel 2.6. Aplikasi PES ... 20
Tabel 2.7. Aplikasi Tipe PES Bubuk (powder) ... 21
Tabel 2.8. Sifat –sifat fisika dan kimia PEG ... 23
Tabel 2. 9. Info produk DMAc... 24
Tabel 2.10. Sifat Fisik DMAc ... 25
Tabel 2.11. Tabel 2.11. Rasio pencampuran dari PES/PEG/DMAc dan strukturnya ... 26
Tabel 2.12. Kondisi persiapan dan performa dari membran ultrafitrasi asimetris 27 Tabel 2.13. Sifat fisika dan kimia air (H2O) ... 28
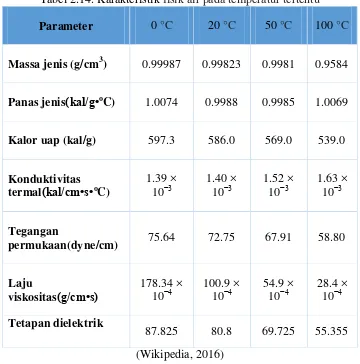
Tabel 2.14. Karakteristik fisik air pada temperatur tertentu ... 29
Tabel 2.15. Tabel 2.15. Sifat fisika dan kimia NMP... 30
Tabel 2.16. Konsentrasi Urea, Na, K, Cl dalam defibrinated bovine blood dan dialisat ... 31
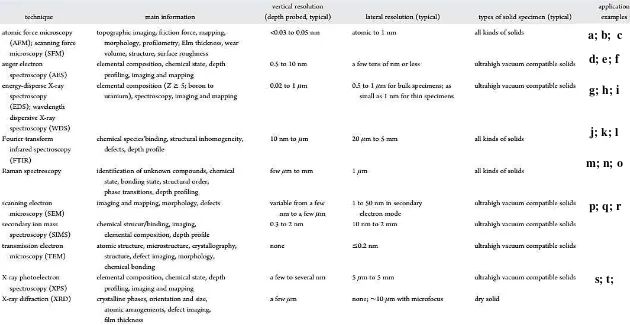
Tabel 2.17. Nilai elektrolit sebelum dan sesudah tes difusi pada membran PES . 32 Tabel 2.18. Teknik Analisa yang paling terkenal untuk karakterisasi kimia fisik membran ... 37
Tabel 2.19. Material membran polimerik dan energi permukaannya ... 39
xvii
Tabel 3.3. Spesifikasi ECTester 11 OAKTON ... 50
Tabel 3.4. Rasio pencampuran larutan membran dan strukturnya (dalam satuan % berat) ... 54
Tabel 3.5. Rasio pencampuran NMP dan akuades sebagai media gelatinisasi ... 55
Tabel 3.6. Alat dan Bahan tes difusi ... 63
Tabel 4.1. Variasi konsentrasi media gelatinisasi ... 73
Tabel 4.2. Pengambilan data dan perhitungan water flux ... 78
xviii
Persamaan 2.2. Koefiseien Difusi ... 34 Persamaan 3.1. Water Flux (WF) ... 66
xix PEG = Polyethylene glycol
DMAc = N, N-Dimethylacetamide
NMP = N-Methyl-2-pyrrolidone
PDMS = Polydimethylsiloxane
MW = Molecular Weight
NaCl = Natrium Chloride
PP = Polypropylene
PE = Polyethylene
PVDF = Polyvinylidene Fluoride
PTFE = Polytetrafluoroethylene
EM = Electron Microscopy
SEM = Scanning Electron Microscope
TEM = Transmission Electron Microscopy
WCA = Water Contact Angle
APD = Alat Pelindung Diri
WAK = Wearable Artificial Kidney
WF = Water Flux (mL/m2.jam.mmHg)
xx Dc = Diffusion coefficient (mm2/detik)
Q = Flow rate dari larutan NaCl (mL/menit)
H = Ketebalan membran (µm)
A = Luas area difusi membran (mm2) CA = Konsentrasi awal larutan NaCl (µS)
CA’ = Konsentrasi akhir larutan NaCl yang terserap (µS)
CB = Konsentrasi awal larutan dialisat (µS)
xxi
Lampiran 1.2. Pengambilan data tes difusi untuk mencari water flux (Pengujian
ke-2) ... 101 Lampiran 1.3. Pengambilan data tes difusi untuk mencari water flux (Pengujian
ke-3) ... 102 Lampiran 1.4. Hasil perolehan water flux (fluks air) dengan luas area difusi (A)
0,000192 m2; waktu pengujian 90 menit; dan tekanan 75 mmHg ... 103 Lampiran 1.5. Hasil perolehan diffusion coeficient (koefisien difusi) dengan laju
xxii
sistem mikrodialisis tanpa cairan dialisis. Sistem mikrodialisis ini menggabungkan antara alat penyaring mikro (mikrofilter) dengan membran berpori yang terbuat dari polyethersulfone (PES). Kesederhanaan dari alat
penyaring mikro ini penting untuk diterapkapkan pada implan sistem dialisis, dimana saat ini wearable artificial kidney (WAK) menimbulkan masalah pada
ukuran dan berat dari pompa dan tangki penyimpanan untuk cairan dialisis. Oleh karena itu, penelitian ini berfokus pada pengembangan membran untuk hemofiltrasi yang tidak memerlukan cairan dialisis tapi memiliki permeabilitas tinggi. Peneliti telah melakukan dua modifikasi untuk meningkatkan permeabilitas dari membran PES, yaitu pada casting solution dan media gelatinisasi. Rasio
konsentrasi yang digunakan pada casting solution merujuk pada penilitian
sebelumnya oleh To dkk, (2015). Sedangkan pada gelatinisasi media, peneliti menggunakan pengaruh dari penambahan n-methyl-2-pyrrolidone (NMP) dalam
media gelatinisasi yang bervariasi. Hasil menunjukkan bahwa pada gelatinisasi dalam NMP 7% memberikan pengaruh yang paling besar terhadap permeabilitas dari membran PES. Dari hasil uji performa dengan melakukan tes difusi diperoleh nilai fluks airsebesar 740,7 L/m2.jam.mmHg dan koefisien difusi mencapai 1,E-01 (0,100) mm2/s. Pengamatan morfologi dengan SEM menunjukkan bahwa ukuran pori – pori membran lebih besar dan distribusi pori yang merata, dimana itu berarti bahwa porositas membran PES meningkat. Sedangkan pada pengamatan water contact angle membran PES yang direndam dalam NMP 7%
memberikan nilai yang terkecil yaitu 43 sehingga dapat dikategorikan membran PES tersebut bersifat hidrofilik. Dari hasil performa dan karakteristik morfologi yang dihasilkan maka dapat disimpulkan bahwa konsentrasi perendaman NMP 7% dapat meningkatkan permeabilitas dari membran PES dengan melakukan modifikasi pada casting solution dan media gelatinisasi.
xxiii
dialysis fluid. This microdialysis system integrates microfilter and nanoporous filtering membrane made of polyethersulfone (PES). The simplicity of this microfilter device is important to be applied in the implantable dialysis system, in which current Wearable Artificial Kidney (WAK) emerges the problems on the size and weight of the pumps and storage tanks for the dialysis fluid. Therefore, this research focuses on developing membranes for hemofiltration that doesn’t require dialysis fluid but its permeability is high. The researcher has conducted two modifications to increase the permeability of PES membranes, that are on casting solution and gelatinization media. The concentration ratio used on casting solution refers to previous research from To et al. (2015). While on gelatinization media, the researcher used the influence of n-methyl-2-pyrrolidone (NMP) additional amout on the varying gelatinization media. The result revealed that the gelatinization of 7 % NMP give the biggest influence on PES membranes permeability. The result of the performance experiment by examining the diffusion shows that the water flux of 740,7 L/m2.hour.mmHg and the diffusion coefficient reaches 1,E-01 (0,100) mm2/s. The morphology monitoring with Scanning Electron Microscopy (SEM) shows that the pores membrane is larger and the pores distribution is spread evenly, in which it means that the PES membranes porosity is increased. While the monitoring of PES membranes water contact angle that submerged in 7 % of NMP shows the smaller value, that is 43 , so it can be categorized that PES membranes are hydrophilic. Hence, by analyzing the result of performance and morphology characteristic, it can be concluded that the gelatinization concentration of 7 % NMP can increase the permeability of PES membranes by modifying casting solution and gelatinization media.
1
1.1.Latar Belakang Masalah
Kejadian penyakit gagal ginjal di Indonesia semakin meningkat. Menurut data statistik yang dihimpun oleh PERNEFRI (Perhimpunan Nefrologi Indonesia), jumlah pasien gagal ginjal di Indonesia mencapai 70.000 orang dan hanya sekitar 13.000 pasien yang melakukan cuci darah atau hemodialisis (Suharjono, 2010). Hemodialisis merupakan terapi pengganti ginjal yang dilakukan 2 sampai 3 kali dalam seminggu dengan lama waktu mencapai 4 – 5 jam, yang bertujuan untuk mengeluarkan sisa – sisa metabolisme protein dan mengoreksi ganguan keseimbangan cairan dan elektrolit menggunakan membran atau dialyzer dengan
bantuan mesin hemodialisis (Black dan Hawks, 2005). Hal yang serupa diungkapkan oleh (Nurani dan Mariyanti, 2013; Smeltzer dkk, 2002) Pasien harus mengeluarkan biaya sangat besar yaitu Rp. 500.000 untuk satu kali cuci darah dan pasien harus menjalaninya sepanjang hidup paling sedikit 3 kali seminggu dengan lama terapi 3 sampai dengan 4 jam per kali terapi.
Selain itu, penggunaan mesin hemodialisis dianggap kurang efisien karena ukurannya yang cukup besar sehingga hanya dapat dilakukan ditempat tertentu atau tempat penyedia layanan hemodialisis seperti rumah sakit, klinik kesehatan, atau dirumah pribadi. Salah satu metode yang dikemukakan oleh Yang dkk (2002) bahwa sistem dialisis implan seperti penggunaan ginjal buatan akan mengurangi frekuensi kunjungan ke rumah sakit dan secara drastis meningkatkan kualitas hidup mereka. Salah satu komponen penting yang menentukan kinerja dialisis adalah membran dialisis. Membran ini memungkinkan molekul yang lebih kecil dari ukuran pori membran untuk menembus lapisan membran dan menghalangi molekul yang lebih besar selama proses dialisis. Sebagian besar sistem dialisis menggunakan polimer sebagai membran dialisis dalam dialyzer
polimer yang secara luas digunakan sebagai membran dalam sistem dialisis karena ukuran pori dan distribusinya mudah dikendalikan dengan mengubah komposisi dari larutan. Sebelumnya, Prihandana dkk, (2012) telah membuat membran yang terbuat dari PES menggunakan inversi fasa basah dan hasilnya membran memiliki stabilitas mekanik tinggi yang cocok untuk sistem dialisis. Mereka juga telah meningkatkan karakteristik compatibility darah membran PES
dengan menempatkan lapisan parylene (Prihandana dkk, 2012) dan lapisan fluorinated diamond-like carbon (F-DLC) (Prihandana dkk, 2013) ke permukaan
membran PES. Tetapi kendala yang dihadapi adalah membran PES yang dilakukan pada penelitian sebelumnya tidak dapat digunakan untuk terapi hemofiltrasi karena membran tersebut belum cukup memiliki permeabilitas yang tinggi terhadap air (water permeability) (Gu dan Miki, 2007).
Oleh karena itu dalam penelitian ini, penulis akan fokus meneliti permeabilitas dari membran PES dengan memodifikasi konsentrasi larutan cetak PES (casting solution) dengan metode pencampuran PES, aditif, dan pelarut, serta
memodifikasi karakteristik permukaan dengan variasi pada media gelatinisasi. PES dengan berat molekul 5200 memiliki kesesuaian yang tinggi terhadap material-material tertentu dan mudah dalam proses pembuatannya. Tetapi PES juga memiliki kelemahan yaitu bersifat hidrofobik (tidak suka air) sehingga akan menyebabkan fouling (penyumbatan) pada membran dan berdampak pada
penurunan aliran dalam proses filtrasi. Oleh sebab itu polyethylene glycol (PEG)
dipilih sebagai aditif, berdasarkan penelitian yang telah dilakukan oleh (Kim dan Lee, 1998) PEG dapat berperan dalam pembentukan pori dan meningkatkan sifat mekanik pada membran serta mengubah karakteristik PES menjadi hidrofilik (suka air). Menurut Idris (2007) menemukan bahwa PEG yang berbeda berat molekul menunjukkan pengaruh yang signifikan terhadap kinerja membran PES. Penambahan zat pelarut pada casting solution menggunakan N-Dimethylacetamide (DMAc). DMAc adalah salah satu pelarut polar organik yang
kelebihan mampu menghasilkan membran dengan lapisan yang rapat dan sangat tipis.
Untuk proses gelatinisasi menggunakan bahan n-methyl-2-pyrrolidone
(NMP) dan akuades, NMP dipilih karena kuat dan mudah larut dalam air, serta memiliki stabilitas kimia dan termal yang tinggi pada semua temperatur air. Media gelatinisasi akan divariasikan untuk mengetahui pengaruh pada masing - masing konsentrasi media gelatinisasi yang berbeda terhadap karakteristik membran PES. Ada 5 variasi media gelatin dalam 300 mL larutan akuades yaitu NMP 1%, 3%, 5%, 7% dan akuades tanpa NMP (0%). Larutan natrium chloride
(NaCl) yang digunakan sebagai molekul nano pengganti darah untuk menguji karakterisik permeabilitas membran dalam tes difusi.
Tujuan yang ingin dicapai dalam penelitian ini adalah memiliki membran PES dengan permeabilitas air yang tinggi untuk diterapkan pada sistem hemofiltrasi dengan melakukan modifikasi pada konsentrasi dari PES, aditif dan pelarut pada casting solution dan modifikasi pada media gelatinisasi sebagai
upaya meningkatkan nilai permeabilitas membran.
1.2.Rumusan Masalah
Perumusan masalah dalam penelitian ini adalah :
1. Bagaimana tahapan dalam pembuatan membran dengan menggunakan PES
molecular weight (MW) 5200 dan menggunakan wet-phase inversion method (metode inversi fasa basah) dengan mencampurkan PEG sebagai zat
aditif dan DMAc sebagai pelarut ?
2. Bagaimana tahapan yang dilakukan dalam pembuatan media gelatinisasi menggunakan variasi pencampuran antara konsentrasi NMP (0%, 1%,3% ,5%, 7%) dan akuades ?
4. Bagaimana hasil pengamatan terhadap karakteristik morfologi dari membran PES berdasarkan uji scanning electron microscopy (SEM) pada
masing – masing variasi media gelatinisasi ?
5. Apakah membran termasuk dalam hidrofilik atau hidrofobik dengan melakukan pengamatan water contact angle (WCA) pada permukaan
membran ?
1.3.Batasan Masalah
Batasan Masalah dalam penelitian ini adalah :
1. Bahan polimer pembuatan membran berupa serbuk PES MW 5200 2. Pembuatan casting solution menggunakan metode inversi fasa basah
3. Pada variasi media gelatinisasi terdapat lima variasi dengan menggunakan campuran NMP 1% ,3%, 5%,7% dan akuades tanpa campuran NMP (0%), kemudian dilarutkan dalam akuades
4. Larutan yang digunakan pada tes difusi menggunakan larutan NaCl sebagai pengganti molekul nano yang akan didifusikan
5. Tes difusi menggunakan mikrofilter dengan desain mengadopsi maze shaped
6. Penelitian ini tidak membahas reaksi kimia yang terjadi selama proses pencampuran polimer, aditif dan pelarut serta media gelatinisasi.
1.4.Tujuan Penelitian
Tujuan penelitian ini adalah :
1. Untuk mengetahui tahapan proses pembuatan membran menggunakan metode inversi fasa basah dengan pencampuran bahan yaitu zat terlarut, pelarut dan adiktif
2. Untuk mengetahui tahapan proses pembuatan media gelatinisasi dengan variasi pencampuran antara konsentrasi NMP (0%, 1%, 3%, 5%, 7%) dan akuades
4. Untuk mengetahui pengaruh media gelatinisasi terhadap karakteristik morfologi membran berdasarkan uji SEM
5. Untuk mengetahui karakteristik pada permukaan membran termasuk dalam hidrofilik atau hidrofobik berdasarkan pengamatan WCA.
1.5.Manfaat Penelitian
Manfaat Penelitian ini adalah :
1. Hasil penelitian ini dapat memperluas pengetahuan pembaca tentang potensi teknologi membran dalam aplikasi hemodialisis, pemurnian air limbah industri maupun medis
2. Dapat mengetahui pembuatan membran dengan metode inversi fasa basah dan media gelatinisasi
3. Dapat mengetahui efek dari konsentrasi NMP terhadap performa membran PES pada uji difusi dan water flux (WF)
4. Dapat mengetahui efek dari konsentrasi NMP terhadap morfologi permukaan membran PES pada uji SEM dan WCA
5. Dapat mengetahui perkembangan alat penyaring mikro (microfilter) yang
digunakan untuk sistem dialisis
6. Hasil dari penelitian ini berpotensi digunakan dalam perkembangan
wearable artificial kidney (WAK) khususnya pada komposisi pembentukan
6
2.1.Tinjauan Pustaka
Membran PES merupakan salah satu jenis material polimer pembuat membran yang digunakan untuk tujuan pemisahan dan penyaringan. Membran PES memiliki karakteristik sifat kimia dan stabilitas termal yang baik dan dapat dibuat pada suhu ruangan. Selain itu, membran PES tahan terhadap metode sterilisasi, termasuk gas epoxy etana, uap, dan -ray, serta sangat permeabel untuk
mendifusikan protein dengan berat molekul yang rendah sehingga mudah diterapkan sebagai membran hemodialisis (Su dkk, 2011). Beberapa peneliti telah mengkaji membran PES pada aplikasi biomedis untuk membuat organ buatan, dan sebagian besar dalam bidang alat-alat kesehatan, membran PES digunakan untuk tujuan pemurnian darah seperti : hemodialisis, hemodiafiltrasi, hemofiltrasi (Tullis, 2002 ; Werner, 1995). Berdasarkan hasil penelitian (To dkk, 2015) mengenai permeabilitas air dari membran PES, hubungan antara konsentrasi larutan PES dan koefisien filtrasi ditunjukkan pada Gambar 2.1.
Berdasarkan garis target (target line) yang terdapat di gambar, nilai yang
diperoleh dari seorang dokter memenuhi persyaratan untuk pengobatan hemofiltrasi manusia. Membran PES terbentuk dari casting solution dengan
konsentrasi PES 17,5 gram memiliki koefisien filtrasi tertinggi di antara semua membran. Hal ini mempengaruhi nilai permeabilitas air lebih tinggi dari nilai target dan secara eksperimen membuktikan konsentrasi ini memiliki kekuatan mekanikal yang cukup (To dkk, 2015). Akan tetapi material polimer PES bersifat hidrofobik yang menyebabkan adanya penyumbatan. Teknik yang dapat diterapkan untuk mengatasi penyumbatan adalah dengan penambahan zat aditif. PEG adalah zat aditif yang paling sering digunakan dalam metode pemisahan fasa dan dapat merubah sifat material polimer menjadi hidrofilik. Membran yang
dibentuk oleh PEG dengan masa molar yang besar memiliki permeabilitas air yang tinggi dan pori – pori yang lebih besar (Chakrabarty dkk, 2008).
Perbandingan antara konsentrasi larutan PES dengan PEG sebagai aditif berpengaruh terhadap nilai permeabilitas air. Seperti yang dipublikasikan oleh Chong dkk, (2012) pada penelitian sebelumnya (dalam To dkk, 2015) memaparkan konsentrasi PEG yang lebih sedikit pada membran dengan konsentrasi PES yang rendah maka akan menghasilkan membran dengan lebih sedikit pori. Oleh karena itu, permeabilitas air akan meningkat sesuai dengan besarnya konsentrasi PES. Untuk meningkatkan porositas membran PES, memodifikasi media gelatinisasi adalah yang paling sering digunakan dalam penelitian. Ghosh dkk, (2009) menemukan bahwa menambahkan 3% konsentrasi
NMP ke dalam air sebagai media gelatinisasi dapat meningkatkan permeabilitas lebih dari 25 %.
Pada penelitian ini, untuk meningkatkan permeabilitas dari membran PES akan dilakukan modifikasi pada konsentrasi casting solution dengan
(0%). Variasi ini dipilih karena pada penelitian sebelumnya penambahan NMP berjarak antara kisaran 1 – 10 %.
2.2. Dasar Teori
2.2.1.Definisi Membran
Membran didefinisikan sebagai suatu media berpori, berbentuk film tipis, bersifat semipermeable yang berfungsi untuk memisahkan partikel dengan ukuran
molekuler (spesi) dalam suatu sistem larutan. Spesi yang memiliki ukuran yang lebih besar dari pori membran akan tertahan sedangkan spesi dengan ukuran yang lebih kecil dari pori membran akan lolos menembus pori membran (Kesting, 1993). Proses pemisahan dengan membran dapat terjadi karena adanya perbedaan ukuran pori, bentuk, serta struktur kimianya. Membran tersebut disebut sebagai membran semipermiable, artinya dapat menahan spesi tertentu, tetapi dapat
melewatkan spesi yang lainnya. Fasa campuran yang akan dipisahkan disebut umpan (feed), hasil pemisahan disebut sebagai permeat (Heru pratomo, 2003).
Skema pemisahan pada membran dapat dilihat pada Gambar 2.2.
2.2.2.Klasifikasi Membran
Membran yang digunakan dalam pemisahan molekul dapat diklasifikasikan berdasarkan morfologi, kerapatan pori, fungsi, bentuknya dan sistem desain filtrasi.
2.2.2.1.Berdasarkan Morfologinya
Dilihat dari morfologinya, membran dapat digolongkan dalam dua bagian yaitu :
a.Membran Asimetrik atau Membran Anisotropik
Membran asimetrik merupakan membran yang mempunyai struktur dan pori yang heterogen. Membran ini meng-kombinasikan selektivitas tinggi dari membran rapat dengan laju permeasi tinggi dari membran tipis sehingga membran asimetris terdiri dari dua lapisan. Lapisan pertama merupakan lapisan kulit yang tipis dan rapat dengan ketebalan 0,1 – 0,5 µm. Lapisan kedua adalah lapisan pendukung yang lebih tebal dan memiliki ukuran pori lebih besar dengan ketebalan 50 -150 µm (Mulder, 1996). Kedua lapisan dapat dibentuk dalam satu kesatuan ataupun terpisah. Selektivitas pemisahan dan laju permasi membran ditentukan oleh lapisan permukaan membran sedangkan lapisan pendukung bertindak sebagai pemberi kekuatan mekanik. Tingginya fluks yang dihasilkan menyebabkan hampir semua proses komersial menggunakan jenis membran ini (Baker, 2004). Penggolongan membran dapat dilihat pada Gambar 2.3.
b.Membran Simetris atau Membran Isotropik
Membran simetris merupakan membran yang memiliki struktur pori homogen dengan ukuran pori yang relatif sama pada kedua sisi membran. Ketebalan membran simetris, baik yang berpori atau tidak adalah sekitar 100-200 µm (Mulder, 1996). Membran simestris dapat dibagi menjadi tiga macam, yaitu membran rapat, membran mikropori, dan membran bermuatan (Baker, 2004). Perbedaan diantara ketiga membran tersebut, digambarkan pada Gambar 2.4.
Gambar 2.4. Penggolongan membran simetris (Baker, 2004)
2.2.2.2.Berdasarkan kerapatan pori
Dilihat kerapatan porinya, membran dapat dibedakan dalam dua bagian yaitu :
a.Membran rapat (Membran tak berpori)
Gambar 2.5. Membran tak berpori (Mulder, 1996)
b.Membran berpori
Membran ini mempunyai ukuran lebih besar dari 0,001 µm dan kerapatan pori yang lebih tinggi. Berdasarkan diameter pori, membran berpori dibagi menjadi tiga, yaitu makropori (diameter pori > 50 nm), mesopori (2 nm < diameter pori < 50 nm), dan mikropori (diameter pori < 2 nm). Membran berpori ini sering digunakan untuk proses ultrafiltrasi, mikrofiltrasi, hiperfiltrasi. Selektifitas membran ini ditentukan oleh ukuran pori dan pengaruh bahan polimer (Mulder, 1996). Berikut ditunjukkan pada Gambar 2.6 :
Gambar 2.6. Membran berpori (Mulder, 1996)
2.2.2.3.Berdasarkan fungsinya
a. Reverse Osmosis
Reverse osmosis merupakan proses perpindahan pelarut dengan gaya dorong perbedaan tekanan, dimana beda tekanan yang digunakan harus lebih besar dari beda tekanan osmosis. Ukuran pori pada proses osmosa balik antara 1-20 µm dan berat molekul antara 100-1000 dalton. Dengan adanya pengembangan membran asimetris proses osmosis balik menjadi sempurna, terutama digunakan untuk memproduksi air tawar dari air laut.
b. Ultrafiltrasi
Ultrafiltrasi mempunyai dasar kerja yang sama dengan osmosa balik, tetapi berbeda dengan ukuran porinya. Untuk ultrafiltrasi ukuran diameter pori yang digunakan yaitu 0,01-0,1 µm dengan berat molekul solut antara 1000-500.000 dalton. Proses pemisahannya ukuran molekul yang lebih kecil dari diameter pori akan menembus membran, sedangkan ukuran molekul yang lebih besar akan tertahan oleh membran.
c. Mikrofiltrasi
Milkrofiltrasi mempunyai prinsip kerja yang sama dengan ultrafiltrasi, hanya berbeda pada ukuran molekul yang akan dipisahkan. Pada mikrofiltrasi ukuran molekul yang akan dipisahkan 500-300.000 dalton, dengan berat molekul solut dapat mencapai 500.000 dalton, karena itu proses mikrofiltrasi sering digunakan untuk menahan partikel-partikel dalam larutan suspensi. d. Dialisa
Dialisa merupakan proses perpindahan molekul (zat terlarut) dari suatu cairan ke cairan lain melalui membran yang diakibatkan adanya perbedaan potensial kimia dari larutan. Membran dialisa berfungsi untuk memisahkan larutan koloid yang mengandung elektrolit dengan berat molekul kecil. Proses secara dialisa sering digunakan untuk pencucian darah pada penderita penyakit ginjal.
Tabel 2.1.Penggolongan diameter pori dan batas berat molekul yang dapat dipisahkan oleh beberapa jenis membran
Tipe Filtrasi Ukuran Partikel Berat Molekul (Dalton) Mikro Filtrasi ≥ 0,1µm ≥ 500.000
Ultra Filtrasi 0,01 – 0,1 µm 1000 – 500.000 Nano Filtrasi 0,001 – 0,01 µm 100 - 1000 Reverse Osmosis ≤ 0,001 µm ≤ 100
(Said, 2009)
Tabel 2.2. Penggolongan nilai fluks dan tekanan pada masing fungsi membran Proses
Mikrofiltrasi 0,1-2(<2) >50 sangat kecil sangat besar Ultrafiltrasi 1-5 10-50 <5% >1000 Nanofiltrasi 5-20 1,4-12 10-80% 200-1000
Osmosa
Balik 10-100 0,05-1,4 90% 50
(Baker, 2004 ; Mulder, 1996)
2.2.3.Sistem Desain Filtrasi Pada Membran
Dua jenis sistem desain membran filtrasi yang sering digunakan adalah sistem filtrasi dead-end dan sistem filtrasi cross -flow (Baker, 2004; Mulder,
1996).
a.Sistem Dead-end
Sistem dead-end adalah sistem desain yang paling sederhana dengan
terbentuk cake atau lapisan partikel di permukaan membran. Ketebalan cake
akan terus meningkat sehingga nilai fluks menurun. Sistem ini masih sering digunakan dalam proses pemisahan mikrofiltrasi, seperti pada bidang farmasi dan medis. Skema dead-end terlihat pada Gambar 2.7.
Gambar 2.7.Sistem desain filtrasi membran dead-end (Baker, 2004)
b.Sistem Cross-flow
Sistem cross-flow merupakan sistem desain yang kompleks dan
memerlukan biaya operasional lebih tinggi dari sistem dead-end. Namun
pilihan sistem desain membran filtrasi ini banyak diaplikasikan di dunia industri karena memiliki kecenderungan penyumbatan yang relatif rendah. Pada sistem cross-flow, larutan dilisat dialirkan paralel terhadap permukaan
membran. Komposisi larutan dialisat dalam modul merupakan fungsi jarak modul, ketika aliran dialisat terbagi menjadi dua, yaitu aliran permeat dan aliran retentat sehingga pembentukan cake akan terjadi sangat lambat karena
tersapu oleh gaya geser aliran cross-flow dialisat. Penurunan fluks dapat
dikontrol dan disesuaikan dengan menggunakan pilihan modul yang tepat dan kecepatan aliran cross-flow. Skema cross-flow terlihat pada Gambar 2.8.
Gambar 2.8.Sistem desain filtrasi membran cross-flow (Baker, 2004) Permeat
2.2.4.Membran Ultrafiltrasi
Ultrafiltrasi adalah suatu proses membran yang sifatnya terletak antara hiperfiltrasi dan mikrofiltrasi. Membran ultrafiltrasi termasuk membran berpori yang mampu menyaring partikel – partikel dengan ukuran 0,01 – 1 mikron. Dimana mampu memisahkan koloid, makro molekul, mikroorganisme, dan partikel penerima yang akan mengalami pengaruh muatan. Mekanisme pemisahan pada proses ultrafiltrasi adalah penyaringan berdasarkan ukuran molekul dengan menggunakan perbedaan tekanan antar membran sebagai gaya dorong. Aliran dari dan ke membran dapat terjadi karena adanya perbedaan tekanan dikedua permukaan membran. Ultrafiltrasi dioperasikan dengan tekanan 1 – 10 atm (Redjeki, 2011).
Membran ultrafiltrasi, dapat dibuat dengan menggunakan modul spiral wound, tubular,hollow fiber serta flat frame filter. Karakteristik tiap – tiap modul
dan membran ultrafiltrasi dapat dilihat pada Tabel 2.3 dan 2.4 berikut :
Tabel 2.3.Karakteristik tiap –tiap modul
Tabel 2.4.Karakteristik membran ultrafiltrasi
(Wenten, 2001)
Membran ultrafiltrasi diaplikasikan antara lain pada industri makanan yaitu untuk pemekatan susu, pembuatan keju, pengambilan protein whey,
klarifikasi juice 32 buah dan alkohol, dan lain - lain. Pada bidang kedokteran, membran ultrafiltrasi digunakan untuk hemodialisis. Membran ultrafiltrasi juga banyak digunakan pada industri obat – obatan, tekstil, kimia, metalurgi, kertas, dan lain – lain (Redjeki, 2011). Ilustrasi proses filtrasi mebran hemodialisis dapat dilihat pada Gambar 2.9. berikut.
2.2.5.Metode Pembuatan Membran
(Mulder, 1996) mengemukakan ada enam metode yang dapat digunakan dalam pembuatan membran, antara lain :
1. Sintering adalah metode sederhana yang digunakan untuk membuat membran
berpori yang terbuat dari bahan organik dan anorganik berbentuk bubuk
(powder) dengan cara menekan dan dipanaskan mencapai suhu mendekati titik
leburnya sesuai dengan material yang digunakan. Bahan yang umum digunakan dengan metode ini seperti polyethylene, polytetrafluoroethylene, polypropylene), logam (stainless steel, steel, tngsten), keramik (aluminium oksida, oksida zirkonium), grafit (karbon) dan kaca (silika).
2. Stretching adalah metode yang digunakan dalam pembuatan film atau foil dari
bahan polimer semi kristal (polytetrafluoroethylene, polypropylene, polyethylene) yang ditarik searah proses ekstrusi sehingga molekul – molekul
kristalnya akan terletak paralel satu sama lain. Pori yang terbentuk dari teknik ini dalah 0,1 – 3 . Porositas membran yang dihasilkan dari teknik ini diatas 90 %.
3. Track-etching adalah metode yang digunakan dalam pembuatan film (polycarbonate) yang diberikan radiasi energi tinggi tegak lurus kearah film.
Partikel radiasi yang diberikan menyebabkan rusaknya matriks polimer dan membentuk satu lintasan. Film yang dibuat kemudian direndam dalam larutan asam atau akali. Selama proses ini polimer yang akan terbentuk berupa silinder berpori seragam dan distribuusi ukuran pori yang sempit.
4. Template-Leaching adalah metode yang digunakan dalam pembuatan membran
dengan cara meleburkan tiga komponen homogen (Na2O – B2O3 – SiO2) pada suhu 1000 – 1500 dan kemudian dikeringkan. Pada proses ini akan terbentuk 2 fase, fase yang pertana lebih didominasi oleh SiO2 yang tidak larut dan fase yang kedua adalah fase yang larut oleh asam atau basa dan akan dihasilkan membran yang memiliki ukuran pori 0,005 atau 5 nm.
5. Coating merupakan teknik pembuatan membran komposit sederhana untuk
mengandung polimer, pre-polimer atau monomer dengan konsentrasi padatan dalam larutan rendah (kurang dari 1%). Membran asimetrik dipisahkan dari bak yang mengandung material pelapis dan pelarut, selanjutnya diperoleh lapisan tipis dari larutan yang menempel pada bak. Setelah itu, film dimasukkan ke dalam oven sehingga pelarut akan menguap dan terjadi crosslinking.
6. Phase Inversion adalah suatu metode persiapan membran yang sering
digunakan untuk menghasilkan membran asimerik. Metode ini ditandai dengan perubahan polimer dari fase cair menjadi padat. Proses solidifikasi diawali dengan trasnsisi fase cair satu (polimer dan pelarut) dan fase cair dua (polimer dan non-pelarut). Selama proses pencampuran, salah satu fase cair (fase polimer konsentrasi tinggi) akan memadat sehingga terbentuk atriks padat. Pengendalian tahap awal transisi fase akan menentukan morfologi membran yang dihasilkan. Konsep dase inversi mencakup berbagai teknik anatara lain penguapan pelarut, presipitasi dengan penguapan terkendali, prespitasi termal, prespitasi fase uap, dan prespitasi imersi. Prespitasi immersi merupakan proses pencetakan film tipis dipermukaan kaca gelas datar, selanjutnya mencampurkan casting solution untuk membentuk membran. Proses ini
dilakukan dengan 2 cara, yaitu evaporasi langsung dan perendaman dalam non-pelarut.
2.2.6.Material Membran Ultrafiltrasi
Ultrafiltrasi menggunakan membran berpori dan mempunyai stuktur asimetrik. Membran yang paling banyak digunakan secara komersial dalam proses ultrafiltrasi dibuat dengan menggunakan proses inversi fasa. Beberapa material yang sering digunakan adalah :
a. Polysulfone/ polyethersulfone
b. Polivinilidene flourida
c. Polyacrilonitrile
d. Cellulosa asetat
Polysulfone dan polyethersulfone mempunyai stabilitas kimia dan termal
yang sangat baik dan diindikasikan dengan nilai Tg ( temperatur perubahan keadaan dari sifat karet ke sifat gelas ) yang cukup tinggi yakni sekitar 190ºC dan 230ºC. Polimer – polimer ini banyak digunakan secara luas sebagai membran ultrafiltrasi dan sebagai bahan penopang pada membran komposit. Pada dasarnya semua polimer dapat digunakan sebagai material utama pembuat membran tetapi adanya bermacam – macam sifat fisika dan kimia, sehingga hanya beberapa saja
yang bisa digunakan. Batasan pH pada temperatur 25˚C dan temperatur max pada
pH 7 untuk polimer membran yang berbeda dan informasi mengenai ketahanan terhadap bahan kimia diperlihatkan pada tabel 2.5 (Redjeki, 2011).
2.2.7.Polyethersulfone (PES)
PES merupakan material polimer yang sangat luas digunakan pada persiapan mikrofiltrasi (MF), ultrafiltrasi (UF) dan membran pemisahan gas. Disamping itu, PES memiliki karakteristik temperatur, toleransi pH, ketahanan terhadap chlorine dan mudah dalam fabrikasi membran dengan bermacam –
macam variasi bentuk dan modul. PES juga memiliki rentang ukuran pori – pori yang dapat diaplikasikan pada UF dan MF dengan kisaran antara 19 Å sampai 0,2
dan tahan pada bahan kimia seperti aliphatic hydrocarbons, alcohols, dan acids (Cheryan, 1998). Struktur molekul PES dapat dilihat pada gambar 2.10.
Gambar 2.10.Struktur molekul PES yang tersedia secara komersial (Sumitomo Chemical Co.Ltd, 2010)
Polimer PES ini dapat diaplikasikan pada berbagai bidang, seperti sektor pertanian, industri makanan, dan kesehatan (biomedical). PES dengan bentuk
serbuk (powder) sangat cocok diaplikasikan pada coating, hollow-fiber maupun
sebagai penguat pada compound dan epoxy. Berikut dijabarkan lebih lanjut pada
tabel 2.6 dan 2.7
Tabel 2.6.Aplikasi PES
Powder Grades
Reduced
Viscosity Main Applications
3600P 0.36 Compounds
4100P 0.41 Paint / coating compounds, adhesives
4800P 0.48 Flat films and hollow-fiber membranes, adhesives
5003P 0.50 Paint / coating compounds, adhesives, impact modifier for epoxy compound
5200P 0.52 Flat films and hollow-fiber membranes
Tabel 2.7.Aplikasi Tipe PES Bubuk (powder)
Baik Cukup - Kurang
2.2.8.Polyethylene Glycol (PEG)
PEG termasuk kedalam golongan polimer sintetis. PEG mempunyai kelarutan yang baik dalam air dan kesamaan secara struktur kimia karena adanya gugus hidrosil primer pada ujung rantai polieter yang mengandung oksietilen (-CH2- CH2-O-). PEG mempunyai sifat stabil dan mudah larut dalam air hangat, tidak beracun, non-korosif, tidak berbau, tidak berwarna, memiliki titik lebur yang sangat tinggi (580 ), tersebar merata, higoskopik (mudah menguap) dan juga dapat mengikat pigmen. PEG berbentuk putih seperti lilin yang menyerupai paraffin. Berupa bentuk padat dalam suhu kamar, dapat mencair pada suhu 104 ) dan memiliki berat molekul rata – rata 1000 (Mitchell, 1972).
Penambahan bahan aditif pada membran berguna untuk meningkatkan atau memodifikasi sifat-sifat mekanik, kimia, dan fisik membran (Kim dkk, 1989). PEG merupakan salah satu diantara zat aditif yang sering ditambahkan pada pembuatan membran yang berfungsi sebagai porogen untuk meningkatkan keteraturan bentuk pori-pori pada membran sehingga struktur pori lebih rapat dan membran yang dihasilkan semakin bagus. Dalam memodifikasi membran, PEG ini berfungsi sebagai zat aditif untuk meningkatkan absorpsi dan disolusi suatu zat aktif yang sukar larut dalam air. Bahan material polimer seperti PES mempunyai
Tipe
For Epoxy Adhesive Membrane
kelarutan yang kecil dalam air, sehingga akan mengakibatkan menurunnya aliran
water flux karena adanya penyumbatan pada area pori – pori membran selama
proses filtrasi (Shargel dkk, 1999).
PEG adalah senyawa hasil kondensasi dari oksietilen dan air dengan rumus molekul H(OCH2CH2)nOH, dimana n merupakan bilangan (jumlah)
rata-rata pengulangan grup oksietilen mulai dari 4 sampai 180. Bilangan yang mengiringi dibelakang PEG menunjukkan berat molekul rata-rata dari pada PEG, seperti PEG dengan n = 80 akan mempunyai berat molekul rata-rata sekitar 3500 Dalton dan dicantumkan sebagai PEG 3500. Sedangkan senyawa dengan berat molekul rendah terdiri dari n = 2 sampai n = 4 seperti diethylene glycol, triethylene glycol, dan tetraethylene glycol, merupakan senyawa-senyawa murni.
Senyawa dengan berat molekul rendah sampai 700 bersifat cairan kental, tidak berwarna, tidak berbau dengan titik beku -10 ºC (diethylene glycol), sementara
senyawa-senyawa hasil polimerisasi dengan berat molekul yang lebih tinggi yaitu sampai 1000 berbentuk padat seperti lilin dengan titik didih mencapai 67 ºC untuk n = 180. Sifat-sifat fisika PEG dapat dilihat pada Tabel 2.7 (Wikipedia, 2007). Keistimewaan dari PEG adalah senyawa tersebut bersifat larut dalam air (Chou dkk, 2007). PEG juga larut dalam berbagai pelarut organik dari golongan hidrokarbon aromatik, seperti metanol, benzen, dichlorometane dan tidak larut
dalam dietil eter dan heksan. Sifat-sifat lain daripada PEG adalah merupakan senyawa yang tidak beracun, netral, tidak mudah menguap dan tidak iritasi. Pelarut PEG banyak digunakan sebagai emulsifier dan detergen, humectants, dan
pada bidang farmasi (Wikipedia, 2007). Berikut ditampilkan pada Tabel 2.8
Tabel 2.8.Sifat –sifat fisika dan kimia PEG PEG (Polyethylene glycol)
Nama Kimia Polyethylene glycol
Rumus kimia C2nH4n+6On+2 Berat molekul 44n + 62 g/mol
Bilangan CAS [25322-68-3]
Densitas 1,1 – 1,2 g/cm
Titik cair 104
Titik lebur 580
Titik api 182 – 287
(Wikipedia, 2007)
Semakin besar nilai berat molekul PEG maka akan semakin padat PEG tersebut dan sebaliknya. PEG berdasarkan molekulnya dibagi menjadi : PEG 200, 400, 600, 1000, 1500, 1540, 3350, 4000, 6000, 8000 dan diatas 100.000 sampai 300.000. PEG dengan berat molekul dibawah 1000 berupa cairan jernih tidak berwarna, PEG dengan berat molekul 1000 – 1500 berupa semi padat. PEG 3000
– 20.000 berupa padatan semi kristalin, dan diatas 100.000 berupa resin pada suhu kamar. Jadi PEG semakin meningkat kekerasannya dengan bertambah besarnya berat molekul. Umumnya PEG dengan berat molekul 1500 – 2000 yang digunakan untuk pembuatan dispersi padat. Sedangkan untuk PEG dibawah 1500 digunakan dalam dispersi cair (Leuner dan Dressman, 2000)
2.2.9.N,N-Dimethylacetamide (DMAc)
pelarut DMAc tidak reaktif dalam reaksi kimia dan juga memiliki konstanta dielektrik yang tinggi, DMAc benar-benar larut dalam air, eter, ester, keton, senyawa aromatik dan senyawa alifatik tidak jenuh. DMAc memiliki kestabilan yang bagus, dan tidak akan mengalami degradasi dan perubahan warna jika dipanaskan dibawah suhu 350 . DMAc memiliki titik leleh 161 dan memiliki titik beku -20 (Delacourt dkk, 2006). Berikut informasi produk dari DMAc dan sifat fisik yang dimiliki pada Tabel 2.9 dan 2.10 berikut.
Tabel 2.9.Info produk DMAc
Tabel 2.10.Sifat fisik DMAc
(Merck Schuchardt OHG, 2016)
2.2.10.Proses Pembuatan Membran
PES merupakan termoplastik yang dapat membentuk membran yang digunakan untuk tujuan pemisahan dan filtrasi. PES terkenal memiliki permeabilitas dan permseleksitivitas tinggi, stabil secara mekanik dan temperatur dan juga tahan terhadap bahan kimia serta dapat dibuat pada suhu ruangan. Selain itu, PES mempunyai toleransi pada berbagai macam metode sterilisasi dan bersifat permeabel untuk mendifusikan molekul-molekul seperti protein ketika diaplikasikan untuk membran hemodialisis (Su dkk, 2011). Beberapa peneliti telah menggunakan PES pada aplikasi biomedikal untuk membuat organ buatan, dan dalam bidang alat – alat kesehatan banyak digunakan untuk tujuan pemurnian darah seperti : hemodialisis, hemodialfiltrasi, plasmapheresis dan pengumpulan plasma (Zhao dkk, 2001 ; Tullis dkk, 2002 ; Samtleben dkk ; 2003). Membran
ultrfiltrasi yang digunakan terbuat dari campuran PES dengan berat molekul 5200,
diatas dapat dilakukan dengan cara memodifikasi membran saat preparasi dan sesudah preparasi.
Dalam penelitian ini, dilakukan modifikasi membran saat preparasi
(casting solution) yaitu dengan penambahan komposisi zat aditif PEG dan pelarut
DMAc dengan metode inversi fase basah, dan modifikasi media gelatinisasi dengan menggunakan NMP. Pemilihan DMAc sebagai pelarut berdasarkan parameter kelarutan ( dimana parameter kelarutan ( yang memiliki polimer PES hampir sama. Kualitas pelarut akan berpengaruh pada morfologi membran. Pelarut yang baik akan mudah melarutkan polimer sehingga meningkatkan viskositas intrinsiknya. Sedangkan pelarut yang buruk mengakibatkan polimer akan berinteraksi dengan sesamanya dibandingkan dengan pelarut. Viskositas dari larutan polimer sangat penting dalam proses pembentukan membran. Dalam pembuatan membran penambahan aditif merupakan senyawa kimia yang dapat larut dalam pelarut maupun dalam non-pelarut. Maka akan terbentuk ruang kosong yang ditinggalkan, sehinga akan terbentuk pori dalam membran. Masaa molekul relatif aditif akan menentukan besar pori yang terbentuk. Berikut modifikasi yang dilakukan oleh beberapa peneliti sebelumnya pada tabel 2.11 dan 2.12:
Tabel 2.11.Rasio pencampurandari PES/PEG/DMAc dan strukturnya
27 Tabel 2.12. Kondisi persiapan dan performa dari membran ultrafitrasi asimetris
2.2.11.Media Gelatinisasi
2.2.11.1.Akuades atau Air murni (H2O)
Air adalah substansi kimia dengan rumus senyawa kimia H2O satu mulekul air yang tersusun atas dua atom hidrogen tidak berwarna, tidak berasa dan tidak berbau pada kondisi standar, yaitu pada tekanan 100 kPa (1 bar) dab pada temperatur 0 . Air merupakan suatu pelarut universal, karena dapat
melarutkan banyak zat kimia seperti garam, gula, asam, beberapa jenis gas dan banyak macam molekul organik. Berikut karakteristik fisika dan kimia air dijelaskan pada Tabel 2.13. dan Tabel 2.14 :
Tabel 2.13.Sifat fisika dan kimia air (H2O)
Air
Nama sistematis Air
Nama alternatif Aquades, dihidrogen, monoksida, Hidrogen hidroksida
Rumus molekul H2O
Massa molar 18.0153 g/mol
Densitas dan Fase 0.998 g/cm³ (cariran pada 20 °C) 0.92 g/cm³ (padatan)
Titik lebur 0 °C (273.15 K) (32 °F) Titik didih 100 °C (373.15 K) (212 °F) Kalor jenis 4184 J/(kg·K) (cairan pada 20 °C)
Tabel 2.14.Karakteristik fisik air pada temperatur tertentu
permukaan(dyne/cm) 75.64 72.75 67.91 58.80
Laju
NMP merupakan salah satu senyawa organik yang terdiri atas 5 lactam.
NMP berbentuk cair dan sebenarnya tidak berwarna, meskipun pada sampelnya terlihat berwarna kuning. NMP mudah larut dalam air dan pelarut organik lainnya. NMP juga termasuk golongan pelarut dipolar aprotic sama seperti dimethylformamide dan dimethylsulfoxide. NMP umumnya digunakan pada
industri pertokimia, industri plastik, pemurnia minyak pelumas, dan sebagai pelarut polimer dalam polimerisasi (Harreus, 2011). Penambahan NMP sebagai pelarut pada media gelatinisasi dengan konsentrasi yang berbeda akan memperngaruhi struktur dari membran PES. Penambahan NMP dengan konsentrasi polimer yang lebih kecil seketika itu juga dapat menghentikan
pori – pori membran. (Ghosh dkk, 2008) menemukan dengan penambahan sedikit persentase dari pelarut ke dalam media gelatinisasi (3% NMP ke dalam air) dapat mempengaruhi permeabilitas dari membran lebih dari 25%. Berikut sifat fisika dan kimia NMP ddapat dilihat pada Tabel 2.15 :
Tabel 2.15.Sifat fisika dan kimia NMP
NMP (N-Methyl-2-Pyrrolidone)
Nama lain N-Methylpyrrolidone; N
-Methylpyrrolidinone; NMP; 1-Methyl-2-pyrrolidone; Pharmasolve
Bentuk Cairan
Berat jenis 99.13 g.mol-1 Ikatan kimia C5H9NO Massa jenis 1.028 g/cm3 Mudah larut dengan air 100 %
Titik didih 202 – 204 °C (396 – 399 ; 475 – 477 K) Titik lebur -24.4°C (-11 ; 249 K)
Tekanan uap 3.4 Tingkat penguapan ~100 Titik nyala 346°C
2.2.12.Pengujian Performa Membran 2.2.12.1.Tes Difusi
Tes difusi dilakukan untuk mengetahui permeabilitas dan biokompatibilitas membran. Prihandana dkk, (2013) mendesain dan merakit miniatur sistem hemodialisis yang dapat dilihat pada Gambar 2.15. Tes difusi dilakukan dengan mengalirkan darah dan larutan dialisat ke dalam dua sisi masuk alat mikrofilter (chamber). Sehingga molekul dengan ukuran pori - pori yang
lebih kecil dari pada ukuran pori – pori membran dapat terdifusi melewati membran. Tes difusi dibagi ke dalam dua tipe yang berbeda, yaitu tes difusi jangka pendek dan tes difusi jangka panjang. Untuk tes didifusi jangka pendek memerlukan waktu pengujian sekitar 3 jam dengan menggunakan sistem single pass yang bertujuan untuk menguji nilai permeabilitas dari membran. Sedangkan
tes difusi jangka panjang memerlukan waktu pengujian yang lebih lama yaitu sekitar 24 hari dengan menggunakan sistem loop. Dalam tes difusi ini diperlukan
adanya larutan yang memiliki konsentrasi molekul yang menyerupai darah dalam sistem hemodialisis. Larutan NaCl dipilih karena merupakan standar kesehatan yang digunakan dalam larutan dialisat. Larutan NaCl dan dialisat akan yang digunakan sebagai media transport. Berikut ditunjukkan pada Tabel 2.16.
konsentrasi dari larutan serta Tabel 2.17 nilai elektrolit. Kemudian skema tes difusi dapat dilihat pada Gambar 2.11.
Tabel 2.16. Konsentrasi Urea, Na, K, Cl dalam defibrinated bovine blood dan
Gambar 2.11.Tes difusi dengan metode yang berbeda : (a) Tes difusi jangka pendek ; (b) Tes difusi jangka panjang ; (c) Parameter yang digunakan dalam
pengukuran koefisien difusi (Prihandana, 2013)
Tabel 2.17.Nilai elektrolit sebelum dan sesudah tes difusi pada membran PES
Molekul Sebelum Tes Difusi Sesudah Tes Difusi
K 148 147
Na 2.3 2.8
Cl 96 93
(Prihandana dkk, 2013)
2.2.12.2.Permeabilitas Membran / Water Flux (WF)
permeabilitas membran adalah nilai WF, yang didefinisikan sebagai volune permeat yang melewati satu satuan luas membran dalam waktu tertentu. WF dapat dinyatakan dalam persamaan 2.1. berikut (To dkk, 2015) :
Water Flux
...(2.1)
Dimana : : Water Flux (mL/m2.jam.mmHg)
Q : Volume permeat (mL)
A : Luas area difusi membran (m2) t : Waktu pengujian (jam)
P : Tekanan pembuluh darah arteri (mmHg)
WF merupakan salah satu parameter kinerja membran yang dipengaruhi oleh beberapa faktor, yaitu (i) parameter operasi seperti konsentrasi umpan, suhu, laju alir, dan tekanan, (ii) sifat-sifat fisik larutan umpan, dan (iii) faktor desain. Kenaikan konsentrasi dialisat menyebabkan fluks akan turun. Perubahan konsentrasi dialisat akan merubah harga viskositas, densitas, dan diffusifitas larutan dialisat. Demikian juga, peningkatan suhu dapat menaikkan fluks baik pada daerah yang dikendalikan oleh tekanan atau yang dikendalikan oleh perpindahan massa. Fluks dapat juga dinyatakan sebagai koefisien permeabilitas. Nilai permeabilitas membran menunjukkan kemampuan membran dalam melewatkan pelarut. Koefisien permeabilitas untuk membran jenis proses ultrafiltrasi berada pada kisaran 0,5 m3/m2.hari.bar (20 L/m2.jam.bar) – 5 m3 /m2.hari.bar (200 L/m2.jam.bar) (Wenten, 1999).
2.2.12.3.Koefisien Difusi
[
Menurut Mulder (1996), karakterisasi membran dapat dikelompokkan menjadi dua, yaitu (1) membran berpori (porous membrane), (2) membran tidak
berpori (nonporous membrane). Pada membran berpori, pemisahan terjadi akibat
perbedaan ukuran antara partikel/molekul dan pori membran dibantu dengan adanya tekanan trans membran sebagai driving force. Mikrofiltrasi dan
ultrafiltrasi merupakan jenis membran berpori. Di sisi lain untuk membran tidak berpori, seperti pervaporasi, separasi gas dan dialisis, pemisahan terjadi akibat perbedaan laju kelarutan (solubility) dan/atau perbedaan diffusivitas (diffusivity).
Tingkat kelarutan dan diffusivitas ditentukan oleh sifat intrinsik bahan membran. Zhao dkk, (2000) menentukan beberapa metode yang dapat dilakukan untuk mengetahui ukuran pori – pori dan distribusi membran berpori, yaitu : (1). mikroskop elektron, (2). Gelembung udara dan transport gas, (3) mercury porosimetry, (5) equilibrium liquid-vapor, (6) liquid-solid equilibrium (thermoporometry) dan, (6) gas-liquid equilibrium (permporometry).
2.2.13.1.Scanning Electron Microscope (SEM)
Electron Microscopy (EM) adalah salah satu alat yang paling baik yang
pori-pori, morfologi, dan struktur membran. SEM dan Transmission Electron Microscopy (SEM) adalah dua alat yang paling sering digunakan untuk
pengematan langsung dalam metode EM. Perbedan dari TEM dan SEM adalah pada cara bagaimana elektron yang ditembakkan oleh pistol elektron mengenai sampel. Pada TEM, sampel yang disiapkan sangat tipis dehingga elektron dapat menembusnya kemudian hasil dari tembusan elektron tersebut yang diolah menjadi gambar (Powers dkk, 2006). Kelemahan yang dihadapi adalah karena sampel yang diperlukan sangat tipis, maka kerusakan memerlukan waktu yang lama untuk preparasi dan dikhawatirkan terjadi kerusakan struktur sampel. Sedangkan pada SEM sampel tidak ditembus oleh elektron sehingga hanya pendaran hasil dari tumbukan elektron dengan sampel yang ditangkap oleh detektor dan diolah. Penggunaan SEM lebih mudah karena sampel yang diperlukan tidak setipis sampel yang digunakan pada TEM. Pori – pori dengan ukuran lebih besar dari 1 nm dapat dilakukan pengujian SEM (Chakrabarty dkk, 2008 ; Yang dkk, 2004). Berikut prinsip kerja SEM dan contoh hasil SEM dilihat pada Gambar 2.12. dan Gambar 2.13. dan Tabel 2.18. teknik analisa yang paling dikenal dari beberapa peneliti sebelumnya :
(a)
(b)
Gambar 2.13.Hasil pengujian SEM ; (a) morfologi permukaan atas membran, (b) penampang melintang membran
37 (Chakrabarty dkk, 2008(a) ; Idris dkk, 2007(b); Oh dkk, 2001(c); Yang dkk, 2003(d); Perez dkk, 193(e) ; Wang dkk, 2006(f) ; Ochoa dkk, 2001(g); Fan dkk,
2008(h); Chen dkk, 2009(i); Yang dkk, 2007(j); Benavete dkk,1998(k); Campos dkk, 1997(l) ; Kim dkk, 1999(m); Bottino dkk, 2001(n); Khulbe dkk, 2000(o); Wei
dkk, 2006(p); Saito dkk, 1998(q); Kazama dkk, 2004(r) ; Ferjani dkk, 2000(s) ; Yang dkk, 2007(t))
a; b; c
d; e; f
g; h; i
j; k; l
m; n; o
2.2.13.2.Water Contact Angle (WCA)
2.2.13.2.1.Membran Hidrofilik dan hidrofobik
Gambar 2.14. Ilustrasi WCA pada membran
(Wenten dkk, 2015)
WCA adalah sudut yang dibentuk oleh sebuah garis singgung terhadap cairan pada garis kontak dan sebuah garis yang melalui dasar dari tetes cairan. Secara umum sifat permukaan membran dibagi menjadi dua, yaitu hidrofilik dan hidrofobik. Pada membran hidrofilik, air akan membasahi membran secara spontan. Sedangkan pada membran hidrofobik, pembasahan membran oleh air tidak terjadi (Wenten dkk, 2015). Bentuk profil tetes air dan WCA pada permukaan membran dapat dilihat pada Gambar 2.15. berikut.
Gambar 2.15.Profil tetes air dan WCA pada permukaan membran dengan hidrofilisitas berbeda
Menurut Albrecht dkk, Material hidropfobik umumnya dibuat dari polimer yang memiliki energi permukaan rendah, seperti: polypropylene (PP), polyethylene (PE), polyvinylidene fluoride (PVDF) atau polytetrafluoroethylene
(PTFE) (dalam Wenten, 2015). Berikut beberapa material membran polimerik dan energi permukaannya dilihat pada Tabel 2.19.
Tabel 2.19.Material membran polimerik dan energi permukaannya
(Mulder, 1996 ; Ahmad dkk., 2014)
2.2.13.2.2.Pengamatan dan Pengukuran WCA
Diantara bermacam – macam motode untuk pengukuran sudut kontak, metode sessile drop adalah metode yang paling umum digunakan (Adamson,
2007). Metode sessile drop dilakukan dengan meneteskan cairan pada permukaan
membran kemudian pengamatan dilakukan dengan menggunakan mikroskop untuk melihat sudut yang dihasilkan antara cairan dan membran. Maksud dari pengukuran sudut kontak air ini adalah untuk mengetahui sifat membran yang hidrofilik atau hidrofobik. Semakin membran bersifat hidrofilik maka membran akan mudah melarutkan air sehingga berpengaruh pada energi permukaan dan kemampuan rejeksi membran (Nunes dkk, 1992).
area berbeda tersebut. Berikut tampilan gambar WCA dan hasil pengujian dari peneliti sebelumnya dapat dilihat pada Gambar 2.16, Tabel 2.20 dan Tabel 2.21.
(a) (b)
Gambar 2.16. Gambar WCA dari material (a) PVP 0, (b) PVP 8 (Kanagaraj dkk, 2015)
Tabel 2.20. Hasil pengujian WCA
Kode Membran WCA (◦)
PVP 0 45.5 ± 0.2
PVP 2 51.0 ± 0.5
PVP 4 55.6 ± 1.2
PVP 6 61.4 ± 1.7
PVP 8 70.2 ± 0.6
(Kanagaraj dkk, 2015)
Tabel 2.21. Hasil pengujian WCA
Membran WCA (◦)
PES 64.5 ± 3.3
PES-PVP 64.1 ± 2.9
PES-PEG 54.1 ± 1.9
PES-Plu 61.7 ± 2.8
PES-PANI 65.2 ± 41.8
41
Pada penelitian ini untuk mencapai tujuan yang ingin dicapai oleh penulis, penulis menggunakan beberapa alat dan bahan yang menunjang penelitian yaitu sebagai berikut :
3.1.Bahan Penelitian
Adapun bahan yang digunakan dalam penelitian ini terdiri dari beberapa bahan kimia yaitu sebagai berikut :
1. PES MW 5200 berbentuk serbuk diproduksi oleh Sumitomo Chemical Co, Tokyo, Japan digunakan sebagai zat pelarut / polimer untuk pembuatan larutan membran seperti yang terlihat pada Gambar 3.1.
Gambar 3.1.PES MW 5200 Powder
Gambar 3.2.PEG MW 1000
3. DMAc diproduksi oleh Merck Schuchardt OHG sebagai pelarut seperti yang terlihat pada Gambar 3.3.
4. NMP diproduksi oleh Merck KGaA, EMD Millipore Co., USA digunakan sebagai pelarut untuk media gelatinisasi sepert yang terlihat pada Gambar 3.4.
Gambar 3.4.NMP
5. Polydimethylsiloxane (PDMS) diproduksi oleh Dow Corning Corp. digunakan
untuk pembuatan bagian layer pada mikrofilter seperti yang terlihat pada Gambar 3.5.
6. Sodium chloride / Natrium Chloride (NaCl) diproduksi oleh Merck KgaA,
EMD Millipore Co., USA digunakan untuk larutan dialisat sebagai pengganti molekul nano dalam pengujian difusi seperti yang terlihat pada Gambar 3.6.
Gambar 3.6.NaCl(Natrium Chloride /Sodium Chloride)
7. Akuades didapat di tempat bahan kimia Progo Mulyo digunakan sebagai larutan dialisat untuk tes difusi seperti yang terlihat pada Gambar 3.7.
3.2.Alat penelitian
Alat – alat yang digunakan pada penelitian ini diantaranya adalah :
1.Alat Pelindung Diri (APD), antara lain : sarung tangan medis, masker, dan kaca mata
2.Timbangan digital
Pada penelitian ini timbangan digital ber-merk ACIS Digital Scale MN-Series yang digunakan untuk menimbang bahan – bahan dengan komposisi
tertentu sebelum dicampurkan, seperti : PES, PEG dan NaCl seperti yang terlihat pada Gambar 3.8 dan Tabel 3.1.
Gambar 3.8.Timbangan digital Tabel 3.1.Spesifikasi ACIS MN Series
Model Number MN-200
Capacity 200g
Ketelitian 0.01 g
Weighing Pan 6.8 cm x 6.3 cm Units g / ct / oz / dwt