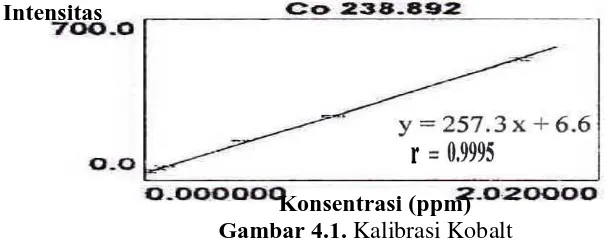
Lampiran 2. Gambar tumbuhan kangkung dan ladang kangkung
Gambar 2.1. Tumbuhan Kangkung (Ipomoea aquatica Forssk.)
Lampiran 3. Bagan alir proses destruksi kering untuk logam kobalt dan molibdenum
Kangkung
Ditimbang 10 gram di atas krus porselen Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering
Hasil
Dilakukan selama 48 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dibersihkan dari pengotoran
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dicuci bersih
Dihaluskan dengan blender
Lampiran 4. Bagan alir proses destruksi kering untuk logam kalium dan natrium
Kangkung
Ditimbang 7 gram di atas krus porselen Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering
Hasil
Dilakukan selama 48 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dibersihkan dari pengotoran
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dicuci bersih
Dihaluskan dengan blender
Lampiran 5. Bagan alir proses pengujian sampel
Sampel yang telah didestruksi
Dilarutkan dengan 5 ml HNO3 (1:1) dalam krus
Dituangkan ke dalam labu ukur 50 ml
Diencerkan dengan akua demineralisata hingga garis tanda
Dimasukkan ke dalam botol Larutan sampel
Disaring dengan kertas saring Whatman No.42 42 42
Filtrat
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kuantitatif dengan Inductively Couple Plasma pada λ 240,7 nm untuk logam kobalt, λ 313,3 nm untuk logam molibdenum, pada λ 766,5 nm untuk logam kalium, λ 589 nm untuk logam natrium
Lampiran 6. Data kalibrasi kobalt dengan inductively coupled plasma, perhitungan persamaan garis regresi dan koefisien korelasi (r)
No. Konsentrasi (mg/l) (X)
Intensitas (I)
1. 0,000000 2,60602
2. 0,050000 16,0638
3. 0,100000 30,1177
4. 0,500000 147,563
5. 1,000000 264,325
6. 2,000000 518,063
No. X Y XY X2 Y2
1. 0,000000 2,60602 0,000000 0,000000 6,791340 2. 0,050000 16,0638 0,80319 0,002500 258,0456 3. 0,100000 30,1177 3,01177 0,010000 907,0758 4. 0,500000 147,563 73,7815 0,250000 21774,83897 5. 1,000000 264,325 264,325 1,000000 69867,70563 6. 2,000000 518,063 1036,126 4,000000 268389,272
∑ 3,65
X = 0,6083
978,73852
Y =163,1230 1378,04746 5,2625 361203,7293
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)(
)
Y = a X + b b = Y − aX
= 163,1230 – (257,2723)(0,6083) = 6,6242
Maka persamaan garis regresinya adalah: Y = 257,2723 X + 6,6242
=
(
)(
)
(
)
Lampiran 7. Data kalibrasi molibdenum dengan inductively coupled plasma, perhitungan persamaan garis regresi dan koefisien korelasi (r)
No. Konsentrasi (mg/l) (X)
Intensitas (I)
1. 0,000000 5,56373
2. 0,050000 56,7261
3. 0,100000 106,575
4. 0,500000 519,565
5. 1,000000 1035,28
6. 2,000000 2010,08
No. X Y XY X2 Y2
1. 0,000000 5,56373 0,000000 0,000000 30,95509151 2. 0,050000 56,7261 2,836305 0,002500 3217,850421 3. 0,100000 106,575 10,6575 0,010000 11358,23063 4. 0,500000 519,565 259,7825 0,250000 269947,7892 5. 1,000000 1035,28 1035,28 1,000000 1071804,678 6. 2,000000 2010,08 4020,16 4,000000 4040421,606
∑ 3,65
X =0,6083
3733,78983
Y = 622,2983 5328,716305 5,2625 5396781,11
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)
Y = a X + b b = Y − aX
= 622,2983 – (1005,0121)(0,6083) = 10,9494
Maka persamaan garis regresinya adalah: Y = 1005,0121X + 10,9494
=
(
)
Lampiran 8. Data kalibrasi kalium dengan inductively coupled plasma, perhitungan persamaan garis regresi dan koefisien korelasi (r)
No. Konsentrasi (mg/l) (X)
Intensitas (Y)
1. 0,000000 213,092
2. 10,00000 4140,00
3. 20,00000 8210,86
4. 40,00000 16118,6
5. 50,00000 19866,0
6. 70,00000 27237,0
No. X Y XY X2 Y2
1. 0,000000 213,092 0,000000 0,0000 45408,20046 2. 10,00000 4140,00 4140 100 17139600 3. 20,00000 8210,86 164217,2 400 67418221,94 4. 40,00000 16118,6 644744 1600 259809266 5. 50,00000 19866,0 993300 2500 394657956 6. 70,00000 27237,0 1906590 4900 741854169
∑ 190
X =31,6
75785,552
Y = 12630,92533 3750251,2 9500 1480924621
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =( )
Y = a X + b b = Y − aX
= 12630,92533 – (378,6679)(31,6) = 380,61969
Maka persamaan garis regresinya adalah: Y = 387,6679+ 380,61969
=
( )
( )
Lampiran 9. Data kalibrasi natrium dengan inductively coupled plasma, perhitungan persamaan garis regresi dan koefisien korelasi (r)
No. Konsentrasi (mg/l) (X)
Intensitas (I)
1. 0,000000 2804,21
2. 10,00000 36227,9
3. 20,00000 76068,5
4. 40,00000 141516
5. 50,00000 171934
6. 70,00000 241095
No. X Y XY X2 Y2
1. 0,000000 2804,21 0,000000 0,0000
7863593,724 2. 10,00000 36227,9 362279 100
1312460738 3. 20,00000 76068,5 1521370 400
5786416692 4. 40,00000 141516 5660640 1600
20026778256 5. 50,00000 171934 8596700 2500
29561300356 6. 70,00000 241095 16876650 4900
58126799025
∑ 190
X =31,6
669645,61
Y = 111607,6017 33017639 9500 114821618661
a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =( )
Y = a X + b b = Y − aX
= 111607,6017– (3391,0607)(31,6) = 4224,013636
Maka persamaan garis regresinya adalah: Y = 3391,0607+ 4224,013636
=
( )
( )
Lampiran 10. Hasil analisis kadar kobalt, molibdenum, kalium dan natrium pada kangkung
1. Hasil analisis kobalt
2. Hasil analisis molibdenum
3. Hasil analisis kalium No Sampel
Berat Sampel
(g)
Intensitas (I) Konsentrasi (µg/mL) Kadar (mg/100g) 1. 2. 3. 4. 5. 6. Kangkung 1 Kangkung 2 Kangkung 3 Kangkung 4 Kangkung 5 Kangkung 6 10,0507 10,0490 10,0620 10,0450 10,0586 10,0500 49,5290 49,1358 51,4377 50,3620 49,6356 51,1006 0,1668 0,1652 0,1742 0,1699 0,1671 0,1728 0,0829 0,0822 0,0865 0,8456 0,0831 0,0859
No Sampel
Berat Sampel
(g)
Intensitas (I) Konsentrasi (µg/mL) Kadar (mg/100g) 1. 2. 3. 4. 5. 6. Kangkung 1 Kangkung 2 Kangkung 3 Kangkung 4 Kangkung 5 Kangkung 6 10,0507 10,0490 10,0620 10,0450 10,0586 10,0500 188,130 160,716 190,400 176,228 183,521 186,214 0,1762 0,1490 0,1785 0,1644 0,1717 0,1743 0,0877 0,0741 0,0887 0,0818 0,0853 0,0867
No Sampel
Berat Sampel
(g)
4. Hasil analisis natrium
No Sampel
Berat Sampel
(g)
Intensitas (I) Konsentrasi (µg/mL)
Kadar (mg/100g) 1.
2. 3. 4. 5. 6.
Kangkung 1 Kangkung 2 Kangkung 3 Kangkung 4 Kangkung 5 Kangkung 6
7,0758 7,0740 7,0707 7,0620 7,0403 7,0420
64102,3 66311,0 65410,1 66022,0 64437,8 66518,6
17,6576 18,3090 18,0433 18,2237 17,7566
18,3702
Lampiran 11. Contoh perhitungan kadar kobalt, molibdenum, kalium dan natrium pada kangkung
1. Contoh perhitungan kadar kobalt
Berat sampel yang ditimbang = 10,0507 g Intensitas (I) = 49,5290
Persamaan Regresi: Y = 257,2723 X + 6,6242
X =
2723
,
257
6242
,
6
5290
,
49
−
= 0,16676Konsentrasi kobalt = 0,16676 µg/mL
(g) Sampel Berat n pengencera Faktor x (mL) Volume x g/mL) ( i Konsentras g/g) ( kobalt Kadar µ = µ = g mLx mLx g 0507 , 10 1 50 / 0,16676
µ
= 0,8295 µg/g = 0,08295 mg/100g
2. Contoh perhitungan kadar molibdenum Berat sampel yang ditimbang = 10,0507 Intensitas (I) = 188,130
Persamaan Regresi: Y = 1005,0121 X + 10,9494
X =
0121
,
1005
9494
,
10
130
,
188
−
= 0,1762(g) Sampel Berat n pengencera Faktor x (mL) Volume x g/mL) ( i Konsentras g/g) ( molibdenum
Kadar µ = µ
= g mLx mLx g 0507 , 10 1 50 / 0,1762
µ
= 0,8765 µg/g = 0,0877 mg/100g
3. Contoh perhitungan kadar kalium
Berat sampel yang ditimbang = 7,0758 g Intensitas (I) = 15336,3
Persamaan Regresi: Y = 387,6679 X + 380,61969
X =
6679
,
387
61969
,
380
3
,
15336
−
= 38,5786Konsentrasi kalium = 38,5786 µg/mL
(g) Sampel Berat n pengencera Faktor x (mL) Volume x g/mL) ( i Konsentras g/g) ( kalium Kadar µ = µ = g mLx mLx g 0758 , 7 5 50 / 38,5786
µ
4. Contoh Perhitungan Kadar Natrium Berat sampel yang ditimbang = 7,0758 Intensitas (I) = 64021,3
Persamaan Regresi: Y = 3391,0607 X + 4224,013636
X =
0607
,
3391
013636
,
4224
3
,
64102
−
= 17,6576
Konsentrasi natrium = 17,6576 µg/mL
(g) Sampel Berat
n pengencera Faktor
x (mL) Volume x
g/mL) (
i Konsentras
g/g) ( natrium
Kadar µ = µ
=
g
mLx
mLx
g
0758
,
7
2
50
/
17,6576
µ
Lampiran 12. Perhitungan statistik kadar kobalt pada kangkung
No. X
(Kadar mg/100g ) X - X (X - X)
2
1 0,08295 -0,001255 0,000001575
2 0,0822 -0,002015 0,00000406
3 0,08656 0,002295 0,000005267
4 0,08462 0,000355 0,000000126
5 0,08310 -0,001145 0,000001311
6 0,08597 0,001765 0,000003115
∑X = 0,50543
X = 0,084205 ∑(X - X)
2
= 0,000015
SD =
(
)
1 -n X -Xi 2
∑
= 1 6 0,000015 − = 0,001732Pada interval kepercayaan 99% dengan nilai α = 0.01 dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung< t tabel.
t hitung =
t hitung 1 =
6 / 001732 , 0 0,001255 = -1,7751
t hitung 2 =
6 / 001732 , 0 0,002015 = -2,8995
t hitung 3 =
t hitung 4 =
6 / 001732 ,
0
0.000355
= 0,5021
t hitung 5 =
6 / 001732 ,
0
0,001145
= -1,6195
t hitung 6 =
6 / 001732 ,
0
0,001765
= 2,4964
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar kobalt sebenarnya dalam kangkung : µ = X ± (t (α/2, dk) x SD / √n )
= 0,084205 ± (4,0321 x 0,001732/ 6) = (0,084205 ± 0,00285) mg/100g
Lampiran 13. Perhitungan statistik kadar molibdenum pada kangkung
No. X
(Kadar mg/100g )
X – X (X - X)2
1 0,08765 0,001604 0,000002572
2 0,07413 -0,011916 0,000142
3 0,08870 0,002654 0,000007044
4 0,08183 -0,004216 0,000018
5 0,08534 0,000706 0,0000004984
6 0,08671 0,000664 0,000000441
∑X = 0,5043
X = 0,086046 ∑(X - X)
2
= 0,00017056
SD =
(
)
1 -n X -Xi 2
∑
= 1 6 0,00017056 − = 0,0058Pada interval kepercayaan 99% dengan nilai α = 0.01 dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung< t tabel.
t hitung =
t hitung 1 =
6 / 0058 , 0 0,001604 = 0,6683
t hitung 2 =
6 / 0058 , 0 0,011916 = -4,965
t hitung 3 =
t hitung 4 =
6 / 0058 , 0
0,004216
= -1,7567
t hitung 5 =
6 / 0058 , 0
0,000706
= -0,2942
t hitung 6 =
6 / 0058 , 0
0,000664
= 0,2766
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar molibdenum sebenarnya dalam kangkung : µ = X ± (t (α/2, dk) x SD / √n )
= 0,086046 ± (4,0321 x 0,0058/ 6) = (0,086046 ± 0,0095) mg/100g Kadar molibdenum sebenarnya terletak antara
Lampiran 14. Perhitungan statistik kadar kalium pada kangkung
No. X
(Kadar mg/100g ) X – X (X - X)
2
1 136,30473 1,45443 2,1154
2 137,68235 2,83205 8,02051
3 137,04053 2,19023 4,7971
4 136,5711 1,7208 2,9612
5 131,3183 -3,532 12,475024
6 130,18496 -4,66534 21,7654
∑X = 809,10197
X = 134,8503 ∑(X - X)
2
= 52,134634
SD =
(
)
1 -n
X -Xi 2
∑
=
1 6
52,134634
−
= 3,2291
Pada interval kepercayaan 99% dengan nilai α = 0.01 dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung< t tabel.
t hitung = SD n
X Xi
/ −
t hitung 1 =
6 / 2291 , 3
1,45442 = 1,1033
t hitung 2 =
6 / 2291 , 3
t hitung 3 =
6 / 2291 , 3
2,19023 = 1,6614
t hitung 4 =
6 / 2291 , 3
1,7208 = 1,3053
t hitung 5 =
6 / 2291 , 3
3,532
- = -3,2013
t hitung 6 =
6 / 2291 , 3
4,66534
- = -3,5389
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar Kalium sebenarnya dalam kangkung : µ = X ± (t (α/2, dk) x SD / √n )
= 134,8503 ± (4,0321 x 3,2291/ 6) = (134,8503 ± 5,3155) mg/100g Kadar Kalium sebenarnya terletak antara
Lampiran 15. Perhitungan statistik kadar natrium pada kangkung
No. X
(Kadar mg/100g ) X - X (X - X)
2
1 24,9550 -0,6232 0,3884
2 25,88212 0,30392 0,0924
3 25,5184 -0,0598 0,0036
4 25,8054 0,2272 0,0516
5 25,22140 -0,3568 0,1273
6 26,08667 0,50847 0,2585
∑X = 153,46899
X = 25,5782 ∑(X - X)
2
= 0,9218
SD =
(
)
1 -n X -Xi 2
∑
= 1 6 0,9218 − = 0,4294Pada interval kepercayaan 99% dengan nilai α = 0.01 dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung< t tabel.
t hitung = SD n
X Xi
/ −
t hitung 1 =
6 / 4294 , 0 0,6232
- = -3,5551
t hitung 2 =
6 / 4294 , 0
t hitung 3 =
6 / 4294 , 0
0,0598
- = -0,3411
t hitung 4 =
6 / 4294 , 0
0,2272 = 1,2961
t hitung 5 =
6 / 4294 , 0
0,3568
- = -2,0354
t hitung 6 =
6 / 4294 , 0
0,50847 = 2,9005
Dari hasil perhitungan di atas didapat semua t hitung < t tabel, maka semua data tersebut diterima.
Kadar natrium sebenarnya dalam kangkung : µ = X ± (t (α/2, dk) x SD / √n )
= 25,5782 ± (4,0321 x 0,4294/ 6) = (25,5782 ± 0,7068) mg/100g Kadar natrium sebenarnya terletak antara
Lampiran 16. Hasil analisis kadar kobalt, molibdenum, kalium dan natrium sebelum penambahan masing-masing larutan baku pada kangkung 1. Hasil Analisis kadar kobalt (Co) sebelum ditambahkan larutan baku kobalt
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 10,0507 49,5290 0,1668 0,0829
2 10,0490 49,1358 0,1652 0,0822
3 10,0620 51,4377 0,1742 0,0865
4 10,0452 50,3620 0,1699 0,0846
5 10,0586 49,6356 0,1671 0,0831
6 10,0500 51,1006 0,1728 0,0859
∑ = 60,3155 0,5052
X = 10,0525 0,084205
2. Hasil analisis kadar molibdenum (Mo) sebelum ditambahkan larutan baku molibdenum
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 10,0507 188,130 0,1762 0,0877
2 10,0490 160,716 0,1490 0,0741
3 10,0620 190,400 0,1785 0,0887
4 10,0452 176,228 0,1644 0,0818
5 10,0586 183,521 0,1717 0,0853
6 10,0500 186,214 0,1743 0,0867
∑ = 60,3155 0,5163
3. Hasil analisis kadar kalium (K) sebelum ditambahkan larutan baku kalium
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 7,0758 15336,3 38,5786 136,3047
2 7,0740 15483,6 38,9586 137,6824
3 7,0707 15406,2 38,7589 137,0405
4 7,0620 15340,0 38,5882 136,6048
5 7,0403 14716,9 36,9808 131,3183
6 7,0420 14596,6 36,6705 130,1849
∑ = 42,3648 809,10197
X = 7,0608 134,8503
4. Hasil analisis kadar natrium (Na) sebelum ditambahkan larutan baku natrium
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 7,0758 64102,3 17,6576 24,9551
2 7,0740 66311,0 18,3090 25,8821
3 7,0707 65410,1 18,0433 25,5184
4 7,0620 66022,0 18,2237 25,8054
5 7,0403 64437,8 17,7566 25,2214
6 7,0420 66518,6 18,3702 26,0867
∑ = 42,3648 153,46899
Lampiran 17. Hasil analisis kadar kobalt, molibdenum, kalium dan natrium setelah penambahan masing-masing larutan baku pada kangkung 1. Hasil analisis kadar kobalt (Co) setelah ditambahkan larutan baku kobalt
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 10,0630 60,0159 0,2057 0,1031
2 10,0501 60,0063 0,2074 0,1032
3 10,0661 61,0068 0,2114 0,1050
4 10,0550 60,1596 0,2080 0,1035
5 10,0515 60,0968 0,2078 0,1033
6 10,0501 61,3501 0,2127 0,1057
∑ = 60,3469 0,6231
X
= 10,0578 0,103852. Hasil analisis kadar molibdenum (Mo) setelah ditambahkan larutan baku molibdenum
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 10,0630 224,218 0,2122 0,1054
2 10,0501 219,986 0,2079 0,1034
3 10,0661 223,160 0,2111 0,1078
4 10,0550 218,985 0,2069 0,1029
5 10,0515 222,069 0,2100 0,1044
6 10,0501 226,098 0,2140 0,1064
∑ = 60,3469 0,6318
3. Hasil analisis kadar kalium (K) setelah ditambahkan larutan baku kalium
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 7,0422 16663,6 42,0024 149,1096
2 7,0742 16678,7 42,0413 148,5726
3 7,0635 16670,1 42,0192 148,7194
4 7,0689 16676,5 42,0357 148,6641
5 7,0515 16668,3 42,0145 148,9559
6 7,0710 16680,1 42,0449 148,6526
∑ = 42,2532 892,6742
X
= 7,0619 148,77904. Hasil analisis kadar natrium (Na) setelah ditambahkan larutan baku natrium
Sampel Berat Sampel
(g) Intensitas (I)
Konsentrasi (µg/mL)
Kadar (mg/100g)
1 7,0422 71699,7 19,8981 28,2555
2 7,0742 72331,6 20,0844 28,3911
3 7,0635 72009,9 19,9895 28,2998
4 7,0689 72010,3 19,9897 28,2783
5 7,0515 71981,7 19,9812 28,3361
6 7,0710 72699,7 20,1927 28,5572
∑ = 42,2532 170,118
Lampiran 18. Contoh perhitungan uji perolehan kembali kadar kobalt, molibdenum, kalium dan natrium pada kangkung
1. Contoh perhitungan uji perolehan kembali kadar kobalt Persamaan regresi : Y = 257,2723 X + 6,6242
mL
g
X
0
,
2075
µ
/
2723
,
257
6242
,
6
0159
,
60
−
=
=
Konsentrasi setelah ditambahkan larutan baku = 0,2075µg/mL
CF =
volume
(mL)
x
Faktor
pengencera
n
sampel
Berat
)
/
i(µ
Konsentras
g
mL
×
1
x
50mL
10,0630
/
µ
2075
,
0
×
=
g
mL
= 1,0311 µg/g = 0,10311mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 0,10311 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 0,084205 mg/100g
Berat sampel rata-rata uji recovery = 10,0578 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
volume
(mL)
rata
-rata
sampel
Berat
n
ditambahka
yang
logam
i
Konsentras
×
= g mL g 0578 , 10 / µ 10x 0,2 mL
= 0,1988 µg/g = 0,01988 mg/100g
Maka % Perolehan Kembali Kobalt = CF−CA
=
100
%
01988
,
0
084205
,
0
0,10311
x
−
= 95,1224 %
2. Contoh perhitungan uji perolehan kembali kadar molibdenum Persamaan regresi : Y = 1005,0121 + 10,9494
mL
g
X
0
,
2122
µ
/
0121
,
1005
9494
,
10
218
,
224
=
−
=
Konsentrasi setelah ditambahkan larutan baku =
0
,
2122
µ
g
/
mL
CF =
volume
(mL)
x
Faktor
pengencera
n
sampel
Berat
)
/
i(µ
Konsentras
g
mL
×
1
x
50mL
10,0630
/
µ
2122
,
0
×
=
g
mL
= 0,1054 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 0,1054 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) =0,086046 mg/100g
Berat sampel rata-rata uji recovery = 10,0578 g Kadar larutan standar yang ditambahkan (C*A)
C*A = volume(mL)
rata -rata sampel Berat n ditambahka yang logam i Konsentras × = g mL g 0578 , 10 / µ 10
x 0,2 mL
Maka % Perolehan Kembali Molibdenum = CF−CA
C∗� � 100%
=
100
%
01988
,
0
086046
,
0
0,1054
x
−
= 97,5464 %
3. Contoh perhitungan uji perolehan kembali kadar kalium Persamaan regresi : Y = 387,6679 X + 380,61969
mL
g
X
42
,
0024
µ
/
6679
,
387
61969
,
380
6
,
16663
−
=
=
Konsentrasi setelah ditambahkan larutan baku =
42,0024
µ
g
/
mL
CF =
volume
(mL)
x
Faktor
pengencera
n
sampel
Berat
)
/
i(µ
Konsentras
g
mL
×
5
x
50ml
7,0442
/
µ
0024
,
42
×
=
g
mL
= 1491,096 µg/g = 149,1096 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 149,1096 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 134,8503 mg/100g
Berat sampel rata-rata uji recovery = 7,0619 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
volume
(mL)
rata
-rata
sampel
Berat
n
ditambahka
yang
logam
i
Konsentras
×
= g mL g 0619 , 7 / µ 1000x 1 mL
= 14,1605 mg/100g
Maka % Perolehan Kembali Kalium = CF−CA
C∗� � 100%
=
100
%
16049
,
14
8503
,
134
149,1096
x
−
= 100,6977 %
4. Perhitungan uji perolehan kembali kadar natrium Persamaan regresi : Y = 3391,0607 X + 4224,013636
mL
g
X
19
,
8981
µ
/
0607
,
3391
013636
,
4224
7
,
71699
−
=
=
Konsentrasi setelah ditambahkan larutan baku =
19
,
8981
µ
g
/
mL
CF =
volume
(mL)
x
Faktor
pengencera
n
sampel
Berat
)
/
i(µ
Konsentras
g
mL
×
2
x
50mL
7,0422
/
µ
8981
,
19
×
=
g
mL
= 282,555 µg/g = 28,2555 mg/100g
Kadar sampel setelah ditambah larutan baku (CF) = 28,2555 mg/100g
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 25,5782 mg/100g
Berat sampel rata-rata uji recovery = 7,0619 g Kadar larutan standar yang ditambahkan (C*A)
C*A =
volume
(mL)
= 28,3209µg/g = 2,83209 mg/100g
Maka % Perolehan Kembali Natrium = CFC−CA
∗� � 100%
=
100
%
83209
,
2
5782
,
25
28,2555
x
−
Lampiran 19. Perhitungan simpangan baku relatif (RSD) kadar kobalt, molibdenum, kalium dan natrium pada kangkung
1. Perhitungan simpangan baku relatif (RSD) kadar kobalt
No.
Kadar Persen Perolehan Kembali (mg/100 g)
( Xi )
(Xi - X ) %
(Xi - X )2 %
1. 95,1224 -4,3366 18,8060
2. 95,3907 -4,0683 16,5510
3. 104,6026 5,1436 26,4566
4. 97,1134 -2,3456 5,5018
5. 96,3216 -3,1374 9,8432
6. 108,2054 8,7464 76,4995
∑= 596,7545 153,6581
X = 99,4590 25,6096
SD =
(
)
1 -n
X -Xi 2
∑
=
1 6 153,6581
−
= 5,5436
RSD =
% 100
x x SD
=
100
%
99,4590
5,5436
x
2. Perhitungan simpangan baku relatif (RSD) kadar molibdenum
No.
Kadar Persen Perolehan Kembali (mg/100 g)
( Xi )
(Xi - X ) %
(Xi - X )2 %
1. 97,5464 4,2662 18,2005
2. 87,2937 -5,9865 35,8381
3. 94,7528 1,4726 2,1685
4. 85,1245 -8,1558 66,5170
5. 92,6199 -0,6603 0,4359
6. 102,3441 9,0639 82,1542
∑= 584,1202 205,3142
X = 97,3533 34,2190
SD =
(
)
1 -n
X -Xi 2
∑
=
1 6 205,3142
−
= 6,4080
RSD = x100%
x SD
=
100
%
97,3533
6,4080
x
= 6,5822% Keterangan:
SD = Standar Deviasi
3. Perhitungan simpangan baku relatif (RSD) kadar kalium
No.
Kadar Persen Perolehan Kembali (mg/100 g)
( Xi )
(Xi - X ) %
(Xi - X )2 %
1. 100,6977 2,318 5,373124
2. 96,9055 -1,4544 2,1153
3. 97,9417 -0,4182 0,17489
4. 97,5516 -0,8083 0,65335
5. 99,6123 1,2524 1,5685
6. 97,4704 -0,8895 0,79121
∑= 590,1594 10,6764
X = 98,3599 1,77994
SD =
(
)
1 -n
X -Xi 2
∑
=
1 6 10,6764
−
= 1,4613
RSD = x100%
x SD
=
100
%
98,3599
1,4613
x
= 1,4857 % Keterangan:
SD = Standar Deviasi
4. Perhitungan simpangan baku relatif (RSD) kadar natrium
No.
Kadar Persen Perolehan Kembali (mg/100 g)
( Xi )
(Xi - X ) %
(Xi - X )2 %
1. 94,5356 -2,4562 6,0329
2. 99,3245 2,3327 5,4414
3. 96,1008 -0,891 0,7939
4. 89,4171 -7,5747 57,3761
5. 97,3848 0,393 0,1545
6. 105,1884 8,1966 67,1843
∑= 581,9512 136,9831
X = 96,9918 22,8305
SD =
(
)
1 -n
X -Xi 2
∑
=
1 6 136,9831
−
= 5,2341
RSD = x100%
x SD
=
100
%
96,9918
5,2341
x
= 5,3965% Keterangan:
SD = Standar Deviasi
Lampiran 20. Perhitungan batas deteksi dan batas kuantitasi pada kangkung 1. Perhitungan batas deteksi dan batas kuantitasi kobalt
Y = 257,2723X + 6,6242 Slope = 257,2723
SY/x =
(
)
2
2
− −
∑
n Yi Y
= 6,9649
4 0448 , 194
=
Batas deteksi (LOD) =
slope xSY/x 3
=
2723 , 257
6,9649 3 x
= 0,08121 µg/mL
Batas kuantitasi (LOQ) =
slope xSY/x 10 No
Konsentrasi (µg/mL)
X
Intensitas
Y Yi Y-Yi (Y-Yi)
2
1 0,000000 2,60602 6,6242 -4,01818 16,1457 2 0,050000 16,0638 19,4878 -3,424 11,7238 3 0,100000 30,1177 32,3514 -2,2337 4,9894 4 0,500000 147,563 135,2603 12,3027 151,3564 5 1,000000 264,325 263,8965 0,4285 0,1836 6 2,000000 518,063 521,1688 -3,1058 9,6459
∑ 3,65
= 2723 , 257 6,9649 10x
= 0,2707 µg/mL
2. Perhitungan batas deteksi dan batas kuantitasi molibdenum
Y = 1005,0121X + 10,9494 Slope = 1005,0121
SY/x =
(
)
2 2 − −
∑
n Yi Y = 4 9941 , 601 = 12,2677Batas deteksi (LOD) =
slope xSY/x 3 = 0121 , 1005 2677 , 12 3x
= 0,0366 µg/mL No
Konsentrasi (µg/mL)
X
Intensitas
Y Yi Y-Yi (Y-Yi)
2
1 0,000000 5,56373 10,9494 -5,38567 29,0054 2 0,050000 56,7261 61,20 -4,4739 20,0158 3 0,100000 106,575 111,4506 -4,8756 23,7714 4 0,500000 519,565 513,45545 6,10955 37,3266 5 1,000000 1035,28 1015,9615 19,3185 373,2044 6 2,000000 2010,08 2020,9736 -10,8936 118,6705
∑ 3,65
Batas kuantitasi (LOQ) =
slope xSY/x 10
=
0121 , 1005
2677 , 12 10 x
= 0,1221 µg/mL
3. Perhitungan batas deteksi dan batas kuantitasi kalium
Y = 387,6679X + 380,61969 Slope = 387,6679
SY/x =
(
)
2
2
− −
∑
n Yi Y
=
4 4306 , 190228
= 218,0756
Batas deteksi (LOD) =
slope xSY/x 3
No
Konsentrasi (µg/mL)
X
Intensitas
Y Yi Y-Yi (Y-Yi)
2
1 0,000000 213,092 380,61969 -167,5277 28065,5261 2 10,00000 4140,00 4257,2987 -117,2987 13758,98502 3 20,00000 8210,86 8133,9777 76,8823 5910,8896 4 40,00000 16118,6 15887,3357 231,2643 53483,18108 5 50,00000 19866,0 19764,0147 101,9853 14010,0035 6 70,00000 27237,0 27517,3727 -280,3727 78608,8453
∑ 190
= 6679 , 387 218,0756 3x
= 1,6876 µg/mL
Batas kuantitasi (LOQ) =
slope xSY/x 10 = 6679 , 387 218,0756 10 x
= 5,6253 µg/mL
3. Perhitungan batas deteksi dan batas kuantitasi natrium
Y = 3391,0607X + 4224,013636 Slope = 3391,0607
SY/x =
(
)
2 2 − −
∑
n Yi Y = 4 95 , 24827342 = 2491,3522 No Konsentrasi (µg/mL) X IntensitasY Yi Y-Yi (Y-Yi)
2
1 0,000000 2804,21 4224,013636 -1419,804 2015842,365 2 10,00000 36227,9 38134,62064 -1906,72064 3635583,584 3 20,00000 76068,5 72045,228 4023,2724 16186720,51 4 40,00000 141516 139866,4416 1649,5584 2721042,796 5 50,00000 171934 173777,0486 -1843,0486 14880,41342 6 70,00000 241095 241598,2626 -503,2626 253273,2808
∑ 190
Batas deteksi (LOD) =
slope xSY/x 3
=
0607 , 3391
2491,3522 3x
= 2,2040 µg/mL
Batas kuantitasi (LOQ) =
slope xSY/x 10
=
0607 , 3391
2491,3522 10 x
Lampiran 21. Gambar alat yang digunakan
[image:45.595.207.412.113.344.2]Gambar 21.1. Varian 715 ES ICP OES
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT.Gramedia Pustaka Utama. Halaman 228, 230, 232.
Baliwati, F.Y., Khomsan, A., dan Dwiriani, M. (2006). Pengantar Pangan dan Gizi. Jakarta: Penebar Swadaya. Halaman 56.
Boss, C. B. and Freeden, K. J. 1997. Concepts, Intrumentation, and techniques in Inductively Coupled Plasma Optical Emision Spectrometry. USA: Perkin Elmer. Halaman 1 – 16.
Budiarto, E. (2004). Metodologi Penelitian Kedokteran. Jakarta: EGC. Halaman 46.
Edelson, M.C., dan Daniel, J.L. (1987). Plasma Spectroscopy for The Analysis of Hazardous Materials: Design and Application of Enclosed Plasma Sources. America: ASTM. Halaman 131.
Ermer, J. dan McB. Miller. J.H. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Halaman 253.
Gandjar, I.G., dan Rohman, A. (2012). Kimia Farmasi Analisis. Cetakan IX. Yogyakarta: Pustaka Pelajar. Halaman 33, 298, 305-312, 319.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 3(1): 119, 121 - 123, 129 - 131.
Issac, R.A. (1990). Metal in Plants. Dalam: Helrich, K. (1990). Official Methods of the Association of Official Analytical Chemists. Edisi XV. Virginia: AOAC International. Halaman 42.
Mangoting, D., Irawan,I., dan Abdullah S. (2005). Tanaman Lalap Berkhasiat Obat. Jakarta: Penebar Swadaya. Halaman 35.
Marzuki, I., Amirullah, S., dan Fitriana, S. (2010). Kimia Dalam Keperawatan.
Makasar: Pustaka As Salam. Halaman 15.
Novary, W.E. Penanganan dan Pengolahan Sayuran Segar. (1999). Jakarta: PT Penebar Swadaya. Halaman: 90.
Ramayulis, R. (2010). Menu dan Resep Untuk Penderita Hipertensi. Jakarta: Penebar Plus. Halaman 13.
Rukmana, R. (1994). Kangkung. Yogyakarta: Kanisius. Halaman 13, 21.
Smith, E.Y. (2002). Terapi Sayuran. Jakarta: Prestasi Pustaka. Halaman 123 – 125.
Soehardi, S. (2004). Memelihara Kesehatan Jasmani Melalui Makanan. Bandung: ITB. Halaman 111.
Sudjana. (2002). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Halaman 168, 226, 249.
Widowati, W., Sastiono, A., dan Jusuf, R. (2008). Efek Toksik Logam.
Yogyakarta: Andi. Halaman 165, 170 – 171, 258 – 259, 263.
Wirakusumah, E.S. (2000). Buah dan Sayuran Untuk Terapi. Bogor: Swadaya. Halaman 18.
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode deskriptif yang bertujuan untuk menggambarkan sifat dari suatu keadaan dalam hal ini menentukan kandungan logam kobalt, molibdenum, kalium dan natrium pada kangkung dataran tinggi.
3.1.Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Bidang Kimia Air Balai Laboratorium Kesehatan Dinas Kesehatan Propinsi Sumatera Utara pada bulan September – Desember 2014.
3.2.Bahan-bahan 3.2.1. Sampel
Sampel yang digunakan pada penelitian ini adalah kangkung yang ditanam di kawasan air panas Desa Semangat Gunung Kecamatan Merdeka, Daulu Kabupaten Karo, Provinsi Sumatera Utara.
3.2.2. Pereaksi
Bahan yang digunakan adalah asam nitrat 65% b/v, akua demineralisata, larutan baku kobalt 1000 µg/mL, larutan baku molibdenum 1000 µg/mL, larutan baku kalium 1000 µg/mL dan larutan baku natrium 1000 µg/mL.
3.3.Alat-alat
hot plate (FISONS), tanur (Naberthem) dan Inductively Coupled Plasma Optical Emission Spectrometry (Varian 715 ES).
3.4.Identifikasi Sampel
Identifikasi sampel dilakukan oleh bagian Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi-LIPI, Bogor.
3.5.Pembuatan Pereaksi 3.5.1.Larutan HNO3 (1:1)
Sebanyak 500 mL larutan HNO3 65% b/v diencerkan dengan 500 mL akua
demineralisata (Helrich, 1990).
3.6.Prosedur Penelitian 3.6.1.Pengambilan sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif
yang dikenal juga sebagai sampling pertimbangan. Metode sampling ini ditentukan atas dasar pertimbangan bahwa sampel yang diambil dapat mewakili populasi (Budiarto, 2004).
3.6.2.Penyiapan sampel
Kangkung sebanyak ± 1 kg dicuci bersih dengan air mengalir dan dibilas dengan akua demineralisata, kemudian ditiriskan sampai air cuciannya kering. Sampel dipotong-potong dan diblender sampai halus.
3.6.3.Proses destruksi kering
masing-temperatur dinaikkan hingga suhu 500ºC dengan interval 25ºC setiap 5 menit. Pengabuan dilakukan selama 48 jam (dihitung saat suhu sudah 500ºC), lalu setelah suhu tanur ± 27ºC, krus porselen dikeluarkan dan dibiarkan hingga dingin pada desikator. Abu ditambahkan 5 ml HNO3 (1:1), kemudian diuapkan pada hot
plate dengan suhu 100-120ºC sampai kering. Krus porselen dimasukkan kembali ke dalam tanur dengan temperatur awal 100ºC dan perlahan-lahan temperatur dinaikkan hingga 500ºC dengan interval 25ºC setiap 5 menit. Pengabuan dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator (Isaac, 1990). Bagan alir proses dekstruksi kering dapat dilihat pada Lampiran 3 dan Lampiran 4, halaman 36 dan 37.
3.6.4.Pembuatan larutan sampel
Hasil dekstruksi yang telah dingin dilarutkan dalam 5 ml HNO3 (1:1), lalu
3.7. Analisis Kuantitatif
3.7.1.Analisis kuantitatif kobalt, molibdenum, kalium dan natrium 3.7.1.1.Pembuatan larutan standar kobalt dan molibdenum
Larutan baku kobalt dan molibdenum (1000 µg/mL) masing-masing dipipet sebanyak 1 mL, dimasukkan ke dalam labu ukur 100 mL lalu dicukupkan hingga garis tanda dengan akua demineralisata (konsentrasi larutan baku 10 µg/mL).
3.7.1.2.Pembuatan kurva kalibrasi kobalt, molibdenum, kalium dan natrium Dibuat 5 deret larutan standar dari larutan baku kobalt dan molibdenum (10 µg/mL), kalium dan natrium (1000 µg/mL) yang terdiri atas: Deret I (0,05 µg/ml kobalt, 0,05 µg/mL molibdenum, 10 µg/mL kalium dan 10µg/mL natrium); deret II (0,1 µg/mL kobalt, 0,1 µg/mL molibdenum, 20 µg/mL kalium dan 20 µg/mL natrium); deret III (0,5 µg/mL kobalt, 0,5 µg/mL molibdenum, 40µg/mL kalium dan 40 µg/mL natrium); deret IV (1µg/mL kobalt, 1µg/mL molibdenum, 50 µg/mL kalium dan 50 µg/mL natrium); deret V (2 µg/mL kobalt, 2µg/mL molibdenum, 70 µg/mL kalium dan 70 µg/mL natrium) kelima deret larutan standar diukur pada panjang gelombang masing-masing yaitu 240,7 nm untuk kobalt, 313,3 nm untuk molibdenum, 766,5 nm untuk kalium, 589 nm untuk natrium.
3.7.1.3.Penetapan kadar kobalt, molibdenum, kalium dan natrium dalam sampel
intensitasnya dengan menggunakan ICP-OES pada panjang gelombang masing-masing yaitu 240,7 untuk kobalt, 313,3 untuk molibdenum, 766,5 nm untuk kalium dan 589 nm untuk natrium. Nilai intensitas yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium dan natrium. Konsentrasi kalium dan natrium dalam sampel dihitung berdasarkan persamaan garis regresi dari kurva kalibrasi.
Menurut Gandjar dan Rohman (2012), kadar logam kobalt, molibdenum, kalium dan natrium dalam sampel dapat dihitung dengan cara sebagai berikut :
Kadar logam (µg/g) =
(g) Sampel Berat
n pengencera Faktor
x (mL) Volume x
g/mL) (
i Konsentras µ
3.8.Analisis Data Secara Statistik 3.8.1.Penolakan hasil pengamatan
Kadar kobalt, molibdenum, kalium dan natrium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik. Menurut Harmita (2004), standar deviasi dapat dihitung dengan menggunakan rumus :
SD =
(
)
1 -n
X -Xi 2
∑
Keterangan : Xi = Kadar sampel
X = Kadar rata-rata sampel n = Jumlah perulangan
Untuk mengetahui data ditolak atau diterima dilakukan dengan uji T yang dapat dihitung dengan rumus:
t hitung =
n SD
X Xi
/
−
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t,
apabila thitung > ttabel maka data tersebut ditolak (Harmita, 2004).
Menurut Sudjana (2005), untuk menentukan kadar kobalt, molibdenum, kalium dan natrium di dalam sampel dengan tingkat kepercayaan 99%, α = 0,01, dk = n-1, dapat digunakan rumus:
Kadar mineral : µ = X ± (tα/2, dk) x SD / √n) Keterangan : X = Kadar rata-rata sampel
SD= Standar deviasi
dk = Derajat kebebasan (dk = n-1)
α = Interval kepercayaan
n = Jumlah perulangan 3.9.Validasi Metode Analisis
3.9.1.Uji perolehan kembali (Recovery)
Uji perolehan kembali (recovery) dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan baku dengan konsentrasi tertentu (Ermer dan Miller, 2005).
ditambahkan larutan baku kalium (konsentrasi 1000 µg/mL) 1 ml dan larutan baku natrium (konsentrasi 1000 µg/mL) 0,2 mL, kemudian dilanjutkan dengan prosedur dekstruksi kering seperti yang telah dilakukan sebelumnya. Prosedur pengukuran uji perolehan kembali dilakukan sama dengan prosedur penetapan kadar dalam sampel.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali =
A A F
C C C
*
− x 100%
Keterangan:
CA = Kadar logam dalam sampel sebelum penambahan baku
CF = Kadar logam dalam sampel setelah penambahan baku
C*A = Kadar larutan baku yang ditambahkan 3.9.2. Simpangan baku relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan (Harmita, 2004).
Menurut Harmita (2004), harga persentase koefisien variasi (% RSD) ditentukan dengan rumus sebagai berikut:
RSD = x100% x
SD
Keterangan:
X = Kadar rata-rata sampel SD = Standar Deviasi
3.9.3.Penentuan batas deteksi (limit of detection) dan batas kuantitasi (limit of
quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan baku
�
�� ��
=�
∑(�−��)2
�−2
Batas Deteksi (LOD) =
3����� �
�����
Batas Kuantitasi (LOQ) =
10 ����� �
BAB IV
HASIL DAN PEMBAHASAN
4.1.Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan di lakukan oleh Herbarium Bogoriense, Bidang Botani, Pusat Penelitian dan Pengembangan Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Bogor, Jalan Raya Jakarta – Bogor Km. 46 Cibinong. Hasil identifikasi Ipomoea aquatica Forssk, suku Convolvulaceae, dapat dilihat pada Lampiran 1, halaman 35.
4.2.Analisis Kuantitatif
4.2.1.Kurva kalibrasi kobalt, molibdenum, kalium dan natrium
Kurva kalibrasi kobalt, molibdenum, kalium dan natrium diperoleh dengan cara mengukur intensitas larutan baku pada panjang gelombang 240,7 nm; 313,3 nm; 766,5 nm; 589 nm. Hasil pengukuran kurva kalibrasi diperoleh persamaan garis regresi yaitu Y=257,2723X + 6,6242 untuk kobalt; Y=1005,0121X + 10,9494 untuk molibdenum; Y=387,6679X + 380,61969 untuk kalium dan Y=3391,0607X + 4224,0136 untuk natrium. Kurva kalibrasi larutan baku kobalt, molibdenum, kalum dan natrium dapat dilihat pada Gambar 4.1, Gambar 4.2, Gambar 4.3 dan Gambar 4.4.
Intensitas
[image:57.595.112.418.624.746.2]
Konsentrasi (ppm)
Intensitas
[image:58.595.114.416.87.215.2]Konsentrasi (ppm)
Gambar 4.2. Kalibrasi Molibdenum
Intensitas
Konsentrasi (ppm) Gambar 4.3. Kalibrasi Kalium
Intensitas
Konsentrasi (ppm) Gambar 4.4. Kalibrasi Natrium
2005). Data hasil pengukuran intensitas larutan baku kobalt, molibdenum, kalium dan natrium serta perhitungan persamaan garis regresi dapat dilihat pada Lampiran 6 sampai lampiran 9, halaman 40 sampai 46.
4.2.2. Pengukuran kadar kobalt, molibdenum, kalium dan natrium dalam sampel
Pada pengukuran kadar kobalt, molibdenum sampel dilakukan secara ICP-OES, terlebih dahulu dikondisikan alat dan diatur metodenya dengan baik dan benar, lalu kadar sampel diukur pada panjang gelombang masing-masing yaitu kobalt 240,7 nm dan molibdenum 313,3 nm. Pada pengukuran kadar kalium dan natrium dilakukan pengenceran terhadap larutan sampel. Pengenceran yang dilakukan yaitu sebesar 5 kali (50mL/10) untuk kalium, lalu kadar sampel diukur pada panjang gelombang yaitu 766,5 nm, dan pengenceran sebanyak 2 kali (50mL/25) untuk natrium, lalu kadar sampel diukur pada panjang gelombang yaitu 582 nm.
Dilakukan pengenceran terhadap sampel dikarenakan kadar mineral yang cukup tinggi untuk memperoleh nilai intensitas yang berada dalam rentang kalibrasi maka sampel harus diencerkan. Konsentrasi kobalt, molibdenum, kalium dan natrium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku kobalt, molibdenum, kalium dan natrium. Data dapat dilihat pada Lampiran 10, halaman 48 sampai 49 dan contoh perhitungan Lampiran 11, halaman 50 sampai 52.
Tabel 4.1 Hasil analisis kadar kobalt, molibdenum, kalium dan natrium dalam sampel
Hasil kadar kobalt, molibdenum, kalium dan natrium dapat dilihat pada Lampiran 10, halaman 48 sampai 49.
No Logam pada kangkung Kadar (mg/100g) 1 Kobalt 0,084205 ± 0,00285 2 Molibdenum 0,086046 ± 0,0095 3 Kalium 134,8503 ± 5,3155 4 Natrium 25,5782 ± 0,7068
Dari hasil analisis kuantitatif kobalt, molibdenum, kalium dan natrium sesuai yang tercantum pada Tabel 4.1, dapat dilihat bahwa kobalt yaitu 0,084205 ± 0,00285 mg/100g, kadar molibdenum yaitu 0,086046 ± 0,0095 mg/100g, kadar kalium yaitu 134,8503 ± 5,3155 mg/100g dan natrium 25,5782 ± 0,7068 mg/100g. Kadar Kalium dan Natrium yang diperoleh lebih kecil dari kadar yang bersumber dari Direktorat Gizi Depkes R.I., (1981) yaitu Kalium 458,00 mg/100g dan Natrium 49,00 mg/100g. Kadar logam kobalt dan molibdenum tidak dicantumkan. Kadar yang berbeda ini dapat disebabkan oleh tempat tumbuh yang berbeda, jenis tanah yang berbeda dan kandungan logam dalam tanah yang berbeda sehingga kadarnya juga berbeda didalam tanaman.
4.3.Validasi Metode
4.3.1. Uji perolehan kembali (Recovery)
(recovery) sebelum dan setelah penambahan masing-masing larutan baku dapat dilihat pada Lampiran 16 dan 17, halaman 61 sampai 64.
[image:61.595.122.515.235.327.2]Persen perolehan kembali (recovery) kadar mineral kobalt, molibdenum, kalium dan natrium dalam sampel dapat dilihat pada Tabel 4.2.
Tabel 4.2 Persen uji perolehan kembali (Recovery) kobalt, molibdenum, kalium dan natrium dalam sampel
No. Mineral Persen perolehan kembali (%)
Syarat rentang persen recovery (%)
1. Kobalt 99,4590
80 – 120
2. Molibdenum 97,3533
3 Kalium 98,3599
4 Natrium 96,9918
Berdasarkan Tabel 4.2 di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) kobalt adalah 99,4590%, molibdenum adalah 97,3533%, kalium adalah 98,3599% dan natrium adalah 96,9918%. Persen perolehan kembali (recovery) tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kobalt, molibdenum, kalium dan natrium dalam sampel. Hasil yang diperoleh dari uji perolehan kembali memberikan ketepatan pada pemeriksaan kadar mineral dalam sampel. Menurut Ermer dan Miller (2005), suatu metode dikatakan teliti jika nilai perolehan kembalinya antara 80-120%.
4.3.2.Simpangan baku relatif
Tabel 4.3 Nilai simpangan baku dan simpangan baku relatif kobalt, molibdenum, kalium dan natrium dalam sampel
No. Mineral Simpangan Baku Simpangan Baku Relatif
1. Kobalt 5,5436 5,5737
2. Molibdenum 6,4080 6,5822
3 Kalium 1,4613 1,4857
4 Natrium 5,2341 5,3965
Berdasarkan Tabel 4.3 di atas, dapat dilihat nilai simpangan baku (SD) mineral kobalt 5,5436 ; molibdenum 2,6160 ; kalium 1,4613 dan natrium 5,2341. Dan nilai simpangan baku relatif (RSD) yang diperoleh kobalt 5,5737% ; molibdenum 2,8045% ; kalium 1,4857% dan natrium 5,3965%. Menurut Harmita (2004), nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per billion (ppb) RSD nya adalah tidak lebih dari 32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki ketelitian yang baik.
4.3.3.Batas deteksi dan batas kuantitasi
[image:62.595.120.515.125.222.2]Berdasarkan data kurva kalibrasi kobalt, molibdenum, kalium dan natrium diperoleh batas deteksi dan batas kuantitasi untuk keempat mineral tersebut. Batas deteksi dan batas kuantitasi kobalt, molibdenum, kalium dan natrium dapat dilihat pada Tabel 4.4.
Tabel 4.4 Batas deteksi dan batas kuantitasi kobalt, molibdenum, kalium dan natrium
No. Mineral Batas Deteksi (µg/mL) Batas Kuantitasi (µg/mL)
1. Kobalt 0,08121 0,2707
2. Molibdenum 0,0366 0,1221
3. Kalium 1,6876 5,6253
[image:62.595.110.511.615.695.2]Dari hasil perhitungan diperoleh batas deteksi untuk pengukuran kobalt 0,08121μg/mL, molibdenum 0,0366μg/mL, kalium 1,6876μg/mL dan natrium 2,2040μg/mL, sedangkan batas kuantitasinya kobalt 0,2707μg/mL, molibdenum 0,1221μg/mL, kalium 5,6253 μg/mL dan natrium 7,3468μg/mL.
BAB V
KESIMPULAN DAN SARAN
5.1.Kesimpulan
a. Berdasarkan hasil pemeriksaan kobalt, molibdenum, kalium dan natrium secara Inductively Coupled Plasma Optical Emission Spectrometry
menunjukkan bahwa kobalt, molibdenum, kalium dan natrium dapat diukur intensitasnya pada panjang gelombang 240,7 nm untuk kobalt, 313,3 nm untuk molibdenum, 766,5 nm dan 589 nm untuk kalium.
b. Hasil penetapan kadar kobalt, molibdenum, kalium dan natrium secara
Inductively Coupled Plasma Optical Emission Spectrometry pada kangkung memiliki kadar kobalt (0,084205 ± 0,00285 mg/100g); kadar molibdenum (0,086046 ± 0,0095 mg/100g); kadar kalium (134,8503 ± 5,3155 mg/100g) dan kadar natrium (25,5782 ± 0,7068 mg/100g).
5.2.Saran
BAB II
TINJAUAN PUSTAKA
2.1.Uraian Sampel 2.1.1. Kangkung
Kangkung merupakan tanaman menetap yang dapat tumbuh lebih dari satu tahun. Tanaman kangkung tidak memerlukan persyaratan tempat tumbuh yang sulit. Salah satu syarat yang penting adalah air yang cukup. Apabila kekurangan air pertumbuhannya akan mengalami hambatan (Rukmana, 1995).
Menurut Rukmana (1994) Kangkung termasuk dalam famili Convolvulaceae. Berikut adalah klasifikasi kangkung air dalam taksonomi tumbuhan
Divisio : Spermatophyta Sub-divisio : Angiospermae Kelas : Dicotyledoneae Ordo : Solanales Famili : Convolvulaceae Genus : Ipomoea
Spesies : Ipomoea aquatica Forssk.
Nama Sinonim : Ipomoea repens Roth, Convolvulus repens Vahl Nama Asing : Kangkong, water cabbage, swamp cabbage, water
Nama Daerah : Rumpun (Aceh); kalayau, lalidik (Sumatera);
pangpung, angodono (Nusa Tenggara); lara (Bima); kangko, tatanggo tango (Sulawesi); kanto (Gorontalo); namiri (Makasar); lare (Bugis); utangko, beehob, takako, kangko (Tidore); kako (Halmahera); ktangko (Pulau Buru) (Mangoting, dkk., 1999).
2.1.2. Habitat
Tanaman kangkung belum diketahui asal usulnya akan tetapi banyak dijumpai didaratan Asia, kangkung tumbuh liar, tumbuh tegak merambat atau tegak dengan batang berair dan menyukai tempat yang berair. Kangkung merupakan tanaman yang berbentuk rumput mempunyai batang yang beruas, berbentuk bulat dan berongga serta bersifat menjalar dan terapung dalam air. Daunnya berupa daun tunggal dengan tangkai panjang yang tumbuh berseling (Smith, 2002).
2.1.3. Varietas dan jenis tanaman
Tanaman kangkung ditinjau dari tempat tumbuhnya terdiri dari: a. Kangkung darat.
Tumbuh didaratan kering dan dapat dijumpai diladang, berdaun panjang dengan ujung runcing berwarna hijau muda atau pucat keputih putihan dan berukuran lebih kecil dan sempit dengan bunga berwarna putih. Perbanyakan biasanya dengan biji.
panjang dengan ujung agak tumpul, berwarna hijau tua segar atau hijau gelap dengan bunga berwarna ungu atau kekuning kuningan. Tangkai daun kangkung air ini lebih panjang dan lebar dibandingkan dengan kangkung darat. Batangnya besar berongga dengan warna keunguan. Perbanyakannya biasanya dari setek batangnya yang agak tua (Smith, 2002).
2.1.4. Kandungan gizi kangkung
Kangkung merupakan salah satu jenis sayuran yang kaya gizi. Sayuran ini merupakan sumber vitamin A, vitamin C dan mineral. Sayuran ini mengandung 29 kalori dalam setiap 100 g (Novary, 1999). Kandungan gizi dalam sayuran kangkung dapat dilihat pada Tabel 2.1.
Tabe 2.1. Kandungan gizi tiap 100 gram sayuran kangkung segar. Komposisi Gizi Banyaknya Kandungan Gizi Kalori
Protein Lemak Karbohidrat Serat Kalsium Fosfor Zat besi Natrium Kalium Vitamin A Vitamin B1
Vitamin B2
Vitamin C Niacin
30,00 kal 3,90 gr 0,60 gr 4,40 gr 1,40 gr 71,00 gr 67,00 mg 3,20 mg 49,00 mg 458,00 mg 4825,00 S.I 0,09 mg 0,24 mg 59,00 mg 1,30 mg Sumber: Direktorat Gizi Depkes R.I. (1981). 2.2.Mineral
mineral mikro dalam tubuh kurang dari 15 mg (Almatsier, 2004). Unsur-unsur mineral makro adalah kalsium, fosfor, kalium, sulfur, natrium, klorida, magnesium. Unsur-unsur mineral mikro adalah besi, seng, selenium, mangan, tembaga, iodium, molibdenum, kobalt, kromium, silikon, vanadium, nikel, arsen, dan fluor (Baliwati, dkk., 2006).
2.2.1. Kobalt
Fungsi biologis kobalt satu-satunya yang diketahui adalah sebagai konstituen dalam vitamin B12 yang dibutuhkan untuk pematangan eritrosit (sel
darah merah) (Marzuki, dkk., 2010). Dalam jumlah sangat kecil, kobalt merupakan unsur yang esensial bagi kesehatan tubuh. Kobalt tidak berbahaya bagi kesehatan manusia bila dikonsumsi dalam dosis rendah. Kobalt yang dikonsumsi dalam dosis besar akan berbahaya bagi kesehatan, terutama pada organ paru-paru dan jantung (Widowati, dkk., 2008).
2.2.2. Molibdenum
Molibdenum bekerja sebagai kofaktor berbagai enzim, degradasi, pembentukan asam urat, membantu metabolisme lemak dan karbohidrat. Gejala kelebihan molibdenum adalah tubuh terasa lemah, bintik merah pada kulit, menurunnya sel darah putih dan anemia (Widowati, dkk., 2008).
2.2.3. Kalium
Kekurangan kalium dapat terjadi karena kebanyakan kehilangan melalui saluran cerna atau ginjal. Kehilangan banyak melalui saluran cerna dapat terjadi karena muntah–muntah, diare kronis atau kebanyakan menggunakan laksan (obat pencuci perut). Kebanyakan kehilangan melalui ginjal adalah karena penggunaan obat–obat diuretik terutama untuk pengobatan hipertensi (Almatsier, 2004). 2.2.4. Natrium
Di dalam tubuh manusia, natrium terutama terdapat dalam plasma darah. Mineral natrium termasuk dalam kelompok zat gizi (nutrisi) pelindung kesehatan tubuh yang diperlukan agar tubuh tetap bugar. Ion natrium amat penting untuk memelihara tekanan osmotik yang normal dari cairan tubuh dan mengatur keseimbangan asam basa dari tubuh (Soehardi, 2004).
Kekurangan natrium dapat menyebabkan kejang, apatis dan kehilangan nafsu makan. Kekurangan natrium dapat terjadi sesudah muntah, diare dan keringat berlebihan (Almatsier, 2004).
2.3. Inductively Coupled Plasma Optical Emission Spectrometry. 2.3.1. Definisi umum
Inductively Coupled Plasma Optical Emission Spectrometry merupakan alat untuk analisa unsur-unsur logam dalam suatu bahan. Bahan yang akan dianalisa harus berwujudlarutan yang homogen (Nugroho, dkk., 2007).
2.3.2.Prinsip umum
sampel kebentuk aerosol yang kemudian diinjeksikan ke ICP. Pada temperatur plasma sampel-sampel akan teratomisasi dan tereksitasi. Atom yang tereksitasi akan kembali ke keadaan awal (ground state) sambil memancarkan sinar radiasi. Sinar radiasi ini didispersi oleh komponen optik. Sinar yang terdispersi, secara berurutan muncul pada masing-masing panjang gelombang unsur dan dirubah dalam bentuk sinyal listrik yang besarnya sebanding dengan sinar yang dipancarkan oleh besarnya konsentrasi unsur. Sinyal listrik ini kemudian diproses oleh sistem pengolah data (Nugroho, dkk., 2007).
2.3.3. Instrumentasi ICP-OES
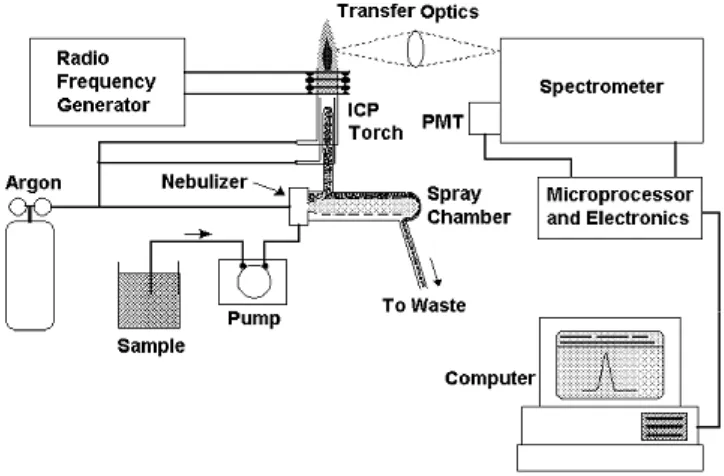
[image:70.595.143.505.382.620.2]Representasi dan tampilan dari ICP-OES dapat dilihat dari gambar berikut:
Gambar 2.1. Komponen utama dan susunan dari peralatan Inductively
2.3.3.1.Pemasukan Sampel a. Nebulizer
Nebulizer adalah perangkat yang digunakan untuk mengkonversi cairan menjadi aerosol yang kemudian dialirkan ke plasma. Proses nebulisasi adalah salah satu langkah yang penting dalam ICP. Cara memperkenalkan sampel yang ideal akan menjadi salah satu penghantar dari semua sampel keplasma pada satu bentuk dimana plasma mungkin akan kembali menghasilkan larutan, uap atomisasi, dan ionisasi.
b.Pompa
Pompa adalah perangkat yang digunakan untuk mengalirkan sampel larutan kedalam nebulizer. Pompa ini menggunakan sebuah penggulungan yang mendorong larutan sampel dimana tabung menggunakan proses peristaltik. c. Spray chamber (tempat penyemprot)
Sampel aerosol terdapat pada nebulizer segera dialirkan pada torch sehingga dapat diinjeksikan ke dalam plasma, karena hanya tetesan kecil aerosol cocok untuk diinjeksikan ke dalam plasma, spray chamber ditempatkan antara nebulizer dan torch yang fungsinya untuk menghilangkan tetesan besar dari aerosol.
d. Drains
2.3.3.2.Penghasil emisi a. Torches
Dari spray chamber aerosol diinjeksikan melalui torch kedalam plasma yang akan terdesolvasi, menguap, teratomisasi, tereksitasi dan terionisasi oleh plasma. Torch terdiri dari tiga tabung konsentrik, untuk aliran argon dan injeksi aerosol. Tiga tabung itu terdiri dari plasma flow, auxiliary flow dan nebulizer flow.
b. Radio frequency generator
Alat yang menyediakan tegangan (700 - 1500 watt) untuk menyalakan plasma dengan argon sebagai sumber gas. Tegangan ini ditransferkan ke plasma. Kumparan, yang bertindak sebagai antena untuk mentransfer daya RF untuk plasma, biasanya terbuat dari pipa tembaga dan didinginkan oleh air atau gas selama operasi.
2.3.3.3.Pengumpulan dan pendeteksian emisi a. Optik
Radiasi biasanya dikumpulkan oleh fokus optik seperti lensa cembung atau cermin cekung. Optik ini bersifat mengumpulkan sinar, sehingga sinar difokuskan menuju celah pada monokromator atau polikromator.
b. Monokromator
beberapa panjang gelombang yang berbeda. Untuk menganalisa multi unsur secara simultan dapat digunakan polikromator.
c. Detektor
Detektor digunakan untuk mengukur intensitas garis emisi setelah garis emisi dipisahkan oleh monokromato/ polikromator. Jenis detector yang paling banyak digunakan pada ICP-OES adalah tabung photomultiplier (PMT).
2.3.3.4.Pemrosesan sinyal dan instrumen kontrol a. Pemrosesan sinyal
Emisi yang telah dideteksi oleh detector (PMT), arus anoda PMT itu dapat dikonversi, yang mewakili intensitas emisi menjadi sinyal tegangan yang diubah menjadi informasi digital. Informasi digital yang mewakili intensitas emisi relative atau konsentrasi dari sampel
b. Komputer dan processor
Komputer digunakan sebagai instrument untuk mengontrol, memanipulasi dan mengumpulkan data analisis. Kemampuan untuk melihat data spectral pengukuran dengan waktu analisis yang sangat cepat merupakan tujuan utama penggunaan computer dalam setiap instrumentasi (Boss and Freeden, 1997).
2.4. Validasi Metode Analisis
a. Kecermatan
Kecermatan merupakan ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan 2 cara, yaitu :
- Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu bahan pembawa sediaan farmasi (plasebo), campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya) (Harmita, 2004).
- Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah baku dengan konsentrasi tertentu pada sampel yang diperiksa dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah baku. Persen perolehan kembali ditentukan dengan menentukan berapa persen baku yang ditambahkan ke dalam sampel dapat ditemukan kembali (Harmita, 2004).
b. Keseksamaan (presisi)
c. Selektivitas (spesifitas)
Selektivitas atau spesifitas suatu metode merupakan kemampuan yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik secara langsung maupun dengan bantuan transformasi matematika, menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima (Harmita, 2004).
e. Batas deteksi (Limit of detection) dan batas kuantitasi (Limit of quantitation) Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
f. Ketangguhan metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda. Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja terhadap hasil uji (Harmita, 2004).
g. Kekuatan (Robustness)
BAB I PENDAHULUAN
1.1.Latar Belakang
Kangkung merupakan tanaman sayuran komersial dan sangat populer. Daunnya digemari seluruh lapisan masyarakat di Indonesia karena rasanya enak dan segar. Kangkung banyak mengandung vitamin A, vitamin C dan mineral. Sayuran ini berfungsi sebagai penenang (sedatif) atau berkhasiat sebagai obat tidur (Aksara, 2013). Di beberapa negara di Asia Tenggara, kangkung dikenal sebagai obat tradisional untuk mencegah beberapa penyakit, seperti menurunkan tekanan darah tinggi, menurunkan kadar kolesterol, mencegah diabetes melitus, mengatasi anemia dan sebagai anti kanker (Yuliarti, 2009). Kangkung dapat tumbuh dengan baik di dataran rendah sampai dataran tinggi (pegunungan) ± 2000 m dari permukaan laut dan diutamakan lokasi lahannya terbuka atau mendapat sinar matahari yang cukup (Rukmana, 1995).
Mineral adalah bagian dari tubuh yang memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan, di samping itu, mineral berperan dalam berbagai tahap metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim (Almatsier, 2004).
Kalium merupakan kation penting di dalam cairan intraselular. Kecukupan asupan kalium dapat memelihara tekanan darah dan membuat perubahan positif pada tekanan darah penderita hipertensi (Ramayulis, 2010). Natrium adalah kation utama dalam cairan ekstraseluler. Kelebihan natrium dapat menimbulkan keracunan yang dalam keadaan akut menyebabkan edema dan hipertensi. Secara normal tubuh dapat menjaga keseimbangan antara natrium di luar sel dan kalium di dalam sel (Almatsier, 2004).
Mineral Kobalt dan molibdenum bersumber dari tanah, debu, lava gunung berapi, kebakaran hutan dan asap kendaraan bermotor (Widowati, dkk., 2008).