PENETAPAN KADAR NITROGEN YANG TERKANDUNG
DALAM PUPUK NITROGEN, FOSFOR, KALIUM (NPK)
DI PT. RISPA MEDAN
KARYA ILMIAH
062401019
WIDIYANDARI
PROGRAM STUDI DIPLOMA-3 KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
Judul : PENETAPAN KADAR NITROGEN YANG
TERKANDUNG DALAM PUPUK NITROGEN, FOSFOR, KALIUM ( NPK) Di P.T. RISPA MEDAN
Kategori : Karya Ilmiah Nama : Widiyandari
NIM : 062401019
Program Studi : Kimia Analis Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di : Medan, Juni 2009
Diketahui/Disetujui Oleh
Departemen Kimia FMIPA USU Komisi Pembimbing
Ketua, Pembimbing,
Dr.Rumondang Bulan,M.S.
NIP. 131 459 466 NIP. 131 273 465
PERNYATAAN
PENETAPAN KADAR NITROGEN YANG TERKANDUNG DALAM PUPUK NITROGEN, FOSFOR, KALIUM ( NPK) Di P.T. RISPA MEDAN
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2009
PENGHARGAAN
Puji syukur penulis panjatkan kepada Allah SWT yang telah melimpahkan rahmat, taufik dan hidayah-Nya sehingga penulis dapat menyelesaikan penulisan Karya Ilmiah ini. Karya ilmiah yang penulis sajikan berjudul “ PENETAPAN KADAR NITROGEN YANG TERKANDUNG DALAM PUPUK NPK di P.T.RISPA MEDAN”.Karya ilmiah ini disusun untuk melengkapi dan sebagai salah satu syarat untuk menyelesaikan Program Diploma-3 Kimia Analis Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Selesainya Karya Ilmiah ini juga tidak lepas dari bimbingan dan bantuan dari berbagai pihak. Oleh karena itu, dengan kerendahan dan ketulusan hati; penulis ingin menyampaikan rasa terima kasih kepada :
1. Bapak Prof.Dr.Zul Alfian,M.Sc, selaku dosen pembimbing yang telah memberikan bimbingan dan pengarahan kepada penulis.
2. Ibu Dr.Rumondang Bulan,M.S., selaku Ketua Departemen Kimia FMIPA USU,Drs.Firman Sebayang,M.Sc, selaku Sekretaris Departemen Kimia FMIPA USU. 3. Ibu Dr.Marpongahtun, selaku Penasehat Akademik beserta seluruh Staff Dosen dan Staff Administrasi Departemen Kimia FMIPA USU Medan yang telah mendidik, membimbing dan membantu penulis selama menjalani masa perkuliahan di Departemen Kimia FMIPA USU.
5. Ayahanda Ir.Hidayat dan Ibunda Suriyani, serta abang yang telah memberikan bantuan moril dan materil serta do’a kepada penulis.
6. Kepada Kakanda Syaiful Bahri Napitupulu.Amd, yang telah memberi saran,motivasi serta doanya selama proses perkuliahan hingga selesainya tugas akhir ini.
7. Untuk teman-teman Nine Balls ( ayu, inggit, isma, kiki, lia, mazda, rina, sherly) serta semua teman-teman Kimia Analis yang telah memberikan semngat serta doa.
Atas bantuan dan dukungan tersebut penulis tidak dapat membalasnya, hanya memohon pada Allah SWT agar mereka memperoleh rahmat dan hidayah serta balasan yang lebih baik dari-Nya.
Penulis menyadari bahwa dalam penulisan Karya Ilmiah ini belum sempurna, oleh karena itu dengan kerendahan hati penulis menerima segala saran dan kritiknya yang bersifat membangun demi kesempurnaan Karya Ilmiah ini.
Akhirnya, penulis berharap semoga Karya Ilmiah ini dapat bermnfaat bagi kita semua.
Medan, Juni 2009
THE VALUE DETERMINATION OF NITROGEN WHICH INCLUDE NITROGEN, PHOSPHOR,CALIUM ( NPK ) MANURE IN P.T.RISPA MEDAN
ABSTRACT
ABSTRAK
DAFTAR ISI
PERSETUJUAN ... i
PERNYATAAN ... ii
PERNGHARGAAN ... iii
ABSTRAK ... iv
ABSTRACT ... v
DAFTAR ISI ... vi
BAB I. PENDAHULUAN ... 1
1.1 Latar belakang ... 2
1.2 Identifikasi Permasalahan ... 2
1.3 Tujuan ... 2
1.4 Manfaat ... 2
BAB II. TINJAUAN PUSTAKA ... 3
2.1 Pupuk ... 3
2.2 Penggolongan Pupuk ... 4
2.3 Jenis – Jenis Pupuk ... 5
2.4 Pupuk NPK ... 6
2.5 Nitrogen ... 8
2.6 Metode Analisa Kjedhal ... 8
BAB III. METODOLOGI PERCOBAAN ... 11
3.1 Penentuan Kadar Nitrogen Dari Pupuk NPK ... 11
3.2 Alat – Alat ... 11
3.3 Bahan-Bahan ... 11
BAB IV HASIL DAN PEMBAHASAN ... 14
4.1 Data Analisis ... 14
4.2 Perhitungan ... 14
4.3 Pembahasan ... 16
BAB V. KESIMPULAN DAN SARAN ... 18
5.1 Kesimpulan ... 18
5.2 Saran ... 18
DAFTAR PUSTAKA ... 19
THE VALUE DETERMINATION OF NITROGEN WHICH INCLUDE NITROGEN, PHOSPHOR,CALIUM ( NPK ) MANURE IN P.T.RISPA MEDAN
ABSTRACT
ABSTRAK
BAB I PENDAHULUAN
1.1 Latar Belakang
Tanah idealnya dapat menyediakan sejumlah unsur hara penting yang dibutuhkan oleh tanaman. Penyerapan unsur hara oleh tanaman semestinya dapat segera diperbaharui sehingga kandungan unsur hara di dalam tanah tetap seimbang. Hutan adalah contoh ekosistem yang seimbang, pengambilan unsur hara oleh ribuan jenis tumbuhan diimbangi dengan pelapukan bahan organik yang menyuplai hara bagi tanah. Proses inilah yang menyebabkan tanah yang di hutan tetap subur.
Mengingat pentingnya unsur hara nitrogen pada tanaman, maka karya ilmiah ini mencoba menjelaskan berapa besar kandungan nitrogen yang terdapat pada pupuk NPK. 1.2 Pemasalahan
Kadar nitrogen pada pupuk NPK sebesar minimum 6 %. Tanah yang kekurangan nitrogen menyebabkan tanaman tumbuh kurus dan kerdil. Daun menjadi hijau muda, terutama daun yang sudah tua, lalu berubah menjadi kuning. Selanjutnya daun mengering mulai dari bawah ke bagian atas. Jaringan – jaringannya mati, mengering, lalau meranggas. Bila pada tanah tersebut tidak diberi pupuk yang mengandung unsur nitrogen maka selamanya tanaman akan tumbuh seperti yang telah dijelaskan.
Namun yang menjadi permasalahn apabila kadar nitrogen pada pupuk NPK tidak sesuai dengan spesifikasi mutu pupuk NPK yang telah ditetapkan.
1.3 Tujuan
Untuk mengetahui kadar nitrogen yang terdapat pada beberapa sampel pupuk NPK apakah sesuai dengan baku mutu pupuk NPK yang telah ditetapkan oleh SNI 2-2803-2000.
1.4 Manfaat
BAB II
TINJAUAN PUSTAKA
2.1 Pupuk
Pupuk didefinisikan sebagai material yang ditambahkan ke tanah dengan tujuan untuk melengkapi ketersediaan unsur hara. Bahan pupuk yang paling awal digunakan adalah kotoran hewan, sisa pelapukan tanaman, dan arang kayu. Pemakaian pupuk kimia kemudian berkembang seiring dengan ditemukannya deposit garam kalsium di Jerman pada tahun 1839, Pengetahuan awal tentang unsur hara dan unsur kimia dalam pertanian moderen ditemukan pada tahun 1840 oleh Justus Von Leibig seorang ahli kimia berkebangsaan Jerman. Ia memberi bukti yang membantah teori humus sebagai unsur hara. Menurut Leibig, tanaman memperoleh zat karbon dari udara dan beberapa unsur mineral (kalium, kalsium, sulfur, dan phosphor) dari dalam tanah. Setelah penemuan Leibig, studi mengenai unsur hara mengalami kemajuan pesat diakhir abad ke-19, yang diikuti perkembangan industri pupuk. Tahu 1842 dimulai pembuatan pupuk superphosphat. Kemudian tahun 1884 berkembang teori-teori dasar untuk pembuatan pupuk amonia melalui penggabungan hidrogen dan nitrogen dari udara.
hara. Saat ini unsur hara dapat disediakan oleh berbagai macam pupuk yang tersedia di pasaran.(2)
2.2 Penggolongan pupuk
Berdasarkan cara pemberiannya, pupuk digolongkan menjadi pupuk akar karena jenis pupuk ini lebih tepat sasaran bila diberikan lewat akar atau tanah. Selain itu, juga ada yang digolongkan sebagai pupuk daun yaitu pupuk yang dapat diberikan melalui daun dengan cara disemprotkan.
Pupuk akar merupakan pupuk yang pertama dikenal manusia, sedangkan pupuk daun baru dikembangkan setelah manusia mengenal penyerapan unsur hara lewat mulut daun (stomata). Pemberian pupuk lewat akar sebenarnya relatif aman jika dibandingkan dengan pemberian lewat daun, tetapi efisiensinya relatif rendah.
2.3. Jenis-jenis pupuk a. Pupuk Sumber Nitrogen
− Amonium Nitrat
Kandungan nitratnya membuat pupuk ini cocok untuk daerah dingin dan daerah panas. Amonium nitrat bersifat higroskopis sehingga tidak dapat disimpan terlalu lama.
− Amonium Sulfat (NH4)2SO4
Pupuk ini dikenal dengan nama pupuk ZA. Mengandung 21% nitrogen (N) dan 26% sulfur (S), berbentuk kristal dan bersifat kurang higroskopis.
− Urea (CO(NH2)2)
Pupuk urea mengandung 46% nitrogen (N).Bersifat sangat higroskopis. Sangat mudah larut dalam air dan bereaksi cepat, juga mudah menguap dalam bentuk amonia.
b. Pupuk Sumber Phosphor
− Superphosphat 36 (SP36)
Mengandung 36% phosphor dalam bentuk P2O5. Pupuk ini terbuat dari phosphat alam dan sulfat. Berbentuk butiran dan berwarna abu-abu.
− Amonium Phosphat
Pupuk ini umumnya digunakan untuk merangsang pertmbuhan awal tanaman ( starter fertilizer ). Bentuknya berupa butiran berwarna coklat kekuningan. Tidak
higroskopis sehingga tahan disimpan lebih lama dan mudah larut dalam air. c. Pupuk Sumber Kalium
− Kalium Khlorida (KCl)
− Kalium Sulfat (K2SO4)
d. Pupuk Sumber Unsur Hara Makro Sekunder
− Kapur Dolomit
Berbentuk bubuk berwarna putih kekuningan. Dikenal sebagai bahan untuk menaikkan pH tanah. Dolomit adalah sumber Ca (30%) dan Mg (19%) yang cukup baik.
− Kapur Kalsit
Berfungsi untuk meningkatkan pH tanah. Dikenal sebagai kapur pertanian yang berbentuk bubuk. Warnanya putih dan butirannya halus. Pupuk ini mengandung 90-99% Ca.
e. Pupuk Sumber Unsur Hara Mikro
Pupuk sebagai unsur hara mikro tersedia dalam dua bentuk yaitu :
− Bentuk garam anorganik
Bersifat mudah larut dalam air. Contoh pupuk mikro yang berbentuk garam anorganik adalah Cu, Fe, Zn, dan Mn yang seluruhnya bergabung dengan sulfat.
− Bentuk organik sintesis
Bentuk organik sintesis ditandai dengan adanya agen pengikat unsur logam yang disebut chelat. Chelat adalah bahan kimia organik yang dapat mengikat ion logam seperti yang dilakukan oleh koloid tanah. Unsur hara mikro yang tersedia dalam bentuk chelat adalah Fe, Mn, Cu, dan Zn. (4)
2.4 Pupuk Nitrogen, Fosfor, Kalium (NPK)
rendah. Kadar NPK yang banyak beredar adalah 15-15-15, 16-16-16, dan 8-20-15. Kadar lain yang tidak terlalu umum beredar adalah 6-12-15, 12-12-12, atau 20-20-20. Tiga tipe pupuk NPK yang pertama sangat umum didapati. Tipe pupuk NPK tersebut juga sangat populer karena kadarnya cukup tinggi dan memadai untuk menunjang pertumbuhan tanaman. NPK yang beredar merupakan pupuk impor, terutama dari Norwegia, Swedia, Jerman, Jepang, dan Amerika Serikat. Beberapa merek pupuk NPK dan unsur hara yang dikandungnya disajikan pada tabel berikut.
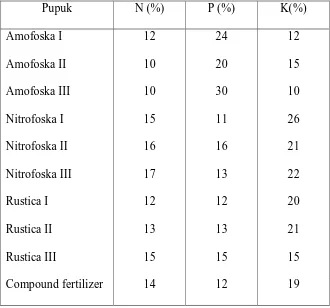
Tabel 2.1 Beberapa Jenis Pupuk NPK dan Unsur Hara Yang Dikandungnya(5).
Pupuk N (%) P (%) K(%)
Amofoska I 12 24 12
Amofoska II 10 20 15
Amofoska III 10 30 10
Nitrofoska I 15 11 26
Nitrofoska II 16 16 21
Nitrofoska III 17 13 22
Rustica I 12 12 20
Rustica II 13 13 21
Rustica III 15 15 15
Compound fertilizer 14 12 19
2.5 Nitrogen
Nitrogen merupakan hara penting untuk pertumbuhan tanaman, yaitu untuk pembentukan protein, sintesis klorofil dan untuk proses metabolisme. Kekurangan N akan mengurangi efisiensi pemanfaatan sinar matahari dan ketidakseimbangan serapan unsur hara. Tanaman yang kekurangan N ditandai oleh daun-daun tua berwarna hijau pucat kekuning-kuningan dan kecepatan produksi daun menurun. Sebaliknya kelebihan N menghasilkan daun yang lemah dan layu, serta berkurangnya buah jadi.
Beberapa hal yang menyebabkan kekurangan N antara lain : berkurangnya mineralisasi N pada tanah tergenang atau pH yang sangat rendah ( pH<4 ), tidak cukupnya atau tidak efektifnya aplikasi nitrogen, adanya saingan dalam penyerapan N dari gulma yang tumbuh dengan baik dan terhambatnya pertumbuhan akar dalam tanah yang dangkal dan padat.(6)
2.6 Metode Analisa Kjedhal
Metode kjedhal merupakan metode yang digunakan untuk menentukan kadar nitrogen. Pada dasarnya analisa nitrogen cara kjedhal dapat dibagi menjadi tiga tahapan yaitu proses dekstruksi, destilasi dan titrasi.
1. Tahap destruksi
Untuk mempercepat proses destruksi sering ditambahkan katalisator. Dengan penambahan katalisator tersebut titik didih asam sulfat akan dipertinggi sehingga destruksi berjalan lebih cepat. Suhu destruksi berkisar antara 370-410oC. selain penggunaan katalisator, kadang-kadang diberikan selenium. Selenium dapat mempercepat proses oksidasi karena zat tersebut selain menaikkan titik didih juga mudah mengadakan perubahan dari valensi tinggi ke valensi rendah atau sebaliknya. Penggunaan selenium lebih reaktif dibandingkan merkuri dan kupri sulfat tetapi selenium mempunyai kelemahan yaitu karena sangat cepatnya oksidasi maka nitrogen nya justru mungkin ikut hilang. Hal ini dapat diatasi dengan menggunakan selenium dengan jumlah yang sangat sedikit yaitu kurang dari 0,25 g. Proses destruksi selesai apabila larutan telah berubah menjadi jernih atau tidak berwarna. Agar analisa lebih tepat maka pada tahap destruksi ini dilakukan pula perlakuan blanko yaitu untuk koreksi adanya senyawa N yang bereaksi dari reagensia.
2. Tahap destilasi
3. Tahap tirasi
BAB III
METODOLOGI PERCOBAAN
3.1 Penentuan Kadar Nitrogen dari pupuk Nitrogen, Fosfor, Kalium (NPK)
Prinsip : Nitrogen dalam contoh dihidrolisis dengan asam sulfat membentuk senyawa ammonium sulfat. Nitrat dengan asam salisilat membentuk nitrosalisilat, kemudian direduksi dengan natrium tiosulfat membentuk senyawa ammonium. Suling senyawa ammonium dalam suasana alkali dengan penampung hasil sulingan larutan asam borat. Titrasi dengan larutan asam sulfat sampai warna hijau berubah menjadi warna merah jambu.
3.2 Alat-alat
− Neraca Analitis
− Labu Takar 100 ml (pyrex)
− Labu Takar 500 ml (pyrex)
− Pipet Volume 25 ml (pyrex)
−Alat Destilasi (pyrex)
−Labu Kjedhal (pyrex)
−Lumpang Porselin
3.3 Bahan-bahan
−Larutan asam sulfat salisilat
25 g asam salisilat larutkan hingga 1 liter dengan H2SO4 (p)
− Natrium tiosulfat (Na2S2O3.5H2O)
− Larutan asam borat
− Indikator conway
0,15 g brom cresol green dan 0,10 g metil merah larutkan hingga 100 ml dengan etanol
− Larutan NaOH 40%
Timbang 40 g NaOH larutkan dengan air suling hingga volume larutan 100 ml
− Larutan H2SO4 0,05 N
Pipet 1,4 ml H2SO4 dimasukkan dalam labu takar 1 L dan tambahakan air suling sampai garis tanda
− Air suling
3.4 Cara Kerja
− Timbang dengan teliti 0,5 g sampel yang telah dihaluskan, dimasukkan ke
dalam labu kjedhal.
− Tambahkan 25 ml larutan asam sulfat salisilat, aduk hingga rata dan
didiamkan selama 24 jam.
− Tambahkan 4 g Na2S2O3.5H2O kemudian panaskan pada suhu rendah hingga
gelembung habis. Naikkan suhu secara bertahap maksimum 300oC ( sekitar 2 jam ) dan biarkan dingin.
− Encerkan dengan air suling, dipindahkan ke dalam labu takar 500 ml, kocok
dan ditepatkan sampai garis tanda.
− Pipet 25 ml larutan sampel, dimasukkan ke dalam labu destilasi , ditambahkan
150 ml air suling dan batu didih.
− Suling setelah penambahan 10 ml larutan NaOH 40% dengan penampung hasil
sulingan 20 ml larutan asam borat 1% yang ditambahkan indikator conway.
− Titrasi dengan larutan H2SO4 0,05 N secara perlahan-lahan, tetes demi tetes
sambil dikocok sampai titik akhir titrasi tercapai ( warna hijau berubah menjadi merah jambu ).
BAB IV
[image:25.595.121.549.222.306.2]HASIL DAN PEMBAHASAN 4.1 Data Hasil Analisis
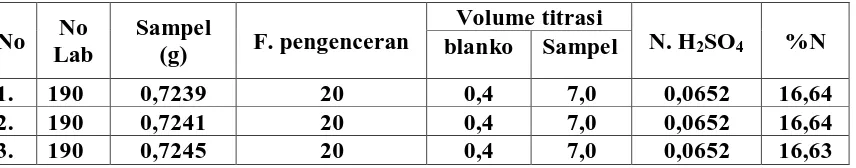
Tabel 4.1. Data dan perhitungan kadar Nitrogen dari pupuk NPK pada minggu pertama tanggal 5 januari 2009
No No Lab
Sampel
(g) F. pengenceran
Volume titrasi
N. H2SO4 %N blanko Sampel
1. 190 0,7239 20 0,4 7,0 0,0652 16,64
2. 190 0,7241 20 0,4 7,0 0,0652 16,64
3. 190 0,7245 20 0,4 7,0 0,0652 16,63
100%
1000
Sampel
Berat
F
F
N
)
V
V
(
)
%N
(
Nitrogen
Kadar
S B P N×
×
×
×
×
−
=
Keterangan :Vs = Volume titrasi sampel Vb = Volume titrasi blanko N = Normalitas H2SO4 Fp = Faktor Pengenceran FN = Faktor Nitrogen
4.1Perhitungan 16,64% 100% 1000 0,7239 14 20 0,0652 0,4) (7,0
%N1 × =
× × ×
× − =
Tabel 4.2. Data dan perhitungan kadar nitrogen dari pupuk NPK pada minggu kedua tanggal 12 januari 2009
No No Lab
Sampel
(g) F. pengenceran
Volume titrasi
N. H2SO4 %N blanko Sampel
1. 189 0,5325 20 0,4 5,2 0,0652 16,46
2. 189 0,5327 20 0,4 5,2 0,0652 16,45
3. 189 0,5330 20 0,4 5,2 0,0652 16,44
4.2Perhitungan
100%
1000
Sampel
Berat
F
F
N
)
V
V
(
)
%N
(
Nitrogen
Kadar
S B P N×
×
×
×
×
−
=
16,46% 100% 1000 0,5325 14 20 0,0652 0,4) (5,2%N1 × =
× × ×
× − =
[image:26.595.98.554.139.225.2]Data selengkapnya dapat dilihat pada tabel 4.2
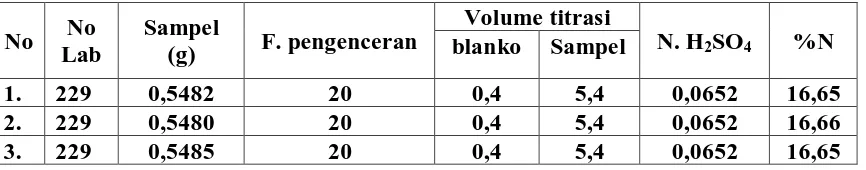
Tabel 4.3. Data dan perhitungan kadar nitrogen dari pupuk NPK pada minggu ketiga tanggal 19 januari 2009
No No Lab
Sampel
(g) F. pengenceran
Volume titrasi
N. H2SO4 %N blanko Sampel
1. 229 0,5482 20 0,4 5,4 0,0652 16,65
2. 229 0,5480 20 0,4 5,4 0,0652 16,66
3. 229 0,5485 20 0,4 5,4 0,0652 16,65
4.3Perhitungan
100%
1000
Sampel
Berat
F
F
N
)
V
V
(
)
%N
(
Nitrogen
Kadar
S B P N×
×
×
×
×
−
=
16,65% 100% 1000 0,5482 14 20 0,0652 0,4) (5,4%N1 × =
× × ×
× − =
[image:26.595.117.550.489.574.2]Tabel 4.4. Data dan perhitungan kadar nitrogen dari pupuk NPK pada minggu keempat tanggal 27 januari 2009
No No Lab
Sampel
(g) F. pengenceran
Volume titrasi
N. H2SO4 %N blanko Sampel
1. 118 0,5779 20 0,4 5,8 0,0652 17,05
2. 118 0,5781 20 0,4 5,8 0,0652 17,05
3. 118 0,5783 20 0,4 5,8 0,0652 17,04
4.4Perhitungan
100%
1000
Sampel
Berat
F
F
N
)
V
V
(
)
%N
(
Nitrogen
Kadar
S B P N×
×
×
×
×
−
=
17,05% 100% 1000 0,5779 14 20 0,0652 0,4) (5,8%N1 × =
× × ×
× − =
Data selengkapnya dapat dilihat pada tabel 4.4 4.3 Pembahasan
Jika tanah yang kekurangan nitrogen menyebabkan tanaman tersebut tumbuh dengan tidak subur dan terhambat. Daun menjadi hijau muda lalu berubah menjadi kuning, buahnya akan tumbuh kerdil kekuningan dan cepat matang. Di dalam tubuh tanaman, nitrogen bersifat dinamis sehingga jika terjadi kekurangan nitrogen pada bagian pucuk, nitrogen yang tersimpan pada daun tua akan dipindahkan ke organ yang lebih muda. Dengan demikian, pada daun-daun yang lebih tua gejala kekurangan nitrogen akan terlihat lebih awal.
Jika tanah yang kelebihan nitrogen, tanaman tampak selalu subur, ukuran daun menjadi lebih besar, batang menjadi lunak dan berair sehingga mudah rebah dan mudah diserang penyakit. Kelebihan nitrogen juga dapat menunda pembentukan bunga, bahkan bunga yang telah terbentuk lebih mudah rontok. Efek lain dari kelebihan nitrogen adalah pematangan buahnya juga terhambat.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil analisis beberapa sampel nitrogen dari pupuk NPK diperoleh kadar nitrogen yang masih memenuhi baku mutu menurut SNI 2-2803-2000 yaitu minimal 6%.
5.2 Saran
DAFTAR PUSTAKA
Isnaini.M.2006.Pertanian Organik.Cetakan Pertama.Yogyakarta : Penerbit Kreasi Wacana.
Novizan.2002.Petunjuk Pemupukan Yang Efektif.Cetakan Pertama.Jakarta : Penerbit P.T. Agro Media Pustaka.
Darmosarkoro.W.2003.Lahan Dan Pemupukan Kelapa Sawit.Edisi Pertama.Medan : Pusat Penelitian Kelapa Sawit.
Paulus.S&Marsono2001.Pupuk Akar Jenis Dan Aplikasi.Jakarta : Penrbit Penebar Swadaya.
Rinsema.W.J.1993.Pupuk Dan Cara Pemupukan.Jakarta.Penerbit Bhratara. Sutejo.2002.Pupuk Dan Cara Pemupukan.Jakarta : Penerbit Rineka Cipta. SNI 2-2803-2000.Pupuk NPK.2000
Tabel-1 : Baku mutu pupuk Nitrogen, Fosfor, Kalium (NPK) Padat Menurut SNI 2-2803-2000.
No Jenis Uji Persyaratan
1. Nitrogen Total Minimal 6%
2. Fosfor larut asam nitrat 2% sebagai P2O5 Minimal 6%
3. Kalium sebagai K2O Minimal 6%
4 Jumlah kadar N, P2O5 dan K2O Minimal 30%
5. Kadar air Minimal 2%
Gambar-1 pupuk NPK
Pupuk NPK 161616