LAMPIRAN I
DATA PENELITIAN
L1.1 DATA HASIL UJI pH TERHADAP SELULOLA MIKROKRISTAL BERDASARKAN VARIASI KONSENTRASI HCl DAN SUHU HIDROLISIS
Tabel L1.1 Data Hasil Uji pH Terhadap Selulola Mikrokristal Berdasarkan Variasi Konsentrasi HCl Dan Suhu Hidrolisis
KonsentrasiHCl
pH
65°C 70°C 75°C 80°C
2 N 6 6 6 7
2,5 N 6 6 7 6
3 N 6 6 7 6
3,5 N 6 6 7 6
L1.2 DATA HASIL ZAT LARUT DALAM AIR TERHADAP SELULOLAMIKROKRISTAL BERDASARKANVARIASI KONSENTRASI HCl DAN SUHU HIDROLISIS
Tabel L1.2 Data Hasil Zat Larut Dalam Air Terhadap Selulola Mikrokristal Berdasarkan Variasi Konsentrasi HCl Dan Suhu Hidrolisis
Konsentrasi HCl
Zat larut dalam air (%)
65 °C 70°C 75 °C 80 °C
2 N 1 0 0,8 0,4
2,5 N 0,2 0,4 0,2 0
3 N 0,2 0,4 0,6 0,2
L1.3 DATA HASIL SUSUT PENGERINGAN TERHADAP SELULOLA MIKROKRISTAL BERDASARKAN VARIASI KONSENTRASI HCl DAN SUHU HIDROLISIS
Tabel L1.3 Data Hasil Susut Pengeringan Terhadap Selulola Mikrokristal Berdasarkan Variasi Konsentrasi HCl Dan Suhu Hidrolisis
Konsentrasi HCl
Susut pengeringan (%) 65°C 70°C 75°C 80°C
2 N 0 1,57 1,58 1,59
2,5 N 1,6 1,64 1,57 1,63
3 N 0 1,61 1,6 0
LAMPIRAN II
CONTOH PERHITUNGAN
L2.1 PEMBUATAN HCl 2 N ; 2,5 N; 3 N ; DAN 3,5 N DALAM 100 ML
DARI HCl37%(
ρ
= 1,19)N = % × 10 × ρ × e Mr
= 37 × 10 × 1,19 × 1 36,45
= 12,07 N Pembuatan HCl 2 N V1 . N1 = V2 . N2
100 . 2 = V2 . 12,07 V2 = 16,57 mL
Pembuatan HCl 2,5 N V1 . N1 = V2 . N2
100 . 2,5 = V2 . 12,07 V2 = 20,7 mL
Pembuatan HCl 3 N V1 . N1 = V2 . N2
100 . 3 = V2 . 12,07 V2 = 24,8 mL
Pembuatan HCl 3,5 N V1 . N1 = V2 . N2
L2.2 PERHITUNGAN RENDEMEN SELULOSA MIKROKRISTAL Jumlah selulosa yang digunakan = 75 g
Jumlah perolehan setelah proses hidrolisis :
Total α-selulosa yang dihasilkan = 32 g
Dari 32 g α-selulosa yang dihasilkan, 16 g digunakan untuk proses pembuatan selulosa mikrokristal dengan menggunakan asam klorida sedangkan 16 g lainnya digunakan untuk proses pembuatan selulosa mikrokristalin dengan menggunkan asam sulfat.
Dari 16 g α-selulosa dihasilkan selulosa mikrokritsal = 8 g
Sehingga perhitungan rendemen α-selulosa yang dihasilkan dari selulosa adalah sebagai berikut :
Rendemen α-selulosa = jumlah α−selulosa yang dihasilkan
jumlah selulosa yang digunakan × 100%
= 32 g
75 g × 100% = 42,67%
Untuk menghitung rendemen selulosa mikrokristal yang dihasilkan dari proses hidrolisis α-selulosa dengan menggunakan asam klorida adalah sebagai berikut :
Rendemen Selulosa Mikrokristal =jumlah selulosa mikrokristal
jumlah α−selulosa × 100%
= 16 g
8 g × 100%
L2.3 PERHITUNGAN ZAT LARUT DALAM AIR SELULOSA MIKROKRISTAL
Sebagai contoh perhitungan nilai susut pengeringan selulosa mikrokristal, di ambil sampel selulosa mikrokristal pada konsentrasi 2 N suhu 65°C dengan data sebagai berikut :
Berat awal sampel = 1 g
Berat sampel setelah perlakuan pada pengujian zat larut dalam air = 0,99 g Sehingga diperoleh perhitungan zat larut dalam air :
X = (Berat awal sampel )−(Berat akhir sampel )
(Berat awal sampel ) × 100% = 1− 0,99
1 × 100% = 1%
L2.4 PERHITUNGAN SUSUT PENGERINGAN SELULOSA
MIKROKRISTAL
Sebagai contoh perhitungan nilai susut pengeringan selulosa mikrokristal, di ambil sampel selulosa mikrokristal pada konsentrasi 2 N suhu 70°C dengan data sebagai berikut :
Berat krus kosong (A) = 56,79 g
Berat krus + selulosa mikrokristal sebelum dikeringkan = 57,79 g Berat krus + selulosa mikrokristal setelah dikeringkan = 56,88 g Sehingga diperoleh perhitungan susut pengeringan :
X = (B−A)−(C−A)
(B−A) × 100% = 57,79 −56,88
L2.5 PERHITUNGAN INDEKS KRISTALINITAS SELULOSA MIKROKRISTAL
Cr = I 002− Iam I002
× 100%
Dimana :
Cr = indeks kristalinitas (%)
I002 = intensitas maksimum pada 2θ (21°) Iam = intensitas minimum pada 2θ(12 – 18°)
Sehingga diperoleh perhitungan indeks kristalinitas selulosa mikrokristal : Cr = I 002− Iam
I002
× 100% = 1000 −271
LAMPIRAN III
DOKUMENTASI PENELITIAN
L3.1 ISOLASI α-SELULOSA DARI SELULOSA TANDAN KOSONG
KELAPA SAWIT
L3.2 PEMBUATAN SELULOSA MIKROKRISTAL
LAMPIRAN IV
HASIL ANALISIS INSTRUMEN
L4.1 HASIL FTIR SELULOSA TANDAN KOSONG KELAPA SAWIT
Gambar L4.1 Hasil FTIR Selulosa Tandan Kosong Kelapa Sawit
L4.2 HASIL FTIR α-SELULOSA
L4.3 HASIL FTIR SELULOSA MIKROKRISTAL
Gambar L4.3 Hasil FTIR Selulosa Mikrokristal
L4.4 HASIL XRD SELULOSA TANDAN KOSONG KELAPA SAWIT
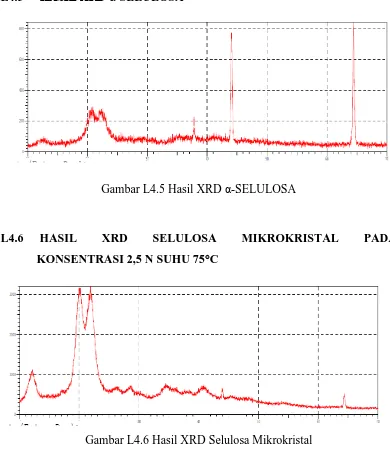
L4.5 HASIL XRD α-SELULOSA
Gambar L4.5 Hasil XRD α-SELULOSA
L4.6 HASIL XRD SELULOSA MIKROKRISTAL PADA
KONSENTRASI 2,5 N SUHU 75°C
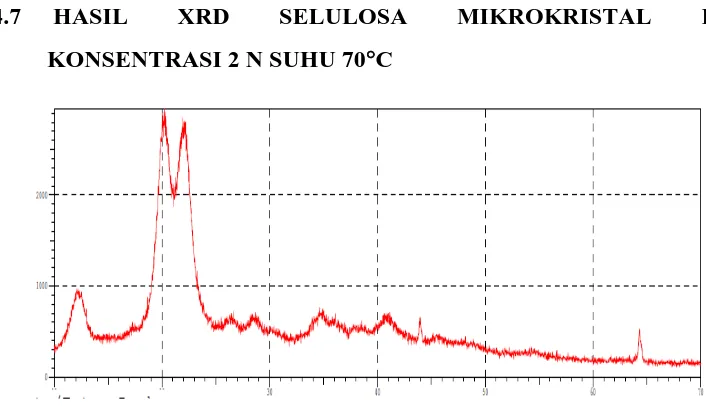
L4.7 HASIL XRD SELULOSA MIKROKRISTAL PADA
KONSENTRASI 2 N SUHU 70°C
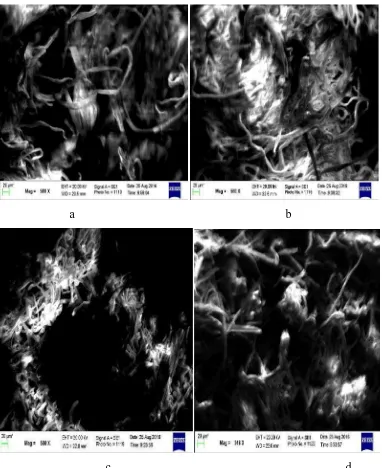
L4.8 HASIL SEM SELULOSA TANDAN KOSONG KELAPA SAWIT, α -SELULOSA, SELULOSA MIKROKRISTAL PADA KONSENTRASI 2,5 N
SUHU 75°C DAN SELULOSA MIKROKRISTAL PADA KONSENTRASI
2 N SUHU 70°C
a b
c d
Gambar L4.8(a) selulosa TKS, (b)α- selulosa, (c) selulosa mikrokristal 2,5 N 75 °C, (d) selulosa mikrokristal 2 N
DAFTAR PUSTAKA
[1] Asep, H., Farah, D., Yeni, M., Dina, S., Nurhaida.“Sifat Kimia Batang Kelapa Sawit (Elaeis guinensis jacq) Berdasarkan Letak Ketinggian dan Kedalaman Batang”.Fakultas Kehutanan, Universitas TanjungPura, Pontianak, Hal. 472-473.
[2] Karbelin, L., Purnamasari,Y.D.”Prarancangan Pabrik Microcrystalline Cellulose Kapasitas 5000 ton/tahun. Universitas Gajdah Mada. Yogyakarta. 2014. Hal 1-10
[3] Putra G., Zulharmita., Harrizul,R.“Preparasi Dan Karakterisasi Mikrokristalin Selulosa Dari Limbah Serbuk Kayu Penggergajian”. Jurnal Sains dan Teknologi Farmasi,16(2)(2011) : hal 180-188.
[4] Arry, Y., Eka, R., Effionora, A,“Preparation and Characterization of Microcrystalline Cellulose from nata de coco for Tablet Excipient, Istecs JournalScience and Technology Policy, IV (December 2003), hal. 71-78.
[5] Toshko, S.T., Nikola, R.G., Evstati, P.V. “Method Of Producing Microcrystalline Cellulose”, United States Patent 111 (3,954,727)(1976).
[6] Halim, A., Elfi, S.B., Erni, S.” Pembuatan Mikrokristalin Selulosa dari Jerami Padi (Oriza sativa linn) dengan variasi Waktu Hidrolisa.” Jurnal Sains dan Teknologi Farmasi,7(2) (2002) : hal 80-87.
[7] Muhammad, A.A.” Pembuatan Mikrokristal Selulosa Dari Tandan KosongKelapa Sawit.”Skripsi.Fakultas Matematika Dan Ilmu Pengetahuan Alam.Universitas Lampung. Bandar Lampung.2016. Hal 18-22.
[8] Rosnah, M S., Halim,K. U., and Wan, H. “The potential of oil palm lignocellulosic fibres for the cellulose derivatives production”.Proc of the research and consultancy seminar.Faculty of Mechanical Engineering, UiTM Shah Alam, Malaysia.(2002). pp 140-145.
[9] Tjahjono,H.,dan Meta, R. “ Karakterisasi Selulosa Mikro-kristal dari Tandan Kosong Kelapa Sawit,” Jurnal Peneltian Kelapa Sawit,21(1) (2013): hal 31-39.
[10] Http//BPPT-HUMAS Tanaman Sawit.ac.id.2010
[12] Fenny, A., Marpongahtun, Saharman, G.”Studi Penyediaan Nanokristal Selulosa Dari Tandan Kosong Sawit (TKS),”Jurnal Saintia Kimia, 1(2) (2013), hal 1-3.
[13] Han, R., Widya, F. “Kemungkinan Pemanfaatan Tandan Kosong Kelapa Sawit Sebagai Bahan Baku Pembuatan Papan Serat Berkerapatan Sedang, hal 1-3. [14] Satia, C.D.S. “Pembuatan Selulosa Mikrokristal Pelepah Pinang (Areca Catechu L.) Sebagai Bahan Tambahan Tablet Ekstrak Etanol Kulit Batang Sikkam (Bischofia Javanica Blume),” Skripsi, Program Studi Sarjana Farmasi Fakultas Farmasi Universitas Sumatera Utara Medan, 2014, hal.8-9.
[15] Sumaiyah,“Pembuatan dan Karakteristik Selulosa Mikrokristal dan Nanokristal Tandan Aren (Arenga pinnata (Wurmb) Merr) dan Penggunaan Sebagai Eksipien Dalam Tablet”, Disertasi, Fakultas Farmasi, Universitas Sumatera Utara, 2014, hal 8-9.
[16] Putri, H., Juanita, T., Karsono, “Pengaruh Selulosa Mikrokristal Kulit Buah Kapuk Terhadap Laju Disolusi Tablet Furosemida, Journal of Pharmaceutics and Pharmacology,1(1) (2012) : hal 55 – 62.
[17] Rosyid., Nurul, H. “Konsentrasi Asam Optimum Pada Isolasi Nanokristalin Selulosa Bakterial Dari Limbah Kulit Nanas”, Universitas Pendidikan Indonesia, 2014, hal.1-3.
[18] Asko, K., Veli, V., Leif, R., Kari, P., Olli, D., Kari,V. “Process For Producing Microcrystaline Cellulose”, United States Patent Application Publication(0112193)(2013).
[19] Erkki, I.S.R., Leif, R., Veli, M.V., Asko, K., Olli, D., Kari, V.“Manufacturing of Microcellulose”,United States Patent Application Publication(0179912)(2014).
[20] Hanna, M., Gerald, B., Vesselin, M.“Production of Microcrystalline Cellulose byReactive Extrusion”. Industrial Agricultural Products Center Publications&Information.9. (2001).
[21] Maha, M.I., El-Zawawy, W.K., Juttke, Y., Koschella, A and Heinze, T. “Cellulose and microcrystalline cellulose from rice straw and banana plant waste: preparation and characterization”. Cellulose.(2013) DOI 10.1007/s10570-013-9992-5.
[23] Zulharmita., Siska, N.D., Mahyuddin, “Pembuatan Mikrokristalin Selulosa Dari Ampas Tebu (Saccharum Officinarum L.),” Jurnal Sains dan Teknologi Farmasi, 17(2)(2012): hal 158-163.
[24] Daniel, B., Aji, M., and Kristina, O.”Optimization of the isolation of nanocrystals from microcrystalline cellulose by acid hydrolysis,”Cellulose 13 (2006) :171 –180.
[25] Dafit, E., Neswati., Ira.D.R,” Pengaruh Konsentasi HCl Dalam Proses
Hidrolisis α-Selulosa Dari Ampas Tebu (Saccharum officinarum,L) Terhadap Karakteristik Mikrokristalin,” Fakultas Pertanian, Universitas Andalas, Padang, Hal 4-10
[26] Anam,“Analisis Gugus Fungsi Pada Sampel Uji Bensin Dan Spritus Menggunakan Metode Spektrofotokopi FTIR, FMIPA, Universitas Diponegoro, 2007
[27] Lawson, D. Introduction to Fourier Transform Infrared Spectrometry (USA: ThermoNicolet, 2001)
[28] Poppy, S.”Pemanfaatan Selulosa Mikrokristal Dari Tandan Kelapa (Cocos Nucifera L) Sebagai Pengisi Plastik Polipropilena Yang Terbiodegradasikan ,” Tesis, Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan, 2013, Hal 31-32.
BAB III
METODOLOGI PENELITIAN
3.1 WAKTU DAN TEMPAT PENELITIAN
Penelitian ini dilaksanakan di Laboratorium Penelitian Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara.Analisis hasil penelitian ini dilaksanakan diLaboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara, Laboratorium Fisika Fakultas MIPA Universitas Negeri Medan dan Laboratorium Pusat Penelitian Kelapa Sawit Medan.
3.2 ALAT DAN BAHAN
3.2.1 Alat
Pada penelitian ini alat yang digunakan antara lain untuk proses : a. Penyediaan selulosa mikrokristal meliputi :
1. Neraca analitik 2. Oven
3. Beaker gelas
4. Termometer 100°C 5. Pipet tetes
6. Batang Pengaduk 7. Hot Plate
8. Gelas ukur
b. Pengujian sifat-sifat fisikokimia selulosa mikrokristal meliputi : 1. Saringan Whatman No.1
2. Cawan porselen 3. Waterbath 4. Corong 5. pH meter
3. Scanning Electron Microscopy(SEM) 3.2.2 Bahan
Pada penelitian ini bahan yang akan digunakan antara lain :
1. Selulosa yang berasal dari serat tandan kosong kelapa sawit yang berfungsi sebagai bahan bakuyang diperoleh dari PPKS, Jl.Brigjen Katamso No.51 Medan.
2. Asam klorida (HCl) yang berfungsi sebagai larutan yang digunakan untuk proses hidrolis yang diperoleh dari Laboratorium Penelitian, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara .
3. Akuades yang berfungsi sebagai pelarut yang diperoleh dari UD Rudang Jaya, Jl. Dr. Mansyur Medan, Sumatera Utara.
4. NaOH berfungsi untuk melarutkan lignin pada selulosa. 5. NaOCl berfungsi untuk memutihkan selulosa.
3.3 PROSEDUR PENELITIAN
3.3.1 Prosedur Isolasiα-Selulosa
Prosedur isolasiα-selulosa adalah sebagai berikut [23] :
1. Sebanyak 75 g selulosa yang didapat dari tandan kosong kelapa sawit ditambah dengan 1000ml NatriumHidroksida (NaOH) 17,5% dan dipanaskan pada suhu 80°C selama 30 menit.
2. Hasilnya kemudian disaring dengan menggunakan kain serbet sambil dicuci dengan airsampai filtrat jernih dan diperas, ampasnya ditambahkan 500 ml campuran Natrium Hipoklorit (NaOCl) 3,5% dan air (1:1) kemudian dipanaskan pada suhu 100°C selama 5 menit, Setelah itu dicuci kembali dengan air sampai filtratnya jernih, disaring dengan kain serbet dan diperas.
3.3.2 Prosedur Pembuatan Selulosa Mikrokristal
Prosedur pembuatan selulosa mikrokristal adalah sebagai berikut [23]: 1. Sebanyak 1 g α-selulosa dimasukkan ke dalam beaker glass dan
dihidrolisis dengan HCl dengan variasi konsentrasi 2 N, 2,5N, 3 N dan 3,5 N dan dididihkan dengan variasi suhu 65°C, 70°C, 75°C dan
80°Cselama 15 menit.
2. Kemudian dituangkan akuades kedalam beaker glass sambil diaduk dengan spatula dan diamkan semalam.
3. Selulosa mikrokristal yang dihasilkan dari proses ini dicuci dengan akuades, disaring dan dikeringkan dengan oven pada suhu 57-60°C selama 2 jam. Maka diperoleh selulosa mikrokristal.
4. Selanjutnya selulosa mikrokristal digerus dan disimpan pada suhu kamar dalam desikator serta dihitung rendemen selulosa mikrokristal yang telah dihasilkan.
3.3.3 Perhitungan Rendemen Selulosa Mikrokristal
Rendemen selulosa mikrokristal dihitung sebagai persentase perbandingan antara berat selulosa mikrokristal hasil hidrolisis terhadap berat bahan yang digunakan berupa α-selulosa dimana perhitungan rendemen selulosa mikrokristal berdasarkan pada berat kering bahan. Rumus perhitungan rendemen selulosa mikrokristal sebagai berikut [3]:
Rendemen = berat selulosa mikrokristal
3.4 DIAGRAM ALIR PENELITIAN
3.4.1 Diagram Alir Isolasiα-Selulosa
Diagram alir pemisahan α-selulosaadalah sebagai berikut [23] :
Ditambahkan dengan 1000 ml NaOH 17,5%
Dicuci bersih dengan air, ampasnya ditambah dengan campuran Natrium Hipoklorit (NaOCl) 3,5% dan air (1:1)
Tidak
ya
Gambar 3.1 Diagram Alir Isolasi α-Selulosa [23]. Diperoleh α-selulosa dan dilakukan uji FTIR
Sebanyak 75 g Selulosa
Dipanaskan pada suhu 800 C selama 30 menit.
Dipanaskan pada suhu 1000C selama 5 menit
Dicuci dengan air sampai filtratnya jernih, disaring dengan kain serbet dan diperas
filtrat lalu dikeringkan pada suhu 600C dalam oven selama 4 jam Apakah
3.4.2 Diagram Alir Pembuatan SelulosaMikrokristal
Diagram alir pembuatan selulosa mikrokristal adalah sebagai berikut [23]:
Dimasukan dalam beaker glass dan dihidrolisis dengan HCl dengan variasi konsentrasi 2 N ; 2,5 N ; 3 N ; 3,5 N
Tidak
ya
Gambar 3.1 Diagram Alir Pembuatan Selulosa Mikrokristal [23].
Dicuci selulosa mikrokristal yang dihasilkan dengan akuades dan disaring Dituangkan akuades kedalam beaker glass sambil diaduk dengan batang pengaduk
dan diamkan semalam.
Dikeringkan dengan oven pada variasi suhu 56-60°C selama 3 jam.
Digerus selulosa mikrokristal dan disimpan pada suhu kamar dalam desikator.
zat larut dalam air Susut
Pengeringan
Organoleptik Uji pH SEM
Apakah filtratnya sudah jernih? Sebanyak 1 g α-selulosa
Dididihkan dengan variasi suhu hidrolisa 65°C, 70°C, 75°C dan 80°C selama 15 menit
3.5 PROSEDUR ANALISIS DAN KARAKTERISASI
3.5.1 Sifat- Sifat Fisikokimia Selulosa Mikrokristal a. Prosedur Pengujian Organoleptik
Prosedur analisis pengujian organoleptik dilakukan dengan mengamati karakteristik sampel yang diletakkan di atas dasar yang berwarna putih, berupa bentuk atau rupa, dan warna [23].
b. Prosedur Uji pH
Prosedur analisis uji pH dilakukan dengan cara mencampurkan 1 g serbuk sampel dengan 100 mL akuades selama 5 menit sambil diaduk dan diukur pHnya dengan pH meter [23].
c. Prosedur Zat Larut Dalam Air
Prosedur analisiszat larut dalam air adalah sebagai berikut [23]:
1. Sebanyak 1 g sampel dikocok dengan 80 mL akuades selama 10 menit.
2. Disaring dengan menggunakan kertas saring whatman No.1, lalu diuapkan di atas waterbath pada suhu 100-105°C selama 1 jam. Berat sisa tidak boleh dari 12,5 mg (0,25%).
d. Prosedur Susut Pengeringan
Prosedur analisis susut pengeringanadalah sebagai berikut [23]: 1. Sebanyak 1 g sampel dimasukkan dalam cawan porselen.
2. Dikeringkan dalam oven pada suhu 100-105°C sampai diperoleh berat konstan.
3. Persentase susut pengeringan dapat ditentukan dengan perbandingan berat sampel dengan berat setelah dikeringkan.
3.5.2 Karakterisasi Selulosa Mikrokristal
Alat FTIRyang digunakan adalah Shimadzu IR-Prestige 21.
b. Pengujian Difraksi Sinar-X (XRD)
Alat XRD yang digunakan adalah 6100 Shimadzu untuk mengetahui perubahan fase dan indeks kristalinitas.
Indeks kristalinitas (Cr) selulosa mikrokristal dihitung dengan persamaan [7] :
Cr =I 002− Iam
I002
× 100%
Dimana :
Cr = indeks kristalinitas (%)
I002 = intensitas maksimum pada 2θ (21°) Iam = intensitas minimum pada 2θ (12 – 18°) c. PengujianScanning Electron Microscopy (SEM)
BAB IV
HASIL DAN PEMBAHASAN
4.1 RENDEMEN SELULOSA MIKROKRISTAL
Dalam penelitian ini, dari 75 gram selulosa dihasilkan α-selulosa sebanyak 32 gram (42,67%). Sementara itu dari 16 gram α-selulosa yang dihidrolisis dihasilkan selulosa mikrokristal sebanyak 8 gram (50%). Rendemen α-selulosa dan selulosa mikrokristal dapat dilihat pada Tabel 4.1 dibawah ini.
Tabel 4.1.Jumlah perolehan alfa selulosa dan selulosa mikrokristal. Jumlah selulosa (g) Jumlah perolehan (g)
α-selulosa Selulosa mikrokristal dari α -selulosa
75 32 8
- Rendemen α-selulosa = 32 g x 100% = 42,67% 75 g
- Rendemen selulosa= 8 g x 100% = 50% Mikrokristal 16 g
Pada Gambar 4.1 di bawah ini dapat dilihat selulosa, α-selulosa, dan selulosa mikrokristal yang dihasilkan.
Gambar 4.1 a. Selulosa, b. α- Selulosa, dan c. Selulosa Mikrokristal dari Selulosa Tandan Kosong Kelapa Sawit
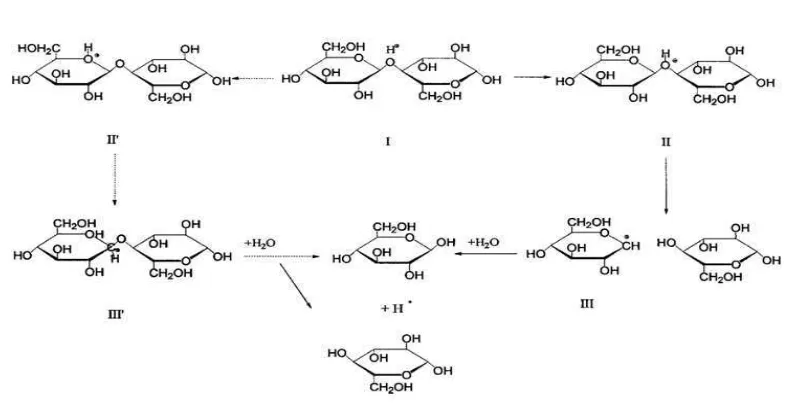
Selama proses pembuatan selulosa mikrokristal terlihat pada mulanya (Gambar 4.1a) selulosa tandan kosong kelapa sawit memiliki struktur permukaan yang masih kasar, kemudian dilakukan proses alkalisasi pada selulosa tandan kosong kelapa sawit dengan menambahkan NaOH 17,5% menghasilkan α -selulosa (Gambar 4.2b). α-selulosa mengalami perubahan bentuk atau struktur permukaan menjadi lebih halus dibandingkan dengan selulosa tandan kosong kelapa sawit dan terjadi perubahan warna menjadi lebih putih akibat adanya penambahan NaOCl 3,5% pada proses bleaching, selanjutnya pada saat proses hidrolisis α-selulosa menggunakan HCl dengan variasi konsentarsi HCl dan suhu hidrolisis menghasilkan selulosa mikrokristal, perubahan bentuk atau struktur permukaan pada selulosa mikrokristal terlihat menjadi semakin lebih halus dibandingkan dengan α-selulosa. Hal ini disebabkankarena pada saat proses hidrolisis menggunakan HCl mengakibatkan sebagian besar amorf yang terdapat dalam α-selulosa larut dan menyisakan bagian kristal. Secara teori, molekul selulosa merupakan makrofibril dari glukosa yang terikat satu dengan lainnya membentuk rantai polimer yang sangat panjang.Adanya lignin serta hemiselulosa di sekeliling selulosa merupakan hambatan utama untuk menghidrolisis selulosa [14]. Berikut ini adalah mekanisme reaksi hidrolisis dari selulosa menjadi selulosa mikrokristal.
Gambar 4.2 mekanisme reaksi hidrolisis dari selulosa menjadi selulosa mikrokristal.
4.2 SIFAT-SIFAT FISIKOKIMIA SELULOSA MIKROKRISTAL 4.2.1 Pengamatan Organoleptik
Pengamatan organoleptik yang dilakukan terhadap selulosa mikrokristal meliputi pengujian yang didasarkan pada proses pengindraan. Sampel diamati bentuknya berupa serbuk halus, dan berwarna putih.Hasil Pengamatan organoleptik yang telah dilakukan menunjukkan bahwa semua variabel yang dilakukan menghasilkan selulosa mikrokristalyang telah memenuhi persyaratan British pharmacoea 2009 yaitu berbentuk serbuk halusdan berwarna putih [23].
4.2.2. Uji pH
Hasil uji pH terhadap selulosa mikrokristal dapat dilihat pada Tabel 4.2 dibawah ini.
Tabel 4.2 Hasil Uji pHTerhadap Selulosa Mikrokristal Berdasarkan Variasi Konsentrasi HCl Dan Suhu Hidrolisis
Konsentrasi HCl
pH
65°C 70°C 75°C 80°C
2 N 6 6 6 7
2,5 N 6 6 7 6
3 N 6 6 7 6
3,5 N 6 6 7 6
Pada Tabel 4.2 terlihat bahwa hasil uji pH terhadap selulosa mikrokristal pada setiap variasi konsentrasi dan suhu hidrolisis menunjukkan nilai pH berkisar antara 6 – 7. Nilai ini tidak jauh berbeda dan memenuhi persyaratan British pharmacoea 2009 yaitu rentang nilai pH 5 – 7 [23]. Hal ini disebabkan pada saat
4.2.3 Zat Larut Dalam Air
Hasil uji zat larut dalam air terhadap selulosa mikrokristal dapat dilihat pada Tabel 4.3 dibawah ini.
Tabel 4.3 Hasil Uji Zat Larut Dalam Air Terhadap Selulosa Mikrokristal Berdasarkan Variasi Konsentrasi HCl Dan Suhu Hidrolisis Konsentrasi HCl
Zat larut dalam air (%)
65 °C 70°C 75 °C 80 °C
2 N 1 0 0,8 0,4
2,5 N 0,2 0,4 0,2 0
3 N 0,2 0,4 0,6 0,2
3,5 N 0,2 0,6 0,2 0,2
Pada Tabel 4.3 terlihat bahwa hasil uji zat larut dalam airterhadap selulosa mikrokristal yang dihasilkan dalam penelitian ini pada masing-masing konsentrasi dan suhu hidrolisis memiliki nilai yang berbeda-beda. Menurut persyaratan British pharmacoea 2009 bahwa nilai zat larut dalam air berkisar ≤ 0,25% [23]. Sehingga dari semua selulosa mikrokristal yang dihasilkan, yang telah memenuhi persyaratan tersebut yaitu selulosa mikrokristal pada variasi konsentrasi HCl 2,5N, 3N, dan 3,5N pada masing-masing suhu hidrolisis 65°C, 75°C dan 80°C. Nilai ini mengindikasikan bahwa fase kristal di dalam selulosa mikrokristal pada variasi konsentrasi dan suhu hidrolisis tersebut telah terbentuk selama proses hidrolisis α-selulosa berlangsung, dimana bagian amorf pada α-selulosa telah dihilangkan oleh asam sehingga penyerapan kadar air sangat sedikit, sementara itu, pada selulosa mikrokristal yang tidak memenuhi persyaratan, hal ini disebabkan karena pada saat proses hidrolisis berlangsung tidak semua fase amorf yang mengandung zat-zat yang dapat larut dalam air dihilangkan oleh asam sehingga penyerapan kadar air menjadi semakin banyak.
4.2.4 Susut Pengeringan
Tabel 4.4 Hasil Uji Susut Pengeringan Terhadap Selulosa Mikrokristal Berdasarkan Variasi Konsentrasi HCl Dan Suhu Hidrolisis.
Konsentrasi HCl
Susut pengeringan (%) 65°C 70°C 75°C 80°C
2 N 0 1,57 1,58 1,59
2,5 N 1,6 1,64 1,57 1,63
3 N 0 1,61 1,6 0
3,5 N 1,57 0 0 0
Pada Tabel 4.4 terlihat bahwa nilai susut pengeringan dari selulosa mikrokristal yang dihasilkan memiliki nilai yang berbeda-beda. Dari perolehan hasil diatas maka terlihat bahwa nilai susut pengeringan seluruh selulosa mikrokristal yang dihasilkan berkisar pada rentang 0-1,64% dimana nilai tersebut telah sesuai dengan persyaratan British pharmacoea 2009 yaitu tidak lebih dari 5% [23]. Hal ini disebabkan selama proses hidrolisis berlangsung bagian amorf yang mengandung air pada α-selulosa telah dihilangkan oleh asam dan meninggalkan fase kristal.Pada saat fase kristal terbentuk, nilai susut pengeringan akan menjadi semakin kecil dikarenakan fase kristal lebih sulit untuk penyerapan kadar air dibandingkan dengan fase amorf.
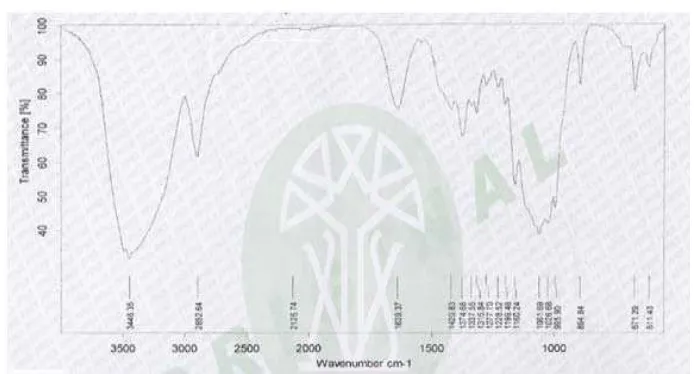
4.3 KARAKTERISASI SELULOSA MIKROKRISTAL 4.3.1 Analisis Fourier Transform Infrared (FTIR)
Hasil FTIR dapat dilihat pada Gambar 4.2 di bawah ini.
Gambar 4.2 Hasil FTIR (a) Selulosa TKKS, (b)α- Selulosa, (c) Selulosa Mikrokristal pada 2,5 N 75 °C
absorbansi 2897cm-1 dari sebelumnya 2892 cm-1. Hal ini dapat dikaitkan dengan semakin berkurangnya serapan bilangan OH menunjukkan bagian amorf pada saat proses hidrolisis oleh asam, lepas dan OH akan berikatan dengan ion asam sedangkan CH akan berubah menjadi CH2[9].Serta juga terjadi regangan serapan pada daerah bilangan gelombang 1064 cm-1 menunjukkan adanya gugus C-O.
4.3.2 Pengujian X-Ray Diffraction (XRD)
[image:30.595.257.395.324.614.2]Untuk mengetahui terjadinya perubahan pada setiap tahapan proses hidrolisis dari selulosa menjadi α-selulosa dan selulosa mikrokristal dan menyimpulkan bahwa selulosa mikrokristal memang berbentuk kristal dapat dilihat dari hasil XRD pada Gambar 4.3 berikut ini
Gambar 4.3 hasil XRD (a) selulosa TKKS, (b)α- selulosa, (c) selulosa mikrokristal pada 2 N 70°C, (d) selulosa mikrokristal pada
2,5 N 75 °C
Dari gambar XRD dapat dilihat bahwa pada Gambar 4.3a (selulosa)belum terbentuk puncak yang dapat menunjukkan adanya fase kristal. Puncak yang terlihat pada gambar cenderung lebih rendah bahkan hampir terlihat rata daripada
I
puncak yang terdapat pada Gambar 4.3b (α-selulosa). Hal ini disebabkan karena selulosa masih banyak mengandung fase amorf. Sedangkan pada Gambar 4.3b, mulai terbentuk dua puncak yang menunjukkan bahwa mulai terbentuknya fase kristal. Sementara itu, pada Gambar 4.3c dan d, diperoleh tiga puncak yang diantaranya terdapat dua puncak yang lebih tajam. Pada Gambar 4.3d (selulosa mikrokristal pada HCl 2,5 N 75°C) terdapat tiga puncak yaitu berada padasudut (2θ) 12°, 20° dan 22°. Hal ini menunjukkan bahwa selulosa mikrokristal memang berbentuk kristal dengan ditandai dua puncak maksimum yangrelatif lebihtajam yaitu berada pada sudut (2θ) 20° dan 22° jika dibandingkan dengan Gambar 4.3c (selulosa mikrokristal pada HCl 2 N 70°C). Hal ini membuktikan bahwa masih terdapat sebagian fase amorf pada α-selulosa yang disebabkan karena asam yang menghidrolisis bagian amorf pada selulosa hanya sebagian saja yang terpenetrasi ke dalam molekul selulosa.Dari hasil XRD diperoleh indeks kristalinitas selulosa mikrokristal pada konsentrasi HCl 2,5 N 75°C sebesar 72,9%. Perhitungan indeks kristalinitas selulosa mikrokristal dapat dilihat pada Lampiran L2.5.
4.3.3 Identifikasi Morfologi SEM Selulosa Mikrokristal
a b
[image:32.595.150.508.85.431.2]
c d
Gambar 4.2 SEM dengan perbesaran 500 X(a) selulosa TKS, (b)α- selulosa,(c) selulosa mikrokristal pada HCl 2,5 N 75 °C,
(d) selulosa mikrokristal pada HCl 2 N 70 °C
yaitu selulosa mikrokristal pada HCl 2 N 70 °C terlihat bahwa masih terdapat α -selulosa yang belum sempurna mengalami proses hidrolisis asam.
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Berdasarkan hasil penelitian yang telah dilakukan dapat diambil kesimpulan sebagai berikut :
1. Rendemen selulosa mikrokristal yang diperoleh dalam penelitian ini sebesar 50% .
2. Penggunaan konsentrasi HCl dan suhu hidrolisis terbaik yang menghasilkan selulosa mikrokristal yaitu pada konsentrasi HCl 2,5N pada 75°C dengan sifat-sifat fisikokimia yang sesuai dengan persyaratan British pharmacoea 2009 yaitu berbentuk serbuk halus dan berwarna putih, nilai pH 7, nilai zat larut air sebesar 0,2 % dan nilai susut pengeringan sebesar 1,57 %.
3. Hasil karakterisasi dengan menggunakan instrumen FTIR (Fourier Transform Infrared) menunjukkan bahwa serapan gugus fungsi OH
5.2 SARAN
Berdasarkan hasil penelitian yang telah dilakukan dapat disarankan : 1. Melakukan penelitian lebih lanjut terkait pengaruh suhu dan lama
reaksi hidrolisis terhadap karakteristik selulosa mikrokristal yang dihasilkan.
2. Pada saat melakukan pengujian organoleptik terhadap warna selulosa mikrokristal sebaiknya menggunakan instrument seperti lovibond
3. Menghitung rendemen α-selulosa dan selulosa mikrokristal
BAB II
TINJAUAN PUSTAKA
2.1 TANAMAN KELAPA SAWIT
Tanaman kelapa sawit (Elaeis guinensis) berasal dari Nigeria, Afrika Barat, pada kenyatannya tanaman kelapa sawit hidup subur di luar daerah asalnya, seperti Malaysia, Indonesia, Thailand, dan Papua Nugini. Bahkan mampu memberikan hasil produksi per hektar yang lebih tinggi.Indonesia merupakan penghasil utama minyak sawit [10]. Tanaman kelapa sawit merupakan tanaman monokotil tergolong kedalam famili Palmacea yang termasuk tanaman yang tingginya mencapai 24 meter, memiliki batas umur produktif relatif pendek 25 – 30 tahun dan setelah mencapai umur daur harus dilakukan peremajaan dengan tanaman muda. Kelapa sawit merupakan komoditas unggulan yang mempunyai kontribusi penting dalam pembangunan ekonomi pada umumnya, dan dalam pembangunan agro industri di Indonesia pada khususnya.Setelah terbukti perkebunan kelapa sawit menghasilkan keuntungan yang cukup tinggi sekitar 17.317.295 ton, banyak perusahaan asing ingin berinvestasi di bidang perkebunan kelapa sawit [10]. Industri minyak sawit merupakan kontributor penting dalam produksi di Indonesia dan memiliki prospek pengembangan yang cerah. Industri ini juga berkontribusi dalam pembangunan daerah, sebagai sumber daya penting untuk pengentasan kemiskinan melalui budidaya pertanian dan pemprosesan selanjutnya [11]
2.2 TANDAN KOSONG KELAPA SAWIT (TKKS)
Secara umum, limbah dari pabrik kelapa sawit terdiri atas tiga macam yaitu limbah cair, padat dan gas. Limbah padat yang berasal dari proses pengolahan berupa tandan kosong kelapa sawit (TKKS), cangkang atau tempurung, serabut atau serat, sludge atau lumpur dan bungkil [12].
Kelapa sawit menghasilkan limbah yang dapat memberikan manfaat yang besar bagi kehidupan, diantaranya sebagai pupuk organik dan sebagai arang aktif. Salah satu limbah padat industri kelapa sawit adalah tandan kosong kelapa sawit (TKKS).Tandan kosong sawit juga menghasilkan serat kuat sebagai bahan pengisi dalam produk serat berkaret, diantaranya jok mobil, matras dan papan komposit.Limbah padat mempunyai ciri khas pada komposisinya. Komponen terbesar dalam limbah padat tersebut adalah selulosa, disamping komponen lain meskipun lebih kecil seperti abu, hemiselulosa, dan lignin [1].
Tandan kosong kelapa sawit merupakan limbah utama berligniselulosa yang belum termanfaatkan secara optimal dari industri pengolahan kelapa sawit. Basis satu ton tandan buah segar akan dihasilkan minyak sawit kasar sebanyak 0,21 ton (21%), minyak inti sawit sebanyak 0,05 ton (0,5%) dan sisanya merupakan limbah dalam bentuk tandan kosong, serat dan cangkang biji yang masing – masing sebanyak 0,23 ton (23%), 0,135 ton (13,5%) dan 0,055 ton (5,5%). Selama ini pengolahan/pemanfaatan tandan kosong kelapa sawit oleh Pabrik Kelapa Sawit (PKS) masih sangat terbatas yaitu dibakar dalam incinerator, ditimbun (open dumping), dijadikan mulsa diperkebunan kelapa sawit, atau diolah menjadi kompos. Namun karena adanya beberapa kendala seperti waktu pengomposan yang cukup lama sampai 6 – 12 bulan, fasilitas yang harus disediakan, dan biaya pengolahan tandan kosong kelapa sawit tersebut. Maka cara – cara tersebut kurang diminati oleh PKS. Selain jumlah yang melimpah juga karena kandungan selulosa tandan kelapa sawit yang cukup tinggi yaitu sebesar 45% maka tandan kosong kelapa sawit berpotensi untuk dikembangkan menjadi barang yang lebih berguna [13].
limbahnya. Langkah tersebut merupakan upaya untuk mengurangi dampak negatif demi mewujudkan industri yang berwawasan lingkungan. Salah satu pemanfaatan limbah dari PKS adalah pemanfaatan limbah sebagai pupuk, seperti limbah padat dapat berupa janjangan kosong (TKKS).Hasil samping dari industri perkebunan kelapa sawit seluruhnya dapat dimanfaatkan jika para pelaku industri ini mampu mengelolanya dengan baik [5].Tandan kosong kelapa sawit mencapai 23% dari jumlah pemanfaatan limbah kelapa sawit sebagai alternatif pupuk organik yang akan memberikan manfaat lain dari sisi ekonomi [11]. Berdasarkan struktur TKKS yang terdiri dari berbagai macam serat (selulosa, hemiselulolsa, dan lignin) menunjukkan TKKS merupakan kumpulan jutaan serat organik yang memiliki kemampuan dalam menahan air yang ada disekitarnya, dan jumlah TKKS ini sangat melimpah.Tetapi belum dimanfaatkan secara baik oleh sebagian besar Pabrik Kelapa Sawit (PKS) di Indonesia.Pengolahan/pemanfaatan TKKS oleh PKS masih sangat terbatas [13]. Sehingga selain hanya dimanfaatkan sebagai bahan baku pembuatan pupuk, dapat dilakukan alternatif lainnya untuk memenuhi potensi tandan kosong kelapa sawit yang masih sangat terbatas pemanfaatannya maka tandan kosong kelapa sawit dapat dimanfaatkan sebagai bahan baku pembuatan selulosa mikrokristal.
Hasil penelitian yang dilakukan oleh Tjahjono Herawan dan Meta Rivani (2013), tandan kosong kelapa sawit seperti biomassa pada umumnya adalah sumber paling penting untuk bahan kimia, material dan produk bernilai lainnya. Salah satu jenis bahan kimia yang dapat dikembangkan dari tandan kosong kelapa sawit adalah selulosa mikrokristal [9].
2.3 SELULOSA
2.3.1 Struktur Selulosa
anhidroglukopiranosa yang tersambung dengan ikatan β-1,4-glikosidik membentuk suatu rantai makromolekul tidak bercabang. Setiap unit anhidroglukopiranosa memiliki tiga gugus hidroksil seperti yang terlihat pada Gambar 2.1. Selulosa mempunyai rumus empirik (C6H10O5)n dengan n ~ 1500 dan berat molekul ~ 243.000 [14].
Gambar 2.1. Struktur Selulosa [14]
Selulosa mengandung sekitar 50 - 90% bagian kristal dan sisanya amorf. Selulosa hampir tidak pernah ditemui dalam keadaan murni di alam, melainkan selalu berikatan dengan bahan lain seperti lignin dan hemiselulosa. Molekul selulosa merupakan mikrofibil dari glukosa yang terikat satu dengan lainnya membentuk rantai polimer yang sangat panjang. Adanya lignin serta hemiselulosa di sekeliling selulosa merupakan hambatan utama untuk menghidrolisis selulosa [14]. Sifat-sifat selulosa terdiri dari sifat fisika dan sifat kimia.Selulosa dengan rantai panjang mempunyai sifat fisik yang lebih kuat, lebih tahan lama terhadap degradasi yang disebabkan oleh pengaruh panas, bahan kimia maupun pengaruh biologis. Sifat fisik lain dari selulosa adalah [14] :
1. Dapat terdegradasi oleh hidrolisa, oksidasi, secara kimia maupun mekanis sehingga berat molekulnya menurun.
2. Tidak larut dalam air maupun pelarut organik, tetapi sebagian larut dalam larutan alkali.
3. Dalam keadaan kering, selulosa bersifat higroskopis, keras dan rapuh. Bila selulosa banyak mengandung air maka akan bersifat lunak.
Turunan selulosa telah digunakan secara luas dalam sediaan farmasi seperti etil selulosa, metil selulosa, karboksimetil selulosa, dan dalam bentuk lainnya yang digunakan dalam sediaan oral, topikal, dan injeksi.Sebagai contoh, karboksimetil selulosa merupakan bahan utama dari SeprafilmTM, yang digunakan untuk mencegah adesi setelah pembedahan.Baru-baru ini, penggunaan selulosa mikrokristal dalam emulsi dan formulasi injeksi semipadat telah dijelaskan. Penggunaan bentuk-bentuk selulosa dalam sediaan disebabkan sifatnya yang inert dan biokompatibilitas yang sangat baik pada manusia [14].
2.3.2 Selulosa Mikrokristal
[image:40.595.217.411.515.604.2]Selulosa mikrokristal adalah selulosa yang dimurnikan secara parsial, berwarna putih, serbuk kristal yang terdiri atas partikel-partikel yang menyerap. Selulosa mikrokristal secara komersial tersedia dalam berbagai ukuran partikel dan tingkat kelembapan sehingga mempunyai sifat dan penggunaan yang berbeda. Selulosa mikrokristal secara luas digunakan dalam farmasi, terutama sebagai pengikat/pengisi dalam formulasi tablet dan kapsul yang dapat digunakan dalam proses granulasi basah dan kempa langsung. Selain digunakan sebagai pengikat/pengisi, selulosa mikrokristal juga mempunyai sifat lubrikan dan disintegran yang dapat berguna dalam pentabletan [15].Struktur selulosa mikrokristaldapat dilihat pada Gambar 2.2.
Gambar 2.2. Struktur Selulosa Mikrokristal [15].
Selulosa mikrokristal telah dibuat dari beberapa sumber alam, seperti dari
mikrokristal memiliki rumus molekul (C6H10O5)n, dimana n ~ 220, dengan berat molekul: ~ 32.400 [15].
Selulosa dapat larut segera dalam asam pekat.Pelarutan dalam asam pekat mengakibatkan pemecahan rantai selulosa secara hidrolitik.Oleh karena itu, selulosa mikrokristal dapat dihasilkan dengan mereaksikan selulosa di dalam larutan asam mineral yang mendidih selama waktu tertentu. Proses tersebut bertujuan untuk menurunkan berat molekul, derajat polimerisasi, dan panjang rantai selulosa sehingga membentuk mikrokristal [3]. Selulosa mikrokristal dikenalkan pada tahun 1960-an dan digunakan sebagai pengikat, pengisi dalam tablet, penghilang lemak, stabilizer dalam industri makanan, komposit dalam kayu, industri plastik, dan kosmetik. Selulosa mikrokristal dianggap sebagai bahan tambahan terbaik untuk pembuatan tablet cetak langsung, bisa sebagai bahan pengisi, pengikat pada tablet dengan konsentrasi 20 % - 90 %, penghancur tablet dengan konsentrasi 5 % – 20 % [16].
Selulosa mikrokristal adalah bentuk selulosa dari bagian non serat yang telah terdepolimerisasi parsial dan dimurnikan, berwarna putih, berbentuk serbuk dan merupakan partikel berpori.Selulosa mikrokristal telah dikembangkan dalam berbagai aplikasi industri seperti edible fil, yogurt, dan khususnya sebagai penguat dan pengisi pada matrik polimer atau biokomposit [9].
2.4. PEMBUATAN SELULOSA MIKROKRISTAL
Pembuatan selulosa mikrokristal dari biomassa tandan kosong kelapa sawit dilakukan dengan mengisolasi selulosa yang terkandung dalam tandan kosong kelapa sawit. Kemudian, selulosa yang diperoleh disiolasi untuk
mendapatkan α-selulosa. α-selulosa kemudian diproses untuk memproduksi selulosa mikrokristal. Beberapa proses yang dapat digunakan untuk memproduksi selulosa mikrokristal, yaitu:
1. Proses hidrolisis asam
(HCl) atau asam sulfat (H2SO4). Larutan asam tersebut berfungsi untuk melarutkan selulosa amorf. Kondisi operasi yang dibutuhkan untuk menjalankan reaksi adalah suhu di atas 160°C. Terdapat beberapa kerugian dalam penggunaan metode konvensional, yaitu beroperasi pada suhu tinggi.Larutan asam yang bekerja pada temperatur atau tekanan tinggi berpotensi menimbulkan masalah korosi terhadap reaktor.Selain itu, membutuhkan larutan asam dalam jumlah besar untuk menghidrolisis selulosa. Sehingga, pada akhir proses reaksi akan menyisakan larutan asam dalam jumlah besar [17].
2. Proses kontak uap
Proses kedua untuk memperoleh selulosa mikrokristal dijelaskan dalam U.S.Pat.No.5,769,934 diproduksi dengan cara mengkontakkan selulosa dengan steam bertekanan pada temperature antara 180°C sampai 350°C selama waktu yang cukup untuk mecapai kondisi LODP (levelling-off degree of polymerization). Proses pengontakkan bertujuan untuk menghidrolisis selulosa dan menghilangkan lignin dan hemiselulosa. Uap jenuh secara terus menerus diumpankan ke dalam reaktor sampai mencapai tekanan 430 psig.Tekanan di dalam reaktor antara 390 psig (2,689 Pa) sampai 430 psig (2,965 Pa). Kelebihan dari proses ini adalah tidak membutuhkan larutan asam. Selulosa mikrokristal yang diproduksi dengan proses kontak berbentuk koloid [18].
3. Proses hidrolisis gas
4. Proses ekstruksi reaktif
Pembuatan selulosa mikrokristal dengan menggunakan proses ekstruksi reaktif menurut U.S.Pat.No.6,228,213, ekstruksi tahap pertama melibatkan natrium hidroksida (NaOH) yang dilakukan pada rentang temperatur 140°C sampai 170°C untuk menghilangkan senyawa kompleks lignocellulosic. Kemudian, tahap kedua yaitu dengan melibatkan larutan asam yang dilakukan pada suhu 140°C. Selulosa dan larutan asam direaksikan dalam screw conveyor.Screw conveyor terdiri atas screw dan barrel. Screw diputar sehingga
menghasilkan tekanan pada selulosa, kemudian selulosa bercampur dengan larutan asam membentuk selulosa mikrokristal. Kelebihan proses ini yaitu dapat dijalankan pada proses kontinyu untuk memproduksi selulosa mikrokristal dengan waktu reaksi lebih cepat dan dengan efisiensi yang baik. Dilihat dari segi produk, partikel selulosa mikrokristal yang dihasilkan kecil sehingga tidak membutuhkan perlakuan tambahan untuk memperkecil partikel [20].
5. Proses enzim
Proses enzim untuk menghasilkan selulosa mikrokristal, hidrolisis dilakukan dengan menggunakan enzim sebagai katalis. Enzim yang digunakan dihasilkan dari mikroba seperti enzim α-amylase yang dipakai untuk hidrolisis pati menjadi glukosa dan maltosa.Dalam hidrolisis selulosa, mikroba yang digunakan dapat berupa Trichoderma viride. Mikroba tersebut akan menghasilkan enzim endo-celullase yang dapat memutus bagian amorf α-cellulose secara selektif. Kondisi operasi yang disarankan dalam proses ini adalah 50-60°C dan pH 2,5 - 3. Proses ini memiliki beberapa kelebihan yaitu, hidrolisis dengan enzim lebih bersih dan prosesnya lebih selektif, bekerja pada tekanan dan temperatur yang sedang. Namun, proses hidrolisis dengan menggunakan enzim terjadi secara lambat dengan waktu reaksi sekitar 24 sampai 48 jam. Ditinjau dari waktu reaksi, proses ini tidak cocok untuk aplikasi secara komersial [21].
karena waktu reaksi berlangsung singkat daripada proses lainnya dan jumlah larutan asam yang digunakan sedikit [22].
Pemilihan metode hidrolisis asam untuk pembuatan selulosa mikrokristal dalam penelitian ini juga di dukung oleh beberapa penelitian sebelumnya yang menggunakan metode yang sama dalam pembuatan selulosa mikrokristal yaitu proses hidrolisis asam, dimana asam yang digunakan adalah asam klorida (HCl).
Hasil penelitian yang telah dilakukan sebelumnya oleh Gusrianto,dkk (2011) dengan judul Preparasi dan Karakteristik Mikrokristalin Selulosa dari Limbah Serbuk Kayu Pengergajian dengan menggunakan metode hidrolisis asam yaitu asam klorida (HCl) menghasilkan selulosa mikrokristal sebesar 33 % [3].
Hasil penelitian lainnya yang telah dilakukan oleh Zulharmita,dkk (2012) Pembuatan Mikrokristalin Selulosa dari Ampas Tebu(Saccharum officinarum L) dengan menghidrolisis alfa selulosa dengan HCl 2,5 N sebanyak 1,2 liter didapatkan selulosa mikrokristal sebanyak 71,5 gram (28,6 %) [23]. Sedangkan Hasil penelitian yang telah dilakukan oleh Halim,dkk (2002) pada Pembuatan Mikrokristalin Selulosa dari Jerami Padi (Oriza sativa linn) dengan Variasi Waktu
Hidrolisa, α-selulosa yang diperoleh dari Jerami Padi dihidrolisa dengan HCl 2,5 N pada temperatur 100°C waktu hidrolisa divariasikan selama 1, 1,5, 2 dan 2,5 jam. Selulosa mikrokristal yang dihasilkan sekitar 40 % dengan hasil terbaik lama proses hidrolisa selama 1,5 jam [6].
2.4.1 Metode Hidrolisis Asam
[image:44.595.189.445.635.728.2]Hidrolisis selulosa dipengaruhi oleh konsentrasi asam yang digunakan. Bagian amorf dari suatu rantai selulosa lebih mudah dihidrolisis dengan asam daripada dalam bentuk kristal. Prosedur khas yang dilakukan adalah menghidrolisis selulosa murni dengan asam kuat dalam kondisi temperatur, pengadukan, dan waktu yang terkendali. Proses kimia dimulai dengan penghilangan ikatan antar polisakarida pada permukaan serat selulosa dan diikuti dengan pecah dan rusaknya bagian amorf sehingga melepaskan bagian kristal selulosa. Setelah hidrolisis dilakukan, suspensi yang dihasilkan diencerkan dengan air, dan dicuci dengan beberapa kali. Jenis asam mineral yang digunakan dalam tahap hidrolisis memiliki pengaruh besar pada sifat permukaan kristal selulosa [15].
Metode hidrolisis selulosa dengan menggunakan asam merupakan metode yang sering digunakan untuk menghilangkan bagian amorf dari selulosa tetapi penggunaan larutan asam masih terbatas hanya dilakukan dalam skala laboratorium. Dari hasil penelitian yang dilakukan Daniel,dkk (2006) ada beberapa faktor yang dapat mempengaruhi hidrolisis selulosa mikrokristal antara lain : konsentrasi awal/jumlah dari selulosa mikrokristal, konsentrasi asam yang digunakan, waktu dan temperatur hidrolisis [24].
2.5 ANALISIS SELULOSA MIKROKRISTAL 2.5.1 Sifat- Sifat Fisikokimia Selulosa Mikrokristal a. Pengujian Organoleptik
Pengujian organoleptik adalah pengujian yang didasarkan pada proses pengindraan. Pengindraan diartikan sebagai suatu proses fisio-psikologis, yaitu kesadaran atau pengenalan alat indra akan sifat-sifat benda karena adanya rangsangan yang diterima alat indra yang berasal dari benda tersebut. Karakteristik bentuk yaitu sampel diletakan di atas dasar yang berwarna putih, diamati bentuk atau rupa dan warna [23].
b. Uji pH
berbagai studi kimia dan biologi di laboratorium dan berbagai bidang industri [25].
c. Zat Larut Dalam Air
Zat larut dalam air adalah kemampuan suatu zat kimia tertentu, zat terlarut (solute), untuk larut dalam suatu pelarut (solvent) [25].
d. Susut Pengeringan
Pengeringan (drying) zat padat berarti pemisahan sejumlah kecil air atau zat cair lain dari bahan padat. Persentase susut pengeringan dapat ditentukan dengan perbandingan berat sampel dengan berat setelah dikeringkan [25]. Kemudian dihitung susut pengeringan dengan rumus [23] :
X = (B−A)−(C−A)
(B−A) × 100% (2.1)
X = Susut pengeringan (g) A = Berat krus kosong (g)
B = Berat krus + sampel sebelum dikeringkan (g) C = Berat krus + sampel setelah dikeringkan (g)
2.5.2 Karakteristik Selulosa Mikrokristal
a. Pengujian Fourier Transform Infrared (FTIR)
Spektroskopi Fourier Transform Infrared (FTIR) merupakanspektroskopi inframerah yang dilengkapi dengan transformasi fourier untuk deteksi dan analisis hasil spektrumnya.Intispektroskopi FTIR adalah interferometer Michelson yaitu alat untuk menganalisisfrekuensi dalam sinyal gabungan [26].
Pada analisa ini, sinar inframerah ditembakkan pada sampel.Sebagian radiasi inframerah diabsorbsi oleh sampel dan sebagian lainnya ditransmisikan. Hasil spektrum memperlihatkan absorbs dan transmisi molekul, membentuk sidik jari molekul sampel [27].
b. X-Ray Diffraction (XRD)
tersebut saling menguatkan. Sinar-X dihamburkan oleh atom – atom dalam zat padat material. Ketika sinar-X jatuh pada kristal dari material maka akan terjadi hamburan ke segala arah yang bersifat koheren. Sifat hamburan sinar-X yang koheren mengakibatkan sifat saling menguatkan atau saling melemahkan pada paduan gelombang [28].
c. Pengujian Scanning Electron Microscopy (SEM)
BAB I
PENDAHULUAN
1.1. LATAR BELAKANG
Kandungan utama yang berpotensi untuk dijadikan sebagai bahan baku pembuatan selulosa mikrokristal yaitu bahan yang berserat dan memiliki kandungan selulosa cukup tinggi. Selulosa terdiri dari ikatan glukosa-glukosa yang tersusun dalam suatu rantai linear dimana C-1 pada setiap glukosa berikatan dengan C-4 pada glukosa selanjutnya [1]. Setiap bahan memiliki jumlah selulosa yang berbeda-beda. Semakin tinggi kandungan selulosa dalam biomassa, maka kemungkinan biomassa dijadikan sebagai bahan baku semakin besar.
Menurut Susanto (1998), tandan kosong kelapa sawit (TKKS) mengandung selulosa sebesar 36 – 42 %. Kandungan selulosa ini cukup tinggi untuk dijadikan sebagai bahan baku pembuatan selulosa mikrokristal. TKKS lebih dipilih dibandingkan dengan kayu keras dan kayu lunak karena sebagian besar kayu sudah menjadi bahan baku industri kertas, sehingga untuk menghindari kelangkaan bahan baku lebih dipilih TKKS. Pemilihan TKKS dibanding pelepah sawit, disebabkan oleh faktor usia tanaman kelapa sawit. Tanaman kelapa sawit memiliki umur yang cukup panjang untuk tetap produktif menghasilkan buah. Jika pelepah sawit dijadikan bahan bakuutama, kemungkinan mendapatkan pelepah sawit dari tanaman yang sudah tidak produktif kecil. Sedangkan untuk TKKS, akan tetap dihasilkan selama industri minyak kelapa sawit tetap beroperasi [2].
Microcrystalline cellulose (MCC) adalah bahan tambahan penting di bidang
farmasi, makanan, kosmetik, dan industri lainnya. Dalam bentuk serbuk, selulosa mikrokristal sering digunakan sebagai eksipien dalam pembuatan tablet terutama untuk tablet kompresi langsung. Pembuatan tablet dengan kompresi langsung semakin banyak dilakukan karena memiliki banyak keuntungan seperti: tidak menggunakan proses granulasi, memberikan ukuran partikel yang seragam, dan membuat tablet lebih stabil dalam waktu yang lama, serta menguntungkan dari segi ekonomi [4]
Toshkov et al (1976) menjelaskan tentang metode hidrolisis untuk memperoleh selulosa mikrokristal dengan kualitas baik yaitu dengan menggunakan hidrolisis asam. Proses reaksi hidrolisis selulosa dengan asam membentuk selulosa mikrokristal yang dilakukan dalam reaktor batch. Larutan asam tersebut berfungsi untuk melarutkan selulosa amorf.Kondisi operasi yang dibutuhkan untuk menjalankan reaksi adalah suhu di atas 160oC [5].
Selulosa dapat segera larut dalam asam pekat. Pelarutan dalam asam pekat mengakibatkan pemecahan rantai selulosa secara hidrolitik. Oleh karena itu, selulosa mikrokristal dapat dihasilkan dengan mereaksikan selulosa di dalam larutan asam yang mendidih selama waktu tertentu. Proses tersebut bertujuan untuk menurunkan berat molekul, derajat polimerisasi, dan panjang rantai selulosa sehingga membentuk mikrokristal [4]. Larutan asam yang dapat digunakan adalah asam klorida (HCl) atau asam sulfat (H2SO4).
Saat ini telah banyak penelitian yang berkaitan dengan pembuatan selulosa mikrokristal, seperti yang dilakukan Muhammad (2015) dengan metode hidrolisis asam yaitu asam klorida (HCl) dengan menggunakan variasi konsentrasi HCl 2N, 2,5N, dan 3 N dan hasil optimum diperoleh pada konsentrasi HCl 3 N dengan tingkat kristalinitas tertinggi 61,6 % [7]. Hasil penelitian lainnya yang telah dilakukan oleh Tjahjono dkk (2013) menggunakan metode hidrolisis asam yaitu asamklorida (HCl) dengan tingkat kristalinitas tertinggi 71,43 % [9].
Berdasarkan uraian di atas, maka perlu dilakukan kajian pengaruh variasi konsentrasi asam klorida (HCl) dan suhu hidrolisa terhadap sifat selulosa mikrokristal yang dihasilkan.
1.2.1 PERUMUSAN MASALAH
Perumusan masalah dalampenelitian iniadalah bagaimana pengaruh konsentrasi HCl dan suhu hidrolisis terhadap sifat-sifat fisikokimia dan karakteristik selulosa mikrokristal yang dihasilkan dari selulosa tandan kosong kelapa sawit.
1.3 TUJUAN PENELITIAN
Tujuan penelitian adalah untuk menentukan konsentrasi HCl dan suhu hidrolisis yang paling sesuai dalam menghasilkan selulosa mikrokristal yang berasal dari selulosa tandan kosong kelapa sawit dengan sifat-sifat fisikokimia dan karakteristik yang paling baik.
1.4 MANFAAT PENELITIAN
1.5 RUANG LINGKUP PENELITIAN
Penelitian ini dilaksanakan di Laboratorium Penelitian, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatra Utara, Medan. Ruang lingkup dalam penelitian ini adalah sebagai berikut:
a. Bahan Penelitian
Bahan utama yang digunakan dalam penelitian ini, yaitu:
- Selulosa dari Tandan Kosong Kelapa Sawit (Elaeis guineensis) yang diperoleh dari Pusat Penelitian Kelapa Sawit, Jl.Brigjen Katamso No.51 Medan.
- Asam klorida (HCl) b. Variabel penelitian
Variabel tetap
- Waktu hidrolisa 15 menit [3]
Variabel berubah:
- Konsentrasi HCl:2 N ; 2,5 N ; 3 N ; 3,5 N [7] - Suhu hidrolisis : 65 °C, 70 °C, 75 °C, 80°C [3]
c. Analisis yang dilakukan dalam penelitian ini meliputi sifat-sifat fisikokimia yaitu pemeriksaan organoleptik, uji pH, zat larut dalam air, susut pengeringan, serta karakterisasi yang terdiri dari pengujian Fourier Transform Infrared (FTIR), X-Ray Diffraction( XRD) dan Scanning
ABSTRAK
Penelitian tentang kajian penyediaan selulosa mikrokristal dari selulosa tandan kosong kelapa sawit (Elaesis guineensis) dengan metode hidrolisis menggunakan asam klorida (HCl) bertujuan untuk menentukan konsentrasi HCl dan suhu hidrolisis yang paling optimum dalam menghasilkan selulosa mikrokristal. Pembuatan selulosa mikrokristal terdiri dari dua tahap yaitu alkalisasi dan hidrolisis asam. Tahap alkalisasi dilakukan dengan merendam selulosa tandan kosong kelapa sawit dengan larutan NaOH 17,5% untuk menghasilkan α-selulosa, selanjutnya tahap hidrolisis asam dengan menghidrolisis α-selulosa pada berbagai konsentrasi HCl yaitu 2 N, 2,5 N, 3 N dan 3,5 N dengan variasi suhu hidrolisis yaitu 65°C, 70°C, 75°C dan 80°C untuk menghasilkan selulosa mikrokristal. Analisis yang dilakukan meliputi sifat-sifat fisikokimia melalui pengamatan organoleptik, uji pH, susut pengeringan, dan zat larut dalam air serta karakterisasi dengan menggunakan instrumen Fourier Transform Infrared (FTIR), X-Ray Diffraction (XRD) dan Scanning Electron Microscopy (SEM) yang masing-masing dilakukan untuk mengetahui struktur molekul, indeks kristalinitas dan morfologi selulosa mikrokristal yang dihasilkan. Pada penelitian ini diperoleh kondisi optimum selulosa mikrokristal yang dihasilkan pada proses hidrolisis yaitu pada konsentrasi HCl 2,5 N suhu 75°C dengan sifat fisikokimia sebagai berikut : berbentuk serbuk halus dan berwarna putih, nilai pH 7, nilai zat larut dalam air 0,2%, nilai susut pengeringan 1,57% dan indeks kristalinitas sebesar 72,9% dan telah memenuhi persyaratan British Pharmacopeia 2009. Hasil karakterisasi dengan menggunakan instrumen FTIR (Fourier Transform Infrared) menunjukkan bahwa serapan gugus fungsi OH pada selulosa mikrokristal mengalami penurunan atau semakin rendah (3340cm-1) jika dibandingkan dengan serapan gugus fungsi OH pada selulosa TKKS dan α-selulosa. Serta terdapat regangan CH2 dari kelompok metoksil aromatik yang terdapat dalam selulosa mikrokristal mengalami peningkatan absorbansi. Hasil XRD menunjukkan bahwa selulosa mikrokristal berbentuk kristal dengan ditandai dua puncak maksimum yang relatif lebih tajam yaitu berada pada sudut (2θ) 20° dan 22°. Indeks kristalinitas selulosa mikrokristal pada konsentrasi 2,5 N pada 75°C adalah sebesar 72,9%. Sementara itu hasil SEM menunjukkan ukuran mikrofibril dari α -selulosa menjadi -selulosa mikrokristal menjadi semakin kecil.
THE STUDY OF PROVISION MICROCRYSTALLINE CELLULOSE FROM OIL PALM EMPTY FRUIT BUNCHES (Elaesis guineensis) BY HYDROLYSIS
METHOD USING HYDROCHLORIC ACID (HCL)
ABSTRACT
Research on the study of provision microcrystalline cellulose from oil palm empty fruit bunches (Elaesis guineensis) by hydrolysis method using hydrochloric acid (HCl) aims to determine the concentrations of HCl and most optimum temperature hydrolysis in producing microcrystalline cellulose. Making the microcrystalline cellulose is composed of two phases, they are alkalization and acid hydrolysis. Alkalization stage is done by soaking cellulose oil palm empty fruit bunches with 17.5% NaOH solution to produce α-cellulose, then acid hydrolysis stage is done by hydrolyzed α-cellulose with various concentrations HCl such as 2 N, 2,5 N, 3 N and 3,5 N and various temperature such as 65°C, 70°C, 75 °C and 80°C to produce microcrystalline cellulose. Analysis was conducted on the physicochemical properties through observation organoleptic, pH test, drying on loss, and substances soluble in water and characterization usingthe instrument such as Fourier Transform Infrared (FTIR), X-ray Diffraction (XRD) and Scanning Electron Microscopy (SEM) each conducted to determine the molecular structure, crystallinity index and morphology of microcrystalline cellulose produced. In this research, the optimum conditions resulting microcrystalline cellulose hydrolysis process is at concentration of HCl 2,5N 75 temperature which has characteristics such as powder form of fine and white, the pH value of 7, the value of water-soluble substances 0,2%, the value of drying shrinkage of 1,57% and has met the requirements of the British Pharmacopeia 2009. The result of characterization with FTIR shows that absorbance of OH group function at microcrystalline cellulose decrease or lower (3340 cm-1) than two other samples. Then there is CH2 streching from metoxcil aromatic group at microcrystalline cellulose also having decrease absorbance value. The result of XRD shows that microcrystalline cellulose is really crystal phase was indicated by two peaks which is relative sharper than two other samples exactly at angle (2θ) 20° and 22°. Crystallinity index of microcrystalline cellulose at concentration HCl 2,5 N 75 °C are 72.9%, meanwhile the resulf of SEM shows that microfibril size from microcrystalline cellulose has been changed to smaller than two other samples.
KAJIAN TERHADAP PENYEDIAAN
SELULOSAMIKROKRISTAL DARI SELULOSA
TANDAN KOSONG KELAPA SAWIT ( Elaeis
guineensis) DENGAN METODE HIDROLISIS
MENGGUNAKAN ASAM KLORIDA (HCl)
SKRIPSI
Oleh :
VERONICHA
130425018
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
KAJIAN TERHADAP PENYEDIAAN
SELULOSAMIKROKRISTAL DARI SELULOSA
TANDAN KOSONG KELAPA SAWIT ( Elaeis
guineensis) DENGAN METODE HIDROLISIS
MENGGUNAKAN ASAM KLORIDA (HCl)
SKRIPSI
Oleh :
VERONICHA
130425018
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PERNYATAAN KEASLIAN SKRIPSI
Saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul:
KAJIAN TERHADAP PENYEDIAAN SELULOSA MIKROKRISTAL DARI SELULOSA TANDAN KOSONG KELAPA SAWIT
(Elaseis guineensis) DENGAN METODE HIDROLISIS MENGGUNAKAN ASAM KLORIDA (HCl)
yang dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini adalah hasil karya saya kecuali kutipan-kutipan yang telah saya sebutkan sumbernya.
Demikian pernyataan ini diperbuat, apabila dikemudian hari terbukti bahwa karya ini bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima sanksi sesuai dengan aturan yang berlaku.
Medan, Januari 2017
PENGESAHAN
Skripsi dengan judul :
KAJIAN TERHADAP PENYEDIAAN SELULOSA MIKROKRISTAL DARI SELULOSA TANDAN KOSONG KELAPA SAWIT
(Elaeis guineensis) DENGAN METODE HIDROLISIS MENGGUNAKAN ASAM KLORIDA ( HCl )
dibuat sebagai kelengkapan persyaratan untuk mengikuti ujian skripsi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini akan telah diujikan pada sidang ujian skripsi pada 27 Januari 2017 dan dinyatakan memenuhi syarat/sah sebagai skripsi pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara.
Mengetahui, Medan,
Koordinator Skripsi Dosen Pembimbing
Ir. Renita Manurung, M.T
NIP. 19681214 199702 2 002 NIP. 19730408 199802 2 002 Dr. Halimatuddahliana, S.T.,M.Sc
Dosen Penguji I Dosen Penguji II
Dr. Maulida, S.T., M.Sc
PRAKATA
Puji dan syukur penulis ucapkan kehadirat Allah SWT atas rahmat-Nya sehingga hasil penelitian ini dapat terselesaikan dengan baik.
Selama mengerjakan hasil penelitian ini penulis banyak menerima bantuan, bimbingan, dan dukungan dari berbagai pihak. Oleh karena itu, Penulis mengucapkan terimakasih sebesar-besarnya kepada :
1. Ibu Dr. Halimatuddahliana, S.T.,M.Sc sebagai dosen pembimbing yang telah membimbing dan memberikan arahan, masukan dan saran selama menyelesaikan hasil penelitian ini.
2. Ibu Dr. Maulida, S.T.,M.Sc. selaku dosen penguji yang telah memberikan saran dan masukan yang membangun dalam penulisan skripsi ini.
3. Bapak M. Hendra S.Ginting, S.T.,M.T. selaku dosen penguji yang telah memberikan saran dan masukan yang membangun dalam penulisan skripsi ini.
4. Bapak Dr. Eng. Ir. Irvan, M.Si., selaku ketua Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
5. Ibu Ir. Renita Manurung, M.T selaku koordinator penelitian yang telah banyak memberikan pengarahannya.
6. Seluruh dosen pengajar Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara yang telah memberikan ilmu kepada penulis selama menjalani studi.
7. Teman-teman angkatan 2013 ekstensi Teknik Kimia yang memberikan dukungan dan semangat kepada penulis.
Semoga laporan penelitian ini dapat bermanfaat bagi kita semua serta bagi perkembangan ilmu pengetahuan khususnya ilmu teknik kimia.
Medan, Januari 2017 Penulis
DEDIKASI
RIWAYAT HIDUP PENULIS
Nama: Veronicha NIM: 130425018
Tempat/tgl lahir: Banda Aceh, 08 Oktober 1992 Nama orang tua: Ruaida
Alamat orang tua:
Jl. Syahbuddin Yatim No. 71 labuhan-Belawan
Asal sekolah
• SD Swasta Wahidin Sudiro Husodo 1998 – 2004
• SMP Swasta Hang Tuah II Titipapan Medan 2004 – 2007
• SMA Negeri 16 Medan 2007 – 2010
• D3 Kimia Universitas Sumatera Utara 2010 – 2013 Beasiswa yang pernah diperoleh:
Beasiswa BIDIK MISI tahun 2010-2013 Pengalaman organisasi/kerja:
1. IMKAN USU periode 2011-2012 sebagai anggota Bidang Bakat dan Minat
2. IMISKA USU periode 2011-2012 sebagai anggota
3. UKMI AD-DAKWAH USU periode 2011-2012 sebagai anggota kajian komtemporer.
4. UKMI AL-FALAK periode 2011-2012 sebagai Sekretaris Departemen Keputrian
5. PEMA MIPA periode 2011-2012 sebagai Bendahara Umum.
6. Praktek Kerja Lapangan di Balai Riset dan Standardisasi Industri Medan tahun 2013
7. Kerja Praktek di PT. Multimas Nabati Asahan (MNA) tahun 2015 Artikel yang telah dipublikasikan dalam Jurnal/Pertemuan Ilmiah:
1. Preparation and Characterization of Cellulose Microcrystalline (MCC) From Fiber Bunch Palm Oil
ABSTRAK
Penelitian tentang kajian penyediaan selulosa mikrokristal dari selulosa tandan kosong kelapa sawit (Elaesis guineensis) dengan metode hidrolisis menggunakan asam klorida (HCl) bertujuan untuk menentukan konsentrasi HCl dan suhu hidrolisis yang paling optimum dalam menghasilkan selulosa mikrokristal. Pembuatan selulosa mikrokristal terdiri dari dua tahap yaitu alkalisasi dan hidrolisis asam. Tahap alkalisasi dilakukan dengan merendam selulosa tandan kosong kelapa sawit dengan larutan NaOH 17,5% untuk menghasilkan α-selulosa, selanjutnya tahap hidrolisis asam dengan menghidrolisis α-selulosa pada berbagai konsentrasi HCl yaitu 2 N, 2,5 N, 3 N dan 3,5 N dengan variasi suhu hidrolisis yaitu 65°C, 70°C, 75°C dan 80°C untuk menghasilkan selulosa mikrokristal. Analisis yang dilakukan meliputi sifat-sifat fisikokimia melalui pengamatan organoleptik, uji pH, susut pengeringan, dan zat larut dalam air serta karakterisasi dengan menggunakan instrumen Fourier Transform Infrared (FTIR), X-Ray Diffraction (XRD) dan Scanning Electron Microscopy (SEM) yang masing-masing dilakukan untuk mengetahui struktur molekul, indeks kristalinitas dan morfologi selulosa mikrokristal yang dihasilkan. Pada penelitian ini diperoleh kondisi optimum selulosa mikrokristal yang dihasilkan pada proses hidrolisis yaitu pada konsentrasi HCl 2,5 N suhu 75°C dengan sifat fisikokimia sebagai berikut : berbentuk serbuk halus dan berwarna putih, nilai pH 7, nilai zat larut dalam air 0,2%, nilai susut pengeringan 1,57% dan indeks kristalinitas sebesar 72,9% dan telah memenuhi persyaratan British Pharmacopeia 2009. Hasil karakterisasi dengan menggunakan instrumen FTIR (Fourier Transform Infrared) menunjukkan bahwa serapan gugus fungsi OH pada selulosa mikrokristal mengalami penurunan atau semakin rendah (3340cm-1) jika dibandingkan dengan serapan gugus fungsi OH pada selulosa TKKS dan α-selulosa. Serta terdapat regangan CH2 dari kelompok metoksil aromatik yang terdapat dalam selulosa mikrokristal mengalami peningkatan absorbansi. Hasil XRD menunjukkan bahwa selulosa mikrokristal berbentuk kristal dengan ditandai dua puncak maksimum yang relatif lebih tajam yaitu berada pada sudut (2θ) 20° dan 22°. Indeks kristalinitas selulosa mikrokristal pada konsentrasi 2,5 N pada 75°C adalah sebesar 72,9%. Sementara itu hasil SEM menunjukkan ukuran mikrofibril dari α -selulosa menjadi -selulosa mikrokristal menjadi semakin kecil.
THE STUDY OF PROVISION MICROCRYSTALLINE CELLULOSE FROM OIL PALM EMPTY FRUIT BUNCHES (Elaesis guineensis) BY HYDROLYSIS
METHOD USING HYDROCHLORIC ACID (HCL)
ABSTRACT
Research on the study of provision microcrystalline cellulose from oil palm empty fruit bunches (Elaesis guineensis) by hydrolysis method using hydrochloric acid (HCl) aims to determine the concentrations of HCl and most optimum temperature hydrolysis in producing microcrystalline cellulose. Making the microcrystalline cellulose is composed of two phases, they are alkalization and acid hydrolysis. Alkalization stage is done by soaking cellulose oil palm empty fruit bunches with 17.5% NaOH solution to produce α-cellulose, then acid hydrolysis stage is done by hydrolyzed α-cellulose with various concentrations HCl such as 2 N, 2,5 N, 3 N and 3,5 N and various temperature such as 65°C, 70°C, 75 °C and 80°C to produce microcrystalline cellulose. Analysis was conducted on the physicochemical properties through observation organoleptic, pH test, drying on loss, and substances soluble in water and characterization usingthe instrument such as Fourier Transform Infrared (FTIR), X-ray Diffraction (XRD) and Scanning Electron Microscopy (SEM) each conducted to determine the molecular structure, crystallinity index and morphology of microcrystalline cellulose produced. In this research, the optimum conditions resulting microcrystalline cellulose hydrolysis process is at concentration of HCl 2,5N 75 temperature which has characteristics such as powder form of fine and white, the pH value of 7, the value of water-soluble substances 0,2%, the value of drying shrinkage of 1,57% and has met the requirements of the British Pharmacopeia 2009. The result of characterization with FTIR shows that absorbance of OH group function at microcrystalline cellulose decrease or lower (3340 cm-1) than two other samples. Then there is CH2 streching from metoxcil aromatic group at microcrystalline cellulose also having decrease absorbance value. The result of XRD shows that microcrystalline cellulose is really crystal phase was indicated by two peaks which is relative sharper than two other samples exactly at angle (2θ) 20° and 22°. Crystallinity index of microcrystalline cellulose at concentration HCl 2,5 N 75 °C are 72.9%, meanwhile the resulf of SEM shows that microfibril size from microcrystalline cellulose has been changed to smaller than two other samples.
DAFTAR ISI
Halaman
PENGESAHAN ii
KATA PENGANTAR iii
ABSTRAK iv
ABSTRACT v
DAFTAR ISI vi
DAFTAR GAMBAR ix
DAFTAR TABEL xii
DAFTAR LAMPIRAN xiii
DAFTAR SINGKATAN xv
DAFTAR SIMBOL xvi
BABI PENDAHULUAN 1
1.1 LATAR BELAKANG 1
1.2 PERUMUSAN MASALAH 3
1.3 TUJUAN PENELITIAN 3
1.4 MANFAAT PENELITIAN 3
1.5 RUANG LINGKUP PENELITIAN 4
BAB II TINJAUAN PUSTAKA 5
2.1 TANAMAN KELAPA SAWIT 5
2.2 TANDAN KOSONG KELAPA SAWIT 6
2.3 SELULOSA 7
2.3.1 Struktur Selulosa 7
2.3.2 Selulosa Mikrokristal 9 2.4 PEMBUATAN SELULOSA MIKROKRISTAL 10 2.4.1 Metode Hidrolisis Asam 13 2.5 ANALISIS SELULOSA MIKROKRISTAL 13 2.5.1 Sifat-Sifat Fisikokimia Selulosa Mikrokristal 14
b. Uji pH 14
c. Zat Larut dalam Air 15
d. Susut Pengeringan 15
2.5.2 Karakteristik Selulosa Mikrokristal 15 a. Pengujian Fourier Transfrom Infrared (FTIR) 15 b. Pengujian X-Ray Diffraction (XRD) 15 c. Pengujian Scanning Electron Microscopy (SEM) 16
BAB III METODOLOGI PENELITIAN 17
3.1 WAKTU DAN TEMPAT PENELITIAN 17
3.2 ALAT DAN BAHAN 17
3.2.1 Alat 17
3.2.2 Bahan 18
3.3 PROSEDUR PERCOBAAN 18
3.3.1 Prosedur Isolasi α-Selulosa 18 3.3.2 Prosedur Pembuatan Selulosa 19 3.3.3 Perhitungan Rendemen Selulosa Mikrokristal 19
3.4 DIAGRAM ALIR PENELITIAN 20
3.4.1 Diagram Alir Isolasi α-Selulosa 20 3.4.2 Diagram Alir PembuatanSelulosa 21 3.5 PROSEDUR ANALISIS DAN KARAKTERISASI 22 3.5.1 Sifat-Sifat Fisikokima Selulosa Mikrokristal 22 a. Prosedur PengujianOrganoleptik 22
b. Prosedur Uji pH 22
c. Prosedur Za



![Gambar 3.1 Diagram Alir Pembuatan Selulosa Mikrokristal [23].](https://thumb-ap.123doks.com/thumbv2/123dok/1044285.634665/21.595.97.568.115.735/gambar-diagram-alir-pembuatan-selulosa-mikrokristal.webp)