SKRIPSI
KAJIAN METODE DETEKSI
BAKTERI PATOGEN PENYEBAB PENYAKIT ASAL PANGAN DI PUSAT RISET OBAT DAN MAKANAN BADAN POM RI
Oleh:
TRI OCTORA ANGELIA F24051927
2009
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
KAJIAN METODE DETEKSI
BAKTERI PATOGEN PENYEBAB PENYAKIT ASAL PANGAN DI PUSAT RISET OBAT DAN MAKANAN BADAN POM RI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
TRI OCTORA ANGELIA F24051927
2009
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
Tri Octora Angelia. F24051927. Kajian Metode Deteksi Bakteri Patogen Penyebab Penyakit Asal Pangan di Pusat Riset Obat dan Makanan Badan POM RI. Di bawah bimbingan Ratih Dewanti-Hariyadi dan Winiati P. Rahayu.
RINGKASAN
Mikroorganisme sering mencemari pangan dan deteksinya dapat dilakukan dengan metode konvensional dan metode cepat. Metode konvensional memerlukan waktu yang lama karena berbasiskan morfologi dan sifat biokimiawi, dan kadang-kadang memerlukan konfirmasi berdasarkan uji serologi. Metode cepat yang berbasiskan Polymerase Chain Reaction (PCR) dapat mengidentifikasi dengan cara memperbanyak DNA target pada patogen. Perbanyakan DNA tersebut dapat berlangsung dengan adanya fragmen oligonukleotida yang komplementer terhadap DNA target tersebut (primer), enzim DNA polimerase, deoksinukleotida, Mg2+, buffer dan thermal cycler. Deteksi patogen dalam pangan juga dilakukan oleh Pusat Riset Obat dan Makanan, Badan POM RI. Penelitian ini bertujuan untuk mempelajari uji serologi untuk konfirmasi Salmonella spp., metode deteksi berbasiskan DNA terhadap B. cereus dalam pangan, dan menetapkan limit deteksi B. cereus dalam nasi goreng.
Konfirmasi Salmonella spp. dilakukan dengan uji serologi antigen O dengan Slide Agglutination Test (SAT). Reaksi positif SAT adalah terbentuknya aglutinasi karena antigen dan antibodi saling mengkompleks. Deteksi B. cereus dengan amplifikasi gen penyandi enterotoksin T menggunakan real-time PCR. Isolat DNA yang digunakan sebagai DNA target dalam amplifikasi diperoleh dari tiga metode isolasi, yaitu metode pendidihan, metode dengan pelarut fenol:kloroform, dan metode dengan kit komersial. Isolat DNA yang sudah diamplifikasi, kemudian ditetapkan limit deteksinya berdasarkan threshold cycle (Ct) amplikon.
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
KAJIAN METODE DETEKSI
BAKTERI PATOGEN PENYEBAB PENYAKIT ASAL PANGAN DI PUSAT RISET OBAT DAN MAKANAN BADAN POM RI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
TRI OCTORA ANGELIA F24051927
Dilahirkan di Medan, 6 Oktober 1987 Tanggal lulus : 28 Agustus 2009
Menyetujui, Bogor, 7 September 2009
Dr. Ir. Ratih Dewanti-Hariyadi, MSc Prof. Dr. Winiati P. Rahayu Dosen Pembimbing I Dosen Pembimbing II / Lapang
Mengetahui,
Dr. Ir. Nurheni Sri Palupi, Msi
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 6 Oktober 1987 di Medan dari pasangan Hisar P. Samosir dan Tiodor Agustina Saragi. Kedua orangtua memberi penulis seorang kakak lelaki, dr. Andre Somba Gugun Samosir dan seorang kakak perempuan Andika Putri Listiawati, STP.
Pendidikan penulis dimulai dari TK Anging Mamiri, dilanjutkan ke SD Negeri Setia Mulya 1, SLTP Negeri 1 Cimahi, dan SMA Negeri 2 Cimahi. Kemudian penulis melanjutkan studi di Institut Pertanian Bogor Fakultas Teknologi Pertanian dengan mayor Ilmu dan Teknologi Pangan dan minor Perkembangan Anak.
i
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan yang Maha Pengasih. Kebaikan-Nya dan kekuasaan-Nya telah memberi penulis kemampuan untuk menyelesaikan skripsi ini.
Penulis juga ingin menyampaikan ungkapan terima kasih yang tulus kepada: 1. Mama dan Papa tersayang, Abang Andre sebagai panutanku, Kakak Andika Putri
sebagai pengaduanku.
2. Ibu Dr. Ir. Ratih Dewanti-Hariyadi, M.Sc sebagai pembimbing yang senantiasa menuntun dan mengarahkan penulis selama studi hingga memperoleh kelulusan ini.
3. Ibu Prof. Dr. Winiati P. Rahayu sebagai pembimbing yang memberi kesempatan magang bagi penulis di Pusat Riset Obat dan Makanan Badan POM RI dan memberi saran-saran untuk penelitian dan penyelesaian skripsi ini.
4. Ibu Siti Nurjanah, STP, M.Si sebagai penguji yang memberi masukan bagi penulis demi kelayakan skripsi ini.
5. Seluruh Dosen dan Staf Departemen Ilmu dan Teknologi Pangan (ITP) atas bantuan dan bimbingan yang diberikan kepada penulis selama menempuh pendidikan di Departemen ITP.
6. Saudara-saudara yang selalu mendukungku, Uda Ridwan beserta Inanguda, Abang Jon, Eda Ika beserta Nate dan Naomi, Nastry, dan Dian yang terkasih. Terima kasih atas doa kalian.
7. Golden Generation ITP 42 yang telah berjuang bersama-sama dalam menempuh studi di ITP. Yanka, Tiyu, Icha, Fahmi, Kamlit, Hesti, Galih, Dina, Ester, Tere senang dapat memiliki pengalaman dan mempelajari hal-hal baru bersama kalian. 8. Ntet, Nonk, Mpe, Ditol, Dini yang terus bersamaku dari awal berada di asrama
IPB hingga studi kita untuk strata-1 ini berakhir.
ii
10.Mike, Tiwi, Upik, dan Fauzan yang telah bersama-sama dengan penulis melaksanakan magang di Pusat Riset Obat dan Makanan, Badan POM.
11.Seluruh pihak yang telah membantu penulis hingga sampai di titik akhir Strata-1 ini.
Penulis menyadari kekurangan ataupun kesalahan tak lekang dari skripsi ini. Oleh karena itu, penulis sangat menghargai dan mengharapkan kritik dan saran bagi skripsi ini. Semoga skripsi ini bermanfaat bagi kemajuan pendidikan dan perkembangan ilmu pengetahuan.
Bogor, 7 September 2009
iii
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... iii
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... viii
I. PENDAHULUAN ... 1
A.LATAR BELAKANG ... 1
B.TUJUAN ... 4
C.MANFAAT ... 4
II. TINJAUAN PUSTAKA ... 5
A.KEADAAN UMUM INSTANSI MAGANG ... 5
1. Sejarah dan Perkembangan Instansi ... 5
2. Lokasi dan Tata Letak Instansi ... 6
3. Visi dan Misi Instansi ... 6
4. Struktur Organisasi Instansi ... 6
B.KERACUNAN PANGAN ... 8
C.Bacillus cereus ... 9
D.Salmonella spp. ... 11
E. METODE DETEKSI KONVENSIONAL ... 14
F. METODE DETEKSI CEPAT (RAPID METHOD) BAKTERI PATOGEN DENGAN PCR ... 17
1. Tahap Pra-Amplifikasi Real-Time PCR ... 19
2. Pembacaan Produk Hasil Real-Time PCR ... 23
III. METODOLOGI PENELITIAN ... 27
A.TEMPAT DAN WAKTU MAGANG ... 27
B.LINGKUP KEGIATAN PENELITIAN ... 27
iv
1. Identifikasi Serovar Salmonella spp. ... 29
2. Metode Deteksi B. cereus Berbasiskan DNA ... 30
D.METODE PENELITIAN ... 31
1. Identifikasi Serovar Salmonella spp. ... 31
2. Metode Deteksi B. cereus Berbasiskan DNA ... 32
IV. HASIL DAN PEMBAHASAN ... 41
A. Identifikasi Serovar Salmonella spp. ... 41
B. Metode Deteksi B. cereus Berbasiskan DNA ... 45
1. Tahap Persiapan Sampel ... 45
2. Tahap Isolasi DNA ... 48
3. Tahap Amplifikasi ... 57
4. Evaluasi Kinerja Real-Time PCR ... 59
V. KESIMPULAN DAN SARAN ... 69
A.KESIMPULAN ... 69
B.SARAN ... 69
DAFTAR PUSTAKA ... 70
v
DAFTAR TABEL
Halaman
Tabel 1. Pembagian subgenus Salmonella berdasarkan karakteristik
biokimia ... 12 Tabel 2. Distribusi serovar dalam genus Salmonella pada tahun 2007 ... 13
Tabel 3. Data uji serologi antigen O dan motilitas... 41 Tabel 4 Data kurva standar dari metode isolasi pendidihan, ekstraksi dengan
fenol:kloroform, dan ekstraksi dengan kit komersial DNA ... 61 Tabel 5. Limit deteksi kultur murni B. cereus dan B. cereus dalam
vi
DAFTAR GAMBAR
Halaman Gambar 1a. Antisera ... 16
Gambar 1b. Visualisasi aglutinasi ... 16 Gambar 2. Grafik sigmoidal proses amplifikasi dengan real-time PCR
(Edwards et al., 2004). ... 23 Gambar 3. Kurva standar amplifikasi kultur murni dari enam tingkat
pengenceran dengan real-time PCR (Edwards et al., 2004) ... 24 Gambar 4. Melt curve yang memiliki sebuah puncak Tm ... 25 Gambar 5. Tahapan kerja pada identifikasi serovar Salmonella spp. ... 27 Gambar 6. Tahapan kerja pada uji amplifikasi DNA kultur murni
B. cereus ... 28 Gambar 7. Tahapan kerja pada uji amplifikasi DNA B. cereus dalam
nasi goreng ... 29 Gambar 8. Koloni tipikal B. cereus pada MYPA + Polymyxin B ... 46
Gambar 9a. Fase aqueous (atas), Interfase (tengah), dan Fase organik (bawah) dalam isolasi fenol:kloroform yang memiliki lapisan
interfase tebal ... 53 Gambar 9b. Fase aqueous (atas), Interfase (tengah), dan Fase organik
(bawah) dalam isolasi fenol:kloroform yang memiliki lapisan
interfase sangat tipis ... 53 Gambar 10a. Grafik amplifikasi DNA B. cereus hasil isolasi
metode pendidihan ... 60 Gambar 10b. Grafik amplifikasi DNA B. cereus hasil isolasi
metode dengan pelarut fenol:kloroform ... 60 Gambar 10c. Grafik amplifikasi DNA B. cereus hasil isolasi
vii
Gambar 10e. Kurva standar kultur murni B. cereus metode dengan pelarut
fenol:kloroform ... 60 Gambar 10f. Kurva standar kultur murni B. cereus metode dengan
kit komersial ... 60 Gambar 11a. Melt curve dari DNA yang diisolasi dengan metode pendidihan 67
Gambar 11b. Melt curve dari DNA yang diisolasi dengan metode ekstraksi
fenol:kloroform ... 66 Gambar 11c. Melt curve dari DNA yang diisolasi dengan metode ekstraksi
viii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Struktur organisasi Badan POM RI... 74
Lampiran 2. Prosedur pembuatan media TSB (Atlas, 2006) ... 75
Lampiran 3. Prosedur pembuatan media MYPA (Atlas, 2006) ... 76
Lampiran 4. Persiapan kultur bakteri (PROM Biotech, 2008) ... 77
Lampiran 5. Data jumlah koloni B. cereus dan konsentrasi kultur murni B. cereus ... 78
Lampiran 6. Isolasi DNA metode pendidihan (Hein et al., 2001 dengan modifikasi) ... 79
Lampiran 7. Isolasi DNA metode ekstraksi dengan fenol:kloroform (Sambrook et al., 1989 dengan modifikasi) ... 80
Lampiran 8. Isolasi DNA sesuai dengan panduan kit komersial ... 81
Lampiran 9. Penetapan Limit of Detection (LOD) Mikroba (PROM Biotech, 2008) ... 82
Lampiran 10. Uji motilitas Salmonella spp. ... 83
1
I. PENDAHULUAN
A. LATAR BELAKANG
Peristiwa keracunan pangan sering dilaporkan di media massa dan sering
pula diasumsikan sebagai penyakit ringan seperti sakit perut, mual, dan
muntah. Asumsi ini menyebabkan kajian dan penelusuran terhadap penyakit
asal pangan dengan gejala tersebut kurang mendapat perhatian dari
masyarakat, pemeriksaan kurang seksama dari pemerintah serta pihak terkait
bidang kesehatan. Hal ini terbukti dengan minimnya data dan laporan
mengenai Kejadian Luar Biasa (KLB) yang diperantarai pangan, padahal
pelaporan sangat penting untuk tindak lanjut investigasi keracunan pangan
dan untuk itu diperlukan pendeteksian dan pengidentifikasian penyebab
keracunan pangan.
Penanganan produk olahan pangan yang buruk dan konsumsi pangan
kurang matang biasanya menjadi penyebab utama keracunan pangan. Salah
satu contoh penyakit akibat keracunan pangan ialah Salmonellosis, hal ini
sering menjadi masalah kesehatan manusia yang disebabkan oleh bakteri
patogen Salmonella (Gast, 2003). Salmonellosis sangat mudah ditularkan dari
hewan ke manusia baik secara langsung ataupun melalui perantara seperti
produk makanan yang berasal dari hewan, tumbuhan, dan lingkungan.
Salmonellaenterica serovar Enteritidis merupakan salah satu penyebab utama
gastroenteritis.
Pangan yang berpeluang tinggi menyebabkan keracunan pangan ialah
pangan yang frekuensi konsumsinya tinggi dan dikonsumsi dalam jumlah
banyak. Pangan yang banyak dikonsumsi oleh penduduk Indonesia ialah nasi
(Deptan, 2009). Nasi selain sebagai sumber karbohidrat bagi manusia, juga
menjadi sumber nutrisi bagi mikroorganisme. Produk olahan nasi yang cukup
banyak diminati oleh penduduk Indonesia ialah nasi goreng. Selain itu, nasi
goreng yang digunakan biasanya berasal dari nasi sisa yang dibiarkan
semalam dan baru dimasak keesokan paginya. Hal ini rentan terhadap
kontaminasi bakteri patogen karena dibiarkan pada zona berbahaya (suhu
2 menganalisis dan menjamin keamanan pangan nasi goreng dari bahaya
mikrobiologi tersebut.
Bakteri patogen yang berkembang dengan baik pada substrat
berkarbohidrat tinggi salah satunya ialah Bacillus cereus (Supardi dan
Sukamto, 1992). Bakteri ini merupakan jenis bakteri Gram positif yang
memiliki peptidoglikan tebal dan mampu menghasilkan spora tahan panas
serta toksin ekstraseluler. Hal ini menyebabkan B. cereus masih mungkin
berkembang walaupun makanan telah dimasak. Jumlah B. cereus yang
mencapai 106 koloni per gram pangan telah mampu menyebabkan keracunan
pangan (USFDA, 2001).
Pendeteksian bakteri patogen dalam pangan pada umumnya dilakukan
dengan metode konvensional yang berbasiskan pada reaksi biokimia. Metode
konvensional memerlukan serangkaian uji, yaitu uji morfologi, uji biokimia,
dan perlu konfirmasi dengan uji serologi. Penetapan serovar melalui uji
serologi merupakan rangkaian pendeteksian Salmonella yang penting sebab
bakteri ini sangat beragam serotipenya. Selain itu, penetapan serovar sangat
membantu studi epidemiologi dan penelusuran sumber bakteri penyebab
penyakit asal pangan. Salah satu metode konvensional untuk menetapkan
serovar Salmonella adalah Slide Agglutination Test (SAT). Melalui uji ini
data kasus epidemiologi keracunan pangan di seluruh dunia dapat
diperbandingkan. Hal ini memakan waktu berhari-hari, padahal konsumsi
pangan terus berlangsung dan perlu tindakan cepat untuk mendeteksi bahaya
mikrobiologi dalam pangan. Oleh karena itu, dibutuhkan metode deteksi yang
mampu menganalisis faktor penyebab keracunan pangan secara cepat, tepat,
dan sensitif.
Metode deteksi terus mengalami perkembangan untuk melengkapi
ataupun mengatasi keterbatasan metode standar sebelumnya. Metode cepat
yang dalam dekade ini berkembang pesat ialah metode deteksi berbasiskan
DNA. Metode berbasiskan DNA memiliki spesifisitas terbaik dan sesuai
untuk mendeteksi patogen dalam pangan (de Boer dan Beumer, 1999).
Prinsip metode ini adalah hibridisasi antara DNA target dan fragmen
3 berbasiskan DNA dibedakan menjadi tiga, yaitu hibridisasi asam nukleat
dengan probe, amplifikasi dengan Polymerase Chain Reaction (PCR), dan
subtyping molekuler.
Amplifikasi DNA dengan PCR, dimana DNA spesifik dari bakteri
patogen diperbanyak mencapai jutaan kopi DNA sehingga tampak sebagai
pita DNA, dilanjutkan dengan deteksi elektroforesis gel agarosa. Namun,
proses amplifikasi dan deteksi yang terpisah ini dianggap berisiko terhadap
kontaminasi pita DNA dan kurang praktis. Oleh karena itu, dikembangkanlah
real-time PCR yang melangsungkan proses amplifikasi dan deteksi sekaligus
dalam sebuah instrumen.
Sensitivitas uji PCR yang tinggi sangat menguntungkan penelusuran
patogen penyebab keracunan pangan (misalnya B. cereus). Secara teoritis
hanya dengan satu molekul DNA dari bakteri dalam pangan, pendeteksian
patogen dapat dilakukan (Naravaneni dan Jamil, 2005). Di samping itu,
teknik ini fleksibel sehingga berkembang secara pesat disesuaikan dengan
kebutuhan analisis. Fleksibilitasnya memberikan keleluasaan bagi peneliti
dalam memodifikasi tahapan persiapan sampel hingga berupa isolat DNA.
Persiapan isolat DNA dan amplifikasi seringkali berbeda bagi setiap bakteri.
Hal ini dilakukan untuk memperoleh optimasi amplikon sehingga deteksi
B. cereus dalam pangan semakin sensitif, akurat, dan valid.
Preparasi isolat DNA sebelum amplifikasi menjadi tahapan penting agar
amplifikasi berjalan lancar. Isolasi DNA menjadi tahapan kritis setiap metode
berbasiskan DNA. Untuk memperoleh isolat DNA dengan kuantitas dan
kualitas yang baik, beragam metode isolasi DNA telah dikembangkan.
Beberapa metode yang digunakan untuk preparasi isolat DNA ialah metode
pendidihan, metode pelisisan dengan pelarut alkalin, dan metode ekstraksi
dengan fenol:kloroform. Metode isolasi DNA dengan fenol:kloroform paling
banyak digunakan untuk mengekstraksi DNA kromosomal dari sel
(Sambrook et al., 1989). Kemurnian isolat DNA berpengaruh besar terhadap
sensitivitas uji real-time PCR. Sensitivitas yang diperoleh dari real-time PCR
lebih tinggi dibandingkan PCR standar, yang ditunjukkan dengan angka limit
4 Hal yang menjadi tantangan dalam deteksi cepat ialah persiapan sampel
yang belum terstandarisasi. Untuk itu diperlukan pengembangan metode pada
tahap persiapan isolat DNA agar metode PCR menjadi metode analisa yang
lebih baik, lebih cepat serta lebih sensitif, dan selanjutnya metode tersebut
dapat divalidasi.
B. TUJUAN
Secara umum, kegiatan magang ini bertujuan untuk memperluas
wawasan, melatih sikap dan kemampuan teknis mahasiswa serta
mengaplikasikan ilmu selama magang di bidang keamanan pangan, Pusat
Riset Obat dan Makanan Badan POM RI. Tujuan khusus dari kegiatan
magang ini, antara lain:
1. Mengidentifikasi serovar Salmonella spp dengan metode deteksi
berbasiskan imunologi.
2. Mempelajari metode deteksi B. cereus berbasiskan DNA dengan
real-time PCR, mencakup tahap isolasi DNA dan amplifikasi.
3. Mengevaluasi limit deteksi dan spesifisitas uji B. cereus dari sampel
pangan nasi goreng.
C. MANFAAT
Manfaat yang dapat diperoleh dari kegiatan ini adalah:
1. Melengkapi data serovar Salmonella spp. yang tumbuh pada sampel
pangan dan data tersebut dapat dipergunakan untuk penelusuran sumber
penyebab kasus keracunan pangan yang mungkin disebabkan oleh genus
Salmonella.
2. Memberikan pengetahuan mengenai perkembangan metode deteksi cepat
dengan real-time PCR serta metode isolasi DNA yang dapat diterapkan
oleh laboratorium-laboratorium uji untuk mendeteksi bakteri patogen
5
II. TINJAUAN PUSTAKA
A. KEADAAN UMUM INSTANSI MAGANG
1. Sejarah dan Perkembangan Instansi
Kemajuan teknologi telah membawa perubahan-perubahan yang cepat
dan signifikan pada industri farmasi, obat asli Indonesia, makanan,
kosmetika dan alat kesehatan. Dengan menggunakan teknologi modern,
industri-industri tersebut kini mampu memproduksi dalam skala yang
sangat besar mencakup berbagai produk dengan range yang sangat luas.
Dengan dukungan kemajuan teknologi transportasi dan entry barrier
yang makin tipis dalam perdagangan internasional, maka produk-produk
tersebut dalam waktu yang amat singkat dapat menyebar ke berbagai
negara dengan jaringan distribusi yang sangat luas dan mampu
menjangkau seluruh strata masyarakat.
Konsumsi masyarakat terhadap produk-produk termaksud cenderung
terus meningkat, seiring dengan perubahan gaya hidup masyarakat
termasuk pola konsumsinya. Sementara itu pengetahuan masyarakat masih
belum memadai untuk dapat memilih dan menggunakan produk secara
tepat, benar dan aman. Di lain pihak, iklan dan promosi secara gencar
mendorong konsumen untuk mengkonsumsi secara berlebihan dan
seringkali tidak rasional.
Perubahan teknologi produksi, sistem perdagangan internasional dan
gaya hidup konsumen tersebut pada realitasnya meningkatkan risiko
dengan implikasi yang luas pada kesehatan dan keselamatan konsumen.
Apabila terjadi produk sub standar, rusak atau terkontaminasi oleh bahan
berbahaya maka risiko yang terjadi akan berskala besar dan luas serta
berlangsung secara amat cepat.
Untuk itu Indonesia harus memiliki Sistem Pengawasan Obat dan
Makanan (SisPOM) yang efektif dan efisien yang mampu mendeteksi,
mencegah dan mengawasi produk-produk termaksud untuk melindungi
keamanan, keselamatan dan kesehatan konsumennya baik di dalam
6 jaringan nasional dan internasional serta kewenangan penegakan hukum
dan memiliki kredibilitas profesional yang tinggi.
2. Lokasi dan Tata Letak Instansi
Badan POM RI terletak di Jalan Percetakan Negara No. 23, Jakarta
Pusat.
3. Visi dan Misi Instansi
Adapun Visi dan Misi dari Badan POM RI adalah :
a. Visi Badan POM RI
Obat dan Makanan terjamin aman, bermanfaat dan bermutu.
b. Misi Badan POM RI
Melindungi masyarakat dari Obat dan Makanan yang berisiko
terhadap kesehatan.
4. Struktur Organisasi Instansi
Badan POM RI ditetapkan berdasarkan Keputusan Presiden Nomor
166 Tahun 2000 tentang Kedudukan, Tugas, fungsi, Kewenangan,
Susunan Organisasi dan Tata Kerja Lembaga Pemerintah Non
Departemen, sebagaimana telah diubah dengan Keputusan Presiden
Nomor 173 tahun 2000. Pembentukan Badan POM RI ini ditindaklanjuti
dengan Keputusan Kepala Badan Pengawas Obat dan Makanan Nomor
02001/SK/KBADAN POM RI, tanggal 26 Februari tahun 2001, tentang
Organisasi dan Tata Kerja Badan Pengawas Obat dan Makanan setelah
mendapatkan persetujuan Menteri Negeri Pendayagunaan Aparatur Negara
Nomor 34/M.PAN/2/2001 tanggal 1 Februari 2001. Berikut ini adalah
struktur organisasi Badan POM:
a. Kepala Badan Pengawas Obat dan Makanan
b. Sekretariat Utama
c. Inspektorat
d. Deputi Bidang Pengawasan Produk Terapetik dan Narkotika,
7
e. Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk
Komplemen
f. Deputi Bidang Pengawasan Keamanan Pangan dan Bahan Berbahaya
g. Pusat Pengujian Obat dan Makanan Nasional
h. Pusat Penyidikan Obat dan Makanan
i. Pusat Riset Obat dan Makanan
j. Pusat Informasi Obat dan Makanan
k. Unit Pelaksana Teknis Badan POM
Struktur organisasi dalam bentuk skema dapat dilihat pada Lampiran 1.
Pusat Riset Obat dan Makanan, bagian dari struktur organisasi Badan
POM RI, merupakan tempat magang dipenuhi. Berikut ini adalah
penjelasan lebih lanjut mengenai sub-instansi ini:
a. Kedudukan
Pusat Riset Obat dan Makanan (PROM) adalah unsur pelaksana
tugas Badan POM RI yang berada di bawah dan bertanggung jawab
kepada Kepala Badan POM. Dalam pelaksanaan tugas sehari-hari
secara teknis dibina oleh Deputi dan secara administrasi dibina oleh
Sekretariat Utama. Pusat Riset Obat dan Makanan dipimpin oleh
seorang kepala pusat.
b. Tugas dan Fungsi
Sesuai dengan SK Kepala Badan POM RI No. 02001/KBADAN
POM RI tanggal 26 Februari 2001, Pusat Riset Obat dan Makanan
mempunyai tugas melaksanakan kegiatan di bidang riset toksikologi,
keamanan pangan dan produk terapetik.
Pusat Riset Obat dan Makanan menyelenggarakan fungsi :
1. Penyusunan rencana dan program riset Obat dan Makanan.
2. Pelaksanaan riset obat dan makanan.
3. Evaluasi dan penyusunan laporan pelaksanaan riset Obat dan
Makanan.
c. Susunan Organisasi
8 1) Bidang Toksikologi
2) Bidang Keamanan Pangan
3) Bidang Produk Terapetik
4) Kelompok Pejabat Fungsional
5) Sub Bagian Tata Usaha
d. Bidang Toksikologi
Bidang Toksikologi mempunyai tugas melaksanakan penyusunan
rencana dan program serta evaluasi dan penyusunan laporan
pelaksanaan riset toksikologi.
e. Bidang Keamanan Pangan
Bidang Keamanan Pangan mempunyai tugas melaksanakan
penyusunan rencana dan program serta evaluasi dan penyusunan
laporan pelaksanaan riset keamanan pangan.
f. Bidang Terapetik
Bidang Produk terapetik mempunyai tugas melaksanakan
penyusunan rencana dan program serta evaluasi dan penyusunan
laporan pelaksanaan riset produk terapetik.
g. Sub Bagian Tata Usaha
Sub Bagian Tata Usaha mempunyai tugas memberikan pelayanan
teknis dan administrasi di lingkungan Pusat Riset Obat dan Makanan.
B. KERACUNAN PANGAN
Pangan merupakan kebutuhan pokok manusia karena di dalamnya
terdapat zat-zat gizi yang penting bagi kehidupan. Zat-zat gizi tersebut
diperlukan untuk memulihkan dan memperbaiki jaringan tubuh yang rusak,
mengatur proses di dalam tubuh, perkembangbiakan, dan menghasilkan energi
untuk beraktivitas. Zat gizi yang dimaksud, antara lain: karbohidrat, protein,
lemak, vitamin dan beberapa mineral. Bahan pangan dengan komponen
tersebut juga merupakan medium yang baik untuk pertumbuhan mikroba.
Pertumbuhan mikroba dalam bahan pangan dipengaruhi oleh berbagai
faktor, seperti tersedianya nutrien, air, suhu, pH, oksigen, dan adanya zat
9 menguntungkan, tetapi juga dapat mendatangkan kerugian. Misalnya jika
kehadiran mikroba tersebut mengubah bau, rasa, dan warna yang tidak
dikehendaki; menurunkan berat atau volume; menurunkan nilai gizi/nutrisi;
mengubah bentuk dan susunan senyawa serta menghasilkan toksin yang
membahayakan di dalam pangan (Supardi dan Sukamto, 1999).
Pangan yang memiliki kandungan mikroba tertentu dapat menimbulkan
penyakit bila dikonsumsi. Menurut penyebabnya, penyakit yang ditimbulkan
oleh makanan dapat digolongkan dalam dua kelompok besar, yaitu keracunan
dan infeksi mikroba. Keracunan dapat terjadi karena tertelannya suatu racun
baik organik atau anorganik yang mungkin terdapat secara alamiah pada bahan
pangan, serta tertelannya toksin yang merupakan hasil metabolisme sel-sel
mikroba tertentu. Gejala keracunan karena toksin tersebut disebut intoksikasi.
Sedangkan tertelannya atau masuknya mikroba ke dalam tubuh, kemudian
menembus sistem pertahanan tubuh dan hidup serta berkembang biak di dalam
tubuh disebut infeksi (Supardi dan Sukamto, 1999).
Menurut Walderhaug (2007), patogen-patogen penyebab keracunan
pangan, antara lain: Salmonella spp., Staphylococcus aureus, Clostridium
perfringens, Bacillus cereus, Campylobacter sp., Shigella sp., Clostridium
botulinum, dan Escherichia coli. Salah satu bentuk kasus keracunan pangan
yang disebabkan oleh bakteri patogen ialah keracunan pangan yang menjadi
Kejadian Luar Biasa (KLB) di Amerika, Inggris, Kanada, dan Norwegia.
Bakteri penyebab KLB tersebut adalah Bacillus cereus yang terdapat pada nasi
putih dan nasi goreng (Supardi dan Sukamto, 1999). Agar KLB tersebut dapat
dicegah di Indonesia, diperlukan metode yang mampu mendeteksi bakteri
patogen tersebut pada sampel pangan secara sensitif, spesifik, akurat, dan cepat
untuk menjamin keamanan pangan.
C. Bacillus cereus
Bacillus cereus adalah bakteri pembentuk spora yang tergolong ke dalam
famili Bacillaceae. Spora B. cereus tahan terhadap panas dan radiasi. Bakteri
ini bersifat aerobik sampai anaerobik fakultatif, katalase positif, dan
10
B. cereus juga memproduksi enterotoksin dan metabolit-metabolit lainnya.
Tidak memproduksi indol, reaksi Voges-Proskauer positif, dapat
menggunakan sitrat sebagai sumber karbon, mereduksi nitrat, tidak
memproduksi urease dan penisilinase, dapat tumbuh secara anaerobik di
dalam media cair yang mengandung 1% glukosa, memproduksi asam dari
glukosa, sukrosa, maltosa dan gliserol, serta tahan terhadap lisozim (Supardi
dan Sukamto, 1999).
Jenis pangan yang sering ditumbuhi B. cereus terutama adalah daging,
nasi, sayuran, sosis, makaroni, dan kadang-kadang ikan, susu atau es krim.
Pangan penyebab keracunan umumnya mengandung sel B. cereus dalam
jumlah tinggi. Analisis mikrobiologi terhadap B. cereus pada agar darah
menunjukkan bahwa dari 17 KLB yang terjadi di Inggris tahun 1971-1976,
kandungan B. cereus pada nasi penyebab keracunan tersebut berkisar antara
3 x 105 – 2 x 109 CFU/g dengan rata-rata 5 x 107 CFU/g (Supardi dan
Sukamto, 1999). Konsumsi pangan yang mengandung lebih dari
106B.cereus/g (USFDA, 2001) sudah dapat menyebabkan keracunan pangan,
khususnya pada pangan yang dibiarkan saat preparasi tanpa dimasukkan ke
dalam lemari pendingin sebelum dihidangkan.
B. cereus tumbuh cepat apabila substratnya mengandung karbohidrat.
Sedangkan bila substratnya tidak mengandung karbohidrat, pertumbuhannya
akan sangat lambat dan tidak dapat membentuk toksin. B. cereus dapat
tumbuh secara baik pada media yang mengandung 0.025 M glukosa dan
mencapai maksimum setelah 4.5 jam (Supardi dan Sukamto, 1999). Produksi
toksin terjadi selama pertumbuhan logaritmik, dan mencapai maksimum
sampai glukosa di dalam medium habis dipecah oleh bakteri tersebut.
Galur B. cereus yang bersifat patogenik digolongkan ke dalam bakteri
penyebab intoksikasi dan dapat dibedakan atas dua grup berdasarkan sifat
patogeniknya, yaitu galur penyebab diare dan galur penyebab muntah. Galur
penyebab diare yang memproduksi enterotoksin dapat tumbuh pada berbagai
pangan dan mempunyai waktu inkubasi sejak tertelan sampai timbulnya
11 emetik mempunyai masa inkubasi lebih pendek, sekitar 1-5 jam (Supardi dan
Sukamto, 1999).
Galur B. cereus yang beragam tersebut dapat dibedakan berdasarkan gen
spesifik yang dimiliki masing-masing galur. Berdasarkan beberapa penelitian
terdapat beberapa gen spesifik yang terdapat pada B. cereus, antara lain: gen
penghasil cereulide (ces), sejenis toksin emetik (Fricker et al., 2007),
phosphotidyl inositol (PI-1) (Myers dan Sakelaris, 2004), gyrase (gyrB)
(Myers dan Sakelaris, 2004), enterotoksin non-hemolitik (Nhe) (Hansen dan
Hendriksen, 2001), sitotoksin (cytK) (Lund et al., 2000), hemolysin (hblA)
(Mantynen dan Lindstrom, 1998), dan enterotoksin T (BceT) (Mantynen dan
Lindstrom, 1998).
Target gen spesifik akan menentukan primer yang digunakan dalam uji
amplifikasi dengan PCR, target gen yang banyak digunakan ialah ces karena
toksin ini spesifik dihasilkan B. cereus emetik (Fricker et al., 2007). Berbeda
dengan sekuens gen 16S rRNA karena identik dengan beberapa bakteri lain,
termasuk B. anthracis. Keidentikan tersebut terlihat dari struktur primer 16S
rRNA Bacillus anthracis, Bacillus cereus, Bacillus mycoides, dan Bacillus
thuringiensis setelah ditetapkan dengan metode sekuensing dideoksi
transkripsi terbalik, hasilnya menunjukkan semua galur memiliki sekuens
serupa (tingkat kemiripannya lebih dari 99%) (Ash et al., 1991).
Penggunaan gen spesifik bersamaan dengan dye fluoresence pada
real-time PCR memberikan limit deteksi (LOD) B.cereus sebesar 101-103 cfu/g
sampel pangan tanpa tahap pre-enrinchment. Dengan pengkayaan, limit
deteksi dapat mencapai 100 cfu/g. Apabila metode isolasi DNA dengan
pendidihan saja, limit deteksi menjadi kurang sensitif (Fricker et al., 2007).
D. Salmonella spp.
Salmonella merupakan bakteri Gram negatif berbentuk batang yang tidak
membentuk spora, fakultatif anaerobik, mampu tumbuh pada pH mendekati
4.0-9.0 dengan pH optimum 7.0, dan termasuk dalam famili
Enterobacteriaceae. Bakteri ini berukuran 0.7-1.5 x 2-5 µm, motil dengan
12 yang tidak motil karena tidak mempunyai flagela. Bakteri ini tumbuh
optimum pada suhu 35-37°C, dapat mengkatabolisme bermacam karbohidrat
menjadi asam dan gas, menggunakan sitrat sebagai sumber tunggal karbon,
memproduksi H2S dan dapat mendekarboksilasi lysine menjadi kadaverin dan
ornithin menjadi putrescin. Salmonella dapat tumbuh pada kadar garam
maksimal 8% (Rusyanto, 2005).
Nama Salmonella pertama kali diberikan oleh Lignieres pada tahun 1990
sebagai penghormatan kepada seorang ahli bakteriologi Amerika Serikat
D.E. Salmon yang telah berhasil mengkarakterisasikan bakteri Bacillus
penyebab kolera pada babi dan memasukkannya dalam famili
Enterobacteriaceae. Taksonomi Salmonella pertama kali diperkenalkan oleh
White (1929) dan dimodifikasi oleh Kauffman (1934). Tahun 1966,
Kauffman mulai mengklasifikasikan 51 grup somatik Salmonella menjadi
4 sub genera dengan menggunakan karakteristik biokimia. Sub genus kelima
lalu ditambahkan setelah ditemukannya beberapa karakteristik yang berbeda.
Adapun karakteristik biokimia masing masing sub genus dapat dilihat pada
Tabel 1.
Tabel 1. Pembagian subgenus Salmonella berdasarkan karakteristik
biokimia*
Klasifikasi Karakteristik
Subgenus 1 Mampu menggunakan dulcitol, banyak berhubungan atau
ditemukan pada manusia atau hewan vertebrata berdarah panas. Isolasi frekuensinya sangat tinggi
Subgenus 2 Mampu menggunakan dulcitol dan malonat
Subgenus 3 Mampu menggunakan malonat dan
O-nitriphenyl-ß-D-galactopyranoside (ONPG)
Subgenus 4 Mampu tumbuh dalam KCN
Subgenus 5 Tidak dapat memetabolisme dulcitol, malonat, mampu
mengkatabolisme ONPG dan tumbuh dalam KCN
*Sumber: D’Aoust (2000)
Genus Salmonella terdiri dari dua spesies, yaitu S. enterica. dan
S. bongori. Spesies S. enterica masih dapat dikelompokkan lagi menjadi
enam subspesies, antara lain: S. enterica subsp. enterica, S. enterica subsp.
salamae, S. enterica subsp. arizonae, S. enterica subsp. diarizonae, S. enterica
subsp. houtenae, and S. enterica subsp. indica berdasarkan antigen (O)
somatik dan antigen (H) flagelar melalui serotyping. Distribusi spesies
13 Spesies dan subspesies dibedakan berdasarkan uji biokimia, serologi, dan
genetik (Mazumdar, 2008).
Tabel 2. Distribusi serovar dalam genus Salmonella pada tahun 2007*
Spesies Subspesies Jumlah serovar
Salmonellaenterica Enterica (I) 1531
Salamae (II) 505
Arizonae (IIIa) 99
Diarizonae (IIIb) 336
Houtenae (IV) 73
Indica (V) 13
Salmonellabongori (VI) 22
Total 2579
*Sumber: World Health Organization (WHO), 2009
Spesies terbanyak dari genus Salmonella adalah Salmonella enterica dan
subspesies terbanyak ialah subspesies enterica yang berjumlah 1531 serovar.
Angka romawi pada masing-masing subspesies, kecuali angka VI pada
spesies Salmonella bongori, digunakan untuk mempersingkat penamaan
serovar.
Pada tingkat genus diferensiasi Salmonella ke dalam spesies didasarkan
pada perbedaan reaksi bakteri terhadap antigen. Hingga tahun 2000 lebih dari
2500 serovar Salmonella telah teridentifikasi (D’Aoust, 2000). Skema yang
disepakati secara internasional untuk menetapkan serovar Salmonella hingga
saat ini ialah skema Kauffmann-White. Seluruh serotipe Salmonella
ditetapkan berdasarkan antigennya (Mazumdar, 2008).
Antigen O merupakan antigen karbohidrat bagian dari lipopolisakarida.
Gram negatif, salah satunya Salmonella, memiliki antigen O yang unik. Dan
antigen H tersusun dari subunit protein, disebut flagelin, yang membentuk
karakteristik flagela. Salmonella merupakan bakteri enterik yang unik karena
bakteri ini dapat mengekspresikan dua antigen flagela yang berbeda. Kedua
antigen flagela dikenal dengan antigen H fase 1 (monofasik) dan fase 2
(bifasik). Isolat dengan flagela monofasik hanya menunjukkan satu tipe
flagelin, sedangkan Salmonella bifasik memiliki fase 1 dan 2 pada antigen H.
Penentuan tipe bifasik dengan cara menginokulasi Salmonella pada media
inversi, yaitu media semi solid yang diberikan antisera positif dari fase 1.
14 meluasnya koloni ke tepi agar, sedangkan Salmonella monofasik tidak motil
sebab antibodi yang terdapat pada sera telah berikatan dengan antigen flagela
pada bakteri tersebut.
Salmonella merupakan bakteri patogen penyebab Salmonellosis. Gejala
klinis salmonellosis pada manusia terbagi menjadi demam tifoid dan non
tifoid. Demam tifoid atau disebut dengan demam enterik disebabkan infeksi
oleh galur tifoid atau paratyphi sehingga disebut salmonellosis tifoid. Demam
enterik dapat ditularkan atau disebarkan oleh individu yang terinfeksi serta
makanan atau minuman yang terkontaminasi. Demam non tifoid disebut juga
gastroenteritis merupakan infeksi terbatas dan terlokalisasi pada epitel
intestinal. Gejala salmonellosis non tifoid hampir mirip dengan salmonellosis
tifoid, yaitu: mual, kram abdominal, diare berair dan mungkin berdarah,
demam dengan durasi kurang dari 48 jam, serta muntah dapat terjadi 8-72 jam
setelah terinfeksi.
Center for Disease Control and Prevention (CDC, 2008) Amerika
Serikat mengestimasi setiap tahunnya di Amerika Serikat jumlah kasus
penyakit Salmonellosis non tifoid dari bahan pangan (foodborne disease)
mencapai 1.4 juta kasus, 15608 harus dirawat dan 553 meninggal (30.6% dari
seluruh kasus kematian yang disebabkan oleh patogen asal pangan).
E. METODE DETEKSI KONVENSIONAL
Analisis pangan terhadap kemungkinan adanya bakteri patogen atau
bakteri pembusuk merupakan standar yang diharuskan untuk mengetahui
kualitas pangan dan menjamin keamanan pangan (de Boer dan Beumer,
1999). Analisis tersebut biasanya menggunakan metode konvensional yang
telah distandarkan sehingga setiap negara di dunia memiliki standar yang
sama dalam menilai kualitas pangan.
Metode deteksi konvensional yang dimaksud ialah metode pengkulturan
bakteri pada media spesifik dan menghitung sel bakteri yang hidup dalam
pangan. Prinsipnya ialah mikroorganisme bermultiplikasi pada media
15 hasil uji baik kuantitatif ataupun kualitatif, dan menjadi standar bagi uji
mikrobiologi terhadap produk pangan secara internasional.
Metode konvensional meliputi persiapan media kultur (pengkayaan,
pengkayaan selektif, dan penumbuhan pada agar selektif), penghitungan
koloni, pengkarakterisasian dengan uji biokimia, yang dapat dilanjutkan
dengan penetapan serotipe (serovar) dengan uji serologi.
Uji biokimia saat ini dipermudah dengan adanya API test. Identifikasi
dengan API, menurut USFDA dalam BAM (2007), tidak dapat menggantikan
uji serologi. API test hanya untuk mengidentifikasi perkiraan spesies tertentu,
misalnya Salmonella spp. Oleh karena itu, penetapan serovar Salmonella
tidak dapat ditentukan dengan uji biokimia API.
Bakteri dari genus yang sama, setelah diuji biokimiawi memiliki sifat
biokimia yang sama, tidak menjamin bahwa bakteri-bakteri tersebut berasal
dari serovar yang sama. Bakteri-bakteri tersebut bisa saja berasal dari
subspesies yang sama, tetapi serotipenya berbeda. Hal ini disebabkan dinding
sel mikroorganisme mengandung protein dan lipopolisakarida. Setiap bakteri
memiliki kemungkinan stuktur molekul protein atau lipopolisakarida yang
berbeda. Antigen merupakan bagian dari struktur tersebut, oleh karena itu
antigen setiap bakteri mungkin pula berbeda-beda. Pada genus Salmonella
pembedaan antar subspesies dapat lebih lanjut dilakukan dengan melihat
antigen O, antigen Vi, dan antigen H spesies tersebut.
Konfirmasi patogen dengan uji imunologi dapat dilakukan dengan Slide
Agglutination Test (SAT) yang diterapkan pada uji serologi. Uji serologi
(serotyping) merupakan tahapan dalam metode konvensional untuk
mengkonfirmasi koloni tipikal yang telah diperoleh dari uji morfologi dan uji
biokimia. Juga mengidentifikasi organisme pada tingkat subspesies dan
menjadi salah satu alat penting bagi klasifikasi taksonomi serta pengawasan
kasus keracunan pangan atau KLB akibat kontaminasi patogen tertentu,
misalnya Salmonella spp. Walaupun uji biokimia juga mengkonfirmasi
koloni tipikal, uji tersebut tidak dapat mensubstitusi uji serologi. Sebab kedua
16 Serotipe galur Salmonella dilakukan dengan mengidentifikasi antigen
permukaan (LPS, antigen O) terlebih dahulu, kemudian antigen flagela
(protein, antigen H). Sebagian besar galur Salmonella menunjukkan 2 fase
antigen H. Setelah keseluruhan serotyping dilaksanakan, barulah serotipe
dapat ditetapkan berdasarkan skema Kauffmann-White, Popoff dan Le Minor,
(WHO, 2009) memanfaatkan kombinasi antigen O dan antigen H spesifik.
Prinsip uji ini adalah aglutinasi antigen pada patogen-antibodi dalam
antisera. Aglutinasi yang diharapkan terjadi (uji positif) pada SAT terbentuk
karena antigen dan antisera berikatan. Proses aglutinasi memerlukan proporsi
antisera dan suspensi bakteri yang tepat atau ekuivalen, agar dapat terlihat
jelas dengan mata telanjang. Penetesan antisera dikendalikan dengan pipet
tetes (lihat tanda panah pada Gambar 1a) yang melengkung dan menyempit di
bagian ujungnya untuk memperkecil volume antisera yang diteteskan.
(a) (b)
Gambar 1. (a) Antisera; (b) Visualisasi aglutinasi [sebelah kiri pada slide]
Kelebihan atau kekurangan salah satu di antara kedua komponen tersebut
tidak akan menghasilkan ikatan yang kompak sehingga aglutinasi tidak
terlihat jelas pada gelas objek. Visualisasi dari aglutinasi ditunjukkan oleh
tanda panah pada Gambar 1b.
Kekurangan dari metode ini ialah memerlukan pengalaman yang baik
dari peneliti untuk melihat aglutinasi, menghabiskan antisera cukup banyak,
memerlukan waktu pengujian serologi saja minimal tiga hari. Prosedur yang
panjang dan diperlukannya waktu inkubasi di setiap tahapan menyebabkan
17 lain dari metode ini ialah diperlukan banyak alat gelas dan tenaga peneliti
(tidak otomatis dengan instrumen).
Saat ini telah banyak teknik yang dikembangkan untuk mempermudah
pelaksanaan metode konvensional, misalnya: gravimetric diluter, pulsifier
dan stomacher yang mempermudah homogenisasi; spiral plater, dipslide, dan
petrifilm untuk enumerasi dan deteksi; colony counter dan kit uji untuk
konfirmasi atau identifikasi (de Boer dan Beumer, 1999). Meskipun demikian
waktu pendeteksian tidak berkurang secara signifikan hingga
dikembangkanlah metode deteksi cepat.
F. METODE DETEKSI CEPAT (RAPID METHOD) BAKTERI
PATOGEN DENGAN PCR
Perkembangan terkini dalam teknologi, secara teori membuat proses
deteksi dan identifikasi bakteri patogen lebih cepat, tepat, sensitif, dan
spesifik dibandingkan dengan metode konvensional (Anonim, 2001). Metode
deteksi dengan teknik molekuler meliputi DNA probes, Polymerase Chain
Reaction (PCR), Restriction Enzyme Analysis (REA), Random Amplification
of Polymorphic DNA (RAPD), Pulsed Field Gel Electrophoresis (PFGE),
dan Restriction Fragment Length Polymorphism (RFLP) (Jay, 1996).
Metode-metode tersebut sering disebut sebagai metode cepat (rapid methods).
Metode deteksi cepat patogen dan kontaminan mikrobiologi lainnya
dalam makanan merupakan hal yang sangat penting untuk menjamin
keamanan pangan konsumen. Keuntungan dari metode cepat dibandingkan
dengan metode konvensional adalah waktu lebih singkat (4–48 jam), tidak
membutuhkan banyak tenaga, serta lebih sensitif dan akurat (Patel dan
Williams, 1994; Anonim, 2001). Sedangkan metode konvensional untuk
mendeteksi patogen asal pangan bergantung pada waktu yang dibutuhkan
untuk pertumbuhan bakteri dalam media kultur, yang diikuti oleh isolasi,
identifikasi biokimia, dan terkadang harus diikuti dengan uji serologi.
Metode uji berbasiskan DNA yang telah dikembangkan secara komersial
untuk mendeteksi patogen asal pangan, antara lain: probes, PCR dan
18 amplifikasi DNA dengan Polymerase Chain Reaction (PCR) (de Boer dan
Beumer, 1999).
PCR adalah metode in vitro untuk memperbanyak sekuens DNA
tertentu, perbanyakan tersebut seperti halnya replikasi DNA pada sel hidup.
Lazimnya metode ini (PCR standar) memerlukan tahapan isolasi DNA,
amplifikasi sekuens target dengan PCR, pemisahan produk amplifikasi
(amplikon) dengan elektroforesis gel agarosa, dan memperkirakan ukuran
fragmen dengan DNA ladder setelah pewarnaan dengan ethidium bromida.
Pada bagian akhir, verifikasi hasil PCR dilakukan dengan pembelahan
spesifik amplikon oleh endonuklease restriksi atau pemindahan amplikon
terpisah ke dalam membran kemudian dihibridisasi dengan probe DNA
spesifik. Alternatif verifikasi lain dengan sekuensing langsung menggunakan
semi-nested PCR. Perkembangan PCR lainnya yang lebih nyaman digunakan
ialah real-time PCR, di mana amplifikasi PCR dan verifikasi dilakukan sekali
jalan dengan probe khusus (oligonukleotida berlabel fluoresen yang spesifik
terhadap gen target).
Real-time PCR melakukan amplifikasi dan deteksi dalam satu tahapan
sebab akumulasi produk spesifik dicatat secara kontinyu selama siklus. Hal
ini tidak dapat dilakukan pada PCR standar yang masih mengandalkan
elektroforesis gel agarosa untuk mengkuantitasi amplikon. Hasil dari
elektroforesis gel agarosa ini memperpanjang waktu deteksi dan kurang tepat
karena pengukurannya berdasarkan ukuran molekul. Padahal molekul yang
berbeda mungkin saja memiliki ukuran yang sama atau hampir sama.
Pendeteksian dengan gel agarosa menganggap molekul yang berbeda tersebut
sebagai molekul yang sama (Dharmaraj, 2009).
Pendeteksian produk real-time PCR secara kuantitatif berbeda dengan
PCR standar yang mengkuantitasi amplikon berdasarkan panjang basa atau
bobot molekul. Kuantitas produk real-time PCR dihitung berdasarkan
threshold cycle (Ct) yaitu waktu di mana intensitas fluoresen lebih besar
daripada fluoresen yang ditimbulkan oleh noise (background fluorescence).
Noise dapat disebabkan oleh penempelan larutan isolat DNA beserta
19 Format PCR standar yang berdasarkan analisis titik akhir (fase plato)
kurang kuantitatif karena hasil akhir produknya tidak didasarkan konsentrasi
sekuens target dalam sampel, tetapi berdasarkan pada ukuran molekul hasil
amplifikasi (amplikon). Berikut ini beberapa kekurangan deteksi amplikon
jika dilakukan pada fase plato dengan elektroforesis gel agarosa: kurang tepat,
sensitivitas rendah, tidak otomatis, hanya berdasarkan ukuran molekul,
pewarnaan ethidium bromida kurang sensitif, dan memperpanjang waktu
deteksi (Dharmaraj, 2009).
Keunggulan real-time PCR adalah pendeteksian diukur tepat pada saat
target amplifikasi terdeteksi pertama kali di setiap siklus (fase eksponensial),
bukan di fase akhir amplifikasi (fase plato) seperti yang terjadi pada PCR
standar. Keunggulan real-time PCR lainnya ialah analisis dapat dilakukan
tanpa membuka tabung sehingga mengurangi risiko kontaminasi amplikon
PCR atau molekul target lainnya. Menurut Edwards et al. (2004), aplikasi
teknologi real-time PCR mengurangi waktu penanganan atau pengujian dan
meningkatkan keakuratan kuantifikasi metode PCR. Dengan demikian,
penggunaan teknik real-time PCR lebih efisien dan efektif dibandingkan PCR
standar (Edwards et al., 2004).
Kuantifikasi real-time PCR dapat dilakukan dengan dua teknik:
(1) penggunaan dyefluoresence yang berikatan dengan DNA untai ganda, dan
(2) penggunaan probe oligonukleotida DNA modifikasi yang mengeluarkan
fluoresen ketika hibridisasi dengan DNA komplementer. Data yang
dihasilkan dapat dianalisis dengan perangkat lunak komputer yang terhubung
dengan thermal cycler untuk menghitung jumlah kopi DNA atau threshold
cycle (Ct) dari patogen dalam sampel pangan tertentu.
Sebelum tahap amplifikasi dengan real-time PCR, diperlukan tahap
persiapan, kemudian setelah tahap amplifikasi diperlukan evaluasi produk
PCR. Tahap persiapan dan evaluasi tersebut dijelaskan lebih lanjut di bawah
ini:
1. Tahap Pra-Amplifikasi Real-Time PCR
Tahap pra-amplifikasi PCR standar dan real-time PCR tidak
20 isolat DNA sebagai DNA target amplifikasi. Prosedur isolasi DNA
merupakan tahapan yang paling banyak dimodifikasi sebelum amplifikasi
dengan PCR dimulai. Terdapat enam tahap dalam mengisolasi DNA,
yaitu preparasi sampel, pelisisan sel, proteksi dan stabilisasi DNA,
pemisahan DNA dari debris sel, presipitasi DNA, dan pemekatan DNA.
Prosedur yang umum digunakan untuk mengisolasi DNA
kromosomal sebagai DNA target untuk uji amplifikasi dikembangkan
oleh Sambrook et al. (1989). Prosedur isolasi DNA juga dikembangkan
oleh Chapaval et al. (2008). Tahapan isolasi DNA prosedur-prosedur
tersebut dapat diperbandingkan berdasarkan enam tahap dalam
mengisolasi DNA. Enam tahap mengisolasi DNA berdasarkan Sambrook
et al., (1989), sebagai berikut:
a. Preparasi sampel
Sampel pangan yang telah diinokulasi secara artifisial dan
dihomogenisasi, kemudian diencerkan.
b. Pelisisisan sel
Pelisisan sel dilakukan dengan 10% sodium dodecylsulphate
(SDS) dan 0.2 mg/ml proteinase K. Selanjutnya divorteks dan
diinkubasi selama 2 jam pada suhu 65°C.
c. Proteksi dan stabilisasi DNA
Suspensi dari tahap persiapan sampel ditambahkan 500 µl buffer
(100 mM NaCl, 500 mM Tris (pH 8.0) untuk menjaga kestabilan
DNA ketika pelisisan sel.
d. Pemisahan DNA dari debris sel dan protein
DNA dipisahkan melalui ekstraksi dengan larutan
fenol:kloroform (1:1 v/v, pH 8.0). Ekstraksi tersebut diulang hingga
tiga kali dan setiap kali pengulangan fase aqueous dipindahkan ke
tabung bersih.
e. Presipitasi DNA
Fase aqueous ditambah etanol 95% (mengandung 0.3 M sodium
21 diinkubasi semalam pada suhu -20°C untuk mengendapkan DNA
kromosomal.
f. Pemekatan DNA
DNA di-recovery dengan sentrifugasi dan pelet DNA dicuci dua
kali dengan etanol 70%.
Enam tahapan mengisolasi DNA berdasarkan metode yang
dikembangkan oleh Chapaval et al. (2008) adalah sebagai berikut:
a. Preparasi sampel
Sebanyak 2.5 ml kultur yang telah diinkubasi semalam dalam
Brain Heart Infusion Broth (BHIB) disentrifus dengan kecepatan
33000 g selama 30 detik, kemudian supernatan dibuang dan pelet
diresuspensi.
b. Pelisisisan sel
Pelet diresuspensi dalam 700 µl buffer ekstraksi (1.4 M NaCl;
100 mM Tris-HCl [pH 8.0]; 200 mM EDTA pH 8.0; 40% PVP
(polyvinylpyrrolidone); 2% CTAB (cetyltrimethylammonium
bromide), 20 mg/ml Proteinase K; 0.2% β-Mercaptoethanol).
Tabung diinkubasi pada suhu 65°C selama 30 menit dengan
pengocokan setiap 10 menit.
c. Proteksi dan stabilisasi DNA
Suspensi dari tahap persiapan sampel diberi buffer 1.4 M NaCl;
100 mM Tris-HCl pH 8.0 untuk menjaga kestabilan DNA ketika
pelisisan sel. Buffer tersebut diberikan bersamaan dengan larutan
pelisis sel.
d. Pemisahan DNA dari debris sel dan protein
Sebanyak 650µl kloroform:isoamil alkohol (24:1) ditambahkan
dan larutan disentrifus pada kecepatan 33000 g selama 7 menit. Fase
aqueous di bagian atas dipindahkan ke dalam sebuah tabung 1.5 ml
dan 200 µl buffer ekstrasi tanpa proteinase K ditambahkan. Larutan
diaduk perlahan dan 650 µl kloroform:isoamil alkohol (24:1)
22 kloroform:isoamil alkohol (24:1) dilakukan dua kali menggunakan
650 µl kloroform:isoamil alkohol.
e. Presipitasi DNA
DNA dipresipitasi dengan penambahan sejumlah volume yang
sama dengan isopropanol pada suhu ruang.
f. Pemekatan DNA
Isopropanol dihilangkan dan pelet dicuci dengan 70 µl etanol
70%. Pelet DNA dikeringudarakan dan diresuspensi dalam 40 µl
buffer Tris-EDTA (TE) (10 mM Tris-HCl pH 8.0; 1 mM EDTA pH
8.0 dan 10 µg/ml RNAse).
Prinsip dasar isolasi DNA adalah serangkaian proses untuk
memisahkan DNA dari komponen-komponen sel lainnya. Hasil ekstraksi
merupakan tahapan penting untuk langkah berikutnya. Oleh sebab itu,
tahapan ini harus dilakukan dengan baik dan bebas kontaminasi. Isolasi
yang banyak digunakan ialah ekstraksi dengan fenol:kloroform, seperti
halnya kedua metode yang telah dijelaskan di atas. Teknik ekstraksi
fenol:kloroform menghasilkan kualitas yang lebih baik dibandingkan
dengan metode pendidihan (Fricker et al., 2007).
Reagen lain yang penting dalam isolasi DNA ialah Phosphate Buffer
Saline (PBS) yang berfungsi melarutkan matriks pangan sehingga berada
dalam kondisi fisiologis, sekaligus mengendapkan inhibitor-inhibitor
yang tidak diperlukan seperti kalsium. Buffer TE digunakan untuk
menjaga tekanan osmotik dan Cetyltrimethyl Ammonium Bromida
(CTAB), Sodium Dodecyl Sulphate (SDS), Ethylene Diamine Tetraacetic
Acid (EDTA) berfungsi untuk melisis matriks pangan dan merusak lipid
pada membran sel sehingga DNA lebih mudah diekstraksi (Anonim,
2008). Proteinase K digunakan untuk merusak protein dan enzim RNAse
berfungsi untuk menghilangkan RNA sehingga dalam suspensi tertinggal
23 2. Pembacaan Produk Hasil Real-Time PCR
Amplifikasi yang dijalankan dalam thermal cycler ditampilkan
dalam bentuk grafik pada layar komputer dengan software yang aplikabel
terhadap thermal cycler, contohnya adalah software IQ-5 (Bio-Rad).
Grafik-grafik yang diperoleh berupa grafik amplifikasi, kurva standar, dan
kurva peleburan (melt curve). Grafik tersebut digunakan untuk
mengevaluasi kinerja amplifikasi real-time PCR.
a. Grafik amplifikasi
Grafik amplifikasi terbentuk semenjak proses amplifikasi
dimulai. Grafik ini berfungsi untuk menentukan apakah dalam
thermal cycler terjadi amplifikasi atau tidak. Grafik amplifikasi
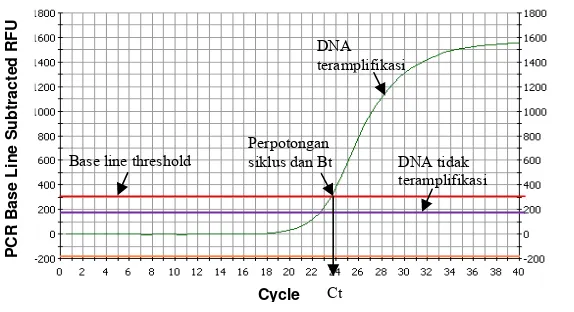
dapat dilihat pada Gambar 2 di bawah ini.
[image:36.595.198.485.334.490.2]
Gambar 2. Grafik sigmoidal proses amplifikasi dengan
real-time PCR (Edwards et al., 2004)
Amplifikasi ditetapkan berdasarkan intensitas fluoresen,
semakin banyak produk amplifikasi yang dihasilkan, semakin besar
akumulasi fluoresen yang terbaca. Peningkatan fluoresen tersebut
ditandai dengan terbentuknya gradik sigmoidal, seperti yang
tergambar pada Gambar 2 (garis hijau). Grafik sigmoid akan
berpotongan dengan base line threshold yang telah ditentukan secara
otomatis oleh program. Titik perpotongan antara grafik sigmoid dan
base line threshold jika direfleksikan terhadap sumbu x (Cycle)
adalah threshold cycle (Ct) bagi sampel yang diamplifikasi. Garis
PCR
Base Line Subtrac
ted RFU
Base line threshold DNA tidak
teramplifikasi DNA
teramplifikasi
Perpotongan siklus dan Bt
Ct
24 biru pada Gambar 2 akan terbentuk jika tidak terjadi amplifikasi
pada thermal cycler.
Nilai Ct adalah siklus di atas noise dimana akumulasi produk
(senilai 2n, n ialah jumlah pengulangan siklus amplifikasi) terbaca
pertama kali pada fase eksponensial. Fase eksponensial berakhir
menjadi fase plato saat pereaksi dalam campuran reaksi PCR sudah
habis. Nilai Ct digunakan dalam kurva standar sebagai fungsi
terhadap log konsentrasi bakteri.
b. Kurva standar
Kultur murni bakteri yang telah diketahui konsentrasinya
(CFU/ml) diencerkan hingga diperoleh konsentrasi bakteri terendah
(1 CFU/ml). Seluruh tingkat pengenceran yang berturut-turut,
misalnya mengandung 100-106 CFU/ml diisolasi DNAnya dan
diamplifikasi. Amplifikasi beberapa tingkat pengenceran suatu kultur
murni secara otomatis oleh software IQ-5 akan digambarkan dalam
bentuk kurva standar, selain grafik amplifikasi. Kurva standar
amplifikasi disajikan dalam Gambar 3.
Gambar 3. Kurva standar amplifikasi kultur murni dari enam tingkat pengenceran dengan real-time PCR (Edwards
et al., 2004)
Enam titik pada kurva standar menunjukkan terdapat enam
tingkat pengenceran yang masing-masing memiliki nilai Ct. Kurva Log konsentrasi bakteri (CFU/ml)
Thres
hold c
y
cle
(
Ct
)
25 standar merupakan hubungan antara log konsentrasi bakteri dan
threshold cycle (Ct). Kurva ini digunakan dalam penetapan limit
deteksi konsentrasi bakteri yang belum diketahui pada suatu sampel
pangan. Penetapan limit deteksi tersebut memanfaatkan persamaan
linear yang dibentuk kurva standar. Nilai Ct yang diketahui setelah
isolat DNA diamplifikasi merupakan nilai y dan log konsentrasi
merupakan nilai x dalam persamaan linear tersebut sehingga
konsentrasi bakteri dalam suatu sampel pangan dapat diketahui.
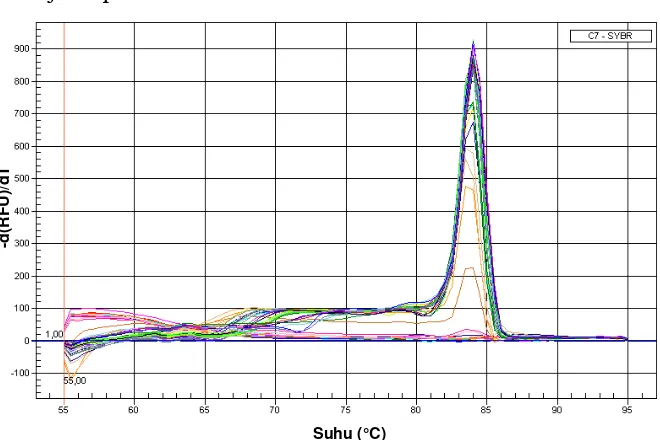
c. Melt curve
Kurva peleburan atau melt curve merupakan kurva hubungan
antara suhu (T) dan turunan dari unit fluoresen (-d(RFU)/dT)
digunakan untuk memonitor perubahan dalam suhu peleburan, yaitu
suhu di mana 50% amplikon DNA untai ganda terpisah menjadi dua
untai tunggal. Melt curve diperoleh berdasarkan siklus yang
ditambahkan setelah siklus amplifikasi. Target amplifikasi dalam
siklus tersebut adalah produk amplifikasi (amplikon). Melt curve
[image:38.595.172.502.449.669.2]disajikan pada Gambar 4.
Gambar 4. Melt curve yang memiliki sebuah puncak Tm
Puncak kurva pada melt curve merupakan nilai Tm amplikon,
jika nilainya dibaca pada sumbu absis. Amplikon yang berasal dari
DNA target yang sama akan memiliki nilai Tm yang sama,
-d(
R
FU
)/d
T
26 ditunjukkan dengan puncak pada titik suhu yang sama. Melt curve
pada Gambar 4 memiliki nilai Tm yang sama, berarti produk berasal
dari DNA yang sama yaitu DNA target dan produknya spesifik.
Selain itu melt curve mampu menunjukkan ada atau tidaknya produk
non spesifik. Produk non spesifik akan membentuk puncak pada
suhu yang berbeda dengan amplikon (produk spesifik) atau melt
curve dapat pula memiliki lebih dari satu puncak suhu.
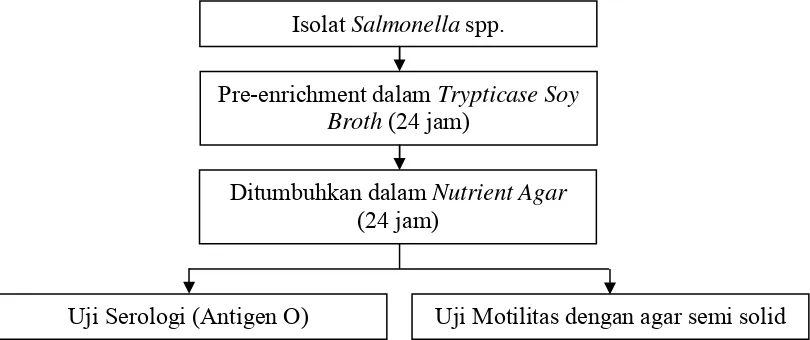
27 Isolat Salmonella spp.
Pre-enrichment dalam Trypticase Soy Broth (24 jam)
Ditumbuhkan dalam Nutrient Agar
(24 jam)
Uji Serologi (Antigen O) Uji Motilitas dengan agar semi solid
III. METODOLOGI PENELITIAN
A. TEMPAT DAN WAKTU MAGANG
Kegiatan magang dilakukan di laboratorium Mikrobiologi Pusat Riset
Obat dan Makanan, Badan POM RI, Jakarta. Waktu penelitian dilaksanakan
dari bulan Februari sampai dengan Juli 2009.
B. LINGKUP KEGIATAN PENELITIAN
Kegiatan yang dilakukan mencakup dua kegiatan, yaitu (1) melakukan
identifikasi serovar Salmonella spp. berbasiskan imunologi dan
(2) melakukan deteksi B. cereus dengan metode berbasiskan DNA.
Identifikasi serovar dengan cara uji aglutinasi pada gelas objek dilakukan
terhadap sepuluh isolat Salmonella spp. yang merupakan koleksi Departemen
Ilmu dan Teknologi Pangan (IPB) dan telah diuji secara biokimiawi. Sepuluh
isolat tersebut diuji serologi untuk mengetahui antigen O yang dimiliki oleh
masing-masing isolat sebab antigen O merupakan dasar pengelompokan
serogrup Salmonella spp. Selain itu, dilakukan uji motilitas untuk mengetahui
masing-masing isolat bersifat motil atau tidak. Antigen O merupakan antigen
yang diuji pertama kali pada uji serologi, sedangkan motilitas diuji sebagai
prasyarat uji antigen H. Diagram alir kegiatan deteksi Salmonella spp. dapat
[image:40.595.110.515.525.695.2]dilihat pada Gambar 5.
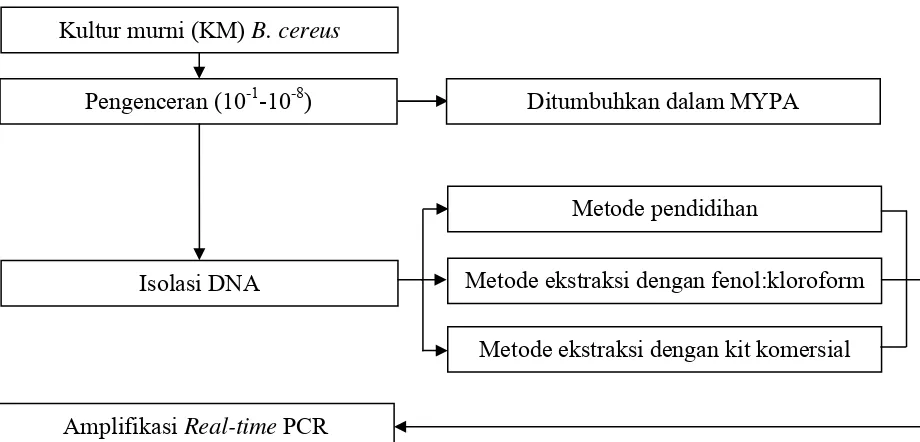
28 Pengenceran (10-1-10-8)
Kultur murni (KM) B. cereus
Ditumbuhkan dalam MYPA
Amplifikasi Real-time PCR Isolasi DNA
Metode pendidihan
Metode ekstraksi dengan fenol:kloroform
Metode ekstraksi dengan kit komersial Kegiatan yang dilakukan untuk mendeteksi DNA B. cereus dengan
real-time PCR meliputi isolasi DNA kultur murni bakteri B. cereus dan isolasi
DNA dari sampel pangan nasi goreng, amplifikasi dan evaluasi kinerja
real-time PCR berupa limit deteksi amplikon. Isolasi DNA dilakukan dengan tiga
metode, yaitu metode pendidihan, metode ekstraksi dengan fenol:kloroform,
dan metode ekstraksi dengan kit komersial. Isolat DNA B. cereus, dari kultur
murni dan nasi goreng, diamplifikasi dengan real-time PCR.
Amplifikasi DNA kultur murni B. cereus digunakan untuk membentuk
kurva standar, sedangkan amplifikasi DNA B. cereus dalam sampel pangan
untuk menetapkan limit deteksi B. cereus dalam nasi goreng. Tahapan kerja
isolasi DNA dari kultur murni B. cereus dan dari sampel pangan disajikan
[image:41.595.91.551.354.575.2]pada Gambar 6 dan 7.
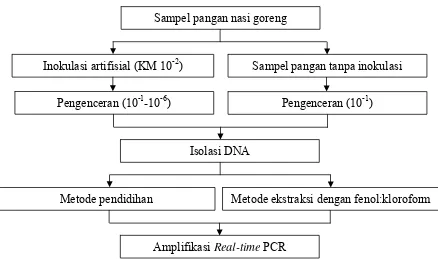
29 Sampel pangan nasi goreng
Pengenceran (10-1) Sampel pangan tanpa inokulasi
Isolasi DNA Pengenceran (10-1-10-6)
Inokulasi artifisial (KM 10-2)
Metode pendidihan Metode ekstraksi dengan fenol:kloroform
[image:42.595.101.539.88.347.2]Amplifikasi Real-time PCR
Gambar 7. Tahapan kerja pada uji amplifikasi DNA B. cereus dalam nasi goreng
C. BAHAN DAN ALAT
1. Identifikasi Serovar Salmonella spp.
a. Kultur bakteri
Galur bakteri yang digunakan dalam uji serologi ialah
Salmonella spp. yang diisolasi dari daging ayam yang berasal dari
pasar lokal. Sepuluh isolat yang disimpan dalam Brain Heart
Infusion Broth (BHIB) merupakan koleksi Departemen Ilmu dan
Teknologi Pangan, Institut Pertanian Bogor dan telah ditetapkan
sebagai Salmonella spp. berdasarkan uji biokimia.
b. Bahan-bahan
Bahan-bahan yang digunakan adalah Nutrien Agar (Merck) dan
Antisera O (National Salmonella Centre – Statens Seruminstitut).
c. Alat-alat
Alat-alat yang digunakan adalah gelas objek (slide), cawan petri,
30 2. Metode Deteksi B. cereus Berbasiskan DNA
a. Kultur bakteri
Galur referensi yang digunakan merupakan jenis bakteri Gram
positif, Bacillus cereus ATCC 11778 dan Bacillus subtilis ATCC
6633 NCTC 10400. Bakteri-bakteri tersebut ditumbuhkan di
Trypticase Soy Broth (TSB) (Merck) pada suhu 37°C. Sel bakteri
dihitung dengan perhitungan cawan sebar (USFDA, 2001) pada
media agar spesifik Mannitol Yolk Polymixin Agar (MYPA) (Oxoid)
dan diinkubasi pada suhu 30°C selama 48-72 jam. Sampel pangan
yang dianalisa adalah pangan yang banyak mengandung karbohidrat
yaitu nasi goreng. Sampel diambil dari tempat penjualan makanan di
sekitar kampus IPB, Bogor.
b. Bahan-bahan
Bahan-bahan yang digunakan adalah Ilustra Bacteria Genomic
Prep Mini Spin Kit (GE Healthcare) yang terdiri dari: buffer lisis,
buffer elusi, dan buffer pencuci. Selain itu juga digunakan Lisozim
(USB), Proteinase K (USB), RNAse A (USB), CTAB (Merck), PBS
(Merck), EDTA (Merck), Tris-HCl solution (USB), Triton-X
solution (USB), SDS solution (USB), Isopropanol (Merck),
Amonium asetat (Merck), Fenol (Merck), Kloroform (Merck), Asam
asetat glasial (Merck), NaCl (Merck), Etanol absolut (Merck),
MiliQ, RNAse free water (USB), IQ SYBR Green (Bio-Rad), Primer
forward dan reverseBceT (Bio-Rad), isolat DNA yang diekstrak dari
kultur murni B. cereus (pengenceran 10-1-10-8), isolat DNA dari
sampel pangan yang tidak diinokulasi (pengenceran 10-1), isolat
DNA yang telah diinokulasi secara artifisial (pengenceran 10-1-10-6).
c. Alat-alat
Alat-alat yang digunakan adalah Stomacher (Seward),
Refrigerator Microsentrifuge (Hettich), Water Bath, Laminar Air
31
Analytical Balance (Shimadzu), Autoklaf (Hirayama), Automatic
Colony Counter (Acolyte), Lampu UV, kamera digital, tabung
mikrosentrifus 1.5 ml, tabung konikal 15 ml (Iwaki), inkubator,
bunsen, pipet mikro (Eppendorf), pipet volumemetrik, bulb, gelas
piala, gelas ukur, labu Erlenmeyer, botol semprot, cawan petri, jarum
ose, tabung reaksi, rak tabung reaksi, sudip, magnetic stirrer, gelas
pengaduk, Real-time PCR (Bio-Rad), micro well, dan adhesive
sealer.
D. METODE PENELITIAN
1. Identifikasi Serovar Salmonella spp. (WHO, 2009)
Konfirmasi Salmonella spp. dengan uji imunologi dilakukan untuk
mendeteksi antigen dengan O Slide Agglutinasion Test (SAT) dan
motilitas dengan agar semi solid. Mula-mula, sepuluh isolat Salmonella
spp. dalam BHIB diinokulasi dan ditumbuhkan pada media NA,
kemudian diinkubasi selama 24 jam pada suhu 35°C. Uji serologi antigen
O dimulai dengan satu tetes antisera O polivalen diteteskan pada gelas
objek, kemudian 1 ose Salmonella spp. diambil dari NA dan dicampur
dengan jarum ose selama 1 menit. Gelas objek tersebut digoyang
perlahan selama 1-2 menit. Uji positif ditunjukkan dengan adanya
aglutinasi. Uji positif berarti antibodi pada sera spesifik berikatan dengan
antigen yang dimiliki bakteri. Aglutinasi tidak akan terjadi jika bakteri
tidak memiliki antigen yang dapat berikatan dengan antibodi.
Uji motilitas dilakukan pada hari yang sama dengan pengujian
antigen O. Satu ose Salmonella spp. diambil dari NA, kemudian
diinokulasi satu titik pada bagian tengah agar semi solid dan diinkubasi
semalam pada suhu 37°C. Isolat yang menunjukkan pergerakan (sekitar
40 mm dari titik inokulasi atau lebih dari 50% jari-jari cawan agar) ke
32 2. Metode Deteksi B. cereus Berbasiskan DNA (Alarcon et al., 2006;
Fricker et al., 2007)
a. Tahap persiapan
1) Persiapan media
Media yang perlu dipersiapkan untuk penyegaran kultur
bakteri adalah media Trypticase Soy Broth. Media selektif untuk
isolasi bakteri adalah Mannitol Egg Yolk Polymyxin Agar
(media selektif B.cereus), Egg Yolk Emulsion serta Polymyxin B
(untuk menghambat pertumbuhan bakteri Gram negatif). Media
selektif digunakan untuk isolasi dan penghitungan kultur bakteri
patogen, baik kultur murni maupun kultur dari sampel pangan.
Prosedur pembuatan media dapat dilihat pada Lampiran 2 dan 3.
2) Persiapan kultur bakteri
Bacillus cereus disegarkan pada media TSB setiap
2 minggu sekali dan diinkubasi pada suhu 37ºC selama 24 jam,
lalu disimpan pada suhu 16°C. Untuk pengecekan kemurnian
kultur, kultur B. cereus dalam TSB diinokulasi sebanyak 1 lup
ke permukaan agar Mannitol Egg Yolk Polymyxin Agar (MYPA)
padat dalam cawan petri steril. Koloni tipikal B. cereus pada
MYPA dengan suplementasi polymyxin B akan berwarna pink
cerah dan dikelilingi zona presipitasi.
Selain bakteri patogen B. cereus, disiapkan juga B. subtilis
yang digunakan untuk menguji spesifisitas primer BceT. Primer
BceT merupakan DNA dari gen penyandi enterotoksin T pada
DNA kromosomal B. cereus. Isolat DNA bakteri tersebut
diamplifikasi kemudian melt curve yang terbentuk dianalisis
untuk mengetahui apakah primer BceT dapat menempel pada
DNA kromosomal selain DNA gen penyandi enterotoksin
B. cereus yang berarti primer kurang spesifik. Bakteri ini pun
33 pada suhu 37ºC selama 24 jam, lalu disimpan pada suhu 16°C.
Prosedur persiapan kultur bakteri dapat dilihat pada Lampiran 4.
B. cereus dan B.subtilis disegarkan dan diinkubasi pada
suhu 37ºC selama 24 jam sehari sebelum DNA diisolasi. Kultur
murni B. cereus yang hendak diisolasi diencerkan terlebih
da
![Gambar 1. (a) Antisera; (b) Visualisasi aglutinasi [sebelah kiri pada (a) (b) slide]](https://thumb-ap.123doks.com/thumbv2/123dok/675372.356150/29.595.153.489.374.527/gambar-antisera-visualisasi-aglutinasi-sebelah-kiri-pada-slide.webp)