1.1 Latar Belakang
Pemerintah telah melakukan berbagai upaya untuk memenuhi kebutuhan
pangan dan meningkatkan gizi masyarakat. Salah satu upaya tersebut yaitu dengan
mempopulerkan aneka ragam jenis makanan. Hal ini didukung dengan
perkembangan teknologi pengolahan pangan yang semakin maju.
Industri pangan yang saat ini berkembang cukup pesat salah satunya adalah
industri frozen dessert. Industri ini merupakan jenis industri pengolahan pangan yang bertujuan meningkatkan nilai ekonomi pangan. Frozen dessert merupakan produk makanan beku pencuci mulut yang digemari masyarakat. Jenis frozen dessert yang sering ditemui antara lain adalah es krim.
Es krim sangat digemari oleh masyarakat karena rasanya yang manis dan
memiliki tekstur yang lembut. Es krim adalah jenis frozen dessert paling populer dan juga paling tinggi kandungan lemaknya. Meskipun memiliki kandungan
lemak yang sangat tinggi, es krim tetap digemari oleh masyarakat di dunia. Salah
satu negara pengkonsumsi es krim terbanyak di dunia adalah Amerika. Produksi
es krim dunia pada tahun 2003 mencapai lebih dari satu miliar liter dan
dikonsumsi oleh miliaran konsumen per tahun (Astawan 2008).
Es krim di Indonesia telah dikenal sejak tahun 1970-an dan hingga saat ini
pemasarannya sudah semakin meluas, walaupun untuk sebagian orang es krim
masih dianggap sebagai makanan mewah. Es krim adalah sejenis makanan semi
padat yang dibuat dengan cara pembekuan tepung es krim atau dari campuran
susu, lemak hewani maupun nabati, gula dan dengan atau tanpa bahan tambahan
pangan lain dan bahan makanan yang diizinkan. Produk es krim yang beredar di
pasaran umumnya digolongkan atas tiga kategori yaitu economy, good average
dan deluxe. Perbedaan utama dari ketiga jenis es krim tersebut berdasarkan kandungan lemak susu. Komponen es krim secara umum adalah lemak, padatan
susu tanpa lemak, gula, bahan penstabil dan bahan pengemulsi (Clarke 2004).
Kandungan lemak susu yang tinggi (high fat) pada es krim membuat konsumen lebih selektif dalam memilih es krim. Kandungan lemak susu pada es
menimbulkan kegemukan. Hal ini tentunya menjadi pertimbangan tersendiri bagi
konsumen yang memperhatikan diet rendah lemak. Alternatif produk yang dapat
menggantikan produk es krim ini adalah melorin atau es krim imitasi.
Melorin adalah jenis makanan pencuci mulut berbentuk beku seperti es krim
yang sebagian atau seluruh lemak susunya diganti dengan lemak nabati dengan
kadar lemak rendah. Produk ini mengandung tidak kurang dari 6 % lemak, dengan
formula, proses pembuatan dan sifat-sifat yang sama seperti es krim
(Hubeis et al. 1996).
Produk melorin kurang disukai oleh konsumen karena memiliki tekstur yang
kurang lembut tidak seperti es krim pada umumnya. Tantangan dalam
memproduksi es krim rendah lemak berhubungan dengan fakta bahwa tidak
adanya atau terganggunya jaringan globula lemak. Hal ini dapat mengakibatkan
dampak serius bagi tekstur produk, karena kehalusan tekstur es krim ditentukan
oleh kandungan lemak susu (Aime et al. 2001).
Formulasi yang tepat dalam pembuatan melorin sangat diperlukan agar
didapatkan produk yang disukai konsumen. Hal ini dapat dilakukan dengan
penambahan zat yang melembutkan dan menstabilkan emulsi yaitu hidrokoloid.
Jenis hidrokoloid yang biasa digunakan adalah karagenan, terutama dari jenis iota
yang diformulasikan dengan gum memiliki sifat sineresis yang rendah sehingga
diharapkan dapat diaplikasikan dalam es krim, jelli, puding, air freshener, dan lain-lain (Sinurat et al. 2006). Sifat-sifat ini dapat dimanfaatkan dalam pembuatan es krim sebagai penstabil. Aplikasi hidrokoloid sebagai penstabil pada es krim
dengan sediaan berbentuk tepung telah dilakukan pada beberapa penelitian
(Prihantoro 2000).
Karagenan belum diaplikasikan pada pengembangan produk diversifikasi
melorin sebagai bahan penstabil. Bahan penstabil dalam pembutan es krim
memiliki fungsi sebagai membantu menahan terjadinya pengkristalan es krim
pada saat penyimpanan dan menstabilkan pengadukan dalam proses pencampuran
bahan baku es krim (Chan 2010).
Larutan karagenan dapat mengentalkan dan menstabilkan partikel-partikel
sehingga mencegah pembentukan kristal es dan memperbaiki rasa pada industri es
bagi penggemar es krim yang memperhatikan diet rendah lemak. Parameter mutu
yang menentukkan penerimaan produk melorin adalah tekstur dan rasa, sehingga
perlu diketahui jenis dan konsentrasi bahan tambahan pangan yang tepat dalam
menentukan tingkat tekstur dan rasa yang disukai.
1.2 Tujuan
Tujuan dilakukannya penelitian adalah mencari formula melorin yang tepat
dengan kombinasi susu kedelai, nangka serta penambahan bahan penstabil
2.1 Karagenan
Karagenan merupakan polisakarida yang diekstraksi dari rumput laut merah
dari jenis Chondrus, Euchema, Gigartina, Hypnea, Iradea dan Phyllophora. Karagenan dibedakan dengan agar berdasarkan kandungan sulfatnya (Hall 2009).
Jumlah dan posisi sulfat membedakan macam-macam polisakarida
Rhodophyceae, polisakarida tersebut harus mengandung 20% sulfat berdasarkan berat kering untuk diklasifikasikan sebagai karagenan (FAO 2007).
Karagenan bukan biopolimer tunggal, tetapi campuran dari
galaktan-galaktan linear yang mengandung sulfat dan larut dalam air. Galaktan-galaktan-galaktan
tersebut terhubung oleh 3-β-D-galaktopiranosa (G-units) dan 4-α
-D-galktopiranosa (D-units) atau 4-3,6-anhidrogalaktosa (DA-units), membentuk unit
pengulangan disakarida dari karagenan. Galaktan yang mengandung sulfat
diklasifikasikan berdasarkan adanya 3,6-anhidrogalaktosa serta posisi dan jumlah
golongan sulfat pada strukturnya (Imeson 2010). Kappa karagenan tersusun dari
α(1,3)-D-galaktosa-4-sulfat dan β(1,4)-3,6-anhidro-D-galaktosa. Karagenan juga
mengandung D-galaktosa-2-sulfat ester (Hall 2009).
Karagenan komersil memiliki kandungan sulfat 22-38% (w/w). Karagenan
dijual dalam bentuk bubuk, warnanya bervariasi dari putih sampai kecoklatan
bergantung dari bahan mentah dan proses yang digunakan. Karagenan yang
umumnya ada di pasaran terdiri atas 2 tipe, yaitu refined karagenan dan
semirefined karagenan. Semirefined karagenan dibuat dari spesies rumput laut
Euchema yang banyak terdapat di Indonesia dan Filipina. Semirefined karagenan mengandung lebih banyak bahan yang tidak larut asam (8-15%) dibandingkan
Gambar 1 Struktur molekul karagenan (a) kappa karagenan, (b) iota karagenan dan (c) lambda karagenan (Hall 2009).
2.2 Sifat Dasar Karagenan
Sifat dasar karagenan terdiri dari tiga tipe karagenan yaitu kappa, iota dan
lambda karagenan. Tipe karagenan yang paling banyak dalam aplikasi pangan
adalah kappa karagenan. Sifat-sifat karagenan meliputi kelarutan, viskositas,
pembentukan gel dan stabilitas pH.
2.2.1 Kelarutan
Kelarutan karagenan dalam air dipengaruhi oleh beberapa faktor diantaranya
tipe karagenan, temperatur, pH, kehadiran jenis ion tandingan dan zat-zat terlarut
lainnya. Gugus hidroksil dan sulfat pada karagenan bersifat hidrofilik sedangkan
gugus 3,6-anhidro-D-galaktosa lebih hidrofobik. Lambda karagenan mudah larut
pada semua kondisi karena tidak memiliki unit 3,6-anhidro-D-galaktosa dan
mengandung gugus sulfat yang tinggi. Karagenan jenis iota bersifat lebih
hidrofilik karena adanya gugus 2-sulfat yang dapat menetralkan
3,6-anhidro-D-galaktosa yang bersifat kurang hidrofilik. Karagenan jenis kappa kurang hidrofilik
karena lebih banyak memiliki gugus 3,6-anhidro-D-galaktosa (Imeson 2010).
Karakteristik daya larut karagenan juga dipengaruhi oleh bentuk garam dari
gugus ester sulfatnya. Jenis sodium umumnya lebih mudah larut, sementara jenis
saat larutan panas menjadi dingin. Proses pembentukan gel bersifat
thermoreversible, artinya gel dapat mencair pada saat pemanasan dan membentuk gel kembali pada saat pendinginan (Gliksman 1983; Imeson 2000).
2.2.2 Stabilitas pH
Karagenan dalam larutan memiliki stabilitas maksimum pada pH 9 dan akan
terhidrolisis pada pH dibawah 3,5. Kondisi proses produksi karagenan dapat
dipertahankan pada pH 6 atau lebih. Hidrolisis asam akan terjadi jika karagenan
berada dalam bentuk larutan, hidrolisis akan meningkat sesuai dengan
peningkatan suhu. Larutan karagenan akan menurun viskositasnya jika pHnya
diturunkan dibawah 4,3 (Imeson 2000). Kappa dan iota karagenan dapat
digunakan sebagai pembentuk gel pada pH rendah, tetapi tidak mudah
terhidrolisis sehingga tidak dapat digunakan dalam pengolahan pangan.
Penurunan pH menyebabkan terjadinya hidrolisis dari ikatan glikosidik yang
mengakibatkan kehilangan viskositas. Hidrolisis dipengaruhi oleh pH, temperatur
dan waktu.
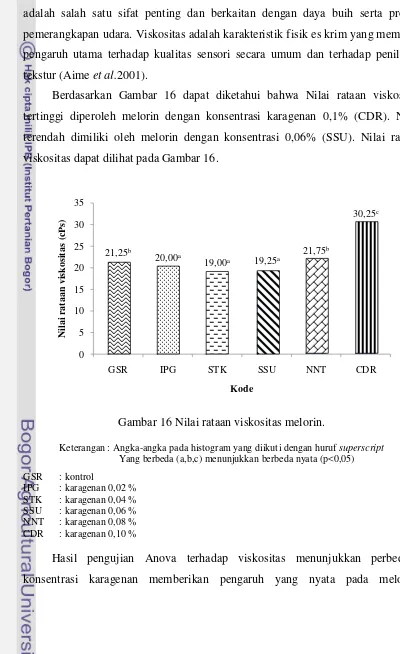
2.2.3 Viskositas
Viskositas adalah daya aliran molekul dalam sistem larutan. Viskositas
suatu hidrokoloid dipengaruhi oleh beberapa faktor yaitu konsentrasi karagenan,
temperatur, jenis karagenan, berat molekul dan adanya molekul-molekul lain. Jika
konsentrasi karagenan meningkat maka viskositasnya akan meningkat secara
logaritmik. Viskositas larutan karagenan terutama disebabkan oleh sifat karagenan
sebagai polielektrolit. Gaya tolakan (repulsion) antar muatan-muatan negatif sepanjang rantai polimer yaitu gugus sulfat, mengakibatkan rantai molekul
menegang. Karena sifat hidrofiliknya, polimer tersebut dikelilingi oleh
molekul-molekul air yang termobilisasi, sehingga menyebabkan larutan karagenan bersifat
kental.
Adanya garam-garam yang terlarut dalam karagenan akan menurunkan
muatan bersih sepanjang rantai polimer. Penurunan muatan ini menyebabkan
penurunan gaya tolakan (repulsion) antar gugus-gugus sulfat, sehingga sifat hidrofilik polimer semakin lemah dan menyebabkan viskositas larutan menurun.
sehingga terjadi depolimerisasi yang kemudian dilanjutkan dengan degradasi
karagenan.
2.2.4 Pembentukan gel
Menurut Fardiaz (1989), pembentukan gel adalah suatu fenomena
penggabungan atau pengikatan silang rantai-rantai polimer sehingga terbentuk
suatu jala tiga dimensi bersambungan. Selanjutnya jala ini menangkap atau
mengimobilisasikan air didalamnya dan membentuk struktur yang kuat dan kaku.
Sifat pembentukan gel ini beragam dari satu jenis hidrokoloid ke jenis lain,
tergantung pada jenisnya. Gel mempunyai sifat seperti padatan, khususnya sifat
elastis dan kekakuan.
Kappa-karagenan dan iota-karagenan merupakan fraksi yang mampu
membentuk gel dalam air. Karagenan memiliki kemampuan membentuk gel pada
saat larutan panas menjadi dingin. Proses pembentukan gel bersifat
thermoreversible, artinya gel dapat mencair pada saat pemanasan dan membentuk gel kembali pada saat pendinginan (Gliksman 1983; Imeson 2000).
Proses pemanasan dengan suhu yang lebih tinggi dari suhu pembentukan gel
akan mengakibatkan polimer karagenan dalam larutan menjadi random coil
(acak). Bila suhu diturunkan, maka polimer akan membentuk struktur double helix
(pilinan ganda) dan apabila penurunan suhu terus dilanjutkan polimer-polimer ini
akan terikat silang secara kuat dan dengan makin bertambahnya bentuk heliks
akan terbentuk agregat yang bertanggung jawab terhadap terbentuknya gel yang
kuat. Jika diteruskan, ada kemungkinan proses pembentukan agregat terus terjadi
dan gel akan mengerut sambil melepaskan air. Proses terakhir ini disebut sineresis
(Fardiaz 1989).
Kemampuan pembentukan gel pada kappa dan iota karagenan terjadi pada
saat larutan panas yang dibiarkan menjadi dingin karena mengandung gugus
3,6 -anhidrogalaktosa. Adanya perbedaan jumlah, tipe dan posisi gugus sulfat
akan mempengaruhi proses pembentukan gel. Kappa karagenan dan iota
karagenan akan membentuk gel hanya dengan adanya kation-kation tertentu
seperti K+, Rb+ dan Cs+. Potensi membentuk gel dan viskositas larutan karagenan
akan menurun dengan menurunnya pH, karena ion H+ membantu proses hidrolisis
Konsistensi gel dipengaruhi beberapa faktor antara lain: jenis dan tipe karagenan,
konsistensi, adanya ion-ion serta pelarut yang menghambat pembentukan
hidrokoloid.
2.2.5 Sifat fungsional karagenan
Karagenan berperan sangat penting sebagai stabilisator (pengatur
keseimbangan), thickener (bahan pengentalan), pembentuk gel, pengemulsi dan lain-lain (Imeson 2010). Sifat ini banyak dimanfaatkan dalam industri makanan,
obat-obatan, kosmetik, tekstil, cat, pasta gigi dan industri lainnya.
Penambahan karagenan (0,01-0,05%) pada es krim berfungsi sebagai
stabilisator yang sangat baik. Penambahan karagenan dapat mencegah
pengendapan coklat pada susu coklat dan pemisahan es krim serta meningkatkan
kekentalan kekentalan lemak dan pengendapan kalsium (Winarno 1996).
Karagenan dapat berfungsi sebagai pengikat, melindungi koloid, penghambat
sineresis dan flocculating agent. Karagenan termasuk senyawa hidrokoloid yang banyak digunakan untuk meningkatkan sifat-sifat tektur dan kestabilan suatu
cairan produk pangan (Distantina et al. 2009).
2.3 Nangka
Nangka merupakan tanaman asli India yang kini telah menyebar ke seluruh
dunia, terutama Asia Tenggara. Nangka adalah nama sejenis pohon, sekaligus
buahnya. Pohon nangka termasuk ke dalam suku Moraceae. Dalam bahasa
Inggris, nangka dikenal sebagai Jackfruit. Menurut Iswanto (2008), nangka dengan nama latin Artocarpus heterophyllus memiliki klasifikasi sebagai berikut: Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Urticales
Famili : Moraceae
Genus : Artocarpus
Gambar 2 Buah nangka (Artocarpus heterophyllus) (Anonim 2011).
Pohon nangka (Artocarpus heterophyllus) memiliki tinggi 10-15 m, batangnya tegak, berkayu, bulat, kasar dan berwarna hijau kotor. Daun nangka
(Artocarpus heterophyllus) tunggal, berseling, lonjong, memiliki tulang daun yang menyirip, daging daun tebal, tepi rata, ujung runcing, panjang 5-15 cm, lebar
4-5 cm, tangkai panjang lebih kurang 2 cm dan berwarna hijau. Buah berwarna
kuning ketika masak, oval, dan berbiji coklat muda.
Daging buah nangka yang sesungguhnya adalah perkembangan dari tenda
bunga, berwarna kuning keemasan apabila masak, berbau harum manis yang
keras, berdaging terkadang berisi cairan (nektar) yang manis. Biji berbentuk bulat
lonjong sampai jorong agak gepeng, panjang 2-4 cm, tertutup oleh kulit biji yang
tipis coklat seperti kulit, endokrap yang liat keras keputihan, dan eksokrap yang
lunak.
Tanaman nangka merupakan tanaman yang potensial untuk dikembangkan.
Banyak manfaat yang dapat diambil dari tanaman ini. Hampir semua bagian
tanaman ini dapat dimanfaatkan. Daging buah nangka yang tebal seringkali
diekstrak, dibersihkan, dan dijual dalam keadaan ekstrak segar. Beberapa produk
olahan daging buah nangka yang umum dijumpai adalah: jus, wajik, pasta, dodol,
keripik, sirop, dan produk awetan dalam kaleng. Saat ini juga telah dikembangkan
penelitian mengenai proses pembuatan bubuk konsentrat nangka yang dapat
digunakan sebagai bahan baku dalam pembuatan sari buah, selai, jeli, atau bahan
pemberi flavor pada es krim dan berbagai jenis makanan lainnya. Kandungan gizi
Tabel 1 Komposisi kimia dan zat gizi daging buah nangka per 100 g bahan
Komposisi Satuan Konsentrasi (%)
Air (%bb) % 83,10
Sumber : Departement of Agricultural Malaysia 2001
2.4 Susu Kedelai
Kedelai merupakan tanaman pangan berupa semak yang tumbuh tegak.
Dalam bentuk protein kedelai dapat digunakan sebagai bahan industri makanan
yang diolah menjadi: susu, vetsin, kue-kue, permen dan daging nabati serta
sebagai bahan industri bukan makanan seperti : kertas, cat cair, tinta cetak dan
tekstil (BPPT 2002).
Tabel 2 Komposisi kedelai per 100 garam bahan
Kandungan asam lemak tak jenuh pada susu kedelai lebih besar serta tidak mengandung kolesterol. Kandungan asam lemak tak jenuh diantaranya seperti asam linoleat, asam linolenat dan asam oleat (Winarsih 2010). Susu kedelai
memiliki manfaat lain yaitu untuk mengatasi keluhan menopause pada wanita.
Kandungan protein dalam susu kedelai dipengaruhi oleh varietas kedelai. Susu
kedelai dapat digunakan untuk meningkatkan nilai gizi protein pada nasi dan
makanan serealia lainnya (BPPT 2002).
2.5 Sistem Koloid
Sistem koloid merupakan suatu bentuk campuran yang keadaannya terletak
antara larutan dan suspensi. Koloid merupakan sistem heterogen, suatu larutan
didispersikan ke dalam suatu media yang homogen. Ukuran zat yang
didispersikan berkisar dari satu nanometer (nm) hingga satu micrometer (µm). Zat
yang didispersikan disebut fase terdispersi sedangkan medium yang digunakan
untuk mendispersikan zat disebut medium dispersi. Fase terdispersi bersifat
diskontinu (terputus-putus) sedangkan medium dispersi bersifat kontinu. Contoh
dari sistem koloid ini adalah sabun, susu, santan, jeli, selai , mentega dan
mayonaise (Purba 2006).
2.6 Produk Emulsi
Emulsi merupakan sistem yang tidak stabil terdiri atas dua fase cairan yang
tidak tercampur tetapi cairan yang satu terdispersi dengan baik dalam cairan yang
lain dalam bentuk butiran, sistem ini dibuat stabil dengan adanya suatu zat
pengemulsi (Pakki et al. 2008). Pada suatu emulsi terdapat tiga bagian utama, yaitu bagian yang terdispersi yang terdiri dari butir-butir yang biasanya terdiri dari
lemak, bagian kedua disebut media pendispersi yang juga dikenal sebagai
continuous phase, yang biasanya terdiri dari air, dan bagian ketiga adalah emulsifier yang berfungsi menjaga agar butir minyak tetap tersuspensi di dalam
air.
Emulsifier merupakan bahan pembentuk pasta kental yang dibuat dari bahan
alami (Chan 2010). Penambahan bahan pengemulsi bertujuan menurunkan
emulsi, sedangkan penambahan bahan penstabil bertujuan meningkatkan
viskositas fase kontinu agar emulsi yang terbentuk menjadi stabil (Muctadi 1990).
Pengemulsi yang sering digunakan diantaranya adalah turunan trigliserida,
asam lemak dan gliserol, baik dalam bentuk monogliserida, digliserida dan garam
asam lemak. Bahan pengemulsi ini dapat dijumpai pada produk-produk pangan
yang mengandung campuran minyak atau lemak dengan air. Contoh produk
emulsi yaitu margarin, spread, es krim, desserts beku, cake, pudding dan lainnya.
2.7 Es Krim
Es krim merupakan salah satu produk olahan susu yang dibuat dengan cara
membekukan dan mencampur bahan baku secara bersama-sama. Bahan yang
digunakan biasanya adalah kombinasi susu dengan satu atau lebih bahan
tambahan seperti gula dan madu dengan atau tanpa stabilizer. Dari sistem tersebut
terbentuk sistem emulsi beku. Oleh karena itu, mutu es krim yang dihasilkan akan
sangat dipengaruhi oleh cara pengolahan dan bahan termasuk stabilizer yang
digunakan (Sinurat et al. 2007). Mutu dan jumlah protein di dalam es krim cukup tinggi. Protein tersebut sebagian besar berasal dari susu dan sisanya berasal dari
bahan penstabil.
Marshall dan Arbuckle (2000) mengklasifikasikan beberapa jenis es krim
komersial menjadi nonfat ice cream, lowfat ice cream, light ice cream, reduced fat ice cream, soft serve ice cream, economy ice cream, deluxe ice cream, sherbet, dan ice. Komposisi dari beberapa jenis es krim tersebut sangat bervariasi, menurut Mc Sweeney & PF Fox (2009) komposisi es krim paling baik adalah 12 % lemak,
padatan susu tanpa lemak 11 %, gula 15 %, bahan penstabil dan pengemulsi 0.3 %
dan total padatan 38.3 %. Menurut SNI 01-3713-1995, syarat mutu es krim adalah
Tabel 3 Syarat Mutu Es Krim (SNI 01-3713-1995)
No. Kriteria Uji Satuan Persyaratan
1 Keadaan:
6 Bahan tambahan makanan 4.1 pewarna tambahan
lemak nabati (CFR 2010). Melorin biasanya menjadi pilihan camilan dingin dan
manis. Hal ini disebabkan karena melorin hampir menyerupai es krim, yang
membedakan hanya komposisinya. Produk ini mengandung tidak kurang dari 6 %
lemak, dengan formula, proses pembuatan dan sifat-sifat yang sama seperti es
krim (Hubeis et al. 1996).
Melorin mengandung kadar lemak yang rendah. Lemak yang terkandung
hanya berasal dari sari buah dan sari kedelai. Lemak nabati yang digunakan dalam
melorin dapat berasal dari minyak kelapa, sari kedelai, minyak biji kapas, minyak
2.9 Bahan Tambahan Pangan
Bahan tambahan pangan merupakan senyawa yang sengaja ditambahkan ke
dalam makanan dengan jumlah dan ukuran tertentu dan terlibat dalam proses
pengolahan, pengemasan dan penyimpanan. Tujuan penggunaan bahan tambahan
pangan adalah dapat meningkatkan atau mempertahankan nilai gizi dan kualitas
daya simpan, membuat bahan pangan lebih mudah dihidangkan, serta
mempermudah preparasi bahan pangan (Cahyadi W 2008).
2.9.1 Stabilizer dan Emulsifier
Stabilizer merupakan bahan aditif yang ditambahkan dalam jumlah kecil untuk mempertahankan stabilitas emulsi sekaligus memperbaiki kelembutan
produk, mencegah pembentukan kristal es yang besar, memberikan keseragaman
produk, memberikan ketahanan agar tidak meleleh atau mencair dan memperbaiki
sifat produk. Bahan penstabil dalam pembutan es krim memiliki fungsi sebagai
membantu menahan terjadinya pengkristalan es krim pada saat penyimpanan dan
menstabilkan pengadukan dalam proses pencampuran bahan baku es krim
(Chan 2010).
Bahan penstabil emulsi atau stabilizer adalah bahan yang berfungsi untuk
mempertahankan stabilitas emulsi. Cara kerja bahan penstabil adalah dengan
menurunkan tegangan permukaan dengan cara membentuk lapisan pelindung
yang menyelimuti globula fase terdispersi, sehingga senyawa yang tidak larut
akan lebih mudah terdispersi dalam sistem dan bersifat stabil (Fennema 2008).
Zat-zat yang termasuk dalam bahan penstabil adalah gum arab, gelatin, agar-agar,
natrium alginat, pektin, karagenan dan karboksi metal selulosa (CMC).
2.9.2 Essence
Penambahan aroma dalam makanan sangat penting karena aroma turut
menentukan daya terima konsumen terhadap makanan. Essence digolongkan sebagai bahan tambahan pangan yang dapat memberikan, menambah,
mempertegas aroma dan rasa. Terdapat dua jenis essence yaitu essence alami dan buatan. Essence alami diekstrak dari senyawa aroma yang terdapat pada bahan pangan (ester volatil), sedangkan essence buatan berasal dari sintesis senyawa yang menimbulkan aroma. Penambahan essence buatan bertujuan untuk mencegah hilangnya flavor akibat pemasakan pada suhu tinggi dan waktu
3.1 Waktu dan Tempat
Penelitian dilakukan pada bulan Maret sampai dengan Juli 2011, bertempat
di Laboratorium Formulasi dan Diversifikasi Hasil Perairan, Laboratorium
Organoleptik, Laboraturium Mikrobiologi Hasil Perairan dan Laboratorium
Biokimia Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas
Perikanan dan Ilmu Kelautan; Laboratorium Pangan dan Gizi serta Laboratorium
Pusat Antar Universitas, Departemen Ilmu dan Teknologi Pangan, Fakultas
Teknologi Pertanian, Institut Pertanian Bogor.
3.2 Bahan dan alat
Bahan yang digunakan dalam penelitian penambahan karagenan dalam
proses pembuatan melorin antara lain: susu kedelai, air, gula, buah nangka,
essence nangka dan karagenan (0,00%; 0,02%; 0,04%; 0,06%; 0,08% dan 0,10%), aquades, H2S04 pekat, NaOH 60%, N2S2O3 5%, HCl 0,02 N, dan H2BO3 4%. Alat
yang akan digunakan dalam penelitian ini antara lain adalah baskom, pisau,
talenan, gelas ukur, toples, panci, timbangan digital, blender, soft ice cream maker, refrigerator, freezer, kertas saring, aluminium foil, viscometer brookfield, refraktometer, gelas piala, oven, desikator, labu Kjedahl, pipet dan pH meter.
3.3 Metode Penelitian
Penelitian ini terdiri dari dua tahap, yaitu tahap penelitian pendahuluan dan
tahap penelitian utama.
3.3.1 Tahapan penelitian pendahuluan
Penelitian pendahuluan bertujuan untuk mencari formula terbaik yang diberi
perlakuan dengan formulasi nangka dan susu kedelai dengan penentuan perbedaan
konsentrasi susu kedelai dan nangka. Formula terbaik ini didapatkan dari uji
oragnoleptik dengan 30 panelis semi terlatih dan akan diambil 1 formula melorin
3.3.2 Tahapan penelitian utama
Penelitian utama bertujuan untuk mengetahui pengaruh tingkat konsentrasi
bahan penstabil yang digunakan terhadap mutu melorin. Pengaruh terhadap mutu
melorin ditentukan dari tingkat penerimaan panelis berdasarkan uji organoleptik
serta analisis laboratorium terhadap beberapa sifat fisik dan kimia produk melorin.
Bahan penstabil yang digunakan adalah karagenan. Jenis bahan penstabil
tersebut dipilih karena karakteristik yang dimilikinya. Karagenan berperan penting
dalam mengontrol pembentukan kristal-kristal es dalam produk makanan beku,
mudah dilarutkan dan mempunyai daya ikat air yang tinggi. Tingkat konsentrasi
penstabil yang digunakan sebagai berikut :
Tabel 4 Formula melorin dengan penambahan karagenan
Konsentrasi Bahan Penstabil
Uji organoleptik digunakan untuk menentukan sampel melorin yang paling
disukai. Uji yang dilakukan adalah uji hedonik (uji kesukaan) dengan sembilan
skala numerik menggunakan 30 orang panelis semi terlatih (Lampiran 1). Data
yang diperoleh kemudian diolah dengan menggunakan Statistical Package for Social Science (SPSS) dan Tukey Test sebagai uji lanjut untuk menentukan sampel produk yang berbeda nyata. Untuk mengetahui parameter mutu organoleptik yang
paling penting bagi produk melorin, diterapkan uji pembobotan (Bayes).
Setiap sampel juga dianalisis secara fisik dan kimiawi antara lain derajat
pengembangan, waktu leleh, total padatan terlarut (TPT), stabilitas emulsi, nilai
pH dan viskositas. Sebagai pelengkap, sampel produk terpilih dengan nilai
parameter mutu yang telah diketahui dianalisis kandungan gizinya dengan analisis
kimia yang mencakup analisis kadar air, kadar protein, kadar lemak, kadar
karbohidrat, dan kadar serat pangan.
Penelitian utama terdiri atas proses pembuatan melorin dengan penambahan
organoleptik). Proses pembuatan melorin yang akan ditambahkan karagenan
sebagai bahan penstabil dengan konsentrasi yang berbeda-beda. Alur proses
pembuatan melorinadalah sebagai berikut :
1) Buah nangka dipilih yang matang, masih segar, tidak rusak/cacat dan
tidak busuk. Buah yang telah dipilih dicuci dengan air bersih yang
mengalir kemudian ditiriskan.
2) Buah nangka yang telah dicuci, dibelah dan dipotong ukuran sedang.
3) Potongan-potongan buah nangka dihancurkan dengan menggunakan
blender dengan penambahan sedikit air (buah:air = 2:1).
4) Sementara menunggu pemblenderan buah nangka, karagenan dengan
masing-masing perlakuan dipanaskan dengan 50 ml air sampai
mendidih.
5) Kemudian air (sesuai perbandingan yang telah ditetapkan) dipanaskan
dan gula dicampur bersama hingga larut. Setelah itu, dimasukkan susu
kedelai dan bahan penstabil (karagenan) dicampurkan bersama buah
sambil terus diaduk-aduk selama 10 menit.
6) Bahan yang telah disatukan tersebut, kemudian didinginkan pada suhu
4 oC selama 24 jam.
7) Setelah itu, bahan-bahan yang telah disatukan dan didinginkan (nangka,
susu kedelai,bahan penstabil dan gula) diaduk dan dihomogenkan di
dalam ice cream maker selama 15 menit.
8) Melorin yang telah dihomogenkan, kemudian dikemas dalam cup.
9) Selanjutnya, melorin, dibekukan di dalam freezer dengan suhu -20 oC selama ± 24 jam.
Gambar 3 Diagram alir penelitian pendahuluan formulasi melorin
Buah nangka
Pencucian dan Pemotongan
Pemblenderan
Bubur buah Air, Susu kedelai, Gula,
Pelembut (vx), Esens
Pencampuran
12,5% nangka 10% susu kedelai
15% nangka 10% susu kedelai
12,5% nangka 12,5% susu kedelai
15% nangka 12,5% susu kedelai
Pemasakan 90-95 °C selama 10 menit
Pendinginan cepat (aging) 4 oC selama 24 jam
Penghomogenan SoftIce Maker selama 15 menit
Pemasukan dalam cup es krim
Pengerasan dalam frezeer -20 oC
Gambar 4 Diagram alir penelitian utama penambahan bahan penstabil pada ...melorin terpilih
Buah nangka
Pencucian dan Pemotongan
Pemblenderan
Bubur buah Air, Susu kedelai, Gula,
Pelembut (vx), Esens
Pencampuran 15% nangka; 12,5% susu
kedelai
Penambahan Bahan Penstabil (Karagenan)
0% 0,02%
Pemasakan 90-95 °C selama 10 menit
Pendinginan cepat (aging) 4 oC selama 24 jam
Penghomogenan SoftIce Maker selama 15 menit
Pemasukan dalam cup es krim
Pengerasan dalam frezeer -20 oC
Melorin
0,06%
3.4 Prosedur Analisis
3.4.1 Uji sensori (Rahayu 2001)
Uji sensori dilakukan untuk menilai sifat organoleptik yang spesifik. Uji
sensori dilakukan oleh 30 orang panelis semi terlatih. Skala yang digunakan
adalah skala numerik dengan 9 skala. Data yang diperoleh kemudian diolah
dengan menggunakan Statistical Package for Social Science (SPSS). Pengujian organoleptik ini dilakukan untuk mencari perbandingan terbaik antara nangka,
susu kedelai dan gula untuk ditambahkan pada melorin.
3.4.2. Analisis fisika
Analisis fisika yang dilakukan pada penelitian ini meliputi analisis padatan
total terlarut, viskositas, pengukuran overrun, pengukuran waktu leleh dan stabilitas emulsi.
(1). Total padatan terlarut (Faridah et al. 2008)
Total padatan terlarut dari melorin diukur dengan menggunakan alat
Refraktometer ABBE. Sampel yang akan diukur diteteskan pada prisma
refraktometer. Nilai yang terbaca pada skala batas gelap dan terang menunjukkan
besarnya total padatan terlarut pada produk tersebut dalam satuan % Brix.
(2). Viskositas (Andrawulan dan Palupi 1991)
Viskositas diukur dengan menggunakan alat BrookfieldViscometer. Sampel sebanyak 100 ml ditempatkan ke dalam gelas piala 100 ml. Dengan menggunakan
spindle 2 dan speed 30 rpm, dilakukan pengukuran viskositas sampel. Pengukuran selama 2 menit hingga diperoleh pembacaan jarum pada posisi yang stabil. Rotor
berputar dan jarum akan bergerak sampai diperoleh viskositas sampel. Pembacaan
nilai viskositas dilakukan setelah jarum stabil. Skala yang terbaca menunjukan
kekentalan sampel yang diperiksa dengan satuan cP (centiPoise).
(3). Pengukuran Overrun (Marshall dan Arbuckle 2000)
Pengembangan volume melorindinyatakan sebagai nilai overrun dan dihitung berdasarkan perbedaan volume es krim dengan volume adonan pada
massa yang sama atau perbedaan massa es krim dan massa adonan pada volume
Overrun = � � � −�( � � )
�( � � ) � %
Keterangan :
Wadonan = berat adonan melorin sebelum dibekukan
Wes krim = berat melorin setelah dibekukan
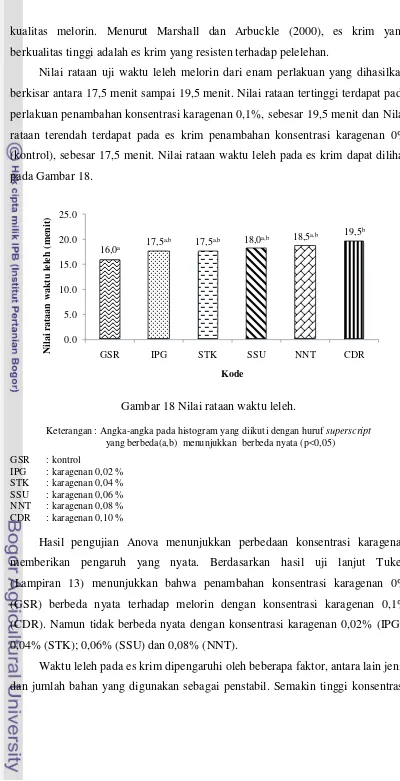
(4). Pengukuran waktu leleh (Roland et al. 1999)
Pengukuran waktu leleh dilakukan terhadap melorin yang telah dikeraskan
selama 24 jam. Waktu leleh diukur dengan cara sebagai berikut: Sebanyak 7,5 g
melorin ditempatkan pada saringan dan ditampung oleh gelas, lalu dibiarkan
mencair seluruhnya pada suhu (25 ± 1) oC. Pengamatan dilakukan pada suhu dan
kelembaban yang sama.
(5). Stabilitas emulsi (AOAC 2005)
Sampel ditimbang sebanyak 5 g dan dimasukkan ke dalam oven bersuhu
45 oC selama 1 jam kemudian dimasukkan ke dalam pendingin bersuhu di bawah
0 oC selama 1 jam. Sampel dimasukkan kembali ke dalam oven bersuhu 45 oC
selama 1 jam dan dibiarkan bobotnya konstan. Pengamatan dilakukan terhadap
kemungkinan terjadinya pemisahan emulsi. Jika terjadi pemisahan, emulsi
dikatakan tidak stabil dan tingkat kestabilannya dihitung berdasarkan persentase
fase terpisah terhadap emulsi keseluruhan. Stabilitas emulsi dapat dihitung dengan
rumus sebagai berikut:
Stabilitas emulsi (%) = x 100%
Keterangan:
Berat fase yang tersisa = (berat emulsi pengovenan kedua + cawan) - berat cawan Berat total bahan emulsi = (berat bahan emulsi + cawan) - berat cawan
3.4.3. Analisis kimia
Analisis kimia yang dilakukan pada penelitian ini meliputi analisis kadar
1). Analisis kadar abu (AOAC 2005)
Sampel basah sebanyak 4 g ditempatkan dalam wadah porselin kemudian
dimasukkan dalam oven dengan suhu 60-105 oC selama 8 jam. Kemudian sampel
yang sudah kering dibakar menggunakan hotplate sampai tidak berasap dengan waktu selama ± 20 menit. Kemudian diabukan dalam tanur bersuhu 600 oC selama
3 jam lalu ditimbang. Untuk menghitung kadar abu digunakan rumus sebagai
berikut :
Kadar abu = ( )
( ) %
2). Analisis kadar air (AOAC 2005)
Cawan kosong yang akan digunakan dikeringkan terlebih dahulu dalam
oven selama 15 menit atau sampai berat tetap, kemudian didinginkan dalam
desikator selama 30 menit dan ditimbang. Sampel kira-kira sebanyak 2 g
ditimbang dan diletakkan dalam cawan kemudian dipanaskan dalam oven
selama 3-4 jam pada suhu 105-110 oC. Cawan kemudian didinginkan dalam
desikator dan setelah dingin ditimbang kembali. Persentase kadar air (berat basah)
dapat dihitung dengan rumus sebagai berikut:
Kadar air = − %
Keterangan :
A = Berat sampel mula-mula (g)
B = Berat sampel setelah dikeringkan (g)
3). Analisis kadar protein (AOAC 2005)
Analisis kadar protein dilakukan dengan metode kjeldahl mikro. Sampel
sebanyak 0,1 g dimasukkan ke dalam labu kjeldahl 30 ml. Kemudian ditambahkan
K2SO4 (1,9 g), HgO (40 mg), H2SO4 (2,5 ml) serta beberapa tablet kjeldahl.
Sampel dididihkan sampai berwarna jernih (sekitar 1-1,5 jam); didinginkan dan
dipindahkan ke alat destilasi. Kemudian dibilas dengan air sebanyak 5-6 kali
dengan akuades (20 ml) dan air bilasan tersebut juga dimasukkan di bawah
kondensor dengan ujung kondensor terendam di dalamnya. Ke dalam tabung
reaksi ditambahkan larutan NaOH 40 % sebanyak 20 ml. Cairan dalam ujung
kondensor ditampung dengan erlenmeyer 125 ml berisi larutan H3BO3 dan 3 tetes
dalam alkohol dengan perbandingan 2:1) yang ada di bawah kondensor. Destilasi
dilakukan sampai diperoleh kira-kira 200 ml destilat yang bercampur dengan
H3BO3 dan indikator dalam erlenmeyer. Destilat dititrasi dengan menggunakan
HCl 0,1 N sampai terjadi perubahan warna menjadi merah. Hal yang sama juga
dilakukan terhadap blanko. Kadar protein dapat dihitung dengan menggunakan
rumus sebagai berikut:
4). Analisis kadar lemak (AOAC 2005)
Sampel diekstrak dengan pelarut heksana. Kemudian pelarut yang
digunakan diuapkan sehingga tersisa lemak dari sampel. Lemak tersebut
kemudian ditimbang dan dihitung presentasenya. Penentuan kadar lemak
dilakukan dengan metode ekstraksi Soxhlet.
Sampel sebanyak 0,5 g ditimbang dan dibungkus dengan kertas saring dan
diletakkan pada alat ekstraksi soxhlet yang dipasang di atas kondensor serta labu
lemak di bawahnya. Pelarut heksana dituangkan ke dalam labu lemak secukupnya
sesuai dengan ukuran soxhlet yang digunakan dan dilakukan refluks selama
minimal 16 jam sampai pelarut turun kembali ke dalam labu lemak. Pelarut di
dalam labu lemak didestilasi dan ditampung. Labu lemak yang berisi lemak hasil
ekstraksi kemudian dikeringkan dalam oven pada suhu 105oC selama 5 jam.
Labu lemak kemudian didinginkan dalam desikator selama 20-30 menit dan
ditimbang. Kadar lemak dapat dihitung berdasarkan rumus:
5). Analisis kadar karbohidrat by fifference (AOAC 2005)
Kadar karbohidrat dihitung dengan menghitung sisa (by difference) yaitu dengan rumus sebagai berikut :
Kadar karbohidrat (%) = 100% - (% air + % abu + % protein + % lemak)
6). Kadar serat pangan
Penentuan kadar serat pangan terdiri dari persiapan sampel dan penetuan
kadar serat pangan tidak larut (IDF) dan serat pangan larut (SDF). Persiapan sampel
a) Sampel homogen diekstrak lemaknya dengan proteleum benzene
pada suhu kamar selama 15 menit, jika kadar lemak sampel
melebihi 6-8%. Penghilangan lemak dari sampel bertujuan untuk
memaksimumkan degradasi pati.
b) Sebanyak 1 ml sampel dimasukkan ke dalam labu Erlenmeyer.
Kemudian ditambahkan 25 ml buffer natrium fosfat dan dibuat
menjadi suspense. Penambahan buffer dimaksudkan untuk
menstabilkan enzim termamyl.
c) Sebanyak 100 µ L termamlyn dimasukkan ke dalam labu
Erlenmeyer. Labu ditutup dan diinkubasi pada suhu 100 oC selama
15 menit, sambil sekali-kali diaduk. Tujuan penambahan termamyl
dan pemanasan adalah untuk memecah pati dengan
menggelatinisasi terlebih dahulu.
d) Labu diangkat dan didinginkan, kemudian ditambahkan 200 ml air
destilata dan pH larutan diatur sampai menjadi 1,5 dengan
menambahkan HCl 4 M. Selanjutnya ditambahkan 100 mg pepsin.
Pengaturan pH hingga 1,5 dimaksudkan untuk mengkondisikan
agar aktivitas enzim pepsin maksimum.
e) Erlenmeyer ditutup dan diinkubasi pada suhu 40 oC dan diagitasi
selama 60 menit.
f) Sebanyak 20 ml air destilata ditambahkan dan pH diatur menjadi
6,8 dengan NaOH. Pengaturan menjadi pH 6,8 ditujukan untuk
g) Ditambahkan 100 mg enzim pankreatin ke dalam larutan. Labu
ditutup dan diinkubasi pada suhu 40 oC selama 60 menit sambil
diagitasi.
h) Selanjutnya pH diatur dengan HCl menjadi 4,5
i) Larutan disaring melalui crucible kering yang telah ditimbang
beratnya (porositas 2) yang mengandung 0,5 g celite kering (serta
tepat diketahui). Kemudian dicuci dengan 2 x 10 ml air destilata
dan diperoleh residu serta filtrat. Residu digunakan untuk
penentuan serat makanan tidak larut, sementara filtrat digunakan
untuk menentukan serat pangan larut.
Penentuan serat pangan tidak larut (IDF)
a) Residu dicuci dengan 2 x 10 ml etanol 95% dan 2 x 10 ml aseton
kemudian dikeringkan pada suhu 105 oC, sampai berat tetap
(sekitar 12 jam) dan ditimbang setelah didinginkan dalam desikator
(D1).
b) Residu diabukan di dalam tanur pada suhu 500 oC selama paling
sedikit 5 jam, lalu didinginkan dalam desikator dan ditimbang
setelah dingin (II).
Penentuan serat pangan larut (SDF)
a) Volume filtrat diatur dengan air sampai 100 ml
b) Sebanyak 400 ml etanol 95% hangat (60 oC) ditambahkan dan
diendapankan selama 1 jam.
c) Larutan disaring dengan crubible kering (porositas 2) yang
mengandung 0,5 g celite kering, kemudian dicuci dengan 2 x 10 ml
etanol 78%, 2 x 10 ml etanol 95% dan aseton 2 x 10 ml.
d) Endapan dikeringkan pada suhu 105 oC selama satu malam
(sampai berat konstan) dan didinginkan dalam desikator dan
ditimbang (D2).
e) Residu diabukan pada tanur suhu 500 oC selama paling sedikit 5
jam, lalu didinginkan dalam desikator dan ditimbang setelah dingin
Penentuan serat pangan total (TDF)
Serat pangan total diperoleh dengan menjumlahkan nilai serat pangan
tidak larut (IDF) dan serat pangan larut (SDF). Blanko yang digunakan
diperoleh dengan metode yang sama, tanpa penambahan sampel. Nilai
blanko yang dipergunakan perlu diperiksa ulang, terutam bila
menggunakan enzim dari kemasan baru.
Rumus perhitungan nilai IDF dan SDF
Nilai IDF (%) = � −� −
� %
Nilai IDF (%) = � −� −
� %
Nilai TDF (%) = Nilai IDF (%) + Nilai SDF (%)
Keterangan :
W= Berat sampel (g)
B= Berat blanko bebas serat (g)
D= Berat setelah analisis dan dikeringkan (g) I= Berat setelah diabukan (g)
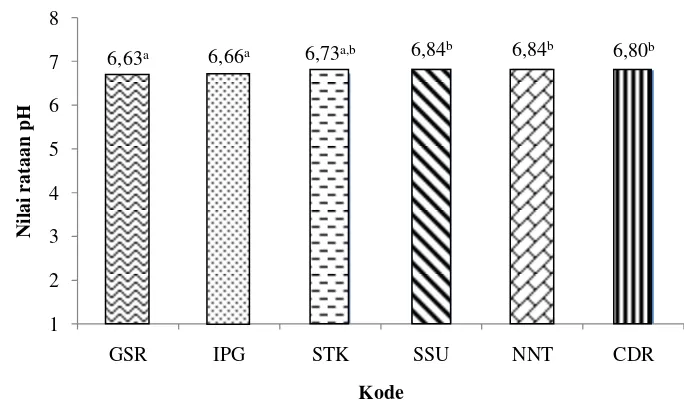
7). Analisis pH (Apriyantono et al. 1989)
Pengukuran pH dilakukan dengan menggunakan pH meter. Melorin diukur
sebanyak 10 ml kemudian dihomogenasi dengan 90 ml air destilat. Kemudian pH
homogenasi diukur dengan menggunakan pH meter yang sebelumnya telah
dikalibrasi dengan buffer standar pH 4 dan 7.
3.4.4 Pengujian Total Plate Count (TPC) (SNI 01-2332.03-2006)
Prinsip kerja dari uji mikrobiologi ini adalah perhitungan jumlah koloni
bakteri yang ada dalam melorindengan pengenceran sesuai keperluan dan
dilakukan secara duplo.Pembuatan larutan sampel dilakukan dengan
mencampurkan 10 ml sampel dalam 90 ml larutan garam fisiologis sampai
homogen.
Pengenceran dilakukan dengan cara mengambil 1 ml larutan sampel dengan
menggunakan pipet steril dimasukkan ke dalam 9 ml larutan garam fisiologis dan
diaduk hingga homogen sehingga terbentuk seri pengenceran 10-1. Pengenceran
dilakukan pada tiap tabung pengenceran sebanyak 1 ml dan dimasukkan ke dalam
cawan petri steril secara duplo dengan menggunakan pipet steril.
Media agar PCA dimasukkan ke dalam cawan petri dan digoyangkan
supaya merata (metode cawan tuang), lalu didiamkan hingga media agar PCA
dingin dan padat.Cawan petri yang berisi agar PCA kemudian dimasukkan ke
dalam inkubator dengan posisi terbalik pada suhu 35oC dan diinkubasi selama
2 x 24 jam. Masa inkubasi berakhir, kemudian dihitung jumlah koloni bakteri
yang ada di dalam cawan petri. Jumlah koloni yang dapat dihitung adalah cawan
petri yang mempunyai koloni bakteri antara 25-250.
3.4.5 Rancangan Percobaan dan Analisis Data
Penelitian ini dilakukan dengan model Rancangan Acak Lengkap (RAL)
dengan model sebagai berikut :
Ŷij = µ + αi + εij
Dimana :
Ŷij = respon yang diamati
µ = efek nilai tengah/nilai rata-rata sebenarnya αi = pengaruh perlakuan α pada taraf ke-i
εij = galat (error) dari perlakuan pada taraf ke-i dan ulangan ke-j
Hipotesis yang diuji pada pembuatan melorin dengan penambahan
konsentrasi karagenan adalah sebagai berikut :
H0 = Penambahan konsentrasi karagenan yang berbeda tidak berpengaruh nyata
terhadap karakteristik melorin yang dihasilkan.
Hi = Penambahan konsentrasi karagenan yang berbeda berpengaruh nyata
terhadap karakteristik melorin yang dihasilkan.
Data peubah yang diamati dianalisis secara statistik dengan analisis ragam.
Pengujian lanjut Tukey dilakukan jika analisisnya berpengaruh nyata. Analisis
non-parametrik yang dilakukan dalam pengujian adalah metode uji Kruskal
Wallis, yaitu :
a) Meranking data dari yang terkecil ke yang terbesar untuk seluruh
perlakuan dalam satu parameter.
b) Menghitung total ranking dan rataan untuk setiap perlakuan dengan
�= 12 ( + 1)
��
−3( + 1)
�′ = �
�
Pembagi = 1− T
n−1 n(n + 1), dimana T = t−1 t(t + 1)
Keterangan:
n = Banyaknya pengamatan dalam perlakuan Ri = Jumlah ranking dalam perlakuan ke-i
4 HASIL DAN PEMBAHASAN
4.1 Penelitian Pendahuluan
Penelitian pendahuluan meliputi formulasi melorin terbaik yang akan
digunakan pada penelitian utama. Formulasi melorin dilakukan dengan pengujian
berbagai perbandingan komposisi nangka dan susu kedelai. Karakterisasi
karagenan dilakukan terlebih dahulu untuk mengetahui standar mutu karagenan
yang digunakan.
4.1.1 Karakterisasi karagenan
Karagenan yang digunakan dalam penelitian diperoleh dari CV Dinar.
Karagenan tersebut dianalisis terlebih untuk mengetahui mutu karagenan yang
akan dipakai dalam penelitian utama. Hasil analisis karakterisasi karagenan
meliputi kadar air, kadar abu, viskositas dan kekuatan gel dapat dilihat pada
Tabel 5.
Tabel 5 Hasil analisis karakteristik karagenan
Parameter Hasil uji Standar*
Kadar Air 14,75 ± 0,12 Max. 12
Tabel 5 memperlihatkan bahwa secara keseluruhan mutu karagenan telah
memenuhi standar mutu karagenan komersil, terutama untuk parameter kekuatan
gel dan viskositas. Karagenan yang digunakan merupakan hasil ekstraksi
campuran antara rumput laut jenis Euchemacottonii dan Euchemaspinosum. Viskositas karagenan hasil penelitian dari kombinasi kappa dan iota
karagenan berada di atas standar viskositas yang ditetapkan oleh FAO dan EU,
yaitu minimal 5 cPs. Hal tersebut kemungkinan dipengaruhi oleh kandungan
sulfat yang ada pada karagenan. Kandungan sulfat dapat menyebabkan larutan
menjadi kental. Adanya sulfat akan menyebabkan terjadinya gaya tolak menolak
antar kelompok ester yang bermuatan sama dengan molekul air yang terikat dalam
polielektrolit. Gaya tolakan antar muatan negatif sepanjang rantai polimer, yaitu
gugus sulfat, akan mengakibatkan rantai molekul menegang (Warkoyo 2007).
Hasil analisis kekuatan gel karagenan adalah 385,63 (g/cm2). Konsistensi
gel dipengaruhi oleh beberapa faktor, antara lain yaitu jenis dan tipe karagenan,
kosentrasi dan adanya ion-ion serta pelarut yang menghambat pembentukan
hidrokoloid. Hal lain yang dapat mempengaruhi gel karagenan yaitu letak gugus
sulfat pada struktur molekulnya. Kadar gugus sulfat tersebut dapat mempengaruhi
kekuatan gel dari karagenan karena tingginya kadar sulfat dapat menyebabkan
terputusnya ikatan 3,6-anhidro-D-galaktosa sehingga kekuatan gelnya menurun.
Ester sulfat terkandung dalam karagenan berkisar 25% untuk kappa karagenan,
serta 32% untuk iota karagenan, sedangkan lambda karagenan mengandung 35%
ester sulfat (Imeson 2010).
Kadar abu karagenan hasil analisis adalah sebesar 14,00%. Kadar abu yang
didapat lebih rendah dari standar yang ditetapkan oleh FAO (2007) yang berkisar
antara 15-40%. Menurut Winarno (1996), tingginya kadar abu karagenan
dipengaruhi oleh adanya garam dan mineral lain yang menempel pada rumput laut
seperti natrium, kalsium dan kalium.
Nilai kadar air karagenan yang digunakan pada penelitian ini adalah sebesar
14.75%. Kadar air suatu produk sangat penting karena terkait dengan daya simpan
produk dan kualitasnya. Kadar air hidrokoloid yang diinginkan rata-rata di bawah
20% untuk standar pasaran internasional (Angka dan Suhartono 2000).
4.1.2 Karakteristik sensori
Penelitian pendahuluan meliputi karakteristik sensori produk melorin.
Karakteristik sensori dilakukan untuk menentukan formula terbaik (yang
mempunyai daya terima tertinggi) dari produk melorin yang meliputi warna,
aroma, tekstur, rasa dan mouthfeel. Penilaian sensori menjadi parameter utama dalam menentukan formula terbaik untuk penelitian utama.
(1) Warna
Warna merupakan salah satu faktor yang mempengaruhi daya terima
konsumen. Penerimaan warna suatu bahan pangan berbeda-beda tergantung dari
faktor alam, geografis dan aspek sosial masyarakat penerima (Winarno 2008).
kuning pucat sampai kuning. Hasil pengujian sensori parameter warna melorin
menunjukkan nilai antara 5,80-6,83. Nilai rataan terendah dimiliki oleh melorin
dengan konsentrasi susu kedelai dan nangka masing-masing 12,5% (perlakuan C),
sedangkan nilai rataan tertinggi dimiliki oleh melorin dengan konsentrasi susu
kedelai dan nangka masing-masing 10% dan 15% (perlakuan B). Nilai rataan
parameter warna melorin dapat dilihat pada Gambar 5.
Gambar 5 Nilai rataan parameter warna melorin.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
yang berbeda (a,b) menunjukkan berbeda nyata (p<0,05)
A :12,5 % nangka; 10 % susu kedelai B : 15 % nangka; 10 % susu kedelai C : 12,5 % nangka; 12,5 % susu kedelai D : 15 % nangka; 12,5 % susu kedelai
Hasil pengujian Kruskall wallis menunjukkan perbedaan konsentrasi antara susu kedelai dan nangka pada melorin memberikan pengaruh nyata (p<0,05)
terhadap warna melorin yang dihasilkan (Lampiran 2). Hasil uji lanjut multiple comparisons (Lampiran 3) menunjukkan bahwa penambahan konsentrasi susu kedelai dan buah nangka pada perlakuan B berbeda nyata dengan perlakuan C.
Namun perlakuan C tidak berbeda nyata dengan perlakuan D.
Warna kuning pada melorin dihasilkan dari buah nangka yang digunakan.
Warna kuning disebabkan oleh salah satu faktor seperti tingkat kematangan.
Nangka akan berwarna kuning keemasan ketika matang. Pigmen warna kuning ini
dsebabkan pigmen yang tergabung dalam kelompok xanthofil. Xanthofil terdiri
dari beberapa macam dan yang paling umum adalah zeaxanthin. Zeaxanthin
kuning, orange, merah orange (Astawan & Andreas 2008). Semakin tinggi
konsentrasi buah nangka yang ditambahkan maka warna es krim yang dihasilkan
menjadi lebih kuning sehingga meningkatkan kesukaan panelis.
(2) Aroma
Aroma merupakan salah satu daya tarik bagi panelis dalam menentukan
nilai kesukaan terhadap suatu produk. Timbulnya aroma atau bau ini karena zat
bau tersebut bersifat volatil (mudah menguap). Oleh karena itu penilaian sensori
tingkat kesukaan aroma perlu dilakukan dalam penelitian ini. Nilai rataan
parameter aroma melorin dapat dilihat pada Gambar 6.
Gambar 6 Nilai rataan parameter aroma melorin.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
yang berbeda (a,b,c) menunjukkan berbeda nyata (p<0,05)
A : 12,5 % nangka; 10 % susu kedelai B : 15 % nangka; 10 % susu kedelai C : 12,5 % nangka; 12,5 % susu kedelai D : 15 % nangka; 12,5 % susu kedelai
Hasil pengujian sensori terhadap parameter aroma menunjukkan nilai rataan
berkisar antara 4,83-7,00. Nilai rataan tertinggi dimiliki oleh melorin dengan
konsentrasi susu kedelai dan nangka masing-masing 15% dan 12,5%
(perlakuan D). Nilai rataan terendah dimiliki oleh konsentrasi nangka 12,5% dan
susu kedelai 12,5% (perlakuan C). Hasil pengujian Kruskall wallis menunjukkan perbedaan konsentrasi antara susu kedelai dan nangka mempengaruhi aroma pada
melorin. Gambar 5 menunjukkan bahwa perbedaan kosentrasi susu kedelai dan
nangka memberikan pengaruh nyata terhadap aroma melorin yang dihasilkan.
Hasil uji lanjut multiple comparisons (Lampiran 4) yang dilakukan menunjukkan bahwa perlakuan A berbeda nyata terhadap perlakuan C dan
perlakuan D, namun tidak berbeda nyata terhadap perlakuan B.
Aroma es krim lebih banyak dipengaruhi oleh sumber lemak yang
digunakan. Lemak yang digunakan dalam penelitian ini berasal dari lemak nabati,
yaitu susu kedelai. Susu kedelai memiliki asam lemak yang menyebabkan bau
langu. Asam lemak pada kedelai mempunyai sifat tidak larut air panas dan air
dingin serta sedikit menguap. Asam lemak tak jenuh pada kedelai yang tinggi
berpengaruh terhadap bau langu karena enzim lipoksidase. Enzim lipoksidase
akan menghidrolisis atau menguraikan lemak kedelai menjadi senyawa penyebab
bau langu yang tergolong pada kelompok heksanal dan heksanol. Senyawa
tersebut dalam konsentrasi rendah sudah dapat menyebabkan bau langu
(Winarsih 2010). Penambahan buah nangka dalam melorin selain sebagai
penambah energi, juga untuk menutupi bau langu dari susu kedelai. Semakin
tinggi konsentrasi buah nangka yang ditambahkan, maka aroma langu dari susu
kedelai dapat tertutupi, sehingga tingkat kesukaan panelis meningkat.
(3) Tekstur
Tekstur es krim dibentuk oleh rongga-rongga udara yang terdispersi di
dalam kristal-kristal es (sistem koloid berupa buih padatan) sehingga es krim
mempunyai konsistensi dan rasa yang unik. Tekstur es krim yang ideal adalah
halus dan partikel padatan terlalu kecil untuk dirasakan mulut.
Hasil pengujian sensori terhadap parameter tekstur menunjukkan nilai rataan
berkisar antara 5,93-6,43. Nilai rataan tertinggi dimiliki oleh melorin dengan
konsentrasi susu kedelai dan nangka masing-masing 15% dan 10% (6,43). Nilai
rataan terendah dimiliki oleh konsentrasi nangka 15% dan susu kedelai 10 %
(perlakuan B) (5,93). Hasil pengujian Kruskall wallis yang dilakukan menunjukkan perbedaan konsentrasi antara susu kedelai dan nangka tidak
mempengaruhi kesukaan panelis terhadap tekstur melorin. Nilai rataan parameter
Gambar 7 Nilai rataan parameter tekstur melorin.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
menunjukkan tidak berbeda nyata (p>0,05)
sangat berperan dalam kelezatan tekstur es krim. Penggunaan susu kedelai sebagai
substitusi penggunaan lemak susu menyebabkan melorin memiliki tekstur tidak
menyerupai es krim. Hal ini disebabkan melorin dalam penelitian ini tidak
menggunakan lemak hewani sebagai sumber lemak. Melorin merupakan produk
dengan sifat-sifat menyerupai es krim, namun menggunakan sumber lemak selain
lemak susu dengan kadar minimal 6% (Hubeis et al. 1996). Lemak susu merupakan bahan baku utama untuk membuat es krim. Marshall et al. (2003), menyatakan bahwa lemak susu berperan dalam pembentukan tekstur es krim yang
lembut, sebagai sumber citarasa dan kalori, meningkatkan nilai gizi dan mencegah
pembentukan kristal es yang besar selama pembekuan es krim.
(4) Rasa
Rasa adalah turunan dari sebagian komponen yang terkait dalam air liur
selama makanan dicerna secara mekanis di mulut. Rasa merupakan sensasi yang
terbentuk dari hasil perpaduan bahan pembentuk dan komposisinya pada suatu
produk makanan yang ditangkap oleh indra pengecap. Suatu produk dapat
diterima oleh konsumen apabila memiliki rasa yang sesuai dengan yang
kimia, suhu, konsentrasi dan interaksi dengan komponen rasa lain
(Winarno 2008).
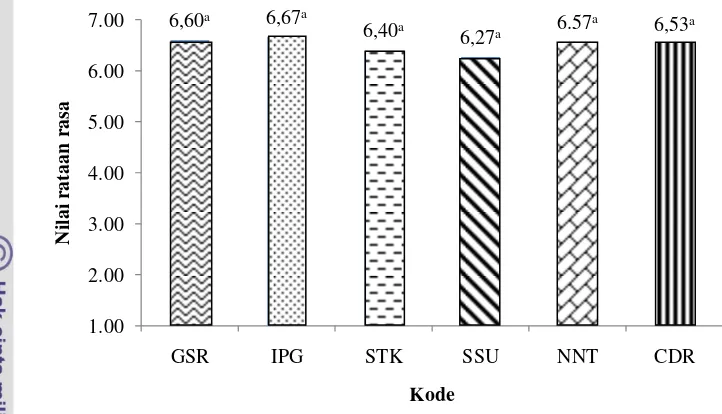
Hasil pengujian sensori parameter rasa menunjukkan nilai rataan antara
5,00-6,73. Nilai rataan tertinggi dimiliki oleh melorin dengan konsentrasi nangka
15% dan susu kedelai 12,5% (perlakuan D). Nilai rataan terendah dimiliki oleh
melorin dengan konsentrasi nangka 12,5% dan susu kedelai 12,5% (perlakuan C).
Hasil pengujian Kruskall wallis pada perbedaan konsentrasi susu kedelai dan nangka memberikan pengaruh nyata terhadap rasa melorin yang dihasilkan. Nilai
rataan parameter rasa dapat dilihat pada Gambar 8.
Gambar 8 Nilai rataan parameter rasa melorin.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
yang berbeda (a,b,c) menunjukkan berbeda nyata (p<0,05)
A : 12,5 % nangka; 10 % susu kedelai B : 15 % nangka; 10 % susu kedelai C : 12,5 % nangka; 12,5 % susu kedelai D : 15 % nangka; 12,5 % susu kedelai
Hasil uji lanjut Multiple Comparisons (Lampiran 5) menunjukkan bahwa perlakuan D berbeda nyata terhadap perlakuan C; perlakuan B dan perlakuan A.
Hal ini disebabkan rasa melorin tersebut sangat dipengaruhi oleh nangka dan susu
kedelai yang digunakan. Penggunaan kombinasi yang tepat antara susu kedelai
dan nangka akan menghasilkan rasa melorin yang disukai oleh panelis. Daging
buah nangka memiliki cairan nektar yang manis. Menurut Sinurat (2007), panelis
(5) Mouthfeel
Mouthfeel merupakan salah satu parameter penting yang terdapat dalam es krim. Parameter ini menjadi pertimbangan oleh konsumen menilai suatu produk.
Nilai rataan parameter mouthfeel dapat dilihat pada Gambar 9.
Gambar 9 Nilai rataan parameter mouthfeel.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
menunjukkan tidak berbeda nyata (p>0,05)
A : 12,5 % nangka; 10 % susu kedelai B : 15 % nangka; 10 % susu kedelai C : 12,5 % nangka; 12,5 % susu kedelai D : 15 % nangka; 12,5 % susu kedelai
Hasil pengujian sensori pada parameter mouthfeel berkisar antara 6,36-6,73. Nilai rataan tertinggi dimiliki oleh melorin dengan konsentrasi nangka 15% dan
susu kedelai 12,5% (perlakuan D). Nilai rataan terendah dimiliki oleh konsentrasi
nangka 12,5% dan susu kedelai 12,5% (perlakuan C). Hasil pengujian Kruskall Wallis terhadap parameter mouthfeel menunjukkan perlakuan konsentrasi nangka dan susu kedelai tidak memberikan pengaruh yang berbeda nyata terhadap
mouthfeel yang dihasilkan, sehingga tidak dilakukan uji lanjut. Mouthfeel dan rasa adalah contoh salah satu parameter yang penting dirasakan oleh panelis terlatih.
Zat yang mudah menguap disebabkan oleh reaksi transfer proton yang terkumpul
pada spektrometri untuk menentukan efek hidrokoloid pada bagian komponen
rasa (Escamilla et al. 2007). Ketika pelelehan terjadi di dalam mulut, partikel-partikel es yang berukuran lebih besar tertinggal sebentar di dalam mulut dan
4.2 Penelitian Utama
Penelitian utama bertujuan untuk mengetahui tingkat konsentrasi terbaik bahan penstabil yang digunakan terhadap mutu melorin. Bahan penstabil yang
digunakan adalah karagenan. Karagenan yang digunakan sebelumnya telah
dianalisis. Tahap ini meliputi uji sensori, uji fisik, uji kimia dan uji mikrobiologi
terhadap melorin.
4.2.1 Uji sensori
(1) Warna
Warna produk es krim harus menarik dan menyenangkan konsumen,
seragam, serta dapat mewakili citarasa yang ditambahkan. Nilai rataan parameter
warna melorin dapat dilihat pada Gambar 10.
Gambar 10 Nilai rataan parameter warna.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
menunjukkan tidak berbeda nyata (p>0,05)
Hasil pengujian sensori parameter warna melorin menunjukkan nilai rataan
antara 6,10-6,50. Nilai rataan terendah dimiliki oleh melorin dengan konsentrasi
karagenan 0,08% dan 0,1%, sedangkan nilai rataan tertinggi dimiliki oleh melorin
dengan konsentrasi karagenan 0% (kontrol). Hasil uji Kruskalwallis (Lampiran 6) 6,50a
GSR IPG STK SSU NNT CDR
yang dilakukan dalam penambahan konsentrasi karagenan tidak memberikan
pengaruh yang berbeda nyata terhadap warna yang dihasilkan.
Panelis tidak dapat membedakan warna antara perlakuan, karena tidak
digunakan pewarna khusus. Panelis umumnya menilai bahwa produk melorin
berwarna kuning, dimana warna ini didominasi oleh perpaduan nangka dan susu
kedelai. Hidrokoloid yang ditambahkan tidak mengandung bahan-bahan volatil
yang dapat menimbulkan aroma dan warna pada bahan pangan, akan tetapi
hidrokoloid dapat memberikan efek sinergis pada penambahan citarasa ke dalam
emulsi (Phillips & Williams 2000).
(2) Aroma
Gambar 11 Nilai rataan parameter aroma.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
menunjukkan tidak berbeda nyata (p>0,05)
GSR IPG STK SSU NNT CDR
Hasil pengujian sensori terhadap parameter aroma menunjukkan nilai rataan
berkisar antara 6,47-6,67. Nilai rataan aroma tertinggi dimiliki oleh melorin
dengan konsentrasi karagenan 0% (GSR) dan 0,02% (IPG). Nilai rataan aroma
terendah dimiliki oleh konsentrasi karagenan 0,1% (CDR). Hasil pengujian
Kruskall wallis (Lampiran 6) yang dilakukan penambahan konsentrasi karagenan tidak memberikan pengaruh yang berbeda nyata terhadap aroma melorin.
Gambar 11 dapat diketahui bahwa nilai rataan tingkat kesukaan panelis
terhadap aroma mengalami penurunan. Hal ini kemungkinan disebabkan oleh
penambahan bahan penstabil, yang memerangkap sebagian komponen aroma di
dalam adonan, terutama bila adonan tersebut mempunyai kekentalan yang lebih
tinggi. Namun secara umum aroma yang dihasilkan berasal dari penambahan buah
nangka dan essens, sehingga penggunaan karagenan terhadap aroma tidak tampak.
(3) Rasa
Rasa dipengaruhi oleh beberapa faktor, diantaranya adalah senyawa kimia,
suhu, konsentrasi dan interaksi dengan komponen rasa lain (Winarno 2008). Rasa
dari suatu makanan merupakan gabungan dari berbagai macam rasa bahan yang
digunakan dalam makanan tersebut.
Hasil pengujian sensori parameter rasa menunjukkan nilai rataan antara
6,27-6,67. Nilai rataan tertinggi dimiliki oleh melorin dengan konsentrasi
karagenan 0,02% (IPG). Nilai rataan terendah dimiliki oleh melorin dengan
konsentrasi karagenan 0,06% (SSU).
Hasil pengujian Kruskall wallis menunjukkan penambahan karagenan tidak berpengaruh nyata terhadap rasa melorin yang dihasilkan. Penambahan karagenan
terhadap rasa tampaknya kurang dikenali oleh panelis. Konsentrasi karagenan
yang ditambahkan termasuk rendah sehingga tidak berhasil dikenali oleh panelis.
Gambar 12 Nilai rataan parameter rasa.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
menunjukkan tidak berbeda nyata (p>0,05)
Rasa yang dihasilkan ditimbulkan oleh gula, nangka dan susu kedelai. Rasa
es krim juga dipengaruhi oleh essens yang ditambahkan. Penambahan essens
bertujuan mencegah hilangnya flavor akibat pemasakan pada suhu tinggi dan
waktu pemasakan lebih lama (Jufrebriyanti 2007). Selain itu, rasa es krim
dipengaruhi pula oleh suhu produk saat disantap (Marshall dan Arbuckle 2000).
Es krim akan terasa lebih manis dengan meningkatnya suhu produk saat disantap.
(4) Tekstur
Tekstur suatu produk es krim dibentuk oleh kristal-kristal es yang
terdispersi didalam gelembung-gelembung udara sehingga es krim mempunyai
konsistensi dan rasa yang unik. Nilai rataan tingkat kesukaan panes terhadap
tekstur dapat dilihat pada Gambar 13. 6,60a 6,67a
GSR IPG STK SSU NNT CDR
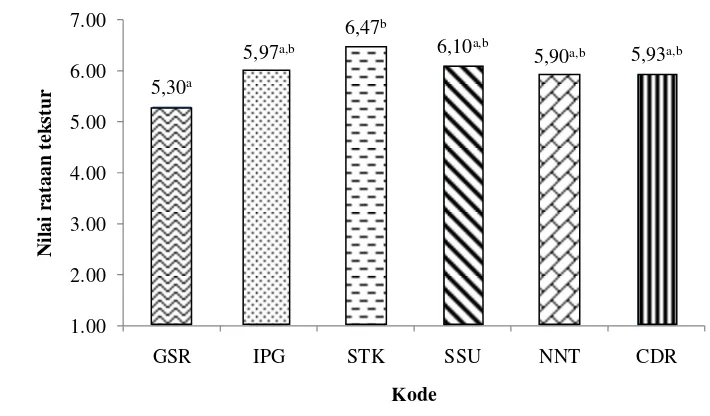
Gambar 13 Nilai rataan parameter tekstur.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
Yang berbeda (a,b) menunjukkan berbeda nyata (p<0,05)
Nilai rataan penilaian sensori terhadap parameter tekstur berkisar 5,30-6,47.
Nilai rataan tertinggi dimiliki oleh melorin dengan kosentrasi karagenan 0,04%
dan nilai rataan terendah dimiliki oleh melorin dengan konsentrasi karagenan 0%
(kontrol). Hasil uji lanjut multiple comparisons (Lampiran 7) menunjukkan bahwa penambahan konsentrasi karagenan 0% (GSR) berbeda nyata terhadap melorin
dengan konsentrasi karagenan 0,04% (STK) namun tidak berbeda nyata terhadap
melorin dengan konsentrasi karagenan 0,02% (IPG); 0,06% (SSU); 0,08% (NNT)
dan konsentrasi 0,1% (CDR).
Tekstur produk es krim ditentukan oleh padatan dalam adonan, konsentrasi
gula dan kekentalan. Gula akan menghalangi pembekuan produk, karena molekul
gula akan menarik molekul air sehingga mengganggu pembentukan kristal-kristal
es. Gula dapat membantu mencegah pembentukan kristal es yang besar, sehingga
tekstur yang dihasilkan lebih lembut (Clarke 2004).
Faktor lain yang mempengaruhi tekstur es krim adalah penambahan bahan
penstabil dan pengemulsi (Aime et al. 2001). Penambahan bahan penstabil ke
GSR IPG STK SSU NNT CDR
dalam adonan es krim akan mencegah pembentukan kristal es yang besar,
memberikan ketahanan agar tidak cepat meleleh atau mencair dan memperbaiki
tekstur produk (Soukoulis et al. 2008). Tekstur es krim dipengaruhi oleh viskositas. Semakin tinggi viskositas maka semakin rendah nilai overrun
sehingga, mengakibatkan tekstur melorin menjadi keras dan menurunkan
palatabilitas panelis.
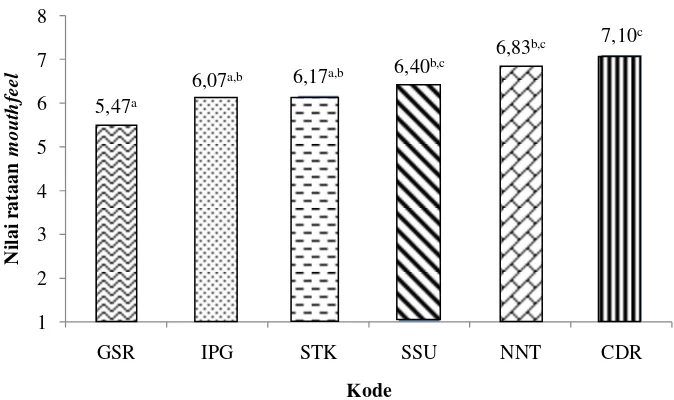
(5) Mouthfeel
Mouthfeel adalah sensasi yang ditimbulkan ketika es krim masuk ke dalam mulut. Apakah waktu meleleh dimulut cepat dan partikel es terasa lembut. Nilai
rataan mouthfeel berkisar antara 5,47-7,10. Rataan nilai tertinggi dimiliki oleh melorin dengan konsentrasi karagenan 0%, sedangkan rataan terendah dimiliki
oleh melorin dengan konsentrasi karagenan 0,1%.
Hasil pengujian Kruskall Wallis terhadap parameter mouthfeel menunjukkan perbedaan konsentrasi karagenan memberikan pengaruh yang nyata. Berdasarkan
hasil uji lanjut multiple comparisons (Lampiran 8) menunjukkan bahwa penambahan konsentrasi karagenan 0% (GSR) berbeda nyata terhadap melorin
dengan konsentrasi karagenan 0,06% (SSU); konsentrasi karagenan 0,08% (NNT)
dan konsentrasi 0,1% (CDR). Namun tidak berbeda nyata dengan konsentrasi
karagenan 0,02% (IPG) dan 0,04% (STK).
Penambahan karagenan berfungsi mengikat molekul air di dalam es krim
sehingga partikel es menjadi lebih kecil dan tidak terlalu terdeteksi oleh lidah saat
es krim dimakan. Hal ini menunjukkan semakin tingggi konsentrasi karagenan
Gambar 14 Nilai rataan parameter mouthfeel.
Keterangan : Angka-angka pada histogram yang diikuti dengan huruf superscript
yang berbeda(a,b,c) menunjukkan berbeda nyata (p<0,05) jumlah bahan pengemulsi dan penstabil yang digunakan, proses pengadukan, serta
suhu dan waktu pembekuan (Marshall dan Arbuckle 2000). Konsentrasi
karagenan yang tinggi menyebabkan adonan es krim lebih kental dan lebih tahan
terhadap pelelehan sehingga ketika didalam mulut es krim tidak langsung cepat
meleleh. Walaupun menghasilkan perubahan tekstur dan mouthfeel yang diinginkan penambahan hidrokoloid akan menyebabkan berkurangnya rasa dalam
es krim (Escamilla FJ et al. 2007).
4.2.2 Uji Fisik
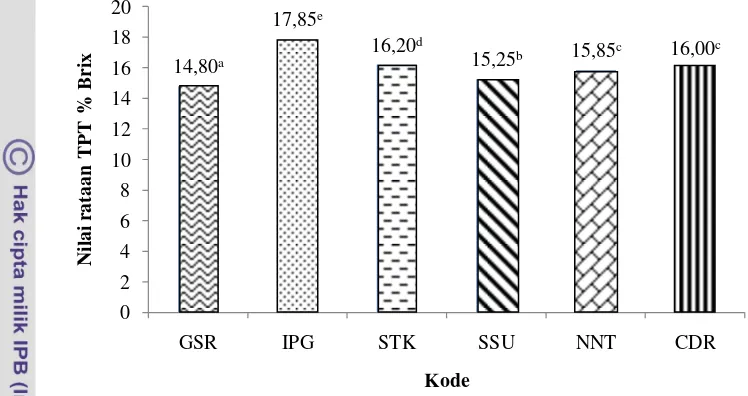
1. Total padatan terlarut
Total padatan terlarut (TPT) merupakan bahan-bahan terlarut dalam air
yang tidak tersaring dengan kertas saring millipore dengan ukuran pori 0,45 µm. Padatan ini terdiri dari senyawa-senyawa anorganik dan organik yang terlarut
dalam air, mineral dan garam-garamnya. Total padatan terlarut umumnya 5,47a
GSR IPG STK SSU NNT CDR