KARAKTERISTIK DAN EFEKTIVITAS PENETRASI
KAFEIN TERJEBAK DAN TERSALUT NANOPARTIKEL
KITOSAN SEBAGAI ANTISELULIT
CANDRA KIRANA HARTUTI SAPUTRO
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK
CIPTA
Dengan ini saya menyatakan bahwa skripsi dengan judul “Karakteristik dan Efektivitas Penetrasi Kafein Terjebak dan Tersalut Nanopartikel Kitosan sebagai Antiselulit.” adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2013
ABSTRAK
CANDRA KIRANA HARTUTI SAPUTRO. Karakteristik dan Efektivitas Penetrasi Kafein Terjebak dan Tersalut Nanopartikel Kitosan sebagai Antiselulit. Dibimbing oleh PIPIH SUPTIJAH dan JOSHITA DJAJADISASTRA.
Kitosan banyak digunakan sebagai penghantar obat karena bersifat polikationik alami dan mudah dimodifikasi dalam sifat kimia maupun fisiknya. Penelitian ini memodifikasi sifat kimia dengan menyalutkan dan menjebak zat aktif antiselulit berupa kafein sedangkan sifat fisiknya dengan memperkecil ukuran partikel kitosan menjadi ukuran nanopartikel. Tujuan penelitian ini adalah mengkarakterisasi nanopartikel kitosan berupa morfologi, ukuran partikel, gugus fungsi, dan nilai efisiensi penjerapan serta membuktikan efektivitas nanopartikel kitosan terhadap penetrasi kafein sebagai antiselulit secara In Vitro menggunakan sel difusi Franz. Pengujian karakterisasi perlakuan kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan menghasilkan morfologi permukaan yang halus, sedikit cembung, dan masih menggumpal; ukuran rata-rata berturut-turut sebesar 232,74 nm dan 226,62 nm; gugus fungsi memiliki adanya pergeseran bilangan gelombang yaitu gugus amida III (-CN) dan gugus hidroksil (-OH); nilai efisiensi penjerapan kafein berturut-turut sebesar 51,35% dan 64,63%. Hasil nilai efektifitas penetrasi berturut-turut 1,089,65 ± 10,7 µg/cm2 dan 2,170,03 ± 6,85 µg/cm2.
Kata kunci: antiselulit; kafein; kitosan; nanopartikel kitosan.
ABSTRACT
CANDRA KIRANA HARTUTI SAPUTRO. Characterization and Effectiveness Penetrasion of Caffeine Trapped and Coated Chitosan Nanoparticles as Anti-cellulite. Supervised by PIPIH SUPTIJAH and JOSHITA DJAJADISASTRA
Chitosan used as drug carrier because of is natural polycationic and easily modified in chemical and physical properties. In this research chitosan was chemically modified by coating and entrapping anti-cellulite active substance of caffeine and physically modified by minimizing chitosan particle size into nanoparticles size. The purpose of this research is to characterize the chitosan nanoparticles from its morphology, particle size, function of group, the value of adsorption efficiency, and effectiveness of chitosan nanoparticles against in vitro penetration of caffeine as anti-cellulite using Franz diffusion cell. The morphology characterization test of caffeine trapped in chitosan nanoparticles and caffeine coated by chitosan nanoparticles resulting a smooth surface, slight convex shape, and agglomerated particles; average size of particles are 232.74 nm and 226.62 nm respectively; the function group showed a shift of wave number of amide III groups (-CN) and hydroxyl groups (-OH); the caffeine adsorption efficiency are 51,35% and 64,63% respectively. The result of effective penetration are 1.089.65 ± 10.7 µg/cm2 and 2.170.03 ± 6.85 µg/cm2 respectively.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan dan Ilmu Kelautan
pada
Departemen Teknologi Hasil Perairan
KARAKTERISTIK DAN EFEKTIVITAS PENETRASI
KAFEIN TERJEBAK DAN TERSALUT NANOPARTIKEL
KITOSAN SEBAGAI ANTISELULIT
CANDRA KIRANA HARTUTI SAPUTRO
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Karakteristik dan efektivitas penetrasi kafein terjebak dan tersalut nanopartikel kitosan sebagai antiselulit
Nama : Candra Kirana Hartuti Saputro NIM : C34090057
Program Studi : Teknologi Hasil Perairan
Disetujui oleh
Dr. Pipih Suptijah, MBA Pharm.Dr.Joshita Djajadisastra, MS, Ph.D
Pembimbing I Pembimbing II
Diketahui oleh
Dr. Ir. Ruddy Suwandi. MS, M.Phil Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT, atas berkat rahmat dan anugerah-NYA penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini dilaksanakan pada bulan Maret hingga Juni 2013 dengan judul Karakteristik dan efektivitas penetrasi kafein terjebak dan tersalut nanopartikel kitosan sebagai antiselulit.
Terima kasih penulis ucapkan kepada Dr. Pipih Suptijah, MBA dan Pharm.
Dr. Joshita Djajadisastra, MS, Ph.D selaku dosen pembimbing, Prof. Dr. Ir. Nurjanah, MS selaku dosen penguji, serta staf dosen dan administrasi
Departemen Teknologi Hasil Perairan. Terima kasih juga penulis sampaikan kepada Ibu, Bapak, dan kakak-kakak tersayang yang telah memberikan semangat dan doa, serta Reza Rizkyawan atas pengertian dan dukungan yang diberikan. Di samping itu ungkapan terima kasih penulis sampaikan kepada teman seperjuangan Kak Gufron, Rita Sahara, Lukman Hakim, Nur Syafiqoh, Bayu Ardhi Kresna, Wenny Tiara, Dina Anggraeni serta teman-teman THP 46 (Alto), THP 44, 45, dan 47 atas segala bantuan dan motivasinya.
Semoga karya ilmiah ini dapat bermanfaat bagi semua pihak yang memerlukannya.
Bogor, September 2013
DAFTAR ISI
Ruang Lingkup Penelitian 2
METODE 3
Efektivitas Penetrasi Kafein Terjebak dan Tersalut Nanopartikel Kitosan 13
DAFTAR TABEL
1 Hasil analisis pengukuran partikel 8
2 Nilai efisiensi penjerapan kafein pada nanopartikel kitosan 12
DAFTAR GAMBAR
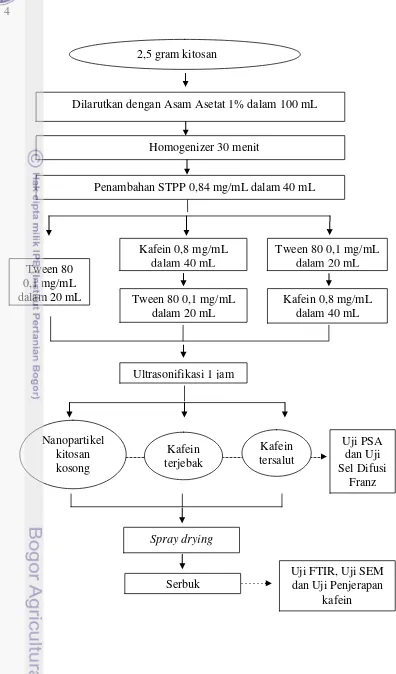
1 Diagram alir penelitian 4
2 Morfologi nanopartikel kitosan yang tidak terisi, kafein terjebak nanopartikel kitosan, dan kafein tersalut nanopartikel kitosan 7
3 Grafik FTIR nanopartikel kitosan dan kafein 9
4 Grafik FTIR kafein terjebak nanopartikel kitosan dan kafein tersalut
nanopartikel kitosan 10
5 Kurva gelombang maksimum kafein 10 ppm dapar fosfat pH 7,4 11 6 Hubungan antara absorbans dan konsentrasi larutan kafein 12 7 Jumlah kumulatif kafein terjebak nanopartikel kitosan dan kafein
tersalut nanopartikel kitosan 13
8 Grafik nilai fluks kafein terpenetrasi 14
DAFTAR LAMPIRAN
1 Hasil data pengujian PSA 19
2 Data serapan kalibrasi kafein 22
3 Data jumlah kumulatif kafein yang terpenetrasi 23
4 Data fluks kafein yang terpenetrasi 23
5 Contoh perhitungan persentasi efisiensi penjerapan 24 6 Contoh perhitungan jumlah kafein yang terpenetrasi 25 7 Contoh perhitungan fluks kafein yang terpenetrasi 26 8 Contoh perhitungan presentasi kafein yang terpenetrasi 26
9 Sertifikat analisis kitosan 27
10 Sertifikat analisis asam asetat 28
11 Sertifikat analisis sodium tripolifosfat 29
12 Sertifikat analisis tween 80 30
13 Sertifikat analisis kafein 31
PENDAHULUAN
Latar Belakang
Kitosan merupakan polimer yang dapat diperoleh dari deasetilasi kitin, tidak beracun, mudah terdegradasi secara biologi, memiliki sifat polikationik pada suasana asam karena terjadi protonasi gugus amino, dan membentuk gel. Struktur kitosan terdiri atas unit berulang poli-(2-amino-2-deoksi-D-glukopiranosa) yang terhubung oleh ikatan β-(1,4) (Sugita 1992). Strukturnya mirip dengan selulosa sehingga memiliki sifat matriks yang sama dalam sistem penghantaran obat (Sutriyo et al. 2005). Kitosan banyak digunakan sebagai matriks penghantaran obat karena bersifat polikationik alami, biodegradabel, biokompatibel,
mucoadhesiveness, dan mudah dimodifikasi dalam sifat kimia dan fisiknya (Lee et al. 2006).
Modifikasi kitosan secara kimia menghasilkan perbaikan stabilitas kitosan melalui aktivitas gugus fungsi yang ada, perbaikan ukuran pori kitosan menggunakan senyawa porogen, dan dapat menaikkan kapasitas adsorpsi kitosan apabila kitosan dipadukan dengan polimer lain. Salah satu modifikasi kimia dapat dilakukan melalui pembentukan ikatan silang dalam struktur kitosan menghasilkan gel kitosan (Wang et al. 2004). Modifikasi kitosan secara fisik mengarah pada bentuk nanopartikel. Menurut Mohanraj dan Chen (2006) nanopartikel memiliki kisaran ukuran 1-1000 nm. Pembuatan nanopartikel kitosan dipengaruhi oleh beberapa faktor, antara lain komposisi material dan metode yang digunakan. Komposisi material yang digunakan dalam pembuatan nanopartikel kitosan adalah kitosan, STPP (Sodium tripolifosfat) dan surfaktan (Tween 80). Banyak metode pembuatan nanopartikel kitosan yang dikembangkan untuk menghasilkan nanopartikel dan morfologi yang seragam (Wahyono 2010).
Nanopartikel kitosan berperan sebagai pembawa (carrier) dengan cara melarutkan, menjebak, mengenkapsulasi, atau menempelkan obat dalam matriksnya dan menghantarkan obat secara oral dan topikal (Tiyaboonchai 2003). Pada penelitian ini dilakukan metode pembuatan nanopartikel kitosan dengan cara menjebak dan menyalutkan zat aktif untuk menghantarkannya secara topikal. Salah satu perawatan topikal pada kulit yang meningkat permintaannya karena menjadi permasalahan estetika kulit wanita dewasa yaitu sediaan antiselulit. Menurut survei WHO (2012) sekitar 90% wanita dewasa di dunia memiliki gangguan selulit. Selulit (Gynoid limphodystrophy) merupakan suatu kondisi berupa parutan-parutan tidak rata pada kulit yang nampak seperti kulit jeruk, terjadi pada wanita dan biasanya muncul pada bagian tubuh tertentu yaitu paha, perut, dan bokong (Rona et al. 2006). Selulit terjadi karena adanya kerusakan pada pembuluh darah dan limfa sehingga menyebabkan perubahan struktur lapisan lemak dan matriks kolagen yang mengelilinginya (Orkin et al. 1991).
2
(Witt dan Bucks 2003). Bahan pembawa berupa nanopartikel kitosan yang dikombinasikan dengan kafein dalam sediaan antiselulit dapat mempengaruhi penetrasi kafein pada kulit. Jika fungsi barier dari kulit bisa diganggu oleh bahan aktif yang diabsorpsi dengan nanopartikel kitosan secara topikal, maka penghambat sintesis lemak dapat juga dimasukkan dalam formulasi antiselulit (Murray et al 2003). Pengujian penetrasi bahan aktif dan efektivitas bahan pembawa ke dalam kulit dapat dilakukan secara In Vitro, secara luas diteliti dengan menggunakan sel difusi Franz tipe vertikal (Junquera dan Kelley 1997).
Perumusan Masalah
Penelitian nanopartikel kitosan sampai saat ini terus dikembangkan, baik
dalam penentuan komposisi maupun pencarian metode yang sesuai. Peran
nanopartikel kitosan sebagai pembawa (carrier) dengan cara melarutkan, menjebak, mengenkapsulasi, atau menempelkan zat aktif dalam matriksnya dan menghantarkan zat aktif secara topikal. Perawatan topikal yang meningkat permintaannya adalah sediaan antiselulit. Zat aktif yang digunakan sebagai antiselulit berupa kafein karena memiliki efek pada lipolisis topikal melalui penghambatan enzim fosfodiesterase dan meningkatkan jumlah monofosfat siklik.
Tujuan Penelitian
Penelitian ini bertujuan untuk menentukan karakteristik perlakuan kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan diantaranya morfologi, ukuran partikel, gugus fungsi, dan nilai efisiensi penjerapan serta membuktikan efektivitas nanopartikel kitosan terhadap penetrasi kafein sebagai antiselulit secara In Vitro dengan menggunakan sel difusi Franz tipe vertikal.
Manfaat Penelitian
Penelitian ini diharapkan memberikan informasi mengenai karakteristik metode pembuatan kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan diantaranya morfologi, ukuran partikel, gugus fungsi, dan nilai efisiensi penjerapan serta membuktikan efektivitas nanopartikel kitosan terhadap penetrasi kafein sebagai antiselulit secara In Vitro dengan menggunakan sel difusi Franz tipe vertikal.
Ruang Lingkup Penelitian
3
METODE
Penelitian ini dilakukan pada bulan Maret sampai dengan Juni 2013. Pembuatan formulasi nanokitosan di Laboratorium Biokimia Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Pembuatan nanokitosan dengan homogenizer di Laboratorium Kimia Fisik dan dengan alat ultrasonifikasi di Laboratorium Kimia Analitik, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Pengujian morfologi nanopartikel kitosan dengan SEM dilakukan di Pusat Penelitian dan Pengembangan (PUSLITBANG) Keteknikan Kehutanan dan Pengolahan Hasil Hutan, Bogor. Pengujian ukuran partikel nanopartikel kitosan dengan PSA dan pengujian gugus fungsi dengan FTIR dilakukan di Laboratorium Biofisik, Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Pengujian penetrasi sel difusi Franz dilakukan di Laboratorium Farmasetika, Fakultas Farmasi, Universitas Indonesia.
Bahan
Bahan yang digunakan dalam pembuatan nanopartikel kitosan antiselulit adalah kitosan (derajat deasetilasi min 70%) (CV. Bio Chitosan, Indonesia), asam asetat 1% (Merk, Jerman), tween 80 (Brataco, Indonesia), sodium tripolifosfat (Aditya Birla, Thailand), kafein anhidrat (Brataco, Indonesia), aquademineralisata (Brataco, Indonesia), kalium dihidrogen fosfat (Merck, Jerman), natrium hidroksida (Brataco, Indonesia), dan tikus betina strain Sprague Dawley usia 2 sampai 3 bulan dengan berat 150 gram (Institut Pertanian Bogor, Indonesia).
Alat
Peralatan yang digunakan dalam pembuatan nanopartikel kitosan adalah ultrasonikasi (As One 110 volt, JBJC Coda Loan), homogenizer (Ultra Turrax T8, Wika), neraca analitik (Tipe EB-330, Shimadzhu), dan alat-alat gelas Laboratorium. Alat yang digunakan untuk analisis adalah sel difusi Franz dengan volume kompartemen reseptor 14,0 mL (Bengkel Gelas ITB, Bandung), spektrofotometer UV-VIS (Tipe 1600, Shimadzu), Mikroskop Elektron Payaran (JSM-5310 LV, JEOL Ltd), Particle Size Analyzer (Delsa TM Nano, Cordouan),
Fourier Trasform Infrared (Tipe MB3000, ABB Group), kamera digital (SEL 1855, Sony), dan alat-alat bedah.
Prosedur Penelitian
4
Penambahan STPP 0,84 mg/mL dalam 40 mL Dilarutkan dengan Asam Asetat 1% dalam 100 mL
5
Pembuatan nanopartikel kitosan
Kitosan dibuat dengan konsentrasi 2,5%. Sebanyak 2,5 gram kitosan dilarutkan menggunakan homogenizer selama 30 menit dalam 100 mL asam asetat 1% sehingga diperoleh konsentrasi kitosan 2,5% (b/v). Kemudian kelarutan kitosan ditambahkan 50 mL STPP sebanyak 0,84 mg/mL larut dalam akuademineralisata Larutan kitosan dengan STPP kemudian dibagi menjadi kontrol dan dua perlakuan. Kontrol dengan kafein yang tidak terisi kafein, perlakuan pertama dengan kafein yang terjebak nanopartikel kitosan (Modifikasi Wahyono 2010, dan perlakuan kedua dengan kafein yang tersalut nanopartikel kitosan (Modifikasi Hermanius 2012).
Perlakuan kontrol larutan kitosan-STPP dengan ditambahkan 20 mL Tween 80 sebanyak 0,1 mg/mL larut dalam akuademineralisata. Perlakuan pertama larutan kitosan-STPP dengan ditambahkan 40 mL Kafein sebanyak 0,8 mg/mL larut dalam akuademineralisata terlebih dahulu, selanjutnya ditambahkan 20 mL Tween 80 sebanyak 0,1 mg/mL larut dalam akuademineralisata. Perlakuan kedua larutan kitosan-STPP dengan ditambahkan 20 mL Tween 80 sebanyak 0,1 mg/mL larut dalam akuademineralisata terlebih dahulu, selanjutnya ditambahkan 40 mL Kafein sebanyak 0,8 mg/mL larut dalam akuademineralisata. Selanjutnya kedua perlakuan tersebut di ultrasonikasi dengan frekuensi 20 kHz selama 1 jam. Larutan nanopartikel kitosan-kafein yang sudah dipecah kemudian dibagi menjadi dua bagian. Bagian pertama dalam bentuk larutan cair dan bagian kedua dikeringkan dengan pengering semprot (spray drying) pada suhu 173 oC sehingga diperoleh hasil dalam bentuk serbuk.
Pengujian Karakteristik Nanopartikel Kitosan
Pengujian yang dilakukan untuk nanokitosan pada penelitian ini yaitu menentukan morfologi nanokitosan dengan pengujian Mikroskop Elektron Payaran (SEM), analisis pengukuran partikel nanokitosan yang dihasilkan dengan pengujian Particle Size Analyzer (PSA), analisis gugus fungsi nanokitosan yang dihasilkan dengan pengujian Fourier Transform Infrared (FTIR), dan pengujian efisiensi penjerapan kafein pada nanopartikel kitosan.
a. Pengujian Mikroskop Elektron Payaran (SEM) (Desai dan Park 2005)
Serbuk nanokitosan diletakkan pada potongan kuningan (stub) berdiameter 1 cm dengan menggunakan selotip dua sisi. Selanjutnya serbuk tersebut dibuat menjadi konduktif secara elektrik dengan seberkas sinar dari platina lapis tipis (coating) selama 30 detik pada tekanan dibawah 2 Pa dan tegangan elektron 10 kV dengan perbesaran 1000x.
b. Pengujian Particle Size Analyzer (PSA) (Triani 2011)
Uji ukuran partikel dilakukan menggunakan mikroskop digital serta pengujian PSA (Particle Size Analyzer). Sampel larutan diambil dengan pipet kemudian dilarutkan dengan etanol 3 mL dan diaduk hingga homogen. Larutan kemudian dimasukkan ke dalam tabung dengan tinggi maksimum 15 mm.
c. Pengujian Fourier Transform Infrared (FTIR) (Kencana 2009)
6
d. Efisiensi Penjerapan Kafein pada Nanopartikel Kitosan (Wahyono 2010)
Sebanyak 25 mg nanopartikel kitosan-kafein serbuk ditimbang dan dilarutkan ke dalam 50 mL dapar fosfat pH 7.4. Campuran tersebut dikocok selama 24 jam lalu disaring. Filtrat yang diperoleh dibaca absorbansinya dengan spektrofotometer UV-VIS pada ʎ maks. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi kafein dengan bantuan kurva standar.
Pengujian Penetrasi Secara In Vitro
Menurut Hadyanti (2008) pengujian penetrasi secara In Vitro dilakukan untuk mengetahui penetrasi bahan aktif dengan membuat kurva kalibrasi bahan aktif. Ada beberapa tahap yang dapat dilihat dibawah ini.
a. Pembuatan larutan dapar fosfat pH 7,4
Kalium dihidrogen fosfat 0,2 M sebanyak 50 mL dicampurkan dengan 39,1 mL NaOH 0,2 N kemudian diencerkan dengan air bebas CO2 secukupnya hingga mendapatkan 200 mL. Nilai pH disesuaikan hingga didapatkan pH 7,4.
b. Pembuatan kurva kalibrasi kafein
Kafein ditimbang sebanyak 100 mg kemudian dilarutkan dengan dapar fosfat pH 7,4 dalam labu ukur 100 mL. Larutan yang diperoleh mempunyai konsentrasi 1000 ppm. Larutan induk ini dipipet sebanyak 10 mL kemudian diencerkan dengan dapar fosfat pH 7,4 hingga 100 mL. Larutan diperoleh memiliki konsentrasi sebesar 100 ppm. Larutan kafein 100 ppm diencerkan dengan dapar fosfat pH 7,4 hingga diperoleh konsentrasi 5, 6, 7, 10, 12, 15 ppm. Pengukuran serapan larutan 10 ppm dilakukan dari panjang gelombang 200 nm sampai 400 nm kemudian panjang gelombang maksimumnya ditentukan dari spektrum serapan yang didapat. Dari masing-masing larutan ini, serapannya diukur pada panjang gelombang maksimum menggunakan spektrofotometer UV-VIS dan dibuat kurva kalibrasinya.
c. Uji penetrasi kafein
Tikus betina strain Sprague Dawley usia 2-3 bulan dengan berat 150 gram dibius menggunakan eter hingga mati. Selanjutnya kakinya diikat di atas papan atas. Bulu tikus dicukur dengan hati-hati menggunakan pisau cukur. Setelah itu, tikus disayat pada bagian perut. Bagian subkutan dan lemak-lemak yang menempel dihilangkan terlebih dahulu secara hati-hati menggunakan tangan. Kulit disimpan dalam dapar fosfat pH 7,4 pada suhu 4 oC. Sebelum digunakan kulit didiamkan hingga mencapai suhu kamar selama 1 jam.
7
HASIL DAN PEMBAHASAN
Karakteristik Nanopartikel Kitosan
Karakteristik kafein terjebak dan tersalut nanopartikel kitosan yang dilakukan pada penelitian ini meliputi analisis morfologi, analisis pengukuran partikel, analisis gugus fungsi, dan efisiensi penjerapan kafein pada nanopartikel kitosan.
Morfologi
Nanopartikel kitosan yang tidak terisi (kontrol) dan terisi kafein (terjebak dan tersalut) dapat dibedakan secara visual dengan menggunakan Scanning electron microscopy (SEM). Analisis SEM ini berfungsi untuk mengidentifikasi morfologi permukaan dan bentuk nanopartikel kitosan yang ditampilkan melalui sebuah gambar. Berdasarkan pencirian dengan SEM pada perbesaran 1000x memperlihatkan bahwa nanopartikel kitosan yang tidak terisi dan perlakuan kafein terjebak nanopartikel kitosan maupun kafein tersalut nanopartikel kitosan yang dihasilkan memiliki permukaan dan bentuk yang berbeda dapat dilihat pada Gambar 2.
(a) (b) (c)
Gambar 2 (a) Nanopartikel kitosan yang tidak terisi (b) Kafein terjebak nanopartikel kitosan (c) Kafein tersalut nanopartikel kitosan.
Hasil morfologi nanopartikel kitosan tidak terisi memiliki permukaan yang kasar dan cekung tetapi sangat menggumpal dapat dilihat pada Gambar 2a sedangkan hasil morfologi kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan memiliki permukaan yang halus dan sedikit cembung terjadi penggumpalan dapat dilihat pada Gambar 2b-c. Nanopartikel kitosan yang sudah terisi akan berbentuk seperti bola yang halus dan cembung, sedangkan kitosan tidak terisi memiliki permukaan yang cekung dan kasar (Desai dan Park 2005)
8
dikurangi dengan mempersingkat waktu pada saat pembuatan nanopartikel kitosan dengan pengeringan semprot (Yongmei dan Yunn 2003).
Berdasarkan Gambar 2 memperlihatkan perbedaan posisi kafein dari setiap perlakuan. Perbedaan yang diperlihatkan pada perlakuan kafein tersalut nanopartikel memiliki lebih banyak bentuk jarum dibandingkan dengan perlakuan kafein terjebak nanopartikel kitosan. Menurut Ansel et.al (1999) kafein berupa serbuk putih, berbentuk jarum mengkilat putih, dan biasanya menggumpal. Hal ini dapat dilihat pada Gambar 2b pada perlakuan kafein terjebak nanopartikel kitosan kafein berada di dalam rongga kitosan sehingga kurang terlihat sedangkan Gambar 2c memperlihatkan kafein terlihat di permukaan rongga matriks nanopartikel pada perlakuan kafein tersalut nanopartikel kitosan.
Ukuran partikel
Keberhasilan suatu sampel menjadi nanopartikel diketahui dengan melihat distribusi ukuran, ukuran rata-rata, dan indeks polidispersitas sampel tersebut dengan menggunakan pengujian PSA (Particles Size Analyzer). Hasil pengujian nanopartikel kitosan dengan perlakuan kafein terjebak nanopartikel kitosan dan perlakuan kafein tersalut nanopartikel kitosan dengan menggunakan pengujian PSA (Particles Size Analyzer) dapat dilihat pada Tabel 1.
Tabel 1 Hasil analisis pengukuran partikel
Perlakuan Distribusi ukuran
Berdasarkan hasil pengujian ukuran partikel dengan menggunakan pengujian PSA (Particles Size Analyzer) pada perlakuan kafein terjebak nanopartikel kitosan didapatkan distribusi ukuran 134,93 – 489,91 nm lebih kecil dibandingkan dengan distribusi ukuran perlakuan kafein tersalut nanopartikel kitosan 141,29 – 446,80 nm. Sedangkan ukuran rata-rata perlakuan kafein terjebak nanopartikel kitosan 232,74 nm lebih besar dibandingkan dengan perlakuan kafein tersalut nanopartikel kitosan 226,62 nm. Hasil kedua perlakuan yang didapatkan sesuai dengan kategori nanopartikel. Menurut Mohanraj dan Chen (2006) nanopartikel didefinisikan sebagai partikel yang berbentuk padat dengan ukuran sekitar 10-1000 nm. Hal yang paling berpengaruh dalam teknologi pembuatan nanopartikel adalah formulasi dan metode yang digunakannya.
9 0 sampai 1. Dimana nilai yang mendekati 0 mengindikasikan dispersi yang homogen, sedangkan nilai yang lebih besar dari 0,5 mengindikasikan heterogen yang tinggi (Avadi et al. 2009)
Gugus fungsi
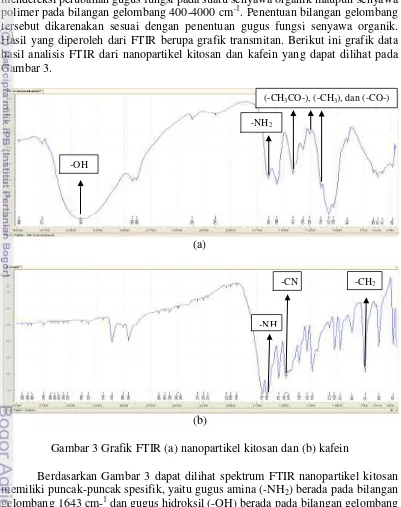
Analisis FTIR (Fourier Transform InfraRed) dapat digunakan untuk mendeteksi perubahan gugus fungsi pada suatu senyawa organik maupun senyawa polimer pada bilangan gelombang 400-4000 cm-1. Penentuan bilangan gelombang tersebut dikarenakan sesuai dengan penentuan gugus fungsi senyawa organik. Hasil yang diperoleh dari FTIR berupa grafik transmitan. Berikut ini grafik data hasil analisis FTIR dari nanopartikel kitosan dan kafein yang dapat dilihat pada Gambar 3.
(a)
(b)
Gambar 3 Grafik FTIR (a) nanopartikel kitosan dan (b) kafein
Berdasarkan Gambar 3 dapat dilihat spektrum FTIR nanopartikel kitosan memiliki puncak-puncak spesifik, yaitu gugus amina (-NH2) berada pada bilangan gelombang 1643 cm-1 dan gugus hidroksil (-OH) berada pada bilangan gelombang 3410 cm-1. Serapan bilangan gelombang gugus amina (-NH2) dan gugus hidroksil (-OH) pada kitosan komersil berada pada bilangan gelombang 1655 cm-1 dan 3441cm-1 (Pebriani et al. 2012). Spektrum FTIR nanopartikel kitosan mengalami pergeseran intensitas transmitans pada daerah spektrum. Perubahan transmitans
-OH
-NH2
-CH2 -CN
-NH
10
ini menunjukkan adanya interaksi antara kitosan, STPP, dan Tween 80 yang digunakan dalam pembuatan nanopartikel kitosan.
Terdapat bilangan gelombang lain pada grafik FTIR nanopartikel kitosan dengan bilangan gelombang 1412 cm-1, 1257 cm-1, dan 1149 cm-1 yang menunjukkan daerah spektrum gugus asetil (-CH3CO-), metil (-CH3), dan carbonil (-CO-). Kitosan yang memiliki gugus asetil metil menunjukkan bahwa proses deasetilasi yang dilakukan kurang optimum, kemurniannya masih rendah, masih mengandung banyak pengotor dan adanya air yang mungkin terserap sehingga mempengaruhi ikatan antar molekul yang menyebabkan perbedaan daerah serapan (Pebriani et al. 2012).
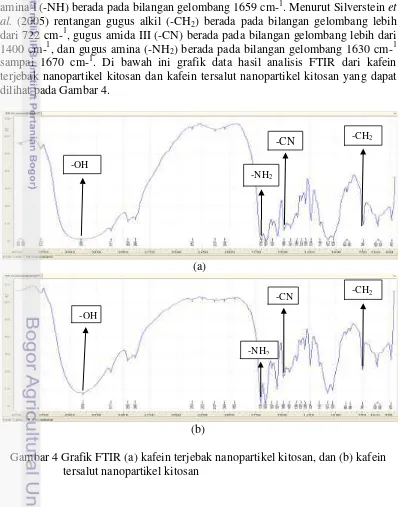
Bedasarkan spektrum FTIR kafein memiliki puncak-puncak spesifik, yaitu daerah spektrum gugus alkil (-CH2) berada pada bilangan gelombang 741 cm-1, gugus amida III (-CN) berada pada bilangan gelombang1481 cm-1, dan gugus amina I (-NH) berada pada bilangan gelombang 1659 cm-1. Menurut Silverstein et al. (2005) rentangan gugus alkil (-CH2) berada pada bilangan gelombang lebih dari 722 cm-1, gugus amida III (-CN) berada pada bilangan gelombang lebih dari 1400 cm-1, dan gugus amina (-NH2) berada pada bilangan gelombang 1630 cm-1 sampai 1670 cm-1. Di bawah ini grafik data hasil analisis FTIR dari kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan yang dapat dilihat pada Gambar 4.
(a)
(b)
11 Grafik hasil FTIR pada Gambar 4 menunjukkan bahwa kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan memiliki gabungan gugus nanopartikel kitosan dengan kafein. Daerah spektrum yang terdapat pada perlakuan kafein terjebak nanopartikel kitosan adanya gugus alkil (-CH2) bilangan gelombang 748 cm-1, gugus amida III (-CN) bilangan gelombang 1489 cm-1, gugus amina (-NH2) bilangan gelombang 1659 cm-1, dan gugus hidroksil (-OH) bilangan gelombang 3394 cm-1. Daerah spektrum perlakuan kafein tersalut nanopartikel kitosan memiliki gugus yang sama dengan perlakuan kafein terjebak nanopartikel kitosan tetapi adanya pergeseran bilangan gelombang yaitu pada gugus hidroksil (-OH) bilangan gelombang 3379 cm-1 dan gugus amida III (-CN) bilangan gelombang 1481 cm-1.
Efisiensi Penjerapan
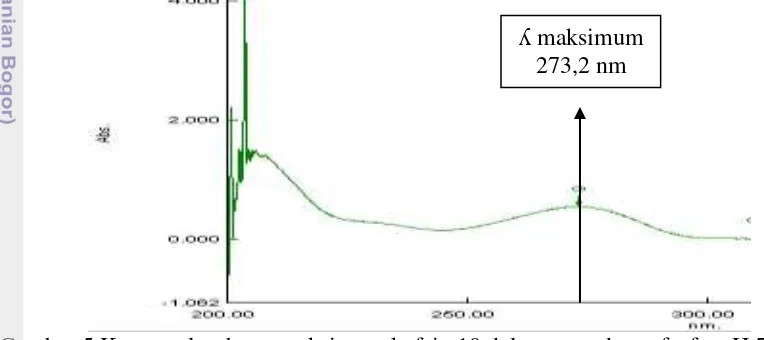
Efisiensi penjerapan kafein dilakukan dengan mengukur jumlah kafein terjebak dan tersalut ke dalam nanopartikel kitosan. Banyaknya kafein terjebak dan tersalut dapat dilihat dari nilai absorbans yang terukur dengan spektrotofotometer UV-VIS pada panjang gelombang maksimum dengan bantuan kurva standar. Oleh karena itu, tahap pertama sebelum menentukan nilai efisiensi penjerapan kafein adalah menentukan panjang gelombang maksimum dan membuat kurva standar. Panjang gelombang maksimum larutan kafein dapat dilihat pada Gambar 5 .
Gambar 5 Kurva gelombang maksimum kafein 10 dalam ppm dapar fosfat pH 7,4 Penentuan panjang gelombang maksimum larutan kafein dilakukan pada konsentrasi kafein 10 ppm dalam dapar fosfat pH 7,4. Nilai pH 7,4 dipilih karena mendekati kondisi pH kulit manusia. Berdasarkan nilai absorbans larutan kafein didapatkan panjang gelombang dengan serapan maksimum untuk senyawa kafein adalah 273,2 nm. Kurva standar untuk larutan kafein pada Gambar 6 memiliki linearitas yang tinggi ditunjukkan dengan r2 = 0,9999% dalam persamaan garis yaitu y = 0,0578x – 0,0337. Persamaan kurva standar ini digunakan untuk menentukan jumlah kafein yang terjebak dan tersalut di dalam nanopartikel kitosan.
12
Gambar 6 Hubungan antara absorbans dan konsentrasi larutan kafein Efisiensi penjerapan menggambarkan banyaknya kafein yang terjebak dan tersalut di dalam nanopartikel kitosan. Dilakukan dengan mengekstraksi nanopartikel kitosan terisi kafein dalam dapar fosfat pH 7,4 selama 24 jam, kemudian mengukur absorbansnya dengan spektrofotometer UV-VIS pada panjang gelombang 273,2 nm. Mengetahui nilai efisiensi ini sangatlah penting dalam bidang farmasi terutama untuk sistem penetrasi obat ke dalam kulit karena dengan adanya nilai efisiensi maka dapat dilihat kemampuan nanopartikel kitosan dalam membawa kafein ke dalam kulit.
Penelitian ini menghasilkan nilai efisiensi yang berbeda pada setiap perlakuan dapat dilihat pada Tabel 2. Perbedaan nilai efisiensi nanopartikel kitosan diduga diakibatkan oleh perlakuan metode pembuatan yang tidak sama sehingga kafein yang terjebak dan tersalut ke dalam masing-masing partikel tidak sama. Nilai efisiensi penjerapan kafein yang paling tinggi dimiliki perlakuan kafein tersalut nanopartikel kitosan, yaitu 64,63% sedangkan perlakuan kafein terjebak nanopartikel kitosan 51,35%.
Tabel 2 Nilai efisiensi penjerapan kafein pada nanopartikel kitosan
Perlakuan Nilai (y) Nilai (x) Bobot a
13
Efektifitas Penetrasi Kafein Terjebak dan Tersalut Nanopartikel Kitosan
Uji penetrasi secara In Vitro dilakukan dengan menggunakan sel difusi Franz. Pengujian penetrasi dilakukan untuk mengetahui jumlah kafein yang dapat berpenetrasi ke dalam membran selama interval waktu tertentu dari nanopartikel kitosan. Membran yang digunakan adalah kulit bagian abdomen tikus betina strain
Sprague Dawley usia 2-3 bulan dengan berat 150 gram. Membran kulit tikus digunakan karena memiliki permeabilitas yang hampir sama dengan permeabilitas kulit manusia (Rawling 2006).
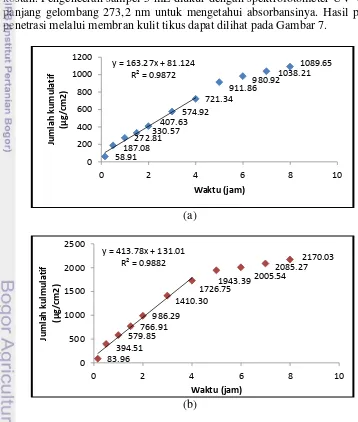
Uji penetrasi sel difusi franz dilakukan selama 8 jam dengan interval waktu 10, 30, 60, 90, 120, 180, 240, 300, 360, dan 480 menit. Setiap interval waktu sampel diambil 0,5 mL cairan dari kompartemen reseptor selanjutnya diencerkan hingga 5 mL dengan dapar fosfat pH 7,4 (Franz 2005). Setiap diambil sampel cairan dari kompartemen reseptor harus selalu digantikan dengan cairan yang sama sejumlah volume yang terambil untuk menjaga volume cairan reseptor tetap kostan. Pengenceran sampel 5 mL diukur dengan spektrofotometer UV-VIS pada panjang gelombang 273,2 nm untuk mengetahui absorbansinya. Hasil pengujian penetrasi melalui membran kulit tikus dapat dilihat pada Gambar 7.
(a)
(b)
14
Hasil pengujian penetrasi melalui membran kulit tikus pada Gambar 7 menunjukkan interval waktu jam ke 8 perlakuan kafein terjebak nanopartikel kitosan 1,089,65 ± 10,7 µg/cm2 sedangkan perlakuan kafein tersalut nanopartikel kitosan 2,170,03 ± 6,85 µg/cm2. Dari hasil tersebut perlakuan kafein tersalut nanopartikel kitosan memiliki kecepatan penetrasi yang lebih cepat dibandingkan kafein terjebak nanopartikel kitosan. Hal ini dipengaruhi oleh karakterisasi nanopartikel dan efisiensi penjerapan. Berdasarkan hasil penelitian karakterisasi nanopartikel memiliki perbedaan setiap perlakuan. Perlakuan kafein tersalut nanopartikel memiliki rata-rata ukuran partikel 226,62 nm lebih kecil dibandingkan dengan perlakuan kafein terjebak nanopartikel 232,74 nm. Ukuran partikel mempengaruhi dalam penghantaran obat, pelepasan obat, dan stabilitas nanopartikel (Mohanraj dan Chen 2006). Nanopartikel dapat meningkatkan penetrasi obat melalui kulit karena ukurannya yang kecil sehingga luas permukaan semakin besar dan semakin kecil ukuran nanopartikel akan membawa zat aktif lebih banyak menembus kulit (Inayat dan Mallikarjuna 2009).
Faktor efisiensi penjerapan mempengaruhi penetrasi obat ke dalam kulit. Berdasarkan hasil penelitian efisiensi penjerapan pada perlakuan kafein tersalut nanopartikel kitosan memiliki 64,63% lebih banyak dibandingkan dengan perlakuan kafein terjebak nanopartikel kitosan memiliki 51,35%. Semakin tinggi nilai efisiensi penjerapan maka zat aktif yang berada di dalam rongga nanopartikel kitosan banyak yang terlepas (Wahyono 2010). Sehingga metode pembuatan nanopartikel kitosan dengan menyalutkan obat ke dalam lebih mudah terlepas dalam sistem penghantaran obat. Sedangkan metode pembuatan nanopartikel kitosan dengan menjebak obat ke dalam larutan kitosan-STTP dengan penambahan Tween 80 dapat menurunkan nilai efisiensi penjerapan. Penjebakan obat dengan penambahan Tween 80 membentuk emulsi partikel dalam larutan akan terstabilkan sehingga obat akan sulit dilepaskan dari dalam rongga nanopartikel kitosan (Silva 2006). Kemudian nilai fluks diperoleh pada keadaan
steady state dengan mengikuti kaidah hukum Fick. Nilai fluks setiap perlakuan dapat dilihat pada Gambar 8.
Gambar 8 Grafik nilai fluks kafein terpenetrasi (a) kafein terjebak nanopartikel kitosan dan (b) kafein tersalut nanopartikel kitosan
15
16
SIMPULAN DAN SARAN
Simpulan
Pembuatan nanopartikel kitosan kafein menggunakan dua perlakuan yang berbeda yaitu kafein terjebak dan tersalut nanopartikel kitosan. Karakteristik nanopartikel kitosan kafein yang dihasilkan pada penelitian ini berdasarkan morfologi pada perlakuan kafein terjebak nanopartikel kitosan dan kafein tersalut nanopartikel kitosan memiliki permukaan yang halus dan sedikit cembung tetapi sedikit menggumpal, ukuran rata-rata berturut-turut 232,74 nm dan 226,62 nm. Analisis gugus fungsi menunjukkan pergeseran bilangan gelombang yaitu pada bilangan gelombang gugus amida III (-CN) dan bilangan gelombang gugus hidroksil (-OH), serta nilai efisiensi penjerapan kafein yang paling tinggi dimiliki perlakuan kafein tersalut nanopartikel kitosan 64,63% sedangkan perlakuan kafein terjebak nanopartikel kitosan 51,35%. Hasil karakteristik nanopartikel kitosan kafein menunjukkan nilai efektifitas penetrasi pada perlakuan kafein tersalut nanopartikel kitosan memiliki kecepatan penetrasi yang lebih cepat sebesar 2,170,03 ± 6,85 µg/cm2 dibandingkan perlakuan kafein terjebak nanopartikel kitosan sebesar 1,089,65 ± 10,7 µg/cm2.
Saran
Perlu dilakukan penelitian selanjutnya untuk melakukan optimasi pembuatan nanopartikel kitosan dengan menggunakan zat aktif yang berbeda. Selain itu, perlu juga dilakukan uji penetrasi nanopartikel kitosan secara In Vitro
17
DAFTAR PUSTAKA
Ansel H, Allen LV, Popovich NG. 1999. Pharmaceutical dosage forms and drug systems 7thedition. Maryland: Lippincot Williams and Willkins.
Avadi MR, Sadeghi AM, Mohammadpour M. 2009. Preparation and characterization of insulin nanoparticles using chitosan and arabic gum with ionic gelation metod. Journal Nanomeicine: 6. 58-63.
Benerjee T, Mitra S, Singh AK, Sharma RK, Maitra A. 2002. Preparation, characterization, biodistribution of ultrafine chitosan nanoparticles.
International Journal of Pharmaceutics. 243. 93-105.
Desai KGH, Park HJ. 2005. Preparation and characterization of drug-loaded chitosan-tripolyphosphate microspheres by spray drying. Drug Development Res. 64: 114-128.
Franz H. 2005. Phosphatdylcholine treatment to induce lipolysis. Journal of Cosmetic Dermatology. 4: 308-313.
Hadyanti. 2008. Pengaruh Tretinoin Terhadap Penetrasi Kafein dan Aminofilin Sebagai Antiselulit dalam Sediaan Krim, Gel, dan Salep Secara In Vitro [skripsi]. Depok (ID): Universitas Indonesia.
Hermanius D. 2012. Sintesis dan karakterisasi nanopartikel ekstrak kulit mahoni (Switenia macrophylla King.) sebagai bahan suplemen antihiperkolesterolemia [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Inayat BP, Mallikarjuna S. 2009. Chemical penetration enhancer for transdermal drug delivery systems. Tropical Journal of Pharmaceutical Research. 8 : 173-179.
Junquera LC, Kelley OR. 1997. Basic Histology. Melville: EGC.
Kencana AL. 2009. Perlakuan sonikasi terhadap kitosan: viskositas dan bobot molekul kitosan [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Lee DW, Shirley SA, Lockey RF, Mohapatra SS. 2006. Thiolated chitosan nanoparticles enhace anti-inflammatory effects of intranasally delivered theophylline. JournalBiology Medical Central. 7: 1-10.
Mohanraj UJ, Chen Y. 2006. Nanoparticles – A Review. Tropical Journal of Pharmaceutical Research 5 (1) : 561-573.
Murray RK, Ganner DK, Mayes PA, Rodwell VW. 2003.Harper’s Biochemistry. Melville: EGC.
Orkin M, Maibach HI, Dahl MV.1991. Dermatolgy. Philadelphia: Appleton and Large.
Ozguney IS, Karasulu HY, Katarci G, Sozer S, Guneri T, Ertan G. 2006. Transdermal delivery of diclofenac sodium though rat skin from various formulations. Journal Pharmacy Science Technology. 7(4): 88-103 .
Pebriani RH, Rilda Y, Zulhajri. 2012. Modifikasi Komposisi Kitosan Pada Proses Sintesis Komposit TiO2– Kitosan. Jurnal Kimia Universitas Padjajaran. 1: 12-34.
Rawling AV. 2006. Cellulite and its treatment. Journal Cosmetic Science. 28: 175-190.
Rona C, Carrera M, Berardesca E. 2006. Testing anticellulite products.
International Journal of Cosmetic Science. 28:169-173.
Rossi ABR, Vergnanini AL. 2000. Cellulite. Journal of Pharmaceutical Research.
18
Silva CM. 2006. Microencapsulation of hemoglobin in chitosan-coasted alginate microspheres prepared by emulsification internal gelation. Pharmaceutical Sciences Journal. 7 (4): 78-89.
Silverstein RM, Webster FX, Kiemle DJ. 2005. Spectrometric identification of organic compounds. English: Willey Amazon.
Sugita. 1992. Isolasi kitin dan komposisi senyawa kimia limbah udang windu (Penaeus monodon) [tesis]. Bogor (ID): Institut Pertanian Bogor.
Sutriyo, Joshita D, Indah R. 2005. Perbandingan pelepasan propanol hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metal selulosa. Majalah Ilmu Kefarmasian. 2: 145-153.
Tiyaboonchai W. 2003. Chitosan nanoparticles: a promosing system for drug delivery. Naresuan University Journal. 11 (3): 51-66.
Triani SUD. 2011. Pengaruh waktu sonikasi dan amplitude gelombang ultrasonic terhadap stabilitas suspensi dan mutu sari kacang hijau. [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Wahyono D. 2010. Ciri nanopartikel kitosan dan pengaruhnya pada ukuran partikel dan efisiensi penyaluran ketoprofen [tesis]. Bogor (ID): Institut Pertanian Bogor.
Wang X, Du Y, Liu H. 2004. Preparation, characterization, and antimicrobial activity of chitosan-Zn Complex. Journal of Medical Sciences. 56: 21-26. [WHO] World Health Organization. 2012. Cellulite [internet]. [diunduh 2012
April 8]. Tersedia pada http://www.who.int /mediacentre/ factsheets/ fs117/en/ index.html.
Witt K, Bucks D. 2003. Studying in Vitro Skin Penetration and Drug Release to Optimize Dermatological Formulations. New York: Advanstar Comunication Inc.
19 Lampiran 1 Data Hasil pengujian Particles Size Analyzer (PSA)
20
22
Lampiran 2 Data kurva kalibrasi kafein anhidrat dalam dapar fosfat pH 7,4 pada ʎ 273,2 nm
Konsentrasi (ppm) Serapan Persamaan garis
5 0.256
Lampiran 3 Data jumlah kumulatif kafein yang terpenetrasi
Menit ke- Jumlah Kumulatif (µg
cm-2
Lampiran 4 Data fluks kafein yang terpenetrasi
Menit ke- Fluks kafein terpenetrasi (µg
23 Lampiran 5 Contoh perhitungan persentasi efisiensi penjerapan perlakuan kafein
tersalut nanopartikel kitosan Serapan (y) = 0,28
y = 0,0578 x – 0,0337 x = 5,4
Rumus : %E = x mg/L + 1L/1000mL x vol ekstraksi x a mg/b mg
Massa kafein awal
Keterangan :
a = berat nanopartikel kitosan cair = 41,43 gram b = berat nanopartikel kitosan serbuk = 3, 42 gram vol ekstraksi = 50 mL
massa kafein awal = 0,8 mg Jawaban:
% E = 5,4 mg/L + 1L/1000mL x 50 mL x 41430 mg/3420 mg
0,8 mg
= 64,63%
24
Lampiran 6 Contoh perhitungan jumlah kafein yang terpenetrasi pada menit ke 10 pada perlakuan kafein tersalut nanopartikel kitosan
Serapan (y) = 0,031 y = 0,0578 x – 0,0337 x = 1,119
Faktor pengenceran (FP) = Volume labu terukur : volume sampling
= 5 mL : 0,5 mL = 10 x
Konsentrasi terpenetrasi = x . FP
= 11,19 µg/mL
Rumus jumlah kumulatif yang terpenetrasi :
Q = {CnV + ∑ S}/A Keterangan :
Q = jumlah kumulatif kafein yang terpenetrasi (µg/cm2) V = volume sel = 14,0 mL
S = volume pengambilan sampling = 0,5 mL A = luas permukaan membran = 1,8376 cm2
Cn = jumlah yang terpetrasi pada pengambilan ke – n (µg/mL) ∑Ci = jumlah yang terpenetrasi pada interval pengambilan sampel 1
hingga n-1
Jawaban :
Q = {(11,19 µg/mL x 14 mL) + (0 x 0,5 mL)}/ 1,8376 = 85,28 µg/cm2
25 Lampiran 7 Contoh perhitungan fluks kafein yang terpenetrasi pada menit ke 10
pada perlakuan kafein tersalut nanopartikel kitosan
Kecepatan penetrasi kafein ( Fluks; J, µg.cm2.jam-1 ) dihitung dengan
rumus : J = M/ s.t
Keterangan :
J = fluks (µg.cm2.jam-1)
M = jumlah kumulatif kafein yang terpenetrasi (µg/cm2) s = luas permukaan membran = 1,8376 cm2
t = waktu (jam) Jawaban:
J = (85,28 µg/cm2) / {1,8376 cm2 x (10/60)} = 278,45 µg.cm2.jam-1
Jadi, jumlah fluks kafein yang terpenetrasi pada menit ke 10 pada perlakuan kafein tersalut nanopartikel kitosan adalah 278,45 µg.cm2.jam-1
Lampiran 8 Contoh perhitungan presentasi kafein yang terpenetrasi pada pada menit ke 10 perlakuan kafein tersalut nanopartikel kitosan Rumus :
% Jumlah kumulatif terpenetrasi = M x s x 100% K
Keterangan :
M = jumlah kumulatif kafein yang terpenetrasi (µg/cm2) s = luas permukaan membran = 1,8376 cm2
26
28
30
31 Lampiran 14 Sertifikat analisis akuademineralisata
32
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada.tanggal 8 Oktober 1991, yang merupakan anak ketiga pasangan bapak H. Suharsono Kartoatmodjo.dan ibu Hj. Katarina Pudji Astuti.
Pendidikan formal ditempuh penulis mulai dari TK Tunas Muda Cibubur, Jakarta Timur pada tahun 1995-1997, SD Sekolah Indonesia Cairo, Mesir pada tahun 1997 dan lulus pada tahun 2003. Penulis melanjutkan pendidikan Menengah di SMP Negeri 147 Cibubur, Jakarta Timur pada tahun 2003 lulus pada tahun 2006, dan SMA Negeri 64 Cipayung, Jakarta Timur pada tahun 2006 dan lulus pada tahun 2009.
Penulis diterima sebagai mahasiswa pada Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB (USMI).
Selama perkuliahan, penulis aktif berorganisasi dalam Divisi Sosial Kemasyarakatan Peduli Pangan (SKPP), Himpunan Mahasiswa Teknologi Hasil Perairan (HIMASILKAN), Fakultas Perikanan dan Ilmu Kelautan tahun kepengurusan 2011-2012. Penulis juga pernah menjadi Asisten Luar Biasa mata kuliah Avertebrata Air pada tahun 2011-2012 dan Teknologi Pengembangan Kitin dan Kitosan pada tahun 2012-2013.
Penulis melakukan praktek lapangan dan menyelesaikan laporan praktek lapangan yang berjudul “Sistem Manajemen Mutu ISO 9001:2008 pada Proses Formulasi Produk Peeling Kulit Kerang Di PT. Mustika Ratu Tbk Ciracas - Jakarta Timur” sebagai salah satu syarat dalam menyelesaikan mata kuliah Praktek Lapangan dan Integrated Quality Assurance (THP497).