ISOLASI DAN PENENTUAN STRUKTUR SENYAWA STEROID
DARI AKAR TUMBUHAN CENDANA (Santalum album Linn)
DISERTASI
OLEH
CHAIRUL SALEH
NIM : 038103006
PROGRAM DOKTOR ILMU KIMIA
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
ISOLASI DAN PENENTUAN STRUKTUR SENYAWA STEROID
DARI AKAR TUMBUHAN CENDANA (Santalum album Linn)
DISERTASI
Untuk memperoleh gelar Doktor dalam Ilmu Kimia pada
Universitas Sumatera Utara dibawah pimpinan Rektor Universitas Sumatera Utara
Prof. Chairuddin P. Lubis, DTM&H,Sp.A(K)
untuk dipertahankan dihadapan Sidang Terbuka Promosi Doktor di
Universitas Sumatera Utara Medan
OLEH
CHAIRUL SALEH
NIM : 038103006
PROGRAM DOKTOR ILMU KIMIA
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
PROMOTOR
Prof. Dr. Tonel Barus
Guru Besar Kimia Bidang Kimia Organik Bahan Alam
Fakultas MIPA USU
CO-PROMOTOR
Prof. Dr. Yunazar Manjang
Guru Besar Kimia Bidang Kimia Organik Bahan Alam
Fakultas MIPA UNAND
Telah diuji dan dinyatakan lulus pada Tanggal : 3 September 2007
Panitia Penguji :
Ketua Komisi Penguji :
Prof. Dr. Tonel Barus
Guru Besar Kimia Bidang Kimia Organik Bahan Alam
Fakultas MIPA Universitas Sumatera Utara
Anggota Komisi Penguji :
1.
Prof. Dr. Yunazar Manjang
Guru Besar Kimia Bidang Kimia Organik Bahan Alam
Fakultas MIPA Universitas Andalas
2.
Dr. M. Pandapotan Nasution, MPS
Lektor Kepala Bidang Farmasi
Fakultas Farmasi Universitas Sumatera Utara
3.
Prof. Dr. Seri Bima Sembiring, M.Sc
Guru Besar Kimia Bidang Kimia Anorganik
Fakultas MIPA Universitas Sumatera Utara
4.
Prof. Dr. Ponten M. Naibaho
Guru Besar Bidang Pertanian
Judul Disertasi
: Isolasi dan Penentuan Struktur Senyawa Steroid dari
akar Tumbuhan Cendana (Santalum album Linn)
Nama :
Chairul
Saleh
NIM :
038103006
Program Studi
: S3 Ilmu Kimia
Menyetujui
Komisi Pembimbing
Prof. Dr. Tonel Barus
Promotor
Prof. Dr. Yunazar Manjang
Co-Promotor
Dr. M. Pandapotan Nasution, MPS
Co-Promotor
Mengetahui
Ketua Program Studi S3 Ilmu Kimia
Prof. Dr. Hemat R. Brahmana, M.Sc
Direktur Sekolah Pascasarjana USU
ABSTRACT
Santalum album Linn. is one of the species belonging to the Santalaceae family. It
is used as a traditional medicine for diabetes mellitus and is known to contain sesquiterpene
compounds. This study was aimed to isolate steroidal compound from the root of S. album
and to determine its chemical structure.
Isolation was accomplished by maceration and was followed by fractionation using
column chromatography with silica gel as the stationary phase. The isolation work resulted
in a pure isolate in the form of white needle crystals, m.p. 135-137°C (uncorrected). The
pure isolate was identified by spectral analyses with infrared, 1H-NMR, 13C-NMR, DEPT
and 2D-NMR (COSY, HMQC and HMBC) spectroscopy. The result indicated that the
compound was found to be steroid and based on the comparison of its spectrum with those
of the database of the compound was concluded to be clionasterol.
Key words: S. album Linn., Steroid, Clionasterol, Anti diabetic mellitus, Isolation,
ABSTRAK
Santalum album Linn. merupakan salah satu spesies dari suku Santalaceae yang
digunakan sebagai obat tradisional seperti diabetes melitus dan diketahui mengandung
senyawa-senyawa seskuiterpena. Penelitian ini bertujuan untuk mengisolasi dan
menentukan struktur molekul steroid dari akar S. album.
Isolasi dilakukan dengan cara maserasi diikuti oleh fraksinasi dengan kromatografi
kolom dengan fase diam silika gel. Dari hasil isolasi diperoleh isolat murni berupa kristal
putih berbentuk jarum dengan titik leleh 135-137°C (tidak terkoreksi). Isolat murni
diidentifikasi dengan menganalisis spektrum inframerah, NMR-1H, NMR-13C, DEPT, dan
NMR-2D (COSY, HMQC dan HMBC). Dari hasil analisa dinyatakan bahwa senyawa
tersebut adalah senyawa golongan steroid dan berdasarkan hasil konfirmasi dengan
membandingkan pada database senyawa tersebut adalah clionasterol.
Kata kunci: S. album Linn., Steroid, Clionasterol, Antidiabetes mellitus, Isolasi,
UCAPAN TERIMA KASIH
Assalamu’alaikum Warahmatullahi Wabarakatuh,
Alhamdulillah, saya ucapkan rasa syukur ke hadirat Allah SWT atas limpahan
rahmat dan hidayahNya sehingga saya dapat menyelesaikan disertasi ini.
Dengan selesainya disertasi ini, perkenankanlah saya dengan hati yang tulus
menyampaikan rasa hormat dan terima kasih serta penghargaan yang setinggi-tingginya
kepada yang terhormat:
1. Rektor Universitas Sumatera Utara, Prof. Dr. Chairuddin P. Lubis, DTM&H, Sp.A(K),
yang telah memberi kesempatan kepada saya untuk mengikuti Program S3 Ilmu Kimia
pada Sekolah Pascasarjana USU Medan.
2. Direktris Sekolah Pascasarjana, Prof. Dr. Ir. T. Chairun Nisa B., M.Sc., yang telah
memberikan kesempatan dan kepercayaan kepada saya untuk menjadi peserta Program
S3 Ilmu Kimia USU Angkatan 2003.
3. Ketua Program S3 Ilmu Kimia, Prof. Dr. Hemat R. Brahmana, M.Sc., yang telah
memberikan dorongan kepada saya untuk dapat segera menyelesaikan Program S3 Ilmu
Kimia.
4. Dengan Tulus Ikhlas penulis mengucapkan terima kasih kepada Promotor saya Prof.
Dr. Tonel Barus, dan Co-Promotor Prof. Dr. Yunazar Manjang dan Co-Promotor Dr.
M. Pandapotan Nasution, MPS., yang dengan segala kesabaran dan tanpa
bosan-bosannya telah banyak memberikan bimbingan dalam menyelesaikan disertasi ini.
5. Tim Penguji saya Prof. Dr. Seri Bima Sembiring, M.Sc. dan Prof. Dr. Ponten Naibaho
saya ucapkan terima kasih yang tak terhingga atas kesediaan beliau untuk memberikan
6. Rektor Universitas Mulawarman, Prof. Dr. Ir. H. Achmad Ariffien Bratawinata, M.Agr
selaku Rektor Universitas Mulawarman yang telah memberikan kesempatan kepada
saya mengikuti Program S3 Ilmu Kimia serta bantuan biaya perkuliahan.
7. Dekan Fakultas MIPA Universitas Mulawarman, Drs. Sudrajat, SU., atas segala
bantuan, ijin, dan semangat yang diberikan kepada saya untuk dapat segera
menyelesaikan Program S3 Ilmu Kimia.
8. Pemerintahan Daerah Kalimantan Timur yang telah memberikan bantuan dana
pendidikan kepada saya sehingga dapat mengikuti Program S3 Ilmua Kimia pada
Sekolah Pascasarjan USU.
9. Yayasan Habibie Center yang telah memberikan beasiswa kepada saya sehingga saya
dapat menyelesaikan Program S3 Ilmua Kimia pada Sekolah Pascasarjan USU.
10. Dr. Nurdin Saidi yang telah meluangkan waktunya dalam pengerjaan spektroskopi di
Jurusan Kimia Fakultas Sains Universitas Malaya – Malaysia.
11. Kepala Laboratorium Penelitian, Dr. Harry Agusnar; Kepala Laboratorium Biokimia,
Drs. Ribu Surbakti, MS.; Kepala Laboratorium Kimia Organik Bahan Alam, Drs.
Johanes Simorangkir, MS.; dan Kepala Laboratorium Farmasi, Dra. Marline
Nainggolan, MS. atas fasilitas yang telah diberikan selama melaksanakan penelitian.
12. Semua teman sejawat dan peserta Program S3 Ilmu Kimia Sekolah Pascasarjana USU
yang memberikan dukungan sehingga disertasi ini dapat selesai dengan baik.
Pada saat ini tak lupa saya mengucapkan rasa terima kasih yang sedalam-dalamnya
kepada kedua orangtua saya atas jasa-jasa mereka yang telah melahirkan, membesarkan,
dan mendidik saya dengan sepenuh hati serta memberikan dorongan kepada saya untuk
terus belajar sehingga saya dapat mencapai tingkat pendidikan seperti sekarang ini. Kepada
Isteriku Nurhasanah, S.Si., anak-anakku Haani Adilah dan Muhammad Rizky Akbar yang
telah memberikan bantuan moril dan semangat sehingga saya dapat meyelesaikan disertasi
Akhirnya kepada semua pihak yang telah banyak membantu, baik langsung maupun
tidak langsung, hanya Allah SWT yang mampu memberikan balasan terbaik.
Mudah-mudahan disertasi ini dapat memberi sumbangan yang berharga bagi perkembangan ilmu
kimia khususnya kimia organik bahan alam. Semoga Allah SWT senantiasa memberi
rahmat dan hidayahNya kepada kita semua. Amin.
Wabillahi taufiq wal hidayah, Wassalamu’alaikum warahmatullahi wabarakatuh
Medan, September 2007
Chairul Saleh
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 31 Maret 1973 di Tanjung Balai, anak dari M. Saleh
Arief dan Asdarwati merupakan anak pertama dari empat bersaudara..
Penulis menjalani masa pendidikan SD Inpres 105300 di Kedai Durian dari tahun
1980 sampai 1986, kemudian SMP Negeri 2 Delitua dari tahun 1986 sampai 1989 dan
selanjutnya SMA Negeri 12 Medan dari tahun 1989 sampai 1992. Kemudian penulis
melanjutkan ke Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera
Utara, Jurusan Kimia. Penulis lulus sebagai Sarjana Kimia dengan penelitian di bidang
Biokimia tahun 1997, dan penulis pernah bekerja pada PT LP3I di Jambi pada tahun 1999.
Penulis melanjutkan Pendidikan Program Magister pada Sekolah Pascasarjana
Universitas Padjadjaran dalam Program Studi Ilmu Kimia pada tahun 1999 dan lulus pada
tahun 2002 yang dibiayai oleh Departemen Pendidikan Nasional Direktorat Jendral
Pendidikan Tinggi, Proyek Pengembangan Pendidikan S-1 (DUE-QUE), Program
Karyasiswa. Penulis bekerja sebagai tenaga pengajar pada FMIPA Jurusan Kimia
Universitas Mulawarman Samarinda sejak tahun 2000. Selanjutnya pada tahun 2003
penulis mengikuti Program Doktor (S3) Ilmu Kimia pada Sekolah Pascasarjana Universitas
DAFTAR ISI
Halaman
ABSTRACT ….……… i
ABSTRAK .………..… ii
UCAPAN TERIMA KASIH ……… iii
RIWAYAT HIDUP ………. vi
DAFTAR ISI …….……….……….. vii
DAFTAR GAMBAR ……….………..… x
DAFTAR TABEL ………..……….…. xiv
DAFTAR LAMPIRAN …….……….….. xvii
BAB I PENDAHULUAN ……… 1
1.1 Latar Belakang ……….. 1
1.2 Perumusan Masalah ……….. 7
1.3 Tujuan Penelitian ……….. 7
1.4 Manfaat Penelitian ……… 8
1.5 Metode Penelitian ………. 8
BAB II TINJAUAN PUSTAKA ……….. 9
2.1 Taksonomi Tumbuhan, Morfologi, Habitat dan Manfaat ……… 9
2.2 Perkembangan Penelitian Kimia dari S. album ………. 11
2.3 Steroid Sebagai Turunan Triterpenoid ……….. 17
2.3.1 Tatanama Senyawa Steroid ……….……….. 19
2.3.2 Penomoran Atom Karbon dalam Senyawa Steroid dan Triterpenoid 19 2.3.3 Kejadian Senyawa Steroid dalam Kayu dan Kulit ……… 23
2.3.4 Biosintesis Senyawa Steroid ………. 24
2.4 Penentuan Struktur Senyawa Steroid ……….………... 27
2.4.1 Spektroskopi IR ……… 27
2.4.2 Spektroskopi NMR proton (NMR-1H) …..……….……….. 29
2.4.3 Spektroskopi NMR karbon (NMR-13C) ……..………. 36
2.5 Diabetes Mellitus ………. 43
2.5.1 Insulin ………... 44
2.5.2 Oral Hypoglycemic Agent (OHA) ………... 47
BAB III METODOLOGI PENELITIAN …………..………. 57
3.1 Tempat dan Waktu ………... 57
3.2 Bahan Penelitian ……… 57
3.2.1 Bahan Tumbuhan ……….. 57
3.2.2 Bahan Kimia ………. 57
3.3 Hewan Percobaan ……….. 57
3.4 Peralatan ……… 58
3.5 Prosedur Kerja ……….………. 58
3.5.1 Pengujian Triterpenoid/Steroid ……….……… 58
3.5.2 Ekstraksi dan Fraksinasi ……… 58
3.5.3 Pemisahan dan Pemurnian ………. 59
3.5.4 Uji Kemurnian dan Penentuan Sifat Fisis ………. 61
3.5.5 Identifikasi dan Penentuan Struktur Molekul ……… 61
3.5.6 Uji Aktivitas Hipoglisemik ……….………..… 61
3.5.7 Penggunaan Alat ……… 63
3.5.8 Metode Perhitungan Pengujian Efek Penurunan Kadar Gula Darah . 64 BAB IV HASIL DAN PEMBAHASAN ……….. 66
4.1 Pengumpulan Bahan Tumbuhan S. album ……… 66
4.2 Tahap Ekstraksi Tumbuhan S. album ………... 66
4.3 Uji Aktivitas Hipoglisemik Ekstrak Metanol ………... 67
4.4 Tahap Fraksinasi ……….….. 74
4.5 Tahap Pemisahan dan Pemurnian ………. 75
4.6 Uji Kemurnian ………... 78
4.7 Penentuan Struktur Molekul ………. 79
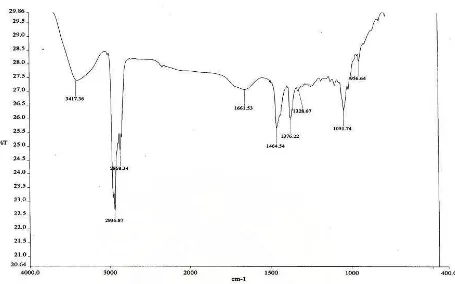
4.7.1 Spektroskopi Inframerah (FTIR) ……..….………... 79
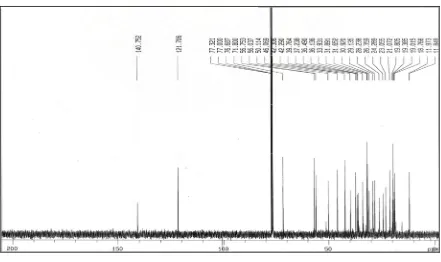
4.7.2 Spektroskopi NMR karbon ……….……….. 82
4.7.3 Spektroskopi DEPT ……….. 84
4.7.5 Spektroskopi NMR proton ……… 94
4.7.6 Spektroskopi HMQC ……….……… 96
4.7.7 Spektroskopi COSY ……….….. 99
4.7.8 Spektroskopi HMBC ………. 102
BAB V KESIMPULAN DAN SARAN ……… 108
5.1 Kesimpulan ……… 108
5.2 Saran ………... 109
DAFTAR PUSTAKA ……… 110
DAFTAR GAMBAR
Halaman
Gambar 1. Senyawa triterpenoid/steroid dalam S. album ………... 2
Gambar 2. Struktur senyawa senegin-II …….………. 4
Gambar 3. Struktur senyawa kotalegenin-16 asetat …………..………. 4
Gambar 4. Empat triterpenoid dari daun Gymnema inodorum ……….….… 5
Gambar 5. Struktur senyawa asam dehidrotrametenolat dan asam colosolat ….… 5 Gambar 6. Lima fitosterol dari Aloe vera ………... 6
Gambar 7. Tumbuhan S. album Linn. ……… 10
Gambar 8. Struktur senyawa α-amirin palmitat ……..………... 11
Gambar 9. Senyawa seskuiterpena dalam minyak S. album ………... 11
Gambar 10. Senyawa santalol dan turunannya dalam minyak S. album …………... 12
Gambar 11. Stereoisomer dari β-bisabolol dalam minyak S. album ………. 12
Gambar 12. Komponen utama minyak S. album ……….…….. 13
Gambar 13. Biosintesis santalena dan bergamotena ……….……. 13
Gambar 14. Jalur biosintesis dari farnesil difosfat ke kurkumena, bisabolena dan bisabolol, dan cis lanceol ……….... 14
Gambar 15. Beberapa senyawa aromatik dari heartwood S. album ……….. 15
Gambar 16. Seskuiterpena tipe camphrenana dan santalena dari heartwood S. album ………. 15
Gambar 17. Struktur senyawa asam betulinat dan β-sitosterol ……… 16
Gambar 18. Berbagai produk yang dihasilkan dari S. album ……… 16
Gambar 19. Kolesterol dan turunan dihidronya ……… 17
Gambar 20. Struktur steroid dasar dengan sistem penomoran ………..……… 19
Gambar 21. Struktur steroid dasar dengan penomoran karbon ………. 20
Gambar 22. Konformasi epimer C-24 dalam steroid ………..……….. 21
Gambar 23. Konformasi kolestana (5α) dan koprostana (5β) ……….. 21
Gambar 25. Struktur senyawa kampesterol dan spinasterol ..……… ….. 23
Gambar 26. Biosintesis skualena oksida ……… 25
Gambar 27. Biosintesis steroid dan triterpenoid tetrasiklik dari skualena oksida …. 26 Gambar 28. Biosintesis sikloartenol dari skualena oksida ……… 27
Gambar 29. Spektrum IR dari kolesterol ……….…….….… 28
Gambar 30. Spektrum NMR-1H dari kolesterol ………..…..…… 31
Gambar 31. Spektrum massa dari kolesterol bebas dan kolesteril asetat .……..…... 38
Gambar 32. Mekanisme kehilangan rantai sisi dan karbon C-15, C-16 dan C-17 dari 5α-stanol ……….…….… 39
Gambar 33. Mekanisme kehilangan rantai sisi dan karbon C-15, C-16 dan C-17 dari Δ7-sterol atau Δ8(14)-sterol ………. 40
Gambar 34. Dua mekanisme fragmentasi dari Δ5-sterol bebas ………... 41
Gambar 35. Fragmentasi ion dalam spektrum massa Δ7-sterol …….………. 42
Gambar 36. Reaksi retro Diels-Alder untuk β-amirin …..…………..………..….. 43
Gambar 37. Metabolisme karbohidrat pada penderita diabetes mellitus ………… 44
Gambar 38. Insulin dalam makhluk hidup ……….……… 45
Gambar 39. Proinsulin manusia dan konversinya menjadi insulin …….…….…... 46
Gambar 40. Sisi aktif insulin ………..……… 46
Gambar 41. Struktur dasar sulfonilurea ……….. 48
Gambar 42. Struktur senyawa tolbutamida ………. 48
Gambar 43. Struktur group toluena-p-sulfonil ……… 48
Gambar 44. Sintesis dari senyawa tolbutamida ……… 49
Gambar 45. Struktur senyawa kloropropamida ……… 49
Gambar 46. Struktur senyawa glibenklamid ………. 50
Gambar 47. Struktur umum senyawa biguanida ……… 50
Gambar 48. Struktur senyawa fenformin ………... 50
Gambar 49. Struktur senyawa metformin ……… 51
Gambar 50. Sintesis dari metformin ……… 51
Gambar 51. Cara kerja obat sebagai Oral Hypoglicemic Agent ………. 52
Gambar 54. Grafik kadar gula darah mencit selama perlakuan ……….. 68
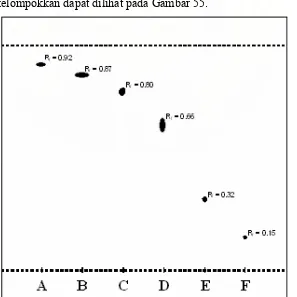
Gambar 55. Kromatografi lapis tipis (silika gel GF254 tebal 0,2 mm, ukuran plat
10 x 9 cm, jarak elusi 8 cm, fase gerak kloroform-etil asetat (9:1),
penampak noda asam sulfat 10% dalam etanol) dari 6 fraksi gabung-
an hasil kromatografi kolom ………. 75
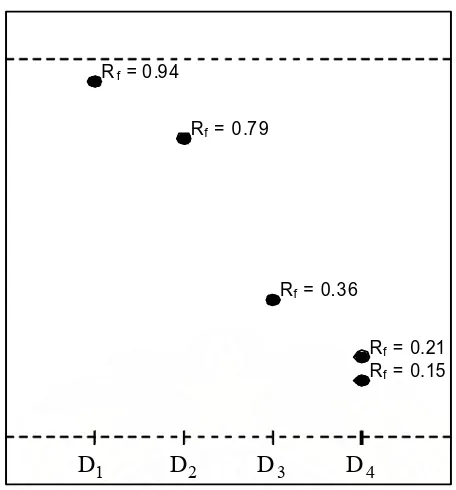
Gambar 56. Kromatografi lapis tipis (silika gel GF254 tebal 0,2 mm, ukuran plat
10 x 6 cm, jarak elusi 8 cm, fase gerak petroleum eter-eter (1:1),
penampak noda asam sulfat 10% dalam etanol) dari 4 fraksi gabung-
an hasil kromatografi kolom ………. 77
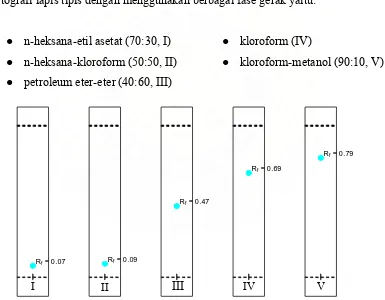
Gambar 57. Kromatografi lapis tipis isolat (fraksi D3) hasil kromatografi kolom
(silika gel GF254 pada berbagai fase gerak, tebal 0,2 mm, ukuran plat
10 x 2 cm, jarak elusi 8 cm, penampak noda asam sulfat 10% dalam
etanol ………. 78
Gambar 58 Spektrum inframerah dari fraksi D3 menggunakan pellet KBr ………. 80
Gambar 59. Posisi gugus OH dalam konformasi ekuatorial ………. 82
Gambar 60. Spektrum NMR-13C (100 MHz, CDCl3) dari fraksi D3 ………….. 82
Gambar 61 Spektrum DEPT dari fraksi D3 ……….. 84
Gambar 62 Spektrum MS dari fraksi D3 ………... 85
Gambar 63 Delapan kemungkinan senyawa dengan massa 414 ……….. 86
Gambar 64 Pemutusan metil terminal disertai dengan pengeluaran molekul air …. 88
Gambar 65 Pembentukan ion molekul m/z 396 dan m/z 371 ………….…………... 88
Gambar 66 Pemutusan rantai sisi disertai dengan pelepasan molekul air …………. 88
Gambar 67 Dua mekanisme fragmentasi dari Δ5-sterol menghasilkan m/z 329
dan 111 ……….. 90
Gambar 68 Pemutusan metil terminal disertai dengan pengeluaran molekul air …. 91
Gambar 69 Pembentukan ion molekul m/z 396 dan m/z 371 ……….………. 91
Gambar 70. Pemutusan rantai sisi disertai dengan pelepasan molekul air ………… 91
Gambar 71 Pemutusan C-16, C-17 dan molekul air ………. 92
Gambar 72 Reaksi retro Diels-Alder dari ikatan Δ7 ……….. 92
Gambar 75 Spektrum NMR-1H (400 MHz, CDCl3) dari fraksi D3 ……….. 94
Gambar 76 Perbesaran spektrum NMR-1H dari fraksi D3 ……… 95
Gambar 77 Spektrum HMQC dari fraksi D3 ……… 96
Gambar 78 Perbesaran spektrum HMQC dari fraksi D3 ………... 97
Gambar 79 Spektrum COSY dari fraksi D3 ……….. 99
Gambar 80 Perbesaran spektrum COSY dari fraksi D3 ………. 100
Gambar 81 Korelasi antara proton-proton dalam spektrum COSY dari fraksi D3 … 101 Gambar 82 Spektrum HMBC dari fraksi D3 ………. 102
Gambar 83 Perbesaran spektrum HMBC dari fraksi D3 ………..…. 103
Gambar 84 Korelasi yang terjadi pada karbon C-1, C-5, C-9, dan C-10 …………. 104
Gambar 85 Korelasi yang terjadi pada karbon C-12, C-13, C-14, C-16, dan C-17 . 104 Gambar 86 Korelasi yang terjadi pada karbon C-17, C-20, dan C-22 …………..… 105
Gambar 87 Korelasi yang terjadi pada karbon C-24, C-25, C-26, C-27, C-28, dan C-29 ………... 105
Gambar 88 Korelasi antara karbon dengan proton dalam spektrum HMBC ………. 106
DAFTAR TABEL
Halaman
Tabel 1. Karakteristik Tumbuhan Santalum album …..……….………... 10
Tabel 2. Nilai absorpsi inframerah ikatan C-O streching untuk senyawa dengan
penggabungan cis- atau trans- cincin A/B, suatu ikatan rangkap dua
dalam cincin B atau suatu group 3α/β-hidroksil ……….………… 29
Tabel 3. Chemical shift (δ, ppm; CDCl3) dari signal H-3 metin dan metil 3-ase-
toksi dalam spektrum NMR-1H dari sterol dan triterpena alkohol ……. 33
Tabel 4. Chemical shift (δ, ppm; CDCl3) dari signal proton olefinat dan allilat
dalam spektrum NMR-1H dari sterol ………. 35
Tabel 5. Karakteristik chemical shift 13C dari sterol dan triterpena alkohol …… 37
Tabel 6. Negara dengan angka tertinggi penderita diabetes mellitus (juta) ……. 44
Tabel 7. Rancangan Penelitian yang digunakan (Rancangan Acak Lengkap) …. 64
Tabel 8. Tabel ANAVA ……… 65
Tabel 9. Hasil uji fitokimia ekstrak metanol pekat akar S. album ….……….….. 66
Tabel 10. Data kadar gula darah mencit setelah pemberian suspensi ekstrak
Akar S. album ………. 67
Tabel 11. Hasil perhitungan Anava kadar gula darah mencit selama 30 menit
perlakuan ……….... 68
Tabel 12. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah
30 menit perlakuan ……….……… 69
Tabel 13. Hasil perhitungan Anava kadar gula darah mencit setelah 60 menit
perlakuan ……… 69
Tabel 14. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah
60 menit perlakuan ……….……… 69
Tabel 15. Hasil perhitungan Anava kadar gula darah mencit setelah 90 menit
perlakuan ……….……….. 70
Tabel 16. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah
Tabel 17. Hasil perhitungan Anava kadar gula darah mencit setelah 120 menit
perlakuan ……… 71
Tabel 18. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 120 menit perlakuan ………..……… 71
Tabel 19. Hasil perhitungan Anava kadar gula darah mencit setelah 150 menit perlakuan ………... 72
Tabel 20. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 150 menit perlakuan ………..……… 72
Tabel 21. Hasil perhitungan Anava kadar gula darah mencit setelah 180 menit perlakuan ……….………. 73
Tabel 22. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 180 menit perlakuan ……….. 73
Tabel 23. Perbandingan aktivitas hipoglisemik berdasarkan uji Anava & Duncan 74 Tabel 24. Hasil uji fitokimia dan perolehan berat ekstrak dari fraksi kloroform dan air ………. 74
Tabel 25. Hasil uji steroid dan perolehan berat ekstrak dari fraksi A, B, C, D, E, dan F ……….. 76
Tabel 26. Hasil uji steroid dan perolehan berat ekstrak dari fraksi D1, D2, D3, dan D4………. 77
Tabel 27. Nilai Rf noda kromatogram lapis tipis dari fraksi D3 pada berbagai fase gerak ………..………. 79
Tabel 28. Interpretasi spektrum inframerah (bilangan gelombang, bentuk pita, intensitas, dan penempatan gugus terkait) dari isolat ………. 80
Tabel 29. Korelasi frekuensi C-O dengan stereokimia …….………. 81
Tabel 30. Data pergeseran kimia fraksi D3 ……….………..……… 83
Tabel 31. Perbandingan data NMR-13C hasil penelitian dan data literatur (Li-Lin Tay, 1997) ………..……… 83
Tabel 32. Data karbon CH2 dan CH/CH3 dari fraksi D3 ………..….. 84
Tabel 33. Data hubungan spektrum NMR-13C dan DEPT ……….…… 85
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Identifikasi Tumbuhan Santalum album Linn. ……… 114
Lampiran 2. Analisis Data dengan Metode Anava ……….. 115
Lampiran 3. Contoh Perhitungan ………. 118
Lampiran 4. Tabel Duncan ………... 122
Lampiran 5. Konformasi Chair-Boat-Chair-Boat-Unfold : Lanostana dan tipe yang berhubungan ………..……. 123
Lampiran 6. Konformasi Chair-Chair-Chair-Boat-Unfold : Dammarana dan tipe yang berhubungan ……… 124
Lampiran 7. Konformasi Chair-Chair-Chair-Boat-Unfold : Lupana dan tipe yang berhubungan ……… 125-126 Lampiran 8. Konformasi Chair-Chair-Chair-Chair-Chair : Hopana dan tipe yang berhubungan ……… 127
Lampiran 9. Konformasi Chair-Boat-Chair-Chair-Boat : Arborana dan tipe yang berhubungan ……… 128
Lampiran 10. Kerangka dan Penomoran Steroid .………..… 129
Lampiran 11. Hidrokarbon induk, cincin dan rantai sisi untuk sterol ……… 130
Lampiran 12. Posisi Karakteristik Pita Inframerah ……… 131
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan salah satu negara yang memiliki hutan tropis yang amat
luas dan negara kedua terkaya dengan keanekaragaman hayati sesudah Brazilia
(Achmad, 1995). Hutan tropis tersebut merupakan sumber daya alam yang menjadi
harta kekayaan serta tambang untuk eksplorasi bahan-bahan kimia yang sangat potensial
untuk dikembangkan sebagai salah satu tiang penyangga pembangunan nasional.
Indonesia memiliki sekitar 25.000 spesies tumbuhan endemik dan 2000 spesies di
antaranya secara etnobotani memiliki kegunaan sebagai bahan pangan, sandang, dan
papan. Selanjutnya sekitar 900 spesies tumbuhan tersebut telah digunakan sebagai obat
tradisional untuk berbagai macam penyakit (Heyne, 1987). Data tersebut menunjukkan
bahwa belum maksimalnya eksplorasi yang dilakukan dalam upaya menelusuri
bahan-bahan kimia (metabolit sekunder) yang terkandung dalam tumbuhan tersebut.
Metabolit sekunder yang dihasilkan oleh tumbuhan terbagi ke dalam beberapa
golongan utama antara lain alkaloid, flavonoid, terpenoid dan terbentuk melalui empat
jalur biosintesis yaitu asam sikimat, asam asetat malonat, poliketida, dan asam
mevalonat. Banyak di antara metabolit sekunder tersebut mempunyai aktivitas biologis
dapat mengobati berbagai penyakit, salah satunya adalah mengobati penyakit diabetes
mellitus yang merupakan penyakit yang terjadi karena defisiensi insulin.
Berbagai obat diabetes mellitus telah disintesis seperti golongan sulfenilurea,
biguanida, thiazolidinedion, dan meglitinida untuk dapat mengatasi diabetes mellitus.
Berbagai kendala terjadi pada obat sintesis yaitu dapat memberikan efek samping
(http://www.med.sc.edu:1082) dan biaya yang lebih besar dalam menghasilkan
obat-obat tersebut (DeFronzo, 1999). Untuk mengatasi hal tersebut maka digalilah sumber
dari tumbuhan-tumbuhan sebagai penghasil metabolit sekunder. Berbagai tumbuhan
seperti bitter melon (Momordica charantia) digunakan sebagai obat tradisional untuk
charantin (steroid glikosida) yang mempunyai aktivitas hipoglisemik. Benih Fenugreek
(Trigonella foenum-gracum) mengandung diosgenin (sapogenin) yang berkhasiat
mengobati diabetes mellitus. Gumar (Gymnema sylvestre) merupakan tumbuhan yang
berpotensi dalam mengatasi diabetes mellitus. Daunnya mengandung senyawa aktif
asam gymnemat (triterpenoid saponin). Aloe vera (Aloe barbadensis Muller) juga
merupakan tumbuhan yang berkhasiat. Senyawa fitosterol yang dihasilkannya
mempunyai aktivitas dalam mengatasi diabetes mellitus
(http://www.nutraceu-ticalsworld.com).
Tumbuhan Santalum album Linn merupakan salah satu tumbuhan yang ada di
Indonesia. Tumbuhan ini oleh masyarakat di Samarinda, akarnya digunakan sebagai
obat tradisional dalam mengobati penyakit diabetes mellitus. Menurut literatur yang
diperoleh bahwa tumbuhan S. album mengandung senyawa-senyawa seskuiterpena.
Senyawa-senyawa ini terdapat dalam minyak S. album (Sandalwood oil). Seskuiterpena
yang terbanyak adalah α-santalol dan β-santalol (Christenson et al., 1981) disamping
santalena dan bergamotena. Senyawa santalol mempunyai aktivitas antibakteri dan
sedatif (Mahon, 2004). Hubungan biosintesis antara seskuiterpena yang terdapat dalam
tumbuhan S. album telah diteliti (Jones et al, 2006). Senyawa triterpenoid/steroid yang
telah dilaporkan dalam S. album (Gambar 1) terdapat dalam daun yaitu β-sitosterol
(steroid) dan dalam kulit batang yaitu amirin palmitat (triterpenoid ester). Amirin
palmitat mempunyai aktivitas insektisida melawan Atteva fabriciella, Eligama norcissu
dan Eupterote geminata (Malavadhani, 2004), sedangkan dalam akar belum ada
publikasi yang menunjukkan adanya steroid.
Gambar 1. Senyawa triterpenoid/steroid dalam S. album
O
H H
H
CH3(CH2)14
O
α-amirin palmitat HO
Biosintesis senyawa seskuiterpena (C15) berasal dari prekursor farnesil
pirofosfat. Bila molekul farnesil pirofosfat mengalami dimerisasi satu sama lain maka
akan dihasilkan suatu molekul lebih besar yaitu skualena. Skualena merupakan
prekursor dari senyawa triterpenoid (C30). Skualena dapat mengalami penataan ulang
dan disertai pembentukan cincin akan menghasilkan berbagai tipe kerangka triterpenoid
sebagai berikut:
a. Konformasi Chair-Boat-Chair-Boat-Unfold menghasilkan senyawa triterpenoid tipe
Lanostana dan turunannya (Lampiran 5)
b. Konformasi Chair-Chair-Chair-Boat-Unfold menghasilkan senyawa triterpenoid
tipe Dammarana dan turunannya (Lampiran 6)
c. Konformasi Chair-Chair-Chair-Boat-Unfold menghasilkan senyawa triterpenoid
tipe Lupana, Oleanana, Ursana dan turunannya (Lampiran 7)
d. Konformasi Chair-Chair-Chair-Chair-Chair menghasilkan senyawa triterpenoid
tipe Hopana dan turunannya (Lampiran 8)
e. Konformasi Chair-Boat-Chair-Chair-Boad menghasilkan senyawa triterpenoid tipe
Arborana dan turunannya (Lampiran 9)
Triterpenoid merupakan famili terbesar ketiga dari terpenoid. Kurang lebih 40
kerangka triterpenoid telah ditemukan. Senyawa triterpenoid dapat diklasifikasikan ke
dalam 4 golongan besar yaitu triterpena dan steroid beserta glikosida dari keduanya
(Dev, 1989). Beberapa senyawa triterpenoid mempunyai aktivitas seperti anti fungal,
anti inflamasi, anti HIV, anti diabetes dan lain sebagainya (Beecher et al., 1989).
Penelitian mengenai kandungan senyawa triterpenoid/steroid dalam tumbuhan
S. album tidak banyak dibandingkan penelitian mengenai senyawa seskuiterpena,
padahal prekursor yang dihasilkan berupa farnesil pirofosfat melimpah. Hal ini dapat
dilihat dari komponen terbanyak yaitu senyawa seskuiterpena.
Beberapa senyawa triterpenoid/steroid ada yang mempunyai aktivitas sebagai
Oral Hypoglycemic Agent (OHA). Senegin-II (Gambar 2), suatu triterpenoid glikosida
dari rhizoma Polygala senega L. var. latifolia Torrey et Gray (Polygalaceae)
menurunkan glukosa darah dari tikus normal dari 191 ± 3 sampai 120 ± 3 mg/dl 4 jam
(Kako et al., 1996).
Kotalegenin-16 asetat (Gambar 3), suatu triterpenoid ester tipe Friedelana dari
akar Salacia oblonga Wall. (Celastraceae) menunjukkan aktivitas menghambat aldosa
reduktase. Aldosa reduktase adalah enzim yang mengubah glukosa menjadi sorbitol dan
dihubungkan pada komplikasi diabetes kronik seperti periferal neuropathy, retinopathy
dan katarak (Matsuda et al., 1999).
Gambar 2. Struktur senyawa senegin-II O
O
OH
HO OH
OH
HO
H H
OH
O
OH H
O
O O
O OH
O
O
O O
O
O O
O O
OH
OH HO
OH OH
HO
OH
OH
senegin-II
O
O OH
O C
O CH3
kotalegenin-16 asetat
Empat triterpenoid (Gambar 4) dari daun Gymnema inodorum menunjukkan
aktivitas menghambat absorpsi glukosa dalam intestinal. Triterpenoid tersebut adalah
asam (3β,16β,22α)-16,28-dihidroksiolean-12-en-3-il-O-β-D-glukopiranosil-β
-D-gluko-piranosidu ronat (GiA-1), asam (3β,4α,16β)-16,23,28-trihidroksiolean-12-en-3-il-β
-D-glukopirano-siduronat (GiA-2), asam (3β,4α,16β,22α
)-22-(N-metilantraniloksi)-16,23,28-trihidroksi-olean-12-en-3-il-3-O-β-D-glukopiranosil-β-D-lukopiranosiduronat
(GiA-3) dan asam (3β,4α,16β,22α
)-22-(N-metilantraniloksi)-16,23,28-trihidroksiolean-12-en-3-il-β-D-gluko-piranosiduronat (GiA-4) (Shimizu et al., 2001).
R6H2C CH2R5
CH3
H3C
R1
CH2R3
R4
R2
CH3 CH3
O O
OR7
HOOC
HO
R8O
CH3
H
H
H
Senyawa R1 R2 R3 R4 R5 R6 R7 R8
GiA-1 H H OH OH H H β-Glu H
GiA-2 H H OH OH OH H H H
GiA-3 H O-NMAt OH OH OH H H β-Glu
GiA-4 H O-NMAt OH OH OH H H Η
β-Glu : -β-glucopyranosyl; O-NMAt : -O-N-methylanthraniloxy
Gambar 4. Empat triterpenoid dari daun Gymnema inodorum
Asam dehidrotrametenolat, suatu triterpenoid tipe Lanostana dari Poria cocos
Wolf (Polyporaceae) yang ditemukan pada akar tumbuhan pine menunjukkan efek
sebagai insulin sensitizer (Sato et al., 2002). Asam colosolat dari daun Langerstonemia
speciosa (L.) Pers. (Lythraceae) menunjukkan sebagai aktivator transportasi glukosa
(Okada et al., 2003). Struktur asam dehidrotrametenolat dan asam colosolat dipaparkan
HO
OH HOOC
asam dehidrotrametenolat
HO O
COOH
asam colosolat
Gambar 5. Struktur senyawa asam dehidrotrametenolat dan asam colosolat
Lima fitosterol (Gambar 6) dari Aloe vera (Aloe barbadensis Muller)
menunjukkan efek anti diabetes. Senyawa triterpenoid tersebut adalah lophenol,
24-metillophenol, 24-etillophenol, sikloartanol dan 24-metilena sikloartanol (Tanaka et al.,
2006).
Gambar 6. Lima fitosterol dari Aloe vera Gambar 6. Lima fitosterol dari Aloe vera HO
24-metil lophenol
HO
24-etil lophenol HO
lophenol
HO
24-me HO
Tumbuhan S. album telah dikembangkan penggunaannya sebagai medisinal dan
aromaterapi. Penggunaannya (Mahon, 2004) adalah sebagai berikut :
a. Sistem pencernaan (digestive) membantu mengobati diare dan mual-mual (nausea)
b. Sistem pernafasan (respiratory) terutama untuk mengobati bronchitis, catarrh, batuk
kering, laryngitis
c. Sistem saraf (nervous) mengobati migraine, insomnia, stres
d. Sistem kulit (skin care) mengobati dermatitis akut, akne, kulit kering (dry chapped
skin) dan kulit berminyak (greasy skin)
e. Aplikasi medisinal untuk mengobati penyakit mata, gonorrhea, herpes, infeksi,
sebagai antiseptik, antibakteri, astringen, carminative, disinfektan, diuretik,
ekspektoran, refrigeran, sedatif dan stimulan
f. Industri parfum : sebagai komponen fragrance dalam sabun, deterjen, kosmetik dan
parfum sedangkan dalam industri makanan sebagai flavor ingredient dalam sebagian
besar kategori makanan termasuk soft drink dan alkoholik drink
1.2 Perumusan Masalah
a. Apakah akar tumbuhan Santalum album Linn mengandung senyawa steroid.
b. Bagaimana cara-cara/teknik mengisolasi dan memurnikan senyawa steroid tersebut.
c. Bagaimana kerangka atau struktur senyawa steroid yang terdapat dalam akar S.
album.
d. Apakah akar tumbuhan S. album mempunyai aktivitas sebagai Oral Hypoglycemic
Agent.
1.3 Tujuan Penelitian
a. Mengisolasi senyawa steroid dari akar tumbuhan Santalum album.
b. Mengetahui cara-cara/teknik mengisolasi dan memurnikan senyawa steroid tersebut.
c. Menentukan struktur senyawa steroid dengan menggunakan metode kimia (uji
kemurnian dengan berbagai pelarut) dan metode fisikokimia (menggunakan
spektrometer IR, NMR-1H, NMR-13C, DEPT, COSY, HMQC, HMBC, dan MS).
1.4 Manfaat Penelitian
a. Memberikan infomasi tentang kandungan senyawa steroid dari akar tumbuhan
Santalum album dan sebagai database tentang penyebaran senyawa steroid dalam
akar.
b. Memberikan infomasi tentang aktivitas dari akar tumbuhan Santalum album sebagai
obat diabetes mellitus alami yang ramah terhadap lingkungan dan murah sehingga
dapat diaplikasikan dalam bidang kesehatan.
1.5 Metode Penelitian
Metode yang digunakan dalam penelitian ini adalah determinasi tumbuhan,
pengambilan sampel, penelusuran pustaka, melakukan skrining fitokimia senyawa
streroid dengan uji Liebermann-Burchard, melakukan isolasi dengan ekstraksi secara
maserasi dan fraksinasi menurut kepolarannya, melakukan pemisahan dan pemurnian
dengan menggunakan kromatografi kolom dan silika gel sebagai fase diam, melakukan
uji kemurnian dengan cara kimia yaitu menggunakan kromatografi lapis tipis dengan
berbagai pelarut, melakukan elusidasi struktur molekul dengan menggunakan
spektrometer IR, NMR-1H, NMR-13C, DEPT, COSY, HMQC, HMBC, dan MS, dan
melakukan uji aktivitas hipoglisemik dari ekstrak metanol akar tumbuhan Santalum
album untuk mengetahui khasiat akar tumbuhan S. album sebagai obat diabetes
BAB III
METODOLOGI PENELITIAN
3.1 Tempat dan Waktu
Penelitian ini dilakukan di Laboratorium Penelitian, Laboratorium Biokimia,
Laboratorium Kimia Organik Bahan Alam, Laboratorium Farmasi di Universitas
Sumatera Utara - Medan, dimulai pada bulan September 2005 sampai Desember 2006.
3.2 Bahan Penelitian 3.2.1 Bahan Tumbuhan
Bahan tumbuhan yang digunakan dalam penelitian ini adalah akar tumbuhan
Cendana (Santalum album Linn.) diperoleh dari pasar tradisional di kota Samarinda.
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense Bogor (Lampiran 1).
3.2.2 Bahan Kimia
Bahan kimia yang digunakan terdiri atas berbagai jenis pelarut organik teknis
dan proanalis yang biasa digunakan di Laboratorium Kimia Organik Bahan Alam
seperti metanol teknis, kloroform, akuades, n-heksan, etil asetat, petroleum eter, eter,
benzena, silika gel Merck GF254 untuk kromatografi lapis tipis, silika gel 60 (70-230
mesh, E. Merck) untuk kromatografi kolom, pereaksi Liebermann-Burchard untuk uji
steroid, dan bahan yang digunakan untuk uji toleransi glukosa (aktivitas hipoglisemik)
yaitu CMC (carboxy methyl cellulose) sebagai pensuspensi, glibenklamid, dan glukosa.
3.3 Hewan Percobaan
Hewan yang digunakan dalam penelitian ini adalah mencit jantan yang sehat
dengan berat badan 25-38 g. Sebelum pengujian terlebih dahulu mencit dipelihara dan
dirawat dengan sebaik-baiknya sekurang-kurangnya selama 2 minggu. Selanjutnya
dapat digunakan lagi secara berulang untuk percobaan berikutnya setelah interval masa
3.4 Peralatan
Alat-alat yang digunakan terdiri atas berbagai alat gelas yang biasa digunakan di
Laboratorium Kimia Organik Bahan Alam seperti seperangkat alat destilasi, corong
pisah, neraca analitik Mettler PM480 Delta Range, evaporator R 114 Buchi dilengkapi
dengan sistem vakum Buchi B 169, oven, kromatografi kolom, sumber UV Matsui
MT-09 MHE dan Mineralight Lamp Model UVG-54, spektroskopi inframerah FTIR Perkin
Elmer 1600, spektroskopi JEOL 400 MHz JNM-FX400 (NMR-1H, NMR-13C, DEPT
dan NMR-2D), dan spektroskopi massa Shimadzu QP2000A 70 eV untuk penentuan
struktur. Neraca hewan (GW-1500), glucometer dan glucotest strip (EZ Smart), Syringe
1 ml, mortir dan pemanas air untuk uji aktivitas hipoglisemik.
3.5 Prosedur Kerja
3.5.1 Pengujian Triterpenoid/Steroid
Sepuluh gram akar tumbuhan S. album halus diekstraksi dengan metanol.
Ekstrak metanol kemudian diuapkan dan diekstraksi dengan eter. Residu yang tidak
larut dalam eter dikocok kuat-kuat. Adanya busa yang stabil selama 30 menit
menunjukkan adanya saponin. Selanjutnya dihidrolisis dengan asam klorida 2 N
sebanyak 4 ml dan disaring. Endapan diuji dengan pereaksi Liebermann-Burchard.
Warna ungu menunjukkan adanya saponin. Ekstrak eter diuji dengan pereaksi
Liebermann-Burchard. Warna hijau menunjukkan adanya steroid dan warna merah
menunjukkan adanya triterpena (Lajis, 1985).
3.5.2 Ekstraksi dan Fraksinasi
Serbuk akar tumbuhan S. album sebanyak 2,0 kg diekstraksi secara maserasi
dengan menggunakan pelarut metanol selama 24 jam sambil diaduk. Ekstrak metanol
dipisahkan dengan cara penyaringan. Maserasi ini dilakukan selama 3 x 24 jam
sehingga kandungan senyawa kimia dalam bahan terekstraksi semaksimal mungkin ke
dalam pelarut metanol. Ekstrak metanol kemudian dipekatkan dengan menggunakan
evaporator sampai diperoleh ekstrak metanol pekat (48,3 g; 2,415%).
Ekstrak metanol pekat yang diperoleh diambil 250,0 mg untuk uji aktivitas
dengan menggunakan pelarut kloroform. Selanjutnya masing-masing fraksi dipekatkan
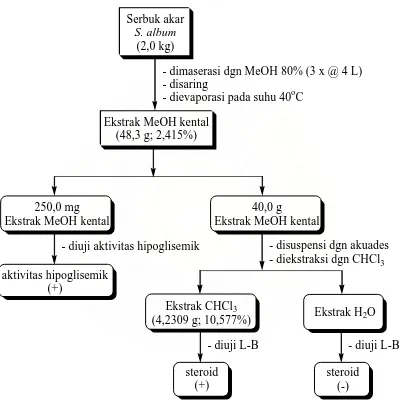
dan diuji steroid. Bagan kerja tahap ekstraksi dan fraksinasi tersebut ditunjukkan pada
Gambar 52, ternyata fraksi ekstrak CHCl3 positif steroid sedangkan fraksi air negatif
steroid.
Serbuk akar
S. album
(2,0 kg)
- dievaporasi pada suhu 40oC
Ekstrak MeOH kental (48,3 g; 2,415%)
- disuspensi dgn akuades - diekstraksi dgn CHCl3
Ekstrak CHCl3
(4,2309 g; 10,577%) Ekstrak H2O - dimaserasi dgn MeOH 80% (3 x @ 4 L) - disaring
- diuji aktivitas hipoglisemik
40,0 g
Ekstrak MeOH kental
aktivitas hipoglisemik (+)
- diuji L-B
steroid (+) 250,0 mg
Ekstrak MeOH kental
- diuji L-B
[image:32.595.103.502.210.617.2]steroid (-)
Gambar 52. Bagan kerja tahap ekstraksi dan fraksinasi
3.5.3 Pemisahan dan Pemurnian
Ekstrak kloroform yang menunjukkan positif steroid dipisahkan dengan cara
kromatografi kolom menggunakan fase diam silika gel 60 dan dielusi secara isokratik
setiap fraksi. Semua fraksi hasil pemisahan kromatografi kolom selanjutnya dilakukan
analisis dengan menggunakan kromatografi lapis tipis untuk melihat noda dengan Rf yang
sama. Fraksi-fraksi dengan noda yang sama pada kromatografi lapis tipis digabungkan dan
diuapkan pelarutnya. Kemudian fraksi yang diperoleh diuji steroid ternyata fraksi A, B, C,
E, dan F negatif terhadap steroid sedangkan fraksi D positif terhadap steorid sehingga fraksi
D dimurnikan kembali dengan menggunakan kromatografi kolom. Bagan kerja dari proses
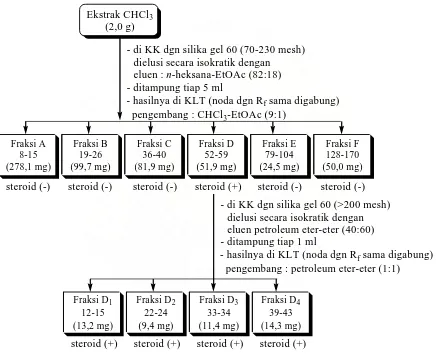
pemisahan dan pemurnian ditunjukkan pada Gambar 53.
- hasilnya di KLT (noda dgn Rf sama digabung) pengembang : CHCl3-EtOAc (9:1)
Fraksi A 8-15 (278,1 mg)
Ekstrak CHCl3 (2,0 g) Fraksi B 19-26 (99,7 mg) Fraksi C 36-40 (81,9 mg) Fraksi D 52-59 (51,9 mg) Fraksi E 79-104 (24,5 mg)
- di KK dgn silika gel 60 (70-230 mesh) dielusi secara isokratik dengan eluen : n-heksana-EtOAc (82:18) - ditampung tiap 5 ml
Fraksi F 128-170 (50,0 mg)
- hasilnya di KLT (noda dgn Rf sama digabung) pengembang : petroleum eter-eter (1:1) - di KK dgn silika gel 60 (>200 mesh)
dielusi secara isokratik dengan eluen petroleum eter-eter (40:60) - ditampung tiap 1 ml
Fraksi D1
12-15 (13,2 mg)
Fraksi D2
22-24 (9,4 mg)
Fraksi D3
33-34 (11,4 mg)
Fraksi D4
39-43 (14,3 mg)
steroid (+) steroid (+) steroid (+) steroid (+)
[image:33.595.84.522.259.618.2]steroid (-) steroid (-) steroid (-) steroid (+) steroid (-) steroid (-)
Gambar 53. Bagan kerja tahap pemisahan dan pemurnian
Fraksi D1, D2, dan D3 telah dikirim ke Malaysia ternyata fraksi D3 yang telah
lengkap data spektroskopinya, fraksi D4 setelah dikromatografi lapis tipis memberikan 2
3.5.4 Uji Kemurnian dan Penentuan Sifat Fisis
Uji kemurnian fraksi D3 dilakukan dengan kromatografi lapis tipis dengan
menggunakan berbagai eluen. Penggunaan GC-MS atau HPLC dapat juga dilakukan
untuk menguji kemurnian. Pengukuran sifat fisis yaitu titik leleh diukur dengan
menggunakan alat Fisher-John Melting Point.
3.5.5 Identifikasi dan Penentuan Struktur Molekul
Penentuan struktur molekul fraksi D3 dilakukan dengan menggunakan
spektroskopi inframerah, spektroskopi NMR 1D yaitu NMR-1H, NMR-13C, DEPT
(Distortionless Enhancement by Polarization Transfer); spektroskopi NMR 2D yaitu
COSY (1H-1H Homonuclear Correlated Spectroscopy), HMQC (1H-13C Heteronuclear
Multiple Quantum Coherence), HMBC (1H-13C Heteronuclear Multiple Bond
Connectivity), dan spektroskopi massa yang dilakukan di Laboratorium Jurusan Kimia
Fakultas Sains Universitas Malaya − Malaysia atas bantuan Dr. Nurdin Saidi dari
Universitas Syiah Kuala – Banda Aceh.
3.5.6 Uji Aktivitas Hipoglisemik
3.5.6.1 Pembuatan Larutan Glukosa 50% (b/v)
Sebanyak 50 g glukosa dilarutkan dengan akuades dalam labu 100 ml.
3.5.6.2 Pembuatan Suspensi CMC (carboxy methyl cellulose) 0,5% (b/v)
Sebanyak 10 ml akuades panas (± 60°C) dimasukkan ke dalam mortir, kemudian
sebanyak 0,5 g CMC ditaburkan secara merata, ditutup dan dibiarkan selama ± 15 menit
hingga diperoleh massa transparan, lalu digerus hingga homogen. Kemudian
ditambahkan akuades, diaduk dengan cepat hingga terbentuk suspensi, lalu dimasukkan
ke dalam labu ukur 100 ml dan dicukupkan dengan akuades hingga garis tanda.
3.5.6.3 Pembuatan Suspensi Glibenklamid 0,02% (b/v)
Sebanyak 0,5 g CMC ditaburkan ke dalam mortir yang berisi akuades panas (±
digerus halus dalam mortir ditambahkan gel CMC sedikit demi sedikit. Kemudian
ditambahkan akuades, diaduk dengan cepat hingga terbentuk suspensi, dimasukkan ke
dalam labu ukur 100 ml, dicukupkan dengan akuades hingga garis tanda.
3.5.6.4 Pembuatan Suspensi Ekstrak Metanol Santalum album 1% (b/v)
Sebanyak 0,5 g CMC ditaburkan ke dalam mortir yang berisi akuades panas (±
60°C) sebanyak 10 ml, ditutup dan dibiarkan ± 15 menit hingga diperoleh massa transparan, lalu digerus hingga homogen. Ke dalam 250 mg ekstrak metanol akar S.
album yang telah digerus halus dalam mortir ditambahkan gel CMC sedikit demi
sedikit. Kemudian ditambahkan akuades, diaduk dengan cepat hingga terbentuk
suspensi, dimasukkan ke dalam labu ukur 25 ml, dicukupkan dengan akuades hingga
garis tanda.
3.5.6.5 Prosedur Kerja Pengujian Efek Farmakologi
Setiap awal percobaan, mencit dipuasakan (tidak makan tetapi tetap minum)
selama 16 jam, kemudian berat badan mencit ditimbang. Kadar gula darah ditentukan
dengan cara mengambil darah melalu vena ekor yang ditusuk dengan menggunakan
jarum suntik. Darah yang keluar dioleskan pada glikostrip yang terpasang pada
glucotest. Dibiarkan selama 8 detik, alat akan bekerja secara otomatis. Angka yang
tampil pada alat dicatat sebagai kadar gula darah (mg/dl).
3.5.6.6 Uji Aktivitas Hipoglisemik
Mencit dipuasakan selama 16 jam. Kemudian berat badan ditimbang dan diukur
kadar gula darah puasa. Mencit kemudian diberi larutan glukosa 50% dosis 4 g/kg berat
badan secara per oral. Kadar gula darah mencit diukur pada selang waktu 30, 60, 90,
120, 150, 180 menit. Cara penentuan kadar gula darah mencit sama seperti point 3.5.6.5.
3.5.6.7 Penentuan Efek Ekstrak Metanol Akar S.album Terhadap Penurunan Kadar
Gula Darah
Mencit dipuasakan selama 16 jam. Kemudian berat badan ditimbang dan diukur
badan secara per oral. Setelah 30 menit diukur kadar gula darah mencit, kemudian
masing-masing mencit diberi:
a. Suspensi kosong (CMC 0,5%) dosis 1% berat badan per oral
b. Suspensi ekstrak metanol akar S. album dosis 25 mg/kg berat badan per oral
c. Suspensi ekstrak metanol akar S. album dosis 50 mg/kg berat badan per oral
d. Suspensi ekstrak metanol akar S. album dosis 75 mg/kg berat badan per oral
e. Suspensi glibenklamid dosis 1 mg/kg berat badan per oral
Kadar gula darah diukur pada selang waktu 60, 90, 120, 150, dan 180 menit.
Cara penentuan kadar gula darah sama seperti point 3.5.6.5.
3.5.7 Penggunaan Alat
Alat glucometer secara otomatis akan hidup ketika strip dimasukkan dan akan
mati ketika strip dicabut. Alat ini tidak menggunakan tombol. Dengan menyentuhkan
setetes darah ke strip, reaksi dari wadah strip secara otomatis menyerap darah ke dalam
strip melalui aksi kapiler. Ketika wadah terisi penuh oleh darah maka alat glucometer
mulai mengukur tingkat glukosa darah. Hasil pengukuran diperoleh selama 8 detik.
2.5.7.1 Prosedur Penggunaan
a. Pengambilan darah mencit dalam keadaan puasa dilakukan dengan cara menyuntik ekor
mencit dengan menggunakan syringe.
b. Ekor yang telah disuntik dengan syringe kemudian diurut ke bawah dengan tujuan agar
darah keluar.
c. Kemudian darah mencit tersebut disentuhkan pad strip sampai terisi penuh. Pada layar
akan muncul angka 8 dan dibiarkan menghitung mundur hingga keluar hasil
pengukuran.
d. Kemudian mencit diberikan larutan glukosa melalui oral dan masing-masing mencit
diberikan CMC 1%, suspensi 25, 50, 75 mg/kg BB dan suspensi glibenklamid. Untuk
pengukuran selanjutnya digunakan strip yang baru.
3.5.8 Metode Perhitungan Pengujian Efek Penurunan Kadar Gula Darah
Data hasil penelitian menggunakan Rancangan Acak Lengkap (Tabel 7),
dianalisis dengan ANAVA (Tabel 8) pada tingkat kepercayaan 95% sedangkan untuk
melihat perbedaan rata-rata yang nyata antar perlakuan dapat digunakan uji rata-rata
Duncan.
Tabel 7. Rancangan Penelitian yang digunakan (Rancangan Acak Lengkap)
Ulangan (r) Perlakuan
(t) W0 W1 W2 W3 Wn
Jumlah (TA)
Rerata (YA)
CMC KGD0C KGD1C KGD2C KGD3C KGDnC ΣCMC YCMC
M25 KGD02 KGD12 KGD22 KGD32 KGDn2 ΣM25 YM25
M50 KGD05 KGD15 KGD25 KGD35 KGDn5 ΣM50 YM50
M75 KGD07 KGD17 KGD27 KGD37 KGDn7 ΣM75 YM75
SG KGD0G KGD1G KGD2G KGD3G KGDnG ΣSG YSG
Jumlah
(TV) ΣW0 ΣW1 ΣW2 ΣW3 ΣWn Tij Yij
Keterangan:
Yij = M + Tij + Eij ……… (1)
dimana : i = 1, 2, 3, ….. t j = 1, 2, 3, ….. r
Yij = respon varietas ke-i dan ulangan ke-j
M = nilai tengah umum Tij = pengaruh perlakuan
Tabel 8. Tabel ANAVA
Sumber
Variasi db JK KT F Hit F Tabel
Perlakuan Galat
t-1 = V1
(rt-1)-(t-1) = V2
JK P JK G
JK P/V1
JK G/V2
KT P/KT G* F (V1,V2)
Total rt-1 JK P + JK G
Keterangan:
FK =Tij2 / rt……….……..…….. (2)
JK Total = T (Yij2) – FK……….. (3)
JK Perlakuan = (TA2 / r) – FK ……..………. (4)
JK Galat = JK Total – JK Perlakuan ……….. (5)
dimana : FK = Faktor Koreksi
JK = Jumlah Kuadrat
db = derajat kebebasan
Bila F Hitung > F Tabel (α = 0,05), maka Ho ditolak artinya ada perbedaan yang
nyata antara kedua nilai rata-rata kadar gula darah mencit. Jadi suspensi ekstrak metanol
akar Santalum album tersebut berkhasiat menurunkan kadar gula darah mencit.
Bila F Hitung < F Tabel (α = 0,05), maka Ho diterima artinya tidak ada
perbedaan yang nyata antara kedua nilai rata-rata kadar gula darah mencit. Dengan
demikian suspensi ekstrak metanol akar Santalum album tersebut tidak berkhasiat
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pengumpulan Bahan Tumbuhan S. album
Bahan tumbuhan berupa akar diperoleh dari kota Samarinda.
4.2 Tahap Ekstraksi Tumbuhan S. album
Pada tahap ekstraksi serbuk akar S. album sebanyak 2 kg dimaserasi dengan
metanol pada suhu kamar. Maserasi dilakukan selama 24 jam dengan tiga kali
perulangan hingga diharapkan semua komponen senyawa terekstraksi ke dalam pelarut
metanol (maserat metanol diuji dengan kromatografi lapis tipis hingga tidak
menunjukkan noda). Maserat dikumpulkan kemudian diuapkan pelarutnya dengan
evaporator pada suhu 40°C. Ekstrak metanol pekat yang diperoleh seberat 48,3 g
(rendemen 2,415% dari 2 kg) dan berwarna merah gelap.
Selanjutnya ekstrak metanol pekat diuji fitokimia. Hasil uji fitokimia
menunjukkan bahwa ekstrak metanol pekat mengandung steroid. Hasil uji tersebut
ditunjukkan pada Tabel 9.
Tabel 9. Hasil uji fitokimia ekstrak metanol pekat akar S. album
Steroid
(Liebermann-Burchard)
Alkaloid (Dragendorff)
Flavonoid (Mg-HCl pekat) Warna hijau
+ - -
Ekstrak metanol pekat kemudian dibagi dua, sebanyak 25,0 mg digunakan untuk
uji aktivitas hipoglisemik dengan menggunakan hewan mencit dan sebanyak 40,0 g
4.3 Uji Aktivitas Hipoglisemik Ekstrak Metanol
Data uji aktivitas hipoglisemik ekstrak metanol akar tumbuhan Santalum album
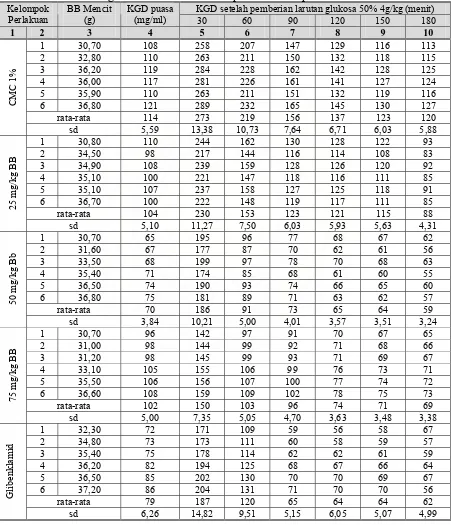
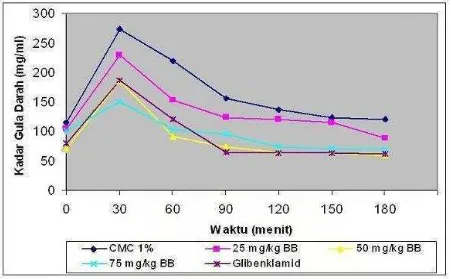
[image:40.595.81.532.209.734.2]Linn terhadap mencit dipaparkan dalam Tabel 10 dan Gambar 54.
Tabel 10. Data kadar gula darah mencit setelah pemberian suspensi ekstrak akar S. album KGD setelah pemberian larutan glukosa 50% 4g/kg (menit) Kelompok
Perlakuan
BB Mencit (g)
KGD puasa
(mg/ml) 30 60 90 120 150 180
1 2 3 4 5 6 7 8 9 10
1 30,70 108 258 207 147 129 116 113
2 32,80 110 263 211 150 132 118 115
3 36,20 119 284 228 162 142 128 125
4 36,00 117 281 226 161 141 127 124
5 35,90 110 263 211 151 132 119 116
6 36,80 121 289 232 165 145 130 127
rata-rata 114 273 219 156 137 123 120
CM
C 1%
sd 5,59 13,38 10,73 7,64 6,71 6,03 5,88
1 30,80 110 244 162 130 128 122 93
2 34,50 98 217 144 116 114 108 83
3 34,90 108 239 159 128 126 120 92
4 35,10 100 221 147 118 116 111 85
5 35,10 107 237 158 127 125 118 91
6 36,70 100 222 148 119 117 111 85
rata-rata 104 230 153 123 121 115 88
25 m g/ k g B B
sd 5,10 11,27 7,50 6,03 5,93 5,63 4,31
1 30,70 65 195 96 77 68 67 62
2 31,60 67 177 87 70 62 61 56
3 33,50 68 199 97 78 70 68 63
4 35,40 71 174 85 68 61 60 55
5 36,50 74 190 93 74 66 65 60
6 36,80 75 181 89 71 63 62 57
rata-rata 70 186 91 73 65 64 59
50 m g/ k g B b
sd 3,84 10,21 5,00 4,01 3,57 3,51 3,24
1 30,70 96 142 97 91 70 67 65
2 31,00 98 144 99 92 71 68 66
3 31,20 98 145 99 93 71 69 67
4 33,10 105 155 106 99 76 73 71
5 35,50 106 156 107 100 77 74 72
6 36,60 108 159 109 102 78 75 73
rata-rata 102 150 103 96 74 71 69
75 m g/ k g B B
sd 5,00 7,35 5,05 4,70 3,63 3,48 3,38
1 32,30 72 171 109 59 56 58 67
2 34,80 73 173 111 60 58 59 57
3 35,40 75 178 114 62 62 61 59
4 36,20 82 194 125 68 67 66 64
5 36,50 85 202 130 70 70 69 67
6 37,20 86 204 131 71 70 70 56
rata-rata 79 187 120 65 64 64 62
G li be nkl am id
Gambar 54. Grafik kadar gula darah mencit selama perlakuan
4.3.1 Pengaruh Pemberian Suspensi Ekstrak Metanol S. album, Glibenklamid dan
CMC 1% terhadap Kadar Gula Darah Mencit pada 30 menit setelah perlakuan
Hasil variansi menunjukkan bahwa pemberian suspensi ekstrak metanol S.
album dan suspensi glibenklamid dengan dosis masing-masing menghasilkan perbedaan
yang signifikan bila dibandingkan dengan kontrol (suspensi CMC 1%). Hal ini terbukti
bahwa F Hitung > F Tabel (Tabel 11) berarti pemberian ekstrak metanol dan
glibenklamid dengan dosis tersebut menyebabkan penurunan kadar gula darah mencit
dibandingkan dengan kontrol.
Tabel 11. Hasil perhitungan Anava kadar gula darah mencit setelah 30 menit perlakuan
Sumber Variasi DB JK KT F Hitung F Tabel
Perlakuan 4 53642,5334 13410,6333 99,0494 2,7587
Galat 25 3384,8333 135,3933
Total 29 57027,3667
Untuk mengetahui perbedaan rata-rata tiap perlakuan dapat dilakukan uji beda
Tabel 12. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 30 menit perlakuan
No. Perlakuan Rata-rata Notasi
1 Suspensi CMC 1% 273 a
2 Suspensi ekstrak metanol 25 mg/kg BB 230 b
3 Suspensi ekstrak metanol 50 mg/kg BB 186 c
4 Suspensi ekstrak metanol 75 mg/kg BB 150,17 d
5 Suspensi Glibenklamid 187 c
Kadar rata-rata gula darah mencit 30 menit setelah pemberian suspensi ekstrak
metanol S. album dengan berbagai dosis menunjukkan perbedaan yang nyata bila
dibandingkan dengan kontrol (CMC 1%) tetapi suspensi ekstrak metanol 50 mg/kg BB
tidak berbeda nyata dengan suspensi glibenklamid. Hal ini berarti pemberian ekstrak
metanol S. album dengan dosis 50 mg/kg BB memberikan efek hipoglisemik yang
relatif sama dengan suspensi glibenklamid (ditunjukkan dengan notasi c).
4.3.2 Pengaruh Pemberian Suspensi Ekstrak Metanol S. album, Glibenklamid dan
CMC 1% terhadap Kadar Gula Darah Mencit pada 60 menit setelah perlakuan
Pemberian ekstrak metanol S. album dosis 25, 50, dan 75 mg/kg BB
menunjukkan berbeda nyata dengan pemberian suspensi glibenklamid pada waktu 60
menit. Hal ini dapat dilihat dari nilai F Hitung > F Tabel (Tabel 13), selanjutnya untuk
mengetahui perlakuan yang menunjukkan perbedaan rata-rata yang bermakna maka
dilakukan uji beda rata-rata Duncan (Tabel 14).
Tabel 13. Hasil perhitungan Anava kadar gula darah mencit setelah 60 menit perlakuan
Sumber Variasi DB JK KT F Hitung F Tabel
Perlakuan 4 63384,8667 15846,2167 249,3896 2,7587
Galat 25 1588,5 63,54
Total 29 64973,3667
Tabel 14. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 60 menit perlakuan
No. Perlakuan Rata-rata Notasi
1 Suspensi CMC 1% 219,17 a
2 Suspensi ekstrak metanol 25 mg/kg BB 153 b
3 Suspensi ekstrak metanol 50 mg/kg BB 91,17 c
4 Suspensi ekstrak metanol 75 mg/kg BB 102,83 c
Dari Tabel 14 terlihat bahwa kadar gula darah mencit pada selang waktu 60
menit setelah pemberian suspensi ekstrak metanol menunjukkan perbedaan yang
signifikan terhadap suspensi glibenklamid dan kontrol (CMC 1%). Hal ini berarti bahwa
suspensi ekstrak metanol 50 dan 75 mg/kg BB mempunyai efek hipoglisemik lebih
besar daripada suspensi glibenklamid dalam menurunkan kadar gula darah mencit.
Suspensi ekstrak metanol dosis 50 mg/kg BB tidak berbeda nyata dengan suspensi
ekstrak metanol dosis 75 mg/kg BB, hal ini berarti bahwa suspensi ekstrak metanol
dosis 50 dan 75 mg/kg BB mempunyai efek hipoglisemik yang relatif sama.
4.3.3 Pengaruh Pemberian Suspensi Ekstrak Metanol S. album, Glibenklamid dan
CMC 1% terhadap Kadar Gula Darah Mencit pada 90 menit setelah perlakuan
Pada selang waktu 90 menit setelah pemberian perlakuan, suspensi ekstrak
metanol dosis 25, 50 dan 75 mg/kg BB menunjukkan berbeda nyata dengan kontrol
(CMC 1%). Hal ini dapat dilihat dari nilai F Hitung > F Tabel (Tabel 15). Untuk
menngetahui perbedaan rata-rata antara perlakuan dilakukan uji beda rata-rata Duncan
(Tabel 16)
Tabel 15. Hasil perhitungan Anava kadar gula darah mencit setelah 90 menit perlakuan
Sumber Variasi DB JK KT F Hitung F Tabel
Perlakuan 4 33594,1334 8398,5333 264,1605 2,7587
Galat 25 794,8333 31,7933
Total 29 34388,9667
Tabel 16. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 90 menit perlakuan
No. Perlakuan Rata-rata Notasi
1 Suspensi CMC 1% 156 a
2 Suspensi ekstrak metanol 25 mg/kg BB 123 b
3 Suspensi ekstrak metanol 50 mg/kg BB 73 c
4 Suspensi ekstrak metanol 75 mg/kg BB 96,17 d
5 Suspensi Glibenklamid 65 c
Dari Tabel 16 menunjukkan bahwa suspensi ekstrak metanol dosis 25 dan 75
mg/kg BB berbeda nyata dengan suspensi glibenklamid dan kontrol (CMC 1%),
kontrol (CMC 1%) tetapi tidak berbeda nyata dengan glibenklamid. Hal ini
menunjukkan bahwa ekstrak metanol 50 mg/kg BB mempunyai efek hipoglisemik yang
relatif sama dengan glibenklamid. Ekstrak metanol dosis 75 mg/kg BB menunjukkan
penurunan efek hipoglisemik bila dibandingkan dengan ekstrak metanol dosis 50 mg/kg
BB dan glibenklamid dimana pada selang waktu 60 menit setalah pemberian perlakuan
dosis 75 mg/kg BB mempunyai efek hipoglisemik lebih besar dari glibenklamid.
4.3.4 Pengaruh Pemberian Suspensi Ekstrak Metanol S. album, Glibenklamid dan
CMC 1% terhadap Kadar Gula Darah Mencit pada 120 menit setelah perlakuan
Pada selang waktu 120 menit setelah pemberian perlakuan, suspensi ekstrak
metanol dosis 25, 50 dan 75 mg/kg BB juga menunjukkan berbeda nyata dengan kontrol
(CMC 1%). Hal ini dapat dilihat dari nilai F Hitung > F Tabel (Tabel 17). Untuk
menngetahui perbedaan rata-rata antara perlakuan dilakukan uji beda rata-rata Duncan
(Tabel 18).
Tabel 17. Hasil perhitungan Anava kadar gula darah mencit setelah 120 menit perlakuan
Sumber Variasi DB JK KT F Hitung F Tabel
Perlakuan 4 28220,2000 7055,0500 248,2424 2,7587
Galat 25 710,5000 28,4200
Total 29 28930,7000
Tabel 18. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 120 menit perlakuan
No. Perlakuan Rata-rata Notasi
1 Suspensi CMC 1% 136,83 a
2 Suspensi ekstrak metanol 25 mg/kg BB 121 b
3 Suspensi ekstrak metanol 50 mg/kg BB 65 c
4 Suspensi ekstrak metanol 75 mg/kg BB 73,83 d
5 Suspensi Glibenklamid 63,83 c
Pada selang waktu 120 menit setelah pemberian perlakuan tidak berbeda dengan
selang waktu 90 menit dimana suspensi ekstrak metanol S. album dosis 50 mg/kg BB
menunjukkan tidak berbeda nyata dengan glibenklamid, hal ini berarti bahwa ektrak
metanol dosis 50 mg/kg BB dan glibenklamid mempunyai efek hipoglisemik yang
berbeda nyata dengan glibenklamid dan kontrol (CMC 1%). Hal ini menunjukkan
bahwa ekstrak metanol dosis 25 dan 75 mg/kg BB tidak mempunyai efek hipoglisemik
yang relatif sama dengan glibenklamid pada selang waktu 120 menit.
4.3.5 Pengaruh Pemberian Suspensi Ekstrak Metanol S. album, Glibenklamid dan
CMC 1% terhadap Kadar Gula Darah Mencit pada 150 menit setelah perlakuan
Pemberian suspensi ekstrak metanol S. album, dan glibenklamid pada selang
waktu 150 menit menunjukkan berbeda nyata pada uji Anava (Tabel 19). Hal ini terlihat
bahwa F Hitung > F Tabel. Untuk mengetahui perbedaan rata-rata dari tiap perlakuan
dilakukan uji beda rata-rata Duncan (Tabel 20).
Tabel 19. Hasil perhitungan Anava kadar gula darah mencit setelah 150 menit perlakuan
Sumber Variasi DB JK KT F Hitung F Tabel
Perlakuan 4 20453 5113,2500 216,0516 2,7587
Galat 25 591,6667 23,6668
Total 29 21044,6667
Tabel 20. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 150 menit perlakuan
No. Perlakuan Rata-rata Notasi
1 Suspensi CMC 1% 123 a
2 Suspensi ekstrak metanol 25 mg/kg BB 115 b
3 Suspensi ekstrak metanol 50 mg/kg BB 63,83 c
4 Suspensi ekstrak metanol 75 mg/kg BB 71 c
5 Suspensi Glibenklamid 63,83 c
Dari Tabel 20 terlihat bahwa ekstrak metanol dosis 50 dan 75 mg/kg BB berbeda
nyata dengan kontrol (CMC 1%) tetapi tidak berbeda nyata dengan glibenklamid. Ini
berarti bahwa ekstrak metanol 50 dan 75 mg/kg BB mempunyai efek hipoglisemik yang
relatif sama dengan glibenklamid, sementara ekstrak metanol dosis 25 mg/kg BB
berbeda nyata dengan kontrol dan glibenklamid, berarti tidak mempunyai efek
hipoglisemik yang relatif sama dengn glibenklamid. Pada selang waktu 150 menit
ekstrak metanol dosis 75 mg/kg kembali menunjukkan efek hipoglisemik yang relatif
sama dengan glibenklamid dan ekstrak metanol dosis 50 mg/kg BB dimana pada selang
4.3.6 Pengaruh Pemberian Suspensi Ekstrak Metanol S. album, Glibenklamid dan
CMC 1% terhadap Kadar Gula Darah Mencit pada 180 menit setelah perlakuan
Pada selang waktu 180 menit setelah pemberian perlakuan suspensi ekstrak
metanol S. album dosis 25, 50, dan 75 mg/kg BB menunjukkan berbeda nyata dengan
kontrol (CMC 1%), hal ini terlihat dalam uji Anava (Tabel 21) bahwa F Hitung > F
Tabel. Untuk mengetahui perbedaan rata setiap perlakuan dilakukan uji beda
rata-rata Duncan (Tabel 22).
Tabel 21. Hasil perhitungan Anava kadar gula darah mencit setelah 180 menit perlakuan
Sumber Variasi DB JK KT F Hitung F Tabel
Perlakuan 4 15424,4667 3856,1167 189,3967 2,7587
Galat 25 509 20,3600
Total 29 15933,4667
Tabel 22. Hasil perhitungan uji beda Duncan kadar gula darah mencit setelah 180 menit perlakuan
No. Perlakuan Rata-rata Notasi
1 Suspensi CMC 1% 120 a
2 Suspensi ekstrak metanol 25 mg/kg BB 88,17 b
3 Suspensi ekstrak metanol 50 mg/kg BB 58,83 c
4 Suspensi ekstrak metanol 75 mg/kg BB 69 d
5 Suspensi Glibenklamid 61,67 c
Dari Tabel 22 menunjukkan bahwa suspensi ekstrak metanol dosis 25 dan 75
mg/kg BB berbeda nyata dengan kontrol (CMC1%) dan glibenklamid, berarti bahwa
dosis 25 dan 75 mg/kg BB tidak mempunyai efek hipoglisemik yang relatif sama
dengan glibenklamid. Ekstrak metanol dosis 50 mg/kg BB menunjukkan berbeda nyata
dengan kontrol (CMC1%) tetapi tidak berbeda nyata dengan glibenklamid. Hal ini
menunjukkan bahwa ekstrak metanol dosis 50 mg/kg BB mempunyai efek hipoglisemik
yang relatif sama dengan glibenklamid. Dari hasil uji Anava dan Duncan dapat
ditabulasikan dalam Tabel 23 aktivitas hipoglisemik dari ekstrak akar S. album dari 30
Tabel 23. Perbandingan aktivitas hipoglisemik berdasarkan uji Anava & Duncan
Menit setelah perlakuan Aktivitas hipoglisemik Keterangan 30 menit setelah perlakuan 50 mg/kg BB & Glibenklamid tn
60 menit setelah perlakuan 50 & 75 mg/kg BB tn
90 menit setelah perlakuan 50 mg/kg BB & Glibenklamid tn 120 menit setelah perlakuan 50 mg/kg BB & Glibenklamid tn 150 menit setelah perlakuan 50 mg/kg BB & Glibenklamid tn 180 menit setelah perlakuan 50 & 75 mg/kg BB & Glibenklamid tn tn = tidak beda nyata
Tabel 23 menunjukkan bahwa dosis 50 mg/kg BB mempunyai kekuatan
aktivitas hampir sama dengan glibenklamid (obat antidiabetes) daripada dosis 75 mg/kg
BB selama perlakuan dari 30 menit sampai 180 menit perlakuan. Semakin besar dosis
akan semakin mahal dan senyawa lain yang terdapat dalam ekstrak MeOH akar S.
album semakin besar kuantitasnya dimana senyawa ini mungkin mempunyai aktivitas
yang berlawanan atau bersifat toksik, namun begitu dosis 75 mg/kg BB tidak diperiksa
dalam penelitian ini.
4.4 Tahap Fraksinasi
Ekstrak metanol pekat sebanyak 40 g disuspensi dengan akuades dan dipartisi
dengan kloroform (CHCl3:H2O; 1:1) (Metode Banthorpe). Perlakuan ini bertujuan untuk
mengekstraksi senyawa steroid bebas (non-glikosida) dalam ekstrak metanol agar
terlarut dalam pelarut kloroform. Masing-masing ekstrak kemudian dipekatkan dan diuji
steroid . Hasil uji fitokimia ditunjukkan pada Tabel 24.
Tabel 24. Hasil uji fitokimia dan perolehan berat ekstrak dari fraksi kloroform dan air.
Fraksi Uji Steroid
(Pereaksi Liebermann-Burchard) Berat (g)
Rendemen (%) dari 40 g Kloroform
Air
Warna hijau -
4,2309 -
10,577 -
Tabel 24 menunjukkan bahwa fraksi kloroform dan air mengandung steroid.
Fraksi kloroform lebih mudah diuapkan daripada fraksi air karena titik didih kloroform
lebih rendah daripada air (100°C). Senyawa-senyawa bahan alam dapat mengalami degradasi karena pemanasan. Fraksi kloroform mengandung steroid non-glikosida (non
dalam fraksi kloroform dapat dilakukan dengan fase normal (fase diam silika gel untuk
senyawa-senyawa non polar) sedangkan pemisahan steroid dalam fraksi air dilakukan
dengan fase terbalik (fase diam C-18 atau shepadex untuk senyawa-senyawa polar).
Harga silika gel lebih murah daripada C-18 atau shepadex. Alasan inilah maka dipilih
fraksi kloroform untuk dilakukan pemisahan lebih lanjut,
4.5 Tahap Pemisahan dan Pemurnian
Sebanyak 2,0 g fraksi kloroform dilakukan proses pemisahan dengan
menggunakan kromatografi kolom dengan silika gel 60 (70 – 230 mesh; 66,67 g)
panjang 40 cm, diameter 2,5 cm menggunakan fase gerak n-heksana–etil asetat (82:18).
Fraksi-fraksi ditampung setiap 5 ml dan diperoleh sebanyak 170 fraksi. Tiap-tiap fraksi
dianalis