PEMANFAATAN HASIL PENGOLAHAN LIMBAH CAIR
PERIKANAN DENGAN LUMPUR AKTIF SEBAGAI PUPUK
NITROGEN PADA TANAMAN BAYAM
(Amaranthus
sp.)
Oleh: Irma C34103017
PROGRAM STUD1 TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
RINGKASAN
IRMA, C34103017. Pemanfaatan Hasil Pengolahan Limbah Cair Perikanan dengan
Lumpur Aktif sebagai Pupuk Nitrogen pada Tanaman Bayam (Amaranthus sp.).
Dibirnbing oleh BUSTAMI IBRAHIM dan ANNA C. ERUNGAN.
Industri perikanan di Indonesia telah mengalami perkembangan yang sangat pesat dan tersebar di berbagai daerah di Indonesia. Dalam pengoperasiannya, industri perikanan ini lnenggunakan air dalam jumlah besar yang menyebabkan besarnya limbah cair yang dihasilkan. Limbah perikanan, khususnya limbah cair, biasanya langsung dibuang ke lingkungan dan dapat menyebabkan pencemaran lingkungan. Di Indonesia, kebutuhan pupuk terutama pupuk organik semakin meningkat dari tahun ke tahun. Peningkatan ini tidak diikuti dengan ketersediaan pupuk di pasar dan harga pupuk yang ada di pasaran cukup mahal. Salah satu altematif untuk mengatasi masalah ini dengan memanfaatkan limbah cair perikanan. Limbah cair perikanan mengandung unsur hara
yang dibutuhkan tanaman dalam jumlal~ tinggi seperti N, P, dan K serta mineral-mineral
yang lain.
Penelitian ini bertujuan untuk memanfaatkan limbah cair perikanan sebagai pupuk organik cair dan mempelajari pengaruh nitrogen dari limbah cair perikanan yang diolah dengan lumpur aktif sebagai pupuk terhadap pertumbuhan tanaman bayam
(Amaranthus sp.). Pada penelitian ini dilakukan pengolahan limbah cair buatan dengan
lumpur aktif dan aplikasinya pada tanaman bayam (Amaranthus sp.). Dosis pemupukan
yang digunakan terdiri atas tujuh taraf yaitu Dl, D2, D3, D4 pemupukan dengan limbah cair yang diolah dengan lumpur aktif dengan volume masing-masing 300 ml, 550 ml, 800 rnl dan 1050 ml, D5 pemupukan dengan 207 ml limbah cair segar, KP pemupukan
dengan 0,45 gr urea, dan KN tanpa pemupukan nitrogen. Dosis ditentukan berdasarkan
kadar
N
yang terdapat dalam pupuk. Masing-masing perlakuan juga dipupuk denganO,4 gr SP-36 dan 0,15 gr KCI. Pemupukan dilakukan sebanyak 2 kali yaitu pada saat
penanaman di polybag sebanyak 112 dosis perlakuan dan pada saat tanaman b e m a - 2
MST (Minggu Setelah Tanam) atau
+
14 hari setelah tanan sebanyak 112 dosisperlakuan.
Pada penelitian pendahuluan didapatkan waktu retensi 48 jam yang merupakan waMu ketika didapatkan kadar nitrat tertinggi. Pada pengolahan limbah cair buatan dengan lunipur &if terjadi peningkatan pada parameter MLSS, MLVSS, nitrat, pH, dan
COD serta te rjadi penurunan pada parameter amonia, TKN, dan DO. Hal ini disebabkan
PEMANFAATAN HASIL PENGOLAHAN LIMBAH CAIR
PERIKANAN DENGAN LUMPUR AKTIF SEBAGAI PUPUK
NITROGEN PADA TANAMAN BAYAM
(Amaranthus
sp.)
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan llmu Kelautan
Institut Pertanian Bogor
Oleh: Irma C34103017
PROGRAM STUD1 TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIIOINAN DAN ILMU KELAUTAN
Judul PEMANFAATAN HASIL PENGOLAHAN LIMBAH CAIR PERIKANAN DENGAN LUMPUR AKTIF SEBAGAI PUPUK NITROGEN PADA TANAMAN BAYAM (Amnratzt/zus sp.).
Narna Irma
N ~ P C34103017
Menyetujui,
Pembirnbing I1
Ir. Anna C. Erunpan, MS. NIP. 131 601 219
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INPORMASI
Dengan ini saya menyatakan bahwa skripsi yang berjudul "Pemanfaatan
Hasil Pengoiahan Limbah Cair Perikanan dengan Lnmpur Aktif sebagai Pupuk Nitrogen pada Tanaman Bayam (Antarantltus sp.)" adalah hasil karya saya sendiri dan belurn diajukan dalam bentuk apapun kepada perguruan tinggi
manapun. Sumber informasi yang berasal atau kutipan dari karya yang
diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam
teks dan dicantumkan dalam Daftar Pustaka dibagian akhir skripsi.
Bogor, Januari 2008
Irma
KATA PENGANTAR
Alhamdulillah, puji dan syukur penulis panjatkan kehadirat Allah SWT,
atas berkat dan rahmat-Nya akhimya penulis dapat menyelesaikan penyusunan
skripsi dengan judul "Pemanfaatan Hasil Pengolahan Limbah Cair Perikanan
dengan Lumpur Aktif sebagai Pupuk Nitrogen pada Tanaman Bayam (Amnrantlzus sp.)", sebagai salah satu syarat untuk memperoleh gelar sarjana
pada Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Pada kesempatan kali ini penulis ingin mengucapkan terimakasih
kepada:
I. Bapak Dr.Ir Bustami Ibrahim, MSc. sebagai komisi pembimbing I dan
Ibu Ir. Anna C. Erungan, MS. sebagai komisi pembimbing 11, terimakasih atas
bimbingan, arahan dan kesabaran yang diberikan kepada penulis.
2. Bapak Dr.1r. Ruddy Suwandi, MS., Mphil. dan Ir. Winarti Zahiruddin, MSc.
sebagai dosen penguji, terimakasih atas bimbingan dan saran yang diberikan
kepada penulis.
3. Kedua orang tua ku terointa, Bapak Ismail dan Ibu Zuriah, terimakasih atas doa, dukungan baik material maupun spiritual dan kasih sayang yang
diberikan kepada penulis selama ini.
4. Kakak ku Inderawati dan Saidun, adik ku Ine Mardina, Kakek dan Nenek ku
serta semua keluarga ku yang ada di Airnyatoh, Bangka, terimakasih atas doa
dan dukungannya selama ini baik material maupun spiritual..
5. Ahmad Kurniawan, SE terimakasih atas saran, kesabaran, pengertian dan doa
yang diberikan selama penulis menyelesaikan skripsi.
6. Yulya Fitria, terimakasih atas kebersamaan, bantuan, semangat dan
persahabatan yang diberikan kepada penulis.
7. Penghuni kosan "Pochan" terutama Ima, Win, Tg dan Jeng K-3 terimakasih
atas bantuan dan kebersamaannya.
8. Ghea, Cha-cha, David, Merry, Nita, Dim, Setyo yang telah membantu penulis
dalam melaksanakan penelitian dan semua teman-teman THP'40 atas
9. Teman-teman THP 38, 39 dan 41, terimakasih atas kebersamaan yang
diberikan kepada penulis selama ini.
10. Semua dosen yang ada di THP dan FPIK, terimakasih atas semua ilmu yang
telah diberikan selama penulis menempuh pendidikan di FPIK, IPB.
11. Semua pihak yang ada di Unit Pembibitan IPB, terimakasih atas bantuannya
selama penulis melaksanakan penelitian.
Akhir kata, semoga skripsi ini bermanfaat bagi semua pihak yang
membutuhkannya.
Bogor, Januari 2008
Penulis mempunyai nama lengkap Irma dan dilahirkan di
Pulau Bangka, pada tanggal 24 Juli 1985. Penulis
merupakan ail& ketiga dari empat bersaudara dari
pasangan Bapak Ismail dan Ibu Zuriah, adik dari
lnderawati dan Saidun serta kakak dari Ine Mardina.
Penulis menempuh pendidikan Sekolah dasar di SD
N
246 (sekarang SD N 8) Aimyatoh dan dinyatakan lulus pada tahun 1997.
Selanjutnya penulis menempuh pendidikan di SMP N 4 Mentok (sekarang SMP
N
1 Simpang Teritip) dan lulus pada tahun 2000. Pada tahun yang sama penulis
diterima di SMU N 1 Mentok dan dinyatakan lulus pada tahun 2003. Kemudian
penulis diterima di lnstitut Pertanian Bogor pada tahun 2003 melalui jalur USMI
di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan.
Selama kuliah penulis pernah menjadi asisten praktikum Mata Kuliah
Teknologi Refrigerasi Hasil Perairan dan Teknologi Proses Thermal Hasil
Perairan pada tal~un ajaran 200612007, Selain itu penulis juga peinah aktif dalam
kepanitiaan SANITASI pada tahun ajaran 200412005 dan 200612007.
Dalam rangka menyelesaikan pendidikan dan sebagai salah satu syarat
untuk memperoleh gelar sarjana pada Fakultas Perikanan dan llmu Kelautan,
Institut Pertanian Bogor, penulis melakukan penelitian dan penyusunan skripsi
dengan judul "Pemanfaatan Hasil Pengolahan Limbah Cair Perikanan
DAFTAR IS1
...
DAFTAR TABEL
...
viiiDAFTAR GAMBAR
...
..ixDAFTAR LAMPIRAN
...
x
1
.
PENDAHLJLUAN 1.1 Latar Belakang...
I 1.2 Tujuan...
22
.
TINJAUAN PUSTAKA 2.1 Limbah Cair...
32.2 Karakteristik Limbah Cair Perikanan
...
42.3 Lumpur Aktif
...
52.4 Nitrogen
...
52.4.1 Nitrogen organik
...
62.4.2 Ammonia
...
62.4.3 Nitrit
...
72.4.4 Nitrat
...
7...
2.5 Proses Nitrifikasi Penmganm Limbah Secara Biologis 8 2.6 Pupuk dan Pemupukan...
112.7 Bayam (Amaranthus sp)
...
133
.
METODOLOGI 3.
1 Waktu dan Tempat...
163.2 Alat dan Bahan
...
163.3 Prosedur Penelitian
...
163.3.1 Penelitian pendahuluan
. .
...
173.3.2 Penelltian utama
...
173.3.3 Analisis
...
183.3.4 Aplikasi pupuk organik cair
. .
...
213.3.5 Rancangan penelltian
...
224
.
HASIL DAN PEMBAHASAN 4.1 Karakteristik Limbah cair Buatan...
244.2 Penentuan Waktu Retensi
...
254.3 Kondisi Nitrifikasi
...
264.3.1 MLSS dan MLVSS
...
26...
4.3.3 Dissolved Oxygen (DO) 28
...
4.3.4 COD (Chemical Oxygen Demand) 29
...
4.3.5 TKN 30
...
4.3.6 Kadar NH3.N (nitrogen amonia) 31
4.3.7 Kadar NO3-N (nitrogen nitrat)
...
32...
4.4 Pengaruh Nitrogen terhadap Tinggi Bayam 33
4.5 Pengaruh Nitrogen terhadap Jumlah bayam
...
375
.
KESIMPULAN DAN SARAN5.1 Kesimpulan
...
40 5.2 Saran...
40...
DAFTAR TABEL
No T e h Halaman
1
.
Karakteristik Limbah Cair Buatan...
24DAPTAR GAMBAR
No Teks Halaman
...
1
.
Komposisi limbah cair secara umum 3...
2
.
Siklus nitrogen dalam proses oksidasi biologis 83
.
Tanaman bayam (Amaranthus sp)...
13...
4.
Kadar nitrat pada penelitian pendahuluan 25...
5.
Nilai MLSS selama proses pengolahan limbah cair 27...
6.
Nilai MLVSS selama proses pengolahan limbah 27...
7.
Derajat keasamam (pH) selama proses pengolahan limbah cair 28 8.
Kadar oksigen terlarut (DO) selama proses pengolahan limbah cair...
299
.
Nilai COD selama proses pengolahan limbah cair...
3010
.
Nilai TKN selama proses pengolahan limball cair...
3111
.
Kadar amonia selama proses pengolahan limbah cair...
3212. Kadar nitrat selama proses pengolahan limbah cair
...
3313
.
Pengaruh nitrogen terhadap pertambahan tinggi bayam...
36DAPTAR LAMPIRAN
No Halaman
1
.
Nilai MLSS dan MLVSS limbah cair buatan selama proses pengolahan...
442
.
Data hasil analisis karakteristik kimia dan fisika linibah cair selama proses pengolahan...
453
.
Perhitungan kebutuhan pupuk tanaman bayarn dan dosis yang digunakan...
pada perlakuan 47 4.
Pertumbuhan tinggi tanaman bayam selama pengamatan...
485
.
Rataan selisih pertambahan tinggi bayam selama pengamatan...
496
.
Rataan pertambahan jumlah daun bayam selama pengamatan...
507
.
Analisis ragam selisih tinggi tanaman bayam...
51...
8
.
Analisis ragam jumlah daun bayarn 55...
1.1 Latar Belakang
Industri perikanan di Indonesia telah mengalami perkembangan yang
sangat pesat dan tersebar di berbagai daerah di Indonesia seperti Jawa Timur,
Jawa Tengah, Jawa Barat, Jakarta serta beberapa daerah lainnya di luar Jawa.
Dalam pengoperasiannya, industri perikanan ini menggunakan air dalam jumlah
besar. Hal ini menyebabkan besamya limbah cair yang dihasilkan. Limbah
perikanan, khususnya limbah cair, biasanya langsung dibuang ke lingkungan dan
dapat menyebabkan pencemaran atau gangguan lingkungan seperti merangsang
pertumbuhan tanaman air, memunculkan toksisitas terhadap kehidupan air,
menurunkan kadar oxygen demand pada lingkungan perairan, bahaya terhadap
kesehatan masyarakat, serta menimbulkan bau yang mengganggu estetika lingkungan (Jennie dan Rahayu 1993).
Beberapa industri perikanan telah menerapkan pengolahan terhadap
limbah cair yang dihasilkan dari operasional industrinya. Salah satu teknologi
yang sering digunakan dalam pengolahan limbah cair adalah menggunakan
reaktor aerobik (nitrifikasi) dan reaktor anaerobik (denirrifikasi) secara biologis
dengan lumpur aktif. Proses pengolahan iimbah ini dilakukan untuk
mengeliminasi nitrogen dalam limbah yang berupa alnoniak sebelum limbah
tersebut dibuang ke lingkungan. Eckenfelder (2000) melaporkan, dalam
lingkungan perairan untuk mengoksidasi setiap milligram NH3-N menjadi nitrat
diperlukan 4,33 miligram oksigen sehingga akan menyebabkan turunnya oksigen
terlarut. Hasil dari proses pengolahan limbah biasanya langsung dibuang ke
lingkungan.
Di Indonesia, kebutuhan pupuk semakin meningkat dari tahun ke tahun.
Peningkatan ini tidak diikuti dengan ketersediaan pupuk di pasaran. Selain ih~
harga pupuk yang ada di pasaran cukup mahai karena bahan baku yang digunakan
dalam pembuatan pupuk harus diimpor. Besarnya dana yang harus dikeluarkan
pemerintah untuk memenuhi kebutuhan pupuk menimbulkan masalah baru yaitu
keterbatasan dana. Salah satu altematif untuk mengatasi masalah ini adalah
mengandung unsur hara N, P, dan K serta mineral-mineral yang lain dalam jumlah
yang cukup tinggi (Anas 2001 diacu dalam Siregar 2003). Unsur-unsur ini sangat
diperlukan dalam pertumbuhan tanaman.
Jenis pupuk yang banyak terdapat di pasaran dan sering digunakan oleh
para petani adalah pupuk anorganik. Penggunaan pupuk anorganik ini
mempunyai beberapa kelemahan, antara lain hampir tidak mengandung unsur hara
mikro. Selain itu pemakaian pupuk anorganik secara terus menerus dapat
merusak tanah bila tidak diimbangi dengan pupuk organik seperti pupuk kandang
dan pupuk kompos (Lingga 1998). Dalam ha1 ini penggunaan pupuk organik
sangat penting karena dapat memperbaiki kesuburan tanah. Kendala yang
dihadapi dalam penggunaan pupuk organik ini adalah penyerapannya yang relatif
lambat. Untuk itu perlu dicari pupuk organik yang mempunyai daya serap tinggi.
Salah satu alternatif yang dapat digunakan adalah lnemanfaatkan cairan hasil
pengolahan limbah cair perikanan yang diduga mengandung unsur hara yang
dapat diserap tanaman dalam waktu cepat terutama unsur nitrogen yang
dibutuhkan dalam jumlah tinggi pada sebagian besar tanaman.
1.2 Tujuan
Penelitian ini bertujuan untuk :
1) Memanfaatkan limbah cair perikanan sebagai pupuk organik cair.
2) Mempelajari pengaruh nitrogen dari limbah cair perikanan yang diolah
dengan lumpur aktif sebagai pupuk terhadap pertumbuhan tanaman bayam
2. TINJAUAN PUSTAKA
2.1 Limbah Cair
Limbah cair merupakan buangan cair yang berasal dari suatu lingkungan
masyarakat dan lingkungan industri dimana komponen utamanya adalah air dan
mengalldung benda padat yang terdiri dari zat organik dan zat anorganik. Bahan
organik yang terkandung dalam limbah cair dapat menghabiskan oksigen yang
terlarut dalam limbah serta menimbulkan bau yang tidak sedap dan akan
berbahaya apabila bahan tersebut merupakan bahan yang beracun (Sugiharto
1987). Kandungan bahan organik yang sangat tinggi dalam badan air akan
menyebabkan terjadinya proses oksidasi bahan organik oleh mikroorganisme.
Proses ini akan menyebabkan turunnya kandungan oksigen terlarut dalam air
sehingga ketersediaan oksigen bagi organisme di lingkungan tersebut berkurang,
bahkan dapat menyebabkan kematian bagi organisme tersebut (Tchobanoglous
dan Burton 1991).
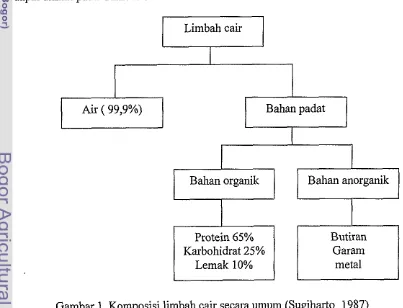
Secara m u m zat-zat yang terdapat dalam limbah cair (Sugiharto 1987),
[image:16.562.75.478.409.717.2]dapat dilihat pada Gambar 1.
Gambar 1. Komposisi limbah cair secara u n ~ m (Sugiharto 1987)
Limbah cair
Air ( 99,9%) Bahan padat
I
Bahan organik Bahan anorganik
Protein 65%
Karbohidrat 25% Lemak 10%
Butiran Garam
Limbah cair mengandung cukup banyak hara (NPK) dan bahan organik. Limbah cair dapat digunakan langsung sebagai pupuk, baik sebagai pupuk dasar
maupun pupuk susulan. Hasil penelitian di China menggunakan bermacam-
macam bahan organik dan kapasitasnya dalam meningkatkan hasil, temyata
limbah cair menduduki tempat teratas dibanding bahan organik lainnya.
Peningkatan hasil dapat mencapai 11% dibanding dengan bahan organik lain.
Kesimpulan yang dapat ditarik bahwa gas metan atau biogas setelah diekstrak dari
bahan organik, maka nitrogen dan hara lainnya tetap berada dalam limbah.
Penggunaan limbah cair untuk tanaman sayuran temyata memperoleh hasil yang
relatif sama dengan penggunaan pupuk kimia (Sutanto 2002).
2.2 Karakteristik Limbah Cair Perikanan
Setiap operasi pengolahan ikan akan menghasilkan cairan yang berasal
dari proses pemotongan, pencucian, dan pengolahan produk. Cairan ini
mengandung darah dan potongan-potongan ikan kecil dan kulit, isi perut,
kondensat dari operasi pemasakan, dan air pendingin dari kondenser (Jenie dan
Rahayu 1993). Liinbzh cair industri perikanan mengandung banyak protein dan
lemak, sehingga mengakibatksn nilai nitrat dan amonia yang cukup tinggi.
Perbedaan itu dipengartihi oleh tingkat produksi, jenis bahan mentah, kesegaran,
dan jenis produk akhir yang dihasilkan. Limbah cair yang dihasikan ole11 industri
pengolahan ikan mempunyai pH mendekati 7 atau alkali, yang disebabkan oleh
adanya dekomposisi bahan-bahan yang mengandung protein dan banyaknya
senyawa-senyawa arnonia. Kandungan limbah cair industri perikanan tergantung
pada derajat kontaminasi dan juga mutu air yang digunakan unttlk proses
(Gonzales 1996 diacu dalam Heriyanto 2006).
Bau yang timbul dari limbah cair perikanan disebabkan oleh dekomposisi
bahan-bahan organik yang menghasilkan senyawa amina mudah menguap,
diamina dan amoniak. Limbah cair industri perikanan memiliki kandungan
nutrien, minyak, dan lemak yang tinggi sehingga menyebabkan tingginya nilai
COD, terutama berasal dari proses penyiangan usus dan isi perut serta proses
2.3 Lumpur Aktif
Lumpur aktif mempakan flokulasi massa mikroba yang terutama terdiri
atas bakteri dan protozoa. Dalam proses lumpur aktif bakteri mempakan
mikroorganisme penting dalam penguraian material organik pada influent
(Liu dan Liptak 2000). Proses lumpur aktif adalah proses biologik yang dapat
digunakan untuk menangani berbagai jenis limbah. Proses lumpur aktif ini
bersifat serba guna, fleksibel dan limbah dengan mutu tertentu yang diinginkan
dapat dihasilkan dengan mengubah parameter proses (Jenie dan Rahayu 1993).
Lumpur aktif mengandung berbagai jenis mikroorganisme heterotrofk
termasuk bakteri, protozoa dan bentuk kehidupan yang lebih tinggi. Jenis
mikroorganisme utama yang mendominasi tergantung pada limbah yang ditangani
dan cara proses yang dioperasikan (Jenie dan Rahayu 1993). Secara m u m ,
bakteri yang terdapat dalam lumpur aktif termasuk ke dalam genus Pseudomonas,
Zooglea, Achromobacter, Flmobacterium, Nocardia, Mycobacterium, Nitrosomonas, dun Nitrobacter (Liu dan Liptak 2000).
2.4 Nitrogen
Nitrogen mempakan nutrient penting dalam sistern biologik. Nitrogen
mengisi sekitar 12% protoplasma bakteri dan 5-6% protoplasma kapang. Dalam
air limbah, nitrogen terdapat dalam bentuk nitrogen organik d m nitrogen amonia,
dimana proporsinya tergantung degradasi bahan organik yang berlangsung.
Dalam sistetn biologik, senyawa nitrogen ditransformasi menjadi nitrogen
ammonium dan dioksidasi menjadi nitrit dan nitrat (Jenie dan Rahayu 1993).
Unsur nitrogen disebut nutrient atan biostimulan karena memiliki peranan yang
penting untuk pertumbuhan protista dan turnbuhan (Davis dan Cornwell 1991).
Nitrogen merupakan unsur utama bagi pertumbuhan tanaman, yang pada
umumnya sangat diperlukan untuk pembentukan atau pertumbuhan bagian-bagian
vegetatif tanaman seperti dam, batang, d m akar. Akan tetapi kalau terlalu banyak
dapat mengha~nbat pembuangan dan pembuahan pada tanamannya. Nitrogen atau
zat lenlas diserap oleh akar tanaman dalam bentuk NO< (nitrat) dan NH~'
(amonium). Apabila nitrogen tersedia lebih banyak daripada unsur lainnya, maka
semakin cepat pula sintesis karbohidrat yang diubah menjadi protein dan
protoplasma (Sutedjo 1994).
Penyerapan NO< dan
N&+
memungkinkan tumbuhan untuk membentukberbagai senyawa nitrogen terutama protein. Pupuk dan tumbuhan mati,
mikroorganisme, serta hewan merupakan sumber penting nitrogen yang
dikembalikan ke tanah, tapi sebagian besar nitrogen tersebut tidak larut dan tidak
segera tersedia bagi tumbuhan (Salisbury dan Ross 1995). Secara umum fimgsi
nitrogen bagi tanaman adalah (Sutedjo 1994) :
1) Untuk meningkatkan pertumbuhan tanaman.
2) Dapat menyehatkan pertumbuhan daun, daun tanaman lebar dengan warna
yang lebih hijau.
3) Meningkatkan kadar protein dalam tubuh tanaman.
4) Meningkatkan kualitas tanaman penghasil daun-daunan.
5) Meningkatkan berkembangnya mikroorganisme dalarn tanah. Sebagaimana
diketahui ha1 itu sangat penting bagi kelangsungan pelapukan bahan organis.
2.4.1 Nitrogen organik
Semua nitrogen yang ada dalam komponen organik bisa dikatakan sebagai
nitrogen organik. Asam amino, amina, amida, imido dan turunan nitro merupakan
golongan yang termasuk ke dalam nitrogen organik. Beberapa nitrogen organik
dihidrolisis menjadi asam amino yang terlarut dan memungkinkan pemecahan
lebih lanjut untuk melepas ion ammonium (N&+) (Sawyer et. al. 1994).
Menurut Metcalf dan Eddy (1991), nitrogen organik berhubungan dengan
suspended solids dalam air limbah dengan sedimentasi dan filtrasi. Nitrogen
organik dalam bentuk padat dapat langsung masuk ke tanah yang memiliki
molekul organik kompleks yaitu karbohidrat, protein dan lignin.
2.4.2 Ammonia
Amonia terdapat dalaln 2 bentuk yaitu anlonia bebas atau tidak terionisasi
(NH,) da11 dalam bentuk ion amonia (N&+). Perbandingan kedua bentuk amonia ini sangat ditentukan ole11 nilai pH dan suhu. Konsentrasi amonia yang tinggi
pada pem~ukaan air akan lnenyebabkan kematian ikan y a ~ g terdapat pada perairan
Amonia dapat menyebabkan keadaan kekurangan oksigen pada air karena
pada konversi amonia menjadi nitrat membutuhkan 4,5 bagian oksigen untuk
setiap bagian amonia. Oleh karena itu, bila terjadi perubahan amonia menjadi
nitrat maka kadar oksigen terlarut dalam cairan akan turun dan menyebabkan
organisme yang ada di dalamnya seperti ikan tidak dapat hidup di sana (Jenie dan
Rahayu 1993).
2.4.3 Nitrit
Konsentrasi nitrit yang tinggi dapat mereduksi aktivitas bakteri nitrifikasi
pada kondisi asam. Daya racun nitrit yang tinggi dipengaruhi oleh bentuk persenyawaan nitritnya, yaitu bila terdapat dalam bentuk asam (HN02) maka akan
lebih toksik daripada dalam bentuk ion nitrit. Dalam larutan, nitrit akan
terdisosiasi sehingga tercapai bentuk keseimbangan, yang ditunjukkan oleh
persamaan di bawah ini :
___+
NO?
+
H~O' HN02 + H20Keseimbangan tersebut sangat dipengaruhi oleh keasaman larutan yaitu
pada kondisi asam, maka konsentrasi asam nitrit akan meningkat bila
dibandingkan dengan keadaan netral (Jenie dan Rahayu 1993). Menurut Alaerts
dan Santika (1987) yang diacu dalam Heriyanto (2006), nitrit biasanya tidak
bertahan lama dan merupakan keadaan sementara oksidasi antara amonia dan
nitrat. Nitrit membahayakan kesehatan karena dapat bereaksi dengan hemoglobin
dalam darah, sehingga darah tidak dapat mengangkut oksigen.
2.4.4 Nitrat
Nitrat merupakan bentuk senyawa yang stabil dan salah satu unsur penting
dalam sintesis protein pada tumbuhan dan hewan. Akan tetapi nitrat pada
konsentrasi yang tinggi akan menstimulasi pertumbuhan ganggang berlebih,
sehingga oksigen terlarut dalam air menurun dan menyebabkan kematian ikan
(Alaerts dan Santika 1987 diacu dalam Heiiyanto 2006).
Konsentrasi nitrat yang tinggi akan menyebabkan methemoglobinema
pada bayi dan akan mempengaruhi kesehatan hewan. Pengaruh negatif tersebut
2.5 Proses Nitrifikasi Penanganan Limbah secara Biologis
Proses penanganan limbah secara aerobik bertujuan untuk mencegah
timbulnya bau selama penanganan limbah, agar memenuhi persyaratan effluent
dan untuk stabilisasi limbah sebelum dialirkan ke lahan. Dalam pencemaan
aerobik, respirasi endogenous merupakan reaksi metabolik yang utama.
Perubahan kecil terjadi pada bahan selulosik selama pencemaan aerobik. Bahan
yang mengandung nitrogen adalah bahan yang paling mudah didegradasi.
Parameter yang berhubungan dengan nitrifikasi dapat digunakan untuk mencatat
kemajuan pencernaan aerobik karena suplai oksigen melebihi kebutuhan dan
digunakan untuk pengadukan (Jenie dan Rahayu 1993). Siklus nitrogen dalam
proses oksidasi biologis dapat dilihat pada Gambar 2.
Nitrogen organik
I
+
Autoksidasi
NH3
+
C02+
H20No3 J
[image:21.559.80.475.252.679.2]+
CH20 ( Denitrifikasi) N2+
N20Gambar
2.
Siklus nitrogen dalam proses oksidasi biologisBerdasarkan kebutuhan proses terhadap oksigen terlamt, proses penyisihan
limbah secara biologis dibagi menjadi tiga (Jenie dan Rahayu 1993), yaitu :
1) Oksidasi bahan-bahan organik dengan menggunakan oksigen sebagai
akseptor elektron. Proses ini mempakan mekanisme untuk menghasilkan
energi kimiawi bagi mikroorganisme yang berperan dalam proses
pengolahan secara aerob.
2) Oksidasi bahan-bahan organik yang menggunakan bahan lain selain oksigen
seperti karbondioksida. Senyawa-senyawa organik yang teroksidasi sebagai
sulfat dan nitrat dapat digunakan mikroorganisme yang berperan dalam
proses pengolahan secara anaerob.
3) proses pengolahan limbah menggunakan mikroorganisme yang bersifat
obligat aerob dan obligat anaerob atau obligat fakultatif. Mikroorganisme
ini dapat melakukan metabolisme terhadap bahan-bahan organik secara
sempurna dengan adanya oksigen terlarut.
Nitrifikasi mempakan proses konversi biologis senyawa amonia menjadi
nitrit dan selanjutnya diubah menjadi nitrat. Da:m proses nitrifikasi bakteri
autotrof aerobik yaitu Nitrosonzonas dan Nitrobacter, akan mengubah amonia
menjadi nitrit dan akhirnya menjadi nitrat. Penghilangan amonia dari limbah cair
sangat penting karena amonia bersifat racun bagi biota akuatik. Proses reaksi ini
akan membutuhkan oksigen dalam jumlah banyak (Sa'id 1994). Menurut
Sutedjo (1994), nitrifikasi tejadi melalui 2 proses yaitu nitrifasi dan nitrafasi.
Nitrifasi merupakan proses perubahan amonia menjadi nitrit yang melibatkan
bakteri Nitrosomonas dan Nitrosococcus. Sedangkan nitrafasi mempakan proses
pembahan nitrit menjadi nitrat yang melibatkan bakteri Nitrobacter. Reaksi
nitrifikasi terdiri atas dua tahap, yaitu:
NH.,'
+
O2 t-~ NOT+
H'+
Hz0+
E (Nitrifasi)NOY
+
O2-
NO?+
E (Nitrafasi)Secara umum, kecepatan reaksi biokimia Nitrobacter lebih cepat daripada
kecepatan reaksi Nitrosomonas akan mengendalikan reaksi keseluruhan
(Eckenfelder 2000). Bakteri autotropic ini tidak menggunakan seluruh amonia
untuk energi. Biomassa aktif akan menggunakan ammonium sebagai surnber
nitrogen selama sintesis sel (Liu dan Liptak 2000). Ada 3 parameter penting
dalam proses nitrifikasi. Pertama, 4,34 mg 0 2 diperlukan untuk mengoksidasi 1 mg NH4+- N. Kedua, 7,07 alkalinitas (sebagai mgll CaC03) dikonsumsi per mg
N H ~ + - N yang dinitrifikasi. Ketiga, 0,13 mg biomassa aktif dihasilkan per mg
NH~+- N yang diubah.
Menurut Jenie dan Rahayu (1993), proses nitrifikasi dipengaruhi oleh
beberapa faktor, yaitu:
1) Amonialnitrit
Amonia mempakan surnber energi bakteri nitrifikasi. Akan tetapi, dalam
jumlah yang berlebihan akan menghambat pertumbuhan bakteri tersebut.
2) Suhu
Suhu optimal proses nitrifikasi adalah 30-36'C. Apabila nitrifikasi
dilakukan pada suhu yang lebih rendah atau lebih tinggi dari suhu
optimalnya maka akan menghambat proses penguraian oleh bakteri.
3) Derajat keasaman
Proses nitrifikasi akan optimal pada pH 7,545. Akan tetapi, bakteri
nitrifikasi mampu beradaptasi pada kondisi pH yang lebih rendah.
4) Waktu retensi
Proses nitrifikasi tergantung dari metabolisme mikroba aerobik dan
mikroba untuk proses nitrifikasi mempunyai waktu generasi yang panjang
yaitu dapat mencapai 10 janl atau lebih tergantung dari lingkungari
mikroba itu berada. Waktu retensi minimum dari nitrifikasi hams lebih
lama daripada laju pertumbuhan mikroba dan juga tergantung dari suhu
proses dan konsentrasi bahan-bahan penghambat. Waktu retensi minimum
sangat penting artinya bagi suatu penanganan biologis karena adanya
kemungkinan laju pertumbuhan mikroba yang lebih lambat daripada laju
2.6 Pupuk dan Pemupukan
Pupuk merupakan suatu bahan yang bermanfaat untuk menyediakan unsur
hara yang kurang atau bahkan tidak tersedia di tanah untuk mendukung
pertumbuhan tanaman. Selain itu pupuk juga bermanfaat secara fisika, yaitu
memperbaiki struktur tanah dari padat menjadi gembur. Berdasarkan komponen
utama penyusun pupuk, pupuk dibagi menjadi pupuk organik dan pupuk
anorganik. Sedangkan dari segi cara pernberiannya, pupuk digolongkan menjadi
pupuk a k a dan pupuk daun (Marsono dan Sigit 2001).
Selain menyediakan unsur hara, pemupukan juga membantu mencegah
kehilangan unsur hara yang cepat hilang seperti N, P dan K yang mudah hilang
oleh penguapan atau oleh air perkolasi. Manfaat lain dari pupuk adalah
memperbaiki keasaman tanah. Tanah yang asam dapat ditingkatkan pH-nya
menjadi pH optimum dengan pemberian kapur dan pupuk organik. Sebaliknya,
tanah yang bersifat basa dapat ditwunkan pH-nya dengan pupuk sulfat dan pupuk
organik (Marsono dan Sigit 2001). Menurut Prihmantoro (1999), pemupukan
yang baik dilakukan pada pagi hari sebelum pukul 09.00 dan pada sore hari
sesudah pukul 15.00.
Tanah dikatakan subur apabila kandungan hara yang dibutuhkan tanaman
lengkap dan tersedia dalam tanah tersebut. Unsur hara yang dibutuhkan oleh
tanaman terdiri atas unsur hara makro dan unsur hara rnikro. Unsur hara makro
dibutuhkan tanaman dalam jumlah yang besar, sedangkan unsur hara mikro
dibutuhkan dalam jumlah yang sangat kecil namun mempunyai peranan yang
sangat penting dalam pertumbuhan tanaman. Unsur-unsur hara makro antara lain:
C, H, 0, N, P, K, Mg, Ca, dan S. Unsur-unsur hara mikro antara lain: B, Fe, Mn,
Cu, Zn, Mo, dan C1 (Salissbury dan Ross 1995).
Berdasarkan bahan baku pembentuknya pupuk dibagi menjadi pupuk
anorganik dan pupuk organik. Bahan baku pupuk anorganik adalah bahan mineral
atau senyawa kimia sedangkan pupuk organik adalah sisa mahkluk hidup seperti
darah, tulang, kotoran, bulu, sisa tumbuhan atau limbah rumah tangga yang telah
mengalami proses pembusukan oleh mikroorganisme pengurai sehiigga warn$
rupa, tekstur, dan kadar aimya tidak serupa dengan bahan aslinya. Nitrogen dan
Penggunaan secara berkesinambungan akan banyak membantu dalam membangun
kesuburan tanah, terutama apabila dilaksanakan dalam waktu yang panjang
(Sutanto 2002). Penggunaan pupuk organik dalam pertanian memberikan
beberapa keuntungan (Marsono dan Sigit 2001), yaitu :
1) Memperbaiki struktur tanah dengan menyediakan ruang pada tanah untuk
udara dan air, yang selanjutnya akan mendukung pertumbuhan bakteri
aerob yang berada di akar. Sementara air yang tersimpan di dalam
ruangan tanah menjadi persediaan bagi tanaman.
2) Menyediakan unsur hara yang diperlukan bagi tanaman, mencegah
kehilangan unsur hara yang cepat hilang.
3) Membantu penyerapan unsur hara.
4) Memperbaiki keasarnan tanah.
5) Menambah mikroorganisme tanah dan mengusahakan kondisi yang
optimum bagi biologis tanah.
Pupuk organik umumnya inerupakan pupuk lengkap artinya mengandung
unsur hara n&o dan unsur hara mikro, meskipun dalam jumlah yang sedikit.
Pupuk organik yang telah umum di masyarakat adalah pupuk kandang, kompos,
humus, pupuk hijau, dan pupuk burung/guano (Prihmantoro 1999). Aplikasi
pupuk organik cair biasanya dilakukan dengan disemprotkan ke daun disebut
pupuk dam dan disirarnkan langsung ke perakaran tanaman disebut pupuk akar.
Pemberian pupuk lewat akar sebenamya relatif aman bila dibandingkan dengan
pemberian lewat mulut d a m (stomata), tetapi efisiensinya rendah. Pada
pemberian pupuk lewat akar sebagian unsur hara di dalamnya akan hilang tercuci
oleh air penyiraman atau air hujan sehingga sebagian unsur hara yang dibutuhkan
tanaman menjadi berkurang (Marsono dan Sigit 2001).
Pupuk dam merupakan bahan-bahan atau unsur-unsur yang diberikan
melalui daun dengan cara penyemprotan atau penyiraman kepada mahkota
tanaman agar langsung dapat diserap untuk mencukupi kebutuhan bagi
pertumbuhan dan perkembangannya (Sutedjo 1994). Pemberian pupuk daun
lebih efisien diserap tanaman. Akan tetapi, pemberiannya hams dilakukan dalam
jumlah yang tepat karena pupuk daun yang diberikan secara berlebihan dapat
organik cair dengan cara disemprotkan ke daun sebaiknya tidak dilakukan pada
kondisi terik matahari atau kelembaban rendah karena larutan pupuk akan cepat
menguap. Pemupukan juga tidak disarankan pada saat hujan karena larutan
pupuk dari daun akan hilang (Marsono dan Sigit 2001).
2.7 Bayam (Anmmnt~zzrs sp.)
Bayam merupakan sayuran yang sangat digemari oleh masyarakat
Indonesia. Bayam merupakan sayuran yang mempunyai rasa yang enak, lunak
dan dapat memberikan rasa dingin dalam perut. Bayam juga banyak mengandung
vitamin A, vitamin B, vitamin C serta garam-garam mineral yang penting sepel-ti
kalsiurn, fosfor, dan besi (Kristyono 1983). Bayam berasal dari Benua Amerika
tropika dan sekarang tersebar ke daerah tropika dan sub tropika. Bayam dapat
tumbuh baik di dataran rendah hingga dataran pegunungan sarnpai ketinggian
1500 m dpl. Deskripsi tanaman bayam dapat dilihat pada Gambar 3. Klasifikasi
umum tanaman bayam menurut Benson (1957) adalah:
Divisi : Spermatophyta
Kelas : Angiospermae
Sub kelas : Dicotyledone
Ordo : Caryophylales
Famili : Amaranthaceae
Genus : Amaranthzrs
[image:26.550.74.447.249.751.2]Spesies : Amaranthus tricolor
Bayam merupakan tanaman ekononlis yang mempunyai keuntungan
komparatif, antara lain tidak terlalu banyak mengalami gangguan hama penyakit
maupun kondisi lingkungan yang sub optimal karena tanaman bayam cukup
responsif menerima masukan yang relatif seadanya. Tanaman bayam, khususnya
bayam cabut dapat dibudidayakan setiap saat (Hadisoeganda 1996). Secara
m u m , tanaman bayam dapat meningkatkan kerja ginjal dan melancarkan pencemaan. Akar bayam merah berkhasiat sebagai obat disentri. Bayam
termasuk sayuran berserat yang dapat digunakan untuk memperlancar proses
buang air besar dan sangat dianjurkan untuk dikonsumsi oleh penderita kanker
usus besar, penderita kencing manis (diabetes mellitus), kolesterol darah tinggi,
dan menurunkan berat badan. Jenis bayam budidaya dibedakan 2 macam (Anonim
2007), yaitu:
1) Bayam cabut atau bayam sekul alias bayam putih (A. tricolor L.). Ciri-ciri bayam cabut adalah memiliki batang benvama kemerah-merahan atau
hijau keputih-putihan, dan memiliki bunga yang keluar dari ketiak cabang.
Bayam cabut yang batangnya merah disebut bayam merah, sedangkan
yang batangnya putih disebut bayam putih.
2) Bayam tahun, bayam skop atau bayam kakap (A. hybridus L.). Ciri-ciri
bayam ini adalah memilii daun lebar-lebar, yang dibedakan atas 2 spesies
yaitu:
a. A. hybridus caudatus L., memiliki d a m agak panjang dengan ujung runcing, benvama hijau kemerah-merahan atau merah tua,
dan bunganya tersusun dalam rangkaian panjang terkumpul pada
ujung batang.
b.
A.
hibridus paniculatus L., mempunyai dasar daun yang lebarsekali, benvarna hijau, rangkaian bunga panjang tersusun secara
teratur dan besar-besar pada ketiak dam.
Pada tanaman bayam, pupuk yang diberikan adalah pupuk N yang dapat
diperoleh dari pupuk urea sebanyak 300 kgha atau ZA sebanyak 500 kgha
dengan cara dilarutkan dalam air
+
25 grad10 liter air, TSP 200 kgiha dan KC1100 kgiha. Pupuk N diberikan dua kali yaitu seteilgah takaran pada waktu tanam
pupuk K diberikan satu kali yaitu pada waktu tanam. Panen pertama bayam
terjadi pada waktu dilakukan penjarangan tanaman. Panen sesunggulmya dimulai
sewaktu ukuran tinggi tanaman telah mencapai 20 cm. Umur tananIan pada waktu
itu bervariasi antara 21 sampai 28 hari, tergantung jenis, kesuburan dan
3. METODE PENELITIAN
3.1 Waktu dan Tempat
Penelitian dilaksanakan pada bulan April - Agustus 2007. Pengolahan
limbah cair buatan dan analisis MLSS serta MLVSS dilakukan di Laboratorium
Limbah dan Hasil Samping serta Laboratorium Biokimia Hasil Perairan,
Departemen Teknologi Hasil Perairan.
Analisis DO, pH, COD, NH3-N, N03-N, dan TKN dilaksanakan di
Laboratorium Lingkungan, Departemen Budi Daya Perairan dan Laboratorium
Proling, Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan
Ilmu Kelautan, Institut Pertanian Bogor. Sedangkan aplikasi limbah cair pada
tanaman bayam (Amaranthus sp.) dilakukan di Unit Pernbibitan, Institut Pertanian
Bogor.
3.2 Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah aerator serta alat-alat
yang digunakan dalam pengujian MLSS, MLVSS, DO, pH, COD, NH3-N,
NO3-N, dan TKN. Pada aplikasi lirnbah cair pada tanaman bayam digunakan juga
alat-alat pertanian seperti cangkul dan parang.
Sedangkan bahan-bahan yang digunakan dalam penelitian ini adalah
lumpur aktif, benih tanaman bayam, tanah, polybag, urea, SP-36, KC1 dan bahan-
bahan yang digunakan dalam pengujian MLSS, MLVSS, DO, pH, COD, NI-13-N,
NO3-N, dan TKN. Lumpur aktif yang digunakan dalam penelitian iai diperoleh
dari Unit Pengolahan Limbah yang terletak di Muara Baru, Jakarta.
3.3 Prosedur Penelitian
Penelitian dilakukan dalarn dua tahap yaitu penelitian pendahuluan dan
penelitian utama. Penelitian pendahuluan dilakukan untuk mendapatkan waktu
retensi yang akan digunakan dalam penelitian utama. Sedangkan penelitian utama
bertujuan untuk mengaplikasikan lirnbah cair perikanan yang diolah dengan
3.3.1 Penelitian pendahuluan
Tahap-tahap yang dilakukan dalam penelitian pendahuluan adalah :
1) Pembuatan limbah cair buatan
Proses pembuatan limbah cair buatan dilakukan dengan memanfaatkan limbah
potongan-potongan daging dan kulit ikan yang diperoleh dari proses
pemfilletan ikan. Potongan-potongan ikan ini dicincang dan selanjutnya
direbus dalam air mendidih selama 10 menit dengan perbandingan berat ikan
(kg) dan volume air (liter) adalali 1 : 5. Setelah itu dilakukan penyaringan untuk memisahkan padatan dan cairan yang akan digunakan setelah dingin.
Limbah buatan yang telah dibuat itu kemudian dianalisa karakteristiknya yang
meliputi analisa pH, COD, NH3, No3, DO, dan TKN.
2) Penentuan waktu retensi
Peilentuan waktu retensi dilakukan dengan melihat kadar nitrat yang paling
tinggi selama proses pengolahan lunbah cair dengan lumpur aktif. Selama
proses pengolahan limbah cair dengan lumpur aktif, setiap 12 jam dilakukan
pengambilan sampel dan dilXkukan pengukuran kadar nitratnya sampai
didapatkan kadar nitrat yang paling tinggi. Lamanya waktu kontak limbah
cair buatan dengan lumpur aktif pada saat didapatkan kadar nitrat tertinggi
merupakan waktu retensi yang akan digunakan dalam penelitian pendahuluan.
3.3.2 Penelitian utama
Pada penelitian utama dilakukan proses pengolahan limbah cair perikanan
secara biologis dengan lumpur aktif melalui proses nitrifikasi. Cairan hasil
pengolahan tersebut kemudian diaplikasikan sebagai pupuk nitrogen pada
tanaman Bayam (Amaranthus sp.).
Proses pengolahan limbah cair dengan lumpur aktif dilakukan pada
kondisi aerobik dengan menggunakan reaktor yang dilengkapi sistem aerasi.
Setiap 12 jam dilakukan analisis MLSS, MLVSS, DO, pH, COD, NH3-N, NO3-N,
dan TKN dari limbah cair tersebut. Sedangkan pada apiikasinya dilakukan
3.3.3 Analisis
Selma proses pengolahan limbah cair buatan dengan lumpur aktif
dilakukan analisis parameter fisika dan kimia dari limbah cair tersebut. Analisis-
analisis yang dilakukan adalah :
1) COD (Clremical Oxygen Dentand) (APHA 1992)
Chemical Oxygen Demand ( COD) merupakan banyaknya oksigen dalam ppm atau milligram per liter yang dibutuhkan dalam kondisi khusus untuk
menguraikan benda organik secara kimiawi ( Sugiharto 1987).
Prosedur penentuan parameter COD adalah 1 gr HgS04 dan batu didih
dimasukkan ke dalam botol refluks. Kemudian ditambah 5 ml H2SO4 d m
diaduk hingga HgS04 lamt. Botol refluks ditempatkan dalam ruang es d m
ditambahkan 25 ml K2Cr207 0,25 N dan reagen H2SOd.Ag2S04 sambil diaduk
perlahan. Kemudian diambil 50 rnl sampel d m diinasukkan ke dalain botol
refluks dengan tetap berada di ruang es. Selanjutnya direfluks selama 2 jam.
Sampel yang telah direfluks didinginkan dan ditambahan dengan 8-10 tetes
indikator ferroin dan dititrasi dengan menggunakan larutan ferrous ammonium
sulfat [Fe(NH4)2(S04)2]. Titrasi dilakukan sampai teijadi perubahan warna
dari hijau terang menjadi kemerahan tajam. Selain itu dilakukan juga titrasi
terl~adap hlanko. Penentuan COD dilakukan dengan menggunakan rumus :
(B-S)xNx800
COD =
v
Keterangan : B =Volume titrasi blanko (ml)
S = Volume titrasi sampel (ml)
N = Normalitas Fe(NH4)2(S04)2
V = Volume sampel yang digunakan (ml)
2) Nilai pH (APHA 1992)
Pengukuran pH dilakukan dengan menggunakan pH meter. PH meter yang
akan digunakan dikalibrasi terlebih dahulu dengan cara mencelupkan
elektroda ke dalam lamtan buffer yang telah diketahui pH-nya. Kemudian
aquades, skala pH meter diatur di angka 7. Selanjutnya elektroda dibilas
dengan aquades dan dilap dengan tissue. Setelah dikalibrasi pH meter dapat
digunakan untuk mengukur pH sampel, dengan cara mencelupkan elektroda
ke dalam sampel yang dimasukkan ke dalam erlenmeyer.
3) MLSS (Mixed Liquor Suspended Solids) (APHA 1992)
Mixed Liquor Suspended Solids (MLSS) merupakan jumlah Total Suspended
Solid (TSS) yang berasal dari bak pengendap Lumpur. Dimana TSS merupakan jumlah berat kering dalam mgll lumpur yang ada dalam air limbah
setelah mengalami penyaringan (Sugiharto 1987).
Kertas saring Whatman 42 dikeringkan dalam oven selama 1 jam pada suhu
100 - 105OC dan selanjutnya didinginkan dalam desikator dan ditimbang.
Kemudian diambil sampel sebanyak 50 ml dengan diaduk terlebih dahulu dan
disaring. Setelah itu kertas saring tersebut dikeringkan dalam oven pada suhu
100-105°C selama 2 jam. Kertas saring didinginkan dalam desikator dan
ditimbang. Konsentrasi MLSS dalam sampel dapat dihitung dengan
menggunakan rumus :
Keterangan : A = Berat akhir kertas saring (gr)
B = Berat awal kertas saring (gr)
V = Volume sampel (ml)
4) MLVSS (Mixed Liquor Volatile Stispended Solids) (APHA 1992)
Mixed Liquor Volatile Suspended Solids (MLVSS) merupakan MLSS yang
telah dipanaskan pada suhu 600°C sehingga benda volatilnya menguap
(Sugiharto 1987). Prosedur penentuan parameter MLVSS adalah cawan
porselin yang akan digunakan dikeringkan dalam tanur selama 10 menit pada
suhu 550°C dan selanjutnya didinginkan dalam desikator dan ditimbang.
Kertas saring dari uji MLSS diasukkan ke dalam cawan porselin dan
diletakkan dalam tanur selama 2 jam pada suhu 550°C. Kemudian cawan
proses pengeringan untuk mendapatkan berat yang konstan. Konsentrasi
MLVSS dapat dihitung dengan rumus :
Keterangan : C = Berat awal cawan (gr)
D = berat akhir cawan (gr)
V = Volume sampel (ml)
5) TKN (Total Kjeldahl Nitrogen) (APHA 1992)
Pengukuran TKN merupakan pengukuran jumlah N-organik dan N-amonia
bebas yang tedapat dalam 1 liter contoh. Prosedumya adalah sebanyak 10 ml
sa~npel dan 10 ml NaOH 45% dirnasukkan dalam peralatan destilasi. Sebagai
penampung gas yang terbeniuk digunakan larutan HC10,05 N sebanyak 25 ml
yang ditambahkan dengan 3 tetes indikator mengsel. Kemudian dilakukan
proses destilasi selama 10 menit atau sampai didapatkan volume penampung
50 ml. Setelah itu dilanjutkan dengan titrasi menggunakan NaOH 0,05 N
sampai tejadi perubahal wama menjadi hijau. Kadar TKN dapat dihitung
dengan -us :
Kadar nitrogen =
-
(A-B)x14.007x ~ ~ ~ ~ 0 ~ x 1 0 0 0C
Keterangan : A = Volume titrasi blanko (ml) B = Volume titrasi contoh (ml)
C = ml contoh
6) Kadar NH3.N (nitrogen ammonia) (APHA 1992)
Contoh yang akan diuji terlebih dahuiu dipisahkan zat padat tersuspensinya
dengan melakukan pemusingan selama 10 menit pada kecepatan 5000 rpm.
Selanjutnya sebanyak 50 ml contoh dipipet dan dimasukkan ke dalam labu
takar dan ditambahkan dengan reagen Nessler sebanyak 2 ml. Kemudian
campuran tersebut dikocok dengan cara membolak-balik dan didiamkan
selama 10 menit. Setelah itu dilakukan pengkuran dengan spektrofotometer
menggunakan kurva kalibrasi yang dibuat dengan menggunakan larutan
NH4Cl pada konsentrasi 0,2 - 0,5 mg NH3-Nlliter.
7) Kadar NO3-N (nitrogen nitrat) (APHA 1992)
Pada penentuan ini digunakan lamtan standar nitrat yang dibuat dengan
melarutkan 721,8 mg KN03 dalam 100 ml air suling dan diencerkan sarnpai
volume 1000 ml. Konsentrasi nitrat untuk pembuatan kurva kalibrasi adalah
0,O-2,O mg/l serta reagen brusin-asam sulfalinik yang dibuat dengan
melarutkan
1
gr brusinsulfat dengan 0,l gr asam sulfalinik dalam 70 ml airsuling. Selanjutnya ditambahkan 3 ml HCl pekat dan diencerkan sampai
volume 100 ml.
Prosedur analisisnya adalah 10 ml contoh yang telah dijernihkan dimasukkan
ke dalam erlenmeyer 50 ml dan ditambahkan 2 ml larutan NaCl 30% dan 10
ml &So4 pekat. Selanjutnya larutan diaduk dan dibiarkan hingga dingin.
Setelah itu ke dalam larutan tersebut ditambahkan 0,5 ml reagen brusin-asam
sulfalinik dan dipanaskan dengan penangas air pada suhu 95OC selama 20
menit dan didinginkan. Kemudian dilakukan pengukuran dengan
spektrofotometer pada panjang gelombang 410 nm. Konsentrasi NO3-N
ditentukan dengan menggunakan kurva kalibrasi.
8) DO (Dissolved Oxygen) (APHA 1992)
Pengukuran oksigen terlamt (DO) dilakukan dengan menggunakan alat DO-
meter. Untuk menjaga ketepatan hasil pengukuran, alat tersebut perlu
dikalibrasi setiap jangka waktu tertentu. Proses kalibrasi dapat dilakukan
dengan cara membandingkan hasil pengukuran alat dengan hasil pengukuran
dengan cara titrasi terhadap contoh yang sama. Misalnya suatu sampel yang
dianalisa dengan metode standar Winkler kadar oksigen terlarutnya sebesar a
dan sampel yang sama ditera dengan DO-meter kadar oksigen terlarutnya
sebesar b, maka faktor koreksinya adalah arb. Setiap hasil pengukuran dengan
DO-meter hams dikalikan dengan faktor koreksi tersebut.
3.3.4 Aplikasi pupnk organik cair
Aplikasi pupuk dilakukan pada tanaman Bayam (Amaranthus
Pemupukan dilakukan sebanyak 2 kali yaitu pada saat penanaman di polybag
setelah tanam) atau
+
14 hari setelah tanam sebanyak 112 dosis perlakuan(Hadisoeganda 1996). Pada pemupukan ini digunakan kontrol positif yaitu
pemupukan dengan pupuk urea dan kontrol negatif yaitu tanpa pemupukan atau
tanpa pemberian nitrogen. Sedangkan untuk perlakuan digunakan 7 taraf dosis.
Tujuh taraf dosis perlakuan yang digunakan dalam penelitian ini adalah :
D 1 = Sampel300 ml
+
SP-36 0,4 gr+
KC1 0,15 grD2 = Sampel550 ml
+
SP-36 0,4 gr+
KC1 0,15 grD3 = Sampel800 ml
+
SP-36 0,4 gr+
KC1 0,15 grD4 = Sampel 1050 ml
+
SP-36 0,4 gr+
KC1 0,15 grD5 = Limbah cair segar 207 ml
+
SP-36 0,4 gr+
KC1 0,15 grKP = Urea 0,38 gr
+
SP-36 0,4 gr+
KC1 0,15 grKN = SP-36 0,6 gr
+
KC1 0,3 grKemudian dilakukan pengamatan terhadap tanaman bayam setiap minggu
selama 3 MST, berdasarkan umur panen tanaman bayam yaitu 21 sampai 28 hari
atau setelah tinggi bayam mencapai 20 cm (Hadisoeganda 1996). Paranleter yang
diamati adalah :
a. Tinggi tanaman. Tinggi +mamail diamati dengan cara mengukur panjang
dari pangkal batang sampai ujung yang paling tinggi.
b. Jumlah daun. Jumlah daun ditentukan dengan cara menghitung jumlah
daun yang telah membuka secara sempurna.
3.3.3 Rancangan penelitian
Penelitian ini menggunakan rancangan acak lengkap (RAL) dengan satu
faktor yaitu dosis pemupukan. Dosis pemupukan yang digunakan terdiri atas
tujuh taraf yaitu Dl, D2, D3, D4, D5, KP, dan KN dimana dosis ditentukan berdasarkan kadar N yang terdapat dalam pupuk. Pada penelitian ini digunakan
juga kontrol positif menggunakan pupuk urea dan kontrol negatif tanpa
pemupukan. Masing-masing perlakuan diulang sebanyak 3 kali sehingga
diperoleli 21 satuan percobaan. Dunana satu satuan percobaan berupa tanaman
yang ditanam di polybag. Semua data pengamatan dianalisis dengan Analisis
dengan uji Tukey's pada selang kepercayaan 95%. Data diolah dengan
menggunakan SPSS 13 for windows.
Model rancangan percobaan yang digunakan adalah :
Yij= p + p i + & i j
Keterangan :
Yij = Nilai pengamatan pada perlakuan perlakuan ke-i, ulangan ke-j
p = Nilai rataan umum
pi = Nilai pengaruh perlakuan ke-i
4. HASIL DAN PEMBAHASAN
4.1 Karakteristik Limbah cair Buatan
Limbah cair merupakan buangan yang berbentuk cair yang berasal dari
lingkungan masyarakat dimana komponen utamanya adalah air dan mengandung
benda padat yang terdiri dari zat organik dan zat anorganik. Pada penelitian ini
digunakan limbah cair buatan karena lebih stabil daripada limbah industri.
Fomulasi yang digunakan dalam pembuatan limbah cair buatan mengacu pada
hasil penelitian Fauzi et. al. (2003), yaitu pembuatan limbah cair buatan dengan
perbandingan limbah padat (kg) dan volume air (liter) adalah 1:s. Pada
pembuatan limbah cair, dilakukan proses perebusan limbah padat yang bertujuan
untuk mendapatkan kadar nitrogen yang tinggi dalarn l i i b a h cair yang dihasilkan.
Limbah Cair yang dihasilkan dari proses pengolahan perikanan yang melalui
tahap perebusan seperti pengalengan, mengandung padatan tersuspensi atau bahan
organik dalarn jumlah yang tinggi (Pradina 1998 diacu dalam Sari 2005).
Karakteristik limbah cair buatan yang dihasilkan dapat dilihat pada Tabel 1.
Tabel 1. Karakteristik limbah cair buatan
Limbah cair buatan mengandung N dalam jumlah yang cukup tinggi. Hal
ini disebabkan karena liibah cair buatan ini berasal dari potongan-potongan ikan.
Ikan banyak mengandung protein sehingga limbah cair buatan yang dihasilkan
mengandung N dalam jumlah yang cukup tinggi. Derajat keasaman
(pH)
darilimbah cair buatan ini mendekati alkali yaitu 6,87. Menurut Gonzalez (1996)
yang diacu dalam Heriyanto (2006), limbah cair yang dihasilkan dari industri
adanya dekomposisi bahan-bahan yang mengandung protein. Sedangkan nisbah
CODITKN limbah buatan ini adaiah 6,44. Limbah cair industri perikanan
mempunyai nisbah CODITKN berkisar 1,l-11,3 (Sendic 1995). Limbah cair
buatan yang digunakan dalam penelitian ini telah memenuhi kriteria limbah cair
industri perikanan.
4.2 Penentuan Waktu Retensi
Waktu retensi merupakan waktu kontak atau waktu tinggal antara limbah cair dan lumpur aktif di dalam reaktor suatu sistem pengolahan limbah cair.
Penentuan waktu retensi atau lamanya limbah cair dan lumpur aktif di aerasi pada
penelitian ini berdasarkan lamanya waktu yang diperlukan untuk mencapai kadar
nitrat tertinggi. Senyawa nitrat merupakan produk akhir dari proses pengolahan
limbah cair dengan lumpur aktif dan merupakan unsur hara yang diperlukan oleh
tanaman dalam pertumbuhannya. Kadar nitrat yang didapatkan pada penelitian
[image:38.559.72.465.164.775.2]pendahuluan dapat dilihat pada Gambar 4.
Gambar 4. Kadar nitrat pada penelitian pendahuluan
Berdasarkan penelitian pendahuluan yang dilakukan terjadi peningkatan
kadar nitrat secara cepat pada waktu retensi 0 jam sampai 12 jam yang disebabkan
nutrien yang tersedia dalan limbah cair masih tinggi. Peningkatan secara
perlahan terjadi pada waktu retensi 12 jam sampai 48 jam serta terjadi penufunan
pada waktu retensi 48 jam sampai 72 jam. Hal ini disebabkan nutrien yang
sebagian mikroorganisme mengalami kematian. Kadar nitrat tertinggi didapatkan
pada waktu retensi 48 jam atau 2 hari yaitu 1,747 mgll. Dengan demikian waktu
retensi atau waktu aerasi limbah cair dan lumpur aktif yang digunakan pada
penelitian ini adalah 48 jam. Menurut Jenie dan Rahayu (1993), waktu retensi
pada proses nitrifikasi limbah cair peternakan unggas selama 2 hari dapat
menghasilkan laju nitrifikasi yang maksimum. Limbah petemakan juga
inengandung bahan organik yang tinggi seperti pada limbah cair perikanan.
4.3 Kondisi Nitrifikasi
Nitrifikasi merupakan proses perubahan amonia menjadi nitrit dan
selanjutnya menjadi nitrat melalui proses oksidasi oleh mikroorganisme. Proses
nitrifikasi membutuhkan oksigen dalam jumlah yang cukup banyak sehingga
menyebabkan penurunan oksigen terlarut dalam limbah cair.
Penanganan limbah cair perikanan secara biologis akan menghasilkan
amonia dari persenyawaan yang terbentuk dan amonia ini akan diuraikan oleh
mikroorganisme menjadi nitrit atau nitrat. Parameter-parameter yang dapat
digunakan untuk melihat kondisi nitrifikzsi limbah cair antara lain parameter
MLSS, MLVSS, DO, pH, COD, NH3-X, NO3-N, dan TKN.
4.3.1 MLSS dan MLVSS
Nilai MLSS dan MLVSS menunjukkan total padatan tersuspensi dalam
reaktor yang merupakan gabungan dari padatan tersuspensi tetap (FSS) dan
padatan tersuspensi yang bisa menguap (VSS). Oleh karena it-, nilai MLSS dan
MLVSS dapat digunakan untuk mengetahui adanya pemimbuhan mikroorganisme
yang ada dalam reaktor. Nilai MLSS dan MLVSS limbah cair buatan selama
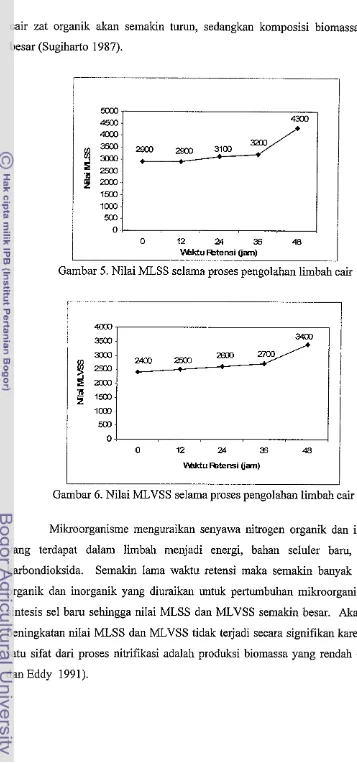
proses pengolahan dapat dilihat pada Gsunbar 5 dan Gambar 6.
Selama proses pengolahan limbah cair dengan lumpur aktif tejadi
peningkatan nilai MLSS yaitu 2900 mgll pada waktu retensi 0 jam sampai
4300 mgll pada waktu retensi 48 jam. Demikian juga dengan nilai MLVSS
mengalami peningkatan dari 2400 mgll pada waktu retensi 0 jam sampai
3400 mgll pada waktu retensi 48 jam. Hal ini disebabkan terjadi pertumbuhan
cair zat organik akan semakin turun, sedangkan komposisi biomassa semakin
besar (Sugiharto 1987).
I
0 12 24 33 48
[image:40.550.73.430.43.807.2]W uWteffii (jan)
Gambar 5. Nilai MLSS selama proses pengolahan limbah cair
Gambar 6. Nilai MLVSS selama proses pengolahan limbah cair
i 4 C 0 3
Mikroorganisme menguraikan senyawa nitrogen organik dan inorganik
yang terdapat dalam limbah menjadi energi, bahan seluler baru, air dan
karbondioksida. Semakin lama waktu retensi maka semakin banyak senyawa
organik dan inorganik yang diuraikan untuk perturnbullan mikroorganisme dan
sintesis sel baru sehingga nilai MLSS dan MLVSS semakin besar. Akan tetapi,
peningkatan nilai MLSS dan MLVSS tidak terjadi secara signifikan karena salah
satu sifat dari proses nitrifikasi adalah produksi biomassa yang rendah (Metcalf
dan Eddy 1991).
I 3503-
--
2w 25CO 28M
=
2ia)/
!
!4
=-
!d
2 0 3 -g
1m-ICCO -
m -
0 -
-
0 12 24 33 48
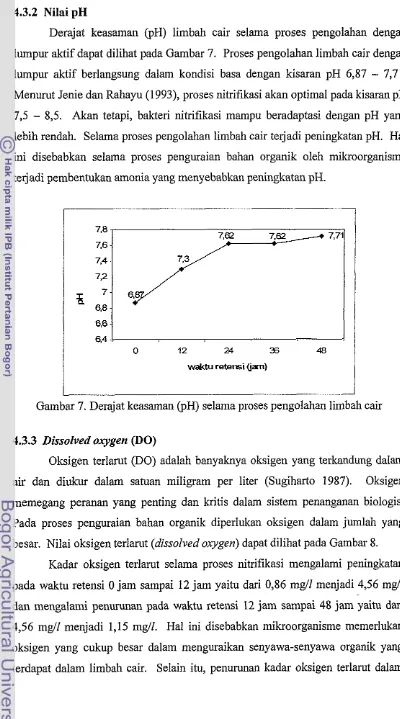
4.3.2 Nilai pH
Derajat keasaman @H) limbah cair selama proses pengolahan dengan
lumpur aktif dapat dilihat pada Gambar 7. Proses pengolahan limbah cair dengan
lurnpur aktif berlangsung dalam kondisi basa dengan kisaran pH 6,87 - 7,71.
Menurut Jenie dan Rahayu (1993), proses nitrifikasi akan optimal pada kisaran pH
7,5 - 8,5. Akan tetapi, bakteri nitrifikasi mampu beradaptasi dengan pH yang
lebih rendah. Selma proses pengolahan limbah cair te rjadi peningkatan pH. Hal
ini disebabkan selama proses penguraian bahan organik oleh mikroorganisme
[image:41.559.72.472.60.779.2]te rjadi pembentukan amonia yang menyebabkan peningkatan pH.
Gambar 7. Derajat keasaman @H) selama proses pengolahan limbah cair
7.8
1:
7 2
5
7 -6.8 -
6,6 -
6.4
4.3.3 Dissolved oxygen (DO)
Oksigen terlarut (DO) adalah banyaknya oksigen yang terkandung da1am
air dan diukur dalam satuan miligram per liter (Sugiharto 1987). Oksigen
memegang peranan yang penting dan kritis dalam sistem penanganan biologis.
Pada proses penguraian bahan organik diperlukan oksigen dalam jumlah y a ~ g
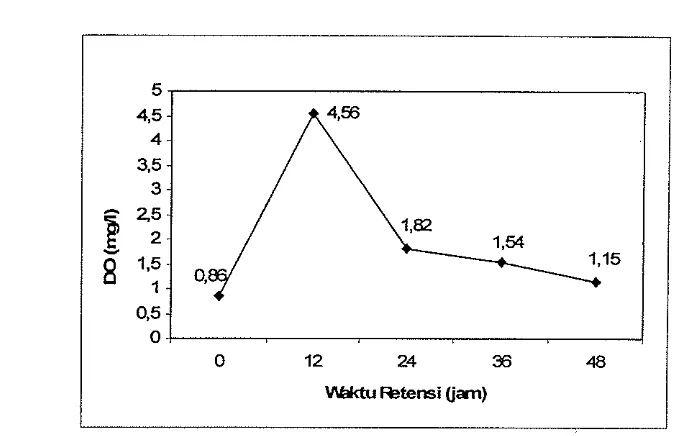
besar. Nilai oksigen terlarut (dissolved oxygen) dapat dilihat pada Gambar 8.
Kadar oksigen terlarut selama proses nitrifikasi mengalami peningkatan
pada waktu retensi 0 jam sampai 12 jam yaitu dari 0,86 mgll menjadi 4,56 mg/l
dan mengalami penurunan pada waktu retensi 12 jam sampai 48 jam yaitu dari
4,56 mgll menjadi 1,15 mgll. Hal ini disebabkan mikroorganisme memerlukan
oksigen yang cukup besar dalam menguraikan senyawa-senyawa organik yang
terdapat dalam limbah cair. Selain itu, penurunan kadar oksigen terlarut dalan
-
/ A -
737'6.
7
0 12 24 33
v.&m retensi (i;m)
*
' I
Ilinlbah dapat disebabkan oleh tingginya kandungan lemak dalam air limbah. Pada
keadaan basa, lemak akan membebaskan gliserin dan membentuk garam basa
yang larut dalam air (Sugiharto 1987). Lemak dalam limbah cair dapat
membentuk lapisan tipis dan selaput sehingga dapat menghambat distribusi
oksigen di dalam limbah cair (Wardhana 2001).
Untuk mempertahankan sistem aerobik diperlukan konsentrasi oksigen
terlarut minimum 0,5 mgll. Pada penanganan limbah secara nitrifikasi,
konsentrasi oksigen terlarut biasanya dijaga untuk tetap sekitar atau diatas 1 mgll
demi menjaga kelangsungan proses nitrifikasi sehingga tidak terjadi masalah
kekurangan oksigen (Jenie dan Rahayu 1993). Pada Gambar 8 dapat dilihat juga
laju pengambilan oksigen semakin tinggi dengan semakin rendahnya waktu
5 43
3 3*:#
$
2:1.5. 1 -
03 - 0 7
retensi. Laju pengambilan oksigeil tinggi pada waktu retensi singkat karena
adanya nisball makanan terhadap massa yang tinggi dan pertunlbuhan mikroba
yang cepat. Laju pengambilan oksigen akan turun dengan cepat bila waktu retensi
meningkat karena terjadi pengenceran limbah yang besar dan nisbah makanan
terhadap massa yang rendah.
L15
OS
4.3.4 COD (cl~ernical oxygen denzand)
Chemical oxygen demand (COD) merupakan parameter yang
0 12 24 33 48
[image:42.550.90.436.166.384.2]VIBMu R?temi (jan)
Gambar 8. Kadar oksigen terlarut (DO) selama proses pengolahan limbah cair
organik yang terdapat dalam limbah secara kimia. Nilai parameter COD selama
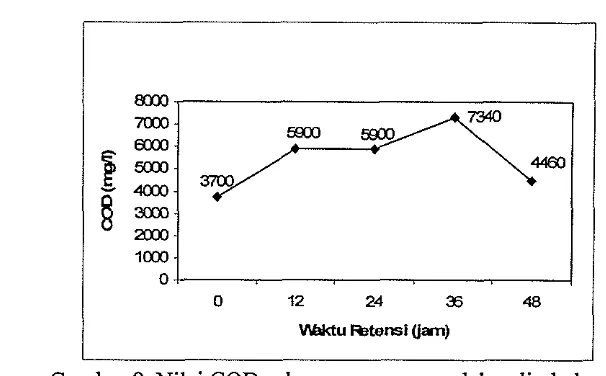
[image:43.559.111.414.112.300.2]proses pengolahan limbah cair dapat dilihat pada Gambar 9.
Gambar 9. Nilai COD selama proses pengolahan limbah cair
Nilai COD mengalami peningkatan sampai waktu retensi 36 jam yang
menunjukkan bahwa derajat pengotoran dalam air limbah masih tinggi. Nilai
COD baru mengalami p e n m a n setelah waktu retensi 48 jam yang berarti derajat
pengotoran dalam air limbah telah berkurang. Hal ini disebabkan pada awal
proses penguraian, rnikroorganisme menguraikan bahan organik secara cepat
sehingga terjadi pembentukan amonia dan nitrit dalam jumlah yang besar pula.
Hal ini dapat dilihat dari sedikitnya kadar nitrat yang terbentuk sampai waktu
retensi 48 jam. Dalam ha1 ini amonia dan nitrit mempakan senyawa yang
mengotori limbah karena memerlukan oksigen dalam penguraiannya sehingga
nilai COD meningkat sampai waktu retensi 36 jam. Selain itu meningkatnya nilai
COD dapat disebabkan kandungan lemak yang sangat tinggi dalam limbah cair.
Lemak akan lebii mudah diuraikan dalam kondisi asam (Sugiharto 1987). Pada
penelitian ini kondisi pengolahan limbah cair dalam keadaan basa sehingga lemak
akan temrai menjadi gliserin dan garam basa (sabun) yang sulit untuk dioksidasi
sehingga nilai COD semakin meningkat.
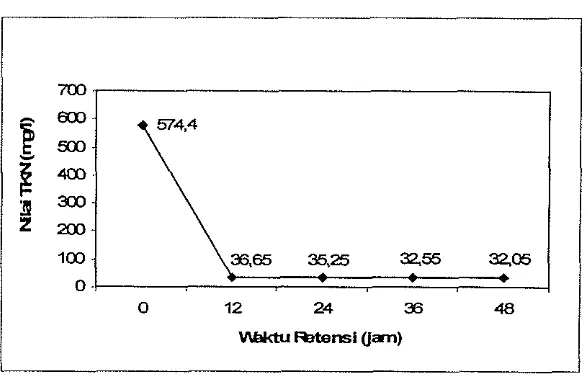
4.3.5 TKN
Total Ijeldahl nitrogen (TKN) menunjukkan jumlah total nitrogen organik yang terdapat dalam limbah. Total nitrogen organik selama proses pengolahan
I I
Gambar 10. Nilai TKN selama proses pengolahan limbah cair
603
200
la,
0 -
Nilai TKN mengalami penunulan yang sangat sigufikan pada selang
\,
2y
z 5 5 : ~waktu retensi 0 jam dan 12 jam. Hal ini menunjukkan pada waktu tersebut jumlah
nitrogen organik yang terurai sangat besar yang disebabkan besarnya nutrient
yang tersedia dalam limbah. Hal ini dapat juga dilihat dari p e n m a n kandungan
DO dalam air limbah secara drastis. Oksigen diperlukan dalam penguraian
nitrogen organik sehingga semakin besar jumlah nitrogen organik yang diuraikan,
semakin banyak oksigen yang digunakan. Selanjutnya tetap terjadi penurunan
nilai TKN walaupun dalam jumlah yang sangat kecil yang disebabkan nutrient
0 12 24 36 48
yang tersedia dalam limbah tinggal sedikit. Nitrogen organik akan diuraikan oleh
mikroorganisme menjadi amonia yang selanjutnya dioksidasi menjadi nitrit serta
nitrat. Selain dalam bentuk amonia, nitrit dan nitrat, nitrogen organik juga diubah
oleh mikroorganisme menjadi biolnassa sel dan mengendap dalam lumpur
(Verstraete dan Vaerenberg 1986 diacu dalam Firdaus 2004).
4.3.6 Kadar NH3.N (nitrogen amonia)
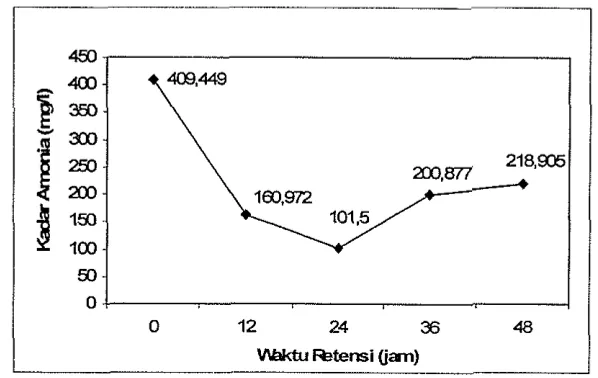
Kadar amonia selama proses pengolahan limbah cair dapat dilihat pada
Gambar 1 1. Kadar amonia selama proses pengolahan lirnbah cair dengan lumpur
aktif mengalami p e n m a n pada waktu retensi 0 jam sampai waktu retensi 24 jam
dan selanjutnya mengalami peningkatan sanlpai waktu retensi 48 jam. Kadar
anlonia pada waktu retensi 0 jam sebesar 409,449 mgll, waktu retensi 12 jam
sebesar 160,972 mgll, waktu retensi 24 jam sebesar 101,500 mgll, waktu retensi
Gambar 1 1. Kadar amonia selama proses pengolahan limbah cair
Pada awal proses pengolahan limbah cair sampai waktu retensi 24 jam
proses nitrifikasi berlangsung sangat cepat dan selanjutnya kecepatannya semakin
menurun. Hal ini mengakibatkan sebagian dari nitrat yang terbentuk mengalami
perubahan menjadi bentuk amonia kembali dan mengalami peningkatan jumlah.
Sistem yang digunakan dalam penelitian ini adalah sistem batch selungga
memungkinkan terjadinya reaksi bolak-balik. Selain itu, ha1 ini dapat juga
disebabkan karena oksigen terlarut yang tersedia dalam air limbah kurang optimal
sehingga bakteri mereduksi kembali sebagian nitrit ke dalam bentuk amonia dan
sebagian dioksidasi menjadi ~ t r a t yang ditunjukkan dengan meningkatnya nitrat
dalam jumlah yang relatif kecil.
4.3.7 Kadar N03-N (nitrogen nitrat)
Kadar nitrat selama proses nitrifikasi lirnbah cair dapat dilihat pada
Gambar 12. Selama proses pengolahan limbah cair, terjadi peningkatan kadar
nitrat sampai batas waktu retensi 48 jam. Kadar nitrat pada awal nitrifikasi
sebesar 0,326 mgll, waktu retensi 12 jam sebesar 0,575 mgll, waktu retensi 24 jam
sebesar 0,864 mgll, waktu retensi 36 jam sebesar 1,323 mgll dan waktu retensi 48
jam sebesar 2,070 mgn. Semakin rendah waktu retensi maka akan semakin
sedikit nitrat yang terbentuk dan semakin besar waktu retensi semakii banyak
nitrat yang akan terbentuk sampai batas waktu retensi dari proses nitrifikasi terseb~~t. Hal ini disebabkan karena semakin lama semakin banyak nitrit yang
0 12 24 33 48
[image:46.556.136.428.59.256.2]\n8ktu retensi (jan)
Gambar 12. Kadar nitrat selama proses pengolahan limbah cair
Pada penelitian utiuna, peningkatan kadar nitrat terjadi secara lambat atau
perlahan apabila dibandingkan dengan peningkatan kadar nitrat pada penelitian
pendahuluan. Hal ini disebabkan perbedaan kondisi mikroorganisme di dalam
lumpur aktif yang digunakan pada penelitian pendahuluan dan penelitian ut