EKSTRAK ENZIM CAIRAN RUMEN DOMBA (Ovis aries)
UNTUK BAHAN PAKAN IKAN NILA (Oreochromis niloticus)
INDIRA FITRILIYANI
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar
Doktor pada Program Studi Ilmu Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa disertasi “Peningkatan Kualitas Nutrisi Tepung Daun Lamtoro Dengan Penambahan Ekstrak Enzim Cairan Rumen Domba (Ovis aries) untuk Bahan Pakan Ikan Nila (Oreochromis niloticus) adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau kutipan dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka dibagian akhir disertasi ini.
Bogor, Oktober 2010
with Addition of Sheep Rumen Liquor Enzyme for Nila Tilapia (Oreochromis
niloticus) feed. Under Advisory by ENANG HARRIS, ING
MOKOGINTA, NAHROWI.
The aims of this experiment were; (1) to evaluate hydrolyze enzyme activity in exctract rumen liquor of sheep fed forage, (2) to improve the nutrient quality of leucaena leaf meal (LLM) by addition with sheep rumen liquor enzyme; (3) to evaluate the suitability of hydrolized LLM as alternative protein source for Nile tilapia. The first stage of experiment showed that the activity of enzyme hydrolyze in rumen fluid of sheep with forage feeding had the largest cellulase activity than amylase, protease, lipase and phytase activity. The second stage was designed in completely randomized design with 6 treatments and 3 replications with different level enzyme addition (0; 20; 40; 60; 80; and 100 ml/kg LLM) and incubated in 2 and 24 hours.. Results of the first experiment showed that nutrient quality of LLM with addition of sheep rumen liquor enzyme 100 ml/kg LLM, within incubated 24 hours have the best result than that of incubated 2 hours.The enzymes significantly (P<0.05) increased soluble glucose (2127,45%) soluble protein (3538,23%), decreased crude fiber (53,640%) and phytic acid (68,088%); but the enzyme did not affect crude lipid and crude protein content. The third stage experiments was conducted with two experimental diet. The first one contained hydrolyzed LLM at level 10% 15% 20% 25% and 30% ( Group I; Diet A, B, C, D and E respectively) and one diet acting as a control (Diet K, 0% LLM), the second experiments contained non-hydrolized LLM at the same level as the first ezperiment ( Group II; Diet F, G, H, I, J). All diets were isoenergy. A seven weeks feeding trial was carried out on triplicate groups of eight fish (9,38 ± 0,41) in aquarium with a recirculating system for group I and II. Fish were fed twice daily at satiation. Results showed that improvement of the quality of hydrolyzed LLM increased daily growth rate, feed efficiency, protein and fat retention. Similarly, the value of Hepato somatic indeks, glycogen content and enzyme activity of protease, amylase and cellulase in fish feeding hydrolyzed LLM were higher than that of non- hydrolyzed LLM. HIS and liver glycogen storage in fish with hydrolyzed LLM in diet increased with the increasing use of hydrolyzed LLM. Histological liver and intestine of tilapia using hydrolyzed LLM in the diet did not show significant differences with those of fish with feed without LLM. It is was concluded that enzymes from rumen liquer capable of increasing the nutritive quality of LLM. Application of hydrolyzed LLM up to 15% in the diet of tilapia show better performance compared with non-hydrolyzed LLM
K
INDIRA FITRILIYANI. Peningkatan Kualitas Nutrisi Tepung Daun Lamtoro dengan Penambahan Ekstrak Enzim Cairan Rumen Domba ntuk Bahan Pakan Ikan Nila (Oreochromis sp). Dibimbing oleh ENANG
ARRIS, ING MOKOGINTA, NAHROWI. u
H
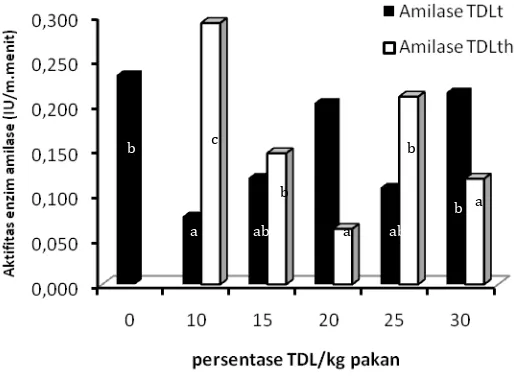
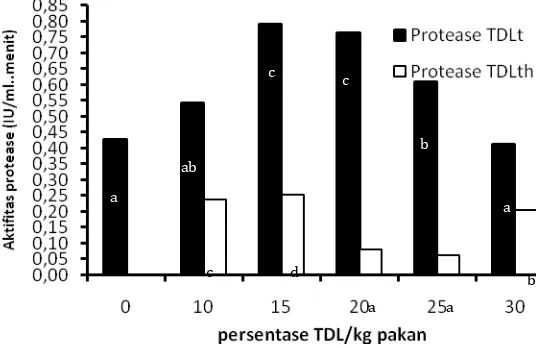
meningkatnya simpanan glikogen dengan meningkatnya kesediaan glukosa/karbohidrat sederhana di dalam pakan. Aktifitas enzim selulase dan amilase menunjukkan kecenderungan terjadinya peningkatan dengan meningkatnya penggunaan TDL terhidrolisis atau TDL tanpa hidrolisis dalam pakan akan tetapi aktifitas enzim selulase ikan perlakuan TDL terhidrolisis lebih rendah dari perlakuan TDL tanpa hidrolisis. Perlakuan kontrol tanpa penggunaan TDL memberikan nilai aktifitas enzim selulase terendah (0,0176 unit/ml/menit) dibandingkan seluruh perlakuan dengan TDL terhidrolisis maupun TDL tanpa hidrolisis. Nilai aktifitas enzim amilase pada saluran pencernaan ikan TDL terhidrolisis berada pada kisaran nilai 0,0758 –0,2148 (unit/ml/menit) sedangkan nilai aktifitas enzim amilase TDL tanpa hidrolisis berkisar 0,06202 – 0,292466 unit/ml/menit. Kisaran nilai aktifitas enzim amilase ini masih lebih rendah dari perlakuan kontrol tanpa penggunaan TDL terhidrolisis dalam pakan. Aktifitas enzim protease perlakuan yang menggunakan TDL terhidrolisis dan tidak terhidrolisis nyata (P<0,05) dipengaruhi oleh perbedaan persentase penggunaan TDL terhidrolisis dalam pakan dimana aktifitas enzim protease perlakuan dengan TDL terhidrolisis lebih tinggi dibandingkan TDL tanpa hidrolisis. Histologi hati dan usus ikan perlakuan dengan TDL terhidrolisis tidak memperlihatkan perbedaan yang signifikan dengan histologi hati dan usus ikan dengan pakan tanpa mengandung TDL. Dapat disimpulkan bahwa enzim selulase, amilase, protease, lipase dan fitase cairan rumen domba dapat meningkatkan kualitas nutrisi TDL. Penggunaan TDL terhidrolisis sampai 15 % dalam pakan ikan nila memperlihatkan kinerja pertumbuhan yang lebih baik dibandingkan penggunaan TDL tanpa hidrolisis pada taraf yang sama.
@ Hak Cipta milik IPB, tahun 2010
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebut sumber
a. Pengutipan hanya untuk kepentingan pendidikan, peneliti, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB 2. Dilarang mengumumkan dan memperbanyak sebagian atau
Dosen Penguji Ujian Tertutup 1. Dr. Ir. Dedi Djusadi, M.Sc
Wakil Dekan Pascasarjana, Institut Pertanian Bogor Staf Pengajar Departemen Budi Daya Perairan Fakultas Perikanan dan Ilmu Kelautan, IPB.
2. Dr. Ir. M. Agus Suprayudi, M.Si
Staf Pengajar Departemen Budi Daya Perairan Fakultas Perikanan dan Ilmu Kelautan, IPB.
Dosen Penguji Ujian Terbuka
1. Dr. Ir. Zafril Imran Azwar, M.Sc
Peneliti di Balai Riset Perikanan Budidaya Air Tawar, Sempur, Bogor.
2. Dr. Nur Bambang Priyo Utomo, M.Si
EKSTRAK ENZIM CAIRAN RUMEN DOMBA (Ovis aries)
UNTUK BAHAN PAKAN IKAN NILA (Oreochromis niloticus)
INDIRA FITRILIYANI
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar
Doktor pada Program Studi Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Cairan Rumen Domba (Ovis aries) untuk Bahan Pakan Ikan Nila (Oreochromis sp)
Nama : Indira Fitriliyani
NRP : C161060061
Program Studi : Ilmu Akuakultur
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Enang Harris, M.S Ketua
Prof. Dr.Ir. Ing Mokoginta, M.Sc Prof. Dr.Ir. Nahrowi, M.Sc Anggota Anggota
Diketahui
Ketua Departemen Dekan Sekolah Pascasarjana Ilmu Akuakultur
Prof.Dr.Ir.Enang Harris, M.S Prof.Dr.Ir. Khairil Anwar Notodiputro, M.S
kurnia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Nopember 2008 ini adalah dengan judul Peningkatan Kualitas Nutrisi Tepung Daun Lamtoro Dengan Ekstrak Enzim Cairan Rumen Domba (Ovis aries) Untuk Bahan Pakan Ikan Nila (Oreochromis sp).
Ungkapan terimakasih disampaikan kepada
1. Tim komisi pembimbing Bapak Prof. Dr. Ir. Enang Harris, M.S; Ibu Prof. Dr. Ir. Ing Mokoginta, MSc dan Bapak Prof. Dr. Ir. Nahrowi, MSc atas semua bimbingan, saran, koreksi, motivasi dan kebijaksanaan.
2. Departemen Pendidikan Nasional Direktorat Jendral Pendidikan Tinggi (DIKTI) yang telah memberikan Beasiawa Program Pascasarjana, memberikan kesempatan untuk mengikuti Sandwich Programme di Fisheries Faculty Kagoshima University dan bantuan Hibah Program Doktor 2009.
3. Rektor, seluruh staf akademis di Fakultas Perikanan Jurusan Budidaya Perairan Universtitas Lambung Mangkurat atas izin tugas belajar.
4. Kedua orang tua tercinta ayahanda H. Anwar Fauzie (alm) dan ibunda Hj Marliah Chairul dan kepada seluruh keluarga besar, teman-teman di AIR atas bantuan yang diberikan.
5. Suamiku H.Muhammad Mabrur Lc MAg, anak-anak tersayang Muhammad Aliif Azhar; Muhammad Rozien dan Muhammad Nabil,. yang setia mendampingi penulis dalam cinta, kerja dan doa.
6. Prof Shunzuke Koshio dan Associate Prof Manabu Ishikawa, yang telah memberikan banyak bimbingan kepada penulis selama di Kagoshima. Semoga Allah SWT memberikan balasan amal dan kebaikan mereka yang tak terhingga. Disertasi ini penulis persembahkan kepada perkembangan ilmu pengetahuan semoga dapat menjadi ilmu yang bermanfaat.
Bogor, Oktober 2010
Penulis dilahirkan di Banjarmasin 5 Oktober 1975 dari Bapak H.Anwar Fauzie (Alm) dan Ibu Hj Marliah Chairul merupakan anak kelima dari lima bersaudara. Pendidikan sarjana ditempuh di Fakultas Perikanan Jurusan Budidaya Perikanan Universitas Lambung Mangkurat 1993-1997. Kesempatan untuk melanjutkan ke program Magister Sains pada Program Studi Ilmu Perairan pada Program Pascasarjana IPB dengan Beasiswa Pendidikan diperoleh dari beasiswa Departemen Pendidikan Tinggi (DIKTI) tahun 2003-2005.
Tahun 2006 penulis diterima sebagai mahasiswa program doktor di Program Studi Ilmu Perairan Sekolah Pascasarjana Institut Pertanian Bogor. Konsentrasi Ilmu Nutrisi Ikan dengan bantuan beasiswa Departemen Pendidikan Tinggi (DIKTI).
xi
DAFTAR ISI ………. xi
DAFTAR TABEL ……… xii
DAFTAR GAMBAR ……….. xiii
DAFTAR LAMPIRAN ……… xv
I. PENDAHULUAN ……… 1
1.1 Latar Belakang ………... 1
1.2 Perumusan Masalah ………... 3
1.3 Tujuan dan Manfaat Penelitian ………. 4
1.4 Perumusan Hipotesis...………..………... 4
II. TINJAUAN PUSTAKA……… 5
2.1 Kebutuhan Nutrien Ikan nila... 5
2.2 Tepung Daun Lamtoro (Leucaena leucocephala)... 8
2.3 Cairan Rumen sebagai Sumber Enzim ... Enzim Pencernaan dan Peranannya dalam Proses Pencernaan... 13 2.4 17 III. METODELOGI……… 21
3.1 Tahap Pertama: Pengujian Aktifitas Enzim-enzim Hidrolisis Cairan Rumen Domba………. 21 3.1.1 Isolasi dan Produksi Ekstrak Enzim Cairan Rumen Domba………... 21
3.1.2 Uji Aktifitas Ekstrak Enzim Cairan Rumen Domba………... 21
3.2 Tahap Kedua: Pengaruh Penambahan Enzim Cairan Rumen Domba (In Vitro) pada Kualitas Tepung Daun Lamtoro……… 22 3.3 Tahap Ketiga: Pengujian In vivo TDL pada pakan Ikan Nila……… 24
xii
Pembahasan……….. 32
4.2. Tahap Kedua: Pengaruh Penambahan Enzim Cairan Rumen Domba (In Vitro) pada Kualitas Tepung Daun Lamtoro 35 4.2.1. Glukosa Terlarut……….. 36
4.2.2. Protein Terlarut……… 39
4.2.3. Kandungan Nutrient Tepung Daun Lamtoro………... 41
Pembahasan……… 48
4.3. Tahap Ketiga: Pengujian In vivo TDL pada pakan Ikan Nila……… 60
4.3.1. Laju Pertumbuhan Harian………... 60
4.3.2. Jumlah Konsumsi Pakan………. 61
4.3.3 Efisiensi Pakan………. 62
4.3.4. Retensi Protein dan Lemak……….. 63
4.3.5. Hepatosomatik Indeks dan Kadar Glikogen Hati……… 65
4.3.6. Aktifitas Enzim Pencernaan……… 67
4.3.7. Kadar Glukosa Darah Ikan Uji Perlakuan TDL Terhidrolisis………. 70
4.3.8. Histologi Hati dan Usus………... 72
Pembahasan……… 77
V. KESIMPULAN DAN SARAN……… 95
5.1. Kesimpulan………. 96
5.2. Saran……… 96
DAFTAR PUSTAKA... 97
xiii
No Halaman 1 Kebutuhan protein ikan Nila Oreochromis sp dengan bobot tubuh yang
berbeda... ...
6 2 Perbandingan komposisi asam amino dan makro, mikro mineral, antara
tepung ikan (TI), bungkil kedelai (TBK) dan tepung daun lamtoro
(TDL)………. 9
3 Komposisi enzim cairan rumen sapi……….. 16
4 Komposisi enzim cairan rumen domba………. 16
5 Karakteristik enzim-enzim cairan rumen sapi asal RPH………. 16
6 Komposisi proksimat dan komponen penyusun serat TDL……….... 23
7 Komposisi pakan perlakuan TDL terhidrolisis ………. Komposisi proksimat pakan perlakuan TDL terhidrolisis……… 25 8 . Komposisi proksimat pakan perlakuan TDL tanpa hidrolisis... 26 9 30 10 Kandungan aktifitas enzim pada setiap perlakuan………. 35
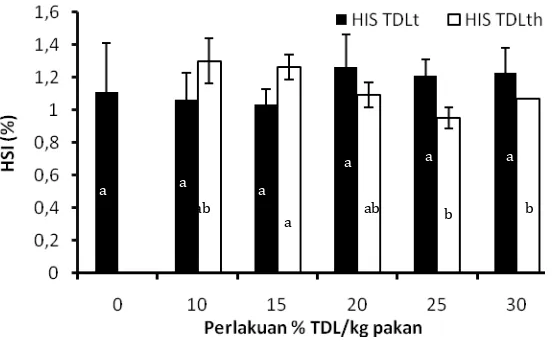
11 Komposisi asam amino tepung daun lamtoro sebelum sesudah inkubasi 24 jam dengan enzim rumen domba sebanyak 100 ml enzim/kg TDL………... 47
12 Komposisi asam amino essensial pakan percobaan ikan nila dengan taraf kandungan TDL terhidrolisis yang berbeda serta kebutuhan asam amino essensil ikan nila (% protein)……….. 77
xiv
No Halaman 1 Struktur molekul asam fitat……….. 11
2 Mekanisme asam fitat mengikat mineral………... 12 3 Mekanisme hidrolisis fosfat oleh enzim fitase (Applegate and Angel,
2004)……… 13
4 Bagian-bagian perut hewan ruminansia……… 13 5 Aktifitas enzim selulase, amilase, protease, lipase dan fitase ekstrak
cairan rumen domba………... 31 6 Nilai rata-rata kadar glukosa terlarut (%) periode inkubasi 2 jam
dan 24 jam………. 37 7 Persentase peningkatan glukosa terlarut perlakuan dibandingkan
kontrol pada inkubasi 2 jam dan 24 jam. ………... 38 8 Kurva respon kadar glukosa terlarut inkubasi 2 jam dengan jumlah
ekstrak enzim rumen berbeda……… 38 9 Kurva respon kadar glukosa terlarut inkubasi 24 jam dengan jumlah
ekstrak enzim rumen berbeda……… 38 10 Nilai rata-rata kadar protein terlarut setiap perlakuan dengan masa
inkubasi 2 jam dan 24 jam………. 39 11 Persentase peningkatan protein terlarut perlakuan dibandingkan
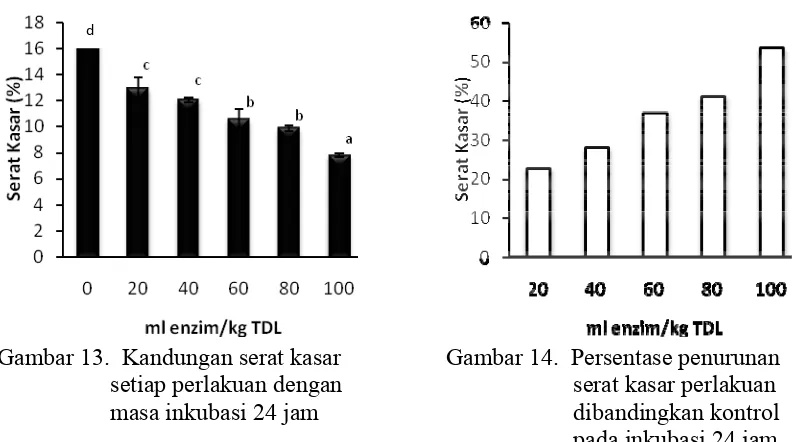
kontrol pada inkubasi 2 jam dan 24 jam……… 40 12 Kurva respon kadar protein terlarut inkubasi 2 jam……….. 41 13 Kandungan serat kasar setiap perlakuan dengan masa inkubasi 24
jam………. 42
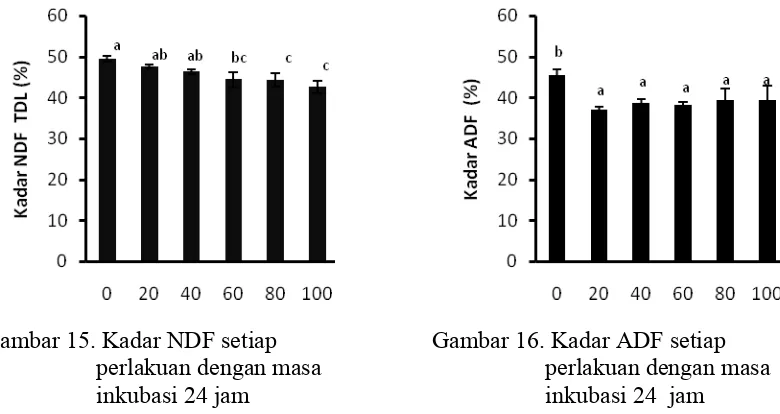
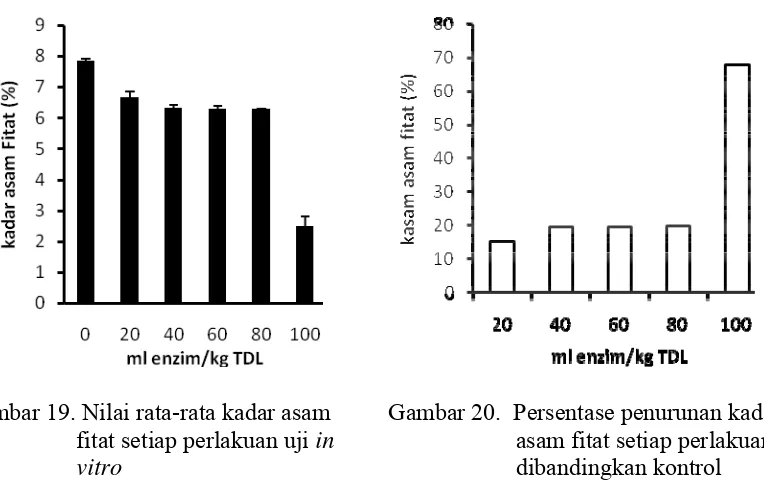
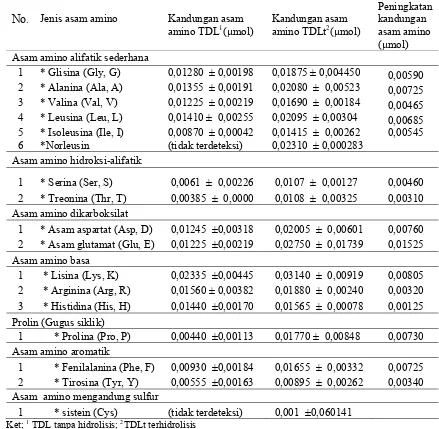
14 Persentase penurunan serat kasar perlakuan dibandingkan kontrol pada inkubasi 24 jam………... 42 15 Kadar NDF setiap perlakuan dengan masa inkubasi 24 jam…………. 43 16 Kadar ADF setiap perlakuan dengan masa inkubasi 24 jam………… 43 17 Nilai rata- rata kadar protein setiap perlakuan uji in vitro………... 44 18 Nilai rata-rata kadar lemak setiap perlakuan uji in vitro…………... 44 19 Nilai rata-rata kadar asam fitat setiap perlakuan uji in vitro………… 45 20 Persentase penurunan kadar asam fitat setiap perlakuan dibandingkan
xv
25 Perbandingan peningkatan kadar glukosa terlarut dan protein terlarut perlakuan dengan penambahan 100 ml enzim/kg TDL dengan perlakuan tanpa enzim pada waktu inkubasi 2 dan 24 jam………
48
26 27
Mekanisme kerja enzim amilase memotong ikatan α-1,4……….. Tiga tipe reaksi yang dikatalisasi oleh enzim selulase………...
50 52 28 Hidrolisis protein oleh enzim eksopeptidase………. 54 29 Nilai Laju pertumbuhan harian perlakuan TDL terhidrolisis dan
TDL tanpa hidrolisis……….. 61 30 Nilai jumlah konsumsi pakan perlakuan TDL terhidrolisis dan TDL
tanpa hidrolisis………... 62 31 Nilai Efisiensi pakan perlakuan TDL terhidrolisis dan TDL tanpa
hidrolisis………. 63 32 Nilai retensi protein perlakuan TDL terhidrolisis dan TDL tanpa
hidrolisis………... 64 33 Nilai retensi lemak perlakuan TDL terhidrolisis dan TDL tanpa
hidrolisis………. 65 34 Nilai hepatosomatik indeks (HIS) perlakuan TDL terhidrolisis dan
TDL tanpa hidrolisis……….. 66 35 Aktifitas enzim selulase (IU/ml.menit) TDL terhidrolisis dan TDL
tanpa hidrolisis………... 68 36 Aktifitas enzim amilase (IU/ml.menit) TDL terhidrolisis dan TDL
tanpa hidrolisis………... 69 37 Aktifitas enzim protease (IU/ml.menit) TDL terhidrolisis dan TDL
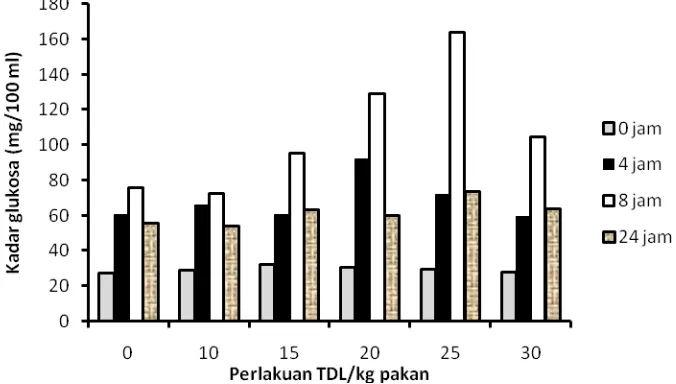
tanpa hidrolisis………. 70 38 Pola kadar glukosa darah (mg/100mL) ikan uji setiap perlakuan pada
jam pengamatan 0, 4, 8 dan 24 jam post prandial………. 71 39 Histologi hati ikan nila perlakuan K (0% TDL dalam pakan) dan
perlakuan A (10% TDL dalam pakan)……….. 72 40 Histologi hati ikan nila perlakuan B (15% TDL dalam pakan) dan
perlakuan C (20% TDL dalam pakan)………... 73 41 Histologi hati ikan nila perlakuan D (25% TDL dalam pakan) dan
perlakuan E (30% TDL dalam pakan)………... 73 42 Histologi usus ikan nila perlakuan K (0% TDL dalam pakan) dan
xvi
44 Histologi usus ikan nila perlakuan B (15% TDL dalam pakan) dan perlakuan C (20% TDL dalam pakan)-penekanan pada struktur……….. 75 45 Histologi usus ikan nila perlakuan B (15% TDL dalam pakan) dan
perlakuan C (20% TDL dalam pakan)-penekanan pada deteksi sel goblet (GC) dan sel vill (VC)………. 75 46 Histologi usus ikan nila perlakuan D (25% TDL dalam pakan) dan
perlakuan E (30% TDL dalam pakan)-penekanan pada struktur……... 76 47 Histologi usus ikan nila perlakuan D (25 % TDL dalam pakan) dan
xvii
Uji aktifitas enzim selulase/FP-ase (Metode Ghosse, 1987)………. Uji aktifitas enzim amilase (Bergmeyer dan Grassi 1983)……… Uji aktifitas enzim protease (Bergmeyer dan Grassi 1983)……….. Uji aktifitas enzim lipase (Tietz dan Friedreck dalamBarlongan, 1990)…….. Uji aktifitas enzim Fitase (Greiner et al. 1997)……… Prosedur analisis kadar glukosa terlarut (Wedemeyer & Yasutake 1977) Prosedur analisis kadar protein terlarut (Bradford, 1976)... Prosedur analisis proksimat (kadar air, kadar abu, kadar protein, kadar lemak dan kadar serat kasar) mengikuti metode AOAC (1990) Penentuan Kadar NDF dan ADF (Van Soest, 1991)……….. Prosedur analisis asam fitat (AOAC, 1990)……… Prosedur analisis HPLC (ICI Intrument Method, 1988)……… Prosedur analisis kadar glikogen (Wedemeyer dan Yasutake, 1977)... Prosedur memperoleh ekstrak enzim saluran pencernaan untuk analisis aktifitas enzim pencernaan……….. Prosedur persiapan preparat histologis organ hati dan usus…………. Penghitungan aktivitas enzim seluase, amilase, protease, fitase dan lipase enzim cairan rumen domba………
108 16 Penghitungan kadar glukosa terlarut daun lamtoro gung inkubasi 2
jam……… 125 17 Penghitungan kadar glukosa terlarut daun lamtoro gung inkubasi 24
jam………
126 18 Analisis ragam kadar glukosa terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 2 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba………... 126 19 Uji Duncan kadar glukosa terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 2 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……….. 127 20 Analisis ragam kadar glukosa terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba………. 127 21 Uji Duncan kadar glukosa terlarut (%) tepung daun lamtoro gung
xviii
23 Penghitungan kadar protein terlarut tepung daun lamtoro gung inkubasi 24 jam ………
129 24 Analisis ragam kadar protein terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 2 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……….. 130 25 Uji Duncan kadar protein terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 2 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba………... 130 26 Analisis ragam kadar protein terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……….. 130 27 Uji Duncan kadar protein terlarut (%) tepung daun lamtoro gung
pada periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba ………. 131 28 Penghitungan kadar serat tepung daun lamtoro gung inkubasi 24
jam………. 131 29 Analisis ragam kadar serat (%) tepung daun lamtoro gung pada
periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……… 132 30 Uji Duncan kadar serat (%) tepung daun lamtoro gung pada periode
inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba………..
132 31 Penghitungan kadar NDF tepung daun lamtoro gung inkubasi 24
jam……… 132 32 Penghitungan ADF tepung daun lamtoro gung inkubasi 24 jam…….. 133 33 Analisis ragam NDF (%) tepung daun lamtoro gung pada periode
inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba………. 133 34 Uji Duncan NDF (%) tepung daun lamtoro gung pada periode
inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba………... 134 35 Analisis ragam ADF (%) tepung daun lamtoro gung pada periode
inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……….. 134 36 Uji Duncan ADF(%) tepung daun lamtoro gung pada periode
inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen………...
xix
38 Penghitungan kadar lemak (% bobot kering) tepung daun lamtoro gung inkubasi 24 jam………
135 39 Analisis ragam kadar protein (%) tepung daun lamtoro gung pada
periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen ……….. 136 40 Analisis ragam kadar lemak (%) tepung daun lamtoro gung pada
periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen ……….. 136 41 Penghitungan kadar asam fitat (%) tepung daun lamtoro gung
inkubasi 24 jam………. 137 42 Analisis ragam kadar asam fitat (%) tepung daun lamtoro gung pada
periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……… 137 43 Uji Duncan kadar asam fitat (%) tepung daun lamtoro gung pada
periode inkubasi 24 jam setelah dihidrolisis dengan berbagai jumlah ekstrak enzim cairan rumen domba……….. 138 44 Perhitungan laju pertumbuhan harian ikan uji pada setiap perlakuan
tahap ketiga dengan menggunakan TDL terhidroisis………... 138 45 Perhitungan laju pertumbuhan (%) TDL tanpa hidrolisis…………... 139 46 Analisis ragam laju pertumbuhan harian (%) ikan uji TDL
terhidrolisis ……….
139 47 Uji Duncan laju pertumbuhan harian (%)TDL terhidrolisis………… 140 48 Analisis ragam laju pertumbuhan harian (%) TDL tanpa hidrolisis... 140 49 Uji Duncan laju pertumbuhan harian (%)TDL tanpa
hidrolisis……… 141 50 Nilai jumlah konsumsi pakan (g) dan efisiensi pakan (%) ikan uji
TDL terhidrolisis……….. 141 51 Nilai jumlah konsumsi pakan (g) dan efisiensi pakan (%) ikan uji
TDL tanpa hidrolisis………
142
xx
59 Nilai retensi protein dan lemak pada ikan TDL tanpa hidrolisis……. 146
60 Analisis ragam retensi protein (%) TDL terhidrolisis ……… 147
61 Uji Duncan retensi protein (%)TDL terhidrolisis ……….. 147
62 Analisis ragam retensi protein (%)TDL tanpa hidrolisis………. 148
63 Uji Duncan retensi protein (%)TDL tanpa hidrolisis……….. 148
64 Analisis ragam retensi lemak (%) TDL terhidrolisis ……… 148
65 Uji Duncan retensi lemak (%)TDL terhidrolisis ……….. 149
66 Analisis ragam retensi lemak (%)TDL tanpa hidrolisis………. 149
67 Uji Duncan retensi lemak (%)TDL tanpa hidrolisis……… 149
68 Hepatosomatik indeks, kecernaan dan kadar glikogen hati ikan uji dengan TDL terhidrolisis………. 150 69 Hepatosomatik indeks, kecernaan dan kadar glikogen hati ikan uji dengan TDL tanpa hidrolisis……… 151 70 Analisis ragam hepatosomatik indeks (%) TDL terhidrolisis………. 151
71 Analisis ragam hepatosomatik indeks (%)TDL tanpa hidrolisis……. 152
72 Uji Duncan hepatosomatik indeks (%)TDL tanpa hidrolisis………… 152
73 Analisis ragam kadar glikogen hati (mg/100mg) TDL terhidrolisis… 152 74 Uji Duncan kadar glikogen hati (mg/100mg)TDL terhidrolisis…….. 153
75 Analisis ragam kadar glikogen hati (mg/100mg) TDL tanpa hidrolisis……….. 153 76 Uji Duncan kadar glikogen hati (mg/100mg)TDL tanpa hidrolisis……….. 153 77 Aktivitas enzim pencernaan pada usus ikan penelitian TDL terhidrolisis……… 154 78 Aktivitas enzim pencernaan pada usus ikan penelitian TDL tanpa hidrolisis……… 155 79 Analisis ragam aktivitas enzim selulase TDL terhidrolisis………….. 155
80 Uji Duncan aktivitas enzim selulase TDL terhidrolisis………... 156
81 Analisis ragam aktivitas enzim selulase TDL tanpa hidrolisis………. 156
82 Analisis ragam aktivitas enzim amilase TDL terhidrolisis…………... 156
83 Analisis ragam aktivitas enzim amilase TDL tanpa hidrolisis……….. 156
xxi
87 Analisis ragam aktivitas enzim protease TDL tanpa hidrolisis……… 158 88 Uji Duncan aktivitas enzim protease TDL tanpa hidrolisis... 158 89 Profil kadar glukosa darah (mg/100ml darah) perlakuan TDL
terhidrolisis………..
159 90 Rekapitulasi data parameter LPH, Konsumsi pakan, efisiensi pakan,
retensi protein dan aktifitas enzim usus percobaan in vivo dengan perlakuan perbedaan persentase TDL terhidrolisis dalam pakan……. 160 91 Rekapitulasi data parameter LPH, Konsumsi pakan, efisiensi pakan,
retensi protein dan aktifitas enzim usus percobaan in vivo dengan perlakuan perbedaan persentase TDL tanpa hidrolisis dalam pakan… 161 92 Rekapitulasi data parameter retensi lemak, HIS dan glikogen hati
percobaan in vivo dengan perlakuan perbedaan persentase TDL terhidrolisis dalam pakan………. 163 93 Rekapitulasi data parameter retensi lemak, HIS dan glikogen hati
I. PENDAHULUAN
1.1. Latar belakang
Peningkatan permintaan ikan nila sebagai salah satu pilihan sumber protein hewani dengan harga yang terjangkau untuk masyarakat di negara berkembang seperti Indonesia, serta di pasar internasional mendorong meningkatnya usaha budidaya ikan nila. Pada tahun 2004 Amerika Utara mengimpor nila sebesar 112.945 ton pada 2004, meningkat 25% dibandingkan pada tahun 2003 dan 68% dibandingkan produksi pada tahun 2002. Setengah dari impor Amerika Utara, dipasok oleh Cina, sedangkan sisanya oleh Taiwan, Thailand dan Indonesia (FAO 2004). Produksi nila nasional pada tahun 2004 sebesar 97.116 ton, dan kemudian meningkat sebesar 23,7% dalam kurun waktu 2004-2008 menjadi sebesar 220.900 ton (DKP 2008). Peningkatan produksi ini memposisikan Indonesia pada peringkat keempat negara produsen nila terbesar di dunia setelah Cina, Mesir dan Philipina. Dengan adanya kasus KHV (Koi Herpes Virus) pada ikan mas, nila menjadi alternatif ikan air tawar yang dibudidayakan masyarakat dan salah satu andalan dalam program revitalisasi perikanan. Perkembangan usaha budidaya ikan nila, sangat bergantung dengan pakan buatan yang dapat mendukung pertumbuhan ikan nila yang optimal, sehingga peningkatan kualitas pakan buatan menjadi suatu yang sangat penting.
Ikan nila mempunyai kemampuan untuk memanfaatkan pakan buatan yang mengandung bahan-bahan dari tumbuhan (Fagbenro 1998; Olvera et al. 1997; E1-Sayed 1999; Fontainhas et al. 1999; Main et al. 2002; Ogunji dan Wirth 2000, Chimatiro dan Costa-Pierce 1996), bakteri (Beveridge et al. 1989), fitoplankton hijau (Pantastico et al.
1982). dan Spirulina (Lu dan Takeuchi 2004). Kemampuan dari ikan nila secara morfologi dan fisiologi untuk mencerna bahan pakan dengan kandungan serat tinggi membuka peluang untuk pengembangan pakan buatan ikan nila dengan menggunakan bahan pakan dari tepung daun dari berbagai jenis tanaman legumes seperti daun lamtoro (El Sayed 1999).
1982), komposisi asam amino yang relatif cukup baik serta kandungan Β -karoten yang relatif tinggi (Agbede dan Aletor 2004). Menurut NAS (1994) tanaman ini dapat menghasilkan bahan kering dari unsur-unsur yang dapat dimakan sebesar 6 - 8 ton per hektar per tahun atau sekitar 20 - 80 ton bahan segar. Di Indonesia tanaman leguminosa ini mudah ditanam sehingga dapat membantu penyediaan pakan secara kontinyu sepanjang tahun.
Pemanfaatan bahan baku pakan ikan nila dari daun khususnya daun lamtoro dibatasi oleh kandungan neutral detergent fiber (NDF) yang tinggi yaitu sebesar 39,5% dan acid detergent fiber (ADF) sebesar 35,10%. (Garcia et al. 1996), defisiensi asam amino esensial (Agr, Thr, He, His, Met) dan kandungan antinutrien seperti mimosin dan asam fitat (Lim dan Dominy 1991; Wee dan Wang 1987; Hertrampf dan Pascual 2000). Defisiensi asam amino dapat diatasi dengan menambahkan asam amino esensial yang menjadi pembatas (Santiago dan Lovell 1988), sedangkan untuk mengatasi mimosin telah dilaporkan beberapa metode yang efektif untuk mereduksi mimosin seperti perendaman dan pemanasan (Wee dan Wang, 1987; Widyastuti 2001). Reduksi anti nutrient asam fitat sangatlah penting sebelum penggunaan TDL dalam pakan, karena asam fitat dapat mengikat protein dan mineral di dalam digesta dan berpotensi untuk menghambat aktivitas enzim-enzim pencernaan (Conrad et al. 1996; Ravindran et al. 2000). Beberapa peneliti membuktikan bahwa penambahan enzim fitase mampu menghidrolisis asam fitat menjadi orthofosfat anorganik dan senyawa inositol yang lebih rendah. Ikan seperti hewan monogastrik lainnya tidak dapat mencerna asam fitat karena ketiadaan enzim fitase di saluran pencernaan (Ravindran et al. 2000).
menghidrolisis tepung daun lamtoro sehingga dapat ditingkatkan kualitas nutriennya. Penggunaan enzim eksogen ini terkendala dengan harga enzim komersil yang mahal di pasaran dan biasanya enzim komersil dijual dengan spesifik aktifitas enzim tertentu. Terkait dengan hal tersebut sangatlah penting dicari sumber enzim yang mengandung multi enzim, murah dan efektif untuk meningkatkan kualitas nutrien dari tepung daun lamtoro.
Cairan rumen domba merupakan salah satu sumber bahan suplemen alternatif yang murah dan dapat dimanfaatkan dengan mudah sebagai sumber enzim hidrolase (Moharrery dan Das, 2002). Cairan rumen domba (Ovies aries) yang didapat dengan memeras isi rumen, merupakan limbah rumah pemotongan hewan (selanjutnya disingkat RPH) ketersediaan cukup melimpah dan berpotensi sebagai sumber enzim. Kung et al. (2000) melaporkan bahwa cairan rumen sapi mengandung enzim protease/ deaminase yang menghidrolisis protein atau peptida, amilase yang menghidrolisis pati, selulase yang menghidrolisis selulosa, hemiselulase (xylanase) yang menghidrolisis hemiselulosa (xylan), lipase yang menghidrolisis emak, fitase yang menghidrolisis fitat dan lain-lain.
Potensi multienzim yang terkandung dalam cairan rumen diharapkan dapat menghidrolisis nutrien dalam TDL sehingga kualitas nutrien TDL dapat ditingkatkan. Selain mengandung enzim, cairan rumen domba juga mengandung asam-asam amino, vitamin dan mineral. Peningkatan kulitas nutrient TDL akan meningkatkan pula kinerja pertumbuhan dan pemanfaatan pakan ikan yang mengandung TDL. Produk yang diekstraksi dari cairan rumen ini diharapkan dapat secara langsung digunakan oleh pembudidaya ikan nila sehingga jauh lebih efisien dibanding bila harus mendirikan sebuah industri enzim yang memerlukan investasi biaya yang sangat besar.
1.2. Perumusan Masalah
dari TDL meningkat. Peningkatan kualitan nutrien ini diharapkan dapat meningkatkan efisiensi pakan sehingga kinerja pertumbuhan ikan nila dapat lebih baik.
Potensi yang dimiliki oleh cairan rumen domba sebagai sumber enzim-enzim hidrolisis seperti amilase, protease, lipase dan selulase menjadikannya sebagai salah satu sumber bahan suplemen alternatif yang murah dan dapat dimanfaatkan dengan mudah untuk meningkatkan kualitas nutrien dari tepung daun lamtoro, sehingga kecernaan dapat meningkat dan pertumbuhan ikan nila dapat lebih optimal.
1.3. Tujuan Penelitian 1.3.1. Tujuan umum :
Meningkatkan kualitas nutrien TDL sebagai sumber protein nabati alternatif pakan ikan nila dengan memanfaatkan dan mendayagunakan cairan rumen domba sebagai sumber enzim hidrolisis (predigestion)
1.3.2. Tujuan khusus :
1. Menguji aktifitas enzim selulase, amilase, protease, lipase dan fitase dalam ekstrak enzim cairan rumen domba yang dipelihara dengan pakan hijauan.
2. Mengkaji pengaruh hidrolisis (predigestion) TDL dengan ekstrak enzim cairan rumen domba terhadap kualitas nutrien TDL.
3. Menguji efektifitas pemanfaatan TDL terhidrolisis (predigestion) dalam pakan untuk ikan nila serta pengaruhnya pada perubahan aktifitas enzim pencernaan dan metabolisme nutrient dalam tubuh ikan.
1.4. Manfaat Penelitian
Hasil penelitian ini diharapkan bermanfaat untuk pengembangan ilmu nutrisi ikan khususnya untuk meningkatkan kualitas nutrien dari TDL dengan menggunakan ekstrak enzim cairan rumen domba, yang selanjutnya dalam jangka panjang teknologi ini dapat diaplikasikan dan dikembangkan dalam budidaya ikan nila.
1.5. Perumusan hipotesis
II. TINJAUAN PUSTAKA
2.1. Kebutuhan Nutrien Ikan Nila
Komponen pakan yang berkontribusi terhadap penyediaan materi dan energi untuk tumbuh adalah protein, karbohidrat dan lemak. Protein pada ikan berperan sebagai sumber nutrient dan sebagai sumber energy. Protein merupakan molekul kompleks yang terdiri dari asam amino esensial dan non essensial. Protein adalah nutrien yang sangat dibutuhkan untuk perbaikan jaringan tubuh yang rusak, pemeliharaan protein tubuh, penambahan protein tubuh untuk pertumbuhan, materi untuk pembentukan enzim dan beberapa jenis hormon, dan juga sebagai sumber energi (NRC 1993). Kebutuhan ikan akan protein dipengaruhi oleh berbagai faktor diantaranya ukuran ikan, temperatur air, kadar pemberian pakan, kandungan energi dalam pakan yang dapat dicerna dan kualitas protein (Furuichi 1988).
Kebutuhan protein ikan berbeda-beda menurut spesiesnya, namun pada umumnya ikan membutuhkan protein sekitar 30 - 40 % dalam pakannya (Jobling 1994). Ikan air tawar umumnya dapat tumbuh dengan baik dengan pemberian pakan yang mengandung kadar protein 25 - 35 % dengan rasio energi protein adalah sekitar 8 kkal/gram protein. Pada Tabel 1 disampaikan data perbedaan kebutuhan protein ikan nila dengan bobot tubuh yang berbeda.
Defisiensi asam amino esensial (Agr,Thr, He, His, Met) dan kandungan mimosin (Lim dan Dominy 1991) merupakan faktor pembatas dalam pemanfaatan TDL dalam pakan ikan. Defisiensi asam amino dapat diatasi dengan menambahkan asam amino esensial yang menjadi pembatas sedangkan untuk mengatasi mimosin telah dilaporkan beberapa metode untuk mereduksi mimosin. Seperti dilaporkan oleh Hasan et al. (1994), kecernaan TDL pada Labeo rorita
sinar matahari memberikan pertumbuhan yang lebih baik pada nila dibandingkan TDL yang ditambahkan sodium hidroksida.
Tabel 1. Kebutuhan protein ikan Nila Oreochromis sp dengan bobot tubuh yang berbeda.
Spesies Bobot tubuh ikan (g)
Keperluan protein (%)
Pustaka1
O.mossambicus 1,0-2,5 29-38 Cruz dan Laudencia (1977)
Fry 50 Jauncey dan Ross (1982) 0,5-1,0 40 Jauncey dan Ross (1982) 6,0 - 30,0 30-35 Jauncey dan Ross (1982)
1,8 40 Jauncey (1982)
O. niloticus 1,5-7,5 36 Kubaryk (1980)
3,2-3,7 30 Wange et al. (1985) 0,838 40 Siddiqui et al. (1988)
40 30 Siddiqui et al. (1988)
O. aureus 0,3-0,5 36 Davis dan Stickney (1978)
0,16 40 Santiago dan Laron (1991)
Tilapia zillii 1,7 35-40 Teshima et al. (1978)
1,65 35 Mazid et al. (1979)
O.niloticus x O. aureus
0,6-1,1 32 Shiau dan Peng ( 1993) 21 28 Twibell dan Brown (1998) 1
di dalam El-Sayed (2006).
(Badawy et al. 1995) pemakaian 15% TDL dalam pakan mengakibatkan pertumbuhan menjadi rendah.
Penyediaan sumber protein pakan baik tepung ikan dan bungkil kedelai masih bergantung pada impor. Tumbuhan leguminosa dan sereal serta produknya telah dicoba digunakan sebagai substitusi dari bungkil kedelai di dalam pakan ikan nila (Meulen et al. 1979). Hal ini sangat memungkinkan digunakan untuk budidaya ikan nila karena ikan nila adalah ikan omnivora yang cenderung herbivora sehingga lebih mudah beradaptasi dengan jenis pakan yang dicampur dengan sumber bahan nabati seperti bungkil kedelai, tepung jagung, tepung biji kapuk, tepung eceng gondok, tepung alfalfa, serta tepung daun dari berbagai jenis tanaman legumes seperti daun lamtoro (El Sayed 1999). Popma (1982) menjelaskan kemampuan ikan nila dan ikan air tawar yang bersifat herbivora dan cenderung omnivora yang dapat mencerna lebih dari 70% energi kotornya dari bahan non-strach, sedangkan pada ikan yang bersifat karnivora seperti ikan trout, Wilson dan Poe (1987) melaporkan hanya mampu mencerna kurang dari 50% .
Karbohidrat merupakan sumber energi yang penting meskipun kandungan karbohidrat dalam pakan berada dalam jumlah yang relatif rendah. Karbohidrat dalam pakan dapat berupa serat kasar serta bahan ekstrak tanpa nitrogen (BETN). BETN mengandung banyak gula dan pati yang bersifat mudah dicerna sedangkan serat kasar kaya akan lignin dan selulase yang sukar dicerna. Energi dari karbohidrat sama efektifnya dengan energi dari lemak (NRC 1993). Pemberian tingkat energi optimum dalam pakan sangat penting karena kelebihan dan kekurangan energi dapat menurunkan pertumbuhan ikan (Lovell 1988).
pakannya sedangkan ikan-ikan omnivora mampu memanfaatkan karbohidrat optimum sebesar 30-40% dalam pakan (Furuichi 1988).
Bungkil kedelai dan tepung ikan adalah bahan yang umum digunakan sebagai sumber protein dalam pakan. Tetapi dengan meningkatnya permintaan manusia akan protein di beberapa negara berkembang, serta diiringi dengan meningkatnya harga bungkil kedelai dan tepung ikan di tingkat dunia haruslah dicari bahan dasar lain sebagai sumber protein pakan yang sifat bahan tersebut adalah lokal sehingga harganya tidak terlalu fluktuatif.
2.2. Tepung Daun Lamtoro (Leucaena leucocephala)
Kale (1987) menyatakan bahwa lamtoro adalah tumbuhan leguminosa tropis, berasal dari Amerika Tengah. Tumbuhan ini disebarkan oleh orang-orang Mayan dan Zapotec ke seluruh Amerika Tengah. Klasifikasi Leucaena leucocephala menurut Brewbaker dan Hylin (1965) adalah, salah satu spesies dari genus Leucaena yang termasuk sub Famili Mimosoideae, Famili Leguminoseae, sub ordo Rosicae, Ordo Resales, Sub Klas Dycotyledonea, Klas Angiospermopsidae, sub Divisio Spermatophyta, Divisio Traceophyta dan sub Kingdom Embryobionta.
Lamtoro (Leucaena) terdiri atas 53 spesies yang digolongkan ke dalam 10 spesies yang telah dikenal. Walaupun seluruh spesies tersebut mungkin sangat berguna bagi daerah tropis, tetapi hanya Leucaena leucocephala yang telah dimanfaatkan secara luas (NAS 1994). Tanaman lamtoro tumbuh baik di daerah dengan curah hujan tahunan antara 1000 - 3000 mm. Sementara Garcia et al.
unsur-unsur yang dapat dimakan (daun dan ranting-ranting kecil) sebesar 6-8 ton per hektar per tahun atau sekitar 20 - 80 ton bahan segar per hektar pertahun.
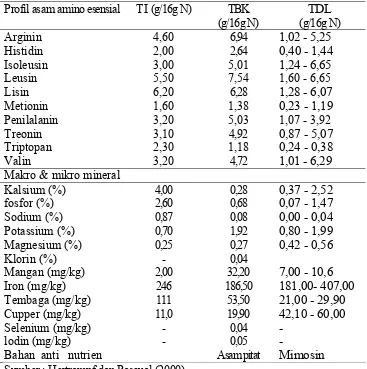
Tabel 2. Perbandingan komposisi asam amino dan makro, mikro serta mineral, antara tepung ikan (TI), bungkil kedelai (TBK) dan tepung daun lamtoro (TDL).
Profil asam amino esensial TI (g/16g N) TBK (g/16g N)
Makro & mikro mineral
Kalsium (%) 4,00 0,28 0,37 - 2,52 Sumber ; Hertrampf dan Pascual (2000)
amino essensial dibandingkan bungkil kedelai, walaupun masih jauh dari kandungan asam amino tepung ikan. Tepung daun lamtoro juga merupakan sumber vitamin A dengan kandungan β-karoten yang relatif tinggi serta kandungan xantofil yang merupakan sumber pigmentasi pada kulit dan kuning telur (Hertrampf dan Pascual 2000).
Pemanfaatan bahan baku pakan ikan nila dari daun tumbuhan khususnya daun lamtoro dibatasi dengan tingginya kandungan neutral detergent fiber (NDF) sebesar 39,5% dan acid detergent fiber (ADF) sebesar 35,10% (Garcia et al. 1996). Serat kasar merupakan komponen karbohidrat yang kaya akan lignin dan selulase yang sukar dicerna. Selulase merupakan kerangka sel tanaman yang terdiri dari rantai D-Glukosa dengan derajat polimerasi sebesar lebih kurang 14.000 (Schlegel 1994). Degradasi polisakarida yang terdapat pada dinding sel tanaman yang merupakan bagian terbesar komponen serat kasar yang kadarnya bervariasi bergantung kepada jaringan tanaman, jenis tanaman dan umur tanaman (Amin 1997). Pada manusia fungsi utama selulase adalah untuk menyediakan bahan bulky
(tidak dapat dicerna) yang dapat meningkatkan efisiensi kerja saluran pencernaan yang fungsinya dapat disamakan dengan fungsi serat dalam pakan ternak (Djojosoebagio dan Pilliang, 1996).
dapat memberikan pertumbuhan harian sebesar 2,2%, sedangkan pada kadar yang sama TDL yang tidak direndam memberikan pertumbuhan harian sebesar 1,1%. Penaflorida et al. (1992) menyatakan bahwa perendaman daun lamtoro selama 30 - 48 jam dapat menurunkan mimosin hingga 90%. Sedangkan penelitian Widyastuti (2001) menunjukkan bahwa ayam broiler yang ransum dasarnya dicampur TDL 10% dengan perlakuan pemanasan kering/oven pada suhu 70°C selama 12 jam memberikan respon pertumbuhan yang terbaik. Dinyatakan pula bahwa metode ini dinilai paling ekonomis dan mudah diterapkan dibanding pemanasan lembab atau penambahan komponen zat besi.
Selain mimosin bahan nutrien lain yang terkandung dalam TDL adalah mio-inositol heksakisfosfat (C6H18O24P6) yang umum disebut asam fitat mempunyai rumus kimia dan struktur cincin yang mirip dengan glukosa yang berikatan dengan fosfor untuk membentuk struktur asam fitat. Struktur asam fitat dapat dilihat pada Gambar 1 Asam fitat mempunyai struktur yang stabil dan mengandung kira-kira 2/3 fosfor tanaman dalam bentuk fosfor organik (Ravindran et al. 2000).
Gambar 1. Struktur molekul asam fitat (Ravindran et al. 2000)
kelompok terminal karboksil pada protein atau kelompok karboksil bebas dari residu aspartat dan glutamat dalam molekul protein (Cheryan 1980). Fitat dapat mengikat protein dan mineral di dalam digesta, sangat potensial untuk menghambat aktifitas enzim-enzim pencernaan seperti protease dan tripsin (Conrad et al. 1996). Penelitian lain menyatakan bahwa interaksi antara asam fitat dan protein akan menurunkan bioavailability protein pada legum (Davies 1982). Fosfor terikat fitat tidak dapat dimanfaatkan ternak dan terbuang dalam feses sehingga akan meningkatkan kandungan fosfor dalam tanah dan air. Mekanisme kerja asam fitat mengikat mineral dapat dilihat pada Gambar 2.
.
Gambar 2. Mekanisme asam fitat mengikat mineral (Cheryan 1980)
yaitu adalah Selenomona ruminantium (Yanke et al. 1998) dan yang terbaru adalah
Mitsuokella jalaludinii (Lan et al. 2002).
Gambar 3. Mekanisme hidrolisis fosfat oleh enzim fitase (Applegate et al. 2004).
2.3. Cairan Rumen sebagai Sumber Enzim
Perut hewan ruminansia terdiri atas rumen, retikulum, omasum dan abomasums (Gambar 4). Volume rumen pada ternak domba berkisar 10 liter. Rumen diakui sebagai sumber enzim pendegradasi polisakarida. Polisakarida dihidrolisis di rumen karena pengaruh sinergis dan interaksi dari komplek mikro-organisme, terutama sellulase dan xilanase (Trinci et al. 1994). Mikroorganisme terdapat pada cairan rumen (liquid phase) dan menempel pada digesta rumen.
Enzim yang aktif mendegradasi struktural polisakarida hijauan kebanyakan aktif pada mikro organisme yang menempel pada partikel pakan. Di dalam retikulo rumen terdapat mikrobia rumen yang terdiri atas protozoa dan bakteri yang berfungsi melaksanakan fermentasi untuk mensintesis asam amino, vitamin B-komplek dan vitamin K sebagai sumber zat makanan bagi hewan induk semang (Hungate 1966). Mikroba rumen dapat dibagi dalam tiga grup utama yaitu bakteri, protozoa dan fungi (Czerkawski 1986) Beberapa jenis bakteri yang dilaporkan oleh Hungate (1966) adalah : (a) bakteri pencerna selulosa (Bakteroidessuccinogenes, Ruminococcus flavafaciens, Ruminococcus albus, Butyrifibriofibrisolvens), (b) bakteri pencerna hemiselulosa (Butyrivibrio fibrisolvens,Bakteroides ruminocola, Ruminococcus sp), (c) bakteri pencerna pati (Bakteroides ammylophilus, Streptococcus bovis, Succinnimonas amylolytica, (d) bakteri pencerna gula (Triponema bryantii, Lactobasilus ruminus), (e) bakteri pencerna protein (Clostridium sporogenus, Bacillus licheniformis). Kehadiran fungi dalam rumen diakui sangat bermanfaat bagi pencernaan pakan serat, karena dia membentuk koloni pada jaringan selulosa pakan. Rizoid fungi tumbuh jauh menembus dinding sel tanaman sehingga pakan lebih terbuka untuk dicerna oleh enzim bakteri rumen. Protozoa rumen diklasifikasikan menurut morfologinya yaitu: holotrichs yang mempunyai silia hampir di seluruh tubuhnya dan mencerna karbohidrat yang fermentabel, sedangkan oligotrichs yang mempunyai silia sekitar mulut dan umumnya merombak karbohidrat yang lebih sulit dicerna (Arora, 1989).
Mikroba-mikroba rumen mensekresikan enzim-enzim pencernaan ke dalam cairan rumen untuk membantu mendegradasi partikel makanan. Enzim-enzim tersebut antara lain enzim yang mendegradasi substrat selulase yaitu selulase, hemiselulase/xylosa adalah hemiselulase/xylanase, pati adalah amilase, pektin adalah pektinase, lipid/lemak adalah lipase, protein adalah protease dan lain-lain (Kamra 2005). Aktivitas enzim dalam cairan rumen juga tergantung dari komposisi atau perlakuan makanan (Moharrery dan Das 2002). Agarwal et al.
persen rumput sampai umur 24 minggu, pada cairan rumennya didapatkan enzim carboxymethyl celulase dengan aktivitas enzim 3,60 µmol glukosa per jam per ml, alpha amilase 0,33 µmol glukosa per menit per ml, xylanase 0,29 µmol xylosa per menit per ml, beta-glukosidase 0,20 µmol p-nitrophenol per menit per ml, alpha-glukosidase 0,008 mol p-nitrophenol per menit per ml, urease 0,05 µmol NHs-N per menit per ml dan protease 452,7 µg hidrolisis protein per jam per ml. Martin
cairan rumen sapi dan aktivitas enzimnya disajikan pada Tabel 3 dan Tabel 4. Sedangkan pada Tabel 5 disajikan hasil penelitian Budiansyah (2010) tentang karakteristik enzim rumen sapi lokal yang mendapat makanan hijauan yang kaya serat.
Tabel 3. Komposisi enzim cairan rumen sapi1)
Enzim Lee et al. (2002)1 Agarwal et al
µmol glukosa/ jam /ml
11 83,7 ±20,39
µg hidrolisis protein
125,6 ±3,83
µg hidrolisis protein
452,7 ± 154,3 µg hidrolisis protein /j / l
Keterangan: 1) Sapi dewasa yang diberi makan ransum dasar alfalfa 2)
Anak domba dengan berat badan 23,5 kg yang diberi air susu sampai 8 minggu dan diteruskan dengan 50 persen konsentrat dan 50 persen rumput sampai umur 24 minggu Selulase -Fpase (ug glukosa / ml/ jam)
Tabel 4. Komposisi enzim cairan rumen domba1)
Enzim Cairan Rumen Tanpa Protozoa
Keterangan1) Sumber : Moharrery dan Das (2002).
Tabel 5. Karakteristik enzim-enzim cairan rumen sapi asal RPH Parameter Enzim-enzim cairan rumen
Selulase Amilase Fitase Protease
Kisaran pH pH 4 – 9 pH 6 - 9 pH 4 - 9 pH 5 - 9 Sapi impor
Suhu 39 oC 50 oC 39 oC 70 oC Kisaran Suhu 29-50 oC 50 oC 29-50 oC 39-70 oC
pH optimum pH 4 pH 7 pH 6 pH 7
Kisaran pH pH 4 – 9 pH 6 - 9 pH 4 - 9 pH 4 - 9
Kohn dan Alien (1994) menggunakan enzim protease dari ekstrak cairan rumen sapi untuk mengukur laju degradasi protein bungkil kedelai dan hay lucerne. Enzim protease hasil ekstraksi dengan butanol dan aseton hanya tersisa 62 persen aktivitasnya dibanding cairan rumen awal. Tidak ada perbedaan antara taraf enzim 3, 5 atau 10 ml dalam mendegradasi protein pakan. Protein bungkil kedelai terdegradasi dengan kecepatan 0,15 mg per gram per jam pada 2 jam pertama dan turun menjadi 0,01 mg per gram per jam dari 8 sampai 24 jam berikutnya. Kejadian yang sama juga terjadi pada protein hay lucerne, degradasi protein dengan kecepatan 0,06 mg per gram per jam pada 2 jam pertama dan turun menjadi 0,01 mg per gram per jam dari 8 sampai 24 jam berikutnya. Laju degradasi protein pakan lebih rendah dari yang diukur sebelumnya dengan menggunakan mikroba hidup. Penggunaan cairan rumen sapi sebagai sumber enzim kasar telah dicobakan ke dalam ransum unggas berbasis wheat pollard dengan adanya perbaikan terhadap performa ayam broiler (Pantaya et al. 2005). Budiansyah (2010) melaporkan pula bahwa performa ayam broiler yang lebih baik dengan penambahan 0,5 % enzim cairan rumen sapi dalam ransum.
2.4. Enzim Pencernaan dan Perannya dalam Proses Pencernaan.
adanya enzim perncernaan seperti protease, karboksilase dan lipase (Zonneveld
et al. 1991).
Kecernaan didefinisikan sebagai bagian pakan yang diserap oleh hewan (Lovell 1988). Pengetahuan tentang kecernaan bahan pakan sangat diperlukan dalam mempelajari kebutuhan energi ikan dan penilaian dari berbagai bahan pakan yang berbeda. Selama pakan berada dalam usus ikan, nutrient yang dicerna oleh berbagai enzim menjadi bentuk yang dapat diserap oleh dinding usus dan masuk ke dalam sistem peredaran darah. Kecernaan ikan terhadap bahan baku pakan dipengaruhi oleh beberapa faktor yaitu, sifat kimia air, suhu air, jenis pakan, ukuran, umur ikan, kandungan gizi pakan, frekuensi pemberian pakan, sifat fisika dan kimia pakan serta jumlah dan macam enzim pencernaan yang terdapat dalam saluran pencernaan pakan (NRC 1993; Tillman et al. 1991; Hepher 1990).
Enzim adalah katalisator biologis dalam reaksi kimia yang sangat dibutuhkan dalam kehidupan. Enzim adalah protein, yang disintesis dalam sel dan dikeluarkan dari sel yang membentuknya melalui proses eksositosis. Enzim yang disekresikan ke luar sel digunakan untuk pencernaan di luar sel (di dalam rongga pencernaan) atau disebut "extra cellular digestion", sedangkan enzim yang dipertahankan dalam sel digunakan untuk pencernaan dalam sel itu sendiri atau disebut "intra celuller digestion" (Affandi
el at. 1992). Enzim pencernaan yang disekresikan dalam rongga pencernaan berasal dari sel-sel mukosa lambung, pilorik kaeka, pankreas dan mukosa usus (Halver dan Hardy 2002).
dan lipase. Ikan yang tidak memiliki lambung dan pilorik kaeka, aktivitas proteolik terutama berasal dari cairan pankreatik. (Watford dan Lam 1993 ).
Kecernaan (digestibility) dipengaruhi oleh tiga faktor yaitu (1) jenis pakan yarg dimakan dan kadar kepekaan pakan terhadap pengaruh enzim pencernaan, (2) aktivitas enzim-enzim pencernaan dan (3) lama waktu pakan yang dimakan terkena aksi enzim pencernaan. Masing-masing faktor di atas dipengaruhi oleh berbagai faktor sekunder yang berkaitan dengan ikan itu sendiri (spesies, umur, ukuran) dan kondisi fisiologis, yang berkaitan dengan lingkungan (temperatur), dan yang berkaitan dengan pakannya (komposisi pakan, ukuran partikel dan jumlah pakan yang dimakan). Kecernaan berbeda antar spesies ikan, hal ini terjadi akibat perbedaan sistem dan enzim-enzim pencernaan (De Silva dan Anderson 1995).
Kemampuan ikan dalam mencerna makanan sangat bergantung pada kelengkapan organ pencernaan dan ketersediaan enzim pencernaan. Perkembangan saluran pencenaan tersebut berlangsung secara bertahap dan setelah mencapai ukuran/umur tertentu saluran pencernaan mencapai kesempurnaan. Perkembangan struktur alat pencernaan ini diikuti oleh perkembangan enzim pencernaan dan perubahan kebiasaan makan (food habit). Kandungan nutrien pakan nampaknya berpengaruh pada aktivitas enzim pencernaan. Kuzmina (1996) mengungkapkan bahwa tersedianya substrat merupakan faktor yang nyata dalam pengaturan aktivitas enzim pada ikan dan mamalia. Kandungan protein pakan yang tinggi dikaitkan dengan kandungan selulase yang rendah dapat meningkatkan aktivitas protease pada ikan rainbow trout . Peningkatan proporsi pati kentang dalam pakan dari 10 menjadi 90% yang diikuti penurunan proporsi tepung ikan akan meningkatkan aktivitas enzim maltase dan amilase pada ikan mas (Hepher 1990).
diberi pakan dari makanan yang mengandung tetrasiklin. Pemanfaatan daun lamtoro sangat dibatasi oleh kecernaan ikan yang terbatas terhadap jenis dedaunan ini. Hal ini berkaitan dengan ketersediaan enzim selulotik yang terbatas dalam saluran pencernaan ikan. Beberapa penelitian telah melaporkan bahwa ikan tidak memiliki enzim selulase dan kemungkinan adanya populasi mikroba selulotik di saluran pencernaan ikan juga masih menjadi kontroversi di kalangan peneliti (Stickney dan Shumway 1974; Prejs dan Blaszczyk 2006; Linsday dan Harris 1980; Lessel dan Lesel 1986; Luczkovich dan Stellway 1993; Saha dan Ray 1998). Kontrofersi tersebut terbantahkan dengan penelitian Prejs dan Blaszczyk 2006; Donovan dan Rosalie 2009; Li et al. 2004; Nibedita dan Koushik 2008 yang mendapatkan aktifitas enzim selulase pada saluran pencernaan ikan.
Enzim protease menguraikan rantai-rantai peptida dari protein. Peptidase diklasifikasikan menjadi endopeptidase dan eksopeptidase yang bergantung pada letak ikatan peptida pada tengah atau akhir molekul. Endopeptidase menghidrolisis protein dan peptida-peptida rantai panjang menjadi peptida-peptida pendek. Endopeptidase penting antara lain pepsin yang dihasilkan dari zimogen pepsinogen, tripsin dari tripsinogen, dan kimotripsin dari kimotripsinogen. Eksopeptidase menghidrolisis peptida menjadi asam-asam amino. Karboksipeptidase, aminopeptidase, dan dipeptidase termasuk dalam kelompok eksopeptidase. Alfa-amilase adalah enzim yang bertanggung jawab menghidrolisis pati menjadi glukosa. Enzim ini memutuskan ikatan 1,4-α -glukosidik dan mengubah pati menjadi glukosa dan maltosa. Lipase adalah enzim penting dalam pencemaan lemak. Lipase memecah lemak menjadi gliserol dan asam lemak (Steffens 1989; Hepher 1990).
III. METODOLOGI
Penelitian dilakukan dalam tiga tahap.
Tahap Pertama : Pengujian aktifitas enzim-enzim hidrolisis pada ekstrak enzim cairan rumen domba
Tahap kedua : Pengaruh penambahan ekstrak enzim cairan rumen domba (in vitro) terhadap kualitas tepung daun lamtoro (TDL).
Tahap ketiga : Efektifitas pemanfaatan TDL terhidrolisis (predigestion) dalam pakan buatan untuk ikan nila serta pengaruhnya pada perubahan aktifitas enzim pencernaan dan metabolisme nutrien.
3.1. Tahap Pertama
Pengujiaan Aktifitas Enzim-enzim Hidrolisis Cairan Rumen Domba
Pada percobaan ini sasaran yang ingin dicapai adalah mendapatkan eksrak enzim cairan rumen domba yang dipelihara dengan pakan hijauan, dan menguji diuji aktifitas enzim selulase, fitase, amilase dan protease. Data aktifitas enzim yang didapatkan akan menjadi dasar perhitungan jumlah enzim yang ditambahkan pada substrat TDL.
3.1.1. Isolasi dan Produksi Ekstrak Enzim Cairan Rumen Domba.
3.1.2. Uji Aktifitas Ekstrak Enzim Cairan Rumen Domba
Ekstrak cairan rumen domba yang telah dilarutkan dalam cairan buffer phosfat dengan perbandingan 1 : 1, selanjutkan akan diuji kandungan aktifitas enzim selulase, amilase, protease dan lipase. Uji aktifitas enzim selulase/FP-ase dilakukan menurut metode Ghosse, (1987) dengan prosedur kerja pada Lampiran 1, aktifitas enzim amilase dan enzim protease dilakukan menurut metode Bergmeyer dan Grassi (1983) dengan prosedur kerja pada Lampiran 2 dan 3. aktifitas enzim lipase dilakukan menurut metode Tietz dan Friedreck dalam Barlongan, (1990) dengan prosedur kerja pada Lampiran 4 dan aktifitas enzim fitase dilakukan menurut metode Greiner et al. (1997) dengan prosedur kerja pada Lampiran 5.
3.2. Tahap Kedua
Pada percobaan tahap kedua, sasaran yang ingin dicapai adalah untuk mendapatkan informasi kualitas TDL yang mendapat perlakuan dengan penambahan ekstrak enzim cairan rumen domba dengan taraf dosis dan waktu inkubasi yang berbeda. TDL dengan kualitas terbaik selanjutnya akan dievaluasi pada pengujian in vitro untuk bahan campuran pakan ikan nila.
3.2.1. Pengaruh penambahan enzim cairan rumen domba (in vitro) terhadap kualitas tepung daun lamtoro
Penelitian dilakukan di Laboratorium Nutrisi Ternak Perah Fakultas Peternakan Institut Pertanian Bogor, untuk menguji pengaruh penambahan enzim cairan rumen domba dengan taraf dosis dan waktu inkubasi yang berbeda terhadap kualitaas TDL.
2 jam dan 24 jam pada suhu kamar (28oC) pH 7,2. Perlakuan yang diberikan adalah sebagai berikut :
Perlakuan K : Pelakuan kontrol tanpa penambahan enzim, hanya ditambahkan air sebanyak volume enzim tertinggi
Perlakuan A : Penambahan enzim cairan rumen 20 ml/kg TDL Perlakuan B : Penambahan enzim cairan rumen 40 ml/kg TDL Perlakuan C : Penambahan enzim cairan rumen 60 ml/kg TDL Perlakuan D : Penambahan enzim cairan rumen 80 ml/kg TDL Perlakuan E : Penambahan enzim cairan rumen 100 ml/kg TDL
Komposisi proksimat TDL sebelum diinkubasi dengan enzim kasar dapat dilihat pada Tabel 6 berikut.
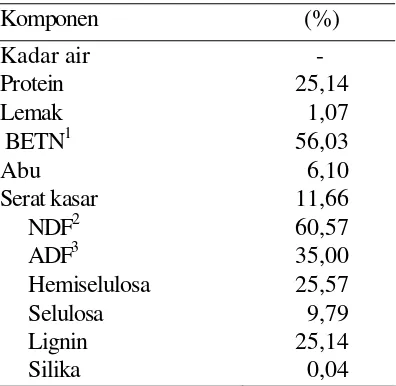
Tabel 6. Komposisi proksimat TDL dan komponen penyusun serat kasar TDL (berat kering).
Komponen (%)
Kadar air -
Protein 25,14 Lemak 1,07 BETN1 56,03
Abu 6,10
Serat kasar 11,66 NDF2 60,57 ADF3 35,00 Hemiselulosa 25,57 Selulosa 9,79 Lignin 25,14 Silika 0,04 1
Bahan ekstrak tanpa nitrogen; 2Neutral detergent fiber; 3Acid detergent fiber;
Prosedur yang digunakan untuk pengujian kadar glukosa terlarut adalah menurut Wedemeyer dan Yasutake (1977) dengan prosedur kerja pada Lampiran 6, kadar protein terlarut menurut Bradford (1976) dengan prosedur kerja pada Lampiran 7 dan analisa proksimat, yang mencakup kadar protein, lemak, serat kasar, abu menurut metode dari AOAC (1990) dengan prosedur kerja pada Lampiran 8, analisa NDF dan ADF menurut metode Van Soest et al. (1991) dengan prosedur kerja pada Lampiran 9 dan asam fitat menurut metode dari AOAC 1990 dengan prosedur kerja pada Lampiran 10. Perlakuan yang terbaik selanjutnya akan dianalisa komposisi asam amino dengan metode HPLC dengan prosedur kerja pada Lampiran 11.
3.3. Tahap Ketiga
3.3.1.Eskperimen 1. Efektifitas pemanfaatan TDLterhidrolisis (predigestion) dalam pakan formulasi untuk ikan nila.
Percobaan ini bertujuan untuk mengkaji efektifitas pemanfaatan TDL terhidrolisis sebagai sumber protein nabati pakan formulasi untuk ikan nila serta pengaruhnya pada aktifitas pencernaan dan metabolisme nutrien. Nilai konsentrasi ekstrak enzim dan lama inkubasi yang digunakan adalah perlakuan yang memberikan hasil terbaik yang didapat dari penelitian tahap 2, yaitu 100ml/kg TDL.
Penelitian dilaksanakan pada bulan Agustus sampai dengan bulan Oktober 2009. Analisa proksimat bahan baku dan pakan uji, pembuatan pakan serta pemeliharaan ikan dilakukan di Laboratorium Nutrisi Ikan, pengujian kualitas air dilakukan di Laboratorium Lingkungan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor
Komposisi pakan perlakuan disajikan pada Tabel 7, dan komposisi proksimat pakan dan kandungan energi pakan percobaan disajikan pada Tabel 8.
Benih ikan nila sebanyak 400 ekor bobot tubuh 7-10 g dipelihara dalam tank ukuran 200 liter untuk aklimatisasi. Selama masa aklimatisasi ikan diberikan pakan komersil. Setelah 1 minggu, sebanyak 144 ekor ikan yang relatif seragam dibagi dalam 18 akuarium berukuran 50x35x40 cm yang terhubung dengan sistem resirkulasi, dengan padat tebar 8 ekor/akuarium dan bobot awal rata-rata 9,38 ± 0,41 gram. Aerasi diberikan pada setiap akuarium serta tandon, sedangkan heater hanya dipasang pada tandon. Sebelum perlakuan, ikan dipuasakan terlebih dahulu selama 24 jam dengan tujuan menghilangkan sisa pakan dalam saluran pencernaan selama masa aklimatisasi.
Tabel 7. Komposisi bahan pakan perlakuan
Perlakuan (% TDLt) Jenis bahan baku
(%) K (0) A (10) B (15) C (20) D (25) E (30)
Tepung Ikan 15,00 15,00 15,00 15,00 15,00 15,00
T.lamtoro gung 0,00 10,00 15,00 20,00 25,00 30,00
T. Bungkil Kedelai 23,00 22,60 20,60 19,60 16,60 13,60
DDGS1 24,00 20,00 19,00 17,00 15,00 15,00
Tepung Pollard 28,03 22,43 20,43 18,43 18,43 16,43
Tepung Sagu 2,00 2,00 2,00 2,00 2,00 2,00
Minyak Jagung 1,00 1,00 1,00 1,00 1,00 1,00
Minyak Ikan 2,00 2,00 2,00 2,00 2,00 2,00
Vit.Mix (tanpa vit c) 0,20 0,20 0,20 0,20 0,20 0,20
Mineral Mix4 0,20 0,20 0,20 0,20 0,20 0,20
Kromium-ragi 3,00 3,00 3,00 3,00 3,00 3,00
Vit C 1,00 1,00 1,00 1,00 1,00 1,00
Choline chloride 0,50 0,50 0,50 0,50 0,50 0,50
Lysin+metionin (1:1) 0,07 0,07 0,07 0,07 0,07 0,07
GE (kkal/g)2 3897,34 3869,97 3853,78 3837,54 3814,92 3759,33 C/P (kkal/g)3 13,68 13,39 13,44 13,40 13,64 13,47
1
Dried Distillers Grains with Solubles 2
GE (Gross energy) adalah energi yang terkandung dalam bahan pakan berdasarkan nilai ekuivalen untuk Karbohidrat 4.1 kcal/g (17.2 kJ/g), lemak 9.5 kcal/g (39.8 kJ/g), dan protein 5.6 kcal/g (23.4 kJ/g)
3
C/P adalah kkal GE per gram protein 4
Tabel 8. Komposisi proksimat pakan perlakuan TDL terhidrolisis (TDLt)
Pakan perlakuan (% TDLt) Komposisi
proksimat (%) K (0) A (10) B (15) C (20) D (25) E (30)
Protein 31,12 29,43 32,90 34,03 32,29 29,60
Lemak 8,79 8,21 9,38 9,26 9,35 9,55
Abu 9,73 9,82 9,71 9,05 10,13 8,91
Serat Kasar 6,03 5,97 5,56 4,78 5,81 5,83
BETN1 36,08 39,38 33,39 34,35 33,09 37,12
GE (kkal/gr)2 4061,53 4042,61 4102,49 4193,73 4053,18 4086,77 C/P (kkal/gr)3 13,02 13,74 12,47 12,32 12,55 13,81
1
BETN = Bahan Ekstrak Tanpa Nitrogen
2 GE (Gross energy) adalah energi yang terkandung dalam bahan pakan berdasarkan nilai ekuivalen untuk Karbohidrat 4.1 kcal/g (17.2 kJ/g), lemak 9.5 kcal/g (39.8 kJ/g), dan protein 5.6 kcal/g (23.4 kJ/g)
3
C/P adalah kkal GE per gram protein
Ikan dipelihara selama 50 hari dan diberi pakan secara at satiation dengan frekuensi 3 kali sehari (07.00; 12.00 dan 17.00 WIB). Untuk mempertahankan kualitas air, setiap hari dilakukan penyiponan dan penggantian sebagian air pada tandon. Faktor kualitas air yang diperhatikan adalah suhu yang diamati setiap pagi hari sebelum pemberian pakan serta pengukuran pH, alkalinitas, kesadahan, TAN dan DO di awal dan di tengah periode pemeliharaan. Rancangan yang digunakan dalam penelitian adalah Rancangan Acak Lengkap (RAL) dengan 6 perlakuan pakan dan 3 ulangan.
Peubah yang diamati adalah : (1) Laju pertumbuhan harian (LPH), (2) jumlah konsumsi pakan (JKP), (3) efisiensi pakan (EP); (4) retensi protein, (5) retensi lemak; (6) hepatosomatik indeks (7) glikogen hati; (8) aktifitas enzim di saluran pencernaan (9) kadar glukosa darah; (10) histologi hati dan usus.
(1) Laju Pertumbuhan Harian
Nilai laju pertumbuhan harian dihitung dengan metode Huissman (1976) dengan menggunakan rumus :
Wt = bobot rata-rata ikan pada waktu t (g) Wo = bobot rata-rata ikan pada waktu awal (g) α = laju pertumbuhan harian (%)
t = waktu pemeliharaan (hari) (2) Jumlah Konsumsi Pakan.
Adalah jumlah total pakan dalam gram yang dikonsumsi ikan selama masa pemeliharaan.
(3). Efisiensi Pakan
Efisiensi pakan (EP) dianalisis berdasarkan rumus efisiensi pakan Takeuchi (1988), dengan rumus :
(Wt + WQ)-W0
X 100 % EP =
F Dimana :
EP = Efisiensi pakan (%)
W0 = Bobot ikan pada awal penelitian (g) Wt = Bobot ikan pada waktu t (g)
Wa = Bobot ikan yang mati selama penelitian (g)
F = Bobot pakan yang dikonsumsi selama penelitian (g)
(4). Retensi Protein
Retensi protein dapat diketahui dengan melakukan analisis proksimat protein tubuh ikan pada awal dan akhir percobaan, mengikuti metode (AOAC 1990). Rumus penghitungan retensi protein adalah :
(
)
% 100 x P
lp Fp
RP= −
Dimana :
(5). Retensi Lemak
Retensi lemak dapat diketahui dengan melakukan analisis proksimat lemak tubuh ikan pada awal dan akhir percobaan, mengikuti metode (AOAC 1990). Rumus penghitungan retensi lemak adalah :
(
)
% 100 x L
ll Fl
RL= −
Dimana :
Fl = jumlah lemak tubuh ikan pada waktu akhir pemeliharaan (g) ll = jumlah lemak tubuh ikan pada waktu awal pemeliharaan (g) L = jumlah lemak yang dikonsumsi ikan selama pemeliharaan (g)
(6). Hepatosomatik Indeks (HIS) Bobot hati (g)
HIS (%) = ————————— x 100 % Bobot tubuh (g)
(7). Glikogen Hati
Kadar glikogen pada hati dan otot dianalisis mengikuti metode Wedemeyer dan Yasutake (1977). Prosedur analisa glikogen hati dijelaskan pada Lampiran 12.
(8). Aktifitas Enzim Pencernaan
Analisis enzim pencernaan dilakukan pada ikan kontrol dan ikan yang mendapat perlakuan.. Analisa meliputi aktifitas selulase (Ghosse 1987) prosedur kerja pada Lampiran 1, protease dan amilase (Bergmeyer dan Grassi 1983) prosedur kerja pada Lampiran 2 dan 3. Sedangkan prosedur memperoleh ekstrak enzim saluran pencernaan untuk analisis enzim pencernaan dijelaskan pada Lampiran 13.
(9). Kadar Glukosa darah (Wedemeyer dan Yasutake, 1977).
(10 ). Histologi hati dan saluran pencernaan
Histologi ini diperlukan untuk memberikan gambaran tentang kondisi hati dan saluran pencernaan ikan pada setiap perlakuan. Prosedur pembuatan preparat histologi hati dan saluran pencernaan dijelaskan pada Lampiran 14.
Analisis data
Data yang diperoleh kemudian ditabulasi dengan program Exel MS. Office 2007 dan untuk uji ANOVA dianalisis menggunakan program SPSS 15.0. Perlakuan yang berbeda nyata dilanjutkan dengan uji lanjut Duncan. Histologi usus dan hati serta profil kadar gula darah beberapa waktu setelah makan, dilakukan analisa secara deskriptif.
3.3.2.Eksperimen 2. Efektifitas pemanfaatan TDL tanpa hidrolisis dalam pakan formulasi untuk ikan nila.
TDL yang digunakan dalam komposisi pakan adalah TDL tanpa perlakuan hidrolisis dengan ekstrak enzim rumen domba. Komposisi pakan digunakan adalah komposisi yang sama dengan penelitian yang menggunakan TDL terhidrolisis (Tabel 7). Analisa proksimat pakan perlakuan disajikan pada Tabel 9. Proses aklimatisasi dan kegiatan yang dilakukan selama pemeliharaan ikan uji sama dengan penelitian dengan menggunakan TDL terhidrolisis. Rancangan penelitian yang digunakan sama dengan penelitian sebelumnya. Perlakuan yang diberikan adalah perbedaan persentase kandungan TDL dalam pakan yaitu perlakuan F (10% TDL), G (15% TDL), H (20% TDL), I (25% TDL) dan J (30% TDL).
Analisa data
Data yang diperoleh kemudian ditabulasi dengan program Exel MS. Office 2007 dan untuk uji ANOVA dianalisis menggunakan program SPSS 15.0. Perlakuan yang berbeda nyata dilanjutkan dengan uji lanjut Duncan.
Tabel 9. Komposisi proksimat pakan perlakuan TDL tanpa hidrolisis
Pakan perlakuan (% TDL) Komposisi
proksimat (%) F (10) G (15) H (20) I (25) J (30)
Protein 26,89 27,79 28,03 28,91 28,96
Lemak 8,36 8,98 9,19 9,20 9,19
Abu 9,80 9,89 9,76 9,97 9,95
Serat Kasar 9,27 9,56 9,78 10,11 10,83
BETN1 36,27 37,43 36,57 36,29 38,11
GE (kkal/gr)2 3787,11 3943,97 3942,10 3980,85 4057,32 C/P (Kkal/gr)3 14,08 14,19 14,06 13,77 14,01
1
BETN = Bahan Ekstrak Tanpa Nitrogen
2 GE (Gross energy) adalah energi yang terkandung dalam bahan pakan berdasarkan nilai ekuivalen untuk Karbohidrat 4.1 kcal/g (17.2 kJ/g), lemak 9.5 kcal/g (39.8 kJ/g), dan protein 5.6 kcal/g (23.4 kJ/g)
3
IV. HASIL DAN PEMBAHASAN
4.1. Tahap 1.
Pengujiaan Aktifitas Enzim-enzim Hidrolisis pada Ekstrak Enzim Cairan Rumen Domba
Hasil pengukuran aktifitas amilase, protease, lipase, selulase dan fitase pada cairan rumen domba disajikan pada Gambar 5. Data pengukuran aktifitas enzim dari dua puluh satu sampel eksrak enzim kasar cairan rumen domba terdapat pada Lampiran 15. Aktifitas selulase lebih besar dari aktifitas enzim lainnya dengan urutan dari nilai aktivitas terbesar berturut-turut adalah selulase (1,66 ± 0,19 IU/ml/menit); amilase (1,32± 0,02 IU/ml/menit); fitase (0,27 ± 0,13 IU/ ml/menit); protease (0,26 ± 0,07 IU/ml/menit); lipase (0,01 ± 0,00 IU/ml/menit).
Ket. Subsrat yang digunakan: uji selulosa (kertas saring); uji amilase (pati); uji protease (kasein); uji lipase (minyak zaitun); uji fitase (asam fitat)
Gambar 5. Aktifitas enzim selulase, amilase, protease, lipase dan fitase ekstrak cairan rumen domba.