SINTESIS BUTIL DIKLOFENAK DAN
ELUSIDASI STRUKTUR MENGGUNAKAN
FOURIER TRANSFORM INFRA RED (FT-IR) DAN
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
SKRIPSI
Diajukan untuk mUnivers
itas Sumatera Uta
Diajukan sebagi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DEVI NURIANTI
NIM 121524113
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
SINTESIS BUTIL DIKLOFENAK DAN
ELUSIDASI STRUKTUR MENGGUNAKAN
FOURIER TRANSFORM INFRA RED (FT-IR) DAN
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
SKRIPSI
Diajukan untuk mUnivers
itas Sumatera Uta
Diajukan sebagi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DEVI NURIANTI
NIM 121524113
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
SINTESIS BUTIL DIKLOFENAK DAN
ELUSIDASI STRUKTUR MENGGUNAKAN
FOURIER TRANSFORM INFRA RED (FT-IR) DAN
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
OLEH:
DEVI NURIANTI
NIM 121524113
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 27 Maret 2015
Disetujui oleh:
Pembimbing I, Panitia Penguji,
Drs. Ismail, M.Si., Apt. Prof. Dr. Ginda Haro, M.Sc., Apt. NIP 195006141980031001 NIP 195108161980031002
Drs. Ismail, M.Si., Apt.
Pembimbing II, NIP 195006141980031001
Drs. Nahitma Ginting, M.Si., Apt. Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195406281983031002 NIP 195201041980031002
Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Medan, April 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I
iv
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah memberikan karunia
yang berlimpah sehingga penulis dapat menyelesaikan penelitian dan penyusunan
skripsi yang berjudul “Sintesis Butil Diklofenak dan Elusidasi Struktur
Menggunakan Fourier Transform Infra Red (FT-IR) dan Gas Chromatography
Mass Spectrometry (GC-MS)”. Skripsi ini diajukan sebagai salah satu syarat
untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan
terima kasih kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi Universitas Sumatera Utara dan Ibu Prof. Dr. Julia Reveny,
M.Si., Apt., selaku Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara
yang telah menyediakan fasilitas kepada penulis selama masa perkuliahan. Penulis
juga mengucapkan terima kasih kepada Bapak Drs. Ismail, M.Si., Apt., dan
Bapak Drs. Nahitma Ginting, M.Si., Apt., yang telah meluangkan waktu dan
tenaga dalam membimbing penulis dengan penuh kesabaran dan tanggung jawab,
memberikan petunjuk dan saran-saran selama penelitian hingga selesainya skripsi
ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Prof. Dr. Ginda
Haro, M.Sc., Apt., selaku ketua penguji, Bapak Drs. Fathur Rahman Harun, M.Si.,
Apt., dan Ibu Dra. Tuty Roida Pardede, M.Si., Apt., selaku anggota penguji yang
telah memberikan saran untuk menyempurnakan skripsi ini, dan Ibu Dra. Suwarti
v
pengajar Fakultas Farmasi Universitas Sumatera Utara yang telah banyak
membimbing penulis selama masa perkuliahan hingga selesai.
Penulis juga mempersembahkan rasa terima kasih yang tak terhingga
kepada orang tua tercinta, Ayahanda Muhammad Nur dan Ibunda Mariati atas
limpahan kasih sayang, doa yang tulus, nasehat dan dukungan baik moril maupun
materil, untuk teman-teman Ekstensi Sarjana Farmasi Tahun 2012 serta semua
pihak atas motivasi dan segala bantuan dalam penyelesaian skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum
sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang
membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, April 2015 Penulis,
vi
SINTESIS BUTIL DIKLOFENAK DAN
ELUSIDASI STRUKTUR MENGGUNAKAN
FOURIER TRANSFORM INFRA RED (FT-IR) DAN
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
ABSTRAK
Diklofenak adalah golongan AINS yang dikembangkan secara khusus sebagai obat antiradang. Pemberian jangka panjang obat ini dapat memberikan beberapa efek samping yang tidak diinginkan seperti tukak dan iritasi lambung. Merancang pro-drug adalah satu dari beberapa strategi untuk mengatasi masalah ini. Pro-drug dalam penelitian ini dibuat dalam bentuk ester yaitu butil diklofenak. Penelitian ini bertujuan untuk mengetahui sintesis dan karakteristik butil diklofenak.
Butil diklofenak dibuat melalui esterifikasi asam diklofenak dengan dry buthanol dengan bantuan katalis asam sulfat. Asam diklofenak diperoleh melalui reaksi antara kalium diklofenak dengan HCl 2Nyang dikarakterisasi dengan uji FT-IR. Hasil sintesis diuji kemurniannya dengan uji titik lebur kemudian dianalisis menggunakan FT-IR dan GC-MS.
Hasil FT-IR asam diklofenak menunjukkan terjadinya perubahan gugus OH karboksilat yang spseifik di bilangan gelombang 2989,66 cm-1; 2885,51 cm-1; 2681,05 cm-1; dan 2573,04 cm-1. Hasil uji titik lebur butil diklofenak menunjukkan bahwa butil diklofenak mempunyai titik lebur 110 - 113oC. Hasil FT-IR menunjukkan sudah terjadinya perubahan gugus O-H asam menjadi gugus CH2CH3 pada bilangan gelombang 1496,76 cm-1 dan 1450,47 cm-1. Hasil GC-MS
menunjukkan telah terbentuknya 49,61% butil diklofenak.
Berdasarkan hasil penelitian yang dilakukan bahwa asam diklofenak dapat diesterifikasi membentuk butil diklofenak dan karakteristik butil diklofenak dapat diperoleh dengan uji titik lebur, FT-IR dan GC-MS.
vii
SYNTHESIS OF BUTHYL DICLOFENAC AND
STRUCTURE ELUCIDATION USING
FOURIER TRANSFORM INFRA RED (FT-IR) AND
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
ABSTRACT
Diclofenac is a NSAID group which was developed specifically as anti-inflammatory drugs. Prolonged the administration of this drug can inhibit some the side effects such as peptic ulcer and irritation in stomach. Design a pro drug is one of several strategies to overcome this problem. In this study, the pro drug is made as an ester that is buthyl diclofenac. The purpose of this study was to know the synthesis and the characteristics of buthyl diclofenac.
Buthyl diclofenac was made by esterification of diclofenac acid with dry buthanol and sulphuric acid as a catalyst. Diclofenac acid was obtained by potassium diclofenac reaction with HCL 2N that was characterized by FT-IR test. The purity of the result of buthyl diclofenac synthesis was seen by melting point test and then analyzed using FT-IR and GC-MS.
The result of FT-IR showed that there were functional group changing became OH of carboxylic in 2989.66 cm-1, 2885.51 cm-1, 2681.05 cm-1, dan 2573,04 cm-1. The result of buthyl diclofenac melting point test were 110 – 1130C. The result of FT-IR test showed there had alteration of O-H functional group became CH2CH3 in 1496.6 cm-1 and 1450.47 cm-1. The result of GC-MS
showed that 49.61% buthyl diclofenac had been formed.
Based on the results of research show that diclofenac acid can be esterificated to form buthyl diclofenac and characteristics of buthyl diclofenac can be obtained by melting point test, FT-IR and GC-MS.
viii DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... v
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Diklofenak ... 5
2.1.1 Kalium diklofenak ... 5
2.1.2 Asam diklofenak ... 6
2.1.3 Diskoneksi asam diklofenak ... 7
ix
2.1.5 Efek farmakologi ... 8
2.1.6 Efek samping ... 9
2.2 Esterifikasi ... 9
2.3 Rekristalisasi ... 10
2.4 Spektrofotometri Inframerah ... 11
2.4.1 Prinsip ... 13
2.4.2 Spektrofotometer FT-IR ... 13
2.5 Kromatografi Gas (Gas Chromatography) ... 14
2.5.1 Prinsip kromatografi gas ... 14
2.5.2 Sistem peralatan kromatografi gas ... 15
2.5.2.1 Fase gerak ... 15
2.5.2.2 Tempat pemasukan sampel (injektor) ... 16
2.5.2.3 Kolom dan fase diam ... 16
2.5.2.4 Detektor ... 16
2.5.2.5 Komputer ... 17
2.6 Spektrometri Massa (Mass Spectrometry) ... 17
2.6.1 Prinsip ... 18
BAB III METODE PENELITIAN ... 19
3.1 Alat dan Bahan ... 19
3.1.1 Alat-alat ... 19
3.1.2 Bahan-bahan ... 20
3.2 Pengambilan Bahan Baku ... 20
3.3 Pembuatan Pereaksi ... 20
x
3.3.2 Pembuatan larutan Na2CO3 5% ... 20
3.3.3 Pembuatan HCl 2N . ... 20
3.3.4 Pembuatan dry ethanol ... 21
3.3.5 Pembuatan dry buthanol ... 21
3.4 Pengubahan Kalium Diklofenak ... 21
3.5 Pencucian Asam Diklofenak ... 22
3.6 Pemurnian Asam Diklofenak ... 22
3.7 Uji Titik Lebur Asam Diklofenak ... 22
3.8 Sintesis Butil Diklofenak ... 22
3.9 Pemurnian Hasil Sintesis ... 23
3.10 Uji Titik Lebur Hasil Sintesis ... 23
3.11 Elusidasi Struktur dengan FT-IR ... 24
3.12 Elusidasi Struktur dengan GC-MS ... 24
BAB IV HASIL DAN PEMBAHASAN ... 25
4.1 Hasil Pengubahan Kalium Diklofenak ... 25
4.2 Hasil Uji Titik Lebur Asam Diklofenak ... 25
4.3 Hasil Uji Asam Diklofenak dengan FT-IR ... 26
4.4 Hasil Sintesis Butil Diklofenak ... 28
4.5 Hasil Uji Titik Lebur Butil Diklofenak ... 29
4.6 Hasil Uji Butil Diklofenak dengan FT-IR ... 29
4.7 Hasil Uji Butil Diklofenak dengan GC-MS ... 31
xi
BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 37
xii
DAFTAR TABEL
Tabel Halaman
2.1 Frekuensi regangan IR ... 12
4.1 Identifikasi gugus fungsi spektrum inframerah asam diklofenak ... 27
4.2 Identifikasi gugus fungsi spektrum inframerah butil
xiii
DAFTAR GAMBAR
Gambar Halaman
2.1 Mekanisme reaksi esterifikasi suasana asam ... 10
2.2 Komponen utama dalam FT-IR ... 13
2.3 Diagram skematik kromatograf gas ... 15
2.4 Diagram blokspektrometri massa ... 18
4.1 Mekanisme reaksi pengubahan kalium diklofenak menjadi asam diklofenak ... 25
4.2 Spektrum inframerah asam diklofenak ... 26
4.3 Spektrum inframerah kalium diklofenak ... 26
4.4 Spektrum inframerah butil diklofenak ... 29
4.5 Kromatogram butil diklofenak hasil GC ... 31
4.6 Spektrum massa puncak butil diklofenak dengan Rt 25,041 menit ... 32
4.7 Fragmentasi spektrum massa puncak butil diklofenak ... 33
4.8 Fragmentasi spektrum massa puncak butil diklofenak (lanjutan ) . ... 34
xiv
DAFTAR LAMPIRAN
Lampiran Halaman
1. Sertifikat analisis kalium diklofenak ... 40
2. Hasil uji kalium diklofenak dengan FT-IR ... 41
3. Hasil uji asam diklofenak dengan FT-IR ... 42
4. Hasil uji butil diklofenak dengan FT-IR ... 43
5. Kromatogram senyawa hasil sintesis ... 44
6. Spektrum massa puncak 1 senyawa hasil sintesis ... 45
7. Spektrum massa puncak 2 senyawa hasil sintesis ... 46
8. Spektrum massa puncak 3 senyawa hasil sintesis ... 47
9. Data perhitungan pengubahan kalium diklofenak menjadi asam diklofenak ... 48
10. Data perhitungan hasil pengubahan kalium diklofenak menjadi asam diklofenak ... 50
11. Data perhitungan sintesis butil diklofenak ... 51
12. Data hasil sintesis butil diklofenak ... 53
13. Bagan kerja pengubahan kalium diklofenak menjadi asam diklofenak ... 54
14. Bagan kerja pencucian asam diklofenak . ... 55
15. Bagan kerja rekristalisasi asam dikofenak . ... 56
16. Bagan kerja sintesis butil diklofenak . ... 57
17. Bagan kerja pemurnian butil diklofenak . ... 59
18. Rangkaian alat pengubahan kalium diklofenak menjadi asam diklofenak ... 60
xv
20. Rangkaian alat refluks . ... 62
21. Hasil sintesis butil diklofenak ... 63
22. Melting point block apparatus ... 64
vi
SINTESIS BUTIL DIKLOFENAK DAN
ELUSIDASI STRUKTUR MENGGUNAKAN
FOURIER TRANSFORM INFRA RED (FT-IR) DAN
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
ABSTRAK
Diklofenak adalah golongan AINS yang dikembangkan secara khusus sebagai obat antiradang. Pemberian jangka panjang obat ini dapat memberikan beberapa efek samping yang tidak diinginkan seperti tukak dan iritasi lambung. Merancang pro-drug adalah satu dari beberapa strategi untuk mengatasi masalah ini. Pro-drug dalam penelitian ini dibuat dalam bentuk ester yaitu butil diklofenak. Penelitian ini bertujuan untuk mengetahui sintesis dan karakteristik butil diklofenak.
Butil diklofenak dibuat melalui esterifikasi asam diklofenak dengan dry buthanol dengan bantuan katalis asam sulfat. Asam diklofenak diperoleh melalui reaksi antara kalium diklofenak dengan HCl 2Nyang dikarakterisasi dengan uji FT-IR. Hasil sintesis diuji kemurniannya dengan uji titik lebur kemudian dianalisis menggunakan FT-IR dan GC-MS.
Hasil FT-IR asam diklofenak menunjukkan terjadinya perubahan gugus OH karboksilat yang spseifik di bilangan gelombang 2989,66 cm-1; 2885,51 cm-1; 2681,05 cm-1; dan 2573,04 cm-1. Hasil uji titik lebur butil diklofenak menunjukkan bahwa butil diklofenak mempunyai titik lebur 110 - 113oC. Hasil FT-IR menunjukkan sudah terjadinya perubahan gugus O-H asam menjadi gugus CH2CH3 pada bilangan gelombang 1496,76 cm-1 dan 1450,47 cm-1. Hasil GC-MS
menunjukkan telah terbentuknya 49,61% butil diklofenak.
Berdasarkan hasil penelitian yang dilakukan bahwa asam diklofenak dapat diesterifikasi membentuk butil diklofenak dan karakteristik butil diklofenak dapat diperoleh dengan uji titik lebur, FT-IR dan GC-MS.
vii
SYNTHESIS OF BUTHYL DICLOFENAC AND
STRUCTURE ELUCIDATION USING
FOURIER TRANSFORM INFRA RED (FT-IR) AND
GAS CHROMATOGRAPHY MASS SPECTROMETRY (GC-MS)
ABSTRACT
Diclofenac is a NSAID group which was developed specifically as anti-inflammatory drugs. Prolonged the administration of this drug can inhibit some the side effects such as peptic ulcer and irritation in stomach. Design a pro drug is one of several strategies to overcome this problem. In this study, the pro drug is made as an ester that is buthyl diclofenac. The purpose of this study was to know the synthesis and the characteristics of buthyl diclofenac.
Buthyl diclofenac was made by esterification of diclofenac acid with dry buthanol and sulphuric acid as a catalyst. Diclofenac acid was obtained by potassium diclofenac reaction with HCL 2N that was characterized by FT-IR test. The purity of the result of buthyl diclofenac synthesis was seen by melting point test and then analyzed using FT-IR and GC-MS.
The result of FT-IR showed that there were functional group changing became OH of carboxylic in 2989.66 cm-1, 2885.51 cm-1, 2681.05 cm-1, dan 2573,04 cm-1. The result of buthyl diclofenac melting point test were 110 – 1130C. The result of FT-IR test showed there had alteration of O-H functional group became CH2CH3 in 1496.6 cm-1 and 1450.47 cm-1. The result of GC-MS
showed that 49.61% buthyl diclofenac had been formed.
Based on the results of research show that diclofenac acid can be esterificated to form buthyl diclofenac and characteristics of buthyl diclofenac can be obtained by melting point test, FT-IR and GC-MS.
1 BAB I
PENDAHULUAN
1.1Latar Belakang
Inflamasi merupakan suatu mekanisme proteksi tubuh terhadap gangguan
dari luar atau infeksi, akan tetapi inflamasi juga menjadi penyebab timbulnya
berbagai gangguan misalnya pada artritis. Pada kasus seperti ini, obat-obat
antiinflamasi mungkin diperlukan untuk memodulasi proses peradangan (Mycek,
et al., 1997; Wibowo dan Gofir, 2001).
Obat antiinflamasi nonsteroid (AINS) adalah suatu golongan obat yang
memiliki khasiat analgetik, antipiretik, dan antiinflamasi. Mekanisme kerja AINS
didasarkan atas penghambatan enzim siklooksigenase. Enzim siklooksigenase ini
berperan dalam memacu pembentukan prostaglandin dan tromboksan dari asam
arakidonat. Prostaglandin merupakan molekul pembawa pesan pada proses
inflamasi. Penggunaan klinis utama AINS adalah sebagai antiradang dalam
penanganan gangguan otot rangka seperti artritis reumatoid, osteoartritis, dan
spondilitis ankilosa. AINS merupakan golongan obat yang relatif aman, namun
terdapat beberapa efek samping utama yang ditimbulkannya, yaitu efek samping
pada saluran pencernaan serta efek samping pada ginjal (Santos, et al., 2012; Tan
dan Rahardja, 2007; Trevor, et al., 2002).
Diklofenak adalah salah satu golongan AINS yang merupakan suatu
turunan asam fenilasetat yang dikembangkan secara khusus sebagai obat
antiradang. Obat ini adalah penghambat siklooksigenase yang relatif non selektif.
2
yang pendek. Akan tetapi pemberian jangka panjang pada obat ini memberikan
beberapa efek samping yang tidak diinginkan seperti tukak dan iritasi lambung
yang disebabkan oleh gugus asam karboksilat. Merancang pro-drug adalah satu
dari beberapa strategi untuk mengatasi masalah ini (Roberts dan Morrow, 2001;
Suryawanshi, et al., 2014).
Pro-drug adalah obat yang diberikan dalam bentuk inaktif yang kemudian
dikonversi menjadi bentuk aktif obat melalui proses metabolisme. Pro-drug
dirancang untuk mengubah sifat fisika – kimia obat. Dengan melindungi gugus
asam bebas pada suatu molekul AINS maka saluran pencernaan dapat terlindungi
dari iritasi lokal. Salah satu cara pembuatan pro-drug adalah dengan pembentukan
ester (Kumar, et al, 2010; Hasan dan Elias, 2014; Suryawanshi, et al., 2014).
Ester dihasilkan melaui suatu reaksi antara asam karboksilat dengan
alkohol yang biasanya menggunakan katalis asam dan dikenal dengan nama
esterifikasi. Pembentukan ester dari suatu zat aktif dapat mengubah kelarutan dan
laju pelarutannya, yang secara umum berarti penurunan proses laju pelarutan.
Pembentukan ester dimaksudkan untuk menghindari peruraian zat aktif di
lambung, yang dapat berfungsi sebagai pro-drug yang ia sendiri tidak larut dalam
cairan lambung tetapi aktivitas dalam cairan usus terjadi karena peruraian
pro-drug oleh sejumlah enzim sehingga membebaskan zat aktif dan menghambat atau
memperpanjang aksi beberapa zat aktif. Kebanyakan pro-drug dari AINS telah
dipersiapkan dengan derivatisasi gugus karboksilnya. Turunan ester mempunyai
aktivitas antiradang karena secara in vivo dihidrolisis menjadi bentuk asamnya.
Memodifikasi substruktur molekul dengan memasukkan gugus dengan nilai pKa
3
Gugus penarik dan pendonor elektron dapat ditambahkan atau dihilangkan
tergantung pada efek yang diinginkan (Aiache, et al., 1982; Hasan dan Elias,
2014; Kerns dan Di, 2008; Riswiyanto, 2009; Suryawanshi, et al., 2014).
Berdasarkan hal di atas penulis tertarik untuk melakukan penelitian
mengenai sintesis butil diklofenak karena sediaan butil diklofenak merupakan
suatu pro-drug berupa senyawa ester yang belum terdapat di pasaran. Sediaan
butil diklofenak ini diperoleh melalui reaksi esterifikasi antara asam diklofenak
dengan butanol dengan bantuan katalisator asam sulfat. Senyawa butil diklofenak
ini diduga mempunyai efek samping yang lebih kecil dibandingkan dengan
senyawa garamnya seperti natrium diklofenak atau kalium diklofenak terutama
dalam hal iritasi lambung karena gugus asam pada diklofenak yang berperan
menyebabkan tukak lambung telah dilindungi oleh gugus butil. Adanya gugus
butil yang merupakan pendonor elektron akan menyebabkan peningkatan harga
pKa. Peningkatan harga pKa menyebabkan daerah absorbsi berada pada daerah
yang lebih basa yaitu usus.
1.2Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah untuk
penelitian ini adalah:
1. apakah asam diklofenak dapat diesterifikasi menjadi butil diklofenak?
2. apakah hasil esterifikasi antara asam diklofenak dan butanol diperoleh
senyawa butil diklofenak yang murni?
3. apakah senyawa hasil sintesis butil diklofenak dapat ditentukan
4 1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis pada penelitian ini
adalah:
1. asam diklofenak dapat diesterifikasi menjadi butil diklofenak.
2. hasil esterifikasi antara asam diklofenak dan butanol diperoleh senyawa
butil diklofenak yang murni.
3. hasil sintesis butil diklofenak dapat ditentukan karakteristiknya.
1.4Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah:
1. untuk mengetahui esterifikasi butil diklofenak.
2. untuk mengetahui kemurnian senyawa butil diklofenak yang merupakan
hasil esterifikasi antara asam diklofenak dan butanol.
3. untuk mengetahui karakteristik senyawa hasil sintesis butil diklofenak.
1.5Manfaat Penelitian
Adapun manfaat dari penelitian ini adalah untuk memberikan informasi
mengenai sintesis butil diklofenak yang berasal dari asam diklofenak dan
5 BAB II
TINJAUAN PUSTAKA
2.1Diklofenak
2.1.1 Kalium diklofenak
Menurut Anonim (2009), uraian tentang kalium diklofenak adalah sebagai
berikut:
Rumus bangun :
Rumus molekul : C14H10Cl2KNO2
Berat molekul : 334.24
Nama kimia : Benzeneacetic acid, 2-[(2,6-dichlorophenyl)amino]
monopotassium salt
Nama lain : Potassium [o-(2,6-dichloroanilino)phenyl]acetate
Nama dagang : Cataflam (Novartis)
Persen komposisi : C 50.31%, H 3.02%, Cl 21.21%, K 11.70%, N 4.19%,
O 9.57%
Kelarutan : Sedikit larut dalam air, mudah larut dalam metanol,
6 2.1.2 Asam diklofenak
Menurut Moffat, et al., (2011), uraian tentang asam diklofenak adalah
sebagai berikut:
Rumus bangun :
Rumus molekul : C14H11Cl2NO2
Berat molekul : 296.15
Nama kimia : 2-[(2,6-dichlorophenyl)amino]benzeneacetic acid
Nama lain : [o-(2,6-dichloroanilino)phenyl]acetic acid
Nama dagang : Voltarol (Novartis)
Karakteristik : Kristal dari eter-petroleum eter
Titik lebur : 156 - 1580C
7 2.1.3 Diskoneksi asam diklofenak
8 2.1.4 Mekanisme reaksi asam diklofenak
(Sumber: Ismail, 2012)
2.1.5 Efek farmakologi
Diklofenak mempunyai aktivitas antiradang, antipiretik dan antiinflamasi.
Senyawa ini merupakan inhibitor siklooksigenase, dan potensinya jauh lebih besar
daripada indometasin, naproksen atau beberapa senyawa lain. Selain itu
diklofenak menurunkan konsentrasi intrasel arakidonat bebas dalam leukosit yaitu
dengan mengubah pelepasan dan pengambilan asam lemak tersebut (Roberts dan
9 2.1.6 Efek samping
Diklofenak menimbulkan efek samping pada sekitar 20% pasien,
akibatnya sekitar 2% pasien menghentikan terapi. Efek saluran cerna merupakan
yang paling umum, perdarahan dan pembentukan ulser atau perforasi dinding
usus. Respon lain yang tidak diinginkan terhadap diklofenak antara lain efek SSP,
ruam kulit, reaksi alergi, retensi cairan, edema dan yang jarang, gangguan fungsi
ginjal. Obat ini tidak dianjurkan untuk anak-anak, ibu menyusui, atau wanita
hamil (Roberts dan Morrow, 2001).
2.2Esterifikasi
Kondensasi alkohol dan asam karboksilat yang dikatalis asam membentuk
sebuah ester dan air yang disebut sebagai esterifikasi Fischer.
Esterifikasi Fischer bersifat reversibel, dan posisi kesetimbangan biasanya
bergeser sedikit ke arah produk. Untuk preparasi ester posisi kesetimbangan dapat
dibuat lebih menguntungkan dengan menggunakan baik alkohol maupun asam
karboksilat yang berlebih. Komponen yang penggunaannya berlebih tergantung
pada ketersediaan dan biaya. Salah satu cara untuk menggeser posisi
kesetimbangan ke arah ester adalah dengan menghilangkan air dari campuran
10
Gambar 2.1 Mekanisme reaksi esterifikasi suasana asam (Riswiyanto, 2009)
Reaksi esterifikasi dikatalis oleh asam. Reaksi ini berlangsung lambat
tanpa adanya asam kuat, tetapi mencapai kesetimbangan dalam waktu yang
singkat ketika suatu asam dan alkohol direfluks bersama dengan asam sulfat atau
asam klorida dalam konsentrasi yang kecil (Solomons, 1988).
2.3Rekristalisasi
Pengkristalan kembali (rekristalisasi) melibatkan pemurnian suatu zat
padat dengan jalan melarutkan zat padat tersebut, mengurangi volume larutannya
dengan pemanasan, dan kemudian mendinginkan larutan. Dengan memanaskan
larutan, pelarut akan menguap hingga larutan mencapai titik lewat jenuh. Saat
larutan mendingin, kelarutan akan berkurang secara cepat dan senyawa mulai
mengendap (Bresnick, 2004).
Agar rekristalisasi berjalan baik, kotoran setidak-tidaknya harus dapat larut
11
senyawa yang diinginkan. Jika hal ini tidak terpenuhi, kotoran akan ikut
mengkristal bersama senyawa yang diinginkan (Bresnick, 2004).
2.4Spektrofotometri Inframerah
Hampir beberapa senyawa mempunyai ikatan kovalen, baik senyawa
organik maupun anorganik akan mengabsorbsi berbagai frekuensi radiasi
elektromagnetik pada wilayah spektrum inframerah. Wilayah inframerah dari
spektrum elektromagnetik berada pada panjang gelombang yang lebih panjang
daripada sinar tampak yang berada pada rentang panjang gelombang 400-800 nm
(1 nm = 10-9 m), tetapi berada pada panjang gelombang gelombang yang lebih
pendek daripada sinar gelombang mikro yang mempunyai panjang gelombang
lebih panjang dari 1 nm. Radiasi inframerah terdapat pada panjang gelombang (λ)
antara 2.5μ dan 15μ (1μ = 1 mikron = 1μm =10-6
m) (Pavia, et al., 1979).
Molekul dengan struktur yang berbeda tidak akan ada yang mempunyai
pola absorbsi dan spektrum inframerah yang sama karena setiap ikatan yang
berbeda mempunyai frekuensi getaran yang berbeda, dan juga karena setiap jenis
ikatan kimia yang sama pada dua senyawa yang berbeda berada pada lingkungan
yang sedikit berbeda (Pavia, et al., 1979).
Dalam proses absorbsi, frekuensi-frekuensi radiasi inframerah yang
bersesuaian dengan frekuensi vibrasi molekul akan diserap dan akan
meningkatkan amplitudo gerakan-gerakan vibrasional ikatan dalam molekul.
Supaya molekul menyerap radiasi inframerah, maka molekul tersebut harus
mempunyai gambaran sspesifik, yakni momen dipol molekul harus berubah
12
Tabel 2.1 Frekuensi regangan IR (Sumber: Pavia, et al., 1979)
Gugus fungsi Frekuensi (cm-1) Intensitas C-H Alkana 3000 - 2850 Kuat
-CH3 1450 dan 1375 Medium
-CH2 1465 Medium
Alkena 3100 - 3000 Medium Aromatis 3150 - 3050 Kuat
Alkuna 3300 Kuat
C=C Alkena 1680 - 1600 Medium - Lemah Aromatis 1600 dan 1475 Medium - Lemah C C Alkuna 2250 - 2100 Medium - Lemah
C=O Aldehid 1740 - 1720 Kuat Keton 1725 - 1705 Kuat Asam karboksilat 1725 - 1700 Kuat Ester 1750 - 1730 Kuat Amida 1670 - 1640 Kuat Anhidrida 1810 dan 1760 Kuat Asam klorida 1800 Kuat
C-O Alkohol, Eter, Ester, Asam
karboksilat, Anhidrida 1300 - 1000 Kuat O-H Alkohol, Fenol
Bebas 3650 - 3600 Medium Terikat 3500 - 3200 Medium Asam karboksilat 3400 - 2400 Medium
N-H Primer, Sekunder dan
Amida 3500 - 3100 Medium C-N Amina 1350 - 1000 Medium - Kuat C=N Imin dan Oxim 1690 - 1640 Lemah - Kuat C N Nitril 2260 - 2240 Medium
N=O Nitro 1550 dan 1350 Kuat C-X Fluorida 1400 - 1000 Kuat Klorida 800 - 600 Kuat Bromida, Iodida < 667 Kuat
Menurut Meislich, et al., (1980), pada bilangan gelombang antara 1400
dan 800 cm-1 ada banyak puncak yang sulit untuk dianalisa. Namun rentang ini
disebut dengan daerah sidik jari, yang digunakan untuk menentukan apakah suatu
13 2.4.1 Prinsip
Radiasi inframerah dari frekuensi yang kurang dari 100 cm-1 diabsorbsi
dan dikonversi oleh molekul organik menjadi energi rotasi molekul. Absorbsi
terukur, maka spektrum rotasi molekul terdiri dari bercirikan garis. Radiasi
inframerah pada rentang 10000-100 cm-1 diabsorbsi dan dikonversi oleh molekul
organik menjadi energi vibrasi molekul. Absorbsi ini terukur, tapi spektra vibrasi
lebih tampak sebagai pita daripada garis karena perubahan energi vibrasi tunggal
diikuti oleh perubahan sejumlah energi rotasi (Silverstein, et al., 2005).
2.4.2 Spektrofotometer FT-IR
Spektrofotometer FT-IR didasarkan pada ide adanya interferensi radiasi
antara 2 berkas sinar untuk menghasilkan suatu interferogram. Interferogram
merupakan sinyal yang dihasilkan sebagai fungsi perubahan celah optik antara 2
berkas sinar. Radiasi yang berasal dari sumber sinar dilewatkan melalui
interferometer ke sampel sebelum mencapai detektor. Selama penguatan
(amplifikasi) sinyal, yang mana kontribusi-kontribusi frekuensi tinggi telah
dihilangkan dengan filter, maka data diubah ke bentuk digital dengan
analog-to-digital converter dan dipindahkan ke komputer untuk menjalani transformasi
[image:30.595.115.510.575.688.2]Fourier (Gandjar dan Rohman, 2012).
Gambar 2.2 Komponen utama dalam FT-IR
(Sumber: Gandjar dan Rohman, 2012)
Sumber
sinar Interferometer Sampel
Detektor (Amplifier)Penguat
Pengubah analog ke digital
14 2.5 Kromatografi Gas (Gas Chromatography)
Kromatografi gas (KG) merupakan metode yang dinamis untuk pemisahan
dan deteksi senyawa–senyawa orgnik yang mudah menguap dan
senyawa-senyawa gas anorganik dalam suatu campuran. Kegunaan umum KG adalah untuk
melakukan pemisahan dinamis dan identifikasi semua jenis senyawa-senyawa
organik yang mudah menguap dan juga untuk melakukan analisis kualitatif dan
kuantitatif senyawa dalam suatu campuran (Gandjar dan Rohman, 2012).
Karena pemisahan campuran senyawa dalam kolom terjadi ketika senyawa
dalam keadaan gas, maka sampel-sampel padat ataupun cairan harus pertama kali
diuapkan. Hal inilah yang membatasi penggunaan KG yang mana KG digunakan
untuk analisis senyawa yang stabil terhadap panas dan mudah diuapkan. Untuk
sampel gas, sampel dapat langsung diambil dengan penyuntik (syringe) yang ketat
terhadap gas (Gandjar dan Rohman, 2012).
2.5.1 Prinsip kromatografi gas
Prinsip kromatografi gas merupakan teknik pemisahan yang mana
solut-solut yang mudah menguap (dan stabil terhadap panas) bermigrasi melalui kolom
yang mengandung fase diam dengan suatu kecepatan yang tergantung pada rasio
distribusinya. Pada umumnya solut akan terelusi berdasarkan pada peningkatan
titik didihnya. Pemisahan pada kromatografi gas didasarkan pada titik didih suatu
senyawa dikurangi dengan semua interaksi yang mungkin terjadi antara solut
dengan fase diam. Fase gerak yang berupa gas akan mengelusi solut dari ujung
kolom lalu menghantarkannya ke detektor. Penggunaan suhu yang meningkat
(biasanya pada kisaran 50 – 3500C) bertujuan untuk menjamin bahwa solut akan
15 2.5.2 Sistem peralatan kromatografi gas
Suatu kromatograf gas tersusun dari berbagai komponen dalam suatu
bingkai khusus. Komponen-komponen ini mencakup injektor, kolom, dan
detektor, yang dihubungkan dengan suatu oven yang dikontrol secara termostatik
yang membuat kolom mampu mencapai suhu tinggi. Fase gerak yang membawa
analit menuju kolom merupakan suatu gas dan dirujuk sebagai gas pembawa.
Aliran gas pembawa, yang dikontrol secara teliti, akan mampu memberikan waktu
retensi yang reprodusibel. Selain itu, kromatograf juga dilengkapi dengan
komputer yang dilengkapi dengan perangkat pengolah data (Gandjar dan Rohman,
[image:32.595.130.513.371.543.2]2012).
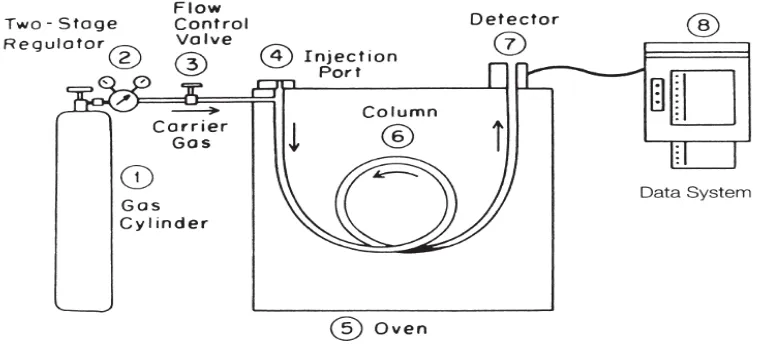
Gambar 2.3 Diagram skematik kromatograf gas (McNair dan Miller, 2009)
2.5.2.1Fase gerak
Fase gerak pada kromatografi gas juga disebut dengan gas pembwa karena
tujuan awalnya adalah untuk membawa solut ke kolom, oleh karena itu gas
pembawa tidak berpengaruh pada selektivitas. Syarat gas pembawa adalah: tidak
reaktif, murni/kering karena kalau tidak murni akan berpengaruh pada detektor,
16 2.5.2.2Tempat pemasukan sampel (injektor)
Injektor merupakan suatu jalan masuk sampel ke kromatograf, mempunyai
fungsi yang berbeda. Disamping peranannya sebagai jalan masuk sampel, injektor
harus mampu menguapkan sampel, mencampurkannya dengan gas pembawa, dan
membawa sampel ke ujung depan kolom (Gandjar dan Rohman, 2012).
2.5.2.3Kolom dan fase diam
Kolom merupakan tempat terjadinya proses pemisahan karena didalamnya
terdapat fase diam. Oleh karena itu, kolom merupakan komponen utama pada
kromatografi gas. Ada 2 jenis kolom yang berbeda dalam hal kinerjanya, yaitu
kolom kemas atau packing column dan kolom kapiler atau capillary column. Pada
kolom kemas, fase diam terdeposit atau terikat dengan reaksi kimia pada
pendukung porus. Pada kolom kapiler, suatu lapisan tipis fase diam terdeposit
pada permukaan kolom atau terikat pada permukaan bagian dalam kolom
(Gandjar dan Rohman, 2012).
Fase diam yang digunakan pada kolom kapiler dapat bersifat non polar,
polar, atau semi polar. Fase diam non polar yang paling banyak digunakan adalah
metil polisiloksan (HP-1; DB-1; SE-30; CPSIL-5) dan fenil 5%-metilpolisiloksan
95% (HP-5; DB-5; SE-52; CPSIL-8). Fase diam semi polar adalah seperti fenil
50%-metilpolisiloksan 50% (HP-17; DB-17; CPSIL-19), sementara itu fase diam
yang polar adalah seperti polietilen glikol (HP-20M; DB-WAX; CP-WAX;
Carbowax-20M) (Gandjar dan Rohman, 2012).
2.5.2.4Detektor
Detektor merupakan perangkat yang diletakkan pada ujung kolom tempat
17
Detektor pada kromatografi adalah suatu sensor elektronik. Sinyal elektronik
detektor sangat berguna untuk analisis kualitatif maupun kuantitatif terhadap
komponen-komponen yang terpisah antara fase diam dan fase gerak (Gandjar dan
Rohman, 2012).
2.5.2.5Komputer
Kromatografi gas modern menggunakan komputer yang dilengkapi dengan
perangkat lunaknya (software) untuk digitalisasi signal detektor yang mempunyai
beberapa fungsi antara lain: memfasilitasi setting parameter-parameter instrumen
seperti aliran fase gas, suhu oven dan pemrograman suhu, serta penyuntikan
sampel secara otomatis; menampilkan kromatogram dan informasi-informasi lain
dengan menggunakan grafik berwarna; merekam data kalibrasi, retensi serta
perhitungan-perhitungan dengan statistik; menyimpan data parameter analisis
untuk analisis senyawa tertentu (Gandjar dan Rohman, 2012).
2.6Spektrometri Massa (Mass Spectrometry)
Konsep spektrometri massa relatif sederhana yaitu senyawa terionisasi, ion
dipisahkan berdasarkan perbandingan massa per muatan dan jumlah ion yang
mewakili masing-masing satuan massa per muatan dicatat sebagai spektrum.
Spektrometer massa memborbardir molekul dalam fase uap dengan berkas
elektron yang tinggi dan mencatat hasil sebagai spektrum dari ion postif yang
dipisahkan berdasarkan massa per muatan (m/z). Puncak ion positif pada m/z
merupakan molekul utuh (M) yang kehilangan satu elektron, ion tersebut
ditunjukkan sebagai M.+. Energi ion molekul tersebut menghasikan serangkaian
18
Teknik ini digunakan sangat luas karena mampu menawarkan batas
deteksi yang lebih kecil (lebih sensitif). Spektrometer massa jika digunakan
sebagai detektor, maka akan mampu memberikan informasi data struktur kimia
senyawa yang tidak diketahui. Dengan menggunakan spektrometer massa untuk
memonitor ion tunggal atau beberapa ion yang karakteristik dalam analit, maka
batas deteksi ion-in ini akan ditingkatkan (Gandjar dan Rohman, 2012).
2.6.1 Prinsip
Menurut Pavia, et al., (1979), spektrometer massa memainkan tiga peranan
penting yaitu:
1. Molekul mengalami bombardir oleh aliran elektron berenergi tinggi,
mengubah beberapa molekul menjadi ion.
2. Ion dipisahkan berdasarkan perbandingan muatan massa pada sebuah bidang
listrik dan magnetik.
3. Pada akhirnya ion dengan perbandingan muatan massa tertentu dideteksi oleh
suatu alat yang mampu menghitung jumlah ion yang diserang. Keluaran
detektor direkam oleh sebuah recorder. Jejak dari recorder adalah sebuah
spektrum massa, suatu grafik dari jumlah partikel yang dideteksi sebagai
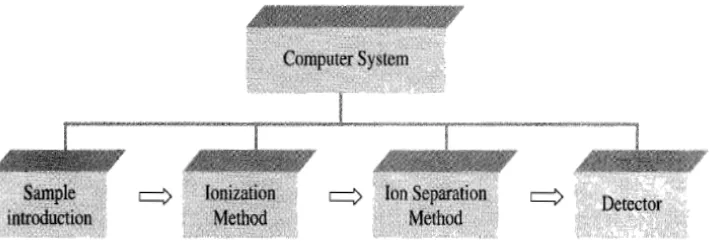
[image:35.595.137.493.587.710.2]fungsi perbandingan muatan massa.
19 BAB III
METODE PENELITIAN
Metode penelitian ini akan dilakukan secara eksperimental. Penelitian
meliputi sintesis butil diklofenak dengan metode esterifikasi, uji kemurnian
dengan uji titik lebur hasil sintesis dan elusidasi struktur senyawa hasil sintesis
dengan menggunakan FT-IR dan GC-MS. Penelitian ini dilakukan di
Laboratorium Sintesa Obat Fakultas Farmasi USU. Elusidasi struktur senyawa
dengan FT-IR dilakukan di Laboratorium Penelitian Fakultas Farmasi USU dan
elusidasi struktur dengan GC-MS dilakukan di Laboratorium Kimia Instrumen
Universitas Pendidikan Indonesia.
3.1Alat dan Bahan
3.1.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas
laboratorium (beaker glass, corong pisah, dropping funnel equalizing, erlenmeyer,
gelas ukur, labu alas bulat leher tiga, pendingin bola, pendingin liebig, pipa
bengkok, pipa cabang tiga, tabung reaksi), cawan porselin, GC-MS-QP2010 Ultra
(Shimadzu), hot plate (Thermo Scientific- Cimarec), magnetic bar, melting point
block apparatus (Gallenkamp), neraca analatik, Spektrofotometer IR (IR
Prestige-21 Fourier Transform Infra Red Spectrophotometer Serial No.
20 3.1.2 Bahan-bahan
Bahan yang digunakan dalam penelitian ini adalah kalium diklofenak,
akuades, akua bidestilata, CaO, gas Nitrogen Ultra High Purity (UHP) dan es
batu. Bahan kimia yang digunakan berkualitas pro analisis produksi E-merck :
etanol, butanol, eter, H2SO4 pekat, HCl pekat, AgNO3, Na2SO4 anhidrat,
n-heksan, Na2CO3, tetrahidrofuran (THF), KBr.
3.2 Pengambilan Bahan Baku
Bahan baku yang digunakan dalam penelitian ini adalah kalium diklofenak
yang diperoleh dari PT. Dexa Medica. Bahan baku disertai dengan Seritifikat
analisis yang terdapat di Lampiran 1, halaman 40.
3.3 Pembuatan Pereaksi
3.3.1 Pembuatan larutan AgNO3 5%
Sebanyak 5 gram AgNO3 dilarutkan dengan akua bidestilata sampai 100
ml.
3.3.2 Pembuatan larutan Na2CO3 5%
Sebanyak 5 gram Na2CO3 digerus di dalam lumpang dengan sejumlah
volume air suling, dienaptuangkan. Dilakukan berulang-ulang hingga volume air
suling yang digunakan 100 ml.
3.3.3 Pembuatan larutan HCl 2N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling sampai
21 3.3.4 Pembuatan dry ethanol
CaO diaktifkan dengan cara dipanaskan di dalam tanur suhu 450 - 500oC
selama 2-3 jam. Etanol dimasukkan ke dalam wadah yang sudah berisi CaO yang
sudah diaktifkan dan didiamkan selama 24 jam, campuran disaring dan didestilasi
pada titik didih etanol. Rangkaian alat destilasi dapat dilihat pada Lampiran 19,
halaman 61 (Armarego dan Chai, 2003).
3.3.5 Pembuatan dry buthanol
Na2SO4 anhidrat diaktifkan dengan cara dipanaskan di dalam oven suhu
100oC selama 2-3 jam. Butanol dimasukkan ke dalam wadah yang sudah berisi
Na2SO4 anhidrat yang sudah diaktifkan dan didiamkan selama 24 jam, kemudian
campuran disaring dan didestilasi pada titik didih butanol (Armarego dan Chai,
2003).
3.4Pengubahan Kalium Diklofenak
Sebanyak 15 gram kalium diklofenak dalam labu alas bulat dilarutkan
dalam 362 ml campuran etanol 99% : THF (3:1) yang ditetesi melalui dropping
funnel equalizing yang dihubungkan dengan tabung gas nitrogen. Larutan
didinginkan (18oC) sambil diaduk selama 10 menit, kemudian HCl 2N
ditambahkan, diikuti dengan penambahan air dingin sebanyak 750 ml, dan
didinginkan di lemari es hingga asam diklofenak mengendap. Asam diklofenak
kemudian disaring dan dikeringkan. Rangkaian alat dapat dilihat pada Lampiran
22 3.5Pencucian Asam Diklofenak
Endapan asam diklofenak yang diperoleh dicuci dengan air suling, di
saring dan filtratnya diuji dengan dengan AgNO3. Bila masih terbentuk endapan
putih AgCl, endapan dicuci lagi sampai tidak membentuk endapan putih dengan
penambahan AgNO3 (Vogel, 1979).
3.6 Pemurnian Asam Diklofenak
Pemurnian asam diklofenak dilakukan dengan menggunakan teknik
rekristalisasi mixed solvent. Sebanyak 1 gram asam diklofenak dilarutkan dalam
30 ml etanol, kemudian ditetesi dengan akuades dingin hingga tidak terbentuk lagi
endapan asam diklofenak. Endapan disaring lalu dikeringkan di dalam oven
(Armarego dan Chai, 2003).
3.7 Uji Titik Lebur Asam Diklofenak
Sampel yang akan diuji dimasukkan ke dalam pipa kapiler secukupnya.
Pipa kapiler dimasukkan ke dalam Melting Point Block Apparatus kemudian
diatur suhu hingga sampel dalam pipa kapiler melebur. Rentang suhu dihitung
mulai dari sampel mulai melebur hingga melebur sempurna (Rodig, et.al., 1990).
3.8 Sintesis Butil Diklofenak
Dimasukkan 2 g asam diklofenak ke dalam labu alas bulat, lalu ditambah
46 ml dry buthanol, sambil diaduk di atas hot plate. Alat refluks dirangkai dan
ditambahkan 1 ml asam sulfat pekat, secara berangsur-angsur melalui dinding
23
dalam corong pisah yang telah berisi 30 ml akuades dan 30 ml eter lalu digojok.
Kemudian dibilas labu alas bulat dengan eterlalu dimasukkan ke dalam corong
pisah kemudian digojok dan didiamkan. Dicuci lapisan atas dengan air suling
sebanyak tiga kali. Digojok dan didiamkan. Dipisahkan lapisan bawah dan
dimasukkan 20 ml larutan Na2CO3 5% ke lapisan atas. Digojok dan didiamkan.
Hal ini dilakukan berulang sebanyak tiga kali. Diambil lapisan atas kemudian
ditambahkan dengan Na2SO4 anhidrat secukupnya. Didiamkan selama 24 jam
pada suhu kamar. Dipipet cairan jernihnya kemudian diuapkan di ruang terbuka
hingga seluruh eter menguap dan terbentuk kristal butil diklofenak (Suryawhansi,
et al., 2014).
3.9 Pemurnian Hasil Sintesis
Zat hasil sintesis yang tidak murni dilarutkan dalam n-heksan yang sudah
didestilasi, digoncang dan diaduk dengan kuat pada suhu 67 – 700C, untuk
membentuk larutan jenuh. Larutan panas disaring untuk menghilangkan
partikel-partikel yang tidak larut. Larutan kemudian dibiarkan dingin agar senyawa yang
larut membentuk kristal. Kristal dipisahkan dari cairan induk (Armarego dan
Chai, 2003).
3.10 Uji Titik Lebur Hasil Sintesis
Titik lebur hasil sintesis diuji dengan menggunakan Melting Point Block
Apparatus. Rentang suhu awal senyawa mulai melebur sampai senyawa melebur
sempurna dihitung. Senyawa hasil sintesis dinyatakan murni apabila rentang
24 3.11 Elusidasi Struktur dengan FT-IR
Bahan uji digerus halus, dicampurkan dengan serbuk KBr yang sudah
dihaluskan, dihomogenkan dan dimasukkan kedalam tempat sampel, kemudian
diukur dengan FT-IR untuk menentukan bilangan gelombangnya.
3.12 Elusidasi Struktur dengan GC-MS
Analisis senyawa hasil sintesis dengan GC-MS menggunakan kolom
kapiler DB 5-MS yang mengandung 5% fenil 95% metil siloksan dengan gas
pembawa Helium dengan tekanan 80,2 kPa. Aliran gas ke kolom 1,31 ml/menit.
Volume penyuntikan adalah 0,20 µl dengan mode penyuntikan split diatur suhu
penyuntikan 280oC pada tekanan 80,2 kPa. Suhu kolom terprogram diatur 60°C
yang diikuti penyuntikan kemudian suhu deprogram 8°C menit-1 hingga pada suhu
290°C ditahan selama 2 menit. Kemudian dideteksi dengan spektroskopi massa
dengan kondisi temperature ion 230°C dan suhu lingkungan penghubung GC dan
25 BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Pengubahan Kalium Diklofenak
Hasil pengubahan kalium diklofenak menjadi asam diklofenak diperoleh
persen rendemen sebesar 87,50%. Perhitungan dapat dilihat pada Lampiran 10,
halaman 50.
4.2 Hasil Uji Titik Lebur Asam Diklofenak
Hasil uji titik lebur asam diklofenak yang diperoleh setelah pemurnian
adalah 158 - 160oC. Menurut Moffat (2011), titik lebur asam diklofenak adalah
156 - 158oC. Titik lebur yang diperoleh tidak sesuai dengan teori hal ini
dikarenakan oleh beberapa faktor yaitu kondisi lingkungan menyangkut
kelembaban, suhu, serta alat yang tidak dikalibrasi. Rentang titik lebur yang
diperoleh adalah 2oC. Rentang titik lebur memperlihatkan bahwa asam diklofenak
yang diperoleh telah murni. Hal ini dikarenakan selama proses pemurnian dengan
etanol air sebanyak 3 kali, kalium diklofenak, KOH, dan 1,4-diklorobutana akan
terlarut dalam air sementara asam diklofenak tidak larut dalam air. Reaksi
pengubahan kalium diklofenak dapat dilihat pada Gambar 4.1.
26 4.3 Hasil Uji Asam Diklofenak Dengan FT-IR
[image:43.595.115.513.165.402.2]Hasil uji asam diklofenak dengan menggunakan FT-IR dapat dilihat pada
Gambar 4.2.
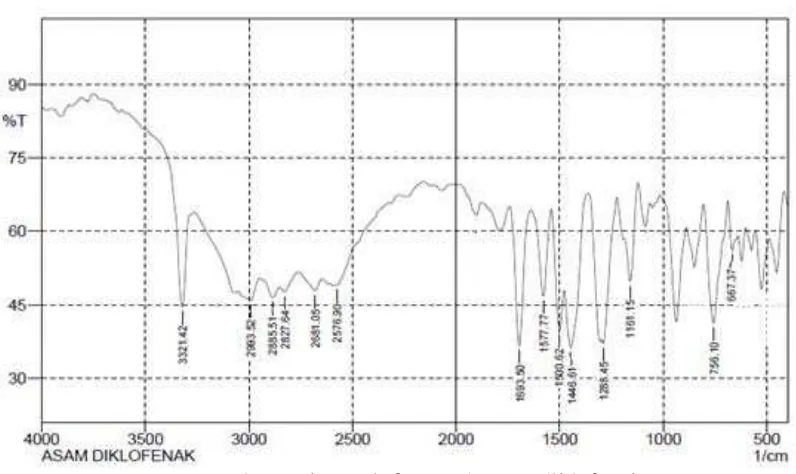
Gambar 4.2 Spektrum inframerah asam diklofenak
Hasil uji kalium diklofenak dengan menggunakan FT-IR dapat dilihat
[image:43.595.118.514.479.693.2]pada Gambar 4.3.
27
Jika spektrum inframerah asam diklofenak pada Gambar 4.2 dibandingkan
dengan spektrum inframerah dari kalium diklofenak pada Gambar 4.3, dapat
dilihat perbedaan pada C-H sp2 masing-masing spektrum. Spektrum C-H sp2 pada
kalium diklofenak masih terlihat jelas pada bilangan gelombang 3070,68 cm-1 dan
2970,38 cm-1, sedangkan pada asam diklofenak karena adanya peleburan
spektrum O-H karboksilat C-H sp2 tidak terlihat jelas. Dapat disimpulkan bahwa
kalium diklofenak telah mengalami perubahan menjadi asam diklofenak.
Ikatan rangkap C=C dengan intensitas lemah menunjukkan absorbsi pada
daerah dekat 1650 cm-1. Intensitas medium hingga kuat diabsorbsi pada daerah
1650-1450 cm-1, biasanya disebut dengan cincin aromatis dan dikonfirmasi
dengan adanya gugus C-H pada daerah diatas 3000 cm-1 (Pavia, et al., 1979).
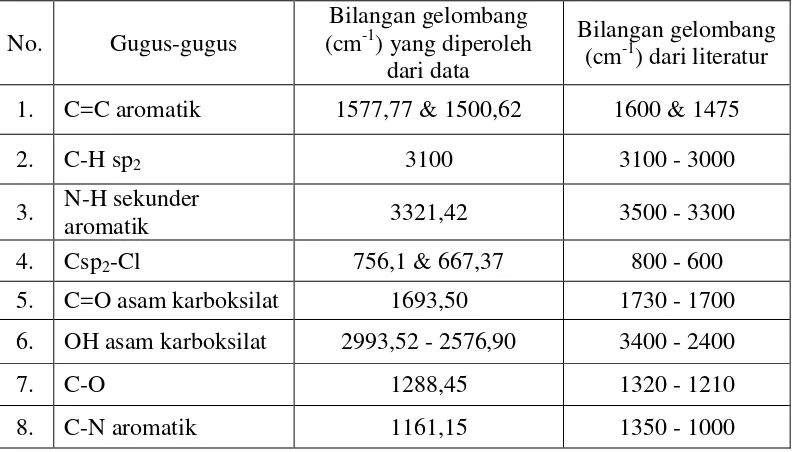
Dari Gambar 4.2 diperoleh gugus-gugus yang dapat dilihat pada Tabel 4.1 sebagai
[image:44.595.115.514.471.697.2]berikut:
Tabel 4.1 Identifikasi gugus fungsi spektrum inframerah asam diklofenak
No. Gugus-gugus
Bilangan gelombang (cm-1) yang diperoleh
dari data
Bilangan gelombang (cm-1) dari literatur
1. C=C aromatik 1577,77 & 1500,62 1600 & 1475
2. C-H sp2 3100 3100 - 3000
3. N-H sekunder
aromatik 3321,42 3500 - 3300 4. Csp2-Cl 756,1 & 667,37 800 - 600
5. C=O asam karboksilat 1693,50 1730 - 1700
6. OH asam karboksilat 2993,52 - 2576,90 3400 - 2400
7. C-O 1288,45 1320 - 1210
28
Terdapat gugus N-H aromatik sekunder dan O-H karboksilat pada rumus
bangun diklofenak yang diserap di bawah sinar inframerah pada bilangan
gelombang yang sama yaitu pada daerah 3500 - 3400 cm-1. Namun keistimewaan
karakteristik dari spektrum asam karboksilat adalah absorbsi O-H yang sangat
luas di daerah 3400-2400 cm-1 sedangkan N-H aromatik sekunder mempunyai
spektrum yang tajam. Hasil uji dengan FT-IR dari asam diklofenak menunjukkan
terjadinya absorbsi O-H karboksilat yang luas di daerah bilangan gelombang
2989,66 cm-1; 2885,51 cm-1; 2681,05 cm-1; dan 2573,04 cm-1 dan satu puncak
N-H aromatik sekunder yang tajam di daerah 3321,42 cm-1 Perbedaan antara N-H
aromatik sekunder dan N-H aromatik primer adalah adalah pada puncaknya. Di
mana pada N-H aromatik primer terdapat dua puncak pada bilangan
gelombangnya sementara pada N-H aromatik sekunder hanya terdapat satu
puncak. Karakteristik lain senyawa asam diklofenak adalah adanya gugus karbonil
asam karboksilat. Menurut Pavia, et al., (1979), gugus karbonil (C=O) berada
pada bilangan gelombang 1725 - 1700 cm-1, dan dari hasil uji asam diklofenak
dengan FT-IR menunjukkan adanya gugus karbonil di daerah 1693,50 cm-1.
4.4 Hasil Sintesis Butil Diklofenak
Hasil sintesis butil diklofenak yang diperoleh mempunyai persen
rendemen sebesar 19,11%. Perhitungan dapat dilihat pada Lampiran 12, halaman
53. Hasil yang diperoleh tidak maksimal disebabkan pada proses pengkristalan,
masih terdapat kristal butil diklofenak yang belum terkristalkan dan asam
diklofenak yang kembali terkristal menjadi asam diklofenak awal. Selain itu
29
penyaring. Hasil sintesis butil diklofenak berupa kristal berwarna coklat kehijauan
terdapat pada Lampiran 21, halaman 63.
4.5 Hasil Uji Titik Lebur Butil Diklofenak
Hasil uji titik lebur butil diklofenak yang diperoleh setelah rekristalisasi
adalah 110 - 1130C dengan rentang 3oC, diamati mulai dari awal senyawa melebur
hingga senyawa melebur sempurna. Berdasarkan rentang tersebut, dapat diduga
senyawa butil diklofenak yang diperoleh belum murni. Rentang yang sempit
menunjukkan kemurnian yang tinggi dari sampel, sedangkan rentang yang tinggi
biasanya menunjukkan senyawa yang di analisis tidak murni (Rodig, et.al., 1990).
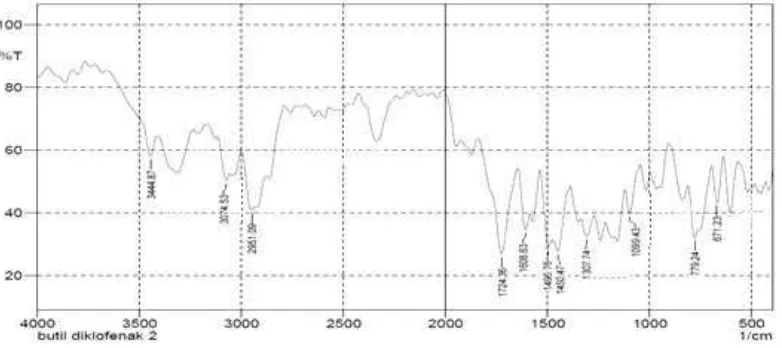
4.6 Hasil Uji Butil Diklofenak dengan FT-IR
[image:46.595.119.510.478.652.2]Hasil uji butil diklofenak dengan menggunakan FT-IR dapat dilihat pada
Gambar 4.4.
Gambar 4.4 Spektrum inframerah butil diklofenak
Butil diklofenak merupakan suatu ester yang akan diabsorbsi di bawah
30
absorbsi gugus C=O dan C-O. Gugus C=O meregang pada bilangan gelombang
1735 cm-1, sedangkan C-O meregang dengan dua puncak atau lebih, satu lebih
tajam dan luas dibandingkan yang lainnya dalam rentang 1300-1000 cm-1 (Pavia,
et al., 1979).
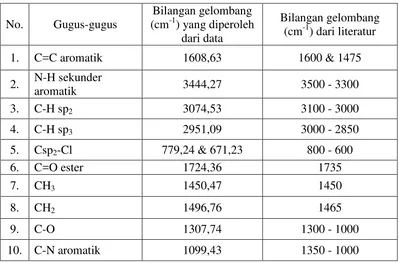
Dari Gambar 4.4 diperoleh gugus-gugus yang dapat dilihat pada Tabel 4.2 sebagai
[image:47.595.113.512.280.543.2]berikut:
Tabel 4.2 Identifikasi gugus fungsi spektrum inframerah butil diklofenak
Hasil uji dengan FT-IR menunjukkan terjadinya absorbsi gugus C=O di
daerah bilangan gelombang 1724,36 cm-1 dan C-O pada 1307,74 cm-1. Jika
dibandingkan absorbsi gugus C=O asam karboksilat pada Gambar 4.2 dengan
absorbsi gugus C=O pada ester butil diklofenak terjadi pergeseran ke bilangan
gelombang yang lebih tinggi yaitu 1693,50 cm-1 (asam diklofenak) menjadi 1724,
36 cm-1 (butil diklofenak). Butil diklofenak mengalami substitusi butil dari No. Gugus-gugus
Bilangan gelombang (cm-1) yang diperoleh
dari data
Bilangan gelombang (cm-1) dari literatur
1. C=C aromatik 1608,63 1600 & 1475
2. N-H sekunder
aromatik 3444,27 3500 - 3300 3. C-H sp2 3074,53 3100 - 3000
4. C-H sp3 2951,09 3000 - 2850
5. Csp2-Cl 779,24 & 671,23 800 - 600
6. C=O ester 1724,36 1735
7. CH3 1450,47 1450
8. CH2 1496,76 1465
9. C-O 1307,74 1300 - 1000
31
butanol sehingga terjadi perubahan absorbsi pada FT-IR. Pada butil diklofenak
tidak terjadi lagi absorbsi gugus OH yang sangat lebar di daerah 3400 - 2400 cm-1
tetapi sebagai gantinya absorbsi gugus CH2 dan CH3. Pada bilangan gelombang
1496,76 cm-1 dan 1450,47 cm-1 menunjukkan adanya gugus CH2 dan CH3. Pada
butil diklofenak juga terdapat C-H sp3 dari gugus butil pada bilangan gelombang
2951,09 cm-1, sedangkan pada asam diklofenak hanya terdapat C-H sp2 yang
berasal dari C-H aromatik.
4.7Hasil Uji Butil Diklofenak dengan GC-MS
Hasil uji butil diklofenak dengan menggunakan GC-MS diperoleh
kromatogram GC dan spektrum MS. Kromatogram GC yang diperoleh ada
sebanyak 3 puncak dapat dilihat pada Gambar 4.5 dan untuk hasil analisis secara
[image:48.595.123.513.444.595.2]lengkap dapat dilihat pada Lampiran 5, halaman 44.
Gambar 4.5 Kromatogram butil diklofenak hasil GC
Kromatogram menunjukkan adanya tiga senyawa yang berbeda yaitu:
asam diklofenak dengan waktu tambat 22,019 menit dan luas area 50,04 %.
Senyawa kedua dengan waktu tambat 24,054 menit dan luas area 0,35 % adalah
asam diklofenak dan ester metil diklofenak dan senyawa ketiga adalah ester butil
32
Menurut Fessenden dan Fessenden (1986), reaksi esterifikasi bersifat
reversibel. Kesetimbangan harus digeser kearah sisi ester untuk memperoleh
rendemen tinggi dari ester. Satu teknik untuk mencapainya adalah dengan
menggunakan salah satu zat pereaksi yang murah secara berlebihan dan
membuang salah satu produk dari campuran reaksi yaitu air. Bertambahnya
halangan sterik dalam zat antara seperti air maka laju pembentukan ester menurun
karena kesetimbangan akan digeser ke arah pembentukan asam diklofenak
kembali.
Kromatogram GC menunjukkan bahwa masih terdapat asam diklofenak
dan ester metil diklofenak pada senyawa hasil sintesis. Hal ini disebabkan karena
peralatan yang digunakan pada setiap proses sintesis tidak dikeringkan pada
pengering khusus, sehingga diperkirakan peralatan belum benar-benar bebas air
dan masih terdapatnya pengotor pada senyawa tersebut.
4.8 Fragmentasi dan Analisis Hasil Spektrometri Massa Butil Diklofenak
Fragmentasi dan analisis hasil spektrometri massa senyawa hasil sintesis
dapat dilihat pada Lampiran 6 sampai dengan Lampiran 8, halaman 45 - 47.
Spektrum massa puncak butil diklofenak dengan waktu tambat 25,041 menit
mempunyai ion molekul (M+) m/z = 351 diikuti fragmen m/z = 277, 242, 214,
[image:49.595.124.509.645.715.2]179, 151, 125, 107, 89, dan 77.
33
Rumus molekul dari fragmen yang muncul dan yang hilang dari fragmentasi butil
[image:50.595.239.511.250.529.2]diklofenak dapat dilihat pada Gambar 4.7, Gambar 4.8 dan Gambar 4.9.
Gambar 4.7Fragmentasi spektrum massa puncak butil diklofenak
Uraian yang dapat dilihat dari Gambar 4.7 adalah sebagai berikut:
1. C18H19Cl2NO2 BM 351,08 melepaskan C4H9OH BM 74,07 memunculkan
spektrum C14H9Cl2NO BM 277,01.
2. C14H9Cl2NO BM 277,01 melepaskan Cl- BM 34,97 memunculkan spektrum
C14H9ClNO+ BM 242,04.
3. C14H9ClNO+ BM 242,04 melepaskan CO4. BM 28,03 memunculkan spektrum
34
Gambar 4.8 Fragmentasi spektrum massa puncak butil diklofenak (lanjutan)
Uraian yang dapat dilihat dari Gambar 4.8 adalah sebagai berikut:
1. C13H9ClN3+ BM 214,04 kemudian melepaskan Cl- BM 34,97 memunculkan
spektrum C13H9N4+ BM 179,07.
2. C13H9N4+ BM 179,07 melepaskan C2H4 BM 28,03 memunculkan spektrum
C11H5N4+ BM 151,04.
3. C11H5N4+ BM 151,04 melepaskan CN- BM 26,00 memunculkan spektrum
35
Gambar 4.9 Fragmentasi spektrum massa puncak butil diklofenak (lanjutan)
Uraian yang dapat dilihat dari Gambar 4.9 adalah sebagai berikut:
1. C10H53+ BM 125,04 melepaskan C3 BM 36 memunculkan spektrum C7H5+
BM 89,04.
2. C7H5+ BM 89,04 melepaskan C4. BM 12 memunculkan spektrum C6H5+ BM
36 BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kesimpulan dari penelitian ini adalah:
1. asam diklofenak dapat diesterifikasi menjadi butil diklofenak dengan persen
rendemen sebesar 19,11%.
2. hasil esterifikasi antara asam diklofenak dan butanol diperoleh senyawa butil
diklofenak yang belum murni.
3. hasil sintesis butil diklofenak dapat ditentukan karakteristiknya dengan uji
titik lebur, FT-IR dan GC-MS. Berdasarkan hasil GC-MS diperoleh senyawa
butil diklofenak dengan luas area 49,61%.
5.2 Saran
Disarankan agar dilakukan penelitian lebih lanjut untuk menetapkan harga
pKa butil diklofenak kemudian dibandingkan dengan metil, etil dan propil
37
DAFTAR PUSTAKA
Aiache, J.M., Devissaguet, J., dan Hermann, A.M.G. (1982). Galenica 2 – Biopharmacie. Second Edition. Penerjemah: Widji Soeratri dan Nanizar Zaman Joenoes. Tahun 1993. Farmasetika 2 Biofarmasi. Edisi II. Surabaya: Airlangga University Press. Halaman 165.
Anonim. (2009). British Pharmacopoeia 2009. London: The Stationery Office. Halaman 1889-1892.
Armarego, W.L.F., dan Chai, C.L.L. (2003). Purification of Laboratory Chemical. Fifth Edition. USA: Elsevier Science. Halaman 14-16.
Bresnick, S.D. (1996). High-Yield Organic Chemistry. Alih bahasa: Hadian Kotong. Tahun 2004. Intisari Kimia Organik. Jakarta: Hipokrates. Halaman 96.
Carey, F.A. (2008). Organic Chemistry. Seventh Edition. New York: McGraw-Hill. Halaman 635.
Fessenden, R.J., dan Fessenden, J.S. (1986). Organic Chemistry. Third Edition. Penerjemah: Aloysius Hadyana Pudjaatmaka. Tahun 2009. Kimia Organik. Edisi III. Jakarta: Erlangga. Halaman 83-84.
Gandjar, I.G., dan Rohman, A. (2012). Analisis Obat Secara Spektrofotometri dan Kromatografi. Yogyakarta: Pustaka Pelajar. Halaman 180-181, 363-396, 407-408 .
Hasan, S.A., dan Elias, A.N. (2014). Synthesis of New Diclofenac Derivatives by Coupling With Chalcone Derivatives as Possible Mutual ProDrugs.
International Journal of Pharmacy and Pharmaceutical Sciences. 6(1): 239-245.
Ismail. (2012). Pedoman Kuliah Teknik Pendekatan Diskoneksi. Fakultas Farmasi Universitas Sumatera Utara. Halaman 118-119.
Kerns, E.H., dan Di, L. (2008). Drug-Like Properties: Concepts, Structure Design and Methods: from ADME to Toxicity Optimization. California: Academic Press. Halaman 54.
38
McNair, H.M., dan Miller, J.M. (2009). Basic Gas Chromatography. Second Edition. USA: John Wiley & Sons, Inc. Halaman 12.
Meislich, H., Nechamkin, H., dan Sharefkin, J. (1980). Theory and Problems of Organic Chemistry. Singapore: McGraw-Hill. Halaman 207.
Moffat, A.C., Osselton, M.D., dan Widdop, B. (2011). Clarke’s Analysis of Drugs and Poisons. Fourth Edition. London: Pharmaceutical Press. Halaman 1238.
Mycek, M.J., Harvey, R.A., Champe, P.C., dan Fisher, B.D. (1997). Lippincott’s Illustrated Reviews: Pharmacology. Second Edition. Alih bahasa: Azwar Agoes. Tahun 2001. Farmakologi Ulasan Bergambar. Edisi II. Jakarta: Penerbit Widya Medika. Halaman 404.
Pavia, D.L., Lampman, G.M., dan Kriz, G.S. (1979). Introduction to Spectroscopy: A Guide for Students of Organic Chemistry. Philadelphia: Saunders College Publishing. Halaman: 13, 26-27, 225.
Riswiyanto. (2009). Kimia Organik. Jakarta: Penerbit Erlangga. Halaman 298.
Roberts, L.J., dan Morrow, J.D. (2001). Senyawa Analgesik-Antipiretik dan Antiradang serta Obat-Obat yang digunakan dalam Penanganan Pirai. Dalam buku: Goodman & Gilman’s Dasar Farmakologi Terapi. Edisi II. Volume 2. Alih bahasa: Tim alih bahasa Sekolah Farmasi ITB. Tahun 2012.. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 666, 688.
Rodig, O.R., Bell, C.E., dan Clark, A.K. (1990). Organic Chemistry Laboratory Standard & Microscale Experiments. United State of America: Saunders College Publishing. Halaman 19, 21.
Santos, J.L., Moreira, V., Campos, M.L., Chelucci, R.C., Barbieri, K.P., Souto, P.C.M.C., Matsubara, M.H., Teixeira, C., Bosquesi, P.L., Peccini, R.G,. dan Chin, C.M. (2012). Pharmacological Evaluation and Preliminary Pharmacokinetics Studies of a New Diclofenac Prodrug without Gastric Ulceration Effect. International journal of Molecular Sciences. 13: 15305-15320.
Silverstein, R.M., Webster, F.X., dan Kiemle, D.J. (2005). Spectrometric Identification of Organic Compounds. Seventh Edition. USA: John Wiley & Sons. Halaman 1,72.
39
Suryawhanshi, S.B., Osman, H.A., Shaikh, Y.I., dan Nazeruddin, G.M. (2014). Synthesis of Various Esters of Diclofenac (NSAIDs) as Pro-Drugs and Their Biological Evaluation. Chemical Science Transactions. 3(2): 562-565.
Tan, H.T, dan Rahardja, K. (2007). Obat-Obat Penting. Khasiat, Penggunaan, dan Efek-Efek Sampingnya. Jakarta: Penerbit PT Elex Media Komputindo. Halaman 330.
Trevor, A.J., Katzung, B.G., dan Masters, S.B. (2002). Katzung & Trevor’s Pharmacology: Examination & Board Review. Sixth Edition. USA: The McGraw-Hill Companies, Inc. Halaman 322-323.
Vogel, A.I. (1979). Textbook of Macro and Semimicro Qualitative Inorganic Analysis. Penerjemah: Setiono dan Hadyana Pudjaaatmaka. Tahun 1990.
Vogel: Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian I. Jakarta: Kalman Media Pustaka. Halaman 217.
40 LAMPIRAN
41
42
43
44
45
46
47
Lampiran 8. Spektrum massa puncak 3 senyawa hasil sintesis
48
Lampiran 9. Data perhitungan pengubahan kalium diklofenak menjadi asam diklofenak
- C14H10Cl2NO2K = kalium diklofenak
BM = 334,3
Mol =
BM massa
C14H10Cl2NO2K =
334,4 gram 15
= 44,8698 mmol
- HCl 37% (b/b)
BM = 36,453
ρHCl = 1, 19 kg/L massa 1L HCl = 1, 19 kg/L 1L
= 1,19 kg
= 1190 gram
Massa 1L HCl 37% = x gram 100
gram 37
1190 gram
= 440,3 gram
N = 1/V
BE massa
×
N HCl 37% =
1L 1 36,5 440,3
×
= 12,06 N
HCl yang digunakan untuk pengubahan kalium diklofenak menjadi asam
diklofenak adalah HCl 2N, sehingga volume yang digunakan untuk reaksi adalah
Volume HCl = n/N
= 44,8698 mmol/2 N
49
Reaksi pengubahan kalium diklofenak menjadi asam diklofenak
M : 44,8698 44,8698 44,8698 - - -
R : 44,8698 44,8698 44,8698 44,8698 44,8698 44,8698
50
Lampiran 10. Data perhitungan hasil pengubahan kalium diklofenak menjadi asam diklofenak
- Massa asam diklofenak teoritis = mol BM
= 44,8698 mmol 296,2
= 13290,4348 mgram
= 13,2904 gram
- Massa asam diklofenak = 12, 216 gram
secara praktek
- % rendemen sebelum rekristalisasi = 100% gram
13,2904 gram 12,216
×
= 91,92%
- % ralat = 100%
gram 13,2904 gram 12,216 -gram 13,2904 × = 8,0840%
- Massa asam diklofenak = 11,6285 gram
setelah rekristalisasi
- % rendemen setelah = 100%
gram 13,2904 gram 11,6285 × rekristalisasi
= 87,50 %
- % ralat = 100%
51
Lampiran 11. Data perhitungan sintesis butil diklofenak
- Asam diklofenak = C14H11Cl2NO2
BM = 296,2
massa C14H11Cl2NO2 = 2,0058 gram
n (mol) C14H11Cl2NO2 = massa/BM
= 2,0058/296,2
= 0,0067 mol
- Butanol = C4H9OH
BM = 74,12
n (mol) = 0,50 mol
Massa C4H9OH = mol BM
= 0,50 mol 74,12
= 37,06 gram
ρ C4H9OH = 0,807 gram/ml
volume C4H9OH = massa/ ρ
= 37,06 gram/0,807 gram/ml
52 Reaksi kesetimbangan sintesis butil diklofenak
M : 0,0067 mol 0,50 mol - -
R : 0,0067 mol 0,0067 mol 0,0067 mol 0,0067 mol
53
Lampiran 12. Data hasil sintesis butil diklofenak
− BM butil diklofenak = 352,25
− Massa butil diklofenak teoritis = mol × BM
= 0,0067 mmol × 352,25
= 2,3600 gram
− Massa butil diklofenak secara praktek = 0,5961 gram
sebelum pemurnian
− % rendemen butil diklofenak = 100% gram
2,3600 gram 0,5961
×
sebelum pemurnian = 25,26%
− % ralat = 100%
gram 2,3600 gram 0,5961 -gram 2,3600 × = 74,74%
− Massa butil diklofenak secara praktek = 0,4510 gram
setelah pemurnian
− % rendemen butil diklofenak = 100% gram
2,3600 gram 0,4510
×
setelah pemurnian = 19,11%
− % ralat = 100%
54
Lampiran 13. Bagan kerja pengubahan kalium diklofenak menjadi asam diklofenak
dimasukkan ke dalam labu alas bulat
dimasukkan magnetic bar
dirangkai dropping funnel yang sudah berisi etanol kering : THF (3:1) di atas labu alas bulat
dihubungkan dropping funnel dengan tabung gas Nitrogen
dibuka keran dropping funnel perlahan-lahan hingga campuran etanol kering dan THF menetes ke labu
sambil diaduk dengan magnetic bar pada suhu 18oC selama 10 menit hingga kalium diklofenak larut sempurna
ditambahkan 23 ml HCl 2N
ditambahkan air dingin sebanyak 750 ml
didinginkan pada lemari es hingga asam diklofenak mengendap
disaring Kalium diklofenak
15 gram
Larutan kalium diklofenak dalam etanol
dan THF
Endapan asam
55
Lampiran 14. Bagan kerja pencucian asam diklofenak
dicuci dengan air suling
disaring
ditetesi dengan AgNO3
Endapan asam diklofenak
Endapan asam
diklofenak Filtrat
56
Lampiran 15. Bagan kerja rekristalisasi asam diklofenak
dilarutkan dalam 30 ml etanol
ditambahkan dengan air suling dingin hingga tidak terbentuk endapan lagi
disaring
dikeringkan di dalam oven selama 15 menit pada suhu 1000C
dimasukkan ke dalam pipa kapiler secukupnya
diuji titik leburnya pada melting point apparatus
Endapan asam diklofenak 1 gram
Endapan asam diklofenak
Filtrat
Kristal asam diklofenak
57
Lampiran 16. Bagan kerja sintesis butil diklofenak
dimasukkan ke dalam labu alas bulat leher tiga
ditambahkan butanol kering