OPTIMASI PROSES HIDROLISIS SERAT MAKANAN (
DIETARY
FIBER
) DARI LIMBAH MENGKUDU DENGAN METODE
RESPON PERMUKAAN
FAIRUZ SARTIKA DEWI
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
ABSTRAK
FAIRUZ SARTIKA DEWI. Optimasi Proses Hidrolisis Serat Makanan (Dietary Fiber) dari Limbah Mengkudu dengan Metode Respon Permukaan. Dibimbing oleh SAPTA RAHARJA.
Produk serat dapat diperoleh dari serat mengkudu (Morinda citrifolia). Ampas yang basah bisa diolah lebih lanjut dengan cara hidrolisis dan pengeringan. Penelitian ini bertujuan untuk meningkatkan nilai tambah ampas mengkudu, mengetahui pengaruh waktu dan konsentrasi asam terhadap respon kadar selulosa, hemiselulosa, SDF dan kadar lignin dengan menggunakan rancangan percobaan RSM orde pertama. Hasil penelitian ini menunjukan bahwa waktu dan konsentrasi asam tidak memberi pengaruh yang nyata terhadap respon hemiselulosa, selulosa dan kadar SDF. Tetapi, kedua faktor ini memberikan pengaruh nyata untuk respon kadar lignin dengan nilai R2 sebesar 0.6489 yang artinya kedua faktor berpengaruh sebesar 64.89% terhadap kadar lignin, sedangkan sisanya 35.11% dipengaruhi oleh faktor lain yang belum diketahui.
Kata kunci: dietary fiber, RSM, SDF (soluble dietary fiber)
ABSTRACT
FAIRUZ SARTIKA DEWI. Hydrolysis Process Optimation of Dietary Fiber From Noni’s Waste with Response Surface Method. Supervised by SAPTA RAHARJA.
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Tujuan 2
Ruang Lingkup Penelitian 2
BAHAN DAN METODE 3
Bahan dan Alat 3
Metode 3
Penyiapan bahan baku 3
Optimasi proses hidrolisis 4
HASIL DAN PEMBAHASAN 5
Karakterisasi Bahan Baku dan Produk 5
Optimasi Proses Hidrolisis 7
SIMPULAN DAN SARAN 12
Simpulan 12
Saran 12
DAFTAR TABEL
1 Nilai rendah (-1) dan tinggi (+1) perlakuan 4
2 Rancangan percobaan orde pertama (first-order model) 5 3 Karakteristik tepung mengkudu sebelum dihidrolisis 5
4 Komposisi Dietary fiber 6
5 Data rancangan percobaan orde 1 7
6 Koefisien parameter dan nilai signifikansi selulosa 8 7 Koefisien parameter dan nilai signifikansi hemiselulosa 9 8 Koefisien parameter dan nilai signifikansi SDF 10 9 Koefisien parameter dan nilai signifikansi lignin 11
DAFTAR LAMPIRAN
1 Prosedur analisis karakterisasi tepung mengkudu 15 2 Prosedur ekstraksi dan hidrolisis serat mengkudu 19 3 Data perubahan komposisi serat mengkudu sebelum dan setelah hidrolisis 22 4 Grafik perubahan komposisi serat pangan sebelum dan sesudah hidrolisis 23 5 Hasil analisis sidik ragam hemiselulosa terhadap pengaruh waktu dan
konsentrasi 23
6 Hasil analisis sidik ragam selulosa terhadap pengaruh waktu dan konsentrasi 24 7 Hasil analisis sidik ragam SDF terhadap pengaruh waktu dan konsentrasi 24 8 Hasil analisis sidik ragam kadar lignin terhadap pengaruh waktu dan
PENDAHULUAN
Latar Belakang
Tanaman mengkudu merupakan tanaman hijau yang banyak ditemukan pada kawasan pantai terbuka dan hutan. Jawa Barat merupakan daerah yang potensial bagi pengembangan mengkudu karena memiliki keunggulan lahan yang subur (Winarti 2005). Menurut data statistik Departemen Pertanian (2003) tanaman mengkudu dibudidayakan di 15 propinsi seluas 23 hektar dengan produksi sekitar 1.910 ton dan meningkat menjadi 73 hektar pada tahun 2004 dengan produksi sebesar 3.509 ton.
Jenis buah ini umumnya dihindari oleh kebanyakan orang karena mempunyai bau yang kurang sedap. Namun, mengkudu mempunyai banyak khasiat untuk kesehatan. Buah mengkudu mengandung dua belas zat aktif yang berkhasiat untuk pengobatan, diantaranya adalah anthraquinon dan scopoletin yang aktif sebagai antimikroba, terutama bakteri dan jamur sehingga penting untuk mengatasi alergi dan peradangan (Hirazumi et al. 1996). Selain itu, buah
mengkudu sampai sekarang masih dimanfaatkan sebagai jamu tradisional untuk mengobati radang tenggorokan, demam dan tekanan darah tinggi. Bahkan, sebagian orang menjadikan buah mengkudu ini sebagai salah satu buah-buahan yang diolah menjadi juice untuk diambil sari buahnya. Selain itu tepung buah mengkudu juga mengandung serat kasar yang tinggi yaitu 33.7 % (Susanti dan Amin 2002).
Pemanfaatan buah mengkudu sebagai bahan baku industri pangan dan non pangan telah banyak dilakukan. Buah mengkudu terdiri dari daging buah, biji dan sari buah. Pada umumnya pemanfaatan mengkudu baru sebatas pada sari buahnya dan bagian lain belum dimanfaatkan dengan optimal. Kebanyakan industri pengolahan mengkudu hanya memanfaatkan sari buahnya, sedangkan limbah padat yang dihasilkan mencapai 60 % masih belum dimanfaatkan dan dibuang sebagai limbah padat atau dikomposkan sebagai pupuk. Limbah yang dihasilkan pada produksi pengolahan sari buah mengkudu adalah kulit buah, biji dan daging buah mengkudu. Daging buah mengkudu yang diambil sarinya berupa ampas merupakan limbah padat yang dihasilkan dari industri pengolahan mengkudu.
Pada tingkat konsumen sebenarnya tidak sulit untuk mendapatkan serat pangan berupa sayur maupun buah-buahan, akan tetapi dengan makin kompleksnya kehidupan masyarakat terutama di daerah perkotaan sehingga kesulitan untuk mendapatkan serat pangan menjadi kendala tersendiri (Jatraningrum 2012). Hasil penelitian menunjukkan bahwa rata-rata konsumsi serat masyarakat Indonesia masih jauh dari kebutuhan serat yang dianjurkan yaitu minimal 30 g/hari, sedangkan konsumsi serat rata-rata antara 9.9–10.7 g/hari (Jahari dan Sumarno 2002). Oleh karena itu, kebutuhan tubuh akan serat harus dipenuhi dari sumber lain berupa tambahan untuk mencegah timbulnya penyakit yang disebabkan oleh pencernaan.
Salah satu alternatif serat pangan dapat diekstraksi dari ampas mengkudu. Proses hidrolisis serat mengkudu menggunakan asam dipengaruhi beberapa faktor diantaranya suhu, konsentrasi asam dan waktu hidrolisis. Perlakuan setiap sampel akan mempengaruhi kadar serat yang dihasilkan seperti rendemen, total serat larut, serat tidak larut, kadar selulosa, hemiselulosa, lignin serta senyawa ekstraktif yang terkandung dalam bahan. Dalam rangka memaksimalkan produksi serat mengkudu dengan kualitas yang baik diperlukan proses optimalisasi faktor-faktor yang berpengaruh. Penggunaan faktor-faktor yang tepat dapat menentukan kondisi optimal setiap faktor dengan jumlah perlakuan dan waktu yang lebih singkat.
Response Surface Method (RSM) merupakan suatu metode yang memungkinkan peneliti pendapatkan penjelasan yang menyeluruh mulai dari desain penelitian, pengolahan data dan solusi optimasi. Menurut Wahjudi dan Amelia (2002) RSM merupakan metode gabungan antara teknik matematika dan statistik untuk membuat model dan menganalisa suatu respon y yang dipengaruhi oleh beberapa faktor x untuk mengoptimalkan respon tersebut. Penggunaan metode ini diharapkan mampu menghasilkan produksi optimal dari serat mengkudu.
Tujuan
1. Mempelajari proses ekstraksi serat makanan (Dietary Fiber) dari limbah padat industri mengkudu dengan cara ektraksi dan hidrolisis asam.
2. Mempelajari pengaruh waktu hidrolisis dan konsentrasi asam sulfat yang digunakan untuk hidrolisis serta menentukan kondisi optimal proses hidrolisis dengan metode respon permukaan
Ruang Lingkup Penelitian
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan pada penelitian ini adalah ampas mengkudu yang didapatkan dari limbah padat industri pengolahan sari buah mengkudu PT. Deherba Indonesia, Bogor Jawa Barat, larutan H2SO4, Na2CO3 1% , aquades, heksana, larutan ADF, aseton, etanol, larutan NDF, CTAB, ADTA-2Na, sodium lauril sulfat, HCl, enzim termamyl, enzim pankreatin dan bahan-bahan kimia umum lainnya yang dibutuhkan untuk analisa tepung dietary fiber.
Alat-alat yang digunakan untuk mendapatkan serat dari ampas mengkudu, hidrolisis dan analisa adalah oven dan penyaring, diskmill, autoklaf, desikator, sentrifuse, vakum, soxhlet lemak, filter glass 2-G-3, alat atau wadah pemisah serat dan pembuatan serat mengkudu serta peralatan laboratorium untuk analisa sifat fisik dan kimia dari serat mengkudu.
Metode
Penelitian ini dilakukan dalam beberapa tahapan yaitu penyiapan bahan baku dan karakterisasi produk serta optimasi proses hidrolisis.
Penyiapan dan karakterisasi bahan baku
Menurut Wardworth et al. (2001) metode ekstraksi dietary fiber dari buah mengkudu dilakukan dengan memisahkan serat dengan sari buah mengkudu. Pada penelitian ini digunakan ampas mengkudu yang didapatkan dari PT Deherba Indonesia. Ampas mengkudu yang masih mengandung sisa-sisa sari buah dan biji, dicuci dan dipisahkan antara ampas bersih dengan biji. Ampas bersih yang didapatkan kemudian dicuci berkali-kali dengan air panas sampai bersih dalam kain saring dan dilakukan secara manual. Ampas yang sudah dicuci kemudian dikeringkan dengan oven pengering pada suhu 55-60 oC selama 5-6 jam. Selanjutnya dilakukan penggilingan menggunakan diskmill untuk mendapatkan tepung mengkudu dengan ukuran 60 mesh. Tepung mengkudu sebelum melalui proses hidrolisis dilakukan karakterisasi sebagai acuan terhadap mutu awal bahan yang didapatkan. Prosedur karakterisasi dan proses ektraksi bahan dapat dilihat pada Lampiran 1 dan Lampiran 2.
Optimasi proses hidrolisis
Permasalahan yang sering ditemukan pada metode permukaan respon adalah belum diketahuinya hubungan antara variabel respon dengan variabel independen. Pengolahan data pada penelitian ini dilakukan dengan menggunakan bantuan software Minitab 16. Langkah-langkah yang dilakukan dalam optimasi menggunakan RSM yaitu menetapkan taraf masing-masing peubah bebas, merancang percobaan orde pertama, melakukan analisis varian, pencarian taraf disekitar daerah optimal dan apabila dalam analisis varian uji simultan signifikan dan model yang didapat sesuai, maka dilakukan rancangan menggunakan orde kedua (Dewi 2013).
Langkah pertama yang dilakukan dalam penelitian ini adalah dengan mencari bentuk hubungan antara respon dengan faktor yang digunakan. Bentuk hubungan linier merupakan bentuk hubungan yang dicobakan pertama kali karena merupakan bentuk hubungan yang paling sederhana. Jika ternyata bentuk hubungan antara respon dengan faktor adalah fungsi linier, pendekatan fungsinya disebut dengan first-order model. Jika bentuk hubungan merupakan kuadrat, maka untuk pendekatan fungsinya digunakan deraat polinomial yang lebih tinggi yaitu second-order model. Hubungan antara respon Y dan faktor A dapat dicari menggunakan first order models dan second order models, dimana first order models digunakan untuk mencari daerah optimal dan second order models digunakan untuk mencari titik optimal (Jari et al. 2002).
Pada penelitian ini dilakukan pendekatan first-order model dengan dua faktor perlakuan yaitu waktu hidrolisis (A) dan konsentrasi asam sulfat (B). Besarnya nilai konsentrasi dan waktu hidrolisis dapat dilihat pada Tabel 1.
Table 1 Nilai rendah (-1) dan tinggi (+1) perlakuan
Jenis Perlakuan Nilai Rendah (-1) Nilai Tinggi (+1)
Waktu [A] (menit) 30 90
Konsentrasi Asam [B] (%) 0.25 0.75
Parameter respon yang digunakan dalam menentukan kualitas serat adalah kadar hemiselulosa, kadar selulosa, kadar serat larut dan kadar lignin. Optimasi dilakukan untuk mengetahui pengaruh dari masing-masing faktor perlakuan terhadap respon tersebut dengan 2k ditambah 5 center point. Rancangan penelitian pada tahap orde pertama dapat dilihat pada Tabel 2. Pada software ini akan dilihat keragaman dan pengaruh faktor terhadap respon.
Model rancangan percobaan untuk mengetahui pengaruh linier dari kedua faktor terhadap respon adalah sebagai berikut.
y = ̥ ∑ ̥ � + �=1
∑ ̥ � � <
Keterangan:
Y = Respon dari masing-masing perlakuan ̥ ,̥ ,̥ j = Koefisien parameter
Tabel 2 Rancangan percobaan orde pertama (first-order model)
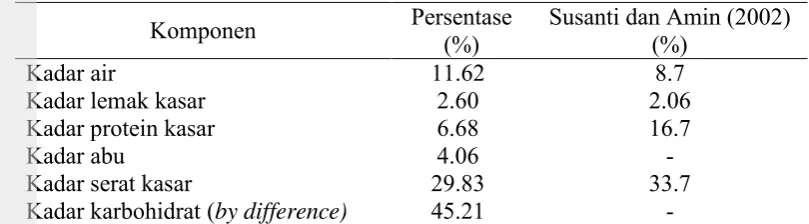
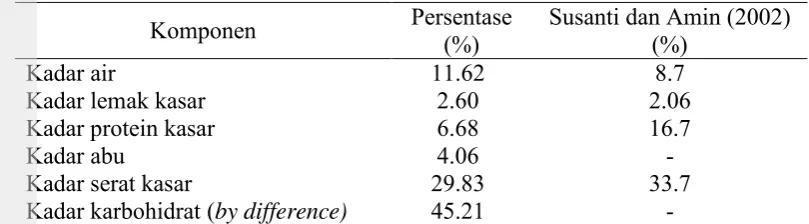
Karakterisasi bahan baku bertujuan untuk mengetahui karakteristik tepung mengkudu. Karakterisasi yang dilakukan meliputi analisis kadar air, kadar abu, kadar lemak kasar, kadar protein kasar, kadar serat kasar dan kadar karbohidrat (by difference). Hasil karakteristik tepung mengkudu terdapat pada Tebel 3.
Tabel 3 Karakteristik tepung mengkudu sebelum dihidrolisis
Komponen Persentase (%) Susanti dan Amin (2002) (%)
Berdasarkan Tabel 3 dapat diketahui bahwa hasil karakterisasi bahan baku yang diperoleh pada penelitian ini berbeda dengan penelitian yang dilakukan oleh Susanti dan Amin (2002). Hal ini disebabkan karena varietas mengkudu yang digunakan berbeda. Tepung mengkudu yang diperoleh dari penelitian ini berasal dari ampas atau limbah buah mengkudu yang telah diambil sari buahnya. Ampas yang digunakan berasal dari varietas buah mengkudu yang berbeda-beda sehingga kemungkinan berpengaruh terhadap karakteristik awal tepung. Akan tetapi kandungan nilai nutrisi dari tepung mengkudu sesuai dengan standar yang biasanya digunakan untuk beberapa jenis tepung-tepungan.
Tabel 2 Rancangan percobaan orde pertama (first-order model)
Karakterisasi bahan baku bertujuan untuk mengetahui karakteristik tepung mengkudu. Karakterisasi yang dilakukan meliputi analisis kadar air, kadar abu, kadar lemak kasar, kadar protein kasar, kadar serat kasar dan kadar karbohidrat (by difference). Hasil karakteristik tepung mengkudu terdapat pada Tebel 3.
Tabel 3 Karakteristik tepung mengkudu sebelum dihidrolisis
Komponen Persentase (%) Susanti dan Amin (2002) (%)
Berdasarkan Tabel 3 dapat diketahui bahwa hasil karakterisasi bahan baku yang diperoleh pada penelitian ini berbeda dengan penelitian yang dilakukan oleh Susanti dan Amin (2002). Hal ini disebabkan karena varietas mengkudu yang digunakan berbeda. Tepung mengkudu yang diperoleh dari penelitian ini berasal dari ampas atau limbah buah mengkudu yang telah diambil sari buahnya. Ampas yang digunakan berasal dari varietas buah mengkudu yang berbeda-beda sehingga kemungkinan berpengaruh terhadap karakteristik awal tepung. Akan tetapi kandungan nilai nutrisi dari tepung mengkudu sesuai dengan standar yang biasanya digunakan untuk beberapa jenis tepung-tepungan.
tumbuh adalah pada kadar air 14-15 % (Ferdiaz 1989). Produk dalam bentuk tepung memang dianjurkan agar memiliki tingkat kadar air yang rendah karena produk ini sangat riskan terhadap pertumbuhan jamur selama proses penyimpanan (Sulistyawati et al 2012).
Kandungan kadar abu yang kecil pada tepung mengkudu menunjukan bahwa kualitas dari bahan bagus. Semakin tinggi kadar abu pada bahan menunjukan kualitas yang kurang baik, karena dalam kandungan nutrisi bahan tersebut banyak terdapat mineral-mineral anorganik (Afrianti 2004). Analisa proksimat menunjukan bahwa tepung mengkudu mengandung serat yang cukup tinggi untuk dapat dimanfaatkan sebagai produk minuman berserat pangan yang mengandung serat.
Selain analisa proksimat dilakukan analisa terhadap komposisi serat yang terdapat pada tepung mengkudu sebelum dihidrolisis. Komposisi seratdari tepung mengkudu pada Tabel 4.
Tabel 4 Komposisi serat tepung mengkudu
Komponen Persentase (%bk)
Setelah dihidrolisis dilakukan karakterisasi terhadap komposisi serat pangan yang dihasilkan. Serat pangan merupakan bagian dari pangan yang tidak dapat dihidrolisis oleh enzim-enzim pencernaan, meliputi selulosa, hemiselulosa, lignin, pentosan, gum, dan senyawa pektin. Deddy Muchtadi (2001),menyebutkan bahwa berdasarkan kelarutannya serat pangan terbagi menjadi dua kelompok, yaitu serat pangan larut (soluble dietary fiber) dan serat tidak larut (insoluble dietary fiber). Serat yang larut terdiri atas pektin dan gum serta sebagian hemiselulosa yang banyak terdapat pada buah dan sayur, termasuk dalam serat ini adalah selulosa, hemiselulosa dan lignin, yang banyak ditemukan pada seralia, kacang-kacangan dan sayuran. Soluble dietary fiber adalah serat makanan yang dapat larut dalam air panas atau dingin serat dapat terendap oleh air yang telah bercampur dalam etanol. Sedangkan insoluble dietary fiber tidak larut dalam air panas maupun dingin. Senyawa-senyawa yang banyak terdapat pada serat pangan ini biasanya ditambahkan ke dalam makanan dan minuman atau digunakan sebagai food suplemen.
Optimasi Proses Hidrolisis
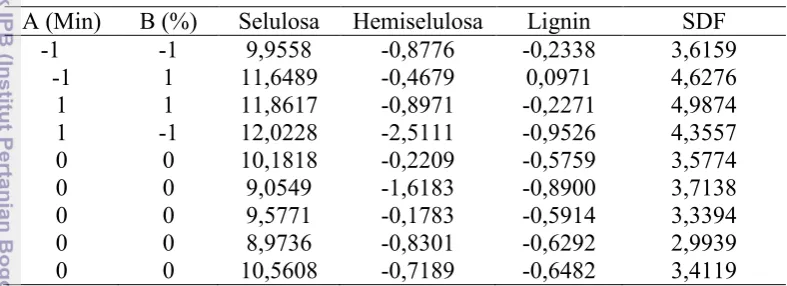
Penelitian ini menggunakan dua faktor yang dianggap mempengaruhi proses hidrolisis serat yaitu waktu (A) dan konsentrasi asam (B). Dalam penelitian ini waktu yang ingin diteliti yaitu 30–90 menit dan konsentrasi asam sulfat 0.25% -0.75%. RSM merupakan suatu metode yang menggunakan dua orde yaitu orde 1 (first-order model) dan orde 2 (second-order model). Pada penelitian ini dilakukan tahapan percobaan orde 1 dimana pada tahapan ini memerlukan rancangan percobaan yang terdiri dari rancangan faktorial 2k dan 5 rancangan titik pusat. Rancangan faktorial terdiri dari kombinasi taraf tertinggi dan terendah masing-masing faktor dan rancangan titik pusat terdiri dari kombinasi nilai tengah dari faktor (Montgomery 2001). Dari rancangan percobaan orde 1 diperoleh data perubahan komponen serat sesudah hidrolisis dengan menggunakan 2 faktor seperti pada Tabel 5.
Tabel 5 Data rancangan percobaan orde 1
A (Min) B (%) Selulosa Hemiselulosa Lignin SDF
Selulosa merupakan senyawa organik yang paling melimpah di bumi. Diperkirakan sekitar 1011 ton selulosa dibiosintesis setiap tahun (Fatmawati 2008). Selulosa juga merupakan senyawa penyusun utama dari jaringan serat dan dinding tanaman. Selulosa adalah komponen serat tidak larut utama dalam diet yang terdiri dari 10.000 atau lebih unit glukosa yang berikatan β-(1,4)-glukosida. Dalam dinding sel, senyawa ini terdapat dalam bentuk mikrofibril yang terdiri dari beberapa rantai molekul dan membentuk kumpulan yang sangat kokoh sehingga mempunyai sifat tahan terhadap reaksi-reaksi kimia. Dalam sel tanaman selulosa juga selalu terdapat bersama-sama dengan hemiselulosa dan lignin. Berdasarkan sifat larutnya selulosa merupakan senyawa yang tidak larut dalam air.
Analisa pengaruh waktu dan konsentrasi terhadap respon selulosa menggunakan software minitab 16 dieroleh model RSM orde 1 adalah :
Y = 10.4264 + 0.5699 A + 0.3830 B – 0.4636 AB.
Tabel 6 Koefisien parameter dan nilai signifikansi selulosa
Dari Tabel 6 dilihat bahwa tidak terjadi perbedaan kadar selulosa dengan adanya perbedaan waktu dan konsentrasi asam. Hal ini juga terlihat dari nilai R2 sebesar 0.2470, artinya secara statistika faktor waktu dan konsentrasi asam hanya berpengaruh sebesar 24.70% terhadap kadar selulosa sedangkan sisanya dipengaruhi oleh faktor lain yang belum diketahui. Namun, pada Lampiran 5 dan dari koefisien intersep (+) dapat dilihat bahwa terjadi penurunan nilai kadar selulosa sesudah dihidrolisis. Penurunan kadar selulosa ini terjadi karena hidrolisis bagian amorf dari selulosa menjadi monosakarida dan oligosakarida. Molekul selulosa terdiri dari bagian amorf dan bagian berkristal. Bagian amorf merupakan bagian yang pertama-tama akan dipecah oleh pelarut atau pereaksi kimia. Tsao et al. (1978), menyatakan bahwa bagian amorf pada selulosa lebih mudah dihidrolisis dari pada bagian berkristal.
Susunan bagian berkristal pada selulosa bersifat lebih teratur dan rapat. Bagian ini sukar bereaksi dengan pereaksi tertentu. Pada bagian ini pengikatan antar struktur selulosa terutama disebabkan karena adanya ikatan hidrogen yang berfungsi untuk memperkuat struktur mikrofibril. Sebagai akibatnya bagian berkristal ini tidak larut dalam air dan bersifat sangat stabil (Whistler et al 1985). Selulosa terdiri dari 15% bagian amorf dan 85% sisanya adalah bagian mengkristal. Untuk menghidrolisis bagian yang mengkristal diperlukan asam kuat dan suhu yang tinggi. Penurunan kadar selulosa pada serat mengkudu yang sudah dihidrolisis tidak terlalu besar diduga karena suhu yang digunakan tidak terlalu tinggi yaitu 121oC, sedangkan selulosa bagian berkristal hanya dapat dihidrolisis dengan suhu yang sangat tinggi.
Kadar hemiselulosa
Hemiselulosa termasuk komponen serat pangan yang sifatnya tidak larut dalam air. Hemiselulosa merupakan polisakarida yang mempunyai derajat polimerisasi yang lebih rendah dari selulosa, lebih mudah larut dalam alkali dan sukar larut didalam asam. Hemiselulosa lebih sedikit mengkristal, oleh karena itu lebih mudah larut daripada selulosa dan dapat dicerna dalam usus besar. Pada analisa pengaruh waktu dan konsentrasi terhadap respon hemiselulosa menggunakan software minitab 16 dieroleh model RSM orde 1 adalah :
Y = - 0.9245 - 0.5157 A + 0.5059 B + 0.3011 AB.
Tabel 7 Koefisien parameter dan nilai signifikansi hemiselulosa
Pada Tabel 7 terlihat bahwa pada selang kepercayaan 84.8 % faktor waktu (A) berpengaruh tetapi tidak signifikan terhadap respon. Semakin tinggi waktu hidrolisis semakin kecil kadar hemiselulosa. Hal ini disebabkan karena semakin lama waktu hidrolisis akan semakin banyak komponen hemiselulosa yang terdegradasi dan mudah larut dalam air sehinngga terbuang pada saat pencucian. Pada selang kepercayaan 84.2 % konsentrasi asam berpengaruh tidak signifikan terhadap respon. Semakin kecil konsentrasi asam semakin kecil kadar hemiselulosa yang dihasilkan.
Hemiselulosa berbeda dengan selulosa, hemiselulosa mempunyai sifat yang mudah larut dalam alkali dan sukar larut dalam asam. Menurut Southgate et al (1985), ada sebagian dari komponen hemiselulosa yang asalnya tidak larut dalam air tapi larut dalam alkali dapat larut pada saat ekstraksi dengan menggunakan asam. Hidrolisis hemiselulosa dengan menggunakan asam kuat atau encer akan menghasilkan heksosa dan pentosa. Hidrolisis lebih lanjut akan menghasilkan furfural dan produk terdekomposisi lainnya (Gong et al 1981).
Berdasarkan koefisien intersep yang bernilai negatif menunjukan bahwa terjadinya peningkatan kadar hemiselulosa setelah dilakukan hidrolisis. Hal ini disebabkan karena adanya ikatan-ikatan kimia antara hemiselulosa dan lignin yang menghambat hidrolisis. Hemiselulosa bersama-sama dengan selulosa membangun dinding sel yang teguh didalam jaringan lignin. Menurut Sjostrom (1981), terdapat ikatan-ikatan kimia antara lignin dan semua kontituen hemiselulosa. Ikatan-ikatan tersebut berupa ikatan ester atau eter dan bahkan mungkin ikatan glikosidik. Hemiselulosa terbungkus oleh jaringan lignin, diduga pada pengukuran kadar hemiselulosa, lignin yang berikatan dengan hemiselulosa juga terukur.
Kadar serat larut (SDF)
Dari persamaan linear diatas dapat diketahui bahwa faktor waktu (A) dan konsentrasi (B) berpengaruh positif terhadap respon. Data hasil pengujian kadar SDF disajikan pada Lampiran 7. Koefisien parameter dan nilai signifikansi analisa selulosa disajikan pada Tabel 8. Nilai R2 SDF pada Tabel 8 sebesar 0.2907 artinya pengaruh kedua faktor terhadap respon SDF hanya sebesar 29.07%, sedangkan sisanya dipengaruhi oleh faktor lain yang belum diketahui.
Tabel 8 Koefisien parameter dan nilai signifikansi SDF
Parameter Koefisien Signifikansi signifikan terhadap respon SDF. Hal ini disebabkan karena tidak adanya pengaruh yang signifikan terhadap faktor hemiselulosa dan selulosa, dimana perubahan kedua kadar tersebut harusnya berpengaruh terhadap kadar SDF karena pada saat hidrolisis semakin banyak komponen tidak larut yang terdegradasi. Tidak adanya pengaruh kedua faktor terhadap ketiga respon diatas diduga karena terlalu jauhnya selang taraf faktor yang diteliti. Menurut Grethlein (1975), hidrolisis dengan menggunakan asam terbagi menjadi dua tahap. Pertama, hidrolisis menggunakan asam encer (H2SO4 1%), suhu 80-121 oC dan waktu 30-240 menit. Kedua, dengan menggunakan asam kuat (H2SO4 5-10 %) pada suhu 180 oC dan waktu diatas 240 menit. Sehingga penggunaan taraf yang pada penelitian ini tidak memperlihatkan perbedaan yang signifikan.
Berdasarkan koefisien intersep yang bernilai positif menunjukan bahwa terjadinya penurunan kadar SDF setelah dilakukan hidrolisis. Hal ini disebabkan karena komponen-komponen senyawa pektat pada serat mengkudu ikut larut pada saat hidrolisis dan pencucian serta proses netralisasi setelah hidrolisis. Pada saat hidrolisis asam akan mendegradasi komponen polisakarida serat menjadi molekul yang lebih kecil dan bersifat lebih larut. Secara alami selulosa bersifat tidak larut dalam air, namun selulosa yang reaktif terhadap asam akan banyak terdegradasi menjadi molekul yang lebih kecil sehingga lebih larut.
Kadar lignin
Lignin merupakan satu-satunya serat pangan yang bukan karbohidrat, yaitu senyawa yang menyebabkan dinding sel menjadi keras. Lignin adalah senyawa gabungan karbon, hidrogen dan oksigen dengan proporsi karbon yang tinggi Howard (2003). Ikatan karbon dan ikatan eter antara unit-unit monomer pada lignin mempunyai kestabilan yang luar biasa terhadap hidrolisis kimia. Disamping itu, lignin juga berikatan dengan komponen dining sel yang lainnya seperti ikatan dengan selulosa dan hemiselulosa menghasilkan suatu struktur dengan ketahanan yang luar biasa terhadap perubahan fisika dan kimia (Theander dan Aman 1979).
Pada analisa pengaruh waktu dan konsentrasi terhadap respon kadar lignin menggunakan software minitab 16 dieroleh model RSM orde 1 adalah :
Y = - 0.5168 - 0.2607 A + 0.2641 B + 0.0987 AB.
Dari persamaan linear diatas dapat diketahui bahwa faktor waktu (A) berpengaruh negatif terhadap respon. Sedangkan faktor konsentrasi asam (B) berpengaruh positif terhadap respon. Data hasil pengujian kadar lignin disajikan pada Lampiran 8. Koefisien parameter dan nilai signifikansi analisa lignin disajikan pada Tabel 9. Nilai R2 lignin pada Tabel 9 sebesar 0.6489 artinya pengaruh kedua faktor terhadap respon kadar lignin hanya sebesar 64.89%, sedangkan sisanya dipengaruhi oleh faktor lain yang belum diketahui.
Tabel 9 Koefisien parameter dan nilai signifikansi lignin
Parameter Koefisien Signifikansi
Dari Tabel 9 dapat dilihat bahwa pada selang kepercayaan 90.6 % faktor waktu (A) memberikan pengaruh yang signifikan terhadap respon. Semakin lama waktu hidrolisis maka akan semakin kecil kadar lignin. Proses hidrolisis dipengaruhi oleh lamanya waktu hidrolisis, semakin lama waktu semakin banyak komponen serat (lignin) yang didegradasi dan bersifat lebih larut. Pada selang kepercayaan 90.09 % konsentrasi asam berpengaruh signifikan terhadap respon. Semakin kecil konsentrasi asam yang digunakan maka akan semakin kecil kadar lignin yang dihasilkan.
komponen-komponen hasil reaksi Maillard yang signifikan dan begabung secara kimiawi dengan fraksi lignin.
Gambar 1 Perubahan warna cairan serat setelah dihidrolisis
SIMPULAN DAN SARAN
Simpulan
Berdasarkan penelitian ini dapat disimpulkan bahwa waktu dan konsentrasi asam tidak memberi pengaruh yang signifikan terhadap respon hemiselulosa, selulosa dan kadar SDF. Hal ini disebabkan karena perbedaan taraf terendah dan tertinggi dari waktu dan konsentrasi yang terlalu jauh, sehingga tidak terlihat perbedaan yang signifikan terhadap respon. Tetapi kedua faktor ini memberikan pengaruh yang signifikan untuk respon kadar lignin dengan nilai R2 sebesar 0.6489. Nilai R2 menunjukan bahwa pengaruh kedua faktor hanya sebesar 64.89%, sedangkan sisanya 35.11 % dipengaruhi oleh faktor lain yang belum diketahui.
Saran
komponen hasil reaksi Maillard yang signifikan dan begabung secara kimiawi dengan fraksi lignin.
Gambar 1 Perubahan warna cairan serat setelah dihidrolisis
SIMPULAN DAN SARAN
Simpulan
Berdasarkan penelitian ini dapat disimpulkan bahwa waktu dan konsentrasi asam tidak memberi pengaruh yang signifikan terhadap respon hemiselulosa, selulosa dan kadar SDF. Hal ini disebabkan karena perbedaan taraf terendah dan tertinggi dari waktu dan konsentrasi yang terlalu jauh, sehingga tidak terlihat perbedaan yang signifikan terhadap respon. Tetapi kedua faktor ini memberikan pengaruh yang signifikan untuk respon kadar lignin dengan nilai R2 sebesar 0.6489. Nilai R2 menunjukan bahwa pengaruh kedua faktor hanya sebesar 64.89%, sedangkan sisanya 35.11 % dipengaruhi oleh faktor lain yang belum diketahui.
Saran
DAFTAR PUSTAKA
Afrianti L.H. 2004. Pati Termodifikasi Dibutuhkan Industri Makanan. http://www.pikiran-rakyat.com [Internet].[17 Juni 2014].
AOAC. 1984. Official Methods of the Association Official Analytical Chemist, AOAC.Washington (US): Inc.
Belo P.S.Jr, B.O.D. Lumen. 1980. Pectic substance content of detergent extracted dietary fiber. J Agr Food Chem. 29:370-373.
Blumenkrantz N,G Asboe-Hamsen. 1973. New methods for quantitative determination of uronic acid. Anal Biochem. 54:484:373.
Departemen Pertanian. 2004. Luas Panen dan Produktivitas Tanaman Mengkudu. http://database.deptan.go.id. [Internet] [20 Maret 2014].
Dewi Ade Kusuma, I wayan Sumarjaya, I Gudti Ayu Made Srinadi. 2013. Penerapan Metode Respon dalam Masalah Optimalisasi. E- J Matematika. 2 (2): 32-36.
Fardiaz S. 1989. Mikrobiologi Pangan I. PAU Pangan Gizi. Bogor [ID]. Institut Pertanian Bogor.
Fatmawati A, N Soeseno, N Chiptadi, S Natalia. 2008. Hidrolisis Batang Padi dengan Menggunakan Asam Sulfat Encer. J Tek Kimia. 3 (1): 187-191. Gong C.S, Li.George. 1981. Conversion of Hemicellulose Carbohydrates. Di
dalam Raharja. Ekstraksi dan Analisa Dietary Fiber dari Buah Mengkudu. J Tek Ind Pert. 14(1): 30-39. Bogor [ID]. IPB.
Hermiati Euis et al. 2010. Pemamfaatan Biomassa Lignoselulosa Ampas Tebu Untuk Produksi Bioetanol. J Litbang Pert. 29 (4): 121-130.
Hirazumi A, E. Furuzawa, S.C. Chou, Y. Hokama. 1996. Immunomodulation contributes to the anticancer activity of morindacitrifolia (noni) fruit juice. Proc West Pharmacol Soc. 39: 7−9.
Howard RL, Abotsi, E Van Rensburg. 2003. Lignocellulose Biotechnology: Issues of Bioconversion and Enzyme Production. African Biotechnol, J Biotech. 12 (4): 602-619.
Jahari A.B, I. Sumarno. 2002. Status Gizi Penduduk Indonesia. Majalah Pangan. Jari Rahardjo et al. 2002. Optimasi Produksi dengan Metode Response Surface. J
Tek Ind. 4 (1): 36-44.
Jatraningrum Diah A. 2012. Analisis Tren Penelitian Pangan Fungsional: Kategori Bahan Serat Pangan. J Teknol Ind Pangan. 23 (1): 64-68.
Marsono Yustinus. 2008. Prospek Pengembangan Makanan Fungsional. J Teknol Pangan. 7 (1): 19-27.
Meyer L.H. 1971. Food Chemistry. Tokyo [JPN]. Chat. E. Tut.CO.
Montgomery DC. 2001. Design and Analysis of Experimental 5th Edition. New York (US): John Wiley & Son.
Muchtadi D. 2001. Sayuran sebagai sumber serat pangan untuk mencegah timbulnya penyakit degeneratif. J Teknol Ind Pangan. 7(1):64-70.
Sjostrom E. 1981. Wood Chemistry Fundamentals and Aplications. California [US]. Academic Press Inc.
Spiller G. 2001. Handbook of Dietary Fiber in Human Nutrition 3rd Edition. London [US]. CRC Press.
Sulistyawati, Wignyanto, Kumalaningsih. Produksi Tepung Buah Lindur Rendah
Tanin dan HCN Sebagai Bahan Pangan Alternatif. J Tek Pert. 13(3):
187-198.
Susanti N. 2002. Pengaruh Pemberian Tepung Mengkudu (Morinda citrifolia L)
dalam Ransum Performans Ayam Broiler [Skripsi]. Bengkulu [ID]. Fakultas pertanian Universitas Bengkulu.
Theander O, P. Aman. 1979. The Chemistry, Morphology and Analysis of Dietary Fiber Components. Di dalam Raharja. Ekstraksi dan Analisa Dietary Fiber dari Buah Mengkudu. J Tek Ind Pert. 14(1):30-39.
Tsao G.T., M. Ladisch, T. Chou. 1978. Fermentation Substrates from Cellulosic Materials Production of Fermentable sugars from Cellulosic Materials. Di dalam D. Perlman (eds). Annual Reports on Fermentation processes Vol 2. New York [US]. Academic Press.
Wadsworth .J.J,S.P. Story C.J.Jensen. 2001. Morinda citrifolia dietary fiber and method. United State of Patent. No.6254913.
Wahyudi Didik, Amelia. 2002. Optimasi Kekerasan Kampas Rem dengan Metode Desain Eksperimen. J Tek Mesin. 4 (1): 60-68.
Whistler R.L, J.R. Daniel. 1985. Carbohydrates. Di Dalam D.R. Fennema. Food Chemistry. New York [US]. Marcell Deckker Inc.
Winarno F.G. 1997. Kimia Pangan dan Gizi. Jakarta [ID]. PT Gramedia Utama. Winarti Christina. 2005. Peluang Pengembangan Minuman Fungsional dari Buah
LAMPIRAN
Lampiran 1 Prosedur analisis karakterisasi tepung mengkudu 1. Kadar Air ( AOAC 1984 )
Sebanyak 5 g contoh tepung dietary fiber ditimbang dalam wadah yang telah diketahui berat keringnya terlebih dahulu. Wadah beserta isinya dipanaskan dalam oven dengan suhu 105oC selama 3-5 jam. Selanjutnya bahan didinginkan dalam desikator dan ditimbang.
Kadar air % = Berat air yang menguap g Berat awal contoh g x %
2. Kadar Abu ( AOAC 1984 )
Sebelum pengabuan, cawan porselin dipanaskan dalam tanur, didinginkan, dikeringkan dalam desikator dan ditimbang sebagai berat cawan. Sebanyak 5 g contoh ditempatkan pada cawan porselin yang telah diketahui beratnya, kemudian dimasukan dalam tanur dan dipijarkan pada suhu 600oC hingga berat tetap, kemudian didinginkan dalam desikator dan ditimbang.
Kadar abu % = berta contoh g x Berat abu g %
3. Kadar Lemak Kasar ( AOAC 1984 )
Metode yang digunakan dalam analisa lemak adalah metode ekstraksi soxhlet. Labu lemak yang digunkan dikeringkan dalam oven, kemudian didinginkan dalam desikator dan ditimbang beratnya. Sebanyak 5 g contoh dibungkus dengan kertas saring dan kemudian dimasukan ke dalam alat ekstraksi soxhlet. Alat kondensor diletakan dibawahnya. Pelarut heksan dimasukan ke dalam labu lemak secukupnya. Selanjutnya dilakukan refluks selama minimal 6 jam selama pelarut yang turun kembali kedalam lemak bewarna jernih. Pelarut dalam lemak didestilasi dan ditampung kembali, kemudian palarut yang berisi lemak hasil ekstraksi dipanaskan dalam oven pada suhu 105oC hingga mencapai berat tatap, kemudian didinginkan dalam desikator. Selanjutnya labu beserta lemak didalamnya ditimbang dan berat lemak dapat diketahui.
Kadar Lemak % = Berat contoh g x Berat lemak g %
4. Kadar Protein Kasar ( AOAC 1984 )
destilat (hasil destilasi) ditampung di dalam erlenmeyer yang berisi 10 ml larutan penampung. Larutan penampung terbuat dari 20 ml asam askorbat, 10 ml Brom kresol hijau (0.1 %) dalam 1 liter aquades. Selanjutnya dititrasi dengan 0.01 N ditambahkan dengan 25 ml H2SO4 0.325 N dan dibawah pendingin balik selama 30 menit. Sebanyak 25 ml NaOH 1.25 N ditambahkan ke dalam sampel dan dipanaskan kembali selama 30 menit. Cairan di dalam labu erlenmeyer disaring dengan kertas saring (Whatmanno. 41) yang telah diketahui bobotnya. Penyaringan dilakukan dengan menggunakan corong Buchner dan pompa vacuum. Selanjutnya residu dicuci berturut-turut dengan 50 ml air panas dan 25 ml aseton. Residu beserta kertas saring dikeringkan dalam oven suhu 105 °C sampai bobotnya konstan kemudian ditimbang.
Kadar Serat Kasar % =a − bc x %
Dimana : a = bobot residu serat dalam kertas saring (g) b = bobot kertas saring kering (g)
c = bobot bahan awal (g)
7. Kadar Acid Detergent Fiber (ADF) (Belo dan Lumen 1980 )
Sebanyak 1 g sampel ditambahkan dengan 100 ml larutan ADF kemudian didinginkan pada pendingin tegak selam 60 menit. Selanjutnya sampel disaring dengan filter glass 2-G-3. Endapan yang diperoleh dicuci dengan aquades panas serta dibilas dengan aseton. Filter glass bersama endapannya dikeringkan dalam oven pada suhu 100 °C dan ditimbang hingga diperoleh bobot konstan. Sampel kemudian diabukan dalam tanur suhu 450–500 °C dan ditimbang hingga diperoleh bobot tetap.
Kadar ADF % =a − bc x %
Dimana : a = berat filter + endapan setelah dikeringkan (g) b = berat filter + endapan setelah diabukan (g) c = berat sampel awal (g)
8. Kadar Lignin (Selvendran dan Dupont 1984 )
selama 60 menit. Larutan disaring dengan filter glass 2-G-4. Filter glass yang berisi residu ditempatkan pada gelas piala 100 ml kemudian ditambah 25 ml H2SO4 72 % dingin (± 15 °C) dan diaduk dengan pengaduk gelas hingga terbentuk pasta halus. Gelas pengaduk dibiarkan berada dalam filter glass selama 3 jam pada suhu 20 hingga 23 °C sambil diaduk setiap 1 jam sekali. Penyaringan dilakukan dengan bantuan pompa vakum. Residu dicuci dengan air panas sampai liter bebas asam. Bagian pinggir filter glass dan pengaduk gelas dicuci dengan air panas. Residu dicuci dengan aseton 2–3 kali kemudian dikeringkan dalam oven pada suhu 105°C. Setelah dingin, sampel ditimbang hingga bobotnya tetap. Filter glass kemudian dimasukkan ke dalam tanur pada suhu 450–500°C hingga bobotnya tidak berubah.
Kadar Lignin % = − x %
Dimana : a = berat endapan + filter setelah dikeringkan (g) b = berat endapan + filter setelah diabukan (g) c = berat sampel awal (g)
9. Kadar Neutral Detergent Fiber (NDF) (Mc Queen dan Nicholson 1979) Sampel ditimbang sebanyak 0.5 g dan dimasukkan ke dalam erlenmeyer 300 ml kemudian ditambahkan 30 ml larutan α-amilase dan diinkubasikan selama 16 menit pada suhu 40°C. Sebanyak 100 ml larutan NDF dan 0.5 g Na2SO3 kemudian ditambahkan ke dalamnya. Campuran dididihkan pada pendingin tegak selam 60 menit kemudian disaring dengan filter glass 2-G-3. Endapan dicuci dengan akuades panas beberapa kali dan dibilas dengan aseton. Filter glass bersama endapan dikeringkan dalam oven pada suhu 105°C dan ditimbang hingga diperoleh bobot yang tetap. Kemudian pengabuan dilakukan pada suhu 450– 500°C dalam tanur dan hasilnya ditimbang hingga bobotnya tetap.
Kadar NDF % =a − bc x %
Dimana : a = berat filter + endapan setelah dikeringkan (g) b = berat filter + endapan setelah diabukan (g) c = berat sampel awal (g)
Larutan α -amilase
Sebanyak 1 g α -amilase dilarutkan dalam 1 L buffer fosfat 0.067 M (KH2PO4– Na2HPO4) pH 7.0 ± 0.05
Larutan NDF
Sebanyak 18.61 g EDTA-2Na; 6.81 Na2B4O7.10H2O; 30 g sodium lauril sulfat; 4.56 g Na2PO4 dan 10 ml 2-etoksi etanol dilarutkan sampai 1 L dengan pH 6.9 – 7.1.
10. Kadar Selulosa (Blumenkrantz dan Absoe-Hemsen 1973 )
Kadar hemiselulosa ditentukan dengan menghitung selisih kadar ADF dengan kadar lignin.
11. Kadar Hemiselulosa (Blumenkrantz dan Absoe-Hemsen 1973 )
Kadar hemiselulosa ditentukan dengan menghitung selisih kadarNDF dengan kadar ADF.
Kadar Selulosa % = Kadar NDF − Kadar ADF
12. Kadar Serat Makanan Metode Enzimatis (Sulaeman et al. 1993)
Sebanyak 1 g sampel dimasukkan dalam erlenmeyer kemudian ditambahkan 25 ml buffer natrium fosfat 0.1 M pH 6 dan diaduk. Enzim α -amilase ditambahkan sebanyak 0.1 ml ke dalam erlenmeyer kemudian ditutup dengan alumunium foil dan diinkubasikan dalam penangas air bergoyang pada suhu 80°C selama 15 menit. Setelah dingin, sebanyak 20 ml akuades ditambahkan dan pH diatur menjadi 6,8 menggunakan NaOH. Sebanyak 20 mg pankreatin ditambahkan kemudian diinkubasikan dalam penangas air bergoyang pada suhu 40°C selama 60 menit. Nilai pH diatur hingga 4.5 menggunakan HCl. Sampel disaring menggunakan filter glass yang telah diketahui beratnya dan mengandung celite kering kemudian dicuci sebanyak 2 x 10 ml dengan akuades.
Residu (Serat Tidak Larut)
Residu dicuci sebanyak 2 x 10 ml dengan etanol 95 % dan 2 x 10 ml aseton kemudian dikeringkan pada suhu 105 °C hingga bobotnya konstan dan ditimbang. Setelah kering, sampel diabukan dalam tanur pada suhu 550 °C selama 5 jam kemudian ditimbang bobotnya.
Filtrat (Serat Larut)
Volume filtrat diatur hingga 100 ml kemudian ditambahkan 400 ml etanol 95 % hangat (±60°C) dan dibiarkan mengendap selama 1 jam. Sampel disaring menggunakan filter glass yang telah diketahui bobotnya kemudian dicuci dengan 2 x 10 ml etanol 95%, dan 2 x 10 ml aseton. Sampel kemudian dikeringkan pada suhu 105°C selama semalam ke mudian didinginkan dalam desikator dan ditimbang. Selanjutnya sampel diabukan dalam tanur dengan suhu 550°C selama 5 jam kemudian didinginkan dalam desikator lalu ditimbang.
Blanko
Blanko dibuat dengan cara yang sama dengan prosedur diatas namun tanpa sampel. Nilai blanko sewaktu-waktu harus dicek bila menggunakan enzim yangg berbeda.
Kadar serat makanan tidak larut % =D − I − BW x %
Kadar serat makanan larut % =D − I − BW x %
Total serat makanan (%) = serat makanan tidak larut + serat makanan larut Keterangan :
W = berat sampel (g)
Lampiran 2 Prosedur ekstraksi dan hidrolisis serat mengkudu
Pencucian dan Pemisahan Biji
Ampas Bersih mengkudu
Pengeringan (55-60oC 5-6 jam) dan penggilingan
Tepung mengkudu Ampas Mengkudu
Biji
Pelarutan dalam asam
Hidrolisis dalam autoklaf 121 oC
Sentrifugasi 2000 rpm 30 menit
Endapan
Penetralan Na2CO3 1` %
Pencucian
Sentrifugasi 2000 rpm 30 menit
Endapan
Pengeringan dengan oven 55-60 oC 5-6 jam
Digiling
Lampiran 3 Data perubahan komposisi serat mengkudu sebelum dan setelah hidrolisis
A B Awal (g) Bahan Akhir (g) Bahan Awal Lignin (g) Akhir bahan Peru- Hemiselulosa (g) Awal Akhir bahan Peru- Awal Selulosa (g) Akhir Perubahan
-1 -1 30.0011 19.6601 1.2333 1.4671 -0.2338 0.8391 1.7167 -0.8776 19.7223 9.7665 9.9558
-1 1 30.0105 16.0728 1.2337 1.1366 0.0971 0.8394 1.3073 -0.4679 19.7285 8.0796 11.6489
1 1 30.0000 16.8192 1.2332 1.4603 -0.2271 0.8391 1.7362 -0.8971 19.7216 7.8599 11.8617
1 -1 30.0005 21.7603 1.2333 2.1859 -0.9526 0.8391 3.3502 -2.5111 19.7219 7.6991 12.0228
0 0 30.0000 22.2411 1.2332 1.8091 -0.5759 0.8391 1.0600 -0.2209 19.7216 9.5397 10.1818
0 0 30.0014 25.4923 1.2333 2.1233 -0.8900 0.8391 2.4574 -1.6183 19.7225 10.6676 9.0549
0 0 30.0005 23.4312 1.2333 1.8246 -0.5914 0.8391 1.0175 -0.1783 19.7219 10.1448 9.5771
0 0 30.0005 25.0610 1.2333 1.8624 -0.6292 0.8391 1.6692 -0.8301 19.7219 10.7483 8.9736
0 0 30.0005 22.0611 1.2333 1.8815 -0.6482 0.8391 1.5580 -0.7189 19.7219 9.1612 10.5608
Lampiran 3a (Lanjutan) Data perubahan komposisi serat mengkudu sebelum dan setelah hidrolisis
A B Awal (g) Bahan Akhir (g) Bahan Awal SE (g) Akhir bahan Peru- Awal SDF (g) Akhir bahan Peru- Awal IDF (g) Akhir Perubahan
-1 -1 30.0011 19.6601 8.2053 6.7098 1.4955 6.5006 2.8847 3.6159 16.1359 12.6797 3.4561
-1 1 30.0105 16.0728 8.2079 5.5494 2.6585 6.5026 1.8751 4.6276 16.1409 10.4961 5.6449
1 1 30.0000 16.8192 8.2050 5.7628 2.4422 6.5004 1.5129 4.9874 16.1353 9.9134 6.2219
1 -1 30.0005 21.7603 8.2051 8.5252 -03200 6.5005 2.1448 4.3557 16.1355 17.2827 -1.1472
0 0 30.0000 22.2411 8.2050 9.8322 -1.6272 6.5004 2.9230 3.5774 16.1353 13.4820 2.6533
0 0 30.0014 25.4923 8.2054 10.2440 -2.0386 6.5007 2.7869 3.7138 16.1360 15.5066 0.6294
0 0 30.0005 23.4312 8.2051 10.4444 -2.2392 6.5005 3.1611 3.3394 16.1355 14.2578 1.8777
0 0 30.0005 25.0610 8.2051 10.7811 -2.5759 6.5005 3.5066 2.9939 16.1355 14.8561 1.2795
0 0 30.0005 22.0611 8.2051 9.4604 -1.2553 6.5005 3.0885 3.4119 16.1355 13.4600 2.6755
Lampiran 4 Grafik perubahan komposisi serat pangan sebelum dan sesudah hidrolisis
Lampiran 4a Keterangan grafik perubahan komposisi serat pangan sebelum dan sesudah hidrolisis (%bk)
Lampiran 5 Hasil analisis sidik ragam selulosa terhadap pengaruh waktu dan konsentrasi
4,11 7,46 7,07 8,68 10,05 8,13 8,33 7,79 7,43 8,53
65,74
27,35 34,13 34,53 34,26 39,18 44,21 40,18 44,57 43,02 42,88
Lampiran 5a Koefisien parameter, standar error dan nilai t analisa kadar selulosa Parameter Koefisien Standar Error T Prob>t
Intersep 10.4264 0.4313 24.18 0.000
A 0.5699 0.6469 0.88 0.419
B 0.3830 0.6469 0.59 0.580
A*B -0.4636 0.6469 -0.72 0.506
Lampiran 6 Hasil analisis sidik ragam hemiselulosa terhadap pengaruh waktu dan konsentrasi
Sumber Varian DF JK KT F-rasio Prob>F
Waktu 1 1.06369 1.0637 2.85 0.152
Konsentrasi 1 1.02380 1.0238 2.75 0.158
Waktu*Konsentrasi 1 0.36254 0.3625 0.97 0.369
Galat 5 1.86295 0.3403
Jumlah 8 4.31299
Lampiran 6a Koefisien parameter, standar error dan nilai t analisa kadar hemiselulosa
Parameter Koefisien Standar Error T Prob>t
Intersep -0.9245 0.2035 -4.54 0.006
A -0.5157 0.3052 -1.69 0.152
B 0.5059 0.3052 1.66 0.158
A*B 0.3011 0.3052 0.99 0.369
Lampiran 5 Hasil analisis sidik ragam kadar SDF terhadap pengaruh waktu dan konsentrasi
Sumber Varian DF JK KT F-rasio Prob>F
Waktu 1 0,30226 0,30226 0,61 0,470
Konsentrasi 1 0,67523 0,67523 1,36 0,295
Waktu*Konsentrasi 1 0,03608 0,03608 0,07 0,798
Galat 5 2,47364 0,07460
Jumlah 8 3,48722
Lampiran 7a Koefisien parameter, standar error dan nilai t analisa kadar SDF Parameter Koefisien Standar Error T Prob>t
Intersep 3,84700 0,2345 16,41 0,000
A 0,27489 0,3517 0,78 0,470
B 0,41086 0,3517 1,17 0,295
Lampiran 6 Hasil analisis sidik ragam kadar lignin terhadap pengaruh waktu dan konsentrasi
Sumber Varian DF JK KT F-rasio Prob>F
Waktu 1 0,271916 0,27192 4,26 0,094
Konsentrasi 1 0,279030 0,27903 4,37 0,091
Waktu*Konsentrasi 1 0,038935 0,03893 0,61 0,470
Galat 5 0,319124 0,01638
Jumlah 8 0,909004
Lampiran 8a Koefisien parameter, standar error dan nilai t analisa kadar lignin Parameter Koefisien Standar Error T Prob>t
Intersep -0,5168 0,08421 -6,14 0,002
A -0,2607 0,12632 -2,06 0,094
B 0,2641 0,12632 2,09 0,091