PENGARUH PENAMBAHAN JUMLAH PLAT NETRAL JENIS
STAINLESS STEEL AISI 302 B PADA
DRY CELL
UNTUK
PEMISAHAN H
2(g) DAN O
2(g) DARI H
2O(l)
Skripsi Yang Diajukan Untuk Melengkapi
Syarat Memperoleh Gelar Sarjana Teknik
WAHID HABIB NIM : 090401017
DEPARTEMEN TEKNIK MESIN
FAKULTAS TEKNIK
UNVERSITAS SUMATERA UTARA
MEDAN
ABSTRAK
Selama bertahun-tahun ketergantungan masyarakat terhadap bahan bakar minyak sangat tinggi. Bahkan untuk menghasilkan energi listrik,bahan bakar minyak tetap dipakai juga. Teknologi fuel cell (sel bahan bakar) merupakan hal yang tepat untuk menghemat penggunaan minyak dengan menggunakan hidrogen untuk menghasilkan energi listrik dan oksigen sebagai pengikat gas buang agar tidak berbahaya bagi lingkungan.Untuk mendapatkan hidrogen dan oksigen, penulis menggunakan dry cell dengan memvariasikan jumlah plat netral. Adapun tujuan penelitian ini adalah untuk mengetahui pengaruh penambahan jumlah plat netral terhadap suhu dan produksi gas yang dihasilkan. Penelitian ini juga bertujuan untuk mengetahui pengaruh KOH dan kuat arus pada dry cell. Penelitian ini dilakukan dengan menggunakan thermocouple agilent sebagai pencatat suhu yang dilahsilkan. Dalam setiap 90 detik, volume gas yang dihasilkan diukur pada setiap variabel uji yang telah dilakukan. Dari hasil penelitian diperoleh, nilai produksi tertinggi dihasilkan pada pengujian 10 plat netral dengan KOH 4,66% . Sedangan suhu tertinggi terjadi pada pengujian 4 plat netral dengan KOH 4,66%. Sehingga dapat diperoleh kesimpulan yaitu, semakin banyak plat netral semakin tinggi pula gas yang dihasilkan, sedangkan suhu yang dihasilkan semakin rendah dan semakin sedikit plat netral semakin tinggi panas yang dihasilkan sedangkan volume gas yang dihasilkan semakin rendah.
ABSTRACT
Over the years people's dependence on fossil fuels is very high. Even for generating electrical energy, fuel continues to be used as well. Fuel cell technology (fuel cell) is the right thing to save the use of oil by using hydrogen to generate electricity and oxygen as a binder so harmless exhaust gas .To obtain hydrogen and oxygen, the authors use a dry cell by varying the number of neutral plates. The purpose of this study was to determine the effect of the number neutral plate with respect to temperature and the resulting gas production. This study also aimed to determine the effect of KOH and strong currents in the dry cell. The study was done using a thermocouple temperature recorder agilent as produced. In every 90 seconds, the volume of gas produced was measured at each test variable that has been done. From the results obtained, the highest production values generated at 10 plates neutral testing with 4.66% KOH. Whereas, the highest temperature occurs in the test 4 neutral plates with 4.66% KOH. So it can be concluded that, the more the higher the plate neutral gases produced, while the lower temperatures generated and the less the higher the neutral plate heat generated while the volume of gas produced lower.
KATA PENGANTAR
Puji dan syukur saya ucapkan kepada Tuhan Yang Maha Kuasa atas berkat, kekuatan dan kesehatan yang diberikan selama pengerjaan skripsi ini, sehingga skripsi ini dapat saya selesaikan.
Skripsi ini merupakan salah satu syarat untuk menyelesaikan pendidikan untuk mencapai gelar sarjana di Departemen Teknik Mesin Fakultas Teknik Universitas Sumatera Utara. Adapun yang menjadi judul skripsi ini yaitu PENGARUH PENAMBAHAN PLAT NETRAL JENIS STAINLESS STEEL EN SERIES 58A (AISI 302 B) PADA DRY CELL PADA PEMISAHAN H2(g) DAN O2(g) DARI H2O(l). Dalam penulisan skripsi ini tidak sedikit hambatan yang dihadapi oleh penulis. Untuk itu penulis secara khusus menyampaikan terima kasih kepada dosen pembimbing Bapak Ir.Abdul Halim Nasution M.Sc, yang telah bersedia meluangkan waktunya untuk memberikan saran dan membimbing serta sumbangan pikiran bagi penulisan skripsi ini.
Selama penulisan skripsi ini, penulis juga mendapat banyak bantuan dari berbagai
pihak. Oleh karena itu penulis juga mengucapkan terima kasih kepada:
1. Ibu Saya, Erni Hasibuan yang mendo’akan dan mendukung penulis dalam
pengerjaan Skripsi ini.
2. Bapak Bapak Dr.Ir.Mulfi Hazwi,MSc dan Bapak Dr.eng.Ir.Indra,MT selaku dosen
pembanding I dan II.
3. Bapak Dr.Ing.Ir.Ikwansyah Isranuri, selaku Ketua Departemen Teknik Mesin
Fakultas Teknik USU.
4. Bapak/Ibu Staff Pengajar dan Pegawai di Departemen Teknik Mesin USU.
5. Saudaraku yang tercinta, Abang saya Dian Prima Senja Sihaloho dan Istri, Irvan
Aspidar dan Istri, Zulfitri Sipahutar dan Istri untuk do’a, dana, dan dukungan dalam
menyelesaikan skripsi ini.
6. Seluruh teman-teman penulis, Umri Nahdi Siregar dan adinda Imam Syaifullah,
adinda Rizki Agustama, dan teman satu angkatan 2009 juga adik-adik yang tidak
dapat penulis sebutkan satu-persatu yang telah menemani dan memberikan
masukan serta semangat kepada penulis
7. Teman-teman Tim Horas USU sebagai inspirasi bagi penulis untuk mendapatkan
ide dalam pengerjaan skripsi ini.
8. Ibu Salmiah Hasibuan dan adinda Fatimah Hanum Lubis yang mendorong,
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh karena itu
penulis mengharapkan kritik dan saran yang bersifat membangun demi penyempurnaan
dimasa mendatang.
Akhirnya penulis berharap skripsi ini dapat bermanfaat bagi kita semua. Terima
kasih.
Medan, Januari 2014
Penulis
DAFTAR ISI
ABSTRAK ... i
KATA PENGANTAR ... ii
DAFTAR ISI... iv
DAFTAR GAMBAR ... vii
DAFTAR TABEL ... viiii
DAFTAR NOTASI ... xiii
BAB I PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Tujuan Pengujian ... 3
1.2.1 Batasan Masalah ... 4
1.3 Metedologi Penulisan ... 4
1.4 Sistematika Penulisan ... 4
BAB II TINJAUAN PUSTAKA 2.1 Fuel Cell ... 6
2.2 Jenis-Jenis Sel Bahan Bakar ... 6
2.3 Polymer Exchanger Membrane Fuel Cell ... 9
2.4 Dry Cell ... 10
2.5 Metode Pemisahan Hidrogen dan Oksigen pada Dry Cell ... 12
BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu ... 13
3.1.1 Tempat ... 13
3.1.2 Waktu ... 13
3.2 Alat dan Bahan ... 15
3.2.1 Alat ... 15
3.2.2 Bahan.... ... 16
3.2.3 Alat Pendukung Proses Pengujian ... 18
3.2.4 Alat Pendukung Pada Proses Pembuatan H2 dan O2 ... 20
3.3 Prosedur Pengujian ... 21
3.4 Instalasi Pengujian ... 24
BAB IV PENGOLAHAN DATA 4.1 Hasil Pengujian ... 25
4.1.1 Besarnya Daya Yang Digunakan Pada Pengujian ... 25
4.2 Besarnya Konsentrasi Larutan KOH ... 26
4.3 Menghitung Besar Volume Hidrogen dan Oksigen ... 26
4.4 Menghitung Laju Produksi Gas H2 dan O2 ... 36
4.5 Besar Energi Yang Digunakan ... 41
BAB V KESIMPULAN DAN SARAN
5.1 Kesimpulan ... 47
5.2 Saran ... 48
DAFTAR PUSTAKA ... xvii
DAFTAR GAMBAR
Gambar 1.1 Rangkaian Dry cell ... 3
Gambar 1.2 Diagram Alir Penelitian ... -- Gambar 2.1 Aliran Hidrogen dan Oksigen Didalam Sel Bahan Bakar PEM ... 7
Gambar 2.2 Reaksi Elektrolisis Pada PEM ... 10
Gambar 2.3 Dry Cell ... 11
Gambar 2.4 Proses Elektrolisis Air ... 11
Gambar 2.5 Bentuk Gasket Yang Dipakai ... 12
Gambar 2.6 Contoh Membran ... 12
Gambar 2.7 Aliran Oksigen dan Hidrogen ... 13
Gambar 3.1 Plat Stainless Steel ... 17
Gambar 3.2 Plat Akrilik ... 17
Gambar 3.3 Susunan Plat Dengan Baut ... 18
Gambar 3.4 Gasket ... 18
Gambar 3.5 Screen Nylon Monofilamen ... 19
Gambar 3.6 Mesin Las ... 19
Gambar 3.7 Termocouple Agilent ... 20
Gambar 3.8 Multimeter ... 20
Gambar 3.9 Stopwatch ... 20
Gambar 3.11 Katup Udara... 21
Gambar 3.12 Regulator ... 22
Gambar 3.13 Instalasi Pengujian ... 25
Gambar 4.1 Grafik Hasil Percobaan Suhu Vs Kuat Arus
dengan KOH 4% ... 33
Gambar 4.2 Grafik Hasil Percobaan Suhu Vs Kuat Arus
dengan KOH 4,33% ... 33
Gambar 4.3 Grafik Hasil Percobaan Suhu Vs Kuat Arus
dengan KOH 4,66% ... 34
Gambar 4.4 Grafik Hasil Percobaan Volume Gas Vs Kuat Arus
Pada KOH 4% ... 35
Gambar 4.5 Grafik Hasil Percobaan Volume Gas Vs Kuat Arus
Pada KOH 4,33% ... 35
Gambar 4.6 Grafik Hasil Percobaan Volume Gas Vs Kuat Arus
Pada KOH 4,66% ... 36
Gambar 4.7 Grafik Hasil Percobaan Volume Hidrogen Vs Kuat Arus
Pada KOH 4% ... 37
Gambar 4.8 Grafik Hasil Percobaan Volume Hidrogen Vs Kuat Arus
Pada KOH 4,33% ... 37
Gambar 4.9 Grafik Hasil Percobaan Volume Hidrogen Vs Kuat Arus
Gambar 4.10 Grafik Hasil Percobaan Volume Oksigen Vs Kuat Arus
Pada KOH 4% ... 38
Gambar 4.11 Grafik Hasil Percobaan Volume Oksigen Vs Kuat Arus Pada KOH 4,33% ... 39
Gambar 4.12 Grafik Hasil Percobaan Volume Oksigen Vs Kuat Arus Pada KOH 4,66% ... 39
Gambar 4.13 Grafik Suhu Vs Jumlah Plat Netral Pada Arus 20 Amper ... 45
Gambar 4.14 Grafik Suhu Vs Jumlah Plat Netral Pada Arus 20 Amper ... 45
Gambar 4.15 Grafik Suhu Vs Jumlah Plat Netral Pada Arus 20 Amper ... 46
DAFTAR TABEL
Tabel 3.1 Lokasi dan Aktivitas Penelitian ... 115
Tabel 4.1 Data Pengujian Voltase 50 V, 4 Plat Netral,
dengan Tebal Gasket 1,5 mm ... 31
Tabel 4.2 Data Pengujian Voltase 50 V, 6 Plat Netral,
dengan Tebal Gasket 1,5 mm ... 31
Tabel 4.3 Data Pengujian Voltase 50 V, 8 Plat Netral,
dengan Tebal Gasket 1,5 mm ... 32
Tabel 4.4 Data Pengujian Voltase 50 V, 10 Plat Netral,
dengan Tebal Gasket 1,5 mm ... 32
Tabel 4.5 Data Pengujian Debit Hidrogen Q H2 (m3/s) dan Laju Produksi Hidrogen ṁ (kg/s) pada 4 Plat Netral ... 40
Tabel 4.6 Data Pengujian Debit Hidrogen Q H2 (m3/s) dan Laju Produksi Hidrogen ṁ (kg/s) pada 6 Plat Netral ... 41
Tabel 4.7 Data Pengujian Debit Hidrogen Q H2 (m3/s) dan Laju Produksi Hidrogen ṁ (kg/s) pada 8 Plat Netral ... 41
Tabel 4.8 Data Pengujian Debit Hidrogen Q H2 (m3/s) dan Laju Produksi Hidrogen ṁ (kg/s) pada 10 Plat Netral ... 42
Tabel 4.9 Data Pengujian Debit Oksigen Q O2 (m3/s) dan Laju Produksi Oksigen ṁ (kg/s) pada 4 Plat Netral ... 42
Tabel 4.10 Data Pengujian Debit Oksigen Q O2 (m3/s) dan Laju Produksi Oksigen ṁ (kg/s) pada 6 Plat Netral ... 43
Tabel 4.11 Data Pengujian Debit Oksigen Q O2 (m3/s) dan Laju Produksi Oksigen ṁ (kg/s) pada 8 Plat Netral ... 43
Tabel 4.12 Data Pengujian Debit Oksigen Q O2 (m3/s) dan Laju Produksi Oksigen ṁ (kg/s) pada 10 Plat Netral ... 44
Tabel 4.13 Data Pengujian Energi Terbuang Hlost (kalori) dan % Lost Persentase Energi Terbuang Pada 4 Plat Netral ... 46
Tabel 4.15 Data Pengujian Energi Terbuang Hlost (kalori) dan % Lost Persentase Energi Terbuang Pada 8 Plat Netral ... 47
DAFTAR NOTASI
Lambang Keterangan Satuan
E Energi Yang Digunakan Watt-hours
V Voltase Volt
I Kuat Arus Ampere
ρ Massa Jenis Gas H2 Kg/m3
ṁ Laju Produksi Gas H2 Kg/s
Q Debit Volume Gas m3/s
Vf Volume Air cm3
H lost Energi Yang Terbuang Kalori
t Waktu Sekon
Tf Temperatur Akhir oC
ABSTRAK
Selama bertahun-tahun ketergantungan masyarakat terhadap bahan bakar minyak sangat tinggi. Bahkan untuk menghasilkan energi listrik,bahan bakar minyak tetap dipakai juga. Teknologi fuel cell (sel bahan bakar) merupakan hal yang tepat untuk menghemat penggunaan minyak dengan menggunakan hidrogen untuk menghasilkan energi listrik dan oksigen sebagai pengikat gas buang agar tidak berbahaya bagi lingkungan.Untuk mendapatkan hidrogen dan oksigen, penulis menggunakan dry cell dengan memvariasikan jumlah plat netral. Adapun tujuan penelitian ini adalah untuk mengetahui pengaruh penambahan jumlah plat netral terhadap suhu dan produksi gas yang dihasilkan. Penelitian ini juga bertujuan untuk mengetahui pengaruh KOH dan kuat arus pada dry cell. Penelitian ini dilakukan dengan menggunakan thermocouple agilent sebagai pencatat suhu yang dilahsilkan. Dalam setiap 90 detik, volume gas yang dihasilkan diukur pada setiap variabel uji yang telah dilakukan. Dari hasil penelitian diperoleh, nilai produksi tertinggi dihasilkan pada pengujian 10 plat netral dengan KOH 4,66% . Sedangan suhu tertinggi terjadi pada pengujian 4 plat netral dengan KOH 4,66%. Sehingga dapat diperoleh kesimpulan yaitu, semakin banyak plat netral semakin tinggi pula gas yang dihasilkan, sedangkan suhu yang dihasilkan semakin rendah dan semakin sedikit plat netral semakin tinggi panas yang dihasilkan sedangkan volume gas yang dihasilkan semakin rendah.
ABSTRACT
Over the years people's dependence on fossil fuels is very high. Even for generating electrical energy, fuel continues to be used as well. Fuel cell technology (fuel cell) is the right thing to save the use of oil by using hydrogen to generate electricity and oxygen as a binder so harmless exhaust gas .To obtain hydrogen and oxygen, the authors use a dry cell by varying the number of neutral plates. The purpose of this study was to determine the effect of the number neutral plate with respect to temperature and the resulting gas production. This study also aimed to determine the effect of KOH and strong currents in the dry cell. The study was done using a thermocouple temperature recorder agilent as produced. In every 90 seconds, the volume of gas produced was measured at each test variable that has been done. From the results obtained, the highest production values generated at 10 plates neutral testing with 4.66% KOH. Whereas, the highest temperature occurs in the test 4 neutral plates with 4.66% KOH. So it can be concluded that, the more the higher the plate neutral gases produced, while the lower temperatures generated and the less the higher the neutral plate heat generated while the volume of gas produced lower.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Selama bertahun-tahun belakangan ini, bahan bakar fosil nyaris menjadi
satu-satunya sumber energi di planet ini. Sehingga tidak heran kalau tahun-tahun
belakangan ini pula kita pun menyaksikan bagaimana wajah dunia babak belur
akibat perebutan kuasa atas sumber utama penghasil energi ini.
Belakangan setelah penggunaan energi fosil dengan skala besar, kita pun
dihadapkan dengan berbagai masalah. Ketika pembakaran berlangsung untuk
menghasilkan energi, bahan bakar fosil ini melepaskan karbon ke udara.
Pelepasan karbon ini menyebabkan polusi dan merusak ozon[5].
Masalah dengan bahan bakar fosil ini tidak hanya sampai di situ. Besarnya
konsumsi bahan bakar ini dalam seabad terakhir, membuat fakta menipisnya
cadangan bahan bakar ini tidak bisa kita hindari. Sementara itu, ketika cadangan
bahan bakar fosil semakin menipis, kebutuhan atas energi bukannya turun malah
semakin hari semakin tinggi. Karena alasan itulah, belakangan kita lihat mulai
banyak usaha umat manusia untuk mulai memanfaatkan sumber energi terbarukan
dengan lebih maksimal. Sumber energi terbarukan itu bisa berupa tenaga
matahari, angin, air, panas bumi, bio massa bahkan gelombang laut. Sebenarnya
selain berbagai sumber energi terbarukan seperti yang disebut di atas, masih ada
satu sumber energi lain yang sangat potensial menggantikan bahan bakar fosil
sebagai sumber energi utama. Sumber energi alternatif pengganti bahan bakar
fosil ini bernama hidrogen. Dibandingkan semua energi terbarukan seperti yang
saya sebut di atas hidrogen memiliki beberapa keunggulan antara lain, bahan
bakar hidrogen bersifat mobil seperti bahan bakar fosil yang kita kenal selama ini.
Bedanya, tidak seperti bahan bakar fosil, pembakaran hidrogen tidak
menyebabkan polusi karbon[3].
Hidrogen adalah unsur yang paling sederhana dari semua unsur yang ada
sendiri bentuk hidrogen yang paling umum kita kenal adalah air (H2O).
Kebanyakan dari hidrogen yang diproduksi sampai hari ini adalah hidrogen yang
didapat dari gas alam (CH4) melalui proses yang disebut steam reforming. Tapi yang lebih potensial untuk dilakukan di masa depan adalah memproduksi
hidrogen dari air melalui proses elektrolisis atau langsung menggunakan reaksi
fotokimia.
Sel bahan bakar (fuel cell) adalah sebuah alat dengan
reaktannya yang terkonsumsi, yaitu dia memproduksi listrik dari penyediaan
bahan bakar
internal dari baterai. Sebagai tambahan, elektrode dalam baterai bereaksi dan
berganti pada saat baterai diisi atau dibuang energinya, sedangkan elektrode sel
bahan bakar adalah katalitik dan relatif stabil[6].
aliran reaktan mengalir masuk dan produk dari reaktan mengalir keluar. Sehingga
operasi jangka panjang dapat terus menerus dilakukan selama aliran tersebut dapat
dijaga kelangsungannya.
Sel bahan bakar sangat menarik dalam aplikasi modern karena efisiensi
tinggi dan penggunaan bebas-emisi, berlawanan dengan bahan bakar umum
seperti
adalah
menggunakan banyak energi. Memproduksi hidrogen membutuhkan carrier
hidrogen (biasanya
juga listrik, yang diproduksi oleh bahan bakar konvensional. Meskipun sumber
sekarang ini sangat mahal, untuk menghasilkan listrik, sel bahan bakar
menggunakan hidrogen dan oksigen sebagai bahan bakar, akan tetapi, teknologi
pembuangan dari fuel cell ini berupa uap air yang tidak berbahaya bagi lingkungan, untuk menghasilkan hidrogen dan oksigen, penulis menggunakan alat
bernama dry cell . Dry cell merupakan alat yang menggunakan prinsip hidrolisis.
Dry cell dibuat sedemikian sehingga jumlah air yang dielektrolisa sesedikit mungkin sesuai dengan kebutuhan. Pada sel konvensional (Wet Cell), jika volume Sel 1000 ml maka semua air yang berada dalam sel semuanya dielektrolisa,
Sedangkan pada dry cell hanya sebagian kecil air yang dielektrolisa sisa air cadangan berada di tangki reservoir. Air dari sel yang terbawa gas akan tersirkulasi dengan sendirinya dan bercampur dengan air dingin yang ada di
reservoir, sebaliknya air dingin dari reservoir masuk kedalam sel. Dengan cara ini
dry cell memiliki keuntungan dalam menjaga temperatur sel.
Gambar 1.1. Rangkaian Dry Cell
1.2 Tujuan Pengujian
1. Mengetahui proses pemisahan H2(gas) dan O2(gas) dari H2O (liquid)
2. Mengetahui pengaruh penambahan plat netral pada dry cell terhadap suhu dry cell dan produksi hidrogen dan oksigen.
3. Mengetahui pengaruh kuat arus (Ampere) terhadap suhu volume
hidrogen dan oksigen yang dihasilkan.
4. Mengetahui pengaruh dan reaksi KOH sebagai katalis terhadap suhu
dan laju produksi hidrogen dan oksigen.
5. Mengetahui besar energi yang dipakai dan energi yang terbuang.
6. Membuat alat untuk menghasilkan energi terbaru dengan biaya yang
Murah.
1.2.1 Batasan Masalah
1. Spesifikasi dry cell yang digunakan adalah hidrogen dry cell dengan spesifikasi; menggunakan 2 plat negatif, 1 plat positif, dengan
memvariasikan jumlah plat netral yaitu 4,6,8, dan 10 plat.
2. Bahan plat yang digunakan adalah stainles stell.
1.3 Metodologi Penulisan
Metodologi penulisan yang digunakan pada penulisan skripsi ini adalah
sebagai berikut :
a. Studi literatur, berupa studi kepustakaan, kajian dari buku-buku dan
tulisan-tulisan yang terkait.
b. Browsing internet, berupa studi artikel-artikel, gambar-gambar dan
buku elektronik (e-book) serta data-data lain yang berhubungan.
c. Metode studi lapangan, yaitu dengan mengambil data dari hasil
pengujian yang dilakukan di laboratorium fakultas teknik.
d. Diskusi, berupa tanya jawab dengan dosen pembimbing yang ditunjuk
oleh Departemen Teknik Mesin Universitas Sumatera Utara
1.4. Sistematika Penulisan
Sistematika penulisan tugas akhir ini akan disusun dalam lima bab, yaitu
studi kasus dan pemecahan masalah yang berisi antara lain : latar belakang, tujuan
penelitian, manfaat penelitian, batasan masalah dan sistematika penulisan dan diagram
alir pengujian. Kemudian bab II yaitu tinjauan pustaka yang berisi tentang dasar teori dari
topik yang dikaji dan digunakan sebagai landasan dalam memecahkan masalah dan
menganalisis permasalahan tersebut meliputi penjelasan mengenai dry cell. Kemudian
bab III metode penelitian berisi tentang beberapa tahapan persiapan sebelum pengujian,
prosedur pengujian. Kemuaian bab IV pengolahan data yakni berisi tentang pembahasan
dari data-data yang diperoleh yakni volume gas hasil elektrolisis air pada dry cell, suhu
yang dihasilkan pada dry cell dan tegangan dan arus yang dipakai pada dry cell, serta %
KOH yang digunakan. Kemudian bab V yang berisi tentang kesimpulan dari hasil analisa
dan saran untuk penyempurnaan hasil penelitian untuk penelitian berikutnya. Dan
Mulai
Penentuan tujuan
Studi literatur, buku refrensi,
Pengumpulan data, Bentuk Geometri, Dimensi, dan
Material Dry Cell
Variasi Jumlah Plat Netral Pada Dry Cell
Hasil
Kesimpulan
Selesai
BAB II
TINJAUAN PUSTAKA
2.1 Fuel cell
Sel bahan bakar (fuel cell) adalah sebuah alat yang mirip denga tetapi berbeda karena dia dirancang untuk dapat diisi terus reaktannya yang
terkonsumsi; yaitu dia memproduksi listrik dari penyediaan bahan bakar
internal dari baterai. Sebagai tambahan, elektrode dalam baterai bereaksi dan
berganti pada saat baterai diisi atau dibuang energinya, sedangkan elektrode sel
bahan bakar adalah katalitik dan relatif stabil[6].
Biasanya, aliran reaktan mengalir masuk dan produk dari reaktan mengalir
keluar. Sehingga operasi jangka panjang dapat terus menerus dilakukan selama
aliran tersebut dapat dijaga kelangsungannya.
Sel bahan bakar dianggap sangat menarik dalam aplikasi modern karena
efisiensi tinggi dan penggunaan bebas-emisi, berlawanan dengan bahan bakar
umum seperti
satunya
murni adala
hidrogen yang menggunakan banyak energi. Memproduksi hidrogen
membutuhkan "carrier" hidrogen (biasanya
dapat dijadikan alternatif), dan juga listrik, yang diproduksi oleh bahan bakar
konvensional. Meskipun sumber
dapat juga digunakan, namun sekarang ini mereka sangat mahal.
2.2 Jenis – Jenis Sel bahan bakar
Sel bahan bakar diklasifikasikan berdasarkan atas jenis dari elektrolit
dalam sel, jenis katalis yang diperlukan, batas temperatur dimana sel tersebut
bekerja, bahan bakar yang dibutuhkan, dan faktor – faktor lainnya. Adapun sel
bahan bakar hingga saat ini terbagi menjadi 7 klasifikasi utama antara lain :
1. Polymer Electrolyte Membrane (PEM)
2. Direct methanol
3. Alkaline
4. Phosporic acid
5. Molten carbonate
6. Solid oxide
7. Regenerative
Proton Exchange Membrane (PEM) lebih dikenal sebagai
PolymerElectrolyte Membranemenyalurkan berat jenis yang inggi dan menawarkan keuntungan pada berat dan volume yang rendah, dibandingkan
dengan sel bahan bakaryang lainnya. Sel bahan bakar PEM menggunakan polimer
solid sebagai elektrolit dan elektroda karbon yang mengandung katalis platinum.
PEM membutuhkan hanya hydrogen, oksigen dari udara, dan air untuk beroperasi
dan tidak memerlukan cairan korosif.
Gambar 2.1 Aliran hidrogen dan oksigen di dalam sel bahan bakar PEM Sumbe
pada sel bahan bakar. DMFC ini tidak mempunyai permasalahan tempat
penyimpanan seperti sel bahan bakar lain pada umumnya.
Alkaline fuel cell adalah salah satu dari teknologi sel bahan bakar yang dikembangkan, dan merupakan yang pertama digunakan secara luas untuk
program penghasil energi listik dan air pada pesawat luar angkasa oleh NASA. Sel
bahan bakar ini menggunakan potasium hidroksida dalam air sebagai elektrolit
dan dapat menggunakan beberapa jenis dari metal sebagaikatalis pada anoda dan
katoda.
Phosporic Acid Fuel Cell (PAFC) menggunakan cairan asam fosfor sebagai elektrolit dan elektroda besi karbon yang mengandung katalis platinum.
PAFC ini lebih dikenal sebagai generasi pertama dari sel bahan bakar modern.
PAFC lebih toleran terhadap ketidakmurnian dari pada bahan bakar yang telah
diubah menjadi hidrogen dari pada Sel bahan bakar PEM.
Molten Carbonate Fuel Cell (MCFC) saat ini sedang dikembangkan untuk gas natural dan batubara untuk kegunaan elektrik, industri, dan aplikasi militer.
MCFC adalah sel bahan bakar yang bekerja pada temperatur tinggi yang
menggunakan elektrolit yang terdiri dari molten carbonate saltmixture, lithium aluminium oksida (LiAlO2) .
Solid Oxide Fuel Cell (SOFC) menggunakan bahan keramik yang keras dan tidak mudah berkarat sebagai elektrolit. SOFC ini diharapkan dapat memiliki
efisiensi 50 – 60 % untuk mengubah bahan bakar menjadi listrik.
Regenerative Fuel Cell menghasilkan listrik dari hidrogen,oksigen, membangkitkan panas dan airsebagai bahan bakar, seperti sel bahan bakar
lainnya. Regenerative fuel cell juga dapat menggunakan elektrolisadari solar power atau sumber lainnyauntuk membagi kelebihan air menjadibahan bakar
hidrogen dan oksigen. Selbahan bakar jenis ini sedangdikembangkan oleh NASA
2.3 Polymer Exchanger Membrane Fuel Cell
Pada saat ini ada beberapa tipe sel bahan bakar yaitu proton exchanger membrane fuel cell (PEM), sel bahan bakar alkali, asam fosfat, karbonat cair dan oksida padat. PEM dan alkali bekerja pada suhu dibawah 2000C. Sehingga
disebut mesin dingin. Beberapa keuntungan sel bahan bakar apabila emisi gas
buang sangat mudah bahkan bisa dikatakan tidak ada yaitu, dapat dioperasikan
terus-menerus, mudah untuk dioperasikan, ringan dan mudah digabung menjadi
kesatuan dari beberapa sel tunggal untuk menghasilkan energi yang besar apabila
diperlukan. Sehingga sel bahan bakar dapat dibuat untuk keperluan
bermacam-macam alat serba guna.
Pada gambar dibawah ini diperlihatkan rangkaian alat sel bahan bakar
secara umum. Bagian-bagian sel bahan bakar terdiri dari, katalis berupa logan Pt
atau campuran Pt-Ru sebagai anode dan katode. Diantara anode dan katode
ditempatkan membran penukar ion. Fungsi membran adalah melewatkan ion H+.
Elektron keluar dari sel menuju ke rangkaian alat dan arus elektron dimanfaatkan
menjadi energi listrik. Kemudian elektron mengalir menuju sisi katode. Katalis di
sisi anode didukung oleh penyangga berupa lapisan hidrolik ( suka air) terbuat
dari karbon, sedangkan di sisi katode katalis didukung oleh lapisan penyangga
hidropobik ( tidak suka air) yang terbuat dari PTFE. Di sisi katode dimasukkan
oksigen dari udara. Oksigen akan bereaksi melalui pembentukan molekul antara (
intermediate) sebelum terbentuk ion O−2. Selanjutnya ion O−2 , elektron dan ion
H+ bereaksi membentuk molekul air ( H2O). Reaksi di sisi anode dan sisi katode
dapat dinyatakan dengan persamaan setengah reaksi di bawah ini.
di sisi anode terjadi ionisasi molekul hidrogen menjadi ion H+ dan elelktron,
2H2 �������⎯⎯⎯�4H+4e−
Di sisi katode terjadi reaksi pembentukan air,
Gambar 2.2 Reaksi Elektrolisis Air Pada PEM 2.4 Dry Cell
Dry cell merupakan sebuah alat yang menggunakan prinsip elektrolisis
untuk memecah ikatan air menjadi hidrogen dan oksigen sekaligus memisahkan
hidrogen dan oksigen tersebut agar tidak tercampur[8]. Elektrolisis air adalah
peristiwa penguraian senyawa air (H2O) menjadi oksigen (O2) dan hidrogen
gas (H2) dengan menggunakan arus listrik yang melalui air tersebut. Pada
katode, dua molekul air bereaksi dengan menangkap dua elektron, tereduksi
menjadi gas H2 dan ion hidroksida (��−). Sementara itu pada anode, dua
molekul air lain terurai menjadi gas oksigen (O2), melepaskan 4 ion
H+.serta mengalirkan elektron ke katode. Ion H+ dan OH mengalami
netralisasi sehingga terbentuk kembali beberapa molekul air. Reaksi
keseluruhan yang setara dari elektrolisis air dapat dituliskan sebagai berikut.
2�2�(�)�������⎯⎯⎯�2�2(g) +�2(g)
Gas hidrogen dan oksigen yang dihasilkan dari reaksi ini membentuk
dimanfaatkan untuk menghasilkan hidrogen dan hidrogen peroksida (H2O2) yang
dapat digunakan sebagai bahan bakar kendaraan hidrogen.
Gambar 2.3 Dry cell 2.4.1 Proses Elektrolisis Air
Dengan menyediakan energi dari baterai, Air (H2O) dapat dipisahkan ke
dalam molekuldiatomik hidrogen (H2) dan oksigen(O2).
Gambar 2.4 Proses Elektrolisis Air
Sumber : http://restukarmela.wordpress.com/2012/05/03/sel-elektrolisis/
Elektrolisis satu mol air menghasilkan satu mol gas hidrogen dan
setengahmol gas oksigen dalam bentuk diatomik. Sebuah analisis yang rinci dari
proses memanfaatkan potensi termodinamika dan hukum pertama termodinamika.
Proses ini berada di 298K dan satu tekanan atmosfer, dan nilai-nilai yang relevan
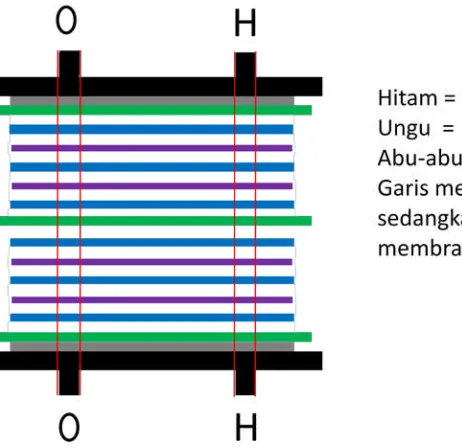
2.4.2 Metode Pemisahan Hidrogen dan Oksigen pada Dry Cell
Hal pertama yang harus diperhatikan agar hidrogen terpisah dengan
Oksigen yaitu memisahkan aliran air yang akan dielektrolisis menjadi dua bagian
aliran. Untuk membagi aliran air ini lobang pada gasketlah yang mnjadi inti
pembagiannya. Gasket dibuat seperti gambar 2.4 di bawah. Ketika disusun, aliran
dibagi menjadi aliran sisi kiri dan aliran sisi kanan, dimana aliran sisi kiri tidak
bersentuhan dengan aliran sisi kanan sehingga gas yang dihasilkan juga tidak
bercampur karna dialirkan pada sisi yang tetap.
Gambar 2.5 Bentuk Gasket Yang Dipakai
Sumber : http://hho4free.com/hydrogen_separator_cell.htm
Membran yang digunakan harus terbuat dari material yang tidak bersifat
ion carier (penangkap ion) karena gas yang dihasilkan memiliki muatan. Bahan yang bisa digunakan bermacam- macam, misalnya poliester atau nilon dan lain-
Gambar 2.6 Contoh Membran
Kemudian plat, membran dan gasket akan disusun seperti gambar 2.6
dibawah sehingga dapat dilihat aliran gas yang akan dihasilkan.
Gambar 2.7 Aliran Oksigen dan Hidrogen
BAB III
METODOLOGI PENELITIAN
3.1 Waktu dan Tempat3.1.1. Waktu
Waktu pelaksanaan penelitian ini sudah mulai dilaksanakan pada bulan
Desember 2013 dan direncanakan akan selesai pada Juni 2014 .
3.1.2.Tempat
Penelitian mengenai pengaruh penambahan plat netral terhadap
perbandingn volume hidrogen dan oksigen pada dry cell dilakasanakan dalam beberapa tahapan , yaitu seperti diuraikan pada Tabel 3.1.
Tabel 3.1. Lokasi dan aktivitas penelitian
No. Aktifitas LokasiPenelitian Keterangan
1. Persiapan lempengan plat dan gasket
Laboratorium Mekanika Teknik,Dept.
TeknikMesin, FT-USU. 2. Pembuatan dry cell
dengan 5-13 cell dan 3 stack, yaitu terdiri dari 2 plat negatif, 1 plat positif, dan 4-10 plat netral dengan dimensi plat 15 x 15 cm.
Laboratorium Mekanika Teknik,Dept.
TeknikMesin, FT-USU.
3. Ujipengaruh
penambahan plat netral dengan 4 plat netral.
Magister Teknik Mesin FT-USU. Lantai 4.
Menggunakan adaptor, gelas ukur, dan penghitung volume.
4 Ujipengaruh
penambahan plat netral dengan 6 plat netral .
Magister Teknik Mesin FT-USU. Lantai 4.
Menggunakan adaptor, gelas ukur, dan penghitung volume.
5 Ujipengaruh
penambahan plat netral dengan 8 plat netral .
Magister Teknik Mesin FT-USU. Lantai 4.
.6 Ujipengaruh
penambahan plat netral dengan 10 plat netral .
Magister Teknik Mesin FT-USU. Lantai 4.
Menggunakan adaptor, gelas ukur, dan penghitung volume.
7 Analisa data/olah data. Software Ms. Excel.
3.2 Alat dan Bahan
3.2.1 Alat
Beberapa alat yang digunakan pada penelitian mengenai pengaruh
penambahan plat netral terhadap perbandingn volume hidrogen pada dry cell
antara lain:
a. Gerinda Tangan
Gerinda berfungsi untuk membuat plat / lempengan yang dipotong
menjadi ukuran yang sama, dan juga dapat digunakan sebagai penghalus
permukaan plat tersebut, gerinda tangan dipilah karena proses pemotongan
dengan gerinda tangan lebih cepat.
b. Mesin Bor
Mesin bor ini berfungsi untuk melubangi beberapa bagian permukaan plat
untuk dapat menyusun plat secara rapi, mesin yang digunakan dalam
pembuatan dry cell adalah mesin bor tangan karena plat yang digunakan melebar sehingga mudah untuk dipindah-pindahkan dalam proses drilling.
c. Tang
Tang berfungsi untuk menahan dan mengunci baut serta memotong plat
agar susunannya lebih rapi pada susunan plat nya.
d. Gunting
Gunting berfungsi untuk memotong gasket agar lebih rapi dan sesuai
untuk susunan platnya.
e. Tang pembolong
Tang ini berfungsi untuk melubangi gasket agar sesuai dengan lubang
f. Gelas ukur
Gelas ukur berfungsi untuk menghitung volume air yang masuk dan
volume hidrogen yang dihasilkan.
3.2.2. Bahan
Bahan yang digunakan dalam penelitian ini adalah bahan yang mudah
didapatkan dan yang harganya murah agar biaya yang digunakan untuk membuat
seluruh rangkaian dry cell tetap terjangkau mengingat penelitian ini bertujuan untuk menghasilkan energi yang murah dan terjangkau. Beberapa bahan yang
digunakan yaitu :
a. Plat Stainless steel
Plat ini berfungsi sebagai pengantar arus dalam proses hidrolisis pada dry cell. Ukuran plat yang digunakan yaitu 15 x 15 cm dan tebal 0,5 mm.
Gambar 3.1. Plat Stainless steel
b. Plat Akrilik
Berfungsi sebagai end plate (plat akhir) pada dry cell. Tujuannya agar reaksi yang terjadi bisa dilihat langsung.
c. Selang dan tempat penampungan (botol)
Berfungsi sebagai saluran air dan tempat menyalurkan hidrogen dan
oksigen kedalam tabung penyimpanan.
d. Air murni
Air berfungsi sebagai fluida yang bergerak untuk proses elektrolisis
tersebut.
e. Baut penyangga
Berfungsi untuk sebagai penahan dan untuk merapikan plat seperti
gambar.
Gambar 3.3. Susunan plat dengan baut
f. Rubber Shet
Rubber shet berfungsi gasket untuk mencegah terjadinya korsleting pada plat yang disusun karena bersifat isolator dan sebagai ruang elektrolisis.
Gambar 3.4. Gasket g. Screen Nylon Monofilamen
Screen Nylon Monofilamen digunakan sebagai mesh membrane yang
berfungsi untuk memisahkan aliran air di dalam Dry Cell agar hidrogen
membran ini tidak menangkap ion. Ukuran Mesh Membrane yang
digunakan yaitu 15 X 15 cm.
Gambar 3.5. Screen Nylon Monofilamen 3.2.3 Alat Pendukung Peroses Pengujian
Alat yang dipakai dalam penelitian ini terdiri dari:
1. Mesin Las
Fungsi dari alat ini dalah sebagai adaptor yaitu alat penyedia arus searah yang
digunakan ketika proses elektrolisis berlangsung.
Gambar 3.6. Mesin Las
2. Thermocouple agilent
Berfungsi sebagai alat pendeteksi suhu pada setiap titik tertentu secara akurat
Gambar 3.7.Thermocouple agilent
3. Multi meter
Berfungsi sebagai pendeteksi arus dan voltase yang diberikan pada dry cell.
Gambar 3.8. Multi meter
4. Stop watch
Stop watch digunakan setiap 90 detik pada setiap variasi pengujian yang sudah disediakan.
3.2.4 Alat Pendukung Pada Proses PembuatanH2 dan O2 Wadah dan Alat Pendukung Penampungan Gas Hidrogen
Gambar 3.10. Wadah Penampungan Hidrogen
Gas hidrogen dan oksigen yang dihasilkan oleh tabung elektrolisis terlebih
dahulu ditampung dalam wadah yang terbuat dari wadah bekas air mineral ukuran
150 ml. Hal ini bertujuan agar ketika proses pengujian berlangsung, hidrogen
dapat segera digunakan tanpa harus menunggu proses elektrolisis itu sendiri yang
memakan waktu yang cukup lama. Selain itu wadah yang kita gunakan haruslah
wadah yang tahan terhadap tekanan 1 bar dan ukuran 150 ml.
Adapun bagian-bagian dari wadah penampungan itu adalah sebagai
berikut :
1. Botol mineral 150 ml
Botol yang digunakan sebagai wadah adalah botol mineral bekas dengan ukuran
150 ml dan tahan terhadap tekanan 1 bar.
2. Katup Udara
Fungsi dari katup udara inilah untuk memutus dan menyambungkan
wadah penampungan dengan tabung elektrolisis tanpa harus ada terbuangnya gas
ke udara.
3. Regulator
Gambar 3.12. Regulator
Regulator berfungsi untuk mengatur tekanan keluaran dry cell.
3.3. ProsedurPengujian
Berikut prosedur pengujian yang dilakukan .
Pengujian I:
a. Plat disiapkan pada pengujian pertama yaitu 4 plat netral. Dry cell disusun menggunakan 4 plat netral
b. Kabeltermocoupledidirekatkanpadabeberapatitikpada plat, sehinggasuhuelektrolisis plat dapatdiketahui.
c. Air dengan KOH 4%, 4,33% dan 4,66% disiapkan dalam masing masing tabung pengisi air.Penampung air dengan KOH 4% dihubungkan.
d. Tabung penampung gas hidrogen dan tabung penampung oksigen disiapkan dan dihubungkan pada gas out masing- masing pada dry cell
dan masing- masing penampung dihubungkan pada flow meter.
e. Data yang terabaca pada termocouple disimpan dan waktu pengujian dicatat.
f. Adaptor dihubungkan pada kutup masing- masing pada dry cell.
h. Saluran penampung air dengan KOH 4,33% dihubungkan dengan dry cell
dan ulangi ulangi prosedur g.
i. Saluran penampung air dengan KOH 4,66% dihubungkan dengan dry cell
dan ulangi ulangi prosedur g.
Pengujian II:
a. digunakan 6 plat netral dengan menambahkan 2 plat pada dry cell pada pengujian I.
b. Kabeltermocoupledidirekatkanpadabeberapatitikpada plat, sehinggasuhuelektrolisis plat dapatdiketahui.
c. Penampung air dengan KOH 4 % dihubungkan pada water inlet pada dry cell.
d. Tabung penampung gas hidrogen dan tabung penampung oksigen disiapkan dan dihubungkan pada gas out masing- masing pada dry cell
dan masing- masing penampung dihubungkan pada Flow meter.
e. Adaptor dinyalakan selama 90 detik kemudian hitung volume masing- masing gas yang dihasilkan pada masing-masing flow meter.
f. Saluran penampung air dengan KOH 4,33% dihubungkan dengan dry cell
dan ulangi ulangi prosedur e.
g. Saluran penampung air dengan KOH 4,66% dihubungkan dengan dry cell
dan ulangi ulangi prosedur e.
Pengujian III:
a. digunakan 8 plat netral dengan menambahkan 2 plat pada dry cell pada pengujian I.
b. Kabeltermocoupledidirekatkanpadabeberapatitikpada plat, sehinggasuhuelektrolisis plat dapatdiketahui.
c. Penampung air dengan KOH 4 % dihubungkan pada water inlet pada dry cell.
d. Tabung penampung gas hidrogen dan tabung penampung oksigen disiapkan dan dihubungkan pada gas out masing- masing pada dry cell
e. Adaptor dinyalakan selama 90 detik kemudian hitung volume masing- masing gas yang dihasilkan pada masing-masing flow meter.
f. Saluran penampung air dengan KOH 4,33% dihubungkan dengan dry cell
dan ulangi ulangi prosedur e.
g. Saluran penampung air dengan KOH 4,66% dihubungkan dengan dry cell
dan ulangi ulangi prosedur e.
Pengujian IV:
a. Digunakan 10 plat netral dengan menambahkan 2 plat pada dry cell pada pengujian I.
b. Kabel termocouple didirekatkan pada bebera patitik pada plat, sehingga suhu elektrolisis plat dapat diketahui.
c. Penampung air dengan KOH 4 % dihubungkan pada water inlet pada dry cell.
d. Tabung penampung gas hidrogen dan tabung penampung oksigen disiapkan dan dihubungkan pada gas out masing- masing pada dry cell
dan masing- masing penampung dihubungkan pada Flow meter.
e. Adaptor dinyalakan selama 90 detik kemudian hitung volume masing- masing gas yang dihasilkan pada masing-masing flow meter.
f. Saluran penampung air dengan KOH 4,33% dihubungkan dengan dry cell
dan ulangi ulangi prosedur e.
g. Saluran penampung air dengan KOH 4,66% dihubungkan dengan dry cell
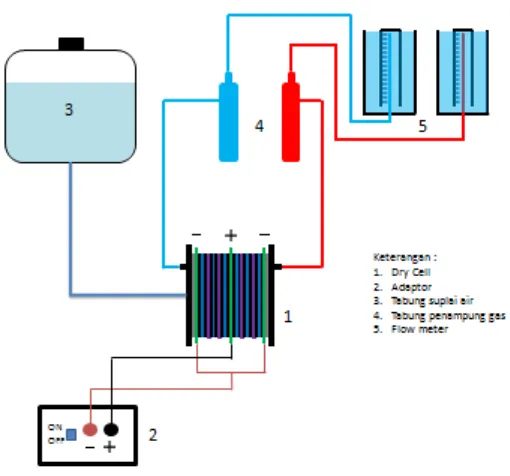
3.4 Instalasi Pengujian
Gambar 3.13.Instalasi Pengujian
Sumber : http://hho4free.com/hydrogen_separator_cell.htm
Dari gambar di atas dapat dijelaskan, arus listrik dialirkan melalui adaptor,
kemudian air yang mengandung KOH mengalir masuk kedalam dry cell. Didalam
dry cell terjadi elektrolisis. Hasil elektrolisis berupa gas hidogen dan oksigen mengalir ke penampung masing-masing yang berisi air yang berfungsi
memastikan adanya gas yang dihasilkan. Dari tabung penampung gas, gas
BAB IV
PENGOLAHAN DATA
4.1 Hasil Pengujian
4.1.1. Besarnya Daya Yang Digunakan Pada Pengujian
Dalampenelitian ini kuat arus divariasikan untuk mengetahui besar
pengaruh kuat arus terhadap produksi H2 dan O2, sedangkan untuk voltasenya
tetap. Sehingga dalam setiap pengujian, daya yang digunakan
berbeda-beda.Besarnya daya dapat dihitung dengan persamaan berikut.
P = V x I
Dimana :
P = Daya yang digunakan mesin dry cell ( Watt ) V = Tegangan yang digunakan mesin dry cell ( Volt ) I = Kuatarus yang digunakan mesin dry cell ( Ampere )
Dalam penelitian ini, perhitungan daya akan dibagi menjadi beberapa
bagian, yaitu untuk kuat arus 20A, 22A, 24A, dan 26 A, dengan voltase 50 Volt
disetiap penambahan plat netral yang digunakan yaitu 4,6,8, dan 10 plat. Sehingga
daya yang digunakan pada setiap pengujian menjadi :
a. P = 50 V x 20 A
= 1000 Watt
b. P = 50 V x 22 A
= 1100 Watt
c. P = 50 V x 24 A
= 1200 Watt
d. P = 50 V x 26 A
4.2. Besarnya Konsentrasi Larutan KOH
Dalam pengujian ini, KOH bereaksi dengan air sehingga terbentuk larutan
KOH. Besarnya konsentrasi larutan KOH kemudian diukur dengan menggunakan
persamaan:
% Konsentrasi larutan = massa (g) KOH x 100/volume (ml) air.
Massa KOH yang digunakan adalah 60,65,70, gram kemudian dilarutkan
didalam air 1.500 ml, sehingga konsentrasi larutan KOH adalah:
A. % Konsentrasi larutan = 60 x 100/1.500.
Larutan KOH merupakan senyawa larutan kimia, dengan melarutkan KOH
kedalam air. Reaksi kimia yang terjadi pada larutan tersebut adalah sebagai
berikut :
2KOH + 2H2O �������⎯⎯⎯� K2 + 3H2 +2O2
Reaksi kimia tersebut menunjukkan jika 3 bagian KOH dilarutkan
kedalam 3 bagian air dan kemudian dielektrolisis, maka akan terjadi penguraian
senyawa yang terjadi, yaitu K2 yang berupa padatan akan tetap bertahan didalam
larutan. Sedangkan 3 bagian H2 dan 2 bagian O2 akan keluar menguap ke udara.
Gas hidrogen inilah yang kemudian ditampung dan dijadikan bahan bakar
alternatif masa depan.
4.3. Menghitung Besar Volume Hidrogen dan Oksigen
Hasil pengujian ini memperoleh volume hidrogen dan oksigen yang
dielektrolisis, volume gas hasil elektrolisis yang telah diketahui kemudian
diuraikan dan diperoleh volume gas hidrogen dan oksigen dengan persamaan
kimia : 2KOH + 2H2O ������
nilaidari; jumlah produksi gas, suhu, volume H2 dan volume O2. Data hasil
percobaannya dapat dilihat pada tabel berikut.
Tabel. 4.1. Data Pengujian Voltase: 50 V, 4 Plat Netral, dengan Tebal Gasket 1,5 mm
Dari tabel di atas dapat dilihat bahwa pada 4 sel netral, suhu yang
dihasilkan mencapai 57,42 °C. Sedangkan nilai produksi tertingginya 701,44 ml.
Tabel. 4.2. Data Pengujian Voltase: 50 V, 6 Plat Netral, dengan Tebal Gasket 1,5 mm
Dari tabel di atas dapat dilihat bahwa pada 6 sel netral, suhu yang
Tabel. 4.3. Data Pengujian Voltase: 50 V, 8 Plat Netral, dengan Tebal Gasket
Dari tabel di atas dapat dilihat bahwa pada 8 sel netral, suhu yang
dihasilkan mencapai 44,68 °C. Sedangkan nilai produksi tertingginya 759,83 ml.
Tabel. 4.4. Data Pengujian Voltase: 50 V, 10 Plat Netral, dengan Tebal Gasket 1,5 mm
Dari tabel di atas dapat dilihat bahwa pada 10 sel netral, suhu yang
dihasilkan mencapai 525,984 °C. Sedangkan nilai produksi tertingginya 876,64
Grafik data hasil percobaan antara jumlah plat netral dengan suhu pada KOH 4%,
4,33% dan 4,66%dapat dilihat pada gambar dibawah ini.
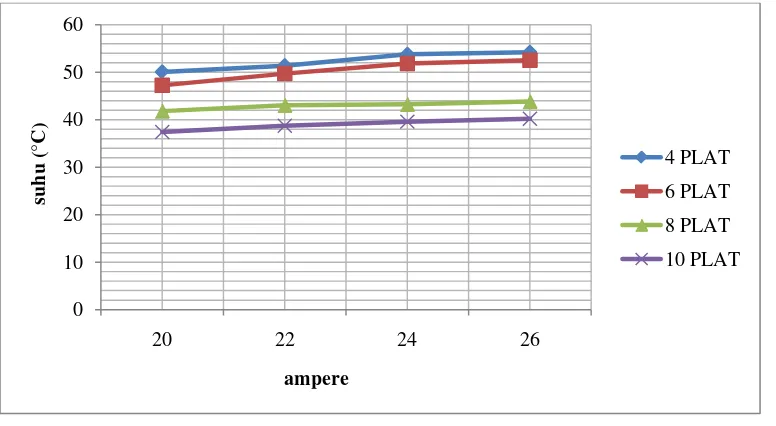
Gambar 4.1. Grafik Hasil Percobaan suhu vs Kuat arus dengan KOH 4%
Gambar 4.2. Grafik Hasil Percobaan suhu vs Kuat arus dengan KOH 4,33%
Gambar 4.3. Grafik Hasil Percobaan suhu vs Kuat arus dengan KOH 4,66%
Dari beberapa grafik di atas dapat dilihat bahwa semakin tinggi arus dan
semakin banyak KOH pada air, maka suhu yang dihasilkan semakin tinggi.
Sedangkan semakin banyak plat netral yang digunakan semakin rendah suhu yang
ditimbulkan.
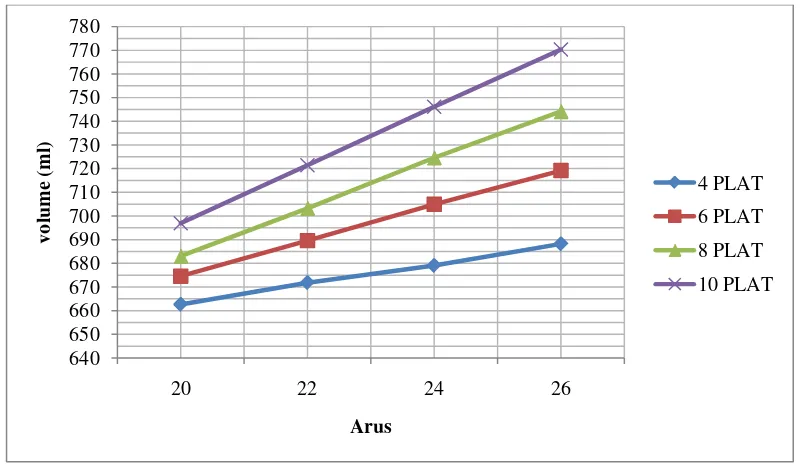
Grafik data hasil percobaan antara jumlah plat netral dengan produksi gas
pada KOH 4%, 4,33% dan 4,66% dapat dilihat pada gambar dibawah ini:
Gambar 4.5. Grafik Hasil Percobaan volume gas vs Kuat arus dengan KOH 4,33%
Dari grafik di atas, dapat dilihat semakin tinggi arus dan semakin banyak
plat netral dan KOH yang dipakai, maka gas yang dihasilkan semakin banyak
juga. Nilai produksi gas tertinggi dihasilkan pada KOH 4,66%, arus 26 Amper
dan 10 Plat netral yaitu 786,64 ml.Sedangkan grafik hasil produksi hidrogen dan
oksigenya dapat kita lihat pada gambar di bawah ini.
Gambar 4.7. Grafik Hasil Percobaan volume hidrogen vs Kuat arus dengan KOH 4 %
Gambar 4.9. Grafik Hasil Percobaan volume hidrogen vs Kuat arus dengan KOH 4,66%
Gambar 4.11. Grafik Hasil Percobaan volume oksigen vs Kuat arus dengan KOH 4 ,33%
4.4. Menghitung Laju Produksi Gas H2 dan O2
Hasil pengujian ini menghasilkan volume hidrogen dari proses elektrolisis.
Pada proses elektrolisis diperoleh waktu untuk memproduksi gas hidrogen dan
pada proses nya terdapat laju aliran produksi gas hidrogen. Laju aliran produksi
dapat diperoleh dengan menggunakan persamaan:
ṁ = �
Dari persamaan di atas didapatkan tabel data debit produksi dan laju
produksi hidrogendan oksigen sebagai berikut :
Tabel. 4.5. Data Pengujian, debit hidrogenQ H2 (m3/s) dan laju produksi hidrogen ṁ H2 (kg/s) pada 4 Plat Netral 20 653,12 391,872 4,35413E-06 4,84331E-05
20 662,61 397,566 4,4174E-06 4,91368E-05
20 673,24 403,944 4,48827E-06 4,99251E-05
22 660,21 396,126 4,4014E-06 4,89588E-05
22 671,82 403,092 4,4788E-06 4,98198E-05
22 683,42 410,052 4,55613E-06 5,068E-05
24 668,97 401,382 4,4598E-06 4,96085E-05
24 679,08 407,448 4,5272E-06 5,03582E-05
24 691,17 414,702 4,6078E-06 5,12547E-05
Tabel. 4.6. Data Pengujian, debit hidrogenQ H2 (m3/s) dan laju produksi hidrogen ṁ H2 (kg/s) pada 6 Plat Netral
6 PLAT
Kuat arus produksi Vol H2 Q H2 (m3/s) ṁ H2 (kg/s)
20 662,26 397,356 4,41507E-06 4,91109E-05
20 674,56 404,736 4,49707E-06 5,0023E-05
20 687,09 412,254 4,5806E-06 5,09522E-05
22 677,92 406,752 4,51947E-06 5,02722E-05
22 689,57 413,742 4,59713E-06 5,11361E-05
22 703,64 422,184 4,69093E-06 5,21795E-05
24 692,72 415,632 4,61813E-06 5,13697E-05
24 704,96 422,976 4,69973E-06 5,22773E-05
24 717,12 430,272 4,7808E-06 5,31791E-05
26 707,15 424,29 4,71433E-06 5,24397E-05
26 719,21 431,526 4,79473E-06 5,33341E-05
26 723,06 433,836 4,8204E-06 5,36196E-05
Tabel. 4.7. Data Pengujian, debit hidrogenQ H2 (m3/s) dan laju produksi hidrogen ṁ H2 (kg/s) pada 8 Plat Netral
8 PLAT
Kuat arus produksi Vol H2 Q H2 (m3/s) ṁ H2 (kg/s) 20 670,31 402,186 4,46873E-06 4,97078E-05
20 683,03 409,818 4,55353E-06 5,06511E-05
20 698,51 419,106 4,65673E-06 5,1799E-05
22 690,07 414,042 4,60047E-06 5,11732E-05
22 703,22 421,932 4,68813E-06 5,21483E-05
22 719,47 431,682 4,79647E-06 5,33534E-05
24 711,12 426,672 4,7408E-06 5,27341E-05
24 724,59 434,754 4,8306E-06 5,3733E-05
24 739,82 443,892 4,93213E-06 5,48624E-05
26 731,71 439,026 4,87807E-06 5,4261E-05
Tabel. 4.8. Data Pengujian, debit hidrogenQ H2 (m3/s) dan laju produksi hidrogen ṁ H2 (kg/s) pada 10 Plat Netral
10 PLAT
Kuat arus produksi Vol H2 Q H2 (m3/s) ṁ H2 (kg/s)
20 682,42 409,452 4,54947E-06 5,06059E-05
20 796,94 478,164 5,31293E-06 5,90983E-05
20 812,72 487,632 5,41813E-06 6,02684E-05
22 810,21 486,126 5,4014E-06 6,00823E-05
22 824,48 494,688 5,49653E-06 6,11405E-05
22 830,39 498,234 5,53593E-06 6,15788E-05
24 828,72 497,232 5,5248E-06 6,14549E-05
24 832,15 499,29 5,54767E-06 6,17093E-05
24 848,87 509,322 5,65913E-06 6,29492E-05
26 846,72 508,032 5,6448E-06 6,27898E-05
26 860,35 516,21 5,73567E-06 6,38005E-05
26 876,64 525,984 5,84427E-06 6,50085E-05
Tabel. 4.9. Data Pengujian, debit oksigenQ O2 (m3/s) dan laju produksi oksigenṁ O2 (kg/s) pada 4 Plat Netral
20 653,12 261,248 2,90276E-06 2,18088E-06
20 662,61 265,044 2,94493E-06 2,21257E-06
20 673,24 269,296 2,99218E-06 2,24807E-06
22 660,21 264,084 2,93427E-06 2,20456E-06
22 671,82 268,728 2,98587E-06 2,24333E-06
22 683,42 273,368 3,03742E-06 2,28206E-06
24 668,97 267,588 2,9732E-06 2,23381E-06
24 679,08 271,632 3,01813E-06 2,26757E-06
24 691,17 276,468 3,07187E-06 2,30794E-06
26 677,83 271,132 3,01258E-06 2,26339E-06
26 688,21 275,284 3,05871E-06 2,29805E-06
Tabel. 4.10. Data Pengujian, debit oksigenQ O2 (m3/s) dan laju produksi oksigenṁ O2 (kg/s) pada 6 Plat Netral
6 PLAT
Kuat arus produksi Vol 02 Q O2 (m3/s) ṁ O2 (kg/s)
20 662,26 264,904 2,94338E-06 2,2114E-06
20 674,56 269,824 2,99804E-06 2,25248E-06
20 687,09 274,836 3,05373E-06 2,29432E-06
22 677,92 271,168 3,01298E-06 2,26369E-06
22 689,57 275,828 3,06476E-06 2,3026E-06
22 703,64 281,456 3,12729E-06 2,34958E-06
24 692,72 277,088 3,07876E-06 2,31311E-06
24 704,96 281,984 3,13316E-06 2,35399E-06
24 717,12 286,848 3,1872E-06 2,39459E-06
26 707,15 282,86 3,14289E-06 2,3613E-06
26 719,21 287,684 3,19649E-06 2,40157E-06
26 723,06 289,224 3,2136E-06 2,41443E-06
Tabel. 4.11. Data Pengujian, debit oksigenQ O2 (m3/s) dan laju produksi oksigenṁ O2 (kg/s) pada 8 Plat Netral
8 PLAT
Kuat arus produksi Vol 02 Q O2 (m3/s) ṁ O2 (kg/s)
20 670,31 268,124 2,97916E-06 2,23828E-06
20 683,03 273,212 3,03569E-06 2,28076E-06
20 698,51 279,404 3,10449E-06 2,33245E-06
22 690,07 276,028 3,06698E-06 2,30427E-06
22 703,22 281,288 3,12542E-06 2,34818E-06
22 719,47 287,788 3,19764E-06 2,40244E-06
24 711,12 284,448 3,16053E-06 2,37456E-06
24 724,59 289,836 3,2204E-06 2,41953E-06
24 739,82 295,928 3,28809E-06 2,47039E-06
26 731,71 292,684 3,25204E-06 2,44331E-06
Tabel. 4.12. Data Pengujian, debit oksigenQ O2 (m3/s) dan laju produksi oksigenṁ O2 (kg/s) pada 10 Plat Netral
10 PLAT
Kuat arus produksi Vol 02 Q O2 (m3/s) ṁ O2 (kg/s)
20 682,42 272,968 3,03298E-06 2,27872E-06
20 796,94 318,776 3,54196E-06 2,66112E-06
20 812,72 325,088 3,61209E-06 2,71382E-06
22 810,21 324,084 3,60093E-06 2,70543E-06
22 824,48 329,792 3,66436E-06 2,75308E-06
22 830,39 332,156 3,69062E-06 2,77282E-06
24 828,72 331,488 3,6832E-06 2,76724E-06
24 832,15 332,86 3,69844E-06 2,7787E-06
24 848,87 339,548 3,77276E-06 2,83453E-06
26 846,72 338,688 3,7632E-06 2,82735E-06
26 860,35 344,14 3,82378E-06 2,87286E-06
26 876,64 350,656 3,89618E-06 2,92726E-06
Dari hasil percobaan di atas dapat dilihat bahwa semakin banyak plat
netral yang digunakan debit dan laju produksi hidrogen dan oksigennya semakin
tinggi. Dapat dilihat laju produksi tertinggi hidrogen pada 10 plat netral yaitu
6,50085 × 10−5kg/s. Sedangkan laju produksi tertinggi oksigen terjadi pada 10
plat netral yaitu 2,92726 × 10−5kg/s.
Analisa:
1. Besarnya laju produktifitas hidrogen dan oksigen meningkat seiring
penambahan plat netral. Semakin banyak plat netral, semakin luas area
elektrolisis, sehingga gas yang dihasilkan semakin banyak.
2. Besarnya laju produktifitas hidrogen dan oksigen sangat dipengaruhi besar
kecilnya kuat arus dan konsentrasi KOH, semakin besar kuat arus dan
konsentrasi KOH maka waktu laju produktifitas semakin cepat, begitu
4.5. Besar Energi Yang Digunakan
Pengujian pengaruh penambahan plat netral terhadap produktifitas gas
hidrogen dan oksigen membutuhkan energi untuk mengelektrolisis air.
Perhitungan energi akan dibagi menjadi beberapa bagian, karena penambahan plat
netral terhadap waktu produksi, laju produksi dan suhu. Voltase yang dipakai pada
setiap penambahan plat, yaitu 50 V sedangkan arus yang dipakai bervariasi, yaitu
20, 22, 24, 26 ampere. Waktu yang digunakan tetap pada setiap pengujian yaitu 90
detik. Maka besar energi yang digunakan dapat dihitung dengan persamaan
berikut:
E=V.I.t
Dimana
E= energi yang digunakan (watt hour)
V= voltase (Volt)
I = Arus (Ampere)
t = waktu (hour) ; (90 s /3600 s =0,025 hour)
1. E= V.I.t = 50 x 20 x 0,025
= 25 watt hour
2. E= V.I.t = 50 x 22 x 0,025
= 27,5 watt hour
3. E= V.I.t = 50 x 24 x 0,025
= 30 watt hour
4. E= V.I.t = 50 x 26 x 0,025
4.6. Energi Yang Terbuang
Setelah mengetahui besar energi yangdigunakan dalam proses elektrolisis,
kita dapat mengetahui besar energi terbuang menggunakan persamaan berikut ;
E = V x I x t
E = Energi yang digunakan dalam mesin drycell (Watt-hours). V = Tegangan yang digunakanmesin drycell (Volt).
I = Kuatarus yang digunakanmesin drycell (Ampere).
t = Waktu yang dibutuhkan untuk proses elektrolisis (hours).
ΔT = Perubahan Temperatur (C). Tf = Tempertur Akhir (C).
TS = Temperatur Awal (25 oC ).
Vf = Volume air (cm3).
HLost = Energi Terbuang (kalori).
%Lost = Persentase energi yang terbuang.
Sehingga didapatkan data dari tabel berikut ;
Tabel. 4.13. Data PengujianEnergi TerbuangHLost (kalori) dan %Lost
Tabel. 4.14. Data PengujianEnergi TerbuangHLost (kalori) dan %Lost
Persentase energi yang terbuang pada 6 Plat Netral
Kuat
Tabel. 4.15. Data PengujianEnergi TerbuangHLost (kalori) dan %Lost
Persentase energi yang terbuang pada 8 Plat Netral
Tabel. 4.16. Data PengujianEnergi TerbuangHLost (kalori) dan %Lost
Persentase energi yang terbuang pada 10 Plat Netral
Kuat
NB: Tanda minus (-) menunjukkan energi yang terbuang
Analisa:
1. Besarnya energi yang digunakan semakin meningkat jika kuat arus
semakin meningkat.
2. Semakin banyak plat netral yang digunakan dan semakin tinggi
Berikut beberapa grafik yang menunjukkan perubahan suhu pada arus
yang tetap;
Gambar 4.13 Grafik Suhu Vs Jumlah Plat Netral pada arus 20 Amper
Gambar 4.15 Grafik Suhu Vs Jumlah Plat Netral pada arus 24 Amper
Gambar 4.16 Grafik Suhu Vs Jumlah Plat Netral pada arus 26 Amper Dari beberapa grafik di atas dapat dilihat bahwa semakin tinggi arus dan
semakin banyak KOH pada air, maka suhu yang dihasilkan semakin tinggi.
Sedangkan semakin banyak plat netral yang digunakan semakin rendah suhu yang
ditimbulkan, hal ini terjadi karena plat pada dry cell merupakan hambatan, semakin besar hambatan maka semakin rendah suhu yang ditimbulkan.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berikut kesimpulan yang dapat diambil dari hasil penelitian ini yaitu:
1. Pengaruh penambahan plat netral pada Dry Cell terhadap produksi hidrogen dan oksigen yaitu terjadinya peningkatan nilai produksi disetiap
penambahan plat netral. Dimana dari hasil tabel menunjukkan nilai
produksi paling tinggi yaitu berada pada penambahan 10 plat. Nilai
produksi hidrogen tertinggi yaitu 525,984ml dan nilai produksi tertinggi
oksigen yaitu 350,656 ml.
2. Penambahan plat netral pada Dry Cell juga berpengaruh pada suhu. Dapat dilihat pada tabel dan grafik, nilai suhu semakin menurun di setiap
penambahan plat. Dimana suhu tertinggi terjadi pada 4 plat netral yaitu
57,42°C dan suhu terendah terjadi pada 10 plat netral yaitu 42,94 °C.
3. Pengaruh kuat arus (Ampere) terhadap suhu yaitu, semakin tinggi arus,
semakin tinggi suhu yang di hasilkan. Dari data yang dihasilkan, suhu
tertinggi terjadi pada arus 26A di setiap penambahan plat netral
4. Kuat arus juga berpengaruh pada nilai produksi, yaitu semakin besar arus,
semakin tinggi nilai produksinya.
5. Penambahan KOH sebagai katalis berpengaruh pada suhu. Disetiap
penambahan %KOH pada setiap pengujian, menunjukkan peningkatan
suhu.
6. Penambahan KOH juga berpengaruh pada nilai produksi, nilai produksi
5.2 Saran
Berikut saran yang berguna dari pengujian ini ;
1. Melengkapi alat ukur pada saat pengujian untuk memperoleh hasil
pengujianyang lebih baik.
2. Menjaga setiap sudut dry cell terhadap kebocoran agar hasil yang diperoleh lebih baik.
3. Menjaga selang hidrogen dan oksigen jauh dari api pada saat pengujian
karna dapat menimbulkan ledakan.
4. Memilih pipa yang tidak bereaksi dengan oksigen maupun hidrogen agar
DAFTAR PUSTAKA
[1] Emoto, M. 2006. The True Power Of Water. MQ Publishing: Bandung.
[2] Gunawan Erri. 2001. Tinjauan Produksi Gas Hidrogen dari 4 Jenis Elektroda
Stainless Steel. Surabaya: Jurusan Teknik Mesin-Institut Teknologi Sepuluh
Nopember.
[3] Jun, W. 2008. Mengubah Air Menjadi Bensin. Pustaka Radja: Yogyakarta.
[4] Wiryawan, Dody. 2013. Pengaruh Variasi Arus Listrik Terhadap Produksi
Brown’s Gas Pada Elektroliser. Malang:UB.
[5
[6
[7] http//:www.hho4free.com
[8] http//:www.gas-hho.blogspot.com
[9