BAB II
TINJAUAN PUSTAKA
2.1 Fuel cell
Sel bahan bakar (fuel cell) adalah sebuah alat yang mirip denga tetapi berbeda karena dia dirancang untuk dapat diisi terus reaktannya yang terkonsumsi; yaitu dia memproduksi listrik dari penyediaan bahan bakar internal dari baterai. Sebagai tambahan, elektrode dalam baterai bereaksi dan berganti pada saat baterai diisi atau dibuang energinya, sedangkan elektrode sel bahan bakar adalah katalitik dan relatif stabil[6].
Biasanya, aliran reaktan mengalir masuk dan produk dari reaktan mengalir keluar. Sehingga operasi jangka panjang dapat terus menerus dilakukan selama
aliran tersebut dapat dijaga kelangsungannya.
Sel bahan bakar dianggap sangat menarik dalam aplikasi modern karena efisiensi tinggi dan penggunaan bebas-emisi, berlawanan dengan bahan bakar umum seperti satunya murni adala hidrogen yang menggunakan banyak energi. Memproduksi hidrogen membutuhkan "carrier" hidrogen (biasanya dapat dijadikan alternatif), dan juga listrik, yang diproduksi oleh bahan bakar konvensional. Meskipun sumber dapat juga digunakan, namun sekarang ini mereka sangat mahal.
2.2 Jenis – Jenis Sel bahan bakar
dalam sel, jenis katalis yang diperlukan, batas temperatur dimana sel tersebut bekerja, bahan bakar yang dibutuhkan, dan faktor – faktor lainnya. Adapun sel bahan bakar hingga saat ini terbagi menjadi 7 klasifikasi utama antara lain :
1. Polymer Electrolyte Membrane (PEM) 2. Direct methanol
3. Alkaline 4. Phosporic acid 5. Molten carbonate 6. Solid oxide 7. Regenerative
Proton Exchange Membrane (PEM) lebih dikenal sebagai
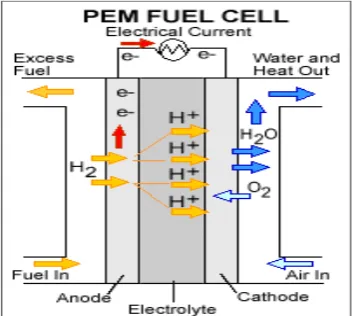
PolymerElectrolyte Membranemenyalurkan berat jenis yang inggi dan menawarkan keuntungan pada berat dan volume yang rendah, dibandingkan dengan sel bahan bakaryang lainnya. Sel bahan bakar PEM menggunakan polimer solid sebagai elektrolit dan elektroda karbon yang mengandung katalis platinum. PEM membutuhkan hanya hydrogen, oksigen dari udara, dan air untuk beroperasi dan tidak memerlukan cairan korosif.
Gambar 2.1 Aliran hidrogen dan oksigen di dalam sel bahan bakar PEM Sumbe
pada sel bahan bakar. DMFC ini tidak mempunyai permasalahan tempat penyimpanan seperti sel bahan bakar lain pada umumnya.
Alkaline fuel cell adalah salah satu dari teknologi sel bahan bakar yang dikembangkan, dan merupakan yang pertama digunakan secara luas untuk program penghasil energi listik dan air pada pesawat luar angkasa oleh NASA. Sel
bahan bakar ini menggunakan potasium hidroksida dalam air sebagai elektrolit dan dapat menggunakan beberapa jenis dari metal sebagaikatalis pada anoda dan katoda.
Phosporic Acid Fuel Cell (PAFC) menggunakan cairan asam fosfor sebagai elektrolit dan elektroda besi karbon yang mengandung katalis platinum. PAFC ini lebih dikenal sebagai generasi pertama dari sel bahan bakar modern. PAFC lebih toleran terhadap ketidakmurnian dari pada bahan bakar yang telah diubah menjadi hidrogen dari pada Sel bahan bakar PEM.
Molten Carbonate Fuel Cell (MCFC) saat ini sedang dikembangkan untuk gas natural dan batubara untuk kegunaan elektrik, industri, dan aplikasi militer. MCFC adalah sel bahan bakar yang bekerja pada temperatur tinggi yang menggunakan elektrolit yang terdiri dari molten carbonate saltmixture, lithium aluminium oksida (LiAlO2) .
Solid Oxide Fuel Cell (SOFC) menggunakan bahan keramik yang keras dan tidak mudah berkarat sebagai elektrolit. SOFC ini diharapkan dapat memiliki efisiensi 50 – 60 % untuk mengubah bahan bakar menjadi listrik.
2.3 Polymer Exchanger Membrane Fuel Cell
Pada saat ini ada beberapa tipe sel bahan bakar yaitu proton exchanger membrane fuel cell (PEM), sel bahan bakar alkali, asam fosfat, karbonat cair dan
oksida padat. PEM dan alkali bekerja pada suhu dibawah 2000C. Sehingga disebut mesin dingin. Beberapa keuntungan sel bahan bakar apabila emisi gas buang sangat mudah bahkan bisa dikatakan tidak ada yaitu, dapat dioperasikan terus-menerus, mudah untuk dioperasikan, ringan dan mudah digabung menjadi kesatuan dari beberapa sel tunggal untuk menghasilkan energi yang besar apabila diperlukan. Sehingga sel bahan bakar dapat dibuat untuk keperluan bermacam-macam alat serba guna.
Pada gambar dibawah ini diperlihatkan rangkaian alat sel bahan bakar secara umum. Bagian-bagian sel bahan bakar terdiri dari, katalis berupa logan Pt atau campuran Pt-Ru sebagai anode dan katode. Diantara anode dan katode ditempatkan membran penukar ion. Fungsi membran adalah melewatkan ion H+. Elektron keluar dari sel menuju ke rangkaian alat dan arus elektron dimanfaatkan menjadi energi listrik. Kemudian elektron mengalir menuju sisi katode. Katalis di sisi anode didukung oleh penyangga berupa lapisan hidrolik ( suka air) terbuat dari karbon, sedangkan di sisi katode katalis didukung oleh lapisan penyangga
hidropobik ( tidak suka air) yang terbuat dari PTFE. Di sisi katode dimasukkan oksigen dari udara. Oksigen akan bereaksi melalui pembentukan molekul antara ( intermediate) sebelum terbentuk ion O−2. Selanjutnya ion O−2 , elektron dan ion
H+ bereaksi membentuk molekul air ( H2O). Reaksi di sisi anode dan sisi katode dapat dinyatakan dengan persamaan setengah reaksi di bawah ini.
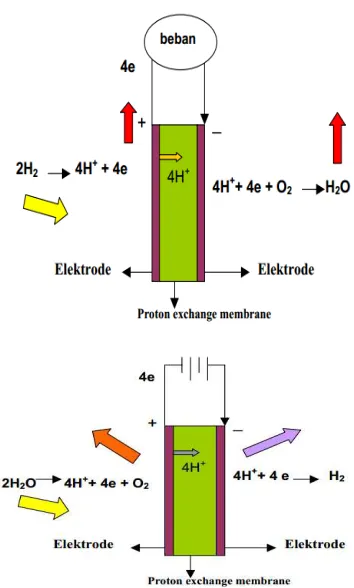
di sisi anode terjadi ionisasi molekul hidrogen menjadi ion H+ dan elelktron,
2H2 𝑅𝑒𝑎𝑘𝑠𝑖�⎯⎯⎯�4H+4e−
Di sisi katode terjadi reaksi pembentukan air,
Gambar 2.2 Reaksi Elektrolisis Air Pada PEM 2.4 Dry Cell
Dry cell merupakan sebuah alat yang menggunakan prinsip elektrolisis untuk memecah ikatan air menjadi hidrogen dan oksigen sekaligus memisahkan hidrogen dan oksigen tersebut agar tidak tercampur[8]. Elektrolisis air adalah peristiwa penguraian senyawa air (H2O) menjadi oksigen (O2) dan hidrogen gas (H2) dengan menggunakan arus listrik yang melalui air tersebut. Pada katode, dua molekul air bereaksi dengan menangkap dua elektron, tereduksi
menjadi gas H2 dan ion hidroksida (𝑂𝐻−). Sementara itu pada anode, dua molekul air lain terurai menjadi gas oksigen (O2), melepaskan 4 ion H+.serta mengalirkan elektron ke katode. Ion H+ dan OH mengalami netralisasi sehingga terbentuk kembali beberapa molekul air. Reaksi keseluruhan yang setara dari elektrolisis air dapat dituliskan sebagai berikut.
2𝐻2𝑂(𝑙)𝑅𝑒𝑎𝑘𝑠𝑖�⎯⎯⎯�2𝐻2(g) +𝑂2(g)
dimanfaatkan untuk menghasilkan hidrogen dan hidrogen peroksida (H2O2) yang dapat digunakan sebagai bahan bakar kendaraan hidrogen.
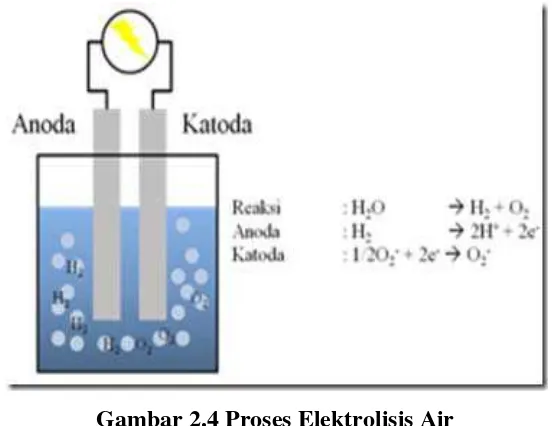
Gambar 2.3 Dry cell 2.4.1 Proses Elektrolisis Air
Dengan menyediakan energi dari baterai, Air (H2O) dapat dipisahkan ke dalam molekuldiatomik hidrogen (H2) dan oksigen(O2).
Gambar 2.4 Proses Elektrolisis Air
2.4.2 Metode Pemisahan Hidrogen dan Oksigen pada Dry Cell
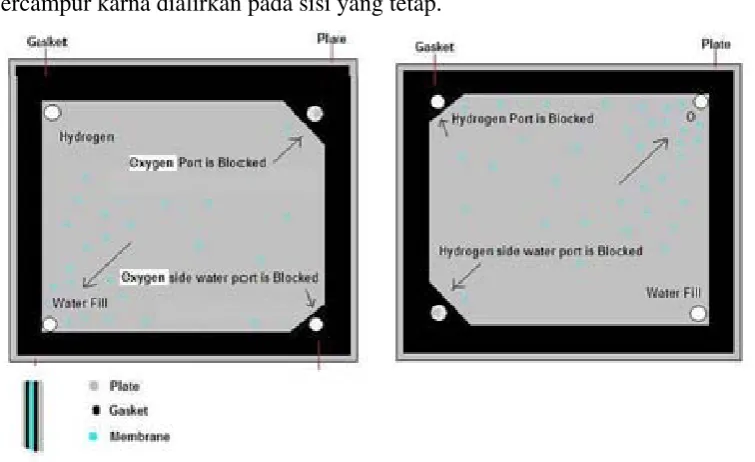
Hal pertama yang harus diperhatikan agar hidrogen terpisah dengan Oksigen yaitu memisahkan aliran air yang akan dielektrolisis menjadi dua bagian aliran. Untuk membagi aliran air ini lobang pada gasketlah yang mnjadi inti pembagiannya. Gasket dibuat seperti gambar 2.4 di bawah. Ketika disusun, aliran
dibagi menjadi aliran sisi kiri dan aliran sisi kanan, dimana aliran sisi kiri tidak bersentuhan dengan aliran sisi kanan sehingga gas yang dihasilkan juga tidak bercampur karna dialirkan pada sisi yang tetap.
Gambar 2.5 Bentuk Gasket Yang Dipakai
Sumber : http://hho4free.com/hydrogen_separator_cell.htm
Membran yang digunakan harus terbuat dari material yang tidak bersifat
Gambar 2.6 Contoh Membran
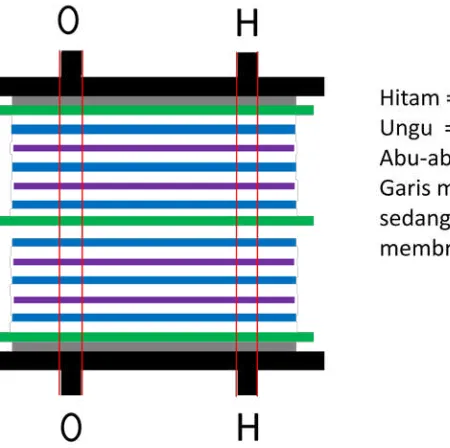
Kemudian plat, membran dan gasket akan disusun seperti gambar 2.6 dibawah sehingga dapat dilihat aliran gas yang akan dihasilkan.
Gambar 2.7 Aliran Oksigen dan Hidrogen