PENGARUH LAMA PENYIMPANAN DAN CARA PENGOLAHAN BUAH
TERUNG BELANDA (Cyphomandra betaceae) YANG DIKUPAS
TERHADAP KANDUNGAN VITAMIN C
SKRIPSI
REZEKIKA HARAHAP
090822053
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH LAMA PENYIMPANAN DAN CARA PENGOLAHAN BUAH
TERUNG BELANDA (Cyphomandra betaceae) YANG DIKUPAS
TERHADAP KANDUNGAN VITAMIN C
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
REZEKIKA HARAHAP 090822053
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH LAMA PENYIMPANAN DAN CARA PENGOLAHAN BUAH TERUNG BELANDA (Cyphomandra betaceae) YANG DIKUPAS TERHADAP KANDUNGAN
VITAMIN C Kategori : SKRIPSI
Nama : REZEKIKA HARAHAP Nomor Induk Mahasiswa : 090822053
Program Studi : KIMIA EKSTENSI Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di Medan, Agustus 2011
Komisi Pembimbing:
Pembimbing II, Pembimbing I,
Drs Ahmad Darwin, MSc Dr Tini Sembiring, MS NIP. 195211161980031001 NIP.194805131971072001
Diketahui/ Disetujui Oleh
Departemen Kimia FMIPA USU
PERNYATAAN
PENGARUH LAMA PENYIMPANAN DAN CARA PENGOLAHAN BUAH TERUNG BELANDA (Cyphomandra beteceae) YANG DIKUPAS TERHADAP KANDUNGAN
VITAMIN C
SKRIPSI
Saya mengakui bahwa skripsi inii adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan seumbernya.
Medan, Agustus 2011
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Allah SWT, Tuhan semesta alam yang telah
melimpahkan rahmat dan karunia-Nya sehingga skripsi ini berhasil diselesaikan dalam waktu
yang telah ditetapkan.
Pada kesempatan ini saya menyampaikan ucapan terima kasih kepada DR.Tini
Sembiring, MS dan Drs.Ahmad Darwin Bangun, Msc selaku pembimbing pada penyelesaian
skripsi ini yang telah memberikan panduan dan penuh kepercayaan kepada saya untuk
menyempurnakan kajian ini. Ucapan terima kasih juga ditujukan kepada ketua Departemen
kimia Dr.Rumondang Bulan ,MS serta semua dosen pada Departemen kimia FMIPA USU.
Akhirnya, tidak terlupakan kepada kedua orang tua saya Syamsul Bahri Harahap dan Cut
Haryani Arsyad yang selalu memberikan doa,dorongan dan materi yang tak ternilai yang sangat
saya perlukan. Saya juga mengucapkan terima kasih kepada abang dan adik saya, sahabat saya
Erna suryani, Titis Utami agung, Novira seseranti, Ryzka H Pane, Jatu Wahyuni, Fenni hrp,
Chairil Fadli dan Fordinand limbong yang memberikan bantuan kepada saya, juga kepada Danu
ilhami yang selalu memberi dukungan penuh kepada saya, serta asisten lab analitik dan
rekan-rekan kuliah yang terlibat dalam penyelesaian skripsi ini. Semoga Tuhan Yang Maha ESA akan
membalasnya.
ABSTRAK
Telah dilakukan penelitian untuk mengetahui kandungan vitamin C dengan adanya pengaruh lama penyimpanan dan cara pengolahan yang terdapat dalam buah terung belanda
(Cyphomandra betaceae) yang dikupas mengunakan metode titrasi iodometri yang dilakukan dengan dua perlakuan. Perlakuan pertama yaitu pengaruh lama penyimpanan 0 hari (kontrol), 1 hari, 2 hari, 3 hari dan 4 hari. Perlakuan kedua yaitu proses pengolahan pemblenderan dan tanpa pemblenderan. Masing-masing perlakuan dilakukan dengan 3 ulangan. Hasil penelitian
menunjukkan bahwa lama penyimpanan dan cara pengolahan berpengaruh terhadap penurunan kandungan vitamin C. Kandungan vitamin C tertinggi yaitu pengaruh lama penyimpanan 0 hari sebesar 225,14 mg/100 g sampel. Sedangkan kandungan vitamin C terendah yaitu lama
DAFTAR LAMPIRAN
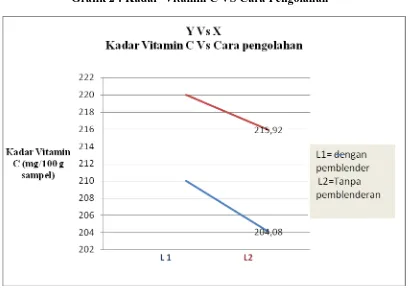
Grafik 1 : Kadar vitamin C vs lama penyimpanan Grafik 2 : Kadar vitamin C vs cara pengolahan
ABSTRAK
Telah dilakukan penelitian untuk mengetahui kandungan vitamin C dengan adanya pengaruh lama penyimpanan dan cara pengolahan yang terdapat dalam buah terung belanda
(Cyphomandra betaceae) yang dikupas mengunakan metode titrasi iodometri yang dilakukan dengan dua perlakuan. Perlakuan pertama yaitu pengaruh lama penyimpanan 0 hari (kontrol), 1 hari, 2 hari, 3 hari dan 4 hari. Perlakuan kedua yaitu proses pengolahan pemblenderan dan tanpa pemblenderan. Masing-masing perlakuan dilakukan dengan 3 ulangan. Hasil penelitian
menunjukkan bahwa lama penyimpanan dan cara pengolahan berpengaruh terhadap penurunan kandungan vitamin C. Kandungan vitamin C tertinggi yaitu pengaruh lama penyimpanan 0 hari sebesar 225,14 mg/100 g sampel. Sedangkan kandungan vitamin C terendah yaitu lama
BAB I
PENDAHULUAN
1.1. Latar Belakang
Terung Belanda (cyphomandra ) atau terung kori mulai di kembangkan di Bogor Jawa Barat
sejak tahun 1941,pertama kali dibawa dan dikembangkan di Indonesia oleh orang belanda pada
waktu itu sehingga dikenal dengan nama Terung Belanda, Selain enak dikonsumsi buah terung
belanda juga punya khasiat untuk menurunkan kolesterol, mengobati darah tinggi, mengatasi
sariawan, mengatasi asam urat dan masih banyak lagi manfaat lainnya.
Buah dengan nama latin solanun guatense termasuk famili solonaceae ini mempunyai
warna bermacam-macam. Buah terung belanda ini dimanfaatkan sebagai buah segar, untuk
bumbu masak, sayuran dan minuman. Terung belanda mengandung provitamin A yang baik
untuk kesehatan mata, dan mengandung Vitamin C untuk mengobati sariawan, panas dalam,
meningkatkan daya tahan tubuh dan mempunyai serat dalam buahnya untuk mencegah sembelit.
Vitamin C disebut juga asam askorbat, merupakan vitamin yang paling sederhana mudah
berubah akibat oksidasi. Struktur kimianya terdiri dari rantai 6 atom C (C6H8O6) dan
kedudukannya tidak stabil karena mudah bereaksi dengan O2 diudara menjadi asam
dehidroaskorbat. Banyak vitamin yang merupakan koenzim. Pada vitamin C asam L-askorbat
dengan adanya enzim asam askorbat oksidasi akan teroksidasi menjadi asam L-dehidroaskorbat.
Asam ini secara kimia juga sangat labil walaupun sifat vitamin C mudah berubah akibat oksidasi
namun stabil jika merupakan kristal murni. (Safaryani, S. 2007)
Selain pengaruh tersebut, kandungan vitamin C juga akan menurun disaat buah sudah
dipanen. Dimana Infeksi mikroorganisme terhadap produk dapat terjadi semasih buah dan
sayuran tersebut berada dilapangan, namun mikroorganisme tersebut tidak tumbuh dan
berkembang, hanya berada di dalam jaringan bila kondisinya memungkinkan terutama setelah
mikroorganisme tersebut segera dapat tumbuh dan berkembang dan menyebabkan pembusukan
yang serius. (Utama, M. S. 2001)
Penyimpanan pada suhu rendah dapat menghambat aktivitas enzim dan reaksi-reaksi
kimia serta menghambat atau menghentikan pertumbuhan mikroba. Penyimpanan pada suhu
rendah dapat memperpanjang masa hidup dari jaringan-jaringan di dalam bahan pangan tersebut.
Hal ini tidak hanya disebabkan proses respirasi yang menurun, tetapi juga karena terhambatnya
pertumbuhan mikroba penyebab kebusukan dan kerusakan. Pada penelitian (Rachmawati, R)
selama penyimpanan kandungan vitamin C pada cabai rawit putih mengalami penurunan terus
menerus hingga menjadi rusak. Hal ini disebabkan terjadinya proses respirasi dan oksidasi
vitamin C menjadi asam L- dehidroaskorbat dan mengalami perubahan lebih lanjut menjadi asam
L – diketogulonat yang tidak memiliki keaktifan vitamin C.
Pada umumnya turunnya asam askorbat lebih cepat pada suhu penyimpanan tinggi. Hal
ini berarti aktivitas enzim yang berperan dalam perombakan vitamin C masih berlangsung terus
dengan bertambahnya waktu penyimpanan sehingga dapat merusak kandungan vitamin C.
(Syafrani, S. 2007)
Pengolahan dengan berbagai cara akan menurunkan kadar vitamin C. Contohnya
pemanasan dan aktivitas air. Kerusakan lainnya terhadap vitamin C dalam sayuran atau
buah-buahan dapat disebabkan oleh enzim Ascorbic oxidase acid bila sayuran atau buah-buah-buahan
dipotong ataupun diiris-iris maka enzim akan terbebaskan dan dapat merusak vitamin C,
sehingga kehilangan vitamin C pun akan semakin terjadi. (Anita, F. P . 1973)
Secara umum buah terung belanda dapat dikonsumsi dengan 2 cara:
1. Dimakan langsung sebagai buah segar (tanpa proses pemblenderan)
2. Dimakan sebagai jus (adanya proses pemblenderan)
Disamping itu, buah terung belanda yang ada dipasaran tidak laku dijual atau langsung
dikonsumsi setelah dipetik, bisa dikonsumsi setelah beberapa hari sehingga diprediksi akan
Penyimpanan dilakukan pada suhu kamar karena umumnya buah terung belanda yang ada
dipasaran tidak disimpan pada suhu yang dingin atau lemari es.
Menurut Egan, H(1981) metode iodometri dapat digunakan untuk menetukan kadar
vit.amin C dalam minuman berwarna seperti sirup Blackcurrent dengan penambahan merkuri
chlorida yang dilarutkan dengan iodin sehingga kelebihan iodin dititrasi untuk menentukan
kandungan vitamin C didalam sirup Blackcurrent.
Selain metode titrasi iodometri penentuan kandungan vitamin C dapat dilakukan dengan
titrasi 2,6 dichloro phenol indophenol, dan menggunakan spektrofotometri uv-visible akan tetapi
metode tersebut tidak digunakan dalam penelitian karena sampel yang digunakan berwarna akan
mengganggu pengukuran karena zat warna yang berasal dari sampel.
Berdasarkan uraian diatas, kita perlu menjaga kandungan vitamin C. Agar kandungan
vitamin C dapat dipertahankan semaksimal mungkin maka pengetahuan tentang pengolahan
vitamin C perlu dipahami sehingga penulis tertarik untuk melakukan studi mengenai pengaruh
lama penyimpanan dan cara pengolahan buah terung belanda yang dikupas terhadap kandungan
vitamin C menggunakan metode iodometri dengan memanfaatkan sifat reduksi vitamin C
terhadap merkuri chlorida yang dapat mengabsorbsi warna dari buah terung belanda yang
dikupas tersebut dengan penambahan asam metapospat untuk menonaktifkan enzim agar enzim
tidak berjalan terus sehingga pengukuran kandungan vitamin C dapat dilakukan.
1.2. Permasalahan
Bagaimanaka kadar vitamin C yang terkandung dalam buah Terung belanda yang dikupas
dengan adanya pengaruh penyimpanan dan cara pengolahan (adanya proses blender dan tanpa
blender).
1.3. Pembatasan Masalah
Penulis membatasi masalah yang berhubungan dengan penelitian ini, yaitu :
2. Varietas terung belanda yang digunakan untuk menentukan kadar vitamin C adalah
varietas terung belanda merah.
3. Vitamin C yang terdapat dalam buah terung belanda ditentukan dengan metode iodometri
dengan memanfaatkan sifat reduksi vitamin C terhadap merkuri chlorida.
1.4. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
a. Untuk mengetahui kadar vitamin C yang terdapat dalam buah terung belanda yang
dikupas dengan adanya pengaruh lama penyimpanan
b. Untuk mengetahui kadar vitamin C yang terdapat dalam buah terung belanda yang
dikupas dengan adanya pengaruh cara pengolahan (adanya proses blender tanpa blender).
1.5. Manfaat Penelitian
Memberikan informasi tentang kadar vitamin C yang dilakukan dengan adanya lama
penyimpanan dan cara pengolahan (adanya proses blender dan tanpa blender) buah terung
belanda yang dikupas
1.6. Metodologi Penelitian
Dalam penelitian penentuan kadar vitamin C dilakukan dengan menggunakan titrasi iodometri
dengan memanfaatkan sifat reduksi asam askorbat terhadap merkuri chlorida. menggunakan
larutan standar Na2S2O3 dan indikator Amilum, dimana dengan adanya penambahan larutan
Iodin 0.01N menyebabkan terjadinya perubahan warna menjadi bening sebagai titik akhir titrasi.
1.7. Lokasi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Terung Belanda
2.1.1. Mengenal Tanaman Terung Belanda
Buah tamarillo atau terung belanda (Cyphomandra betacea) merupakan tanaman yang sangat
populer di new Zealand. Tanaman ini termasuk keluarga solanaceae yang berasal dari peru dan
masuk ke Negara Indonesia. Buah ini bentuknya bulat panjang berasa kombinasi antara tomat
dan jambu biji sehingga tidak mengherankan masyarakat di New Zealand sangat menyukainya.
Pohon terung belanda mempunyai akar yang dangkal, pohonnya kecil setengah berkayu, tidak
memerlukan perawatan yang sulit dan belum banyak dibudidayakan secara masal melainkan
tumbuh liar di kawasan hutan. Tanaman ini memiliki daun yang berbulu berbentuk hati dan
ukurannya besar berwarna hijau. Buahnya berbentuk seperti telur dengan ukuran panjang antara
5-6 cm dan lebarnya di atas 5 cm.
2.1.2. Jenis Tanaman Terung Belanda
Terung belanda dapat dibedakan menjadi tiga kategori atas dasar tipe buahnya yaitu:
1. Terung belanda merah
terung belanda merah merupakan buah yang memiliki kulit merah, dan merah gelap disekitar
bijinya. Sisa daging berwarna kuning emas. Mempunyai rasa manis dan bau yang enak terutama
yang berukuran kecil sehingga memungkinkan pemanfaatan sebagai bahan baku untuk sirup, sari
buah, permen.
Jenis ini mempunyai warna kulit kuning emas kemerah-merahan dan tidak ada warna di sekitar
biji sedangkan sisa dagingnya berwarna kuning keemasan. Terung yang kuning emas lebih
manis, tetapi baunya kurang tajam dan mudah rusak bila dibandingkan dengan yang berwarna
merah. Tapi warnanya yang kuning keemasan rasanya lebih manis sangat disukai untuk sari
buah.
3. Terung belanda kuning
Jenis tanaman ini mempunyai warna kulit kuning terang dan daging disekitar biji kuning emas.
Merupakan jenis tanaman terung belanda yang mempunyai buah paling besar dibandingkan
terung merah dan terung keemasan.
(Kumalaningsih, S. 2006)
2.1.3. Klasifikasi Tanaman Terung Belanda
Adapun klasifikasi dari tanaman terung belanda yaitu:
Kingdom : Plantae
Species : Cyphomandra betacea sent (Http://www.plantamor.com)
2.1.4. Manfaat dan Kandungan Gizi Terung Belanda
Buah terung Belanda tekstur dagingnya keras, kulitnya licin dan liat sehingga mudah dikelola.
Selain bisa dikonsumsi dalam bentuk mentah, rasa terung Belanda yang segar juga enak diolah
sebagai campuran sayuran. Buah mentah dapat digunakan untuk masakan acar, kari ataupun
sambal sedangkan buah matang untuk sirup atau rujak. Cocok juga diolah menjadi sirup, selai,
minuman juice atau menjadi bahan campuran salad.
Terung Belanda selain kaya akan air juga mengandung provitamin A yang bagus untuk
Mineral penting seperti potasium, fosfor dan magnesium mampu menjaga dan memelihara
kesehatan tubuh.
Serat yang tinggi didalam terung Belanda bermanfaat untuk mencegah kanker dan sembelit /
konstipasi. Adapun kandungan zat gizi yang terdapat dalam terung belanda adalah sebagai beriku
Table 2.1 Kandungan Gizi Buah Terung Belanda/100 gram
Kandungan Nutrisi Terong Belanda mg/100 g
Dalam setiap 100 gram bagian terung Belanda yang dapat dimakan mengandung air 85 gram, protein 1,5 gram, lemak 0,006 – 1,28 gram, karbohidrat 10 gram, dan
serat 1,4 – 4,2 gram, (
2.2. Vitamin C
2.2.1. Sejarah dan Struktur Kimia Vitamin C
Pada akhir tahun 1930-an penelitian serius telah dimulai pada peran biologis vitamin C.
dan keterlibatan biokimia vitamain C. Keterlibatan ini diakui bahwa vitamin C adalah reduktor
kuat dan keterlibatannya dalam reaksi oksidasi-reduksi. Suatu tema yang penting dalam biokimia
sebelum perang. Tapi yang jelas, kemajuan vitamin C berasal dari studi-studi biosintesis. Pada
awal 1950-an jalur untuk pembentukannya dari gula sederhana yang telah berhasil. (Egan, H,
1981)
Vitamin ini digolongkan sebagai vitamin yang larut dalam air. Susunan kimia vitamin C
ditemukan pada tahun 1933 oleh ilmuwan Inggris dan Swiss. Isolasi vitamin C mula-mula
ditemukan oleh King dari USA dan Szent-gyorgy dari Hungaria. Vitamin ini mempunyai dua
bentuk, yaitu bentuk oksidasi (bentuk dehydro) dan bentuk reduksi. Kedua bentuk ini
mempunyai aktivitas biologi. Dalam makanan bentuk reduksi yang terbanyak. Bentuk dehydro
dapat terus teroksidasi menjadi diketogulonic yang inaktif. Keadaan vitamin C inaktif ini sering
terjadi pada proses pemanasan (bila sayur-sayuran dimasak). Didalam suasana asam vitamin ini
lebih stabil dari pada dalam basa yang menjadi inaktif. Formula vitamin C mirip dengan
glukosa, oleh karena itu para ahli kadang-kadang memasukkan sebagai derivat karbohidarat.
(Prawirokusumo, S, 1987)
Secara sederhana penguraian suatu senyawa atau substrat oleh suatu enzim dapat digambarkan
ES = komplek enzim substrat
P = hasil reaksi
Michaelis dan menten berkesimpulan bahwa kecepatan reaksi tergantung pada konsentrasi
komplek enzim substrat (ES), sebab apabila tergantung pada konsentrasi substrat (S) maka
penambahan konsentrasi substrat akan menghasilkan pertambahan kecepatan reaksi yang apabila
digambarkan akan merupakan garis lurus
Grafik 3 : kinetika enzim terhadap kecepatan reaksi dan konsentrasi
Sehingga secara umum dituliskan sebagai berikut E + S ES E + P
K1, k2, k3 masing-masing adalah tetapan kecepatan reaksi pembentukan kompleks ES adalah
tetapan kecepatan reaksi pembentukan kembali E dan S, Apabila konsentrasi substrat sangat
besar sehingga semua enzim membentuk komplek enzim substrat, maka kecepatan reaksi ialah
maksimal.
2.2.2. Sifat Umum Vitamin C
Sifat vitamin C seperti rasa asam dan pereduksi yang kuat disebabkan adanya struktur
enediol yang berkonyugasi dengan gugus karbonil dalam cincin lakton.
Vitamin C yang mempunyai rumus empiris C6H8O6 dalam bentuk murni merupakan kristal
putih, tidak berwarna, tidak berbau, dan mencair pada suhu 190-1920C.
senyawa ini bersifat reduktor kuat dan mempunyai rasa asam. Vitamin C sangat mudah larut
dalam air, sedikit larut dalam alkohol, dan tidak larut dalam benzene, eter, khlorofrom, minyak
Vitamin C merupakan nutrient organik yang dibutuhkan dalam jumlah kecil untuk
berbagai fungsi kimiawi dan umumnya tidak disintesis oleh tubuh sehingga harus dipasok dari
makanan.
Kadar vitamin C didalam berbagai tumbuhan sangat bervariasi. Dalam suatu buah sumber
sumber vitamin C, kadar vitamin ini lebih banyak terdapat pada bagian kulitnya dibanding
bagian dagingnya, dan bagian buah yang paling sedikit mengandung vitamin C adalah bijinya.
Juga pada buah yang sama jenisnya didapati
pula perbedaan kadar vitamin C karena perbedaan lingkungan tempat tumbuh, pemakaian
berbagai jenis pupuk, tingkat kematangan buah dan lain-lain.
Oleh karena itu perbedaan kadar vitamin C yang terdapat dalam suatu buah harus diperhatikan.
(Kumalaningsih, S. 2006)
2.2.3. Metabolisme Vitamin C
Vitamin merupakan senyawa organik yang diperlukan dalam jumlah kecil untuk reaksi
metabolisme dalam sel dan penting untuk melangsungkan pertumbuhan normal serta memelihara
kesehatan. Kebanyakan vitamin ini tidak disentesis oleh tubuh, namun kecepatan
pembentukannya sangat kecil sehingga jumlah yang terbentuk tidak dapat memenuhi kebutuhan
tubuh. Oleh karena itu tubuh harus memperoleh vitamin dari makanan sehari-hari. (poedjiadi, A.,
1994)
Bila jaringan tubuh ada dalam kondisi jenuh oleh vitamin C maka dari dosis yang
diberikan parenteral, sebagaian besar akan dieksresikan didalam urine, sebaliknya bila suplai
vitamin ini didalam jaringan tidak mencukupi, maka sebagian besar dari dosis vitamin C yang
diberikan akan diretensi didalam tubuh dan sedikit sekali yang dieksresikan di dalam urine,
sebagian kecil di dalam tinja dan sebagian kecil lagi di dalam keringat. (Sediaoetama, A. D.,
2004)
2.2.4. Kegunaan Vitamin C
adalah sejenis protein yang merupakan salah satu komponen utama dari jaringan ikat, tulang
rawan, matriks tulang dan lapisan pembuluh darah lainnya. Vitamin ini bertindak sebagai
koenzim atau kofaktor pada proses hidroksilasi, baik secara aktif sebagai zat reduktor. Vitamin C
sangat esensial dalam proses penyembuhan luka dan kemampuan tubuh untuk mengadapi stress
dan injeksi. ( Tjokonegoro, 1985)
Vitamin C bersifat reduktor, maka digunakan sebagai antioksidan. Disamping sebagai
antioksidan, vitamin C diperlukan untuk kesehatan substansi matriks jaringan ikat, integritas
epitel melalui zat perekat antar sel, pertumbuhan tulang dan gigi, kesehatan epitel pembuluh
darah dan menurunkan kadar kolesterol.
(Hardjasasmita, H. 1991)
Vitamin C juga membantu absorpsi kalsium dengan menjaga agar kalsium berada dalam
bentuk larutan. Didalam industri pangan vitamin C digunakan untuk mencegah proses menjadi
tengik, perubahan warna (browning) pada buah-buahan dan untuk mengawetkan daging. Vitamin
C dikatakan dapat mencegah penyakit kanker kemungkinan karena vitamin C dapat mencegah
pembentukan nitrosamine yang bersifat karsinogenik. Tubuh dapat menyimpan hingga 1500 mg
vitamin C bila dikonsumsi mencapai 100 mg sehari. Jumlah ini dapat mencegah terjadinya
skorbut selama tiga bulan.Tanda dini kekurangan vitamin C dapat diketahui bila kadar vitamin C
darah dibawah 0,20 mg/dl. (Almatsier, S. 2004)
2.3. Faktor-faktor yang menyebabkan hilangnya vitamin C
2.3.1. Pengaruh mikroorganisme
Pada produk buah-buahan dengan keasaman tinggi maka mikroorganisme yang tumbuh
kebanyakan jamur. Mikroorganisme pembusuk dengan mudah menginfeksi produk melalui luka
yang diakibatkan penanganan selama periode pascapanennya. Seperti pada produk yang
mengalami luka maka akan sangat memudahkan mikroorganisme tumbuh pada bagian luka
tersebut. Demikian pula dengan serangga pengganggu seperti lalat buah, peletakan telur lalat
biasanya terjadi saat buah masih berkembang di lapangan. Telur ini baru tumbuh dan
pascapanennya.
Buah dan sayuran mengandung air dalam jumlah yang banyak dan juga nutrisi yang
mana sangat baik bagi pertumbuhan mikroorganisme.. Mikroorganisme pembusuk dapat tumbuh
bila kondisinya memungkinkan seperti adanya pelukaan-pelukaan, kondisi suhu dan kelembaban
yang sesuai dan sebagainya. Adanya mikroorganisme pembusuk pada buah dan sayuran adalah
merupakan faktor pembatas utama di dalam. Pembusukan pada buah-buahan umumnya sebagai
akibat infeksi jamur sedangkan pada sayur-sayuran lebih banyak diakibatkan oleh bakteri. Hal
ini diperkirakan disebabkan oleh pH yang rendah (kurang dari 4.5) atau keasamannya yang
tinggi dibandingkan dengan sayuran yang pH nya rata-rata lebih besar dari 5. (Utama, S. M.
2006)
Bentuk kerusakan vitamin C yang disebabkan mikroorganisme dapat dikenali sebagai berikut :
1. Berjamur
Terdapat dibagian luar permukaan akibat adanya kapang anaerob hasil produksi miselium
dan spora kapang
2. Pembusukan
Rusaknya bahan pangan menjadi lunak dan berair yang disebabkan oleh rusaknya
struktur jaringan tersebut.
3. Perubahan warna
Terjadinya perubahan pigmen dari bahan pangan akibat terbentuknya koloni
mikroorganisme. (Aprianti, D. N. 2009)
2.3.2. Pengaruh aktifitas air
Vitamin C bersifat sangat larut dalam air, akibatnya sangat mudah hilang akibat luka
dipermukaan atau pada waktu pemotongan bahan pangan. Pengaruh aktivitas air terhadap
stabilitas vitamin C juga telah mendapat perhatian para ahli. Beberapa para ahli telah
membuktikan bahwa kecepatan kerusakan vitamin C dalam bahan pangan akan meningkat
dengan meningkatnya aktivitas air.
(Andarwulan, N. 1992)
Kehilangan vitamin C pada pemasakan atau pengolahan sayuran sangat bergantung pada jenis
sayuran dan proses yang digunakan. Seperti halnya vitamin yang larut dalam air. Kehilangan
yang terbesar terjadi pada bleaching dengan air panas karena adanya bleaching vitamin dari
jaringan. Hal yang harus diperhatikan adalah suhu air pembleaching jangan sampai
menyebabkan kenaikan aktivitas enzim. Dalam berbagai jenis sayuran, perlakuan panas pada
waktu memasak sayuran mengakibatkan kerusakan vitamin C yang besarnya lebih dari 50%
selama 1 jam. (Andarwulan, N. 1992)
Vitamin C mempunyai sifat pereduksi yang kuat sehingga mudah rusak. Kehilangan vitamin C
lainnya jika sayuran atau buah-buahan dicelupkan kedalam air mendidih maka vitamin C akan
rusak. ( Anita, F. P. 1973)
2.3.4. Proses pembekuaan
Stabilitas asam askorbat biasanya meningkat dengan penurunan suhu penyimpanan, akan tetapi
selama pembekuan terjadi kerusakan yang cukup besar. Kerusakan ini bervariasi untuk setia
jenis bahan pangan, tetapi suhu penyimpanan dibawah -180C dapat menyebabkan kerusakan
cukup berarti. (Andarwulan, N. 1992)
2.3.5. Pengaruh oksidasi oleh udara
Pada pemotongan dan pengirisan buah atau sayur-sayuran mentah, sebagian sel-selnya rusak
terpotong, sehingga isinya termasuk vitamin C menjadi keluar. Keadaan ini menyebabkan
terbuka pengaruh udara yang mengandung oksigen dan pengaruh sinar matahari yang
mengandung sinar ultraviolet. Mengiris-iris buah atau sayur menjadi potongan yang semakin
halus menyebabkan kerusakan semakin berat bila sesudah dipotong-potong masih dibiarkan saja
beberapa lama sebelum dimasak. Pengirisan buah atau sayur mentah sebaiknya dilakukan segera
sebelum dimasak lebih lanjut
2.3.6. Pengaruh logam-logam berkadar rendah
kerusakan vitamin C dapat dihindari dengan menggunakan alat pemasak berlapis email atau
terbuat dari bahan stainless steel.
2.3.7. Pengaruh cara pengolahan
Semua bahan pangan yang diolah akan mengalami derajat kehilangan vitamin tertentu
(tergantung cara pengolahan). Pada umumnya, diinginkan suatu pengolahan pangan yang dapat
meminimumkan kehilangan zat gizi dan menghasilkan produk yang aman dikonsumsi. Enzim
vitamin C oksidase dapat menyebabkan perombakan oksidatif vitamin C. Didalam buah utuh
sistem enzimnya terkendali hanya bila terjadi perubahan sturktur sel akibat kerusakan mekanis
enzim oksidase menjadi aktif. Selain itu, enzim oksidase vitamin C dengan molekul oksigen
menyebabkan kerusakan vitamin C secara langsung. (Andarwulan, N. 1992)
Enzim vitamin C oksidase adalah enzim yang terdapat dalam sel-sel tanaman yang dapat
menaikkan kecepatan oksidasi. Dalam sel-sel yang utuh enzim tersebut terpisah dari vitamin,
tetapi bila sayuran dan buah-buahan dipotong atau diiris vitamin C akan kontak dengan enzim
dan mengalami kerusakan. Enzim akan terbebaskan ketika sel-sel dipotong. Pada pengirisan dan
pemotongan buah atau sayuran mentah, sebagian sel nya akan rusak terpotong hingga isinya
termasuk vitamin C menjadi keluar. Keadaan ini menyebabkan terbuka pengaruh udara yang
mengandung oksigen dan pengaruh sinar matahari. Mengiris-iris buah atau sayuran menjadi
potongan yang semakin halus menyebabkan kerusakan semakin berat. (Gaman, P. M. 1981)
2.3.8. Pengaruh lama penyimpanan
Secara statistik pengaruh lama penyimpanan terhadap kandungan vitamin C tidak berbeda nyata,
akan tetapi cenderung mengalami penurunan. Hal ini disebabkan karena tertundanya penguapan
air yang menyebabkan struktur sel yang semula utuh menjadi layu. Dimana enzim askorbat
oksidase tidak dibebaskan oleh sel sehingga tidak mampu mengoksidasi vitamin C lebih lanjut
menjadi senyawa yang tidak mempunyai aktivitas vitamin C lagi. Tetapi apabila sel mengalami
kelayuan enzim askorbat oksidase akan dibebaskan dengan cara kontak langsung dengan asam
askorbat sehingga vitamin C mengalami kerusakan.
Penurunan kadar vitamin C paling cepat, hal ini disebabkan pada suhu kamar kondisi lingkungan
berjalan dengan sempurna. Pernyataan ini juga didukung oleh Trenggono dkk. (1990) yang
menyatakan penyimpanan buah-buahan pada kondisi yang menyebabkan kelayuan akan
menurunkan kandungan vitamin C dengan cepat karena adanya proses respirasi dan oksidasi.
(Rachmawati, R. 2009)
2.4. Metode Penentuan Vitamin C
Metode yang dapat digunakan untuk menentukan vitamin C dalam buah-buahan atau suplemen
vitamin antara lain yaitu :
1. Metode spektroskopi
Metode ini berdasarkan pada kemampuan vitamin C yang terlarut dalam air untuk menyerap
sinar ultra violet, dengan panjang gelombang maksimum pada 265 nm. Karena vitamin C dalam
larutan mudah sekali mengalami kerusakan, maka pengukuran dengan cara ini harus dilakukan
secepat mungkin. Untuk memperbaiki hasil pengukuran, sebaiknya ditambahkan senyawa
pereduksi yang lebih kuat disbanding vitamin C. Hasil terbaik diperoleh dengan menambahkan
sejumlah larutan KCN (sebagai stabilizer) kedalam larutan.
2. Metode polarografik
Metode ini berdasarkan pada potensial oksidasi vitamin C dalam larutan asam atau bahan pangan
yang bersifat asam, misalnya ekstrak buah-buahan dan sayuran.
3. Titrasi dengan 2,6 dikhlorofenol indofenol
Metode ini pada saat sekarang paling banyak digunakan untuk menentukan kadar vitamin C
dalam bahan pangan. Disamping mengoksidasi vitamin C, pereaksi indifenol juga mengoksidasi
senyawa-senyawa lain, misalnya senyawa thiosianat,dan senyawa piridinium. Titik akhir dengan
pereaksi indifenol dapat ditentukan secara visual atau menggunakan alat calorimeter.
Titik akhir titirasi pada larutan yang berwarna gelap dapat ditentukan dengan mengekstrak
kelebihan pereaksi setelah oksidasi vitamin berlangsung dengan sempurna.
4. Titrasi dengan iodine
iodine 0,01 N. Metode ini tidak efektif untuk mengukur kandungan asam akorbat dalam bahan
pangan, karena adanya komponen lain selain vitamin yang juga bersifa pereduksi.
Senyawa-senyawa tersebut mempunyai warna titik akhir titrasi yang sama dengan warna titik akhir titrasi
vitamin C dengan iodine (Andarwulan, N. 1992)
5. Titrasi tidak langsung
Larutan standar yang digunakan dalam kebanyakan proses iodometri adalah natrium thiosulfat.
Garam ini biasanya berbentuk pentahidrat Na2S2O3.5H2O. Larutan tidak boleh distandarisasi
dengan penimbangan secara langsung, tapi harus distandarisas. Iod Iodium merupakan oksidator
lemah, sedangkan ion iodida merupakan pereaksi reduksi yang cukup kuat. Suatu kelebihan ion
iodida ditambahkan kepada pereaksi oksidasi yang ditentukan dengan pembebasan iodium yang
kemudian dititrasi dengan larutan natrium thiosulfat. (Day & Underwood, 1981)
Titrasi tidak langsung merupakan titrasi dimana Na2S2O3 sebagai titrant. Analat harus
berbentuk oksidator yang cukup kuat, karena dalam metoda ini analat selalu direduksi dengan KI
sehingga terjadi I2. I2 inilah yang dititrasi dengan N2S2O3. Amilum dengan I2 membentuk
suatu kompleks berwarna biru tua yang masih sangat jelas sekalipun I2 sedikit sekali. Pada titik
akhir yod yang terikat itu pun hilang bereaksi dengan titran sehingga warna biru lenyap
mendadak dan perubahan warnanya tampak sangat jelas. Penambahan amilum ini harus
menunggu sampai mendekati titik akhir titrasi (bila yod sudah tinggal sedikit yang tampak dari
warnanya yang kuning-muda). Maksudnya ialah agar amilum tidak membungkus yod dan
menyebabkan sukar lepas kembali. Hal itu akan berakibat warna biru sulit sekali lenyap sehingga
titik akhir tidak kelihatan tajam lagi. Bila yod masih banyak sekali bahkan dapat menguraikan
amilum dan hasil penguraian ini menggangu perubahan warna pada titik akhir.
Sumber kesalahan titrasi :
Adapun Sumber kesalah yang sering terjadi dalam melakukan titrasi adalah sebagai berikut :
1. Kesalahan oksigen
Oksigen di udara dapat menyebabkan hasil titrasi terlalu tinggi karena dapat mengoksidasi ion
yodida menjadi I2 sebagai berikut :
O2 + 4 I- + 4 H+ 2 I2 + 2 H2O
oleh cahaya dan panas. Kebanyakan titrasi yodometri dilakukan pada pH antara 5 dan 9, maka
kesalahan oksigen menjadi kecil. Namun jangan membiarkan larutan untuk dititrasi tergeletak
terlalu lama, untuk mencegah banyaknya I2 yang menguap.
Pada pH tinggi muncul bahaya lain, yaitu bereaksinya I2 yang terbentuk dengan air (hidrolisa)
yang menyebabkan penggunaan Na2S2O3 menurun.
2. Pemberian amilum terlalu awal
Banyaknya reaksi analat dengan KI yang berjalan lambat, karena itu sering kali harus ditunggu
sebelum dititrasi, sebaliknya menunggu terlalu lama tidak baik karena kemungkinan yod
menguap. (Harjadi, W, 1993)
BAB 3
BAHAN DAN METODE PENELITIAN
3.1. Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian adalah sebagai berikut :
Terung belanda
KI p.a.E.merk
Alat-alat yang digunakan dalam penelititan adalah sebagai berikut :
Pisau
Saringan
Botol aquadest
Spatula
Plastik
Karet
3.3. Prosedur Penelitian
3.3.1. Pembuatan Larutan Pereaksi
1. Pembuatan Larutan Standard Na2S2O3 0,01N
Pembuatan Larutan Standard Na2S2O3 0,01N dari Kristal Na2S2O3.5H2O
Ditimbang 2,482 gram Na2S2O3.5H20 kemudian diencerkan dalam labu takar 2000 ml
sampai garis tanda lalu dihomogenkan
2. Pembuatan larutan Standard CuSO4 1N dari Kristal CuSO4.5 H2O
Ditimbang 1,248 gram CuSO4.5H2O kemudian diencerkan dalam labu takar 100 ml
sampai garis tanda lalu dihomogenkan.
labu takar 1000 ml sampai garis tanda lalu dihomogenkan.
4. Pembuatan KI 10%
Ditimbang 10 gram KI kemudian diencerkan dengan aquadest dalam labu takar 100 ml
sampai garis tanda lalu dihomogenkan.
5. Pembuatan CH3COOH 5%
Ditimbang 5ml CH3COOH kemudian diencerkan dengan aquadest dalam labu takar 100
ml sampai garis tanda lalu dihomogenkan.
6. Pembuatan asam asetat panas 10%
Diukur 10 ml asam asetat kemudian dipanaskan dengan suhu 500C dan diencerkan
dengan aquadest dalam labu takar 100 ml sampai garis tanda lalu dihomogenkan.
7. Pembuatan Amilum 1%
Ditimbang 1 gram tepung amilum lalu dilarutkan dengan aquadest sebanyak 100 ml,
kemudian dipanaskan sampai larutan jernih.
8. Pembuatan asam metapospat (larutan pengekstraksi)
Dilarutkan 15 gram asam pospat kedalam 40 ml asam asetat dan ditambahkan 200 ml air
destilat, kemudian diencerkan hingga 500 ml dan disaring.
9. Pembuatan larutam Merkuri Clorida jenuh
Dilarutkan 7 garm merkuri clorida kedalam 100 ml aquadest sampai diperoleh larutan
jenuhnya.
3.3.2. Prosedur Standarisasi larutan Standard Na2S2O3 0,01 N dengan Larutan Standard
CuSO4 1N
1. Dipipet 0,5 ml CuSO4 1 N
2. Dimasukkan kedalam labu takar 100 ml
3. Diencerkan sampai garis tanda lalu dihomogenkan
4. Dipipet larutan sebanyak 10 ml
5. Dimasukkan kedalam gelas Erlenmeyer
6. Ditambahkan 5 ml CH3COOH 5%
7. Ditambahkan 4 ml KI 10%
9. Dititrasi dengan Na2S2O3 0,01 N sampai terjadi perubahan warna dari kuning
menjadi kuning pucat
10.Ditambahkan 3 tetes indikator amilum
11.Dititrasi kembali dengan Na2S2O3 sampai terjadi perubahan waarna dari biru menjadi
bening
12.Dihitung volume larutan standard Na2S2O3 yang terpakai
13.Diulangi percobaan sebanyak 3 kali
3.3.3. Prosedur Penentuan kadar Vitamin C
3.3.3.1. Persiapan Sampel
Bahan sampel yang digunakan adalah terung belanda yang diolah dengan cara :
1. Untuk terung belanda dengan proses pemblenderan :
Terung belanda yang telah di potong-potong kemudian direndam isinya dengan asam
metapospat. lalu disaring, kemudian residu diblender dengan kecepatan 20000 rpm selama 5
menit,disaring lalu diekstraksi residu dengan aquadest.
2. Untuk terung belanda tanpa pemblenderan :
Terung belanda yang telah di potong-potong kemudian direndam isinya dengan asam
metapospat lalu disaring,dan diekstraksi residu yang diperoleh dengan aquadest.
3. Untuk terung belanda dengan lama penyimpanan yang disimpan dalam suhu kamar :
Terung belanda dibiarkan selama 0, hari kemudian dipotong-potong lalu isinya direndam dengan
asam metapospat,disaring lalu diekstraksi residu yang diperoleh dengan aquadest. Dilakukan hal
3.3.3.2. Penentuan Kadar Vitamin C
1. Ditimbang buah terung belanda sebanyak 50 gram, dipotong- potong lalu direndam isinya
dengan asam metapospat kemudian diblender dengan kecepatan 20000 rpm selama 5
menit
2. Disaring
3. Diekstraksi residu dengan aquadest
4. Disaring sampel, lalu dimasukkan filtrat yang diperoleh sebanyak 10 ml kedalam gelas
beaker
5. Ditambahkan 5 ml larutan merkuri (II) klorida jenuh
6. Diaduk dengan menggunakan batang pengaduk
7. Dicuci batang pengaduk dengan aquadest
8. Didiamkan sampai terbentuk endapan merkuro klorida
9. Disentrifugasi larutan merkuro klorida dengan kecepatan 2500 rpm selama 10 menit
10.Diambil supernatant dengan pipet kemudian dibuang
11.Ditambahkan 20 ml asam asetat panas 10% kedalam tabung sentrifugasi
12.Disentrifugasi kembali larutan dengan kecepatan 2500 rpm selama 10 menit
13.Diambil supernatant yang terbentuk dengan pipet kemudian dibuang
14.Dipindahkan residu dengan aquadest kedalam gelas Erlenmeyer
15.Dilarutkan residu dengan iodine 0,01 N berlebih sampai larut sempurna
16.Ditambahkan KI 10% sebanyak 5 ml
17.Ditutup dengan plastik dan diikat dengan karet
18.Dititrasi dengan larutan standard Na2S2O3 0,01N sampai terjadi perubahan warna dari
kuning menjadi kuning pucat
19.Ditambahkan 3 tetes indikator amilum 1%
20.Dititrasi kembali dengan larutan standard Na2S2O3 0,01N sampai terjadi perubahan
warna dari biru menjadi bening
21.Dicatat volume titrasi larutan standard Na2S2O3 0,01N yang terpakai
22.Diulangi percobaan sebanyak 3 kali
DAFTAR PUSTAKA
Almatsier, S. 2004. Prinsip prinsip Dasar Ilmu Gizi. Cetakan Keempat. Jakarta : Gramedia Pustaka Utama.
Anita, F. P. 1973. Clenical Dietetics And Nutrition. London : Oxford University Press. Andarwulan, N. 1992. Kimia Vitamin. Jakarta : Rajawali. Aprianti, H. D. 2009. Pengawetan Makanan yang Aman. Usu Repository Anonim 2011. http://www. Arienugraha. Word Press. com.
Anonim 2011. http://www. library. usu. ac. id 2009. Anonim 2011. http://www. plantamor. com
Day & Underwood. 1981. Quantitative Analysis. 2nd Edition. California : Berkeley University Press.
Egan, H. Krik. R. S. Sawyer. R. 1981. Pearson’s Chemical Analysis Of Foods. Eight Edition. New York : Butler and Tanner Ltd.
Gaman, P. M. Sherrington. K. B. 1981. Ilmu Pangan. Yogyakarta : Gajah Mada University Press. Hardjasasmita, P. 1991. Ikhtisar Biokimia. Jakarta : Fakultas Kedokteran Universitas Indonesia. Harjadi, W. 1993. Ilmu Kimia Analitik Dasar. Jakarta : Gramedia Pustaka Utama.
Rachmawati, R. 2009. Pengaruh Suhu Dan Lama Penyimpanan Terhadap Kandungan Vitamin C Pada Cabe Rawit (Capsicum frustescens). Bali : Universitas Udayana.
Safaryani, N. 2007. Pengaruh Suhu Dan Lama Penyimpanan Terhadap Penurunan Kadar Vitamin C Brokoli (Brassica oleracea). Fmipa Undip.
Sudarmadji, dkk. 1981. Prosedur Analisa Untuk Bahan Makanan dan Pertanian. Yogyakarta : Liberti.
Prawirokusumo, S. 1987. Biokimia Vitamin. Edisi Pertama. Universitas Yogyakarta : Gajah Mada.
Poedjiadi, A. 1994. Dasar-Dasar Biokimia. Jakarta : UI-press
Sediaoetama, A. D. 2004. Ilmu Gizi Untuk Mahasiswa Dan Profesi Di Indonesia. Jilid I. Cetakan Kelima. Jakarta : Dian Rakyat.