DAYA SERAP PEKTIN DARI KULIT BUAH DURIAN (Durio zibethinus) TERHADAP LOGAM TEMBAGA dan SENG
SKRIPSI
OLEH : M. NASRIL SYAH
NIM 071524039
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2010
▸ Baca selengkapnya: format target kurikulum dan daya serap
(2)DAYA SERAP PEKTIN DARI KULIT BUAH DURIAN (Durio zibethinus) TERHADAP LOGAM TEMBAGA dan SENG
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai Gelar Sarjana Farmasi pada Falkutas Farmasi
Universitas Sumatera Utara
OLEH: M. NASRIL SYAH
NIM 071524039
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
LEMBAR PENGESAHAN SKRIPSI
DAYA SERAP PEKTIN DARI KULIT BUAH DURIAN (Durio zibethinus) TERHADAP LOGAM TEMBAGA dan SENG
OLEH: M. NASRIL SYAH
NIM 071524039
Dipertahan di hadapan Panitia Penguji
Falkutas Farmasi
(Prof. Dr. Jansen Silalahi., M.App.Sc, Apt.)
NIP 195006071979031001 (Drs. Muchlisyam, M.Si., Apt.)
Universitas Sumatera Utara
Dekan,
(Prof. Dr. Sumadio Hadisahputra, Apt.)
NIP 195311281983031002
KATA PENGANTAR
Puji syukur kehadirat Allah Subhana wata’ala yang telah memberi rahmat dan
karuniya-Nya, sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi
ini. Terimakasih dan rasa hormat yang besar kepada Ayahanda Mohd. Nazir Adam
dan Ibunda Tjut Usmawati serta seluruh keluarga besar yang selalu mendukung,
memberi semangat dan do’a kepada penulis untuk menyelesaikan studi serta
kesuksesan penulis.
Penulis juga mengucapka terimakasih sebesar-besarnya kepada:
1. Ibu Prof. Dr. Siti Morin Sinaga., M.Sc.Apt dan Bapak Prof. Dr. Jensen
Silalahi., M.App.Sc.Apt yang telah membimbing penulis dengan penuh
kesabaran dan tanggung jawab selama penelitian hingga selesainya
penyusunan skripsi ini.
2. Bapak Dekan dan para pembantu Dekan Falkutas Farmasi Universitas
Sumatera Utara, yang telah memberikan fasilitas kepada penulis sehingga
dapat menyelesaikan pendidikan.
3. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, SU., Apt., Bapak Drs.
Muchlisyam, M.Si., Apt dan Ibu Dra. Saleha Salbi, M.Si., Apt selaku dosen
penguji yang telah memberikan masukan dalam penyusunan skripsi ini.
4. Bapak dan Ibu pengajar Falkutas Farmasi USU yang telah mendidik penulis
hingga menyelesaikan pendidikan.
5. Bapak kepala Laboratorium Kimia Bahan Makanan beserta staf yang telah
6. Teman-teman mahasiswa/i Falkutas Farmasi USU khususnya ekstensi 2007
yang telah memberikan bantuan dan dorongan kepada penulis selama
perkuliahan maupun pendidikan hingga selesainya pendidikan.
Semoga Allah subhana wata’ala melindungi dan melimpahkan rahmat dan
karunia-Nya kepada kita semua. Penulis berharap semoga skripsi ini menjadi
sumbangan yang berarti bagi ilmu pengetahuan khususnya dibidang Farmasi.
Medan, Oktober 2010
Penulis
(M. Nasril Syah)
Daya Serap Pektin dari Kulit Buah Durian (Durio zibethinus)
Terhadap Logam Tembaga Dan Seng
Abstrak
Kulit durian merupakan limbah yang dianggap tidak memiliki nilai
ekonomis, namun kulit durian mengandung pektin yang memiliki daya serap
terhadap logam berat seperti tembaga dan seng. Tujuan penelitian ini adalah untuk
mengetahui daya serap pektin kulit buah durian terhadap logam tembaga dan seng.
Kulit durian yang digunakan merupakan limbah dari penjual buah durian di
Jl. Iskandar Muda Medan dan diekstraksi dengan pemanasan selama 4 jam pada
suhu 90°C dengan penambahan asam klorida hingga pH 2 dan diendapkan dengan
menggunakan etanol asam. Pektin yang diperoleh dilakukan pengujian terhadap
kemampuan penyerapan logam berat tembaga dan seng yang diukur menggunakan
spektrofotometri serapan atom.
Dari hasil penelitian diperoleh kandungan pektin dalam kulit buah durian
sebesar 2,56% dan menunjukan daya serap 1% pektin terhadap logam tembaga dan
logam seng sebesar 48,38±0,62% dan 7,79±1,37%.
Kata Kunci: Kulit Durian, Pektin, Daya Serap, Tembaga Dan Seng, Spektrofotometer
Absorption Pectin from Durian Peel (Durio zibethinus)
On Copper and Zinc Metal
Abstract
Durian peel is a side product that is considered not to have economic value,
but it contains pectin which has the absorption ability for heavy metals such as copper
and zinc. The purpose of this study was to determine the absorption ability of durian
peel pectin on copper and zinc metal.
Durian peel used is a waste of durian fruit seller on Jl. Iskandar Muda Medan
and pectin was extracted by heating for four hours at a temperature of 90°C under
condition of hydrochloric acid until pH 2 and precipitated using acidic ethanol.
Absorption ability of pectin obtained was done by having heavy metals copper and
zinc measured using atomic absorption spectrophotometry.
From the research obtained pectin content in the durian peel was 2,56% and
showed 1% pectin absorbtion of copper metal and zinc metal was 48,38±0,62% and
7,79±1,37%.
Keywords: Durian Peel, Pectin, Absoptions Ability, Copper And Zinc Metal, Atomic
Absorption Spectrophotometer.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... iv
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
BAB I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II. TINJAUAN PUSTAKA ... 4
2.1 Durian ... ... 4
2.2 Pektin ... ... 4
2.2.1 Sifat Pektin ... 5
2.2.2 Ekstraksi Pektin ... 6
2.3 Mekanisme Penyerapan Logam Oleh Pektin ... 8
2.4 Logam Berat ... 9
2.4.1 Tembaga ... 9
2.4.2 Seng ... ... 10
2.5 Keracunan Logam ... ... 11
2.6 Penetapan Kadar Logam Tembaga dan Seng ... 13
BAB III. METODOLOGI PENELITIAN... 14
3.1 Alat ... . 14
3.2 Bahan ... 14
3.3 Prosedur ... 14
3.3.1 Pembuatan Pereaksi ... . 14
3.3.1.1 Pembuatan Larutan Asam Klorida... 14
3.3.1.2 Pembuatan Larutan Alkohol Asam ... 15
3.3.2 Persiapan Sampel ... 15
3.3.3 Ekstraksi Pektin ... . 15
3.3.4 Identifikasi Pektin ... 16
3.3.5 Pembuatan Kurva Kalibrasi ... ... 16
3.3.5.1 Pembuatan Kurva Kalibrasi Larutan Baku Tembaga .... 16
3.3.5.2 Pembuatan Kurva Kalibrasi Larutan Baku Seng ... 16
3.3.6 Pengujian Penyerapan Logam ... . 17
3.4 Rata-rata Persentasi Tembaga dan Seng ... 17
BAB IV HASIL DAN PEMBAHASAN... 18
4.1 Ekstraksi Pektin ... . 18
4.2 Kurva Kalibrasi Tembaga dan Seng ... . 19
4.3 Uji Kemampuan Serap Logam ... 20
BAB V KESIMPULAN DAN SARAN ... .. 23
5.1 Kesimpulan ... 23
5.2 Saran ... 23
DAFTAR PUSTAKA ... 24
DAFTAR TABEL
Tabel 1. Daya Serap Pektin Terhadap Logam ……… 21
Tabel 2. Data Kalibrasi Tembaga ………... 27
Tabel 3. Data Kalibrasi Seng ………...…………. 27
Tabel 4. Daya Serap Pektin Terhadap Logam Tembaga……….…… 32
Tabel 5. Daya Serap Pektin Terhadap Logam Seng ………... 35
DAFTAR GAMBAR
Gambar 1. Kurva kalibrasi larutan standar Tembaga ……… 19
Gambar 2. Kurva kalibrasi larutan standar Seng ………... 20
Gambar 3. Buah Durian ………. 40
Gambar 4. Kulit Buah Durian ………...…… 40
Gambar 5. Potongan kulit dalam Durian ……….... 40
Gambar 6. Pektin Kering ……….... 41
Gambar 7. Serbuk Pektin ……… 41
DAFTAR LAMPIRAN
Lampiran 1. Flowshet ekstraksi pektin ……… 26
Lampiran 2. Data kalibrasi Tembaga dan Seng Menggunakan
Spektrofotometer Serapan Atom ……… 27
Lampiran 3. Perhitungan Persamaan Garis Regresi
dan Koefisien Korelasi (r) dari Data Kalibrasi Tembaga …… 28
Lampiran 4. Perhitungan Persamaan Garis Regresi
dan Koefisien Korelasi (r) dari Data Kalibrasi Seng .………. 29
Lampiran 5. Perhitungan Konsentrasi Tembaga dalam Larutan Logam….. 30
Lampiran 6. Perhitungan Pengurangan Konsentrasi Logam Tembaga….... 32
Lampiran 7. Perhitungan Konsentrasi Seng dalam Larutan Logam …….... 33
Lampiran 8. Perhitungan Pengurangan Konsentrasi Logam Seng ……….. 35
Lampiran 9. Perhitungan Statistik Persentase Tembaga dan Seng ……….. 36
Lampiran 10. Gambar Sampel ……….. 40
Lampiran 11. Gambar Pektin ……… 41
Lampiran 12. Gambar Alat Spektrofotometri Serapan Atom ……… 42
Daya Serap Pektin dari Kulit Buah Durian (Durio zibethinus)
Terhadap Logam Tembaga Dan Seng
Abstrak
Kulit durian merupakan limbah yang dianggap tidak memiliki nilai
ekonomis, namun kulit durian mengandung pektin yang memiliki daya serap
terhadap logam berat seperti tembaga dan seng. Tujuan penelitian ini adalah untuk
mengetahui daya serap pektin kulit buah durian terhadap logam tembaga dan seng.
Kulit durian yang digunakan merupakan limbah dari penjual buah durian di
Jl. Iskandar Muda Medan dan diekstraksi dengan pemanasan selama 4 jam pada
suhu 90°C dengan penambahan asam klorida hingga pH 2 dan diendapkan dengan
menggunakan etanol asam. Pektin yang diperoleh dilakukan pengujian terhadap
kemampuan penyerapan logam berat tembaga dan seng yang diukur menggunakan
spektrofotometri serapan atom.
Dari hasil penelitian diperoleh kandungan pektin dalam kulit buah durian
sebesar 2,56% dan menunjukan daya serap 1% pektin terhadap logam tembaga dan
logam seng sebesar 48,38±0,62% dan 7,79±1,37%.
Kata Kunci: Kulit Durian, Pektin, Daya Serap, Tembaga Dan Seng, Spektrofotometer
Absorption Pectin from Durian Peel (Durio zibethinus)
On Copper and Zinc Metal
Abstract
Durian peel is a side product that is considered not to have economic value,
but it contains pectin which has the absorption ability for heavy metals such as copper
and zinc. The purpose of this study was to determine the absorption ability of durian
peel pectin on copper and zinc metal.
Durian peel used is a waste of durian fruit seller on Jl. Iskandar Muda Medan
and pectin was extracted by heating for four hours at a temperature of 90°C under
condition of hydrochloric acid until pH 2 and precipitated using acidic ethanol.
Absorption ability of pectin obtained was done by having heavy metals copper and
zinc measured using atomic absorption spectrophotometry.
From the research obtained pectin content in the durian peel was 2,56% and
showed 1% pectin absorbtion of copper metal and zinc metal was 48,38±0,62% and
7,79±1,37%.
Keywords: Durian Peel, Pectin, Absoptions Ability, Copper And Zinc Metal, Atomic
Absorption Spectrophotometer.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Pencemaran logam berat dalam lingkungan merupakan suatu proses yang
erat hubungannya dengan penggunaan logam tersebut oleh manusia sendiri. Seperti
penggunaan logam berat dalam bentuk garam untuk industri yang menjadi salah satu
faktor utama dari pencemaran logam berat dalam lingkungan dari limbah industri
tersebut, sehingga logam-logam yang relatif mudah menguap dan larut dalam air akan
diikuti oleh peningkatan kadar logam berat dalam organisme air seperti ikan, kerang
dan biota lainnya, sehingga pemanfaatan organisme ini sebagai bahan makanan dapat
membahayakan kesehatan. Adapun logam yang dapat menyebabkan keracunan adalah
jenis logam berat saja, logam ini termasuk logam esensial seperti tembaga dan seng,
kedua logam ini dibutuhkan oleh tubuh dalam jumlah yang relatif kecil di dalam
beberapa proses metabolisme dalam tubuh (Darmono, 1995).
Berbagai usaha dilakukan untuk menetralisir pencemaran lingkungan akibat
dari logam berat, seperti pemanfaatan berbagai produk biomaterial sebagai penyerap
logam. Pemanfaatan dari bahan biomaterial ini merupakan alternatif yang dapat
dipilih karena memiliki biaya yang minimal dalam proses produksinya. Salah satu
biomaterial yang dapat dimanfaatkan sebagai penyerap logam adalah pektin. Gugus
karboksilat dari pektin inilah yang dapat mengikat logam membentuk senyawa
kompleks yang tidak larut dalam air (Kupchik, et al., 2005).
Durian (Durio zibhetinus) merupakan buah yang memiliki aroma yang
sangat khas, buah ini juga merupakan buah yang banyak diminati masyarakat karena
rasa enak dan aromanya yang harum. Pada saat musim buah durian, maka masalah
memiliki nilai ekonomis. Hal ini terjadi karena orang-orang mengetahui hanya bagian
dari buah saja yang memiliki nilai ekonomis sedangkan kulit buah tidak memiliki
nilai ekonomis. Kulit durian dapat dimanfaatkan sebagai sumber pektin, yaitu pada
bagian kulit dalam durian yang berwarna putih yang disebut juga dengan mesocarp
(Anonim, 2010).
Pektin memiliki daya serap terhadap logam berat seperti tembaga dan seng.
Pektin dapat diekstraksi dengan pemanasan selama 4 jam pada suhu 90°C dengan
penambahan asam klorida hingga pH 2. Filtrat yang diperoleh diendapkan dengan
menggunakan etanol asam (HCl 4% dalam etanol 95%) dan kemudian dicuci
beberapa kali menggunakan etanol 95% (Wong, et al., 2008).
Tujuan penelitian untuk mengetahui daya serap terhadap logam berat
tembaga dan seng menggunakan pektin dari kulit durian. Penetapan kadar tembaga
dan seng dapat dilakukan dengan titrasi pengendapan dan spektrofotometri (Rohman
dan Gandjar, 2007). Pada penelitian ini dilakukan penetapan kadar tembaga dan seng
dengan menggunakan spektrofotometri serapan atom, karena metode ini adalah salah
satu metode yang mudah, cepat, teliti dan tidak memerlukan pemisahan (Khopkar,
1990).
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut :
a. Berapakah kandungan pektin dalam kulit buah durian.
b. Apakah pektin kulit buah durian memiliki daya serap terhadap logam tembaga
dan seng.
1.3 Hipotesis
a. Kulit buah durian memiliki kandungan pektin lebih besar dari 1%.
b. Pektin kulit durian memiliki daya serap terhadap logam tembaga dan seng.
1.4 Tujuan Penelitian
a. Untuk mengetahui kandungan pektin pada kulit bagian dalam buah durian.
b. Untuk mengetahui berapa besar daya serap pektin kulit buah durian terhadap
logam tembaga dan seng.
1.5 Manfaat Penelitian
a. Untuk memberikan informasi kepada masyarakat tentang nilai ekonomi
limbah kulit durian sebagai sumber pektin.
b. Alternatif penyerap logam berat terhadap pencemaran lingkungan dan
BAB II
TINJAUAN PUSTAKA
2.1Durian
Durian adalah nama
sekaligus nama buahnya yang bisa dimakan. Nama ini diambil dari ciri khas kulit
buahnya yang keras dan berlekuk-lekuk tajam sehingga menyerupai
namanya yang juga populer adalah duren. Adapun klasifikasi ilmiah dari durian
adalah sebagai berikut :
Kingdom : Plantae
Class : Agnoliophyta
Ordo : Magnoliopsida
Family : Bombacea
Genus : Durio
Species : Durio zibethinus
tumbuhan dari
biasa (tanpa imbuhan apa-apa) adalah yang memilik
(Anonim, 2009).
2.2 Pektin
Pektin merupakan produk karbohidrat yang dimurnikan dan diperoleh dari
ekstrak asam encer dari bagian dalam kulit buah jeruk sitrus atau apel, terutama terdiri
dari asam poligalakturonat yang termetoksilasi sebahagian. Berbentuk serbuk kasar
atau halus, berwarna putih kekuningan, hampir tidak berbau dan memiliki rasa seperti
musilago. Hampir larut sempurna dalam 20 bagian air, membentuk cairan kental,
O
praktis tidak larut dalam etanol atau pelarut organik lainnya (Ditjen POM, 1995).
Pektin memiliki struktur molekul sebagai berikut (Lihat Gambar 1).
Gambar 1. Rumus Bangun Pektin
Pektin merupakan polisakarida diperoleh dari buah-buahan dan biasanya
digunakan dalam pembuatan jeli dan sebagai bahan tambahan untuk pengental dalam
makanan. Pektin ialah polimer linier dari asam D-galakturonat yang berikatan dengan
ikatan 1,4-α-glikosidik. Asam D-galakturonat memiliki sturktur yang sama seperti
struktur D-galaktosa, perbedaannya terletak pada gugus alkohol primer C6 yang
memiliki gugus karboksilat (Hart, et al., 2003). Sebagian gugus karboksilat pada
polimer pektin mengalami esterifikasi dengan metil menjadi gugus metoksil dan
biasanya mengandung sekitar 8,0-11,0% gugus metoksil (Ranganna, 2000).
2.2.1 Sifat Pektin
Ditinjau dari sifat fisika pektin dapat bersifat koloid reversibel, yaitu dapat
dilarutkan dalam air, diendapkan, dikeringkan dan dilarutkan kembali tanpa
perubahan sifat fisiknya. Pada penambahan air pada pektin kering akan terbentuk
gumpalan seperti pasta yang kemudian menjadi larutan. Proses tersebut dapat
dipercepat dengan ekstraksi dan penambahan gula. Larutan pektin yang berupa larutan
koloid bereaksi asam terhadap lakmus, tidak larut dalam alkohol dan dalam pelarut
organik lainnya seperi metanol, aseton, atau propanol. Kelarutan pektin akan
meningkat dengan derajat esterifikasi dan turunnya berat molekul. Semakin mudah
pektin larut dalam air maka akan semakin mudah untuk mengendapkannya dengan
Pemanasan dengan asam akan menyebabkan hidrolisis gugus ester metil, seperti
halnya hidrolisa ikatan glikosida yang akhirnya menjadi asam galakturonat (Cruess,
1988).
Berat molekul rata-rata preparat pektin sangat bervariasi, berkisar antara
30.000 hingga 300.000, tergantung pada sumber, metode pembuatan dan metode
pengukuran. Sedangkan viskositas larutan pektin bergantung pada berat molekul,
derajat esterifikasi, pH, temperatur dan konsentrasi elektrolit. Peningkatan konsentrasi
elektrolit akan menyebabkan menurunnya viskositas (Kirk dan Othmer, 1967).
2.2.2 Ekstraksi Pektin
Ekstraksi pektin dapat dilakukan secara biokimia dan kimia. Secara kimia
pektin dapat diekstraksi dari jaringan tanaman dengan pemanasan dalam asam encer
sedangkan ekstraksi secara biokimia dengan menggunakan enzim, dimana
enzim-enzim ini berperan pada degradasi hidrolitik dari subtansi pektin yang terdiri dari
pektin metilesterase dan pektin poligalakturonase (Kirk dan Othmar, 1967).
Ekstraksi pektin secara kimia dapat dilakukan dengan cara mengekstraksi
dari berbagai kulit buah-buahan segar dengan pemanasan pada suhu 90-95°C selama
satu jam dalam asam encer pada pH 4,5 menggunakan asam yang sesuai seperti asam
klorida. Pektin dalam filtrat diendapkan dengan menggunakan etanol 96% (Ranganna,
2000).
Lamanya waktu ekstraksi yang dilakukan mempengaruhi berat pektin yang
didapat, semakin lama waktu ekstraksi yang dilakukan maka semakin besar pula berat
pektin yang diperoleh dan kenaikan berat pektin sejalan dengan peningkatan suhu
pada proses ekstraksi dilakukan. Pencucian pektin dengan alkohol menghasilkan
jumlah pektin yang tidak terlalu jauh dengan pencucian tanpa menggunakan alkohol,
namun pektin yang dihasilkan memberikan warna yang lebih baik yaitu putih
kekuningan (Akhmalludin dan Kurniawan, 2005).
Pektin yang lebih mudah larut dalam air dapat diperoleh dengan
memodifikasi pH dan suhu pada metode ekstraksi. Pektin yang diperoleh dengan cara
ini memiliki rantai lebih pendek dan tidak bercabang sehingga akan lebih mudah larut
dibandingkan pektin yang memiliki rantai yang lebih panjang (Wong, et al., 2008).
2.2.3 Penggunaan Pektin
Pektin digunakan dalam bidang industri makanan dan dalam bidang farmasi.
Dalam bidang makanan pektin digunakan sebagai bahan pembentuk gel untuk
pembuatan jam dan jelly. Dimana kemampuan pektin membentuk gel tergantung pada
kandungan gugus metoksilnya. Kemampuan pektin untuk dapat membentuk gel
merupakan sifat yang unik dari pektin. Penggunaan pektin selain dari pembentuk gel
pektin juga digunakan dalam produk buah-buahan kemasan, juice dan es krim sebagai
penstabil (Cruess, 1988).
Penggunaan pektin dalam bidang farmasi digunakan untuk diare, dimana
pektin bekerja sebagai adsorbent dalam usus dan juga digunakan untuk obat luka
sebagai hemostatik agent. Selain itu pektin digunakan sebagai anti koagulan yang
memiliki efek heparin dan juga dapat digunakan untuk menurunkan kolesterol darah
pada diet kolesterol. Juga telah dilakukan penelitian penggunaan pektin juga dapat
digunakan sebagai antidotum yang efektif terhadap keracunan logam berat, melalui
pembentukan garam-garam yang tidak larut (Kirk dan Othmer, 1967).
2.3 Mekanisme Penyerapan Logam Berat oleh Pektin
Gugus karboksilat dari pektin dapat bereaksi dengan ion logam berat untuk
melalui feses. Reaktivitas pektin terhadap ion logam berat sangat tergantung pada
derajat esterifikasinya (Kupchik, et al., 2005).
Didalam larutan, pektin berkumpul membentuk kantung-kantung dimana kantung ini
dapat membentuk komplek dengan kation logam. Setiap kantung tersebut bermuatan
negatif sehingga memiliki daya tarik yang kuat terhadap muatan positif dari kation
logam. Namun, pada logam yang beracun, terutama raksa, kadmium, dan logam
radioaktif memiliki afinitas yang lebih tinggi dibandingkan dengan logam esensial.
Setelah logam terikat pada serat pektin maka dengan mudah dapat diekskresikan dari
tubuh melalui feses (Eliaz, et al., 2007).
2.4 Daya Serap Pektin
Pektin terdapat diseluruh jaringan tumbuhan terutama pada buah, pektin
memiliki kemampuan sebagai antidotum untuk pertama kali ditemukan pada tahun
1951, dan pada tahun 1952 dibuktikan secara in vivo terhadap penyerapan strontium
dalam jaringan gastroinstestinal. Strontium 0,1% yang terdapat dalam darah setelah
diberikan pektin dalam waktu 24 jam kandungan strontium dalam darah berkurang.
Pengikatan logam oleh pektin karena adanya gugus-gugus yang memiliki pasangan
elektron bebas terhadap kation logam seperti gugus karboksilat dan hidroksi yang
terdapat pada polimer pektin, sehingga kation logam dapat tertarik dan berikatan
membentuk kompleks pektin dan logam. (Endress, 1991).
Daya serap pektin dapat ditingkatkan dengan memodifikasi pektin, seperti
yang telah dilakukan Wong, at al (2008) yang memodifikasi pektin dari kulit buah
durian dan kulit buah jeruk membentuk rantai yang lebih pendek dan lebih larut.
Urutan efektifitas penyerapan logam dari pektin kulit durian adalah Cu > Pb > Ni >
Cd > Zn. Kelarutan pektin akan meningkat dengan derajat esterifikasi dan turunnya
berat molekul dan semakin mudah pektin larut dalam air maka akan semakin mudah
untuk mengendapkannya dengan suatu elektrolit. Sedangkan yang dilakukan
Kupchik, et al (2005) pada pectin dari kulit buah jeruk pomace yang ditujukan untuk
penggunaan antidotum dilakukan modifikasi dengan mengurangi gugus metoksil dari
pektin, sehingga jumlah gugus karboksilat yang mengikat logam menjadi lebih besar
dibandingkan dengan jumlah logam yang terikat pada pektin yang tidak dimofikasi
(Cruess, 1988).
2.5 Logam Berat
Logam berat memiliki respon biokimia spesifik terhadap organisme hidup
yang dibagi dalam 3 kelompok, yaitu: logam-logam yang mudah mengalami reaksi
dengan unsur oksigen, logam yang mudah bereaksi dengan unsur nitrogen dan atau
sulfur dan logam transisi yang memiliki sifat khusus sebagai logam pengganti untuk
logam atau ion logam dari kelas A atau logam dari kelas B. Logam dapat
dikelompokan menjadi logam berat (berat jenis > 5) dan logam ringan (berat jenis <
5), logam esensial dan tidak esensial, dan logam yang terdapat dalam jumlah yang
sangat kecil dalam kerak bumi (≤ 1000 ppm) (Palar, 2008; Soemirat, 2003).
Logam berasal dari kerak bumi yang berupa bahan murni. Secara alami
siklus perputaran logam adalah dari kerak bumi yang kemudian ke lapisan tanah,
kemudian ke mahkluk hidup (tanaman, hewan dan manusia) lalu kedalam air,
mengendap dan akhirnya kembali ke kerak bumi. Adapun logam yang dapat
menyebabkan keracunan adalah jenis logam berat saja. Logam ini termasuk logam
esensial seperti Cu dan Zn (Darmono, 1995).
2.4.1 Tembaga
Tembaga (Cu) merupakan logam yang berwarna merah muda yang lunak,
dapat ditempa dan liat. Memiliki titik lebur 1038°C, tidak larut dalam asam klorida
diidentifikasi dengan beberapa reaksi pengendapan, uji katalitik dengan thiosulfat dan
uji kering (uji nyala) menghasilkan nyala hijau dengan pembasahan asam klorida
pekat sebelum pemanasan (Vogel, 1989).
Unsur tembaga di alam ditemukan dalam bentuk logam bebas, namun lebih
banyak ditemukan dalam bentuk persenyawaan ion seperti CuCO3+, CuOH+ dan lain
sebagainya. Unsur tembaga juga terdapat dalam bentuk mineral yang teradapat pada
tanah dan batuan seperti kalkosit (Cu2S), kalkopirit (CuFeS2) dan bornit (Cu5FeS4).
Secara alamiah unsur tembaga dapat masuk ke dalam tatanan lingkungan sebagai
akibat dari peristiwa alam seperti erosi dari batuan mineral. Masuknya unsur tembaga
ke dalam tatanan lingkungan secara tidak alamiah akibat dari aktivitas manusia seperti
limbah dari industri yang menggunakan unsur tembaga dalam proses produksinya
(Palar, 2008).
2.4.2 Seng
Seng (Zn) merupakan logam yang berwana putih kebiruan, memiliki titik
lebur 410°C dan mendidih pada 906°C, sangat mudah larut dalam asam klorida encer
dan asam sulfat encer. Seng dapat diidentifikasi dengan beberapa reaksi pengendapan,
uji ditizon membentuk senyawa kompleks berwarna merah yang dapat diekstraksi
dengan tetraklorida (Vogel, 1989).
Seng di alam tidak berada dalam keadaan bebas, namun dalam bentuk terikat
dengan unsur lainnya berupa mineral seperti kalamin, franklinit, smithsonit, willemit
dan zinkit. Seperti halnya unsur tembaga, seng memasuki tatanan lingkungan secara
alamiah melalui proses erosi dan secara tidak alamiah terjadi oleh faktor limbah
industri (Widowati, dkk., 2008).
2.5 Keracunan Logam
Kejadian keracunan logam paling sering disebabkan pengaruh pencemaran
lingkungan dari logam berat, seperti penggunaan logam untuk pembasmi hama
(peptisida), pemupukan atau limbah buangan pabrik yang menggunakan logam.
Logam tembaga dan seng termasuk logam esensial yang dalam dosis tertentu
dibutuhkan sebagai unsur nutrisi pada hewan, namun bila kadar logam ini melebihi
jumlah dosis tertentu akan menyebabkan keracunan (Darmono, 1995).
Sumber keracunan logam juga dapat terjadi akibat dari penggunaan bahan–
bahan rumah tangga, seperti penggunaan alat masak dan wadah penyimpanan
makanan atau minuman. Logam yang terlarut dari alat masak atau wadah tempat
penyimpanan makanan atau minuman dapat melarutkan logam, umumnya karena
makanan tersebut bersifat asam, seperti logam kadmium, tembaga dan seng. Makanan
yang bersifat basa juga dapat melarutkan logam, antara lain alumunium atau seng
(Sartono, 2002).
Logam dapat memasuki tubuh secara inhalasi ataupun oral. Absorbsi secara
inhalasi dapat terjadi bila ukuran logam cukup halus antara 2-5 μ. Efek yang terjadi
tergantung pada jumlah, tempat absorbsi dan sifat kimia fisis logam. Logam yang
masuk secara oral dapat diabsorbsi melalui saluran pencernaan, akan berdifusi pasif
dan ditranspor ke organ target ataupun bereaksi sehingga terjadi berbagai transformasi
senyawa logam sehingga efeknya menjadi beragam (Soemirat, 2003).
Toksisitas logam dapat bersifat kronis dan akut, sangat bergantung pada
berbagai faktor. Adapun yang mempengaruhi toksisitas logam yang akut tergantung
pada dosis tinggi sekaligus dalam waktu pendek maka biasanya berefek akut dan
parah, waktu pemaparan yang pendek namun massif, dan tergantung pada penyerapan
dengan cepat. Toksisitas kronis tergantung pada dosis yang tidak tinggi, tetapi
paparan yang menahun, gejala yang tidak mendadak dan terpapar pada seluruh bagian
organ (Soemirat, 2003).
Logam tembaga diketahui sebagai mineral esensial sejak tahun 1924 pada
waktu dilakukan penelitian pada tikus. Kegunaan tembaga sebagai logam esensial
yaitu sebagai pembentukan hemoglobin, pembebasan Fe dari sel ke plasma, berperan
dalam metabolisme oksigen dan berperan dalam pigmentasi pada rambut. Namun
kelebihan logam tembaga dapat menyebabkan keracunan. Keracunan logam tembaga
dapat menyebabkan keracunan yang kronis. Keracunan yang diakibatkan dari logam
tembaga adalah mual, muntah, diare, sakit perut hebat, hemolisis darah,
hemoglobinuria, nefrosis, kejang hingga menyebabkan kematian (Darmono, 1995).
Senyawa garam seng yang larut dalam air, biasanya digunakan pada
generator asap dan pengelasan, keracunan biasanya terjadi karena menghirup uap
seng tersebut, selain itu keracunan juga terjadi dari pemotongan logam, dan
melelehkan logam campuran seng. Akibat keracunan logam seng terutama iritasi
saluran pernafasan yang dapat menyebabkan edema paru dan kerusakan saluran nafas.
Batas paparan uap seng adalah 5 mg/meter3, dan batasan paparan uap seng klorida 1
mg/meter3 (Sartono, 2002). Namun logam seng juga merupakan logam esensial,
karena seng merupakan logam yang terbanyak yang berkaitan dengan enzim dimana
sekitar 200 jenis enzim mengandung seng (Darmono, 1995).
2.6 Penentuan Kadar Logam Tembaga dan Seng
Penentuan kadar logam tembaga dan seng dapat dilakukan dengan metode
titrasi kompleksometri menggunakan reaksi zat-zat pengkompleks organik dengan ion
logam. Zat pengkompleks yang paling sering digunakan adalah asam etilen diamina
tetra asetat (EDTA) yang membentuk senyawa kompleks yang stabil terhadap logam,
termasuk logam tembaga dan seng, kemudian dititrasi langsung dengan EDTA dalam
suasana asam dan ditentukan titik akhir titrasi menggunakan indikator jingga xylenol
atau dapat dititrasi dengan penambahan larutan penyangga menggunakan indikator
4-(2-piridilazo) resorsinol. Logam tembaga dan seng juga dapat dititrasi pada suasana
basa menggunakan indikator Murexide (Sukardjo, 1990).
Penentapan kadar logam tembaga dan seng juga dapat dilakukan dengan cara
metode ekstraksi yang terdiri dari tahap pengkhelatan dengan ammonium pyrolidin
dithiocarbamate (APDC) dan dilakukan ekstraksi dalam methyl isobutyl keton
(MIBK) dan dilakukan pengukuran pada panjang gelombang 324,7 nm dan 213,9 nm
untuk analisis logam tembaga dan seng dengan tipe nyala udara asitilen (2200°C)
menggunakan spektrofotometer serapan atom. Metode ini dilakukan untuk penetapan
kadar logam yang sangat kecil (Sofyan, 2010). Menurut Sony (2009) penetapan kadar
logam dapat dilakukan dengan tahap destruksi sampel terlebih dahulu yang kemudian
dapat dilarutkan dengan menggunakan pelarut yang sesuai seperti asam nitrat yang
kemudian dapat dilanjutkan dengan pengukuran menggunakan spektrofotometri
BAB III
METODOLOGI PENELITIAN
Penelitian ini dilakukan di Laboratorium Kimia Bahan Makanan Fakultas
Farmasi USU dan Laboratorium Penelitian Pabrik Kelapa Sawit RISPA Medan.
3.1 Alat-alat
Alat-alat yang digunakan antara lain: Spektrofotometri Serapan Atom (GBC
Avanta ∑) (Gambar dapat dilihat pada lampiran 11 gambar 8), lemari asam, alas
pemanas, pengaduk magnetik, Neraca listrik (AND GF-200), pisau dapur, blander,
lemari pengering, termometer 100°C, spatula, kertas saring Whatman no.42,
sentrifugasi dan alat – alat gelas.
3.2 Bahan-bahan
Kulit buah durian, akuades, larutan CuSO4 10 mmol/L, larutan ZnSO4 10
mmol/L, HCl 1N, HCl 3N, HCl 4%, NaOH 2N, Etanol 95%, larutan standar tembaga
(Cu) 1000 ppm dan larutan standar seng (Zn) 1000 ppm.
3.3 Prosedur
3.3.1 Pembuatan Pereaksi
3.3.1.1 Pembuatan Larutan Asam Klorida
Untuk pembuatan larutan HCl 1N dengan cara mengambil larutan HCl pekat
sebanyak 8,5 ml yang dimasukan kedalam labu ukur 100 ml dan dicukupkan
volumenya dengan akuades hingga garis tanda. Untuk pembuatan larutan HCl 4%,
dengan mengambil larutan HCl pekat sebanyak 10,8 ml yang dimasukan kedalam
labu ukur 100 ml dan dicukupkan volumenya dengan akuades hingga garis tanda
(Ditjen POM, 1994).
3.3.1.2 Pembuatan Larutan Alkohol Asam
Untuk pembuatan larutan alkohol asam yaitu, 960 ml larutan etanol 95%
dalam labu ukur 1000 ml dan ditambahkan larutan HCl 4% hingga garis tanda (Wong,
et al., 2008).
3.3.2 Persiapan Sampel
Teknik pengambilan sampel dilakukan dengan cara sampling purposif dan
diasumsikan semua jenis durian yang ada di Kota Medan adalah homogen. Durian
yang diperoleh dari penjual durian di pasar Pringgan Jl. Iskandar Muda Medan. Kulit
buah durian segar yang diambil adalah bagian kulit dalam yang berwarna putih
dengan cara mengiris bagian kulit terluar buah durian (Gambar sampel dapat dilihat
pada lampiran 10). Kemudian kulit bagian dalam durian yang telah dipisahkan dari
bagian kulit terluar, dicuci bersih dari kotoran menggunakan air.
3.3.3 Ekstraksi Pektin
Bagian dalam kulit buah durian ditimbang 460 g dan ditambahkan akuades
sebanyak 4,14 L dan dihaluskan menggunakan blender, kemudian ditambahkan
dengan larutan HCl 1N hingga pH 2, kemudian dipanaskan pada suhu 90°C selama 4
jam. Selanjutnya disaring menggunakan kain saring. Filtratnya diambil dan
didinginkan pada suhu ruang dan ditambahkan 13,36 L etanol asam dan biarkan
selama 1 jam. Kemudian disaring menggunakan kain saring sehingga diperoleh
bagian gelnya yang kemudian ditambahkan 1,28 L akuades, lalu ditambahkan lagi 3 L
etanol 95% dan disaring kembali menggunakan kain saring, sehingga diperoleh pektin
basah. Pektin basah kemudian dikeringkan pada suhu 25°C. Kemudian pektin kering
3.3.4 Identifikasi Pektin
Larutkan 1 g pektin dalam 100 ml air suling, kemudian ditambahkan etanol
95% dengan perbandingan yang sama lalu ditambah NaOH 2N sehingga didapat
bentuk gel, yang bila ditambahkan HCl 3N serta dipanaskan akan terbentuk gumpalan
(Ditjen POM, 1995).
3.3.5 Pembuatan kurva kalibrasi
3.3.5.1 Pembuatan Kurva Kalibrasi Larutan Baku Tembaga
Larutan standar tembaga (1000 mcg/ml) dipipet 10 ml dimasukkan kedalam
labu ukur 100 ml, kemudian ditambah air suling sampai garis tanda (konsentrasi 100
mcg/ml). Larutan standar tembaga konsentrasi 100 mcg/ml dipipet 10 ml dimasukkan
kedalam labu 100 ml ditambah air suling sampai garis tanda (konsentrasi 10 mcg/ml).
Pipet 3, 4, 5, 10, 15, 20 ml larutan baku (10 mcg/ml), dimasukkan kedalam labu ukur
50 ml lalu ditambah air suling sampai garis tanda. Larutan tersebut mengandung 0,6
mcg/ml, 0,8 mcg/ml, 1 mcg/ml, 2 mcg/ml, 3 mcg/ml, 4 mcg/ml. Diukur pada panjang
gelombang 324,7 nm.
3.3.5.2 Pembuatan Kurva Kalibrasi Larutan Baku Seng
Larutan standar seng (1000 mcg/ml) dipipet 10 ml dimasukkan kedalam labu
ukur 100 ml, kemudian ditambah air suling sampai garis tanda (konsentrasi 100
mcg/ml). Larutan standar seng konsentrasi 100 mcg/ml dipipet 10 ml dimasukkan
kedalam labu 100 ml ditambah air suling sampai garis tanda (konsentrasi 10 mcg/ml).
Pipet 2, 3, 4, 5, 6, 7 ml larutan baku (10 mcg/ml), dimasukkan kedalam labu ukur 50
ml lalu ditambah air suling sampai garis tanda. Larutan tersebut mengandung 0,4
mcg/ml, 0,6 mcg/ml, 0,8 mcg/ml, 1,0 mcg/ml, 1,2 mcg/ml, 1,4 mcg/ml. Diukur pada
panjang gelombang 213,9 nm.
SD
3.3.6 Pengujian Daya Serap Pektin Terhadap Logam
Dimasukan 1 gram pektin dalam labu tentukur 100 ml yang masing-masing
berisi 50 ml larutan CuSO4 10 mmol/L dan ZnSO4 10 mmol/L, kemudian diaduk
selama 2 jam menggunakan pengaduk magnetik. Lalu larutan tersebut disentrifugasi
pada 3000 rpm selama 5 menit, ambil bagian supernatannya dan diukur konsentrasi
logam menggunakan spektrofotometer serapan atom pada panjang gelombang 324,7
nm dan 213,9 nm masing-masing untuk tembaga dan seng (Wong, et al., 2008). Nilai
absorbansinya yang diperoleh berada dalam rentang nilai kurva kalibrasi larutan baku
sehingga konsentrasi tembaga dan seng dalam larutan dapat dihitung dengan
menggunakan persamaan garis regresinya. Besar daya serap pektin terhadap logam
dapat dihitung dalam bentuk persen menggunakan rumus sebagai berikut:
%
Keterangan:
% = daya serap pektin, Lb = larutan blanko (tanpa penambahan pektin), Ls = larutan
sampel (dengan penambahan pektin). Persen daya serap pektin berdasarkan rata-rata
dari enam kali perlakuan (Eliaz, at al., 2007).
3.4 Rata – Rata Persentasi Tembaga dan Seng
Konsentrasi tembaga dan seng yang diperoleh dari hasil pengukuran masing–
masing enam larutan sampel, menggunakan persamaan regresi yang didapat dari
perhitungan kurva kalibrasi dan ditentukan rata–ratanya secara statistik dengan taraf
kepercayaan 95% dengan rumus sebagai berikut:
µ =
BAB IV
HASIL DAN PEMBAHASAN
4.1 Ekstraksi Pektin
Penelitian yang dilakukan pada proses ekstraksi pektin menggunakan bagian
dalam kulit durian yang telah dihaluskan bersama air. Pektin yang telah halus ini
kemudian diasamkan dengan penambahan asam klorida 1N hingga pH 2. Hal ini
dilakukan untuk mengeluarkan pektin dari sel pada jaringan dengan cara
menghidrolisa protopektin untuk menjadi pektin (Krick dan Othmer, 1967). Proses
selanjutnya dilakukan pemanasan pada suhu 90°C. Pada proses pengekstraksian
pektin, suhu yang digunakan dibawah titik didih air untuk mengurangi kehilangan
volume air yang terlalu besar akibat penguapan dari proses pemanasan selama
pengekstraksian dilakukan. Pada hasil penyaringan filtrat pektin dari hasil ektraksi
diperoleh filtrat pektin yang lebih kecil dibandingkan dengan jumlah volume sebelum
pemanasan, hal ini terjadi karena kehilangannya sebahagian kecil volume air akibat
dari penguapan yang terjadi selama proses pemanasan.
Pemisahan pektin dalam filtrat dilakukan dengan penambahan etanol asam
untuk memisahkan zat terlarut lainnya seperti glukosa. Penambahan etanol asam
dilakukan karena pektin praktis tidak larut dalam pelarut organik seperti etanol.
Penambahan etanol kembali dilakukan untuk memperoleh pektin basah yang murni
yaitu sebesar 320 gram. Menurut Akhmalludin dan Kurniawan (2005), pencucian
pektin menggunakan etanol akan menghasilkan warna pektin yang lebih baik (putih
kekuningan) dibandingkan dengan tanpa pencucian menggunakan etanol (flowshet
dapat dilihat pada lampiran 1).
Pektin kering yang diperoleh digerus hingga menjadi serbuk pektin yang
selanjutnya diayak untuk mendapatkan ukuran serbuk yang homogen. Berat serbuk
pektin yang didapat adalah sebesar 11,804 gram dari 460 gram kulit durian atau
sebesar 2,56% (gambar pektin dapat dilihat pada lampiran 11). Pektin yang diperoleh
berbentuk serbuk halus, berwarna coklat kemerahan dan praktis tidak larut dalam
etanol. Dari hasil identifikasi pektin yang dilakukan positif terhadap reaksi dengan
penambahan etanol 95% dan NaOH 2N terjadi gel yang apabila ditambahkan HCl 3N
dan dipanaskan terbentuk gumpalan.
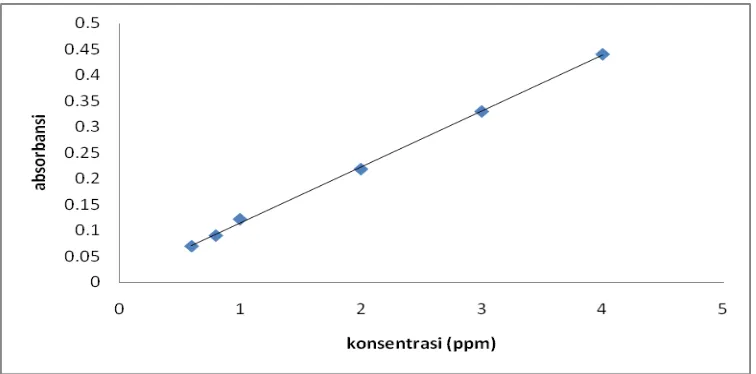
4.2 Kurva Kalibrasi Tembaga dan Seng
Dari hasil pengukuran absorbansi larutan standar tembaga yang berada
dalam konsentrasi rentang kerja tembaga pada panjang gelombang 324,7 nm
diperoleh persamaan garis regresi y = 0,10811x + 0,006608 dengan koefisien
korelasi r = 0,9996 (Data dan perhitungan dapat dilihat pada lampiran 2 dan 3).
Berdasarkan hasil pengukuran tersebut diperoleh kurva kalibrasi larutan standar
tembaga yang dapat dilihat pada gambar 1 :
Gambar 1. Kurva kalibrasi larutan standar tembaga
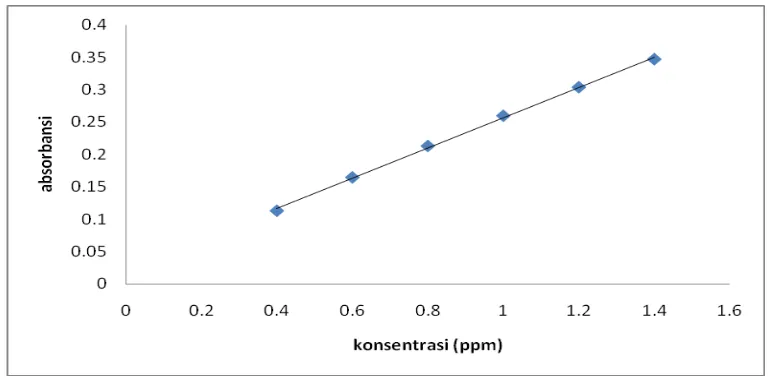
Dari hasil pengukuran absorbansi larutan standar seng yang berada dalam
konsentrasi rentang kerja seng pada panjang gelombang 213,9 nm diperoleh
persamaan garis regresi y = 0,2338x + 0,023263 dengan koefisien korelasi r =
pengukuran tersebut diperoleh kurva kalibrasi larutan standar seng yang dapat dilihat
pada gambar 2 :
Gambar 2. Kurva kalibrasi larutan standar seng
Harga koefisien korelasi (r) yang mendekati 1 dari masing–masing kurva
kalibrasi tembaga dan seng menunjukkan korelasi antara konsentrasi dengan
absorbansi. Hal ini sesuai dengan Hukum Lambert – Beer yaitu A = a.b.c dimana nilai
absorbansi (A) berbanding lurus dengan nilai konsentrasi (c) (Day dan Underwood,
1980).
4.3 Uji Kemampuan Daya Serap Pektin Terhadap Logam
Pektin yang diperoleh dilakukan pengujian terhadap penyerapan larutan
logam, yaitu larutan logam tembaga dan seng yang kemudian pada masing-masing
larutan logam ditambahkan pektin yang diaduk selama dua jam. Pektin dalam larutan
logam berbentuk larutan keruh, hal ini terjadi karena pembentukan senyawa
kompleks antara logam dan pektin yang memiliki sifat yang tidak larut dalam air.
Larutan ini selanjutnya dipisahkan dari senyawa kompleks pektin dan logam
menggunakan sentrifugasi. Pengukuran dilakukan terhadap supernatannya
menggunakan spektrofotometer serapan atom masing–masing pada panjang
gelombang yang memberikan absorbansi maksimum yaitu pada panjang gelombang
324,7 nm dan 213,9 nm masing-masing untuk tembaga dan seng. Hal yang sama
dilakukan tanpa penambahan pektin terhadap larutan blanko. Untuk menghitung
konsentrasi tembaga dan seng diperoleh dari persamaan garis regresi larutan
standarnya. Hasil analisis kuantitatif tembaga dan seng dapat dilihat pada tabel 1
(Data dan perhitungan daya serap pektin terhadap logam dapat dilihat pada lampiran 6
dan lampiran 8).
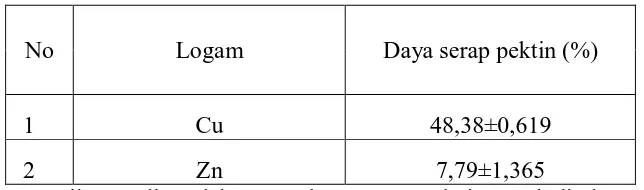
Tabel 1. Daya Serap Pektin Terhadap Logam
No Logam Daya serap pektin (%)
1 Cu 48,38±0,619
2 Zn 7,79±1,365
Keterangan: Hasil yang diperoleh merupakan rata-rata dari enam kali ulangan.
Pada hasil pengukuran logam tembaga menggunakan spektrofotometri
serapan atom, diperoleh konsentrasi blanko sebesar 2,148 ppm dan konsentrasi
sampel sebesar 1,109 ppm sehingga dapat dihitung besar peyerapan pektin terhadap
logam tembaga adalah sebesar 48,38±0,619%. Hasil pengukuran pada logam seng
diperoleh konsentrasi blanko sebesar 1,052 ppm dan konsentrasi sampel sebesar 0,970
ppm dengan besar penyerapan logam seng menggunakan pektin adalah 7,79±1,365%.
Dari data yang diperoleh dapat dilihat bahwa pektin mampu menyerap logam berat
seperti tembaga dan seng dan memiliki afinitas yang bevariasi terhadap logam
berat(data dan perhitungan dapat dilihat pada lampiran 9).
Proses pengikatan logam terhadap pektin adalah dengan adanya gugus
karboksilat dari pektin yang dapat bereaksi membentuk senyawa kompleks antara
pencemaran lingkungan dan antidotum dari logam berat karena pektin memiliki
afinitas terhadap logam yang dapat bereaksi dengan gugus karboksilat dari pektin
membentuk senyawa kompleks yang tidak larut dalam air (Kupchik, et al., 2005).
Dari hasil penelitian Wong, et al (2008), pada pengujian daya serap pektin
terhadap logam tembaga lebih besar dibandingkan terhadap logam seng, yaitu sebesar
54,94% dan 8,46%. Sedangkan pada penelitian yang dilakukan, daya serap pektin
terhadap logam tembaga dan seng diperoleh masing-masing sebesar 48,38% dan
7,79%. Perbedaan besar daya serap pektin ini mungkin diakibatkan dari perbedaan
jenis kulit durian yang digunakan memiliki variasi kandungan pektin. Menurut Cotton
(1989), besar jumlah pengikatan logam tembaga dan seng bergantung pada sifat
kestabilan kompleks yang terjadi pada pektin dengan logam tembaga ataupun logam
seng, dimana energi penstabil medan ligan mempengaruhi atas kecendrungan umum
pembentukan senyawa kompleks dari suatu senyawa dengan logam.
BAB VI
KESIMPULAN DAN SARAN
6.1 Kesimpulan
a. Berdasarkan hasil penelitian yang telah dilakukan, kulit bagian dalam durian
mengandung pektin yaitu sebesar 2,56%.
b. Dari hasil pengukuran logam tembaga dan seng menggunakan spektrofotometri
serapan atom, pektin memiliki daya serap terhadap logam tembaga dan logam seng
tersebut masing-masing sebesar 48,38±0,62 % dan 7,79±1,37%.
6.2 Saran
Disarankan agar peneliti selanjutnya untuk meneliti jumlah kandungan
pektin dalam berbagai buah-buahan lainnya sebagai sumber pektin yang dapat
DAFTAR PUSTAKA
Akhmalludin dan Kurniawan, A. (2005). Pembuatan Pektin Dari Kulit Cokelat Dengan Cara Ekstraksi. Universitas Diponegoro-press. Semarang.
Anonim (2009). Durian. Diambil dari http://id.wikipedia. org/ wiki/ Durian.
Anonim (2010). Fruit anatomy. Diambil dari http://wikipedia/fruit_anatomy.htm.
Cotton, F.A dan Wilkinson, G. (1989). Kimia Anorganik Dasar. Penerjemah: Suharto, S: Yanti R.A. Penerbit Universitas Indonesia. Hal. 429-435.
Crues, W.V. (1988). Commercial Fruit and Vegetable Products. Fourth Edition. Mc. Graw Hill Book Company Inc. New York. Hal. 427.
Darmono, (1995). Logam Dalam Sistem Biologi Makhluk Hidup. UI Press. Jakarta. Hal. 9-25.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta. Departemen Kesehatan RI. Hal. 654-655.
Eliaz, I., Weil E., and Wilk, B. (2007). Integrative Medicine and the Role of Modified
Citrus Pectin/Alginates in Heavy Metal Chelation and Detoxification – Five Case Reports. Forsch Komplementärmed; Amitabha Medical Clinic and
Healing Center Sebastopol and Eco Nugenics Inc. Santa Rosa, CA. USA. Vol.14:358–364.
Endress, H.U. (1988). Nonfood Use of Pectin. Hebstreith and Fox Kg Pectin-Fabrik. Neuenburg. Jerman. Hal 257.
Harmita, (2004). Petunjuk Pelaksanaan Validasi Metode Dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. Departemen Farmasi FMIPA-UI. Vol. I. Jakarta. Hal. 117-133.
Hart, H., Craine, L.E, and Hart, D.J. (2003). Kimia Organik. Penerjemah: Achmadi S.S., Edisi Kesebelas. Jakarta. Penerbit Erlangga. Hal. 511.
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Edisi kedua. UI Press. Jakarta.
Kirk & Othmer, (1967). Encyclopedia of Chemical Technology. Second Edition. Volume 14.Jhon Wiley & Sons Inc. Hal. 635.
Kupchik, L.A., Kartel, N.T., Bogdanov, E.S., Bogdanova, O.V. and Kupchik, M.P. (2005). Chemical modification of pectin to improve its sorption properties. Russian Journal of applied chemistry. National University of Alimentary Technologies. Kiev. Ulkraine. Vol.79. No.3. Hal. 457.
Palar, H. (2008). Pencemaran dan Toksikologi Logam Berat. Penerbit Rineka Cipta. Jakarta. Hal. 23-61.
Ranganna, S. (2000). Hand Book of Analysis and Quality Control for Fruit and
Vegetable Products. second edition. Tata McGraw-Hill Publisshing Company
Limited. New Dehli. Hal. 35.
Rohman, A., dan Gandjar, I.G. (2007). Kimia Farmasi Analisis. Penerbit Pustaka Pelajar. Hal. 298-322.
Sartono, (2002). Racun dan Keracunan. Penerbit Widya Medika. Jakarta. Hal. 52-264.
Soemirat, J. (2003). Toksikologi Lingkungan. Gadjah Mada University Press. Jogjakarta. Hal. 36-49.
Sony, (2009). Penetapan Kadar Logam Tembaga (Cu) dan Logam Seng (Zn) pada Air Minum yang Menggunakan Penyaring YAMAHA Drinking. Skripsi Jurusan Kimia FMIPA USU Medan.
Sofyan, (2010). Penetapan Kadar Logam Dengan Ekstraksi Menggunakan Metode Air-Acetylene Flame. UM Communitty. Diakses Juli 2010. Diambil dari : file:///F:/pk%20logam/showthread.php.htm.
Vogel, (1989). Kimia Analisis Kuantitatif Anorganik. Penerjemah: Pudjatmaka dan Setiono. Edisi Keempat. Jakarta: EGC Kedokteran. 229-289.
Widowati, W., Sastiono, A., dan Jusuf, R. (2008). Efek Toksik Logam. Penerbit ANDI. Yogyakarta. Hal. 303.