ISOLASI DAN KARAKTERISASI SIFAT FUNGSIONAL
KQMPONEN
PEMBENTUK
GEL CINCAU HIJAU
(CycIea barbata
L.
Miers)
OLEH :
NYOlMAN ARTHA
PROGRAM PASCA SARJANA
INSTITUT PERTANIAN BOGOR
NYOMAN ARTHA. Isolasi ?&tn W e r i s a s i Sifat Fungsional Yomponen Pembentuk Gel Cincau Hijau (CycCea barbata L Miers). Dibawah tim komisi pembimbing DEDI FARDIAZ (ketua). ANTON APRIYANTONO (anggota),
C.
HANNY
WLJAYA (anggota), PURWZYATNO HARIYADI (anggota].Ifidrokoloid menrpakan polimer bersifat larut di dalam air dan &pat meningkatkan kualitas reologi produk pangan. SaLah satu surnber hidrokoioid yang berpotensi untuk dikembangkan sebagai #ahan tambahan pangan adalah komponen pembentuk gel
dari
gel cincau hijau (Cyclea barbata L. Miers).Penelitian ini bertujuan untuk mendaptkan identitas komponen pembentuk gel (KPG) dam cincau hijau d m memplajari sifat-sifitt reologi dari komponen tersebut. Tahapan penelitian yang dilaksmakan meliputi isolasi, frhinasi, dan karakterisasi sifat reologi. Iso#asi KPG dilakukan dengm mengebtrak gel cincau men- larut= 0.028 M EDTA, pH 2.5, suhu 90°C selarna 30 menit. W G yang diperoleh berkisar 0.89-1.89 (g) dari 50 g daun cincau. Fmksinasi larutan 0.25% b/v KPG dengan membmn ultrafiltrasi, menunjukkan M w a KPG dapat dibagi atas fraksi tertahan mernbran 5 pn (F5) BM 1.(j00.0O0-2.000.000 Da (52% bh), fraksi 1010s m e m h 5 pn tetapi tertahan membran 3 pm (F3) BM 300.000-500.000 Da (36% b h ) dan fraksi 1010s n~embran 1.2 p n tetapi tertahan membran 0.6 pn (F0.6)
B M
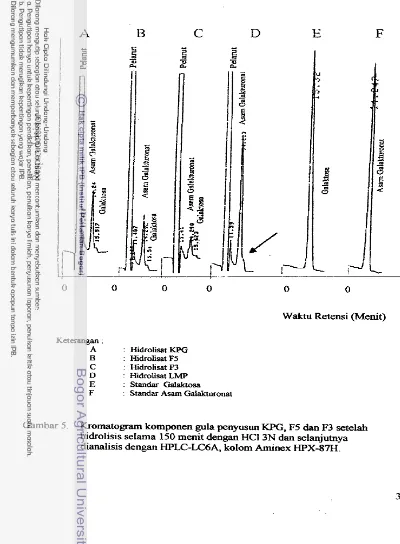
10.000-100.000 D a (Woo). AnalisisHPLC
memberikan i n d h s i bahwa KPG, F5 dan F3 tersusun oleh asam gaiakturonat dan galak-tosa dengan rasio 12:7 pada KPG. 33:lO pada F5 dan 35:9 pada F3.Lamtan 0.5-2.5% KPG dan fraksinya bersifat plastis semu pada laju geser O- 400 '/s, dengan kekentalan terukur tebih tinggi dari larutan alginat, tetapi iebih rendah dari larutan gom xantan pada konsentrssi yang sama. Model yang paling sesuai untuk menggambarkan ketergantungau kekentalan t . , konsentrasi KPG, F5, F3 (=-O.SO/ob/v) dan laju geser add& model Herschel-BurRley. Kekentalan terukur 9 rnl larutan KPG, F5 clan F3 meningkat dengan penam- CaC12 sampai taraf 0.4 mrnol dan penyimpanan beku selama I bulan, namun menurun setelah pH lsrutan dinaikkan dari 4.0 menjadi 8.0. Perilaku reologi larutan KPG, F5 dan F3 bersifat reversibel setelah dipanaskan dari 24OC sainpai 90°C dan didinginkan kembali sampai suhu 25°C. Hasil seleksi hidrokoloid komersial menunjukkan
bahwa
hanya dginat dan pektin bemetoksi rendah (LMP) yang mampu bersinergis dan rnembentuk gel dengan KPG, F5 maupun F3. Berdasarkan parameter yang diuji, temyata interaksiABSTRACT
NYOMAN ARTHA. Isolation and Characterization of the Functional Properties of Gel Forming Components from Cyclea barbata L Mien Leaves. Under the direction of DEDI FARDIAZ as a chairman, ANTON APREYANTONO, C. M Y WIJAYA, P U R W A T N O HARIYADI as members of suvervisory commitee.
H y d r ~ ~ ~ l l o i d s are water solub!a polymer which have the ability to improve rheological quality of food products. One of potential hydrocolloid sources to be
developed as food additive is gel forming components (GFC) of Cyclea barbata L Miers leaves.
This research was aimed to identify GFC from CycIu barbata L Mien leaves and to investigate the rheological properties of GFC solutions. The research was dcvidect intc
three
steps, as Follows: isolaticn of GFC, fractionation and characterization of rheological behaviour of GFC and its fractions solution. Isolation of GFC was wried out by extraction using 0.028 M EDTA solution, pH 2.5, at 90°C for 30 min. The yield of GFC after freeze-drying was 0.89-1.89 g &om 50 g Cyclea ba.*bata L. Miers leaves. Fractionation of 0,25 % GFC solution using ultrafiltration, showed that frsction F5 cuntaining GFC with molecular weight0
of 1,000,000- 2,000,000 Da had the highest yield (52%), followed by fraction F3 with h4W of 300,000-500,000 Da (36%) and 6-action F 0.6 with M W of 100,000-10,000 Da (8%). HPLC analysis showedthat
GFC and its fractions composed ofthe
same simple sugars, i. e. galacturonic acid and galactose with ratio 12:7 for GFC, 33:lO forF5
and 35:9 for F3 fractions.The GE'C. F5 and F3 solutions with concentration from 0.5%-2.5% w/v have a pseudoplatic characteristic with yield value (ro) on shear rate of 0-400 '/s.
The
apparent viscosity of GFC and F5 solutions were higher than that of alginate solution but lower than that of xanthan gum solution of the same concentration. If the concentration of GFC md shear rate increased, the apparent viscosity of solutions will increase. The apparent viscosity of all solutions studied increased, with addition of CaC12 up to 0.4 mmol for 9 ml, 1.5% GFC, F.5 and F3 solutions, and prolonged freeze storage periode up to 4 week. However its viscosity apparent decreased when the pH increased up to 8.0. The apparent viscosity of GFC was reversible when heated up to 90°C and cooled down to 2S°C. From the examined commercial hydrocolloids, only commercial alginate and low methoxyl pectin were able to form gel with GFC and its fractions. The gel strength and rigidity of mixtures gel of LMP- GFC and its fractions were much higher than that of mixtures gel of Alg-GFC and its fractions but the syneresis was lower.&~dul disertasi : ISOLASX DAN KARAKTERISASI SIFAT
I
FUNGSIONAL KOMPONEN PEMBENTUK GELCXNCAU HLTAU (CycCea barbata L. Miers) d a m e Mahas~swa : Nyornan Artha
Hornor Pokok : 975041 /IPN
Menyetujui Komisi Pembimbing
s-==T
(Prof. Dr. Ir. H. Dedi Fardiaz. MSG.) K e t u a
I
I A n g g o t a A n g g o t a
I
i
a m Pasca Sarjana
frida Manuwoto, MSc.)
I
I
PRAKATA
I
Ketika merenungkan realita, kita tidak hanya terpaku melihat fenomena, karena
sebab intrinsik yang disebut nomena. Fenomena selalu membatasi wujud absolut
uatu obyek, karena ada sebab yang bersembunyi dibaliknya Begitu pula dengan
neliiian mengemi gel cincau ini, tentu saja beium mampu mengungkapkan makna
i
penyebab yang tersembunyi di dalamnya, mengingat kegiatan sairls selalu l/emkhir pa& keheningan waWu yang rnenjauhi wins itu sendiri.I Syukur kehadapan keheningan yang menuntun kami melalui ide mumi dan
bagian biayz dari Yth, Bapak
Prof.
Dr. Zr. W Fardiaz, MSc., dan bimbinganang sangat intensif dari Bapaic Dr. Ir. Anton Apriyantono, MS., Prof. Dr.
Ir.
hristofora Hanny Wijaya, MSc., dan Dr. Ir. Pwwiyatno Hariyadi, MSc. yang sangat
rpe- dalam memberikan htma, r & q kslrsa, serta makna gada Nisan ini. Untuk
s mua staf Program Studi Umu Pangan karni ucapkan terimakasih. Atas doa yang
I
+us I Gede K u m k Ni Nyoman Siki, Nyornan Sutjiarka (almachum) dan Made
lendri, Drs Wayan Rai Suarthana Ak,
MM..
serta Made Mayuni, kami berusahaenyelami makna hening j n d a bersama yang tercinta Wayan Sudiarsi, SE
dan
Gde7
ddhitya Prabhawa.Bogor, 23 November 2001
I N y o m n A h a lahir dan pasan,- keluarga petani tulen I Gde Kumba d m
A i Nyornan Siki, tanggal 10 Denember 1962 di Desa T e e Bali SD dilewatkan di
tegak (1974) clan SMF dilewatkan di SMP 1 Klunghag (1977). Lemudian lvlus h4A tahun 1981 di Singaraja Bali. Tahun yang sarna mengikuti Proyek Per~nfis I n diterima pada
Jurusan
Teknologi Hasil Pertanian(TE-IP)
Universitas Brawijaya1
lang, .sampai 1ul.m tahun 1986. Tahun 1992 mengikuti Program Pasca SajanaJurusan THP-UGM dan lulus tahun 1994. Tahun 1997 berkesempatan
engikuti
Program Pasca Sarjana p d a Program Studi llmu Pangan, Sub Program'mia Pangan dengan sponsor d m Beasism Pendidikan Pesca Sajana @PPS)-
irektorat Pendidikan Tinggi (Dikti-IPB).
f
Sebelumnya tahun 1988 menikah dengan Ni Wayan sudiarsi, SE dan dikaruniais o-g anak yang diberi nsma Gde Adithya Prhabawa (Adhit) yang
kini
telah duduk d'b
angku SMP.Bogor, 23 November 2001
DAFTAR IS1
DAFTAR TABEL ...
DAFTAR GAPVZBAR ...
DAFTAR L A W I R A N ...
DAFTAR ISTILAH
...
PENDAHULUAN
...
Latar Belakang . .
...
Tujuan Penellaan ...Kerangka Penefitian ...
Hipotesis ...
Hidrokoloid
...
Konformasi Hidrokoloi d....
...
Ebrakteristik ReologiDaftar Pusta ka.
...
ISOLASI. FRAKSINASI DAN KAFUKTEIUSASI KOMPONENPEMBENT-LJK GEL DARI DAWN T A N A M A N CINCAU HUAU
(Cyclea barbata L
.
Miers)Absiract
...
Pendahuluan...
...
Bakm clan Metode PenelitianHasiI dan Pembahasan ...
Kesimpulan ... ... Daftar Pustaka iv vi vii 1 1 4 5 6
KARAKTERISTIK REOLOGI HWROKOLOlD DARl DAUN TANAMAN CINCAU f-IIJAU (L'ycleo barbata L . Miers)
Abstract
...
43...
Pendahul uan. 43
...
Bahan dan Metode Penelitian 45
HasiI dan Pembahasan ... 47 ...
Kesimpulan 67
KARAKTEFUSTIK GEL CAMPURAN KOMPONEN PEMBENTUK GEL DAUN TANAMAN CINCAU HIjAU (Cyclea barbata L
.
Mers) DENGAN HIDROKOLOID KOMERSIALAbstract ... ...
Pendahuluan
Bahan dm Metode Penelitian ...
Hasil dan Pembahasan ...
Kesimpulan ...
Daftar Pustaka ...
DISKUSI UMUM
...
DAFTAR
TABEL
Model hubungan kekentatan terukur dengan laju geser larutan KPG, F5 clan F3 pada berbagai konsentrasi..
....
50Model hubungan konsentrasi dengan indeks konsistensi lamtan KPG, F5 dan F3 pa& berbagai
konsentrasi.. ... 5 1 Hubun.gan komenbmi dan laju geser terhadap kekentalan terukur larutan KFG, F5 dan F3 pada berbagai 51
...
konsentrasiModel hub- kekentalan
terukur
d e n w suhu pemanasan 6424OC sampai 9Q°C den- laju p i n m a m i 1°C permenit dari larum LPG, F5, F3 pada konsentrasi 1.5% b/v, diukur
....
aecara kcmtinyu pada Iaju 400 '/s.....
Karakteristik fisiko-khia KPG, F5 dan F3.. 92DAFTAR GAMBAR
Gambar 1.
Gambar 2.
Gambar 3.
Gsmba? 4.
Gambar 5
[image:140.517.69.417.68.573.2]Gambar 6
Gambar 7
Gambar 8
Gambar 9
Gambar 10
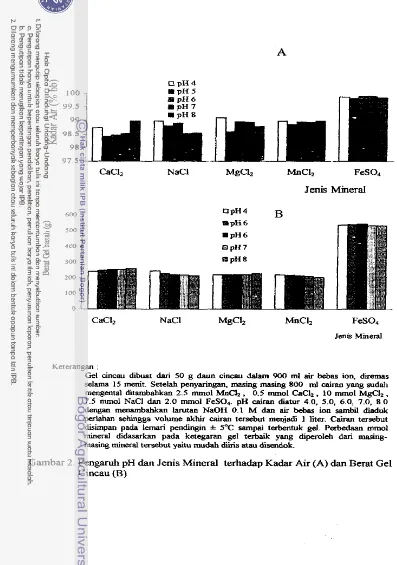
Diagram alir proses 6aksinasi larutan KPG 0.25% b/v dengan membran ultrafiltrasi pa& porositas berbeda.. ... 26 Pengaruh pH dan Jenis Mineral terhadap Kadar air (YO hbb) gel cincau (A) dan Berat gel cincau (g) (B).
...
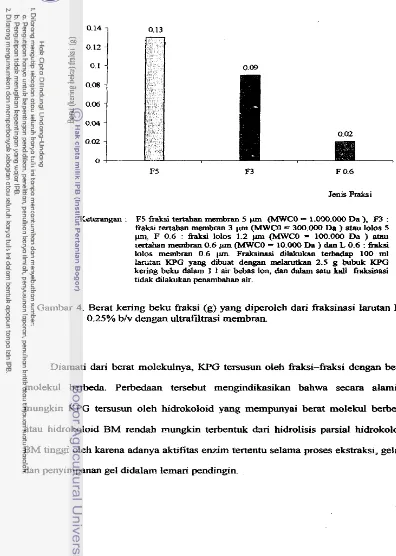
29 PenganIh Jenis Mineral dan pH pada saat ekstraksi terhadap persentase KPG (Yobk) yang diperoleh.. ...Berat kering beku fraksi yang diperoleh dari fiaksinasi larutan KPG 0.25% b/v dengan uitrafiltrasi m e m k (g) ... 32
Kromatogram komponen y l a penyusun KE'G, F5 dan F3 setelah hidrolisis selama 150 menit den- HCI 3N dan seIanjutnya dianalisis dengan nenggmakm HPWdA,
...
kolom Aminex WX-87H 35
Model Herschel-Burkley dari hubungaa gaya geser dengan laju geser lamtan KPG. F5
dan
F3 masing-masing dengan konsenirasi larutan >0.5% blv, diukur pada laju 47... geser 0-400 '/s, suhu 2S°C..
Kekentalan Terukur larutan KPCi, F5 dan F3 masing- masing pada konsentrasi 0.5-2.5% blv, diukur pada laju
geser 0-400 l/s, suhu 2S°C.. ... 48
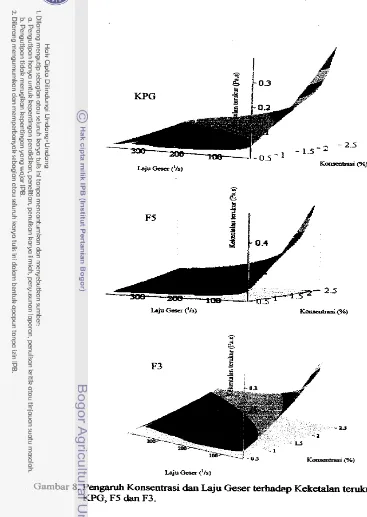
Penganih Konsentrasi dan Laju Geser terhadap Kekentalan ... terukur larutan KPG, F5 clan F3.. 52 Perbandingan kekentalan larutan KPG, F5, €3, gom xantan dan alginat komersial masing-masing pada konsentrasi 1.5% b/v, diukur secara kontinyu selama 10 menit pada laju eeser 0-100 '/s, suhu 25°C.. ... 53 Kekentalan terukur larutan KPG, F5 dan F3 masing- masing pada konsenmsi 1.5% b/v d e n p . penambahan 0.1-0.4 mmol CaCI,, diukur secara kontinyu selama 10
...
Gambar 11
Gambar 12
[image:141.517.37.425.31.553.2]Gambar 13
Gambar 14
Gambsr 15
Gambar 16
Gambar 17
Kekentalan larutan KPG, F5 dan F3 pada konsentrasi 1.5 % blv padapH 4.0, 5.0,6.0,6.0, 7.0 dan 8.0, diukur secara
kontinyu selama 10 rnenit pada iaju geser 400 '/s, suhu 25°C ... 57
Kekentalan larutan KPG, F5 dan F3 masing-masing pada konsentrasi 1.5 % b/v setelah dilakukan thawing dan suhu larutan tersebut mencapai 25OC selama penyimpanan beku (-20T), diukw secara kontinyu selama 10 menit pada laju
.
...geser 400 '/s suhu 2 5 " ~ . 60
Kekentalan terukur lamtan F5 (A), KPG (B) dan F3 (C) masing-masing pada konsentrasi 1.5% b/v pada pemanasan 24-C sampai 90°C dengan Iaju peningkatan 1°C permenit
dan diukur pa& laju geser 400 '/s ... 63
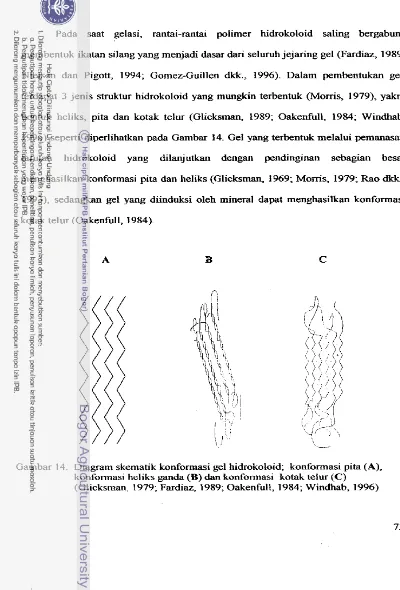
Diagram skematik k o n f m a s i %el hidrokoloid; konfonnasi pita (A), koaformasi heliks ganda (B) dan
kanformasi kotak telw (C) (Gliclcsman, 1979; Fardiaz, 1989; Oakenfi~il, 1984; Windhab, 1996) ... 72 Sketsa umum kurva hasil pengukuran Stevens W R A
T d u r e Analper
...
76Kekuatan gel (x), Kekakuan gel (y) dan Sineresis gel (2) campuran
w ,
F5, F3 (2.5 % b/v) dengan LMP atau Alginat pada konsentrasi 0.5-2.5% b/v setelah disimpan padas&u*PCselama5jam,15jamdan25jam...
78Kemungkinan model k o n f m a s i gel campwan KPG- alginat, FS-alginat, F3-alginat (A), KPG-LMP, FS-LIvP
! DAFTAR ISTILAH
KPG
M ~ P P Y 'I K Da Pas g "C GFC M W
: Komponen Pembentuk Gel yang terdiri dari fiaksi F5, F3, F0.6 dan komponen dengan beat molekul i l 0 . 0 0 0 Da.
: Fraksi KPG textahan membran 5 pn dengan rentang berat molekul (BM) 1.000.000-2.000.000 Da
: Fraksi KPG teatahan membran 3 pn, tetapi 1010s mernbran 5 pm.
Rentang BM 300.000-500.000 Da
: Fraksi KPG tertahsn membran 0.6 pm, tetapi 1010s membran 1.2 p. Rentang BM 10.000-100.000 D a
: Kekentalan terukur lanitan non Newtonian : Laju Geser
: Tekanan Geser
: indeks konsistensi model Herschel-B&ey : Dalton
: Pascal. detik
: Gram
: Derajat Celsius
PENDAHULUAN
1
Hidrokoloid merupakan suatu polimer berantai panjang, umumnya polisakarida engan berat molekul besar, bersifat larut d m terdispersi di dalam air, menyerap danengikat air dalam porsi besar, membentuk koloid, mampu meningkatkan kekentalan
dan sebagian dapat membentuk gel (Glicksman, 1969; 1979; Mithcell, 1979;
omeranz, 1991). Oleh m a n y s hidrokoloid mempunyai fungsi sangat sirategis
am perkembangan i n d u d pangan, mengingat tujuan utama dari penambaban
drokoloid ini berkai+m &ngan q a y a rneningkatkan penerimaan konsumen alum
uk tersebut. Secara spesifik. penggunaan hidrokoloid ditujukan untuk
e n i n g k a t ! sifat fimgsiod suatu produk padgan, terutama yang berhubwigau
In.@= tekstur produk yang diinginkan, seperti: kekentalan, kekuatan gei, kestabilm emulsi. retensi air, rnengubah laju p c m b e b clan
v o d i f i k a s i pembentukan laistal es (Gliclcunan, 1969; Bell, 1989; Ear&- 1989)
Perdagangan hidrokoloid di Asia Tenggara berkembang pesat pa& dasawarsa
b lakangan ini. Kebutuhan hidrokoloid Malaysia 2.6 juta kg, Indonesia 2.2 juta kg, F lipina 0.7 juta kg
dan
Thailand 0.7 juta kg, dengan rata-rata peningkatan secaraenyeluruh sekitar 14.2 persen setiap tahun (Anonim, 1993). Biro fusat Statistik
lam laporan Statistik Perdagangan Luar Negeri (1999) melaporkan bahwa impor
hi okoloid Indonesia pa& bulan Agustus 1999 telah mencapai 22.289.048 kg
d ngan estimasi harga sekitar 12.206.325 doIar Amerika clan laju peningkatan sekitar
1 persen per tahun. Potensi pasar hidrokoloid diproyeksikan semakin meningkat
arena pergeseran pola konsumsi di perkotaan ke arah yang sederhana, praktis dart
saji s e w akibat peninaatan kesibukan dan berkembangnya diet kesehatan.
eluang ini perlu dimanfaatkan selain permintaan pasar sangat terbuka, juga
engingat potensi sumber daya dam Indonesia yang memadai.
1
Saat ini sudah dikenal beberapa jenis hidrokoloid komersial baik yang berasaltamman, hewan, hasil fermentasi mikroorganisme maupun yang sintetis. Namun
miluan, hidrokoloid alamiah asal tananan masih tetap diminati, karena iebih murah
aman dikonsumsi. Cincau hijau (Cyclen barbata L. Miers) rnerupakan salah satu
ber hidrokoloid murah, namun beIum digali potensinya. Gel yang dihasilkan dari ini telah Mas* secara turun-temurun oleh nenek moyang bangsa
sia sebagai bahsn campuran minuman.
Kell~lggulan hidrokoloid cincau hiijau dari hidt'okoloid lain adalah sangat mudah
engaIarni gelasi pada air dingin dan gel yang dihasilkan bersifat m e n i b e l , serta
k kentalannya dapat ditingkatkan dengan penambahan mineral. Kurciati dkk. (1999) elaporkan bahwa rasio daun cincau : air yang terbaik untuk menghasilkan gel
c ncau adalah sebanyak 5% @/v). I n f o m i tersebut sangat penting berkaitan dengan
p osedur lanjutan yang akan dikembangkan untuk mengisotasi hidrokoloid tersebut
I
tetap mernberikan hasil yang reversibel. Oleh karena itu d a m cincau merupakan s ber hidrokoioid potensial untuk dikaji secara mendalam.ar
Beberapa penelitian teIah dilakukan untuk mendapatkan hidrokoloid alamiah ri sumber baru yang berpotensi komersial. Setiap hidrokoloid baru mungkinm mpunyai sifat yang relatif sama atau
\
be- dengan hidrokoloid lain, akan tetapidasar suatu Mdrokoloid agar &pat diterapkan ke dalam W a n lain adalah mudah
1
terdispersi, mudah !arut, dapat meningkatkan kekentalan larutan, mempunyai sifat fungsional lebih baik dari hidrokoloid yang telah dike.laI, jumlahnya memadai,murab, serta bersifat aman untuk dilconsumsi (Baird d m Pettitt, 1993).
I,
I Gelasi cincau hijau diinduksi oleh logam poIivaIen, dimana matrik gel yang !
dihasilkztn bersifat sangat tegar. Untuk mernpelajari sifat-sifat dasar dari gel cincau I
hijau, rnaka komponen pembentuk gel ( n G ) cincau h a s diisolasi. Diduga gel Eincau tersusun olch tcomponen p e m ~ t u i c gel, semt, ~ o m m , air dan ion logsm.
benm demikian unmk mengisolasi KPG dari gel cincau, diperluk= langkah
bistematis yang mampu merninimalkan keberadaan komponen lain selaia KPG.
bisamping itu perlu diupayakw suatu kondisi yang d a p t menyebabkan gugus h g s i
/lidmkoioid menjsdi &if, sehingga ikatnn komplek hidrokoloid-ion Logam llun
bejadi lemah, dan dengan semakin lemallnya ikatan tersebut maka ah peluang
i
b t u k melakukan kelasi logam tersebut dengan senyawa pengkelat logam seperti
~ D T A . Senyawa pengkelat logam yang diperldcan a;ialah pengkelat yang rnampu
i
henarik dan mengikat ion logam secara kuat, cepat dan efisien, sehingga KPG akan
I
i:,
blh mudah dipisahkan.Aktivasi gugus hngsi hidrokoloid sangat dipecgaruhi oleh kondisi lingkungan,
+pexti pH dan suhu. Penurunan p H ekstrak diantara 2-3.5 dapat menyebabkan
*asi gugus fungsi clan mengakti- ion logam sehingga Lebih mudah dikelat. dementara kenaikan suhu ekstrak sampai 90°C telah dilaporkan &pat rneningkatkan
i
qelarutan hidrokoloid (Christensen, 1973), sehingga hidrokoloid akan lebih mudah
pisahkan dari komponen lain. Informasi ini sangat penting untuk diperynakan lam isolasi komponen pembentuk ge! dari gel cincau hijau.
1
Untuk dapat diterapkan &lam skala komersial, maka sifat hngsional KPGI
pncau hams dipelajan secara mendalam. Sifat tersebut dipengaruhi oleh berat I
fmlekul, konsentrasi, keberadaan mineral, kondisi lingkungan dan unit gula
pdrokoloid. Untuk mempelajari struktur hidrokoloid, pendekatan yang paling
ungkin dilakukan adalah dengan rnempelajari unit gula penyusunnya, oleh k a n a tu hidrokoloid hams dihidrolisis dengan menggunakan asam klorida atau asam
I
iulfat. Hidrof isat yang diperoleh dianalisis dengan kromatografi (Southgate, 1991). $ujuan Penelitiani
Tujuan u m u m dari penelitian ini adalah untuk mendapatkan identitasiornponm pembentuk gel cinssu hijau dan memperoleh infomasi mengenai rifai-
fhi . t a r dari KPG beserta fkaksinya. Tujuan khusus yang ingin dicapai da1am
hnelitian ini adalah :
!
1. Mernperkirakan herat molekul dari masing-masing fraksi.
:
2. Memperoleh informasi mengenai jenis gula penyusun KPG dan fraksi KPG Icincau hijau.
1 3. Mempelajari sifat fungsional larutan KPG d m fraksi masing-masing pada
I
~
konsentrasi 0.5-2.59'0 (blv) sesuai dengan penerapan hidrokoloid komersialsebagai pengental atav sebagai agen pembentuk gel.
4 Mempelajari sifat-sifat gelasi KPG, melalui intemkri sinergistik dengan I
Ferangka Penelitian
! Pendekatan sistematis diperlukan agar dapat memisahkm komponen
4mbenb.k gel (KF'G) dari matrik gel yang telah terbentuk, mengingat gel cincau Srdiri dari berbagai komponen. Komponen tersebut berinteraksi membentuk matik
&ns kornpak clan tegar. Kecepatan gelasi dan tin- lcekentaian gel mengaiami ningkatan apabila dilakukan penambahan mineral tertentu (Kurniati dkk., 1999) ha1
i i rnenandakan bah.wa gelasi c i n a u hijau bersifat ionik. Oleh kareaa itu pendebtan
ilg dipergunakan untuk mengisolasi KPG cincau hijau adalah sebagai berikut :
i
1. EkstraLsi dilakukan dalarn larutan pengkelat logam. Etilendiamin tetra asam
(
asetat (EDTA) merupakan pengkelat logam yang dapat rnembent.uk 6 lingkamn1
kelat yang h a t . Penggunaan EDTA didasarkan pada: (1) reaksi sang berlangsung secara spontan pa& rentang pH yang luas, ( 2 ) reaksi berlangsung I1
satu tahap, dan (3) konstanta kestabilan kelat ion logarn dengan EDTA sangat 1 besar sehingga reaksi ber1angs-g lebih sempuma.L]
Ekstraksi diatw pada pH rendah, dengan pertimbangan ion logam akanmengalami diwaiasi shingga lebih mudah dikelat oleh EDTA.
i
I . I Ekstraksi dilakukan pada suhu 90°C dengan maksud agar ikatan yang membentuk rnatrik gel menjadi lemah, dan kelarutan KPG akan lebih besar
~
sehingga lebih mudah dipisahkan.5 . Bubuk KPG kasar yang diperoleh dimurnikan dengan melarutkannya &am 4 r bebas Ion clan selanjutnya disimpan pada lemari pendingin (5°C) guna
I
memisahkan bagian eudapannya. Bagian yang jemih digumpalkan, dicuci d a r ~
dikeringbekukan kembali.
/i.
Larutan bubuk KPG, difraksinasi dengan ultrafiltrasi membran pa& W C OI
tertentu (1.000.000
Da,
300.000Da,
100.000 Da clan 10.000 Da), sehinggadiperoleh fraksi dengan interval berat molekul tertentu.
Untuk mernprediksi peluang penerapannya, maka dilakukan analisis sifat reologi.
Parameter yang dipergunabn dalam analisis reologi adalah: Pengaruh laju
geser,
pH, penambahan mineral, pembekuan, pemanasan techadap kekentalan
terukumya serta perbandinom kekentalan tersebut d m g w lamtan hidrokoloid
,
k~mersial pada konsentrasi y a w sama.81 Untuk mempelajari sifat gelasi, maka dilakukan a d i s i s kekuatan pecah, titik pecah dan sineresis gel hasil sinergisme KPG dengan hidrokoloid komersial.
91 Untuk mendapatkan informasi struktur KPG, dilakukan hidrolisis asam, I
(
netralisasi dan d i s i s HPLC.Komponen pembentuk gel cincau hljau diduga suatu potisakarida yaitu pektin
~ r m e t o k s i rendah (LMP) dengan berat molekul berkisar sampai 500.000 dalton,
TINJAUAN PUSTAKA
~ R O K O L O E D
Hidrokoloid damiah asal tanaman sudah lama dipergunakan sebagai bahan
+*wan pda pngolahan makanan (Meer, 1977). Berdasarkan komponen
hnyusunnya, sebagian besar hidrokoloid mempakan polisakarida (Walter, 1991).
ang &pat meningkatkan kekentalan larutan dan membentuk gel (Glicksman, 1969).
'drokoloid tergolong senyawa yang relatif sulit dicema (Jenkin d m Jenkin, 1985;
b
dtrobe~ dkk., 1986), namun di dalam pengolahan pangan senyawa ini digunakan
&tuk memodifikasi t e b r suafv p d u k pangftn (Monis, 1979; Niwa dkk., 1988). kenaberhubungan ciengan tingkat penerirnaan k m u m e n (Fardiaz, 1989; Chung
Lee, 1990).
I
Hidrokoloid terdistribusi secara luas di daIarn tanaman terutarna sebagai
+mponen penyusun dinding sel dan lamela tengah (Pantatico, 1981) serta penyusun
s 1 merismatik (Pomeranz, 1991), dimana kandungan hidrokoloid sangat tergantung
I
4 r i umur, jenin dan kondisi tanaman (Walter, 1991).
I
Sarnpai saat ini telah d i k e d berbagai jenis hidrokoloid (Pomeranz, 1991).
B/erdasarkan sumbe. asalnyn. hidrok01oid dikelompokkan menjadi kelompok getah
dperti gom arab, karaya, gom gati clan traga*an. gom asal biji-bijian yang meliputi;
gbm guar, gom biji lolcus, p i ; ekstrak rumput law seperti agar-agar, slginat,
k
i.
ragenan, I^urselaran, ekstrak tanaman darat seperti pektin; ehtrak hewan yang +lipufi gelatin, Laseinat sedangkan gom hasil fumentasi wped gom xantan,Hidrokoioid juga dlkelompokkan berdasarkan sifat kimianya menjadi bidrokoloid anionik dan non anionik. Kelompok hidrokoloid anionik meliputi
kolongan gom anionik ekstrak rumput laut, anionik eksudat, anionik biji dan anionik
basis fermentasi rnikroorganisme (Meer, 1977). Berdasarkan komponen mononernya
'pidrokoloid digolongkan menjadi hidrokoloid yang tersusun oleh heksosa, pentosa
q
b
asam uronat (Bell, 1989). Disamping itu, hidrokoloid juga dikelompokkanNenjadi hidmkoloid dengan gugus fimgslonal karboksil, ester sulfat, h i b k s i l dan
dster metil (Moms, 1979). Berdasarkan konfonnasinya, hidrokoloid dikelompkkan
rhenjadi hidrokotoid yang menghasilkan konfonnasi heliks, pita,
dan
kotak telur(bimmerman, 1979).
1
Hidrokoloid dibedakan menjadi hidrokoloid tradisiomldan
hidrokoloidqomersial. Hidrokoloid tradisional sudah biasa dikonsumsi oleh masyardat pada
s b t u daerah tertentu, namun keterbatasan informasi sifat
dasar
menyebabkaa p)enggunaan hidrokoloid tersebut menjadi sangat terbatas. Beberapa contohYidrokoioid tradisional adalah Premna oblongrfol~a Men (Untoro, 1985), Cyclea
bbbata L. Miers (K-iati dkk., 1999) d m Mesona palwtr~s B L (Asyar. 1989; Nuraint, 1994; Hasbulah dart Fardiaz, 1998).
Hidrokoloid komersial berasal
dan:
hidrokoloid tradisional yang diolah menjadiabitif makanan, karena sifat dasar hidrokoloid tersebut telah diketahui (Pomeranz.
189 1). H~drokoloid komersial yang sudah dipergunakan sebagai campuran makanan a#alah alginat, karagenan, pektin, gom xantan, gom biji lokus, gom arab,
1 Pomeranz (
199 1 ) menggolongkan hidrokoloid menjadi homopolisakarida yang terdiridari rangkaian p f a sejenis dan heteropolisakarida yang ter&ri dari rangkajan gula
yang beragam. Perbedaan jenis gula bukan saja memberikan kontribusi terhadap
geometn akhir, tetapi berpengaruh terhadap berat molekul (BM) dan sifat
fungslonalnya (Meer, 1977; Birch, 1984; Barbut dan Foegeding, 1993; Turquois clan
plena, 2000).
Menurut Morris (1 979). ada empat stnrktw dasar yang membentuk konformasi
bdrokolold, yaitu; struktur primer, sekunder, tersier d m m m e r . Struktur primer
berupakan r a n g b a n utama yang tersusun oleh satu atau beberap jenis gda, struktur
Sekunder terbentuk karena adanya rantai samping
dan
ikatan antar gula, strukturjersier terjadi karena ikatan kovaler., sementara struktur quarterner terbentuk karena
Fanya ikatan antar rangkaian polimer.
Struktur primer dipelajari melalui i d e n t i h i jenis gula hasil hidrolisis, struktur
$ekunder dismati d m hldrolisis parsial melalui deteksi oligosakarida, struktuF tersier
biasanya hpelajari dari pengbambatan kompetitif dengan EDTA
dan
strukturTuarterner d~pelajan dengan mengevaluasi sifat tekstur gel yang dihasilkan dari
jnteraksi dengan hidrokolotd lain.
Menurut Moms (19911, struktur primer berkaitan &ngan kekuatan gel
dan
l$erkura.ngnya gugus fungs~ aktif di bagian aksial dapat menyebabkan fleksibilitas gel
eenmgkat (Rees, 1971), sedangkan struktur sekunder berkaitan dengan rigiditas gel,
dimzna jenis ikatan antar gula seperti ikatan a(1-4) akan menghasilkan kekuatan gel
$ang berbeda dengan lkatan a ( l d ) , karena daiam rangkaian panjang konformzsi yang
Struktur tersier menghasilkan model pita yang dijumpai pada selulosa, pita
panda pada karagenan (Anderson dkk., 1969, Moms, 1991), heliks ganda pada
Cgarosa (Arnott dkk., 1974), heliks rangkap tiga pada curdlan, kotak telur pada
Uginat (Grant dkk., 1973; Moms dkk., 1978), 3 dimensi pada protein (Xu dkk.,
1997). Struktur kuarterner terbentuk karena sinergisme hidrokoloid (Dea, 1979).
Reologi menjadi pertimbangan penting dalam penerapan hidrokoloid sebagai pampuran bahan makanan, karena interaksi hidrokoloid dengan komponen lain dapat
bempengitruhi kualitas produk pangan yang bersangkutm- (Sanford das Baird, 1993).
bntuk memprediksi peluang penerapan hidrokoloid di dalam industri pangan
blpergunakan pendekatan model reologa (Glicksman, 1969; Holdsworth, 1993). Model reologi tersebut diperoleh dengan mempelajari pengaruh laju geser, pengaruh
konsentrasi, suhu dan pH (Hariyadi dkk., 1998). Parameter umum yang dipergunakan
h t u k mengevaluasi sifat reologi larutan hidrokoloid adaIah parameter kekentalan
((Mitchell, 1979; Toledo, 1991). Menurut D~ckinson dan Pawlowsky (1996) kekentalan larutan h~drokoloid sangat dlpengaruhi oleh berat molekul, unit dasar,
pH, suhu dan laju geser yang diterapkan.
Berdasarkan karakteristik reologinya, fluida dibedakan menjadi fluida
bewtoman dan fl~uda non Newtonian. Fluida Newtonian menunjukkan perilaku
popors~onal konstan antara laju geser dengan tegangan geser. Fluida non-Newtonian
ditunjukkan oleh sebagian besar hidrokotoid dengan berat molekul besar, kecuali
engan konsentrasi yang sangat rendah (Holdswoth, 1993). Sampai saat ini telah
k
iketahui ada 5 karakteristik fluida non-Newtonian, khususnya pada larutan bdrokoloid, yaitu pseudoplastik, plastilc binghsm dilatan, tiksotropik dan reopektikpardiaz, 1989).
i
Pada dasamya penambahan hidrokoloid ditujukan untuk meningkatkan sifatb
gsional produk pangan (Fardiaz, 1989; Eaird dan Penitt, 1993). Sifat h g s i o n a l (ersebut re1atif b e r i i antara hidmkoloid satu dengan yang lain (Bell, 1989).Meskipun d e n ~ i k i ~ , sifat utama hidrokoloid adalah meningkatkan kekentalan hedim. air dan sebagian dapat membentuk get Ciitchell, 1979; Moms, 1979).
ungsi hidrokoloid di dalam produk pangan adalah sebagai adesif, pengikat, anti
.staiisasi, penjernih, pengeruh, pelapis, pengemulsi dan pemantap (Dickinson dan
cclements, 1995). Pen~gunaan hidrokoloid
pada
skala industri berkisar antara 0.5-1
2.5% b h (Mitchell. 19791, d m pada Lo-ntrasi tersebut hidrokoloid dapat
~
henstabilkan sistem air di &lam matrik pangan (Sloan, 1994; Tang dkk., 1995).
Sifat fungsional utama dari hidrokoloid yaitu sebagai pengental dirn
P
rnbentuk gel, dapat dievaluasi dengan mengukur kekentalan lamtandan
sifat gelidrokoloid Kekentalan larutan hidrokoloid biasanya dianalisis dengan viskometer,
Ln
gkan sifat geI hidrokoloid dievaiuasi dari kekuatan gel, kekakuan gel, sineresis +ngan menggumkan Stevens LFRA Texture Analyzer (Fry dan Hudson. 1983;i
DAFTAR PUSTAKA
Anderson, D. M. W. 1988. Water food gums and their role in product development, J. Carbohydr. Res. (33). 848-850.
. 1993. Imported ingredients in the Asian market. J. Food Indust. 34-37. JAngaIet, S. A. 1986. Evaluation of the voland-stevens LFRA texture analyzer for
measuring the strength of pectin sugar jellies. J. Text. Stud. (1 1). 87- 96
Wnott, S., Fulmer, A., Scott, W. E., Dea, I. G. M. Moorhouse, R. dan Rees, D. A.
1974. Food fcom gels. J. Mol. Bid. 90, 269-284.
JAsyru, C. 1988. Isolasi dan Karskterisasi Komponen Pembentuk Gel dari Cincau Hitam (Mesonapol2lsfris B. L.). Skripsi, Fateta-PB, Bogor.
Paird, J. K. dan D. J., Pettitt. 1993. Biogum used in food made by fermentation. Di &lam Golberg. editor. Biotechnology and Food Ingredient. Van
I Nortrand Reinhold. New York.
barblit, S. dan E. A, Foegeding. 1993.
ca2+
induced gelation of preheated whey protein isolate. J. Food Sci. 58 (4). 867- 869.I
bell, A. E. 1989. Gel Structure and Food Biopolymer. Reading Univ. 251-273.
birch, G. G. 1984. Analysis of food carbohydrate. Elsevier Appl. Sci. Pub.London.
@PS) Biro Pusat Statistik Indonesia. 1998. Statistik Ekspor Impor Indonesia; Statistik Perdagangan Luar Negeri Indonesia, Jakarta.
ehristensen, B. E. 1989. The role of extracellular polysaccharides in biofilm. J Biotechnol. (10) 181-202.
@hung, K. H. dan C. M., Lee. 1990. Relationship bemeen physicochemical properties of non fish protein and textural properties of protein incorporated surimi gel. 3. Food Sci. 55 (4) 972-988.
eross, H. L dan M. W., Kearsley. 1989. Carbohydrate-iron interactions. Di h i a m Birch G. G.
d m
M. G. Lindley. editor. Interactions of Food Components. Elsevier Appl. Sci. Pub. London dan New York.Dickinson, E. dan D. J., McClements. 1996. Advances in Food Colloids. Blackie A d . and Professional, Western Cledens, Glaslow.
.
dan D., Pawlowsky. 1995. Effect of high pressure treatment of protein on the rheology of floculated emulsions containing protein and polysaccharide. J. Agric. Food Chem. (44) 2992-3000.Fardiaz, D. 1989. Hidrokoloid. Laboratorium Kimia d m Biokimia Pangan. Pusat Antar Universitas Pangan dan Gizi. lPB, Bogor.
.
dan E., Wahab.
1985. The effect of types of starch on gelling properties of black cincau. Proceding Seminar on Food Tech. Nutr. Yogyakarta.(Fry,
J. C . dan J.B.,
Hudson. 1983. Development of a Psnetrometer Test of the Gel,Research report. The Britania Food Mimutirc. Indust. Res. Assoc.
wicksman, M. 1969. Gom Technology in the
F
d
Industry, b a d . Press, New YorkGlilicksman, M. 1979. Gelling Hidrocolloids in Food Product Aplications. Tat-tytown, New York.
Graham, H. D.
dan
C. G., Horace. 1977. Analyticalmethods
for major plantI
hydrocolloids. DJ datum Dickinson, E. editor. Food Colioids. The Avi Pub. Corn. Inc. West Port, Connecticut. 540- 579.
&ant, G. T., Morris, R., Rees, D. A., Smith, P. J . C. dan D., Thom. 1973. Bioiogycd interaction between po!ysaccharides and divalent cations; The egg-box model. FEBS Letter, 32: 195.
eegoxy, D. J. H. 1986. The Functional properties of pectins in various food systems. Elsevier Appl. Sci. Pub. London. 210-225.
qariyadi, P. Lilis, N. dan H. P., Eko. 1998. Karakterisasi sfat rologi bogum Enterobacrer agIomrans
N.
Risalah paper sminar PATPI. Yogyakarta.E$asbullah, R. dan D., Fardiaz. 1998. Pengembangan proses instanisasi bubuk cincau hitam. PKPT, Lembaga Penelitian, IPB-Bogor.
I-doldsworth, S. D. 1993. Rheological models used for the prediction of the flow properties of food products. J. Trans. ChemE, 71 ( c ) t 39
-
171.Kumiati, I. 1999. Mempelajari Pengaruh pH, Penambahan MnCh dan CMC terhadap Karakteristik Gel Cincau Hijau (Cyclea barbata L. Miers), Slaipsi. Fakultas Teknologi Pertanian.
PB,
Bogor.&urniawan, 0. 1999. Mempelajari Pengaruh pH, Penambahan FeS04 dan Xantan Gom terhadap Karakteristik Gel Cincau Hijau (Cyclea barbata L. Miers), Skripsi, Fakultas Teknologi Pertanian. IPB, Bogor.
Meer, W. A. 1977. Plant Hydrocolloids. The Avi Publishing Company, Inc. West Port, Connecticut. 540-579.
Mei, I. F., Laye, I., Karleskind, D.
dan
C. V. Morr. Gelation of calcium reduced and lipid reduced whey protein concentrates as affected by total and ionic mineral concentrations. J. Food Sci. 61 (5) 899-904.$litchell. 1. R. 1979. Rheology of Polysaccharide Solutions and Gels. Butterworth. London. 51-138.
*orris, E. R. 1979. Polysaccharide structure and conformation in solutions and gels. Unilever Res. London. 15-50.
$amtion, R., I. 1999. Mempelajari Pengaruh pH, Penambahan NaCl dan C5m Arab terhadap Karakteristik Gel Cincau Hijau (Cyclea barbafa L. Miers), Skripsi, Fakultas Teknologi Pertanian. IPB, Bogor.
I#ielsen, R. G. dan G. M., Pigott. 1994. Gel strength increased in low-grade heat-set surirni with blended phosphates. J. Food Sci. 59 (2). 246-250.
qiwa , E., Wang, T. T., Kanoh, S. dan T., Nakayama 1988. Contribution of gelling substance to muscular protein network structure with in karnaboko. Nippon Suisan Gakaishi. (540). 989-992.
#uraini, D. 1994. Pengaruh Hidrokoloid terhadap Pernbentukan Gel Cincau Hitarn (Mesona palustris B. L.) Tesis. Program Pasca Sarjana.
LPB,
Bogor.dantastico, E. B. 1993. Postharvest Physiology, Handling and Utilization of Tropical and Sub Tropical Fruits and Vegetables. The Avi. Publ. Corn. Inc. Connecticut.
F/omeranz, Y. 1991. Functional Properties of Food Components. Academic Press, I Inc. New York.
1 Rees, D. A 1977. Polysaccharide gels. A Molecule view. Chem. Ind 630-636.
1
Rendeman, A. J. 1986. Carbohyrirate-mined complexes in foodDi
d~/a?i: Birch, G.G. dan M. G., Lindley. editor. Interactions of Food Components. Elsevier Appl. Sci. Pub. London dan New York.
.
1982. Polysaccharides conformation in solutionand
gels-recent results on pectins. J. (khohidr. Polym. (2) 254-263.., Moms, E. R., Thom, D. dan J. K., hhkkn 1982. Shapes and interaction of' carbohydrate chains. DI dalarn Aspinall., editor. Polysaccharides. Ac. Press, New York. 195-290.
Sandsnon, G. R. 1990. Gellan gom.
Di
aalam Food Gels. Harris, P(zd).
Elsevier Science Publ.T,td.,
New York. 201-230.Sanford, P. A. 1979. Exocelluler microbial plysaccharides.
Di
d a I m n Tipson R. S.clan D. Horton., editor.
Advances
in Carbohydrate Chemistry andBioshemistry.
Ac.
Press. New York. 265-3 13.I
.
dan J. K., B a a 1993. Industrial utilktion of polysaccharides,new product and their commercial applications. J. Pure Appl. Chem. 56 (7). 879-892.
bloan, A. E., Anderson, I. L. 5., Gedsdalen, H, Larsen, B.
dan
T.,
Painter. 1980. The top ten trend in United States. J. Food Technol. 48 (7) 89-100.bmidsrod, O., Anderson, I. L., Geddalen, H J., Larsen, B.
dan
T.,
Painter. 1980. Evidence for a salt promoted fieeze-out on linkage conformation in carrageenans. J. Carbohydr. Res. (8) 11-15.Fumarti, L. 1999. Mempelajari Pengaruh pH, Penambahan MgCh dan Metil Selulosa terhadap Karakteristik GeI Cincau Hijau (Cyclea barbata L. Mien), Skripsi, Fahltas Teknologi Pertmian. IPB, Bogor.
eutherland, I. W. dan G.H., Elwood., 1972. Microbial exopolysacchatides. Potential Process Biochem. 7 : 27-30.
tang, J., Mariva, A.T. clan Y., Zeng. 1995. Mechanical properties of gellan gels in relation to divalent cations. J. Food Sci. 60 (4) 748-752.
Turquois, T dan H., Gloria 2000. Determination of absolute molecular weight averages and molecular weight distributions of dginate used a s ice cream stabilizers by using mdtiangle laser light scaterring measurements. J. Agric. Food Chem. (48) 5455545%.
bntoro, A. 1985. Mempelajari Beberapa Sifat Dasar dalam Pembentukan Gel dari Cincau Hijau (Prema oblongifolia, Merr). Skripsi FakuItas Telcnologi Pertanian. IPB, Bogor.
baker, R. H. 1991. The Chemistry and Technology cf Pectin. Academic Press, Inc.
San
Diego, California 92 10 1 .Xu.
J, Shimoyamada, M dan K., Watacabe. 1997. Gelation of egg white protein as affected by combined heating and freezing, J. Food Sci. (5) 963-966. kixntn-ann R. 1979. Die fi~nktionellen eigenschaften der kohlenhydrate.DAN KARAKTERlSASI KOMPONEN
EMBENTUK GEL DARI DAUN TANAMAN
CZNCAU
L. Niiers)
lation, Fractionation and Characterization of Gel Forming Components btained from Leaves of Cyclea barbafa L. Miers Plant
t
Isolation of the gel forming components (GFC) from Cyclea barbata L. Miers 1 aves was canied out by extraction using 0.028 M EDT-4 solution, pH 2.5, at 90°C
r 30 min. The yield of GFC after freeze-drying was 0.89-1 89 g from 50 g Cyclea arbatu L. Miers leaves. Fractionation of 0.25 % GFC solution using ultrafiltration, howed that fraction 1 3 containing GFC with M W of 1,000,000-2,000,000 Da had
e highest yield (52OA), followed by fraction F3 with MW of 300,000-500,000 Da ( 6%) and fracuon F 0.6 with MW of 100,000-10,000 Da (8%).
I
Acid hydrolysis of GFC was used to investigate the composition of its simple gars Acid hydrolysis laas conducted with hydrochloric acid, and than the drolysates were analyzed for their sugar composition usingHPLC
with Aminex%
X-87H ion exchange column. The results showedthat
GFC and its fractions Cpmposed ~f the same simple sugars, i. e. galacturonic acid and galactose.Hey
word : Gel f m i n g components (GFC). Acid ~ d y s i s , GaIrscturcmic acidand Galactose.DI dalam tanaman sebagian besar hidrokobid bet-interaksi dengan komponen
Iz/in pembentuk sbuktur jaringan (Hespell, 1998; Southgate, 199 1 ; Maede dkk., 1994;
S/tark dan Zecharia, 1994). Dengan demikian, pemisahan hidrokoloid dari komponen
tqrsebut memerlukan langkah sistematis seperti ekstraksi, filtrasi, sentrifusi,
&nggumpalan dan pengeringan. Keberhasilan pernisahan suatu komponen tergantung d h konsentrasi, sifat fisiko-lnmia d m tingkat kernmian yang ingin dicapai (Smith
Konsentrasi hidrokoloid &lam tanaman diperkirakan berkisar antara 2.5%
Sampai 5% clan total berat kenngnya (Christensen, 1973; Walter, 1991), oleh karena itu dibutuhkan metode ekstraksi yang memadgi untuk memperoleh hasil yang baik
ombo bouts
dan Thabault, 1986). Agar-agar, karagenan, b l a r a n ,dan
alpnat dapat&ekstrak dengan larutan alkali (Glicksman, 1979; Hespell, 1998), pektin diekstrak
&dam kondisi asam (Christensen, 1973; Walter, 1991; Bruneton, 1999), selulosa
dengan larutan NaOH 17.5 %. sedangkan lignin dengan asam sulfat 2% (Southgate,
1991). Larutan EDTA 2% dapat dipergunakan untuk rnengisolasi selulosa g d a bit
&m larutan EDTA 0.5 % dapat dipergurdcan wtuk mengisolasi pektin (Wen
dkk,
1988; Southgate, 1991; Haryadi, 1991; Companion, 1991; Hespell, 1998; B-eton,
1999).
Menurut Phatak dkk (1988) salah satu f w r yang
harus
diperhatikan dalamibolasi hidrokoloid adalah pH. Penurunan pH dapat menyebabkan gugus aktif
didrokoloid mengalami protonasi sehingga menjadi reaktif
dan
gaya tolakdlektrostatiknya &an semakin besar untuk rnenggerakkan mtai-rantai hidrokoloid.
@isis1 yang lain, penunman pH juga menyebabkan ionisasi logam yang mempw-yai
t+ndensl untuk bereaksi dengan gugus aktif hidrokoloid Oleh karena ~ t u , untuk
*emisahkan hidrokoloid maka reaksi tersebut perlu dikendalikan sedini mungkin
&ngan menambahkan pengkelat logam seperti EDTA (Haxyadi, 1991), dengan
$wapan agar hidrokoloid lebih mudah dipisahkan dari komponen yang fain (Birch
&
Lindley, 1986, Yalpani dan Sanford, 1987).Menurut Christensen (1973), suhu dapat lpergunakan untuk memacu proses
selama 15 menit, sedangkan ekstraksi hidrokofoid dari rumput !aut seperti alginat,
karagenan, agar-agar dan furselaran dilakukan pada suhu 100CC dalam suasana basa
(Glicksman, 1969; Walter 198 1).
Sebagian besar hidrokoloid mempunyai distribusi berat molekul dengan rentang luas, oleh karenanya untuk mempelajari sifat-sifat dasar hidrokoloid tersebut
perlu dilakukm ffaksinasi (Houghton dan Raman, 1998). Fraksinasi bertujuan mtuk
pnemisahkan komponen berdasarkan ukuran molekul, muatan. bentuk, polaritas
tmaupun volatilitas. Fraksinasi dengan cam ultrafiltrasi &pat &per-nunakan untuk tnemisahkan suatu komponen berdasarkan berat molekulnya, dan proses tersebut
ldilalcukan pa& suhu rendah @rock, 1983; Bruneton, 1999).
Ada beberap faktor yang perlu dipertimbangkan seiama fhlcsinasi, yakni pH
ban
konsentrasi larutan hidrokoloid yang akan difraksinasi. Pada pH rendah (2.5-2.8)*ri-pori membran akan cepat tersumbat, karena gugus fungsional yang terprotonasi
# a p t berinteraksi dengan sisi aktif membran yang menyebabkan penyumbatan pada p i - p o r i membran (h4acrae dkk., 1993). Efisiensi fraksinasi juga dipengaruhi oleh
konsentrasi (Chen dkk., 1998). semakin tinggi konsentrasi hidrokoloid yang
akan
aipisahkan, maka pori-pori membran akan sernakin cepat tersumbat. Setyantngsih
(1998) berhasil melakukan fraksinasi peptida filtrat moromi dengan ultrafiltrasi
inembran menjadi fraksi den- berat moiekul antara 3000 Da-10.000 Da, d m antara
$00 Da-3000 Da, oleh karena itu fraksinasi larutan KPG juga dilakukan dengan
$emodifikasi kondrsi dari metode tersebut.
Sebagian besar hidrokoloid tersusun oleh unit monomer berbeda, sehingga
hidrokoloid yang dihasilkan (Morris, 1979; Pomeranz, 1991). Struktur suatu
bidrokoloid tergantung dari jenis *la penyusunnya (Bell, 1989). Sdah satu
pndekatan yang mungkin dilaksanakan untuk mempelajari struktur suatu
bdrokoloid, adalah dengan melakukan hidrolisis komponen tersebut (Nollet, 1990).
Hidrolisis hidrokoloid untuk mendapatkan unit penyusunnya dapat diiakukan
$ecara enzimatis ataupun hidrolisis asam (Bellitz d m Grosh, 1999). Hidrolisis enzim
biasanya dilakukan apabila jenis polimer hidrokoloid telah diketahui (Graham, 1979;
$ay!or dan Folkes, 1992). Apabila stdctcrnya belum diketahui maka dapat dilakukan qdrolisis asam (Southgate, 1991; Waiter, 1991; Hougth~n dan Raman, 1998).
Dalam reaksi hidrolisis yang seimbang, ti& semua polisakarida diubah
Wenjadi gula sederhana (Scott, 1990). namun sebagian diubah menjadi disakarida
+au oligosakarida (Nielsen, 1998). Hidrolisis asam biasanya berlangsung secara
ajcak, dan pemutusan ikatan glikosidik tidak teratur sehingga hasilnya akan sulit
qprediksi (Helmy dan El-Motagali, 1992). Apabila reaksi hidrolisis sulit dikontrol,
+aka akan te jadi enolisasi yang melepskan molekul air (Belitz dan Grosch, 1999),
s+hingga akan dihasilkan prodl~k dehidrasi gula seperti; fu-, firan, fixaidehid
qaupun furanon (Feather, 1972; Souleymane dan Croyset, 1982; Weenen, 1998)
.
Dalam analisis &a, pemilihan metode analisis selalu dijadikan pertimbangan
&ntmg (Graham, 1979; Southgate, 1991; Taylor dan Folkes, 1992), karena setiap
4etode anaIisis mempunyai keterbatasan dalam haI deteksi (Nollet, 1990). Menurut ~ / i n d e r (1980) dan Scott (1990) deteksi gula sederhana biasanya dilakukan dengan
wmatografi k ~ n e j a tinggi, dan detektor yang diperguna.kan biasanya addah detektor ~qkleks bias (Taylor dan Folkes, 1992) Prinsip dasar dari detektoi ini adalah
$erbedaan indeks bias kornponen dalam larutan dengan fase gerak yang dipergunakan
@ i s h a n dkk., 1984, Hicks dkk., 1985; Schols dkk.. 1989; Macrae, 1992; Hernaneez
Qkk.,
1994; Primer, 1996).Menurut Black clan Bagley (1978), pelarut yang banyak dipergunakan daIam
*alisis @a sederhana adalah campwan asetonitril : air. Perbandingan tersebut relatif
qervariasi d m tergantung dari sampel yang dianalisa, seperti d i s a gula kedeIe
c$pergunakan perbandingan 3 : 1, sedangkan pada analisis
sirup
jagung perbandingan &ng dianggap baik adalah 62 : 38 (Taylor dan Folkes, 1992).Tujuan dari penelitian ini adalah (1) untuk mendapatkan fraksi-fiaksi KPG,
BAHAN DAN METOIiE PENELITIAN
Daun Cincau
Daun cincau diperoleh dari Desa Renon, Denpasar-Bali, daun dipetik jam
17" WZB waktu setempat. Pemetikan &UIII cincau dimulai pada daun kelima dari
pucuk kearah pangkat, yaitu masing-masing sebanyak 10 Iembar, d m dalam sekali
pemetikan d a m yang diperoleh sekitar 10 k g Daun cincau yang dipilih adalah daun
berukuran sedang, unh& dibungkus den- pelepah batang psang masing-masing
berisi 250 g perkemasan. Kemasan tersebut dimasukkan kedalam lardus beiulcuran
bedang mtuk selanjutnya dikirirn ke Bogor. S o m i - dilakukan kembali berdasarkan dam bmjang 8-9 cm, lebar 7-8 cm) untuk kemudian dikemas keinbali dan
@isimpan didalam lemvi pendiagin selama 10 hari.
@l Cincau
Dam cincau segar ditimbang sebanyak 50 g, kernudian diremas selama 10
&enit dalam 900 ml air bebas ion sampai cairan menjadi kentai, kemudian disaring
bengan kain kasa sambil diperas dengan tangan sehingga bagian cairamya t e r p i d
bagian ampas. Sebanyak 800 ml cairan kentaf yang diperoleh, masing-masing
Ftambahkan garam mineral sesuai perlakuan sambil &ad& perlahan, yaitu 2.5
rn
+ol MnCIz (Kumiati, 19991, 0.5 mmol CaCL2 (EMmyu, 1999), 10 mmol MgC12
Q~umarti, 1999). 7.5 mmol NaCl (Nasution, I999), 2 mmol FeS04 M (Kurniawan,
4999). Setelah penambahan larutan garam mineral maka pH larutan diatur 4.0. 5.0, I
buah cetakan paralon berukuran tinggi 1 inci, diameter 2 inci yang diberi alas plastik,
kemudian disimpan pada lemari es (*5"C) selama 48 jem untuk selanjutnya diIakukan
analisis berat clan kadar air (Apriyantono w 1 9 8 9 ) .
Isolasi KPG
Gel yang diperoleh dari setiap kali percobaan (1 1 cctakan gel) dihancukan
4engan blender sambil ditambah 100 ml lanitan EDTA 0.028 M, Ialu dipanaskan
90°C
selama 15 mznit. Setelah dingin larutan tersebut disaring dengan menggunakan &ain kasa. Ekstrak didinginkan dalam lemari pendingin selama 5 jam, kemudianVagian jernih larutan dipisahkan dari hgian yang mengendap. Sagian supematan
pang diperoleh (* sebmyak 800 ml) diendapkan dengan eta1101 95% pada rasio
volume (3: 1) sehingga KPG akan menggumpal. Gumpalan KPG dipisahkan dengan
&nyaringan, sedangkan cairan yang lolos saringan disentriksi pada kecepatan 3000
q r n selama 15 menit. KPO hasil sentrifusi dikunzpulkan bersarna KPG