PENGARUH KONSENTRASI SURFAKTAN LINEAR
ALKYLBENZENE SULPHONATE TERHADAP TEGANGAN
ANTARMUKA DAN VISKOSITAS SISTEM
AIR-MINYAK TANAH
SKRIPSI
SRI MEGA WATI
050802015
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENGARUH KONSENTRASI SURFAKTAN LINEAR ALKYLBENZENE
SULPHONATE TERHADAP TEGANGAN ANTARMUKA DAN VISKOSITAS
SISTEM AIR-MINYAK TANAH
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
SRI MEGA WATI
050802015
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH KONSENTRASI SURFAKTAN
LINEAR ALKYLBENZENE SULPHONATE
TERHADAP TEGANGAN ANTARMUKA DAN VISKOSITAS SISTEM AIR-MINYAK TANAH
Kategori : SKRIPSI
Nama : SRI MEGA WATI
Nim : 050802015
Program studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Januari 2012
Komisi Pembimbing :
Pembimbing II, Pembimbing I,
Drs. Amir Hamzah Siregar, M.Si Drs. Darwin Yunus Nasution, M.S
NIP. 196106141991031002 NIP. 195508101981031006
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENGARUH KONSENTRASI SURFAKTAN LINEAR ALKYLBENZENE
SULPHONATE TERHADAP TEGANGAN ANTARMUKA DAN VISKOSITAS
SISTEM AIR-MINYAK TANAH
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2012
SRI MEGA WATI
050802015
PENGHARGAAN
Bismillahirrahmanirrahim
Puji syukur kehadirat Allah SWT yang telah melimpahkan Rahmat dan Karunia-Nya sehingga penulis mampu menyelesaikan penelitian dan penulisan skripsi ini sebagai salah satu syarat untuk mendapatkan gelar Sarjana Sains pada jurusan Kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam Universias Sumatera Utara.
Keberhasilan dari penulisan skripsi ini tidak terlepas dari bantuan berbagai pihak yang terlibat secara langsung maupun tidak langsung dan telah memberikan dukungan baik secara moril maupun materil. Untuk itu penulis menyampaikan penghargaan dan cinta kasih yang terdalam buat Ibunda Harisah Nasution yang selalu mendoakan, memberi perhatian, dan menjadikan inspirasi di setiap langkah hidup saya. Serta abangda Obob beserta istri dan pangeran kecil Rahmansyah yang selalu mendukung saya dalam suka dan duka. Tak lupa pula suamiku terkasih yang selalu menyemangati dan mendukung setiap langkah yang saya ambil.
Dengan segala kerendahan hati tidak lupa saya ucapkan terima kasih yang sebesar-besarnya kepada :
Bapak Dr. Darwin Yunus Nasution, MS selaku dosen pembimbing I dan Bapak Drs. Amir Hamzah Siregar, M.Si selaku dosen pembimbing II yang telah dengan sabar meluangkan waktu, tenaga, dan pikirannya serta memberikan masukan, saran, dan petunjuk kepada penulis dalam melakukan penelitian dan penyusunan skripsi ini. Ibu DR. Rumondang Bulan. Nst, MS dan Bapak Drs. Albert Pasaribu, M.Sc selaku ketua dan skretaris jurusan Kimia FMIPA-USU, serta seluruh staff pegawai Departemen Kimia.Bapak dan Ibu dosen yang telah membagikan ilmunya kepada saya selama studi. Dan tak lupa saya menyampaikan penghargaan kepada kepala laboratorium Kimia Fisika dan Kimia Polimer, staff, serta seluruh rekan asisten, Misbah, Mail, Destia, Rafika, Wulan, Tisna, Wimpy, Rudnin, dan Rinna yang telah memberi semangat dan kerjasama yang baik selama ini. Teman satu bimbingan yang mendorong saya untuk lebih baik lagi. Teman-teman stambuk 2005 yang selalu memberikan dukungan dan semangat walaupun telah lebih dulu meninggalkan kampus tercinta ini. Hanya Allah yang dapat membalas segala kebaikan yang telah kalian berikan kepada penulis. Penulis berharap Allah memberikan Berkah-Nya berlipat ganda kepada kalian, amin ya Rabbalalamin
ABSTRAK
Pengaruh konsentrasi surfaktan Linear Alkylbenzene Sulphonate(LAS) terhadap tegangan antarmuka dan viskositas sistem air-minyak tanah telah dilakukan. Variasi konsentrasi surfaktan LAS adalah 0,25%;0,5%;1,0%;1,5% dan 2,0% v/v dengan laju pengadukan 800 rpm
pada suhu kamar(30oC). Nilai densitas ditentukan menggunakan piknometer, nilai tegangan
THE EFFECT OF LAS SURFACTANT CONCENTRATION TO THE INTERFACIAL TENSION AND VISCOSITY OF WATER-KEROSENE SYSTEM
ABSTRACT
The effect of Linear Alkylbenzene Sulphonate LAS surfactant to the interfacial tension and viscosity of water-kerosene system have been perfomed. Variation of LAS surfactant concentration was 0.25%;0.5%;1.0%;1.5% and 2.0% v/v with stirring speed 800 rpm at room
temperature (30oC). Density value was determined by using picnometer, interfacial tension
DAFTAR ISI
2.3.2. Faktor-Faktor yang Mempengaruhi Tegangan Permukaan 12
2.3.3. Metode Penentuan Tegangan Permukaan 13
2.3.4. Metode Cincin Du Nouy 14
2.4. Viskositas 15
2.4.1. Faktor-Faktor yang Mempengaruhi Viskositas 16
2.4.2. Metode Penentuan Viskositas dengan Viskometer Ostwald 17
3.3.2.1. Perhitungan Nilai Densitas dari Sistem Air-Minyak
Tanah 23
3.3.3.2. Perhitungan Nilai Tegangan Antarmuka Sampel 23
3.3.3.3. Perhitungan Nilai Viskositas Sampel 24
3.3.3.3. Analisis Variansi 24
3.4. Skema Pengambilan Data 26
3.4.1. Pembuatan Sistem Air-Minyak Tanah 26
3.4.2. Pengukuran Densitas 26
3.4.3. Pengukuran Tegangan Antarmuka 27
3.4.4. Pengukuran Viskositas 27
BAB 4 HASIL DAN PEMBAHASAN
4.1. Hasil 28
4.2. Pembahasan 29
BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan 32
5.2. Saran 32
DAFTAR PUSTAKA 33
DAFTAR TABEL
Halaman
Tabel 2.1. Perubahan tegangan permukaan oleh konsentrasi surfaktan 7
Tabel 2.2 Tegangan permukaan cairan 10
DAFTAR GAMBAR
Halaman
Gambar 2.1. Pori batuan 1
Gambar 2.2. Struktur Linear alkylbenzene sulphonate 8
Gambar 2.3. Kerja adhesi dan kohesi 12
Gambar 4.1. Grafik hubungan konsentrasi terhadap tegangan antarmuka sistem
air-minyak tanah 29
Gambar 4.2. Grafik hubungan konsentrasi terhadap viskositas sistem air-minyak
DAFTAR LAMPIRAN
Halaman
1. Lampiran I. Hasil Pengukuran Tegangan Antarmuka Sistem Air-Minyak Tanah dengan Variasi Konsentrasi LAS 33 2. Lampiran II. Hasil Pengukuran Densitas Lapisan Atas dan Lapisan Bawah
Sistem Air-Minyak Tanah dengan Variasi Konsentrasi LAS 33 3. Lampiran III. Hasil Perhitungan Tegangan Antarmuka Sistem Air-Minyak
Tanah dengan Faktor Koreksi 34 4. Lampiran IV. Data dari Tabel III untuk Perhitungan ANAVA 34 5. Lampiran V. Hasil Perhitungan ANAVA Tabel III 34 6. Lampiran VI. Hasil Pengukuran Densitas Sistem Air-Minyak Tanah dengan
Variasi Konsentrasi LAS 34 7. Lampiran VII. Hasil Pengukuran Waktu Alir Sistem Air-Minyak Tanah dan
DAFTAR SINGKATAN
LAS = Linear alkylbenzene sulphonate
AS = Alkohol sulfonat
AOS = Alpha olefin sulfonat
SAS = Secondary alkana sulfonat
JKT = Jumlah kuadrat total
JKA = Jumlah kuadrat antar kelompok
JKD = Jumlah kuadrat dalam kelompok
RKA = Rata-rata kuadrat antar kelompok
RKD = Rata-rata kuadrat dalam kelompok
cP = Centi Poisse
rpm = Rotary per minute
ABSTRAK
Pengaruh konsentrasi surfaktan Linear Alkylbenzene Sulphonate(LAS) terhadap tegangan antarmuka dan viskositas sistem air-minyak tanah telah dilakukan. Variasi konsentrasi surfaktan LAS adalah 0,25%;0,5%;1,0%;1,5% dan 2,0% v/v dengan laju pengadukan 800 rpm
pada suhu kamar(30oC). Nilai densitas ditentukan menggunakan piknometer, nilai tegangan
THE EFFECT OF LAS SURFACTANT CONCENTRATION TO THE INTERFACIAL TENSION AND VISCOSITY OF WATER-KEROSENE SYSTEM
ABSTRACT
The effect of Linear Alkylbenzene Sulphonate LAS surfactant to the interfacial tension and viscosity of water-kerosene system have been perfomed. Variation of LAS surfactant concentration was 0.25%;0.5%;1.0%;1.5% and 2.0% v/v with stirring speed 800 rpm at room
temperature (30oC). Density value was determined by using picnometer, interfacial tension
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Perlu diketahui bahwa minyak di dalam bumi bukan berupa wadah yang menyerupai
danau, namum berada di dalam pori-pori batuan bercampur bersama air. Reservoar
adalah batuan yang merupakan wadah bagi hidrokarbon untuk berkumpul dari proses
migrasinya. Reservoar ini biasanya adalah batupasir dan batuan karbonat, karena
kedua jenis batu ini memiliki pori yang cukup besar untuk tersimpannya hidrokarbon.
Reservoar sangat penting karena pada batuan inilah minyak bumi di produksi.
Apabila sistem pori-pori batuan dapat dipandang sebagai sistem kapiler yang
terdiri dari badan berpori dan saluran berpori, maka untuk batuan yang basah air,
tekanan yang diperlukan untuk mendorong minyak bumi terlalu besar. Salah satu cara
untuk memperkecil tekanan kapiler adalah dengan menurunkan tegangan antarmuka
dan kekentalan (viskositas) sistem air-minyak bumi.
Adapun bahan kimia yang dapat digunakan untuk menurunkan tegangan
antarmuka sistem air-minyak bumi adalah larutan alkali ataupun surfaktan. Dalam
pemakaiannya larutan alkali dengan variasi antara 0,05N–0,30N membentuk surfaktan
secara alami dengan asam organik dari minyak bumi sebagaimana penelitian terdahulu
oleh Juharuddin Nasution, 1996.
Surfaktan anionik merupakan surfaktan yang paling banyak digunakan dalam
industri detergen dan merupakan salah satu surfaktan yang memiliki peran yang baik
dalam menurunkan tegangan antarmuka sistem minyak-air sebagaimana dilaporkan
Leksono Mucharam, 2007.
Salah satu surfaktan anionik adalah Surfaktan Linear Alkilbenzena Sulfonat
(LAS). Pengaruh Surfaktan Linear Alkylbenzene Sulphonate telah diteliti dalam
Penelitian ini mengevaluasi pengaruh konsentrasi surfaktan Linear
Alkylbenzene Sulphonate (LAS) terhadap tegangan antarmuka dan viskositas sistem
air-minyak tanah.
1.2. Permasalahan
1. Apakah ada pengaruh konsentrasi surfaktan terhadap tegangan antarmuka dan
viskositas dari sistem air-minyak tanah.
1.3. Pembatasan Masalah
Dalam penelitian ini permasalahan dibatasi pada :
1. Minyak tanah yang digunakan diperoleh dari pangkalan minyak tanah di
Jl.S.M.Raja, Medan.
2. Surfaktan yang digunakan adalah surfaktan anionik Linear Alkylbenzene
Sulphonate (LAS).
3. Laju pengadukan 800 rpm
1.4. Tujuan Penelitian
Penelitian ini bertujuan untuk melihat pengaruh antara konsentrasi surfaktan terhadap
tegangan antarmuka dan viskositas sistem air-minyak tanah.
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat digunakan sebagai bahan informasi mengenai aplikasi
surfaktan dalam pengeboran minyak bumi untuk minyak bumi yang tertinggal di
dalam reservoar dengan cara menurunkan tegangan antarmuka dan viskositas sistem
air-minyak bumi.
1.6. Metodologi Penelitian
Penelitian ini bersifat eksperimental laboratorium dengan menggunakan minyak tanah
bersifat homogen yang kemudian diaduk dengan larutan surfaktan dengan berbagai
variasi. Adapun tahapan-tahapannya meliputi :
1. Pembuatan sistem air-minyak tanah
Ditentukan tegangan antarmuka dengan menggunakan tensiometer Du Nouy,
viskositas menggunakan viskometer Ostwald dan densitas dengan
menggunakan piknometer dari sistem air-minyak tanah dengan berbagai
variasi konsetrasi surfaktan.
2. Analisa data dilakukan dengan menggunakan Analisis Variansi (ANAVA)
untuk melihat ada atau tidaknya pengaruh dari penambahan surfaktan terhadap
tegangan antarmuka dan viskositas sistem air-minyak tanah
1.7. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Fisika FMIPA USU dan Laboratorium
BAB 2
TINJAUAN PUSTAKA
2.1. Pembentukan Minyak Bumi
Minyak bumi (bahasa Inggris: petroleum, dari bahasa Latin: petrus ), dijuluki juga
sebagai emas hitam adalah cairan kental, coklat gelap, atau kehijauan yang mudah
terbakar, yang berada di lapisan atas dari beberapa area di kerak bumi. Minyak bumi
dan gas alam berasal dari jasad renik lautan, tumbuhan dan hewan yang mati sekitar
150 juta tahun yang lalu. Sisa-sisa organisme tersebut mengendap di dasar lautan,
kemudian ditutupi oleh lumpur. Lapisan lumpur tersebut lambat laun berubah menjadi
batuan karena pengaruh tekanan lapisan di atasnya. Sementara itu, dengan
meningkatnya tekanan dan suhu, bakteri anaerob menguraikan sisa-sisa jasad renik
tersebut dan mengubahnya menjadi minyak dan gas.
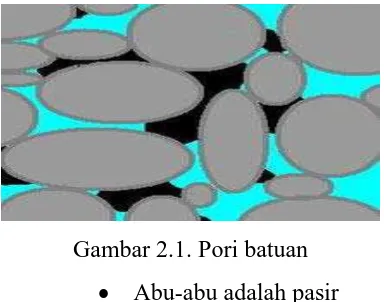
Gambar 2.1. Pori batuan
• Abu-abu adalah pasir
• Biru adalah air
• Hitam adalah minyak
Proses pembentukan minyak bumi dan gas ini memakan waktu jutaan tahun.
kemudian terkosentrasi jika terhalang oleh lapisan yang kedap. Walaupun minyak
bumi dan gas alam terbentuk di dasar lautan, banyak sumber minyak bumi yang
terdapat di daratan. Hal ini terjadi karena pergerakan kulit bumi, sehingga sebagian
lautan menjadi daratan.
Ada tiga macam teori yang menjelaskan proses terbentuknya minyak dan gas
bumi. Teori pertama adalah teori biogenetik atau lebih di kenal dengan teori organik.
Yang kedua adalah teori anorganik, sedangkan yang ketiga adalah teori duplex yang
merupakan perpaduan dari kedua teori sebelumnya. Teori duplex yang banyak di
terima oleh kalangan luas menjelaskan bahwa minyak dan gas bumi berasal dari
berbagai jenis organisme laut baik hewani maupun nabati.
Di perkirakan bahwa minyak bumi berasal dari materi hewani dan gas bumi
berasal dari materi nabati. Yang jelas minyak dan gas bumi terdiri dari senyawa
kompleks yang unsur utamanya adalah karbon (C) dan unsur hidrogen (H). secara
sederhana senyawa ini dapat ditulis dengan rumus kimia CXHY
Pada zaman purba, di darat dan di laut hidup beraneka ragam binatang dan
tumbuh-tumbuhan. Binatang serta tumbuh-tumbuhan yang mati ataupun punah itu
akhirnya tertimbun di bawah endapan Lumpur. Endapan Lumpur ini kemudian di
hanyutkan oleh arus sungai menuju lautan, bersama bahan organik lainnya dari
daratan.
, sehingga sering di
sebut sebagai senyawa hidrokarbon.
Akibat pengaruh waktu, temperatur tinggi dan tekanan beban lapisan batuan di
atasnya binatang serta tumbuh-tumbuhan yang mati tadi berubah menjadi bintik-bintik
dan gelembung minyak atau gas.
Akibat pengaruh yang sama, maka endapan Lumpur berubah menjadi batuan
sediment. Batuan lunak yang berasal dari Lumpur yang mengandung bintik-bintik
minyak dikenal sebagai batuan induk. Selanjutnya minyak dan gas ini akan bermigrasi
menuju tempat yang bertekanan lebih rendah dan akhirnya terakumulasi di tempat
yang di sebut perangkap (trap).
Suatu perangkap dapat mengandung:
• Minyak, gas, dan air
• Minyak dan air
Karena perbedaan berat jenis, apabila ketiga-tiganya berada dalam suatu
perangkap dan berada dalam keadaan stabil, gas senantiasa berada di atas, minyak di
tengah dan air di bagian bawah. Gas yang terdapat bersama-sama minyak bumi di
sebut associated gas sedangkan yang terdapat sendiri dalam suatu perangkap disebut
non-associated gas.
Dalam proses pembentukan minyak bumi diperlukan waktu yang masih belum
bisa di tentukan sehingga mengenai hal ini masih terdapat pendapat yang
berbeda-beda. Ada yang mengatakan ribuan tahun, ada yang mengatakan jutaan tahun bahkan
ada yang mengatakan lebih dari itu (anonim, 2008).
2.2. Surfaktan
Istilah surfaktan (surface active agent ) pada umumnya digunakan untuk
menggambarkan molekul yang berinteraksi pada permukaan cairan. Surfaktan terdiri
dari dua bagian, yaitu gugus hidrofobik dan hidrofilik. Surfaktan dapat digunakan
dalam sistem cairan ataupun bukan cairan. Pernyataan lain adalah amfifil yang
mengingatkan bahwa molekul atau ion mempunyai afinitas tertentu baik terhadap
pelarut polar maupun nonpolar. Sebagai contoh, alkohol – alkohol rantai lurus, amina
– amina dan asam – asam adalah amfifil yang berubah dari hidrofilik dominan
menjadi lipofilik apabila jumlah atom karbon dalam rantai alkil naik. Amfifilik
merupakan sifat dari zat aktif permukaan yang menyebabkan zat ini diadsorbsi pada
antarmuka, apakah ini cair/gas atau cair/cair. Jadi dalam suatu disperse dalam air dari
amil alkohol, gugus alkoholik polar dapat bergabung dengan molekul – molekul air
(Miller, 1930).
Surfaktan merupakan senyawa yang dapat menurunkan tegangan permukaan
dari suatu larutan, tegangan antarmuka antara dua larutan, atau bahkan tegangan
antarmuka antara larutan dan zat padat. Surfaktan dapat berfungsi sebagai detergen,
zat pembasah, emulsifier, zat pembusa dan zat pendispersi (Rosen, 2010)
Apabila pada permukaan antara dua fasa yang bersih (seperti gas-cairan dan
cairan-cairan) dtitambahkan komponen ketiga, maka komponen ketiga ini akan
teradsorbsi pada permukaan dan komponen ini akan sangat mempengaruhi sifat
mengadsorbsi adsorbat polar secara kuat dan mengadsorbsi adsorbat nonpolar secara
lemah. Sebaliknya adsorben nonpolar cenderung umtuk mengadsorbsi secara kuat
adsorbat nonpolar dan mengadsorbsi adsorbat polar secara lemah (Alberty, dkk,1984).
Surfaktan dapat menurunkan tegangan permukaan dengan baik jika digunkan
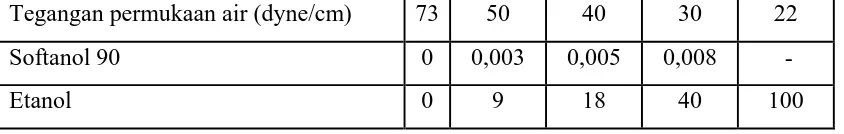
dalam konsentrasi yang sangat rendah. Contohnya Softanol 90 menurunkan tegangan
permukaan air dari 73 menjadi 30 dyne/cm pada konsentrasi 0,005% dan etanol pada
konsentrasi 20% menurunkan tegangan permukaan air menjadi 38 dyne/cm,
sebagaimana terlihat pada tabel dibawah ini:
Tabel 2.1. Perubahan tegangan permukaan oleh konsentrasi surfaktan
Tegangan permukaan air (dyne/cm) 73 50 40 30 22
Softanol 90 0 0,003 0,005 0,008 -
Etanol 0 9 18 40 100
2.2.1. Pembagian Surfaktan
Pada umumnya gugus hidrofobik merupakan gugus hidrokarbon yang berantai
panjang dan gugus hidrofil merupakan gugus yang mempunyai kepolaran yang tinggi
yang dapat meningkatkan kelarutan. Berdasarkan sifat dari gugus hidrofiliknya
surfaktan dibagi menjadi empat jenis, yaitu :
• Anionik, yaitu surfaktan dengan bagian aktif permukaannya mengandung
muatan negatif. Contohnya RC6H4SO3-Na+
• Kationik, yaitu surfaktan dengan bagian aktif permukaan mengandung muatan
positif. Contohnya RNH
(alkil benzena sulfonat).
3+Cl
-• Nonionik, yaitu surfaktan dengan bagian aktif tidak mengandung muatan
apapun. Contohnya ROCH
(garam amina rantai panjang).
2CH2
• Ampoterik atau zwitterionik yaitu surfaktan yang mengandung muatan negatif
maupun muatan positif pada bagian aktif permukaannya. Contohnya
RN
O-(polioksietilen).
+
2.2.2. Surfaktan Anionik
Surfaktan anionik merupakan komponen utama dari detergen, dimana penjualannya
mencapai 60 juta dolar di seluruh pasar Dunia. Surfaktan anionik juga digunakan
dalam pembersih permukaan, produk perawatan tubuh, bahan – bahan farmasi dan lain
sebagainya. Di dalam berbagai aplikasi, surfaktan anionik dicampur dengan surfaktan
anionik lainnya ataupun surfaktan nonionik untuk mendapatkan sifat – sifat yang
diinginkan seperti penurunan tegangan permukaan, penurunan tegangan antarmuka,
kelarutan substrat minyak dan lain sebagainya (Khan, dkk, 1999).
Sifat hidrofiliknya berasal dari bagian kepala ionik yang biasanya merupakan
gugus sulfat atau sulfonat. Pada kasus ini, gugus hidrofob diikat kebagian hidrofil
dengan ikatan C-O-S yang labil, yang mudah dihidrolisis. Beberapa contoh dari
surfaktan anionik adalah linier alkilbenzen sulfonat (LAS), alkohol sulfat (AS), alpha
olefin sulfonat (AOS) dan parafin atau secondary alkana sulfonat (SAS) (Permono,
2003).
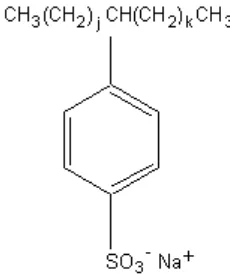
Struktur dari LAS seperti terlihat pada gambar :
Gambar 2.2. Struktur Linear alkilbenzen sulfonat
Dalam hal ini nilai j + k adalah antara 7 sampai 11 (Kosswig, 2005).
Berikut merupakan sifat-sifat umum dari surfaktan anionik :
• Jenis surfaktan yang paling besar (jumlahnya)
• Tidak kompatibel dengan jenis surfaktan kationik
• Sensitif terhadap air sadah atau hard water. Derajat sensitifitasnya :
karboksilat > fosfat > sulfat (sulfonat)
• Rantai pendek polioksietilen antara gugus anionik dan hidrokarbon
• Rantai pendek polioksipropilene antara gugus anionik dan hidrokarbon
meningkatkan kelarutan dalam solven organik.
• Jenis sulfat mudah terhidrolisa oleh asam-asam dalam proses autokatalitik.
Jenis yang lain stabil, asalkan tidak digunakan pada kondisi ekstrim (Porter,1994).
2.3. Tegangan Permukaan
Tegangan permukaan dari suatu cairan adalah gaya per satuan panjang pada
permukaan yang menurunkan pemanjangan daerah permukaan. Defenisi ini
diilustrasikan berdasarkan percobaan, dimana perpindahan pembatas didorong oleh
gaya F untuk memperluas film cairan yang diperpanjang seperti film gelembung sabun
dalam suatu bingkai wayar. Tegangan permukaan dari ilustrasi ini dapat dinyatakan
dengan persamaan sebagai berikut :
Dimana l adalah panjang pembatas, dan faktor 2 karena terdapat dua permukaan
larutan, satu pada bagian depan dan satu lagi pada bagian belakang. Tegangan
permukaan air pada suhu 25 OC adalah 71,97 x 10-3 N m-1
Tegangan permukaan disebabkan karena adanya kecenderungan permukaan
cairan untuk memperkecil luas permukaan secara spontan. Pada tingkat molekular hal
ini dapat dijelaskan sebagai berikut : molekul yang berada di dalam cairan akan
mengalami gaya tarik-menarik (gaya Van der Waals) yang sama besarnya ke segala
arah. Tetapi, molekul pada permukaan cairan akan mengalami gaya resultan yang
mengarah ke dalam cairan dan akibatnya molekul dipermukaan cenderung untuk
meninggalkan permukaan masuk ke dalam cairan sehingga permukaan cairan
cenderung untuk menyusut. Hal ini pulalah yang menyebabkan butiran cairan atau
gelembung gas cenderung untuk membentuk lingkaran (karena pada lingkaran nisbah
luas permukaan-volume minimum).
(Alberty, 1988).
Tegangan permukaan yang dapat diukur bukan hanya tegangan permukaan
antara permukaan cairan dan gas, tetapi juga tegangan permukaan antara permukaan
permukaan antara permukaan dua cairan biasanya terletak antara nilai tegangan
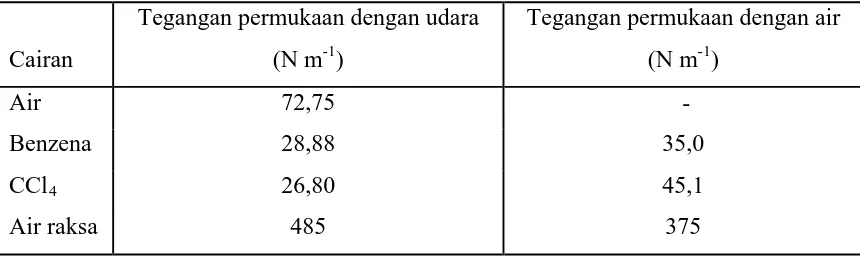
permukaan cairan-gas masing-masing cairan. Hal ini dapat dilihat pada tabel :
Tabel 2.2. Tegangan permukaan cairan
Cairan
Tegangan permukaan dengan udara
(N m-1
Tegangan permukaan dengan air
) (N m-1)
Air 72,75 -
Benzena 28,88 35,0
CCl4 26,80 45,1
Air raksa 485 375
(Bird, 1993).
Persamaan Young-Laplace adalah
yang menggambarkan perbedaa
, seperti
dinding sangat tipis. Persamaan Laplace Young-perbedaan tekanan berkaitan dengan
bentuk permukaan atau dinding dan secara mendasar penting dalam studi statis
antarmuka , dimana antarmuka dianggap sebagai permukaan(titik nol):
Dalam hal ini Δp adalah perbedaan tekanan di antarmuka fluida, γ adala
2.3.1. Kohesi dan Adhesi
Adhesi adalah kemampuan dari partikel-partikel yang tidak sejenis untuk saling
tarik-menarik satu sama lain, dimana kohesi adalah kemampuan dari partikel-partikel
sejenis untuk saling tarik-menarik satu sama lain(Israelachvili, 1985).
Bahan-bahan adhesif mengisi rongga-rongga ataupun pori-pori dari permukaan
dan mengikat permukaan dengan ikatan dalam. Adapun adhesi dapat terjadi melalui
beberapa cara, meliputi :
• Adhesi kimia
Dua bahan dapat membentuk senyawa sebagai bentuk gabungannya melalui
pemakaian elektron bersama(ikatan ionik dan kovalen) ataupun dalam bentuk
yang lebih lemah yaitu dengan ikatan hidrogen.
• Adhesi dispersi
Dalam hal ini adhesi terjadi melalui adanya ikatan van der Waals antara
molekul-molekul yang tidak sejenis.
• Adhesi elektrostatik
Beberapa bahan konduktor dapat melewatkan elektron-elektron untuk
membentuk suatu perbedaan muatan listrik sebagai gabungannya.
• Adhesi difusi
Pada beberapa bahan dapat terjadi penggabungan molekul yang berbeda pada
suatu bagian yang sam melalui difusi (Kendall, 1994).
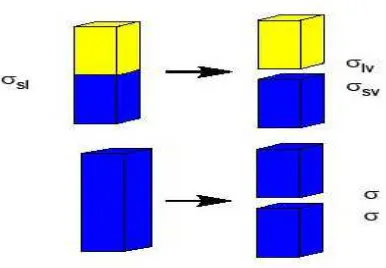
Kerja adhesi adalah pemisahan untuk membentuk dua permukaan baru dari
satu antarmuka:
Kerja kohesi adalah pemisahan untuk membentuk dua permukaan baru:
Gambar 2.3. Kerja adhesi dan kohesi
2.3.2. Faktor - Faktor yang Mempengaruhi Tegangan Permukaan
Ada beberapa faktor yang mempengaruhi tegangan permukaan, yaitu :
• Elektrolit
Adanya elektrolit dapat menyebabkan kenaikan tegangan permukaan,sehingga
disebut juga negative surface activity (Sukardjo, 1985).
• Temperatur
Tegangan permukaan cairan menurun dengan naiknya temperatur dan bernilai
nol pada temperatur kritis.
• Tekanan
Tegangan permukaan cairan berbanding lurus dengan tekanan,sehingga jika
tekanan naik maka tegangan permukaan cairan tersebut juga meningkat dan
sebaliknya jika tekanan menurun maka tegangan permukaan cairan juga turun.
• Zat terlarut
Adanya penambahan zat terlarut ke dalam suatu larutan dapat menurunkan
tegangan permukaan larutan tersebut karena zat terlarut menurunkan besarnya
energi Gibbs yang berdampak pada menurunnya tegangan permukaan
(Alberty, 1988).
• Luas permukaan bidang
Besarnya tegangan permukaan berbanding terbalik dengan luas permukaan
bidang, maka semakin luas permukaan bidang menyebabkan tegangan
• Konsentrasi
Semakin besar konsentrasi maka nilai tegangan permukaan juga semakin
besar, demikian pula sebaliknya bila konsentrasi menurun maka tegangan
permukaan cairan juga menurun.
• Densitas
Densitas berhubungan lurus dengan tegangan permukaan suatu cairan sehingga
semakin besar densitas tegangan permukaan cairan tersebut juga semakin besar
(Glasstone, 1959).
2.3.3. Metode Penentuan Tegangan Permukaan
Dalam penentuan energi bebas permukaan, perlu diingat kenyataan penting yang
sangat mendasar. Ada beberapa metode yang berbeda untuk menentukan energi bebas
permukaan, namun tidak satupun yang dapat menentukannya secara langsung.
Biasanya melalui penentuan beberapa parameter lainnya dan tegangan
permukaan dihitung berdasarkan beberapa perhitungan secara matematis. Penentuan
tegangan permukaan dibedakan menjadi dua, yaitu metode dinamis dan statis. Adapun
contoh penentuan tegangan permukaan tersebut adalah :
a. Penentuan tegangan permukaan dengan metode statis :
• Kenaikan kapiler
b. Penentuan tegangan permukaan dengan metode dinamis :
Untuk penentuan tegangan permukaan dibawah sekitar 1 dyne/cm hampir
seluruh metode dapat digunakan, tetapi pengukuran tegangan antarmuka dapat
meliputi beberapa kendala penelitian. Untuk pengukuran tegangan antarmuka dengan
nilai dibawah sekitar 1 dyne/cm dapat dilakukan dengan menggunakan metode cincin
Du Nouy, plat Wilhelmy, sessile drop, ataupun pendant drop. Untuk penentuan
tegangan antarmuka yang sangat rendah lebih sering menggunakan metode spinning
drop.
2.3.4. Metode Cincin Du Nouy
Dalam metode ini yang diukur adalah gaya yang dibutuhkan untuk mengangkat cincin
dari permukaan cairan. Gaya ini diukur dengan jalan mencelupkan cincin yang
digantung pada lengan neraca dan perlahan – lahan mengangkatnya sampai cincin
tersebut meninggalkan cairan. Metode ini tidak hanya dapat digunakan mengukur
tegangan permukaan cairan-udara, tetapi juga dapat digunakan mengukur tegangan
permukaan cairan-cairan seperti misalnya tegangan permukaan minyak-air.
Gaya yang dibutuhkan untuk mengangkat cincin dari permukaan air dapat
dihitung dari persamaan :
2.4. Viskositas
Diantara semua sifat – sifat fluida, viskositas memerlukan perhatian yang terbesar
dalam telaahan tentang aliran fluida. Viskositas adalah sifat fluida yang mendasari
diberikannya tahanan terhadap tegangan geser oleh fluida tersebut. Hukum viskositas
Newton menyatakan bahwa untuk laju perubahan bentuk sudut fluida yang tertentu
maka tegangan geser berbanding lurus dengan viskositas.
Viskositas gas meningkat dengan suhu, tetapi viskositas cairan berkurang
dengan naiknya suhu. Perbedaan dalam kecenderungan terhadap suhu tersebut dapat
diterangkan dengan menyimak penyebab – penyebab viskositas. Tahanan suatu fluida
terhadap tegangan geser tergantung pada kohesinya dan pada laju perpindahan
momentum molekularnya. Cairan dengan molekul - moekul yang jauh lebih rapat
daripada gas mempunyai gaya – gaya kohesi yang jauh lebih besar daripada gas.
Kohesi nampaknya merupakan penyebab utama viskositas dalam cairan, dan karena
kohesi berkurang dengan naiknya suhu, maka demikian pula viskositas. Sebaliknya,
gas mempunyai gaya –gaya kohesi yang sangat kecil. Sebagian besar dari tahanannya
terhadap tegangan geser merupakan akibat perpindahan momentum molekular
(Sukardjo,2002).
Perilaku zat cair, terutama air banyak dipelajari dalam bidang teknik sipil,
sedangkan gas banyak dipelajari dalam bidang teknik mesin, kimia, aeronotika, dan
sebagainya. Zat cair mempunyai beberapa sifat berikut ini :
• Apabila ruangan lebih besar dari volume zat cair, akan terbentuk permukaan
bebas horizontal yang berhubungan dengan atmosfer
• Mempunyai rapat massa dan berat jenis
• Dapat dianggap tidak termampatkan
• Mempunyai kohesi, adhesi dan tegangan permukaan
• Mempunyai viskositas (kekentalan) (Wylie, 1992)
Viskositas merupakan ukuran yang menyatakan kekentalan suatu cairan atau
fluida. Di dalam Satuan Internasional (SI), satuan viskositas adalah N s m-2 (kg m-1 s-1)
atau Pa s (Paskal sekon). Di dalam CGS satuan viskositas adalah dyne s cm-2 (g cm-2 s
-1
penghargaan kepada ilmuwan Prancis, “Poisseuille” yang menurunkan rumus
penentuan viskositas dan metode untuk menentukan viskositas larutan. Satuan
viskositas lain adalah centipoises (1/100 poise) dan millipoise (1/1000 poise) (Yazid,
2005).
Koefisien viskositas adalah kekuatan dalam dyne yang menggunakan tekanan
di antara dua lapisan sejajar, dapat juga dianggap sebagai gaya per satuan luas yang
diperlukan untuk menggerakkan ataupun memindahkan satu lapisan cairan yang
mempunyai kecepatan 1 cm det-1
Ketika suatu zat cair mengalir melalui suatu pipa, lapisan dari cairan dalam
kontak dengan dinding pipa adalah tetap dimana cairan pada pusatnya mempunyai
kecepatan yang tertinggi untuk mengalir. Konstanta η adalah koefisien viskositas
dalam unit cgs mempunyai dimensi gcm
melewati garis sejajar yang lain yang berjarak 1 cm.
-1
det-1 dan unitnya adalah poise. Kuantitas
lain adalah fluiditas, f = 1/η dan viskositas kinematik (v) didefenisikan sebagai viskositas dibagi densitas (v = η /d) (Findlay, 1960).
2.4.1. Faktor – Faktor yang Mempengaruhi Viskositas
Ada beberapa faktor yang mempengaruhi viskositas, yaitu :
• Tekanan
Viskositas cairan naik dengan naiknya tekanan, sedangkan viskositas gas
tidak dipengaruhi oleh tekanan.
• Temperatur
Viskositas cairan akan turun dengan naiknya temperatur, sedangkan viskositas
gas naik dengan naiknya temperatur. Pemanasan zat cair menyebabkan
molekul – molekulnya memperoleh energi. Molekul –molekul cairan bergerak
sehingga gaya interaksi antar molekul melemah. Dengan demikian viskositas
cairan akan turun dengan kenaikan temperatur.
• Kehadiran zat lain
Penambahan gula tebu meningkatkan viskositas air. Adanya bahan tambahan
seperti bahan suspensi (misalnya albumin dan globulin) menaikkan viskositas
air. Pada minyak ataupun gliserin adanya penambahan air akan menyebabkan
• Ukuran dan berat molekul
Viskositas naik dengan naiknya berat molekul. Misalnya laju aliran alkohol
cepat, larutan minyak laju alirannya lambat dan kekentalannya tinggi. Larutan
minyak misalnya CPO memiliki kekentalan tinggi serta laju aliran lambat
sehingga viskositas juga tinggi.
• Bentuk molekul
Viskositas akan naik jika ikatan rangkap semakin tinggi.
• Kekuatan antar molekul
Viskositas air naik dengan adanya ikatan hidrogen, viskositas CPO dengan
gugus OH pada trigliseridanya naik pada keadaan yang sama (Alberty, dkk,
1984).
• Konsentrasi
Untuk suatu larutan viskositasnya bergantung pada konsentrasi atau kepekatan
larutan. Umumnya larutan yang konsentrasinya tinggi, viskositasnya juga
tinggi. Sebaliknya larutan yang viskositasnya rendah , konsentrasinya juga
rendah (Sukardjo,2002).
2.4.2. Metode Penentuan Viskositas dengan Viskosimeter Ostwald
Viskositas suatu cairan murni atau larutan merupakan indeks hambatan alir cairan.
Viskositas dapat diukur dengan mengukur laju alir cairan yang melalui tabung
berbentuk silinder. Cara ini merupakan salah satu cara yang paling mudah dan dapat
digunakan baik dalam cairan maupun gas.
Pada viskosimeter Ostwald, yang diukur adalah waktu yang dibutuhkan oleh
sejumlah tertentu cairan untuk mengalir melalui pipa kapiler dengan gaya yang
disebabkan oleh berat cairan itu sendiri. Pada percobaan sebenarnya, sejumlah tertentu
cairan (misalkan 10 cm3
Ketika permukaan cairan turun melewati batas atas, stopwatch mulai
dinyalakan dan ketika caiaran melewati batas bawah, stopwatch dimatikan. Jadi, , bergantung pada ukuran viskosimeter) dipipet ke dalam
viskosimeter. Cairan kemudian dihisap melalui labu pengukur dari viskosimeter
sampai permukaan cairan lebih tinggi dari batas atas. Cairan kemudian dibiarkan
waktu yang dibutuhkan cairan untuk melalui jarak antara batas atas dan batas bawah
dapat ditentukan (Bird, 1993).
Pengukuran viskosimeter Ostwald dapat dihitung berdasarkan Hukum
Poiseuille berikut :
η = viskositas larutan
V = total volume larutan
t = waktu yang dibutuhkan larutan dengan volume V untuk mengalir melalui
viskometer
P = tekanan yang bekerja pada cairan
l = panjang pipa
Pengukuran viskositas yang tepat dengan cara di atas sulit dicapai. Hal ini
disebabkan harga r dan l sukar ditentukan secara tepat. Kesalahan pengukuran
terutama r sangat besar pengaruhnya karena harga ini dipangkatkan empat. Untuk
menghindari kesalahan tersebut dalam prakteknya digunakan cairan pembanding.
Untuk dua cairan yang berbeda dengan pengukuran alat yang sama diperoleh
hubungan :
Karena tekanan berbanding lurus dengan rapatan cairan, maka berlaku :
= viskositas air (poise)
= viskositas larutan yang diuji (poise)
t1
t
= waktu alir air (detik)
2 =waktu alir larutan yang diuji (detik)
Jadi, bila η dan d cairan pembanding diketahui, maka dengan mengukur waktu
yang diperlukan untuk mengalir kedua cairan melalui alat yang sama dapat ditentukan
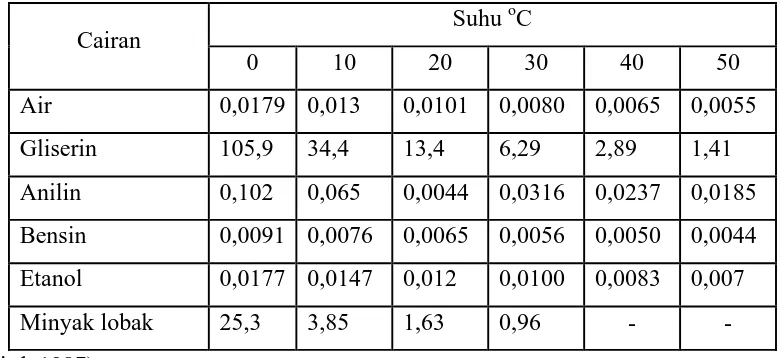
η cairan yang sudah diketahui rapatannya (Sukardjo,2002). Tabel 2.3 memperlihatkan
viskositas beberapa cairan pada suhu yang berbeda-beda.
Tabel 2.3. Viskositas cairan pada berbagai suhu (dalam satuan Poise)
Cairan Suhu
o C
0 10 20 30 40 50
Air 0,0179 0,013 0,0101 0,0080 0,0065 0,0055
Gliserin 105,9 34,4 13,4 6,29 2,89 1,41
Anilin 0,102 0,065 0,0044 0,0316 0,0237 0,0185
Bensin 0,0091 0,0076 0,0065 0,0056 0,0050 0,0044
Etanol 0,0177 0,0147 0,012 0,0100 0,0083 0,007
Minyak lobak 25,3 3,85 1,63 0,96 - -
BAB 3
BAHAN DAN METODE PENELITIAN
3.1. Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah:
Asam sulfat p.a Merck
Kalium bikromat p.a Merck
Linear alkylbenzene sulphonat (LAS) Bratachem
Minyak tanah -
Akuades -
3.2. Alat
Alat – alat yang digunakan dalam penelitian ini adalah :
Neraca analitis Tettler Toledo
Gelas ukur Pyrex
Gelas beaker Pyrex
Tensiometer Du Nouy Fisher
Viskosimeter Ostwald Fisher
Statif dan klem -
Oven Metler
Hot plate stirrer Fisher
Magnetic stirrer -
Labu alas Pyrex
3.3. Metode Penelitian
Jenis penelitian ini adalah eksperimen laboratorium dengan menggunakan hipotesa
dan analisa variansi pada satu jenis surfaktan.
3.3.1.Populasi
Dalam penelitian ini yang digunakan sebagai populasi adalah minyak tanah. Adapun
minyak tanah yang dipakai diperoleh dari pangkalan minyak tanah Jl.S.M.Raja,
Medan. Populasi yang digunakan bersifat homogen. Variabel – variabel yang
digunakan dalam penelitian ini adalah sebagai berikut :
1. Variabel bebas :
- Tegangan antarmuka sistem air-minyak tanah
- Viskositas sistem air-minyak tanah
3.3.2.Pengambilan Data
1. Pembuatan Sistem Air – Minyak Tanah
a. Dirangkai labu alas pada statif dan klem, dengan hotplate stirrer berada di
bawahnya.
b. Dimasukkan 25 ml larutan LAS dengan variasi konsentrasi 0,25% – 2,0%
v/v dan 25 ml minyak tanah.
c. Diaduk selama 5 menit dengan laju pengadukan 800 rpm, kemudian
didiamkan selama 30 menit.
d. Diukur tegangan antarmuka dengan cincin Du Nouy dan viskositas dengan
viskosimeter Ostwald
2. Pengukuran Densitas
a. Piknometer kosong dikeringkan dan dibersihkan, kemudian ditimbang pada
neraca analitis dan dicatat massanya (mo
b. Diisi piknometer kosong dengan sistem air-minyak tanah sampai tidak ada
gelembung udara, kemudian ditimbang pada neraca analitis dan dicatat
massanya (m
)
1
c. Dihitung densitas sistem air-minyak tanah yang diuji berdasarkan data yang
diperoleh dengan rumus sebagai berikut : )
(1)
3. Pengukuran Tegangan Permukaan
a. Diukur 45 ml sistem air-minyak tanah
b. Dimasukkan ke dalam gelas cincin Du Nouy
c. Diukur tegangan permukaan dengan cincin Du Nouy dan dicatat hasilnya
d. Dihitung tegangan antarmuka yang sesungguhnya dengan menggunakan
persamaan di bawah ini :
(2)
4. Pengukuran Viskositas
a. Dimasukkan 10 ml sistem air-minyak tanah ke dalam viskometer Ostwald
b. Dihisap dengan bola karet hingga batas atas
c. Dicatat waktu yang dibutuhkan oleh sistem air-minyak tanah untuk
mengalir dari batas atas sampai batas bawah
d. Dihitung viskositas sistem air-minyak tanah tersebut berdasarkan data
yang diperoleh dengan menggunakan rumus sebagai berikut :
3.3.3.Pengolahan dan Analisa Data
3.3.3.1. Perhitungan Nilai Densitas pada Sistem Air-Minyak Tanah
Nilai densitas dihitung berdasarkan persamaan berikut :
dimana : d = densitas larutan (g/mL)
m0
m
= massa piknometer kosong
1
V = volume (mL)
= massa piknometer berisi
3.3.3.2. Perhitungan Nilai Tegangan Antarmuka Sampel
Nilai tegangan antarmuka dihitung berdasarkan persamaan di bawah ini :
Dimana = tegangan antar permukaan sebenarnya
= tegangan antar permukaan percobaan
= faktor koreksi
Faktor koreksi dihitung dengan menggunakan rumus :
Dengan : F = faktor koreksi
R = jari-jari cincin (0,6366 cm)
r = jari-jari kawat dari cincin (0,0157 cm)
= nilai tegangan antar permukaan yang diukur pada percobaan
(41,50)
D = densitas fase bawah (0,9842)
d = densitas fase atas (0,8803)
C = keliling cincin (3,9978 cm)
Sehingga diperoleh nilai , maka nilai tegangan antarmuka yang sebenarnya
adalah :
3.3.3.3. Perhitungan Nilai Viskositas Sampel
Nilai viskositas dapat dihitung dengan menggunakan persamaan sebagai berikut :
Dengan harga pada suhu 30 oC adalah 0,8007 cP.
3.3.3.4. Analisis Variansi
Dalam menguji hipotesa yang telah diajukan maka dipakai rancangan acak sederhana.
Dalam rancangan ini tidak terdapat lokal kontrol, sehingga sumber keragaman yang
diamati hanya perlakuan yang diragam sebanyak kelompok.
Analisis jumlah kuadrat untuk nilai viskositas dan tegangan antarmuka
1. Jumlah kuadrat total (JKT)
2. Jumlah kuadrat antar kelompok (JKA)
3. Jumlah kuadrat dalam kelompok (JKD)
4. Rata – rata kuadrat antar kelompok (RKA)
6. FHitung
Dengan berdasar pada hipotesis :
Dengan criteria tolak H0 jika , dimana diperoleh dari
daftar distribusi frekuensi F dengan peluang (1- α), dk(v1,v2), dan α adalah taraf
3.4. Skema Pengambilan Data
3.4.1. Pembuatan Sistem Air-Minyak Tanah
3.4.2. Pengukuran Densitas
25 mL Minyak tanah
Dimasukkan 25 ml larutan LAS dengan variasi konsentrasi 0,25% - 2,0% v/v
Diaduk selama 5 menit dengan laju pengadukan 800 rpm
Didiamkan selama 30 menit
Diukur tegangan antarmuka dengan cincin Du Nouy dan viskositas dengan viskosimeter Ostwald
Dipisahkan Sistem Air-Minyak bumi
Diukur densitasnya Diukur densitasnya
Lapisan atas
Dipipet 5 mL sistem air-minyak tanah,dimasukkan ke dalam
piknometer
Ditimbang berat piknometer berisi sampel
Dilakukan penimbangan sebanyak 3 kali
3.4.3. Pengukuran Tegangan Antarmuka
3.4.4. Pengukuran Viskositas
45 mL sistem air-minyak tanah
Hasil
Dimasukkan ke dalam gelas cincin Du Nouy
Diukur tegangan permukaan sistem air-minyak tanah dengan cincin Du Nouy
Sistem air-minyak tanah dalam gelas cincin Du Nouy
10 mL sistem air-minyak tanah
Hasil
Dimasukkan ke dalam viskosimeter Ostwald
Dihisap sampel memakai bola karet sampai garis batas atas
Dilepaskan bola karet dan stopwatch dihidupkan
Dicatat waktu alir dari batas atas sampai batas bawah
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
4.1.1.Hasil Pengukuran Tegangan Antarmuka Sistem Air-Minyak Tanah dengan
Penambahan Surfaktan LAS
Dari hasil penelitian yang telah dilakukan , diperoleh data tegangan antarmuka sistem
air-minyak tanah yang menunjukkan bahwa terjadi perubahan tegangan antarmuka
sistem air minyak tanah sebelum dan sesudah penambahan surfaktan LAS dengan
variasi konsentrasi antara 0,25% - 2,0%. Dalam hal ini tegangan antarmuka sistem
air-minyak tanah mengalami penurunan seiring dengan bertambahnya konsentrasi dari
surfaktan LAS yang ditambahkan ke dalam sistem tesebut, sebagaimana terlihat pada
lampiran III pada lampiran.
4.1.2.Hasil Pengukuran Waktu Alir Sistem Air-Minyak Tanah dengan
Penambahan Surfaktan LAS
Dari hasil penelitian yang telah dilakukan , diperoleh data waktu alir sistem
air-minyak tanah yang menunjukkan bahwa terjadi perubahan waktu alir sistem air
minyak tanah sebelum dan sesudah penambahan surfaktan LAS dengan variasi
konsentrasi antara 0,25% - 2,0%. Dalam hal ini waktu alir sistem air-minyak tanah
mengalami peningkatan seiring dengan bertambahnya konsentrasi dari surfaktan LAS
yang ditambahkan ke dalam sistem tersebut yang berbanding lurus dengan naiknya
nilai viskositas sistem tersebut berdasarkan perhitungan yang dilakukan, sebagaimana
4.2. Pembahasan
4.2.1. Pengaruh Konsentrasi Surfaktan LAS Terhadap Tegangan Antarmuka
Sistem Air-Minyak Tanah
Dari hipotesa 1 diperoleh harga Fhitung lebih besar dari ftabel, maka diterima dan
ditolak. Hal ini berarti bahwa ada pengaruh penambahan surfaktan LAS terhadap
perubahan tegangan antarmuka sistem air-minyak tanah seperti ditunjukkan pada
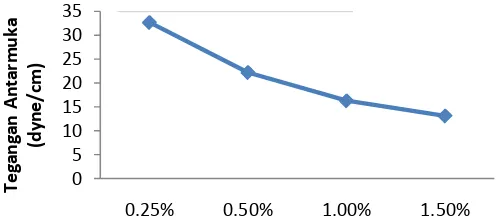
grafik di bawah ini.
Konsentrasi Linear Alkylbenzene Sulphonate (v/v)
Gambar 3.1. Grafik hubungan konsentrasi terhadap tegangan antarmuka sistem
air-minyak tanah
Berdasarkan grafik dapat terlihat bahwa semakin besar konsentrasi surfaktan
LAS yang ditambahkan, maka semakin kecil nilai tegangan antarmuka dari sistem
air-minyak tanah. Hal ini terjadi karena molekul surfaktan yang ditambahkan berinteraksi
dengan molekul-molekul dari air dan minyak tanah, sehingga akan mengubah susunan
molekul-molekul fase non polar dan polar. Perubahan susunan molekul-molekul air
dan minyak tanah akan menyebabkan energi dari sistem akan berubah.
Hal ini bersesuaian dengan sebagaimana yang telah dilaporkan oleh Juharuddin
Nasution, dimana yang bersangkutan meneliti tentang pengaruh jenis dan konsentrasi
alkali terhadap tegangan antarmuka sistem air-minyak bumi dengan hasil bahwa
semakin tinggi konsentrasi alkali yang ditambahkan maka nilai tegangan antarmuka
juga akan semakin tinggi. Dimana dalam penelitian ini juga diperoleh nilai tegangan
antarmuka yang semakin menurun dengan bertambahnya konsentrasi surfaktan yang
Bertambah besar konsentrasi surfaktan di antarmuka sistem air-minyak tanah
menyebabkan energi dalam berkurang, dengan mekanisme bahwa semakin besar
daerah antarmuka sistem tersebut. Sesuai dengan persamaan Gibbs bahwa perubahan
energi dalam suatu sistem adalah energi yang dibutuhkan dikurang usaha yang
dilakukan (P-dV), semakin besar nilai dV maka perubahan energi dalam sistem akan
semakin kecil.
Dengan meningkatnya surfaktan yang ditambahkan menyebabkan jumlah
molekul-molekul surfaktan yang teradsorpsi pada permukaan larutan semakin besar,
sehingga konsentrasi permukaan dari kedua fase meningkat. Keadan ini menyebabkan
semakin besar gaya interaksi molekul surfaktan dengan molekul permukaan melawan
gaya tarikan antara molekul permukaan dengan molekul fase ruah, akibatnya tegangan
permukaan masing-masing fase menjadi kecil.
4.2.2. Pengaruh Konsentrasi Surfaktan LAS Terhadap Tegangan Antarmuka
Sistem Air-Minyak Tanah
Dari hipotesa 1 diperoleh harga Fhitung lebih besar dari ftabel, maka diterima dan
ditolak. Hal ini berarti bahwa ada pengaruh penambahan surfaktan LAS terhadap
perubahan viskositas sistem air-minyak tanah seperti ditunjukkan pada grafik di
bawah ini.
Konsentrasi Linear Alkylbenzene Sulphonate (v/v)
`
Gambar 3.2. Grafik hubungan konsentrasi terhadap viskositas sistem air-minyak tanah
Berdasarkan grafik dapat terlihat bahwa semakin besar konsentrasi surfaktan
alir sistem air-minyak tanah karena surfaktan dapat menurunkan tegangan antarmuka
sistem yang berpengaruh terhadap kemampuan membasahi(wettabillity) dinding kaca.
Penurunan tegangan antarmuka berpengaruh terhadap sudut kontak antara
dinding kaca yang bersifat padat dengan sistem air-minyak tanah yang bersifat cair.
Menurunnya sudut kontak ini menyebabkan dinding kaca lebih mudah dibasahi oleh
sistem air-minyak tanah yang menyebabkan nilai viskositasnya akan semakin
menurun.Dengan menurunnya tegangan antarmuka, maka gaya adhesi dari sistem
air-minyak tanah yang tidak saling campur juga akan meningkat sehingga kelarutannya
pun akan meningkat. Hal ini juga berpengaruh terhadap semakin menurunnya nilai
viskositas dari sistem air-minyak tanah.
Dalam penelitian sebelumnya yag dilakukan oleh Ircham Hendani Haqiqi yang
meneliti Analisa pengaruh konsentrasi surfaktan anionik dan temperatur terhadap
waktu alir surfaktan dan minyak pada pipa kapiler juga telah dilaporkan bahwa
semakin besar konsentrasi surfaktan anionik yang ditambahkan maka waktu alir akan
semakin menurun yang berarti bahwa nilai viskositas juga semakin menurun.
Namun dalam penelitian ini ditemukan kendala yakni timbulnya busa sebagai
akibat pengadukan menyebabkan waktu alir dari sistem air –minyak tanah mengalami
kenaikan seiring dengan pertambahan konsentrasi dari surfaktan LAS yang
ditambahkan. Dalam hal ini kenaikan waktu alir dari sistem air-minyak tanah
menyebabkan nilai viskositas dari sistem air-minyak tanah tersebut karena nilai
viskositas berbanding lurus terhadap waktu alir.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian dapat disimpulkan bahwa:
• Ada pengaruh konsentrasi surfaktan LAS terhadap tegangan antarmuka dan
viskositas sistem air-minyak tanah, semakin besar konsentrasi surfaktan yang
ditambahkan maka nilai tegangan antarmuka akan semakin kecil dan nilai
viskositas dari sistem air-minyak tanah akan semakin besar.
• Surfaktan dapat digunakan untuk meningkatkan faktor perolehan minyak
dengan cara diinjeksikan ke dalam reservoar sehingga minyak yang terjebak
dalam pori batuan dapat diproduksikan.
5.2. Saran
Dari hasil penelitian yang telah dilakukan disarankan untuk memvariasikan jenis dan
konsentrasi surfaktan yang digunakan serta suhu untuk menentukan tegangan
DAFTAR PUSTAKA
Alberty,A.Robert. 1988. Physical Chemistry. Seventh Edition.New York : John Wiley and Sons.
Alberty,A.Robert dan Daniels Farrington.1984. Kimia Fisika. Jakarta : Erlangga.
Anomim.2008.http://kimia.upi.edu/utama/bahanajar/kuliah_web/2008/Riski%20S eptiadevana%200606249_IE6.0/halaman_7.html. Diakses 20 April 2011.
Batchelor, G.K. 1967. Sebuah Pengantar Untuk Dinamika Fluida. New York : Cambridge University Press.
Bird,Tony. 1993. Kimia Fisik Untuk Universitas. Jakarta : Gramedia Pustaka Utama.
Brien, B.M. 1982. Anhanced Oil Recovery Chemical Needs. New York : Journal American Oil Chemical Sociate. Vol 59. No 10.
Castellan,G.W. 1973. Physical Chemistry. Second Edition. New York : Wisley Publishing Inc.
Daniel,F. 1956. Experiment Physical Chemistry. Sixth Edition. New York : Mac Graw Hill Book Company.
Findlay,A.1960.Practical Physical Chemistry.Eight edition. London : William Clowes and Sons Limited.
Glasstone,Samuel.1959. Physical Chemistry. Second Edition. New York : D.Van Nostrand Company,Inc.
Israelachvili, J. N. 1985. Intermolecular and Surface Forces. New York : Academic Press.
Jaycock,M.J and Parfitt,G.D. 1981. Chemistry of Interface. Chichester : Harwood Limited.
Kendall, K. 1994. Adhesion: Molecules and Mechanics. Science 263 (5154):
Khan, A and Marques.E.F.1999.Synergism And Polymorphism in Mixed Surfactant Systems.Curr Opin Colloid Interface Sci 4:402
Kosswig, Kurt. 2005. Surfactants in Ullmann's Encyclopedia of Industrial
Miller,B.1930. Organic Chemistry The Basis of Life. California : The Benjamin/Cummings Publishing Company.
Permono, A. 2003. Membuat Sabun Tangan Cair. Jakarta : Pustaka Pembangunan Swadaya Nusantara.
Porter,M.R. 1994. Handbook of Surfactant. Second Edition. Madras : Blackie Academic and Profesional.
Rosen, M.J. 2010. Surfactants and Interfacial Phenomena. Thirrd edition. New Jersey : John Wiley & Sons
Sukardjo. 1985. Kimia Fisika. Yogyakarta : Bina Aksara.
Wylie,E.B.,1992.Mekanika Fluida. Jakarta : Erlangga.
Lampiran I. Hasil Pengukuran Tegangan Antarmuka Sistem Air-Minyak Tanah dengan Variasi Konsentrasi LAS
No. Konsentrasi Tegangan antarmuka(dyne/cm)
1 2 3
Lampiran II. Hasil Pengukuran Densitas Lapisan Atas dan Lapisan Bawah Sistem Air-Minyak Tanah dengan Variasi Konsentrasi LAS
No. Konsentrasi Densitas (g/mL)
Lampiran III. Hasil Perhitungan Tegangan Antarmuka Sistem Air-Minyak Tanah dengan Faktor Koreksi
No. Konsentrasi Tegangan antarmuka(dyne/cm)
1 2 3
Lampiran IV. Data dari Tabel III untuk Perhitungan ANAVA
Konsentrasi Tegangan antarmuka(dyne/cm) Jumlah Rata-rata
1 2 3
Lampiran V. Hasil Perhitungan ANAVA Tabel III
Sumber variasi Dk JK RJK FHit FTab
Rata-rata 1 5134,664
Konsentrasi 4 1051,351 262,8378 5,53 3,48
Kekeliruan 10 475,33 47,533
Jumlah 15 6661,345
Lampiran VI. Hasil Pengukuran Densitas Sistem Air-Minyak Tanah dengan Variasi Konsentrasi LAS
No. Konsentrasi Densitas (g/mL)