ANALISA KADAR KLORIDA PADA AIR MINUM DAN AIR SUMUR
DENGAN METODE ARGENTOMETRI
KARYA ILMIAH
NOVITA SANI SIANTURI
102401061
DEPARTEMEN KIMIA
PROGRAM DIPLOMA – 3 KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ANALISA KADAR KLORIDA PADA AIR MINUM DAN AIR SUMUR
DENGAN METODE ARGENTOMETRI
KARYA ILMIAH
Diajukan Untuk Melengkapi Tugas Dan Memenuhi Syarat Mencapai
Gelar Ahli Madya
NOVITA SANI SIANTURI
102401061
DEPARTEMEN KIMIA
PROGRAM DIPLOMA – 3 KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul :ANALISA KADAR KLORIDA PADA AIR MINUM DAN AIR SUMUR DENGAN METODE ARGENTOMETRI
Kategori : KARYA ILMIAH
Nama : NOVITA SANI SIANTURI
NIM : 102401061
Program Studi : DIPLOMA – 3 KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM
(FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di : Medan, Juni 2013 Diketahui Oleh :
Ketua
Program studi DIII Kimia Dosen Pembimbing
Dra. Emma Zainar Nst, MSi
NIP.195512181987012001 NIP. 195510131986011001 Dr.Mimpin Ginting, MS
Ketua
Departemen Kimia FMIPA USU
PERNYATAAN
ANALISIS KADAR KLORIDA PADA AIR MINUM DAN AIR SUMUR DENGAN METODE ARGENTOMETRI
KARYA ILMIAH
Saya mengakui bahwa karya ilmiah ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Juni 2013
NIM 102401061
PENGHARGAAN
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa atas berkat dan karunia-Nya yang besar sehingga penulis dapat menyelesaikan Penulisan karya ilmiah yang berjudul ANALISA KADAR KLORIDA PADA AIR MINUM DAN AIR SUMUR DENGAN METODE ARGENTOMETRI , yang merupakan salah satu syarat Kelulusan Program Diploma III Jurusan Kimia Analisis Fakultas Matematika dan Ilmu Pengetahuan Alam di Universitas Sumatera Utara .
Penulisan tugas akhir ini berdasarkan hasil kerja praktek lapangan di balai teknik kesehatan lingkungan dan pemberantasan penyakit ( BTKL & PP ).
Dalam penulisan karya ilmiah ini , penulis telah banyak mendapat bimbingan dan bantuan dari berbagai pihak . oleh karena itu sudah selayaknya penulis mengucapkan terima kasih kepada :
1. Kedua orang Tua penulis Bapak W.Sianturi dan S.Hutajulu yang telah memberikan dukungan moril dan bantuan materi sampai selesainya karya ilmiah ini
2. Bapak Dr. Mimpin Ginting , MS selaku dosen pembimbing yang telah banyak memberikan masukan dan bimbingan dalam penulisan karya ilmiah ini.
3. Ibu Dr. Rumondang Bulan, MS selaku Ketua Jurusan Departemen Kimia F-MIPA USU.
4 Dra. Emma Zainar Nst, MSi selaku Ketua Program studi DIII Kimia
5 Ibu Pimpinan , Staf dan seluruh pegawai Balai Teknik Kesehatan Lingkungan & Pemberantasan Penyakit (BTKL & PP ).
6 Dosen dan Staf dan Seluruh pegawai Universitas Sumatera Utara
7 Adikku Okta Sariito dan kakakku Rina Sianturi Tersayang yang memberikan dukungan dan kasih sayang, serta keponakaan aku yang lucu Boas Gabriel Pasaribu yang memberikan penulis semangat dengan tingkah nya yang lucu. 8 Rekan-rekan Mahasiswa Kimia Analis Stambuk 2010 yang telah semakin
kompak dan telah memberikan masukan dan dukungan selama penulisan karya ilmiah ini.
9 Abang, Kakak, dan Adik-adik kami angkatan 2009, 2011, dan 2012 yang senantiasa memberi dukungan moril bagi penulis.
Semoga segala kebaikan dan kemurahan hati Bapak/ Ibu dan Saudara-saudari sekalian yang telah meluangkan waktu dan pemikiran serta memberikan motivasi kepada kami, mendapat berkat yang melimpah dari Tuhan Yang Maha Esa
Akhir kata penulis mengucapkan banyak terima kasih dan berharap semoga tulisan ini bermanfaat dan dapat dipergunakan sebagaimana mestinya.
Medan, Juni 2013 Penulis
ABSTRAK
Air merupakan zat yang paling penting dalam kehidupan setelah udara. Sekitar tiga perempat bagian dari tubuh kita terdiri dari air dan tidak seseorang pun yang dapat bertahan hidup lebih dari 4-5 hari tanpa minum air. Air Sumur merupakan sumber utama persedian air bersih bagi penduduk yang tinggal didaerah perdesaan maupun diperkotaan Indonesia. Kadar klorida yang tinggi, misalnya pada air laut, yang diikuti oleh kadar kalsium dan magnesium yang juga kadarnya tinggi dapat meningkatkan sifat korosivitas air serta kadar klorida 250 mg/liter dapat mengakibatkan air menjadi asin. Salah satu zat kimia yang terkandung didalam air minum dan air sumur adalah klorida. Klorida yang berlebih merupakan suatu senyawa kimia yang bersifat toksik terhadap lingkungan. Untuk itu perlu dilakukannya analisa klorida dalam beberapa contoh air minum maupun air sumur. Dalam penelitian karya ilmiah ini dilakukan penentuan kadar klorida menggunakan metode argentometri dalam air minum yakni air minum 613/k/AM/02/13, dan air minum 615/k/AM/02/13, demikian juga air sumur yang berasal dari air sumur gaharu, air sumur velankani, air sumur marelan.
BAB 4. HASIL DAN PEMBAHASAN……...26
4.1. Data percobaan………... 26
4.2. Reaksi Percobaan……… 27
4.3. Perhitungan Kadar Klorida……… 27
4.3.1. Pada Air Sumur………... 27
4.3.2. Pada Air Minum………. 29
44.5. Pembahasan………... 30
BAB 5. KESIMPULAN DAN SARAN………31
5.1. Kesimpulan……….... 31
5.2. Saran………... 32
ABSTRAK
Air merupakan zat yang paling penting dalam kehidupan setelah udara. Sekitar tiga perempat bagian dari tubuh kita terdiri dari air dan tidak seseorang pun yang dapat bertahan hidup lebih dari 4-5 hari tanpa minum air. Air Sumur merupakan sumber utama persedian air bersih bagi penduduk yang tinggal didaerah perdesaan maupun diperkotaan Indonesia. Kadar klorida yang tinggi, misalnya pada air laut, yang diikuti oleh kadar kalsium dan magnesium yang juga kadarnya tinggi dapat meningkatkan sifat korosivitas air serta kadar klorida 250 mg/liter dapat mengakibatkan air menjadi asin. Salah satu zat kimia yang terkandung didalam air minum dan air sumur adalah klorida. Klorida yang berlebih merupakan suatu senyawa kimia yang bersifat toksik terhadap lingkungan. Untuk itu perlu dilakukannya analisa klorida dalam beberapa contoh air minum maupun air sumur. Dalam penelitian karya ilmiah ini dilakukan penentuan kadar klorida menggunakan metode argentometri dalam air minum yakni air minum 613/k/AM/02/13, dan air minum 615/k/AM/02/13, demikian juga air sumur yang berasal dari air sumur gaharu, air sumur velankani, air sumur marelan.
BAB I PENDAHULUAN
1.1.1. Latar Belakang
Air merupakan zat yang paling penting dalam kehidupan setelah udara. Sekitar
tiga perempat bagian dari tubuh kita terdiri dari air dan tidak seseorang pun yang dapat bertahan hidup lebih dari 4-5 hari tanpa minum air. Selain itu juga biasanya air
dipergunakan untuk mencuci ,mandi , memasak dan membersihkan kotoran sekitar dirumah kita . Disamping itu juga air dipergunakan untuk keperluan lainnya seperti memadamkan kebakaran , industri , peternakan , tempat rekreasi, dan transportasi.
Tetapi dewasa ini air merupakan masalah yang perlu diperhatikan dengan seksama dan cermat. Untuk mendapatkan kualitas air yang baik, sesuai standar tertentu, saat ini
menjadi barang mahal karena sudah banyak air yang tercemar oleh bebagai macam limbah dari kegiatan manusia, baik dalam limbah industri maupun limbah rumah tangga serta kegiatan lainnya
Peningkatan kualitas air minum dan air sumur dengan jalan mengadakan pengolahaan terhadap air yang akan diperlukan sebagai air minum dan kebutuhan rumah
tangga sehari-hari dengan mutlak diperlukan terutama apabila air tersebut berasal dari air permukaan. Air sumur mengandung padatan yang terbentuk , keruh , dan juga mengandung mikroorganisme yang berasal dari sumber seperti bahan kimia yang
Salah satu unsur dari senyawa yang terkandung dalam air sumur dan air minum
adalah klorida, tergolong dalam unsur halogen , yang molekulnya merupakan gas Cl2 berwarna kuning kehijauan dan dapat bersenyawa dengan hampir semua unsur. Dialam klorida ditemukan dalam keadaan bersenyawa terutama dengan natrium sebagai garam
(NaCl) . Klorida digunakan untuk proses pembuatan kertas , zat pewarna , tekstil , produk olahan minyak bumi , obat-obatan , antiseptik , insektisida, makanan , pelarut ,
cat, plastik , dan banyak produk lainnya. Kebanyakan klorida diproduksi untuk digunakan dalam pembuatan senyawa klorin untuk sanitasi , pemutih kertas , desifektan , dan proses tekstil . Kerugian dari penggunaan senyawa klorida dapat mengiritasi sistem
pernafasan dan dalam bentuk cair bisa membakar kulit. Baunya dapat dideteksi pada konsentrasi 3,5 ppm dan pada konsentrasi 1000 ppm dapat berakibat fatal setelah terhisap
. Walaupun klorida sangat larut , klorida memiliki stabilitas yang memungkinkan bisa bertahan dari perubahaan dan tetap konstan dalam air apapun. Konsentrasi yang tinggi dari klorida mengakibatkan pertambahaan kemampuan konduktivitas listrik air
(Darmono,2001).
Dari uraian yang telah ditemukan diatas penulis ingin meneliti tentang penentuan kadar klorida dengan mengangkat judul “ANALISA KADAR KLORIDA PADA AIR
SUMUR DAN AIR MINUM DENGAN METODE ARGENTOMETRI”.
1.1. Permasalahan
2. Apakah kadar klorida yang dihasilkan sesuai dengan peraturan Menteri
Kesehatan RI No: 907/MENKES/SK/VII/2002, dimana setiap komponen yang dikandung dalam air minum harus sesuai dengan yang ditetapkan.
1.2. Tujuan
1. Untuk mengetahui kadar hasil analisis klorida yang terkandung dalam air minum
dan air sumur.
2. Untuk mengetahui kadar klorida dalam air minum dan air sumur apakah sesuai dengan standar peraturan Menteri Kesehatan RI No: 907/MENKES/SK/VII/2002
tentang standart air minum.
1.3. Manfaat
• Hasil yang diperoleh dari penulisan ini dapat memberikan informasi tentang
BAB II
TINJAUAN PUSTAKA
2.1. Air
2.1.1. Sifat air
Air memiliki karakteristik yang khas yang tidak dimiliki oleh senyawa kimia yang lain. Karakteristik tersebut adalah sebagai berikut:
1. Pada kisaran suhu yang sesuai bagi kehidupan, yakni 0°C (32°F) - 100°C, air berwujud cair. Suhu 0°C merupakan titik beku (freezing point) dan suhu 100°C merupakan titik didih (boiling point) air. Tanpa sifat tersebut, air yang terdapat didalam
jaringan tubuh makhluk hidup maupun air yang terdapat dilaut, sungai, danau dan badan air yang lain akan berada dalam bentuk gas atau padatan , sehingga tidak akan terdapat
kehidupan di muka bumi, karena sekitar 60 % - 90 % bagian sel makhluk hidup adalah air.
2. Perubahan suhu air berlangsung lambat sehingga air memiliki sifat sebagai penyimpan panas yang sangat baik. Sifat ini memungkinkan air tidak menjadi panas atau pun dingin seketika. Perubahan suhu air yang lambat mencegah terjadinya stress pada makhluk hidup
karena adanya perubahan suhu yang mendadak dan memelihara suhu bumi agar sesuai bagi makhluk hidup. Sifat ini juga menyebabkan air sangat baik sebagai pendingin mesin.
3. Air memerlukan panas yang tinggi dalam proses penguapan. Penguapan (evaporasi)
jumlah yang besar. Sebaliknya, proses perubahan uap air menjadi cairan (kondensasi)
melepaskan energi panas yang besar. Pelepasan energi ini merupakan salah satu penyebab mengapa kita merasa sejuk pada saat berkeringat. Sifat ini juga merupakan salah satu faktor utama yang menyebabkan terjadinya penyebaran panas secara baik di bumi.
4. Air merupakan pelarut yang baik. Air mampu melarutkan berbagai jenis senyawa kimia. Air hujan mengandung senyawa kimia dalam jumlah yang sangat sedikit,
sedangkan air laut dapat mengandung senyawa kimia hingga 35.000 mg/liter. Sifat ini memungkinkan unsur hara (nutrient) terlarut diangkut ke seluruh jaringan tubuh makhluk hidup dan memungkinkan bahan – bahan toksik yang masuk kedalam jaringan tubuh
makhluk hidup dilarutkan untuk dikeluarkan kembali. Sifat ini juga memungkinkan air digunakan sebagai pencuci yang baik dan pengencer bahan pencemar (polutan) yang
masuk kebadan air.
5. Air memiliki tegangan permukaan yang tinggi. Suatu cairan dikatakan memiliki tegangan permukaan yang tinggi jika tekanan antar molekul cairan tersebut tinggi.
Tegangan permukaan yang tinggi menyebabkan air memiliki sifat membasahi suatu bahan secara baik. Tegangan permukaan yang tinggi juga memungkinkan terjadinya sistem kapiler, yaitu kemampuan untuk bergerak dalam pipa kapiler (pipa dengan lubang
yang kecil). Dengan adanya sistem kapiler dan sifat pelarut yang baik, air dapat membawa nutrient dari dalam tanah ke jaringan tumbuhan (akar, batang, dan daun).
6. Air merupakan satu – satunya senyawa yang merenggang ketika membeku. Pada saat membeku, air merenggang sehingga es memiliki nilai densitas (massa/volume) yang lebih rendah daripada air. Dengan demikian, es akan mengapung di air. Sifat ini mengakibatkan danau –danau didaerah yang beriklim dingin hanya membeku pada bagian
permukaan (bagian di bawah pemukaan masih berupa cairan) sehingga kehidupan organisme akuatik tetap berlangsung. Sifat ini juga dapat mengakibatkan pecahnya pipa
air pada saat air di dalam pipa membeku. Densitas (berat jenis) air maksimum sebesar 1 g/cm3 terjadinya pada suhu 3,95 °C. Pada suhu lebih besar maupun lebih kecil dari 3,95 °C, densitas air lebih kecil dari satu (Effendi,2003).
2.1.2 Penggolongan Air
Menurut Keputusan Menteri Negara Kependudukan dan Lingkungan hidup Nomor: KEP-02/MEN KLH/I/1998 tentang Pedoman Penetapan Baku Mutu Lingkungan Air, maka air dapat dibagi atas beberapa kriteria yaitu:
- Golongan A: Yaitu air yang dapat digunakan sebagai air minum secara langsung tanpa pengolahan terlebih dahulu. Contoh: mata air.
- Golongan B: Yaitu air yang dapat dipergunakan sebagai air baku untuk diolah sebagai air minum dan keperluan rumah tangga. Contoh: air sungai.
- Golongan C: Yaitu air yang dapat dipergunakan untuk keperluan perikanan dan
peternakan. Contoh: air tanah.
- Golongan D: Yaitu air yang dapat dipergunakan untuk keperluan pertanian dan
2.1.2. Pencemaran Air
Menurut Peraturan Menteri Kesehatan RI no 173/Menkes/VII/77 yaitu pencemaran air adalah suatu peristiwa masuknya zat kedalam air yang mengakibatkan kualitas (mutu) air tersebut menurun sehingga dapat mengganggu atau membahayakan kesehatan masyarakat. Menurut Peraturan Pemerintah RI no 20 tahun 1990 yaitu pencemaran air
adalah masuknya atau dimasukkannya mahluk hidup, zat, energi, dan atau komponen lain kedalam air oleh kegiatan manusia sehingga kualitas air turun sampai ketingkat tertentu
yang membahayakan , yang mengakibatkan air tidak berfungsi lagi sesuai dengan peruntukkannya ( Mukono,2005).
Pencemaran air dapat merupakan masalah regional maupun lingkungan global dan
sangat berhubungan dengan pencemaran udara serta penggunaan lahan tanah atau daratan. Pada saat udara yang tercemar jatuh ke bumi bersama air hujan , maka air tersebut sudah tercemar. Beberapa jenis bahan kimia untuk pupuk dan pestisida pada
lahan pertanian akan terbawa air kedaerah sekitarnya sehingga mencemari air pada permukaan lokasi yang bersangkutan. Pengolahan tanah yang kurang baik akan dapat
menyebabkan erosi sehingga air permukaan tercemar dengan tanah endapan. Dengan demikian banyak sekali penyebab terjadinya pencemaran air ini, yang akhirnya akan bermuara kelaut-an, menyebabkan pencemaran pantai dan laut sekitarnya (Darmono
2.1.3. Penanggulangan Terhadap Pencemaran Air
Pencemaran dapat menimbulkan dampak yang sangat luas dan merugikan sehingga perlu dilakukan usaha untuk menanggulanginya. Ada dua macam cara untuk menanggulangi pencemaran tersebut yaitu :
1. Penanggulangi secara non teknis
Yaitu suatu usaha untuk menanggulangi dan mengurangi pencemaran dengan cara
menciptakan peraturan perundangan yang dapat merencanakan, mengatur segala macam kegiatan industri yang meliputi :
• Penyajian informasi lingkungan (PIL)
• Analisis mengenai dampak lingkungan (AMDAL)
• Perencanaan kawasan kegiatan industri dan Teknologi
• Pengaturan dan pengawasan Kegiatan
• Menanamkan perilaku disiplin
2. Penanggulangi secara teknis
Yaitu suatu usaha menanggulangi pencemaran dengan cara teknis
Penanggulangi dengan cara ini adalah : • Mengubah proses
• Mengelolah limbah
• Menambah alat bantu (Wardhana,1999).
2.1.4. Dampak dari pencemaran Air
a. Mineral
Beberapa jenis mineral yang dapat memberikan dampak lingkungan pada pencemaran air
1. Cu (tembaga)
Dalam jumlah besar menyebabkan rasa tidak enak dilidah dan menimbulkan kerusakan pada ginjal dan hati.
2. Pb (timah hitam)
Keracunan Pb menimbulkan anemia, gangguan ginjal dan pada dalam jangka lama Pb berkumpul pada gigi dan tulang.
b. Mikrobiologi dalam air
Contoh penyakit yang ditimbulkan seperti disentri, disebabkan oleh Entamoeba histolitytica.
c. Pepstisida
Diantaranya yang paling berbahaya adalah senyawa organo klor seperti DDT
(Dichlor Diphenyl Trichloretan). DDT dapat larut dalam lemak sehingga memungkinkan terakumulasi dalam tubuh organisme. Percemaran air oleh
pestisida dapat menyebabkan kanker kulit, keracunan, kerusakaan jaringan dan pada konsentrasi tertentu akan menyebabkan kematian (Mukono,2005).
2.2. Air Tanah
Air Tanah merupakan sebagian air hujan yang mencapai permukaan bumi dan
tempat air tanah, air hujan akan menembus beberapa lapisan tanah dan menyebabkan
terjadinya kesadahaan pada air. Contoh air tanah adalah air sumur.
Sumur merupakan sumber utama persedian air bersih bagi penduduk yang tinggal didaerah perdesaan maupun diperkotaan indonesia. Secara teknis sumur dapat dibagi
menjadi 2 jenis :
1. Sumur dangkal (Shallow well)
Sumur semacam ini memiliki sumber air yang berasal dari resapan air hujan diatas permukaan bumi terutama didaerah dataraan rendah. Jenis sumur ini banyak terdapat di Indonesia dan mudah sekali terkontaminasi air kotor yang berasal dari kegiatan
mandi-cuci-kakus (MCK) sehingga persyaratan sanitasi yang ada perlu sekali diperhatikan.
2. Sumur Dalam (deep well)
Sumur ini memiliki sumber air yang berasal dari proses purifikasi alami air hujan oleh lapisan kulit bumi menjadi air tanah. Sumber airnya tidak terkontaminasi dan memenuhi
persyaratan sanitasi (Chandra,2005).
Kadar air tanah bervariasi antara batas-batas yang luas. Kadar air tanah dapat dikurangi, setelah pengeringan buatan, sampai pada air yang dihidrasi secara terpadu, dipihak lain, suatu tanah lapang dapat dipadati air sama sekali, dengan semua rongga
yang tak ditempati benda padat, diisi dengan air. Antara kedua hal yang ekstrim ini , pori-pori tanah dapat diisi dengan air sampai pada bermacam-macam tingkat, dengan
saluran-saluran yang tidak berputus-putus tetapi tak teratur, bervariasi dalam ukuran antara
saluran-saluran yang tak terhingga kecilnya sampai saluran-saluran yang berdiameter sekian banyak millimeter (Otto,1984).
2.3. Klorida
Kotoran manusia, khususnya urine, mengandung sejumlah klorida oleh karena
sebagian dari pada garam yang terdapat didalam makanan dan minuman turut dibuang dalam sampah tubuh itu . Tubuh manusia mengeluarkan delapan sampai lima belas gram
sodium klorida seharinya (Otto,1984).
Klorida dalam konsentrasi yang layak adalah tidak berbahaya bagi manusia. Klorida dalam jumlah kecil dibutuhkan untuk desinfektan, dapat menyebabkan rasa asin, dan
dapat merusak pipa-pipa air. Konsentrasi maksimal klorida dalam air yang ditetapkan sebagai standar persyaratan oleh Dep. Kes. R.I. adalah sebesar 200,0 mg/l sebagai konsentrasi maksimal yang dianjurkan, dan 600,0 mg/l sebagai konsentrasi maksimal
yang diperbolehkan (Sutrisno, 2004).
Ion klorida adalah anion yang dominan diperairan laut. Sekitar ¾ dari klorin (Cl2)
yang terdapat dibumi berada dalam bentuk larutan , Unsur klor dalam air terdapat dalam bentuk ion klorida (Cl-). Ion klorida adalah salah satu anion anorganik utama yang ditemukan diperairan alami dalam jumlah lebih banyak daripada anion halogen lainnya
Kadar klorida mencapai ratusan mg/liter. Keberadaan klorida pada perairan alami
berkisar antara 2-20 mg/liter. Air yang berasal dari daerah pertambangan mengandung klorida sekitar 1.700 ppm. Kadar klorida 250 mg/liter dapat mengakibatkan air menjadi asin. Air laut mengandung klorida sekitar 19.300 mg/liter dan urine mengandung klorida
hingga 200.000 mg/liter.
Kadar klorida yang tinggi, misalnya pada air laut , yang diikuti oleh kadar kalsium dan magnesium yang juga tinggi dapat meningkatan sifat korosivitas air. Perairan yang demikian mudah mengakibatkan terjadinya perkaratan peralatan yang terbuat dari logam (Mahida, 1984).
Klorida tidak bersifat toksik bagi mahluk hidup, bahkan berperan dalam pengaturan tekanan osmotik sel. Perairan yang diperuntukkan bagi keperluan domestik , termasuk
air minum , pertanian, dan industri. Sebaiknya memiliki kadar klorida lebih kecil dari 100 mg/liter.
Klorin sering digunakan sebagai desinfektan untuk menghilangkan mikroorganisme
yang tidak dibutuhkan , terutama bagi air yang diperuntukkan bagi kepentingan domestik. Proses penambahan klor dikenal dengan istilah klorinasi. Klorin yang
digunakan sebagai desinfektan adalah gas klor yang berupa molekul klor (Cl2) atau kalsium hipoklorit. Namun, penambahaan klor secara kurang tepat akan menimbulkan bau dan rasa pada air (Effendi, 2003).
Anion yang memberi garam-garam perak yang tidak dapat larut dalam asam nitrat encer , tak boleh ada ; ini meliputi bromida , iodida , tiosianat, sulfida, tiosulfat,
harus disingkirkan dengan pengendapan. Jika klorida itu tak dapat larut, ia perlu
dididihkan, dengan larutan natrium karbonat jenuh yang sangat berlebih, atau meleburnya dengan natrium karbonat dan mengekstraksi leburan dengan air (Vogel,1994).
Analisa klorida dapat dilakukan dengan beberapa cara, diantaranya analisa titrimetri dengan menggunakan metode argentometri. Metode yang sering digunakan pada
penetapan klorida adalah metode argentometri. Metode argentometri (titrasi pengendapan) dapat dilakukan dengan beberapa cara yang melibatkan ion perak,
diantaranya adalah cara Mohr, cara Volhard, dan cara Fajans. Pada titrasi ini biasanya digunakan larutan baku perak nitrat 0,1 M dan larutan baku Kalium Tiosianat 0,1 M. Kedua pereaksi ini dapat diperoleh sebagai zat baku utama, namun Kalium Tiosianat
sedikit mudah menyerap air sehingga larutannya perlu dibakukan dengan larutan perak nitrat. Namun, karena amonium tiosianat sangat mudah menyerap air, maka harus dibakukan dulu dengan larutan baku perak nitrat memakai cara titrasi Volhard (Rivai,
1995).
Faktor yang menyebabkan kelebihan titran berpengaruh kecil, tetapi untuk larutan
encer, masalahnya menjadi serius. Maka diperlukan faktor koreksi, yang dicapai dengan titrasi blanko (blank titration), yaitu diambil suspensi CaCO3 yang bebas ion Cl- dengan volume dan indikator sebanyak yang digunakan dalam titrasi sebenarnya,
lalu ditambah AgNO3 sampai tercapai wama tertentu; jumlah AgNO3 dikurangkan dari hasil titrasi sebenarnya, yang dilakukan sampai mencapai warna seperti blanko
2.4. Penentuan klorida dalam air
-Penentuan kadar klorida dalam air dapat dilakukan melalui beberapa metode yaitu metode merkurium (II) kloranilat , Metode merkur ium (II) tiosianat dan metode titrasi argentometri.
2.4.1 Metode merkurium (II) kloranilat.
Garam merkurium (III) asam dari klora nilat (2,5-dikloro-3,6-dihidroksi-p-benzokuinona dapat digunakan untuk penetapan jumlah kecil ion klorida. Reaksinya adalah:
HgC6Cl2O4 + 2Cl- + H+→ HgCl2 + HC6Cl2O
Banyaknya ion klora nilat-asam yang ungu kemerahan yang disebabkan itu sebanding
dengan konsentrasi ion-klorida. 2-Metoksi-etanol ditambahkan untuk menurunkan keter-larutan merkurium (II) kloranilat dan menekan disosiasi merkurium (II) klorida, asam nitrat ditambahkan (konsentrasi 0,05M) untuk memberikan absorbansi maksimum.
Pengukuran dilakukan pada 530 nm dalam daerah nampak atau 305 nm dalam daerah ultraviolet. Batas deteksi 0,2 ppm ion klorida; batas atas sekitar 120 ppm. Kebanyakan
kation, tetapi ion ammonium tidak mengganggu dan harus disingkirkan. Perak kloronilat tak dapat digunakan dalam penetapan karena menghasilkan perak klorida koloidal.
2.4.2. Metode merkurium (II) tiosianat.
hadirnya ion besi(III) akan terbentuk kompleks besi(III) tiosianat yang sangat berwarna,
dan intensitas warnanya itu berbanding lurus dengan konsentrasi ion-klorida yang asli. 2Cl- + Hg (SCN)2 + 2Fe3+↔ HgCL2 + 2[Fe(SCN)]2+
Metode ini dapat ditetapkan pada jangka kuantitas ion-klorida 0,5-100µg (Vogel,1994).
2.4.3. Titrasi Argentometri
2.4.3.1. Prinsip Argentometri
Reaksi pengendapan yang cepat mencapai kesetimbangan pada setiap penambahaan titran , tidak ada pengotor yang menggangu dan diperlukan indikator untuk melihat titik
akhir titrasi. Dimana zat yang hendak ditentukan kadarnya diendapkan oleh larutan baku AgNO3. Zat tersebut misalkan garam-garam halogenida (Cl, Br, I) , sianida (CN) ,
tiosianida (SCN) dan fosfat (Underwood dan Day,1994).
2.4.3.2. Jenis-Jenis Titrasi Argentometri
1. Metode Mohr
Metode ini terkenal dari keadaan demikian adalah yang disebut titrasi Mohr dari
klorida dengan ion perak , yang dalam hal ini ion khromat yang kemerah-merahan dianggap sebagai titik akhir titrasi. Akan tetapi konsentrasi yang demikian tinggi tidak dapat digunakan didalam praktek , karena warna kuning ion khromat membuat sukar
khromat sebesar 0,005 sampai 0,01 M digunakan. Titrasi Mohr terbatas pada
larutan-larutan dengan harga pH dari kisaran 6 sampai 10.
Cara Mohr dapat juga digunakan untuk titrasi ion bromida dengan perak dan juga ion sianida dalam larutan sedikit alkalis . Akibat absorpsi membuat titrasi ion iodida dan
tiosianat tidak mungkin dapat dilaksanakan. Perak tidak dapat dititrasi secara langsung dengan klorida dengan menggunakan indikator khromat. Endapan perak khromat, yang
semula ada, larut kembali hanya perlahan-lahan dekat titik ekuivalen. Akan tetapi larutan standart dalam jumlah berlebih dapat ditambahkan dan kemudian dititrasi kembali dengan menggunakan indikator khromat (Underwood dan Day, 1994).
Kelebihaan Metode Mohr
• biasanya digunakan untuk menitrasi ion halida seperti NaCl, dengan
AgNO3 sebagai titran dan K2CrO4 sebagai indikator.
• Cara Mohr dapat juga digunakan untuk titrasi ion bromida dengan perak dan juga
ion sianida dalam larutan sedikit alkalis.
Kekurangan metode Mohr yaitu:
• Pengaturan pH sangat perlu, agar tidak terlalu rendah ataupun tinggi. Bila terlalu
tinggi, dapat terbentuk endapan AgOH yang selanjutnya terurai menjadi Ag2O
sehingga titran terlalu banyak terpakai.
Bila pH terlalu rendah, ion CrO4- sebagian akan berubah menjadi Cr2O72- karena
reaksi
2H+(aq) + 2CrO42-(aq)↔ Cr2O72- +H2O(l)
Selama titrasi Mohr, larutan harus diaduk dengan baik. Bila tidak, maka akan terjadi
kelebihan titrant yang menyebabkan indikator mengendap sebelum titik ekivalen tercapai (Rivai, 1995).
2. Metode Volhard
Metode Volhard menggunakan NH4SCN atau KSCN sebagai titrant, dan larutan
Fe3+sebagai indikator. Sampai dengan titik ekivalen harus terjadi reaksi antara titrant dan Ag sehingga membentuk endapan putih.
Ag+(aq) + SCN-(aq)↔ AgSCN(s)↓ (putih)
Cara Volhard didasarkan pada pengendapan perak tiosianat dalam larutan asam nitrat, dengan menggunakan ion besi (III) untuk meneliti ion tiosianat berlebih. Cara ini dapat digunakan untuk titrasi langsung dari perak dengan larutan tiosianat standar atau untuk
titrasi tak langsung dari ion klorida. Pada keadaan terakhir ini perak nitrat berlebih ditambahkan dan kelebihannya dititrasi dengan tiosianat standar. Anion-anion lain
seperti bromida dan iodida dapat ditentukan dengan prosedur sama. Anion asam-asam lemah seperti oksalat ,karbonat dan arsenat, dengan garam-garam peraknya yang larut dalam asam,dapat ditentukan dengan pemgendapan pada pH lebih tinggi dan penyaringan
Cara Volhard secara luas digunakan untuk perak dan klorida karena kenyataan bahwa
titrasi dapat dilakukan dalam larutan asam. Cara-cara umum lain untuk perak dan klorida memerlukan larutan hampir netral agar titrasi berhasil baik. banyak kation mengendap pada keadaan demikian , dan karenanya mengganggu pada cara-cara ini. merkuri
merupakan kation umum satu-satu-nya yang mengganggu dengan cara Volhard (Underwood dan Day,1994).
Kelebihaan metode Volhard yaitu :
• Cara Volhard dapat digunakan untuk titrasi langsung dan tidak langsung.
• Penentuan kadar perak dapat menggunakan titrasi langsung.
• Cara titrasi tidak langsung dapat digunakan untuk menentukan kadar klorida,
dimana pada cara tidak langsung, cuplikan klorida direaksikan dengan perak nitrat berlebih. Kelebihan perak nitrat dititrasi dengan tiosianat standar yang diketahui
konsentrasinya. Titik akhir titrasi dapat diketahui dengan terbentuknya warna merah dari kompleks besi (III) tiosianat
Kekurangan metode Volhard yaitu :
• Konsentrasi indikator dalam titrasi Volhard juga tidak boleh sembarang, karena
titrant bereaksi dengan titrat maupun dengan indikator, sehingga kedua reaksi itu saling mempengaruhi.
• Sedikit kelebihan titrant kemudian bereaksi dengan indikator, membentuk ion
SCN-(aq) + Fe3+(aq)↔ FeSCN2+(aq) (Rivai, 1995).
• Merkuri merupakan kation umum satu-satu-nya yang mengganggu dengan cara
Volhard (Underwood dan Day,1994).
2.4.2.3. Metode Fajans
Dalam titrasi Fajans digunakan indikator adsorpsi. Indikator adsorpsi ialah zat yang
dapat diserap pada permukaan endapan (diadsorpsi) dan menyebabkan timbulnya warna. Penyerapan ini dapat diatur agar terjadi pada titik ekivalen, antara lain dengan memilih
macam indikator yang dipakai dan pH.
Cara kerja indikator adsorpsi ialah sebagai berikut: indikator ini ialah asam lemah atau basa lemah organik yang dapat membentuk endapan dengan ion perak.
Misalnya fluoresein yang digunakan dalam titrasi ion klorida. Dalam larutan, fluoresein akan meng-ion (untuk mudahnya ditulis HFl saja).
HFl(aq) ↔ H+(aq) +Fl-(aq)
Ion Fl- inilah yang diserap oleh endapan AgX dan menyebabkan endapan berwarna merah muda. Apabila suatu senyawa organik berwarna diserap pada permukaan suatu endapan .
Perubahaan struktur organik mungkin terjadi, dan warnanya sebagian besar kemungkinan telah berubah dan mungkin menjadi lebih jelas. Peristiwa ini dapat dipakai untuk
Mekanisme bekerja dari indikator demikian berbeda dari apapun. Beberapa fluoresein
yang disubstitusikan dapat bekerja sebagai indikator untuk titrasi perak. Jika perak nitrat ditambahkan kepada suatu larutan natrium klorida , maka partikel perak klorida yang terbagi halus itu cenderung menahan pada permukaannya (menyerap) beberapa ion
klorida berlebih yang ada didalam larutan (Underwood dan Day,1994).
Kelebihan metode Fajans yaitu:
• Titrasi menggunakan indikator adsorpsi biasanya cepat, akurat dan terpercaya
Kelemahan metode Fajans yaitu:
• Suatu kesulitan dalam menggunakan indikator adsorpsi ialah, bahwa banyak
diantara zat warna tersebut membuat endapan perak menjadi peka terhadap cahaya
(fotosensifitasi) dan menyebabkan endapan terurai.
• Sebaliknya penerapannya agak terbatas karena memerlukan endapan berbentuk
BAB III
METODOLOGI PERCOBAAN
3.1. Alat dan Bahan
3.1.1. Alat-Alat
• Buret 50 ml
• Gelas Erlenmeyer 250 ml
• Gelas ukur 100 ml
• Corong gelas
• Labu ukur 100 ml
• Beaker Glass 250 ml
• Pipet Volume 5 ml
• Botol Aquadest
• Neraca Analitis
• Spatula
• Gelas Arloji
• Desikator
• Statif dan klem
• pipet Tetes
3.1.2. Bahan
• Larutan indikator Kalium Kromat (K2CrO4) 5% b/v
• Kertas Saring
• Air Sumur
• Air Minum
• Larutan Natrium Hidroksida (NaOH) 1 N
• Larutan Asam Sulfat (H2SO4) 1 N
• Air suling bebas klorida
• Larutan Natrium Klorida (NaCl) 0.0141 N
• Larutan baku Perak Nitrat (AgNO3) 0.0141 N
3.2. Prosedur Kerja
3.2.1. Pembuatan Larutan
1. Larutan Natrium Klorida (NaCl) 0.0141 N
a. Keringkan serbuk NaCl dalam oven pada suhu 140ºC selama 2 jam, kemudian
b. Timbang 824 mg NaCl kering, kemudian larutkan dengan air suling bebas
klorida di dalam labu ukur 1000 ml. tepatkan sampai tanda tera dengan air suling bebas klorida
1. Larutan indikator Kalium Kromat (K2CrO4) 5% b/v
Timbang kasar K2CrO4 dan masukkan kedalam Beaker gelas. Tambahkan akuades kedalam Beaker gelas yang berisi K2CrO4 dan homogenkan.
2. Larutan baku Perak Nitrat (AgNO3) 0.0141 N
Larutkan 2.395 g AgNO3 dengan air suling bebas klorida dalam labu ukur 1000 ml dan tepatkan sampai tanda tera. Lakukan pembakuan dengan menggunakan
larutan NaCl 0.0141 N. simpan di dalam botol berwarna coklat.. 3. Larutan Natrium Hidroksida (NaOH) 1 N
Larutkan 4 gr NaOH dengan air suling bebas klorida ke dalam labu ukur 100 ml dan tepatkan sampai tanda tera.
4. Larutan Asam Sulfat (H2SO4) 1 N
pipet 2.8 ml asam sulfat pekat kedalam labu ukur 100 ml yang sudah berisi 50 ml air suling bebas klorida. Tambahkan air suling bebas klorida sampai tepat tanda
tera.
3.2.2 Persiapan Sampel
c. Jika pH tidak pada kisaran 7 s/d 10, atur dengan menambahkan larutan NaOH 1 N
atau H2SO4 1N
3.2.3. Standarisasi Larutan Perak Nitrat (AgNO3)
a. Pipet 25 ml larutan NaCl 0.0141 N masukkan ke dalam gelas Erlenmeyer 100 ml.
buat larutan blanko menggunakan 25 ml air suling
b. Tambahkan 1 ml larutan indikator K2CrO4 5% b/v dan diaduk
c. Titrasi dengan larutan AgNO3 sampai terjadi warna merah kecoklaan
d. Catat volume larutan AgNO3 yang digunakan untuk contoh uji (A ml) dan blanko (B ml)
e. Hitung normalitas larutan baku AgNO3 dengan rumus
N AgNO3= V1 x N1
VA x VB
Dimana :
VA = volume larutan baku AgNO3 untuk titrasi larutan NaCl (ml)
VB = volume larutan baku AgNO3 untuk titrasi blanko (ml) V1 = volume larutan NaCl yang digunakan (ml)
N1 =normalitas larutan NaCl yang digunakan
3.2.4. Prosedur Analisa klorida dalam air
1. Pipet 100 ml larutan sampel, masukkan ke dalam gelas Erlenmeyer 250 ml. Buat
3. Titrasi dengan larutan baku AgNO3 sampai titik akhir titrasi yang ditandai dengan
terbentuknya warna kuning kemerahan dari AgCrO4. Catat volume AgNO3 yang digunakan.
4. Lakukan titrasi blanko seperti langkah no. 3.
Perhitungan
Kadar Klorida (mg L ) =
(A – B)x N x 35450
� x 1000
Dimana:
A = volume larutan baku AgNO3 untuk titrasi sampel (ml)
B = volume larutan baku AgNO3 untuk titrasi blanko (ml) N = normalias larutan baku AgNO3
BAB IV
HASIL DAN PEMBAHASAN
4.1. Data Percobaan
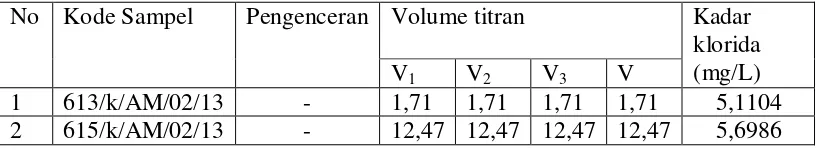
Tabel 4.1. Hasil Analisa Klorida Untuk Air Minum
No Kode Sampel Pengenceran Volume titran Kadar klorida (mg/L) V1 V2 V3 V
1 613/k/AM/02/13 - 1,71 1,71 1,71 1,71 5,1104 2 615/k/AM/02/13 - 12,47 12,47 12,47 12,47 5,6986
Tabel 4.2. Hasil Analisa Klorida untuk Air Sumur
4.3. Perhitungan kadar Klorida
4.3.1. Pada air Sumur
Penentuan Normalitas AgNO3
AgNO3 =� ���� �� ���� � AgNO3
= 25 x 0.0141
25,8
= 0,0136 N
Penentuan Kadar Klorida pada Sampel Air Sumur
- Sampel Air Sumur Gaharu
mg/ L Cl- =(6,03−0,65)X 0,0136 X35,45 x 1000
100
- Sampel Air Sumur Velankani
mg/L Cl- = (2,1−0,65) X 0,0136 X 35,45 X 1000
100
= 6,9907
- Sampel Air Sumur Marelan
mg/L Cl- = (8,46−0,65) X 0,0136 X 35,45 X 1000
100
= 37,6535
• Pada Air Minum
- Kode Sampel 613/k/AM/02/13
mg/L Cl- =(1,71−0,65)X 0,0136 X 35,45 X 1000
100
= 5,1104
- Kode Sampel 615/k/AM/02/13
mg/L Cl- = (12,47−0,65 )X 0,0136 X 35,45 X 100
100
4.5. Pembahasan
Berdasarkan PERMENKES 416/MENKES/PER/IX/1990 dan PERMENKES 492/MENKES/PER/IV/2010 nilai maksimum untuk parameter klorida di dalam air
tanah adalah 600 mg/L dan di dalam air minum adalah 250 mg/L.
Berdasarkan pengendapan bertingkat dimana Cl- dari NaCl dititrasi dengan larutan standart AgNO3 menghasilkan AgCl↓ yang mengalami perubahaan warna putih dan kelebihaan AgNO3 akan bereaksi dengan indikator K2CrO4 5% akan menghasilkan AgCrO4↓ yang mengalami perubahaaan warna kuning kemerahaan. dan hasil kali kelarutan (Ksp) AgCl diperoleh 1,78 x 10-10 lebih besar dari pada hasil kali kelarutan
(Ksp) Ag2CrO4 diperoleh 1,29 x 10-12 , Apabila Hasil kali kelarutan (Ksp) AgCrO4 lebih besar dari pada hasil kali kelarutan (Ksp) AgCl maka AgCl akan mengendap.
Dan dari percobaan yang telah dilakukan , sampel air minum 613/k/AM/02/13 diperoleh hasil 5,1104 mg/l, sampel air minum 615/k/AM/02/13 diperoleh hasil 5,6986 mg/l dan sampel air sumur gaharu adalah 25,9380 mg/l , air sumur velankani adalah
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Dari hasil uji kadar Klorida (Cl-) pada beberapa uji dapat diperoleh kesimpulan bahwa kadar klorida yaitu untuk sampel air sumur gaharu: 25,9380 ml/L. Untuk sampel air sumur velankani: 6,9907 mg / L. Untuk sampel Air sumur marelan : 171,52 mg / L dan air minum kode sampel 613/k/AM/02/13 : 5,1104 mg/L dan air minum kode sampel 615/k/AM/02/13 : 5,6986 mg/L .
2. Dan yanmg dianalisa bahwa kadar klorida pada sampel air minum dan air sumur tersebut berada dibawah batas maksimal yang telah ditetapkan oleh PERMENKES 416/MENKES/PER/IX/1990 dan PERMENKES 492/MENKES/PER/IV/
201 0sehingga layak untuk dikonsumsi dan dipakai sehari-hari
.
5.2. Saran
DAFTAR PUSTAKA
Chandra, B. 2005. Pengantar Kesehatan Lingkungan. Jakarta : Penerbit Buku Kedokteraan EGC.
Darmono. 2001. Lingkungan Hidup dan Pencemaran . Jakarta: Penerbit UI. Press
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Yogyakarta: Kanisius
Harjadi, W. 1986. Ilmu Kimia Analitik Dasar. Jakarta : PT Gramedia
Harizul, Rivai. 1995. Asas Pemeriksaan Kimia. Jakarta : UI Press
Mukono, H.J. 2005. Prinsip Dasar Kesehatan Lingkungan. Jakarta : Airlangga. University Press.
Mahida, U. N. 1984. Pencemaran Air dan Pemanfaatan Limbah Industri. Jakarta : C.V. Rajawali.
Otto, S. 1984. Pencemaran Air. Jakarta: Penerbit C.V. Rajawali
Sutrisno, T., 2004. Teknologi Penyediaan Air Bersih, PT Rineka Cipta, Jakarta.
Underwood .A.L.dan Day.R.A. 1994. Analisa Kimia Kuantitatif. Terjemahaan Bahasa Aloysius Hadyana Pudjaatmaka. Edisi Ke-4. Jakarta : Erlangga.
Vogel. 1990. Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Jakarta : PT. Kalman Media Pustaka.
13 ZAT ORGANIK mg/l 10
14 SIANIDA mg/l 0,1
15 pH - 6,5 – 9
16 NITRAT mg/l 10
17 SUHU C DEVIASI 3 C
18 KLORIDA mg/l 600
19 KROMIUM VAL 6 mg/l 0,05
20 DETERJEN mg/l 0,5
21 WARNA TCU 50
22 KEKERUHAN NTU 25
23 TDS mg/l 1500
24 SULFAT mg/l 400
25 KESADAHAN mg/l 500
Lampiran 5 AIR MINUM
PERMENKES 492/MENKES/PER/IV/2010
NO PARAMETER SAT BAKU MUTU
1 BAU - Tdk Berbau
2 RASA - Tdk Berasa
3 Fe mg/l 0,3
4 Mn mg/l 0,4
Lampiran 6
BAKU MUTU MIKROBIOLOGI AIR PADA AIR MINUM NOMOR : 492/MENKES/PER/IV/2010
BAKU MUTU MIKROBILOGI AIR PADA AIR BERSIH PERMENKES 416/MENKES/PER/IX/1990
NO. Jenis Parameter Satuan Kadar Max yang diperbolehkan 1. Total Bakteri Coliform Jumlah/100ml - Perpipaan
10 Jumlah/100ml - Non