THE FORMULATION AND SHELF LIFE DETERMINATION OF
FUNCTIONAL BEVERAGE MADE FROM THE MIXTURE OF RED BETEL
EXTRACT, CINNAMON, GINGER, AND LIME EXTRACT
Sarinah Monica and Sedarnawati Yasni
Department of Food Science and Technology, Faculty of Agricultural Engineering
and Technology, Bogor Agricultural University, IPB Darmaga Campus,
PO BOX 220, Bogor, West Java, Indonesia
Phone: +62 8999 89 4129, e-mail: sarinahmonica@gmail.com
ABSTRACT
There were many studies about potential of red betel leaves in case of diabetes prevention. One study showed the potential of red betel as antihyperglicemic either alone or in a mixture with other materials. This study aims to improve the taste of the functional beverage, analyze volatile components, and determine the shelf life of the functional beverage. This study begins with the preparation of raw materials, followed by selected functional beverage formulation, bottling, shelf life estimation, and the transformation of a shelf life into expiration time. At the beginning of the study, improvement of beverage is done by adding lime juice in 5 levels of comparison, either in the form of extracts of whole fruit or fruit juice broth, sensory testing to get 3 formula was selected, and determination of the characteristics of functional drinks. The results showed that the addition of lime juice at volume ratio of red betel, ginger, cinnamon, and lime is 5:4:3:4 with panelists approached the level of preference “rather like”. Level of preference is approximately equal to the level of preference
drinks before coupled with lemon, but increased inhibition of the enzyme α-glucosidase to 79.51%, has the antioxidant capacity of 442.09 ppm AAE and 411.75 ppm for total phenols.
The bottling process is done by pasteurization at a temperature of 63°C for 30 minutes and drink packaged in dark glass bottle. The beverages that have been bottled is then stored at three different temperatures (5°C, 30°C, and 50°C). Furthermore, the stability observed during 6 weeks of storage products includes pH, TAT, total phenol, TPC, and color using the Accelerated Storage Studies (ASS). Determination of the reaction rate of food deterioration by temperature differences do with the Arrhenius method. Now we know the shelf life of each of the above parameters, the two parameters are determined for the shortest shelf life, namely pH and color (value b). Improvement formula-based beverages with the addition of red betel lime juice can increase preference panelists to drink with the main volatile components are α-curcumene and zingiberene, and shelf life of beverages was 87 days.
Sarinah Monica. F24080029. Formulasi dan Penentuan Umur Simpan Minuman Fungsional Campuran Sirih Merah, Jahe, Kayu Manis, dan Jeruk Nipis. Di bawah bimbingan Sedarnawati Yasni. 2012
RINGKASAN
Indonesia memiliki sumber daya alam yang berlimpah, termasuk tanaman-tanaman herbal yang bermanfaat bagi kesehatan. Sirih merah diketahui dapat mengobati berbagai macam penyakit, termasuk diabetes mellitus. Berkaitan dengan posisi Indonesia sebagai peringkat ke-4 jumlah penderita diabetes, kemampuan sirih merah untuk menurunkan kadar glukosa darah perlu dimanfaatkan secara maksimal dalam rangka mendukung program pemerintah terkait dengan peningkatan kesehatan masyarakat menggunakan bahan alami. Penelitian ini merupakan penelitian lanjutan terkait perbaikan formula minuman fungsional berbahan utama sirih merah agar penerimaan citarasanya dapat ditingkatkan dengan penambahan ekstrak jeruk nipis. Oleh karena itu, tujuan penelitian ini adalah: (1) memperbaiki citarasa dengan penambahan jeruk nipis dan mengkaji pengaruhnya terhadap peningkatan kapasitas antioksidan dan aktivitas enzim α-glukosidase, (2) menganalisis komponen volatil yang berperan dalam pembentuk citarasa, dan (3) menentukan umur simpan minuman fungsional formula terpilih dengan metode akselerasi.
Penelitian terdahulu menunjukan potensi sirih merah sebagai antihiperglikemik baik secara tunggal maupun dalam campuran dengan bahan lain. Penelitian ini diawali dengan persiapan bahan baku, dilanjutkan dengan perbaikan formula minuman fungsional dengan penambahan jeruk nipis dan pembotolan formula minuman fungsional terpilih untuk selanjutnya dilakukan pendugaan umur simpan, serta transformasi umur simpan menjadi waktu kadaluwarsa. Persiapan bahan baku berupa pengeringan dan ekstraksi dengan air, kecuali jeruk nipis digunakan dalam bentuk segar. Perbaikan formula minuman fungsional dilakukan dengan penambahan jeruk nipis pada 5 tingkat perbandingan, baik dalam bentuk ekstrak buah utuh atau perasan air daging buah, dan dilanjutkan uji sensori dengan panelis terbatas untuk mendapatkan 3 formula terpilih, serta penentuan karakteristik minuman fungsional. Penambahan jeruk nipis dalam bentuk air perasan daging buah pada perbandingan volume sirih merah:jahe:kayu manis:jeruk nipis 5:4:3:4 menunjukkan tingkat kesukaan panelis mendekati agak suka. Karakteristik dari minuman fungsional terpilih adalah kadar air 85,24% (bb), kadar abu
2,37% (bk), kadar protein 0,41% (bk), total gula 5,0525%, massa jenis 1,07 g/ml, TPT 15,63 oBrix,
viskositas 9,62 mPa.s, kapasitas antioksidan 1348,0909 ppm, total fenol 424,75 ppm, pH 3,84, TAT 278,75 ml NaOH/100 ml contoh, dan warna coklat kekuningan. Komponen volatil utama yang
teridentifikasi dari minuman fungsional adalah -curcumene, geraniol acetate, p-menth-1-en-8-ol, dan
zingiberene.
Pada tahap proses pembotolan dilakukan pasteurisasi pada suhu 63oC selama 30 menit dalam
wadah botol gelas gelap kemudian minuman yang sudah dibotolkan disimpan pada tiga suhu berbeda,
yaitu 5oC, 30oC, dan 50oC selama 6 minggu, dan parameter merliputi pH, TAT, total fenol, TPC, dan
warna dengan metode Accelerated Storage Studies (ASS). Penentuan kecepatan reaksi penurunan
mutu bahan pangan pada suhu penyimpanan yang berbeda dilakukan dengan metode Arrhenius. Setelah diketahui umur simpan pada masing-masing parameter, dipilihlah dua parameter dengan umur simpan tersingkat, yaitu pH dan warna (nilai b). Perbaikan formula minuman berbahan dasar sirih merah dengan penambahan air perasan jeruk nipis dapat meningkatkan kesukaan panelis terhadap
minuman dengan komponen volatil utama adalah α-curcumene dan zingiberene, serta umur simpan
1
I.
PENDAHULUAN
1.1.
Latar Belakang
Indonesia memiliki sumber kekayaan alam yang berlimpah, termasuk berbagai jenis tanaman-tanaman herbal. Dari berbagai macam tanaman herbal, hanya beberapa jenis yang telah diketahui manfaatnya bagi kesehatan karena terbatasnya pengetahuan masyarakat dalam mengolah tanaman-tanaman herbal tersebut menjadi minuman fungsional yang bermanfaat bagi kesehatan (Menteri Kesehatan Indonesia 2007). Proses pengolahan tanaman herbal menjadi minuman fungsional memerlukan pengetahuan tentang kandungan senyawa aktif dan teknik formulasi agar citarasa yang dihasilkan dapat diterima masyarakat serta fungsinya bagi kesehatan dapat dipertanggungjawabkan.
Salah satu tanaman herbal yang tercatat memiliki manfaat untuk kesehatan adalah sirih merah. Menurut Duryatmo dan Nyuwan (2005), pada era 1990-an tanaman sirih merah masih dikenal sebagai tanaman hias saja dan sampai dengan tahun 2005 belum ada penelitian yang mengungkapkan kandungan sirih merah meskipun sudah lebih dikenal sebagai tanaman obat. Sebagai tanaman obat (fitofarmaka), sirih merah dapat mengobati diabetes melitus, hipertensi, leukemia, hepatitis, TBC, maag akut, batu ginjal, ambeien, serangan jantung, radang prostat, asam urat, dan kanker payudara (Sudewo 2005).
Kemampuan sirih merah untuk menurunkan kadar glukosa darah perlu dimanfaatkan secara maksimal dalam rangka mendukung program pemerintah terkait dengan peningkatan kesehatan masyarakat menggunakan bahan alami. Oleh karena itu, kajian mengenai formulasi minuman fungsional berbahan dasar sirih merah ini bertujuan untuk mengoptimalkan daya guna sirih merah. Hasil penelitian Yasni et al. (2010) menunjukkan bahwa minuman fungsional yang terdiri dari campuran ekstrak air sirih merah, kayu manis, dan jahe terbukti dapat menghambat aktivitas enzim alfa-glukosidase sebesar 71.9%, memiliki kapasitas antioksidan sebesar 774.4 ppm (AAE), dan dapat menurunkan kadar glukosa darah sebesar 55.4%. Meskipun sifat fungsional yang baik
tersebut, penerimaan terhadap rasa, warna, dan overall dari minuman fungsional tersebut masih
belum optimal (masih pada skala agak disukai). Oleh karena itu, perlu dilakukan perbaikan formula melalui penambahan ekstrak air jeruk nipis untuk memperbaiki citarasa dan sekaligus dapat meningkatkan kapasitas antioksidan dan/atau aktivitas enzim α-glukosidase dari minuman fungsional tersebut. Selanjutnya, perlu dilakukan kajian umur simpan produk guna mendukung aspek komersialisasinya.
1.2.
Tujuan
Tujuan penelitian ini adalah:
1. memperbaiki citarasa minuman fungsional berbasis sirih merah terdahulu dengan penambahan ekstrak air jeruk nipis, dan mempelajari pengaruhnya terhadap kapasitas antioksidan dan aktivitas enzim α-glukosidase
2. menganalisis komponen volatil yang berperan dalam pembentuk citarasa minuman fungsional berbasis sirih merah
2
II.
TINJAUAN PUSTAKA
2.1.
Pangan Fungsional
Ada berbagai macam definisi atau pengertian mengenai pangan fungsional. Istilah pangan fungsional bukanlah istilah gizi biasa, tetapi ada berbagai istilah yang digunakan untuk
menyatakan pangan fungsional, seperti nutraceuticals, medical foods, atau designer foods (Guo
2000). Menurut ILSI Europe, sebuah forum yang mewakili industri, akademisi, dan pemerintahan, pangan fungsional adalah suatu pangan yang dapat memberikan manfaat bagi satu atau lebih fungsi dalam tubuh, melebihi manfaat gizi biasanya dari suatu pangan, dalam kaitannya dengan kesehatan dan/atau dalam mengurangi risiko dari suatu penyakit (Arnoldi 2000). Pangan fungsional dapat dikonsumsi seperti pangan pada umumnya dan memiliki penampakan seperti pangan pada umumnya (Guo 2000).
Indonesia sudah memiliki ketentuan pangan fungsional, yaitu Ketentuan Pokok Pengawasan Pangan Fungsional yang ditetapkan melalui Peraturan Kepala Badan POM No. HK.00.5.52.0685 tahun 2005. Menurut ketentuan tersebut, pangan fungsional adalah pangan olahan yang mengandung satu atau lebih komponen fungsional yang berdasarkan kajian ilmiah mempunyai fungsi fisiologis tertentu, terbukti tidak membahayakan, dan bermanfaat bagi kesehatan. Kelompok komponen pangan fungsional adalah vitamin, mineral, gula alkohol, asam lemak tidak jenuh, asam amino, serat pangan, prebiotik, probiotik, kloin, lesitin dan inositol, karnitin dan skualen, isoflavon, fitosterol dan fitostanol, dan polifenol.
2.2.
Sirih Merah
Tanaman sirih termasuk dalam famili Piperaceae, tumbuhan jenis ini merambat dan bersandar pada batang pohon lain (Duryatmo dan Nyuwan 2005). Salah satu jenis sirih yang termasuk ke dalam famili Piperaceae adalah sirih merah. Berdasarkan kajian ilmiah sirih merah termasuk : kingdom Plantae, subkingdom Tracheobionta, super divisi Spermatophyta, divisi
Magnoliophyta, kelas Magnoliopsida, ordo Piperales, famili Piperaceae, genus Piper, dan spesies
Piper crocatum.
Tanaman sirih merah tumbuh menjalar seperti halnya sirih hijau keunguan dan tidak berbunga. Daun bertangkai membentuk jantung dengan bagian atas meruncing, bertepi rata, dan permukaannya mengkilap atau tidak berbulu. Panjang daunnya dapat mencapai 15 -20 cm. Warna daun bagian atas hijau bercorak warna putih keabu-abuan. Bagian bawah daun berwarna merah hati cerah. Daunnya berlendir, berasa sangat pahit, dan beraroma wangi khas sirih. Batang tanaman bersulur dan beruas dengan jarak buku 5-10 cm dan disetiap buku tumbuh bakal akar. Tanaman sirih merah dapat tumbuh baik ditempat yang teduh dan tidak telalu banyak terkena sinar matahari (Sudewo 2005). Menurut Salim (2006) rebusan daun sirih merah mengandung alkaloid, flavonoid, dan tanin, serta tidak bersifat toksik bagi hewan coba dan dapat menurunkan kadar glukosa darah pada dosis 20 g/kg BB. Penurunan kadar glukosa darah tersebut terjadi melalui
3
2.3.
Jahe
Jahe adalah umbi dari pohon Zingiber officionale Roscoe yang termasuk dalam famili
Zingiberaceae. Tanaman ini tergolong tanaman herba, tegak, dan dapat mencapai ketinggian 40-100 cm. Akarnya sering disebut rimpang jahe, bercabang tak beraturan, berserat kasar, menjalar mendatar, dan bagian dalam rimpang berwarna kuning pucat (Koswara 2006).
Jahe mengandung minyak atsiri dan oleoresin yang menyebabkan aroma harum dan rasa pedas. Kandungan minyak atsiri sebesar 1-3 persen dengan kandungan utama berupa zingiberen dan zingiberol. Komponen oleoresinnya terdiri atas gingerol dan zingiberen, shagaol, minyak atsiri, dan resin. Pemberi rasa pedas utama adalah zingerol. Jahe diketahui mengandung antioksidan yang membantu menetralkan efek merusak dari radikal bebas di dalam tubuh (Koswara 2006). Jahe ini juga diketahui memiliki potensi antihiperglikemia dengan dosis sebesar
500 mg/kg BB pada tikus yang diinduksi diabetes dengan streptozotocin (STZ) (Al-amin et al.
2006).
2.4.
Kayu Manis
Kayu manis merupakan tumbuhan berdaun rimbun yang tingginya mencapai 16 m.
Tumbuhan ini termasuk famili Lauraceae. Kayunya agak pejal dan berat tetapi tidak keras serta
berwarrna coklat atau merah muda. Daunnya berwarna merah atau hijau (Syukur dan Hernani
2002). Minyak atsiri kayu manis dari Indonesia digolongkan dalam cassia oil karena kesamaan
kandungan sinamiladehidanya dalam tanaman dan memiliki aroma yang disukai masyarakat,
sehingga banyak digunakan sebagai flavor makanan (Wuri et al. 2004).
Salah satu potensi ekstrak kayu manis bagi kesehatan adalah sebagai
anti-hiperkolesterolemia yang terbukti dapat menurunkan kolesterol total serum (Azima et al. 2004).
Potensi lain kayu manis adalah sebagai antioksidan karena kandungan senyawa tannin dan eugenolnya (King 2000). Sinamaldehid pada minyak kayu manis diketahui dapat menghambat
enzim -glukosidase dengan konsentrasi penghambatan sebesar 93,29% pada konsentrasi 50 ppm
(Ngadiwiyana et al. 2011).
2.5.
Jeruk Nipis
Jeruk nipis (Citrus aurantifolia) merupakan tumbuhan yang diduga berasal dari dataran
Cina dan menyebar luas ke berbagai negara di dunia. Jeruk nipis tumbuh optimal pada dataran
rendah sampai dataran tinggi dengan suhu udara berkisar 25oC–30oC. Buah yang dihasilkan
berbentuk bundar, pada waktu muda berwarna hijau namun setelah tua (matang) berubah menjadi kuning cerah. Cita rasa buah sangat masam dan berbau sedap dengar kadar asam sitrat ±6%. Daging buah berwarna putih, berair asam, wangi, dan kadar vitamin C-nya tinggi. Komposisi
minyak atsirinya antara lain limonen, α-pinen, mirsen, β-pinen, sabinen, dan isokamfen yang
4
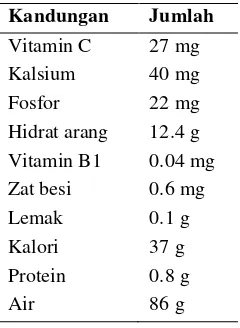
Kandungan vitamin C yang tinggi dari jeruk nipis sangat berguna sebagai antioksidan dan meningkatkan daya tahan tubuh sehingga kuman-kuman patogen dapat dimatikan oleh tubuh. Kandungan buah jeruk nipis dalam tiap 100 g dapat dilihat pada Tabel 1 (Trisbiantara 2008).Tabel 1. Kandungan buah jeruk nipis
Kandungan Jumlah
Vitamin C 27 mg
Kalsium 40 mg
Fosfor 22 mg
Hidrat arang 12.4 g
Vitamin B1 0.04 mg
Zat besi 0.6 mg
Lemak 0.1 g
Kalori 37 g
Protein 0.8 g
Air 86 g
2.6.
Antioksidan
Antioksidan adalah senyawa yang dapat menyumbangkan satu atau lebih elektron kepada radikal bebas, sehingga radikal bebas dapat diredam (Sunarni 2005). Antioksidan dibagi menjadi dua kelompok, yaitu antioksidan primer yang dapat bereaksi dengan radikal bebas membentuk produk yang lebih stabil dan antioksidan sekunder atau antioksidan pelindung yang berperan dalam mereduksi kecepatan rantai inisiasi melalui berbagai macam mekanisme dan berperan dalam memperlambat laju autooksidasi lemak dengan cara mengikat ion logam, memecah hidroperoksida menjadi spesies non radikal, menyerap radiasi ultraviolet, dan menginaktifkan oksigen singlet (Winarti 2010).
Ada berbagai macam antioksidan yang ditawarkan pada masyarakat, yaitu antioksidan alami dan antioksidan sintetik. Menurut Sofia (2006), antioksidan alami dalam makanan dapat berasal dari (a) senyawa endogenous dari satu atau lebih komponen makanan, (b) substansi yang terbentuk dari hasil reaksi selama pengolahan, dan (c) bahan tambahan makanan yang diisolasi dari sumber alami. Sebagian besar antioksidan alami berasal dari tanaman. Beberapa sumber umum antioksidan alami berasal dari tanaman. Beberapa sumber umum antioksidan alami dari tanaman adalah alga, serealia, produk kokoa, sitrus, tanaman bumbu dan rempah, legume, biji-bijian berminyak, ekstrak tanaman, protein hidrolisat, resin, lada, bawang merah dan bawang putih, dan zaitun.
Antioksidan alami dapat berfungsi dengan satu atau lebih cara seperti (a) sebagai senyawa
pereduksi, (b) sebagai penangkap radikal bebas, (c) pengkelat logam prooksidan, dan (d) quencher
dari bentuk singlet oksigen. Senyawa-senyawa ini umumnya dari kelompok fenolik atau polifenolik dari sumber tanaman. Antioksidan alami yang paling umum adalah flavonoid (flavonol, isoflavon, flavon, katekin, dan flavonol), derivat asam sinamat, kumarin, tokoferol, dan asam organik polifungsional (Sofia 2006).
5
pembuluh darah atau mempercepat artesoklorosis (Miyamoto et al. 2010). DM terlibat dalam
proses pembentukan radikal bebas (Droge W 2002) melalui autooksidasi glukosa, glikasi protein, dan aktivasi jalur metabolisme poliol yang selanjutnya mempercepat pembentukan senyawa oksigen reaktif. Pembentukan senyawa oksigen reaktif tersebut dapat meningkatkan modifikasi
lipid, DNA, dan protein pada berbagai jaringan (Ueno et al. 2002). Modifikasi molekuler pada
berbagai jaringan tersebut mengakibatkan ketidakseimbangan antara antioksidan protektif (pertahanan antioksidan) dan peningkatan produksi radikal bebas. Hal itu merupakan awal kerusakan oksidatif yang dikenal sebagai stres oksidatif (Sofia 2006). Untuk meredam kerusakan oksidatif tersebut diperlukan antioksidan. Peningkatan suplai antioksidan yang cukup akan membantu pencegahan komplikasi klinis diabetes mellitus.
2.7.
Enzim Alfa Glukosidase
Enzim α-glukosidase dengan nama kimia α-D-glukosida glukohidrolase terletak dalam
permukaan membran dalam sel usus (Gao et al. 2008). Enzim ini merupakan enzim utama
pemecah karbohidrat menjadi glukosa dalam usus kecil (Lee et al. 2007). Enzim α-glukosidase
diketahui merupakan enzim yang dapat mengkatalisis pemecahan ikatan 1,4 α-glukosida dan
ikatan 1,6 α-glukosida. Kerja enzim ini adalah melanjutkan kerja dari enzim α-amilase yakni menghidrolisis α-limit dekstrin menjadi glukosa (Berdanier et al. 2006). Enzim α-glukosidase
terlibat dalam degradasi glikogen dan memiliki pH optimum 7. Enzim ini sering digunakan untuk
mengetahui potensi tumbuhan sebagai antidiabetes secara in vitro dengan mekanisme
penghambatan. Penghambatan kerja enzim ini dapat menunda penyerapan glukosa ke dalam darah
setelah adanya asupan makanan (Elya et al. 2012). Semakin besar potensi tumbuhan sebagai
antidiabetes, semakin tinggi pula penghambatan aktivitas enzim ini (Azizah 2005).
2.8.
Pembotolan dan Pasteurisasi
Pengemasan pangan adalah salah satu proses terakhir dalam suatu rantai produksi pangan. Pengemasan pangan ini bertujuan untuk melindungi produk pangan dari berbagai pengaruh luar yang memungkinkan kerusakan pada produk pangan, mempermudah dalam proses pengangkutan produk pangan, dan berguna dalam memberikan informasi mengenai komposisi dan informasi gizi
bagi konsumen (Coles et al. 2003). Ada berbagai bahan pengemas yang umum digunakan, yaitu
kaca, logam, plastik, dan karton. Pemilihan bahan pengemas yang tepat akan dapat memperpanjang umur simapn suatu produk pangan (Marsh dan Bugusu 2007).
Berbagai macam pangan dapat dikemas dalam kemasan kaca, contohnya adalah kopi instan,
rempah, makanan bayi, produk susu, selai, sirup, bir, wine, air mineral, dan lain-lain (Coles et al.
2003). Keuntungan dari bahan pengemas kaca adalah tidak berbau, tahan terhadap bahan kimia, tidak tembus gas dan uap, tahan terhadap suhu tinggi, dapat diproduksi dalam berbagai bentuk, serta dapat digunakan kembali dan dapat didaur ulang. Bahan pengemas kaca dapat pula diproduksi dalam berbagai warna maupun transparan (Marsh dan Bugusu 2007).
6
Pada kemasan kaca tidak transparan atau berwarna terdapat bahan tambahan lain yang ditambahkan, seperti besi oksida (Fe2O3) yang memberikan warna hijau pucat, kromium oksida (Cr2O3) yang menghasilkan warna biru kehijauan yang halus, penambahan besi oksida dan kromium oksida menghasilkan warna hijau tua, penambahan karbon dan peleburan komposisi yang mengandung besi oksida pada kondisi reduksi menghasilkan warna coklat, serta penambahancobalt pada kaca dengan kandungan besi yang rendah menghasilkan warna biru (Coles et al. 2003).
Dalam pembuatan suatu produk pangan, sering dilakukan proses pemanasan. Proses pemanasan bertujuan untuk menginaktifkan mikroorganisme patogen atau perusak. Proses pemanasan dapat mempengaruhi fisik dari suatu produk atau menyebabkan perubahan karena reaksi kimia pada produk pangan, contohnya adalah reaksi pencoklatan. Proses ini berlangsung dengan memberikan panas pada produk dan ditahan selama jangka waktu tertentu untuk menginaktifkan mikroorganisme sebelum kemudian didinginkan (Lewis dan Heppell 2000).
Salah satu faktor yang paling penting untuk diperhatikan dalam proses pemanasan adalah tingkat keasaman dari produk pangan. Berdasarkan tingkat keasaman ini, produk pangan dapat dibagi menjadi dua, yakni pangan berasam tinggi (pH < 4.5) dan pangan berasam rendah (pH
>4.5). Pembagian ini didasarkan pada viabilitas dari bakteri Clostridium botulinum. Bakteri ini
biasa tidak aktif dan tidak bereproduksi pada pH di bawah 4.5. Tujuan proses pemanasan pada produk berasam tinggi adalah untuk menginaktivasi kapang dan khamir. Nilai pH umumnya akan menurun selama proses pemanasan sebesar kurang lebih 1 unit pH tetapi dapat kembali mendekati nilai awalnya setelah proses pendinginan (Lewis dan Heppell 2000).
Pasteurisasi adalah salah satu cara pengawetan panas yang ringan untuk menginaktivasi mikroorganisme yang tidak tahan panas, seperti bakteri vegetatif, kapang, dan khamir yang dapat menyebabkan kerusakan produk pangan ataupun keracunan pangan (Lewis dan Heppell 2000). Prinsip pasteurisasi adalah pemanasan produk dalam waktu yang singkat sampai mencapai kombinasi suhu dan waktu tertentu yang cukup untuk membunuh semua mikroorganisme patogen, tetapi hanya menyebabkan kerusakan sekecil mungkin terhadap produk akibat panas. Proses pengawetan dikatakan ringan karena jumlah kerusakan secara kimia maupun perubahan karakteristik sensori yang dihasilkan sangat minimal.
Lewis dan Heppell (2000) mengatakan bahwa proses pasteurisasi yang dipadukan dengan pendinginan secara cepat dan penyimpanan pada suhu rendah umumnya akan menghasilkan produk yang lebih bertahan lama. Namun, penting pula untuk menjaga agar tidak terjadi
rekontaminasi setelah proses pasteurisasi dilakukan atau dikenal dengan PPC (postpasteurization
contamination).
Menurut Fellows (2000), berdasarkan kombinasi suhu dan waktu pasteurisasi metode pasteurisasi dapat dibagi menjadi dua, yaitu :
1. pasteurisasi dengan suhu tinggi dan waktu singkat (High Temperature Short Time/HTST),
yaitu proses pemanasan susu selama 15 detik pada suhu 72oC
2. pasteurisasi dengan suhu rendah dan waktu lama (Low Temperature Long Time/LTLT)
yakni proses pemanasan susu pada suhu 63oC selama 30 menit.
2.9.
Umur Simpan
Salah satu faktor terpenting dalam pembuatan produk pangan adalah umur simpan produk.
7
yang memuaskan pada sifat-sifat penampakan, rasa, aroma, tekstur, nilai gizi, serta layak dikonsumsi (Robertson 2010). Hasil dari berbagai reaksi kimiawi yang terjadi di dalam produkmakanan bersifat akumulatif dan irreversible selama penyimpanan, sehingga pada saat tertentu
hasil reaksi tersebut mengakibatkan mutu makanan tidak dapat diterima (Robertson 2010). Faktor yang mempengaruhi umur simpan dapat dikategorikan menjadi faktor internal dan eksternal (Robertson 2010). Faktor internal merupakan karakteristik produk akhir, misalnya aktivitas air (aw), pH, nilai gizi, penggunaan bahan pengawet dan biokimia alami produk (enzim dan komponen kimia). Faktor eksternal adalah faktor yang mempengaruhi produk selama pengiriman hingga diterima konsumen. Faktor eksternal diantaranya adalah suhu penyimpanan, RH penyimpanan, RH proses, RH pengiriman, komposisi udara dalam kemasan dan penanganan selama di konsumen.
Umur simpan produk pangan dapat diduga dan kemudian ditetapkan waktu kadaluarsanya
dengan menggunakan dua konsep studi penyimpanan produk pangan yaitu Extended Storage
Studies (ESS) dan Accelerated Storage Studies (ASS). ESS sering juga disebut sebagai metode konvensional yaitu penentuan tanggal kadaluarsa dengan menyimpan suatu seri produk pada kondisi normal sehari-hari dan dilakukan pengamatan terhadap penurunan mutunya sehingga mencapai tingkat kadaluarsa. Metode ini akurat dan tepat, namun memerlukan waktu yang panjang dan analisa parameter mutu yang relatif banyak. Metode ESS sering digunakan untuk produk yang mempunyai kadaluarsa kurang dari 3 bulan (Arpah 2001).
Metode Accelerated Shelf Life Testing (ASLT) atau metode akselerasi digunakan untuk
8
III.
METODOLOGI PENELITIAN
3.1.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini terdiri dari bahan yang digunakan dalam pembuatan minuman fungsional, penentuan umur simpan, dan analisis. Bahan yang digunakan dalam pembuatan minuman fungsional dan penyimpanan adalah sirih merah, jahe, kayu manis, jeruk nipis, dan air. Bahan yang digunakan dalam analisis adalah air destilata, larutan buffer fosfat, larutan DPPH 1.5 mM, metanol, etanol, asam askorbat, indikator phenolptalein, NaOH 0.1 N, asam galat, etanol 95%, Folin Ciocalteau 50%, larutan Na2CO3, larutan enzim α-glukosidase (0.5 mg dilarutkan dalam 10 ml 0.1 M larutan buffer fosfat pH 7 yang mengandung 100 mg bovin albumin), p-nitrofenil α-D-glukopiranosida (p-NPG) 20 mM, buffer fosfat 0.1 M pH 7, acarbose, Na2CO3 200 mM, HCl 25 %, heksana, PCA, larutan pengencer steril K2SO4, HgO, H2SO4, batu didih, NaOH 60 %, Na2SO3 5%, H3BO3, indikator metilen red-metilen blue, HCl 0,02 N, bubur Al(OH)3, larutan Pb asetat, Na2CO3 anhidrat, K/Na oksalat anhidrat, Na fosfat, HCl 30%, NaOH 45%, larutan Luff Schrool, KI 20%, dan H2SO4 26.5%.
Alat yang digunakan dalam penelitian ini terdiri dari alat yang digunakan dalam pembuatan minuman fungsional, penyimpanan, dan analisis. Alat yang digunakan dalam pembuatan minuman fungsional dan penyimpanan adalah neraca analitik, blender kering, panci, kompor, centong, alat pemeras jeruk, baskom, kain saring, botol kaca, gelas ukur 500 ml dan termometer. Alat yang digunakan dalam analisis adalah sudip, gelas pengaduk, pipet tetes, botol semprot, penangas air, tabung sentrifus, sentrifus, gelas piala 100 ml, gelas piala 250 ml, erlenmeyer 100 ml, erlenmeyer 250 ml, tabung reaksi, tabung reaksi berulir, mikropipet, labu destilasi, pipet volumetrik 1 ml, pipet volumetrik 5 ml, pipet volumetrik 10 ml, kuvet, labu takar 10 ml, labu takar 50 ml, labu takar 100 ml, labu takar 250 ml, gelas ukur 10 ml, gelas ukur 100 ml, gelas arloji, cawan petri, cawan
aluminium, cawan porselen, alat vortex, spektrofotometer UV-Vis, alat GCMS (gas
chromatography and mass spectrometry), chromameter, pH meter, piknometer, viskometer
Brookfield, refraktometer, kertas saring, dan kapas.
3.2.
Metode Penelitian
Penelitian dilakukan dengan beberapa tahapan, dan secara rinci dapat disimak pada Gambar 1.
3.2.1.
Persiapan Bahan Baku
9
kering, dikemas dalam plastik yang diseal dan dimasukkan dalam toples kaca bersilika gel,
kemudian disimpan untuk digunakan pada proses-proses selanjutnya.
Semua sampel yang telah dikeringkan kemudian diekstrak dengan cara seperti yang telah
dilakukan sebelumnya oleh Yasni et al. (2010). Bubuk sirih merah, jahe, dan kayu manis
masing-masing ditimbang sebanyak 20 gram direbus dalam 100 ml air (1:5) dalam keadaan tertutup dengan api sedang. Setelah ekstrak mendidih, proses pemanasan ditahan selama 15 menit untuk sirih merah dan jahe, serta 5 menit untuk kayu manis dengan menjaga volume air agar tetap
melalui penambahan air panas (suhu 70oC). Ekstrak didapatkan melalui penyaringan menggunakan
kain saring. Residu hasil penyaringan dari ekstrak masing-masing kemudian diekstrak kembali dengan air yang jumlahnya setengah dari jumlah air pada proses ekstraksi pertama. Filtrat hasil ekstraksi kedua disatukan dengan filtrat pertama, dan disebutkan sebagai hasil ekstrak bahan baku utama.
3.2.2.
Formulasi Minuman Fungsional Berbasis Sirih Merah
Usaha memperbaiki tingkat kesukaan dari minuman fungsional dilakukan dengan penambahan jeruk nipis. Jeruk nipis yang dipilih adalah jeruk nipis berwarna kuning dan empuk. Jeruk nipis ditambahkan dalam bentuk ekstraknya dan dalam bentuk perasan air jeruk nipis. Proses ekstraksi jeruk nipis dilakukan dengan memotong-motong jeruk nipis ke dalam bentuk yang lebih kecil, kemudian merebusnya dalam air dengan perbandingan 1:10 (kondisi potongan jeruk dapat terendam seluruhnya) dan ditutup. Setelah mendidih, proses pemanasan ditahan selama 15 menit
dengan penambahan air panas (suhu 70oC), lalu disaring menggunakan kain saring. Cara kedua
adalah penambahan air perasan jeruk nipis yang didapat dengan memotong jeruk nipis ke dalam bagian yang lebih kecil dan diperas agar air dari buah jeruk nipis keluar. Hasil perasan disaring menggunakan kain saring. Pemilihan bentuk jeruk nipis yang ditambahkan pada formula baku didasarkan pada kapasitas antioksidan yang dihasilkan keduanya. Bentuk yang memiliki kapasitas yang lebih tinggi yang akan dipilih.
Pembuatan formula minuman mengikuti formula baku dari minuman fungsional berbahan
dasar sirih merah yang telah dilakukan sebelumnya oleh Yasni et al. (2010), yaitu dengan
mencampurkan 5 ml ekstrak sirih merah, 4 ml ekstrak jahe, dan 3 ml esktrak kayu manis (5:4:3 (v/v)). Untuk perbaikan formula, ditambahkan sari jeruk nipis pada lima tingkat perbandingan, sehingga dihasilkan lima formula baru (Tabel 2). Pada tahap akhir pembuatan formula, ditambahkan 12% (b/v) pemanis stevia.
Tabel 2. Formulasi Penambahan Jeruk Nipis
Deskripsi Komposisi
Sirih merah : Jahe : Kayu manis : Jeruk nipis (v/v)
Formula 1 5 : 4 : 3 : 1
Formula 2 5 : 4 : 3 : 2
Formula 3 5 : 4 : 3 : 3
Formula 4 5 : 4 : 3 : 4
11
Kelima formula diujikan kepada 5 orang panelis terlatih untuk mengetahui kesukaannya terhadap formula yang diujikan. Pada tahapan ini, panelis diminta untuk mengurutkan formula yang paling disukai sampai yang paling tidak disukai, kemudian dipilihlah 3 formula yang palingdisukai. Selanjutnya, pada 3 formula terpilih tersebut dilakukan uji rating hedonik oleh 70 orang
panelis tidak terlatih untuk mengetahui tingkat kesukaan panelis (Meilgaard et al. 1999) dan akan
dipilih 1 formula yang memiliki tingkat kesukaan paling tinggi, berdasarkan parameter aroma,
rasa, warna, dan overall. Formula yang terpilih dilakukan pengujian umur simpan dengan metode
akselerasi.
3.2.3.
Proses Pembotolan Minuman Fungsional
Persiapan dalam penentuan umur simpan meliputi pencucian botol kaca, sterilisasi botol kaca dengan perebusan, pengeringan botol kaca, ekstraksi bahan baku, pencampuran ekstrak bahan baku, dan proses pembotolan. Proses perebusan botol dilakukan dengan cara memasukkan botol ke dalam air mendidih selama 30 menit. Botol kemudian dikeringkan pada udara terbuka. Proses pembotolan meliputi pemasukan minuman fungsional ke dalam botol, proses pasteurisasi, penutupan, dan proses pendinginan botol.
Proses ekstraksi bahan baku dilakukan satu hari sebelum proses pembotolan, karena dilanjutkan dengan tahap dekantasi. Ekstrak bahan baku kemudian dicampur dan dipanaskan sambil diaduk serta ditambahkan pemanis stevia menjadi minuman fungsional yang siap dikemas.
Proses pemanasan dalam mencampur bahan-bahan ini dilakukan pada suhu 70oC dan dalam
keadaan tertutup. Minuman fungsional tersebut kemudian diisikan dalam keadaan panas (hot
filling) ke dalam botol kaca yang sudah kering sampai pada bagian leher botol, kemudian
dipasteurisaasi selama 30 menit pada suhu 63oC (Fellows 2000), lalu botol langsung ditutup,
diseal, dan langsung didinginkan pada air mengalir.
Botol-botol setelah dingin diberi label dan siap disimpan pada 3 suhu berbeda (5oC, 30oC,
dan 50oC). Proses penyimpanan minuman dilakukan selama 6 minggu dengan mengamati 6
parameter kerusakan, yaitu pH, warna, total asam tertitrasi (TAT), total plate count (TPC), total
fenol, dan sensori. Parameter total fenol dan sensori dilakukan pada minggu ke-0, 2, 4, dan 6, sedangkan 4 parameter yang lain dilakukan mulai dari minggu ke-0 sampai minggu ke-6.
3.2.4.
Pendugaan Umur Simpan dengan Metode Arrhenius
12
keterangan :
k t = nilai k pada suhu penyimpanan t
T = suhu penyimpanan
Ea = energi aktivasi (J/mol) = slope model Arrhenius
R = konstanta gas (8,314 J/molK)
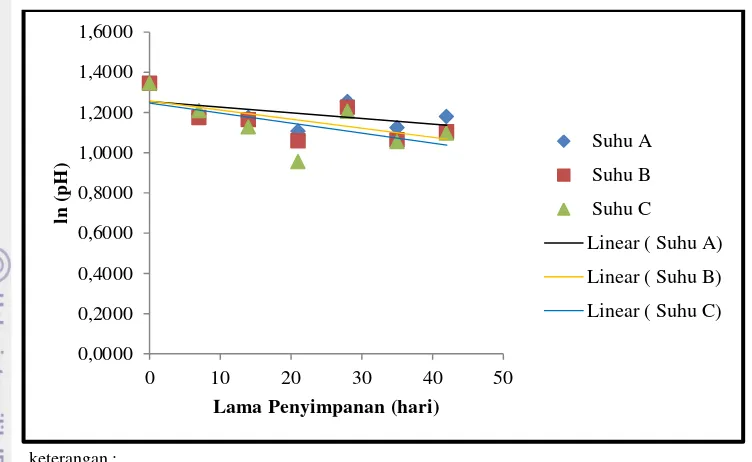
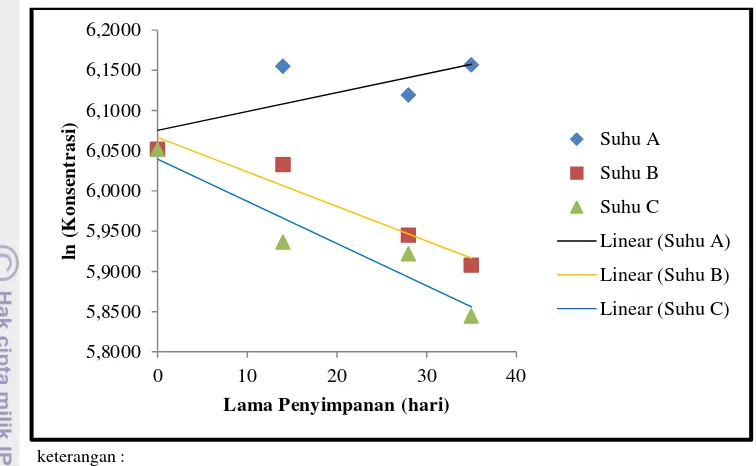
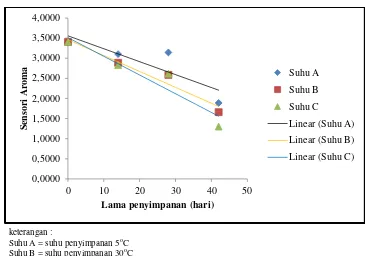
Hasil pengamatan umur simpan selama periode tertentu penyimpanan diplotkan pada grafik hubungan antara lama penyimpanan (hari) dengan rata-rata penurunan mutu (k). Jika reaksi kerusakan pangan belum diketahui model orde reaksinya, maka nilai plot tersebut dilakukan pada Orde Nol dan Orde Satu. Plot pada Orde Nol dilakukan langsung antara lama penyimpanan (hari) dan penurunan mutu (k), sedangkan pada Orde Satu nilai k diubah menjadi bentuk lon (ln) dulu lalu diplot terhadap lama penyimpanan dan masing-masing ditentukan persamaan regresi liniernya. Hasil plot tersebut memberikan informasi nilai k, intersep, dan koefisien korelasi masing-masing suhu penyimpanan. Langkah selanjutnya adalah memplotkan nilai k atau ln k terhadap suhu penyimpanan dalam bentuk Kelvin (K, 1/T). Plot kedua ini memberikan informasi nilai k, intersep, dan koefisien korelasi. Nilai k hasil plot ini merupakan nilai energi aktivasi dibagi dengan konstanta gas (Ea/R), karena persamaan garis linier hasil plot akan mengikuti persamaan Arrhenius. Umur minuman fungsional dapat dihitung dengan persamaan :
keterangan :
ts = waktu kadaluarsa (hari)
Q0 = mutu awal produk
Qs = mutu akhir produk
k = konstanta laju penurunan mutu
3.2.5.
Transformasi Nilai Umur Simpan Menjadi Waktu Kadaluarsa
Transformasi umur simpan menjadi waktu kadaluwarsa didasarkan pada parameter yang
13
3.3.
Prosedur Analisis
3.3.1.
Analisis Antioksidan dengan Metode DPPH (Kubo
et al. 2002;
Molyneux 2004)
Analisis antioksidan minuman fungsional diawali dengan pengukuran kapasitas antioksidan dengan membuat kurva standar menggunakan asam askorbat pada konsenrasi 0 sampai 250 ppm. Prosedur pembuatan larutan standar sama dengan prosedur pengujian sampel, yaitu dengan memasukkan 1.5 ml larutan buffer fosfat ke dalam tabung reaksi, lalu ditambah 2,85 ml etanol,
dan larutan DPPH 1.5 mM sebanyak 150 l, lalu dikocok dengan alat vortex, dan kemudian
ditambahkan 45 l asam askorbat. Selanjutnya, dibuat kurva standar asam askorbat dengan
memplot hubungan antara konsentrasi asam askorbat dan selisih antara absorbansi blanko dan absorbansi sampel.
Prosedur pengujian sampel dimulai dengan memasukkan 1.5 ml larutan buffer fosfat ke
dalam tabung reaksi, lalu ditambah 2,85 ml etanol, dan larutan DPPH 1.5 mM sebanyak 150 l,
lalu dikocok dengan alat vortex, dan kemudian ditambahkan 45 l sampel. Campuran didiamkan
selama 30 menit pada suhu ruang dan diukur absorbansinya (A sampel) pada panjang gelombang 520 nm. Absorbansi blanko diperoleh melalui prosedur yang sama kecuali tanpa ada penambahan sampel. Selanjutnya selisih absorbansi blanko dengan absorbansi sampel disubstitusi pada
persamaan kurva standar asam askorbat untuk menentukan AAE (Ascorbic Acid Equivalent).
Kapasitas antioksidan dihitung berdasarkan persamaan berikut :
Kapasitas antioksidan (%) =
3.3.2.
Analisis Total Asam Tertitrasi (AOAC Official Method 940.15 1995)
Sampel dituang ke dalam gelas piala lalu diaduk hingga homogen, dan disaring dengan kertas saring. Sampel sebanyak 4 ml dilarutkan menjadi 250 ml dengan air destilata dalam labu takar. Dari 250 ml larutan tersebut, diambil 25 ml dan kemudian ditambahkan 2-3 tetes indikator phenolptalein. Titrasi dilakukan dengan larutan NaOH 0.1 N yang sudah distandarisasi secara duplo, dan volume NaOH yang digunakan dicatat. Total asam tertitrasi dihitung dengan persamaan berikut :
TAT (ml NaOH 0.1 N/100 ml sampel) =
3.3.3.
Analisis pH (AOAC Official Method 981.12 1995)
14
3.3.4.
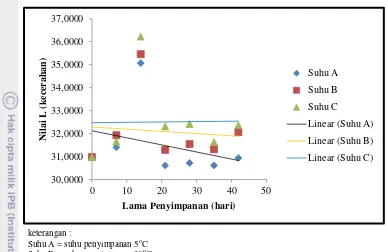
Analisis Warna dengan Chromameter (Hutching 1999)
Analisis warna dilakukan dengan menggunakan alat Chromameter Minolta CR-200. Sebelum dilakukan pengukuran, alat dikalibrasi menggunakan plat yang sesuai warnanya dengan sampel. Pengukuran dilakukan dengan meletakkan sampel di dalam wadah berukuran seragam dan selanjutnya dilakukan pengukuran pada skala nilai Y, x, y. Hasil pengukuran dikonversi ke dalam
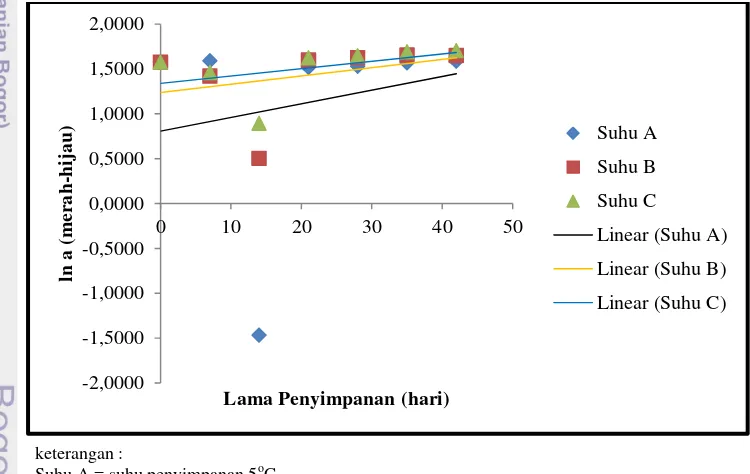
sistem Hunter L, a, b. Nilai L menyatakan parameter kecerahan (lightness) yang mempunyai
rentang nilai dari 0 (hitam) sampai 100 (putih). Nilai a menyatakan cahaya pantul yang menghasilkan warna kromatik campuran merah-hijau dengan rentang nilai +a (positif) dari 0 – 100
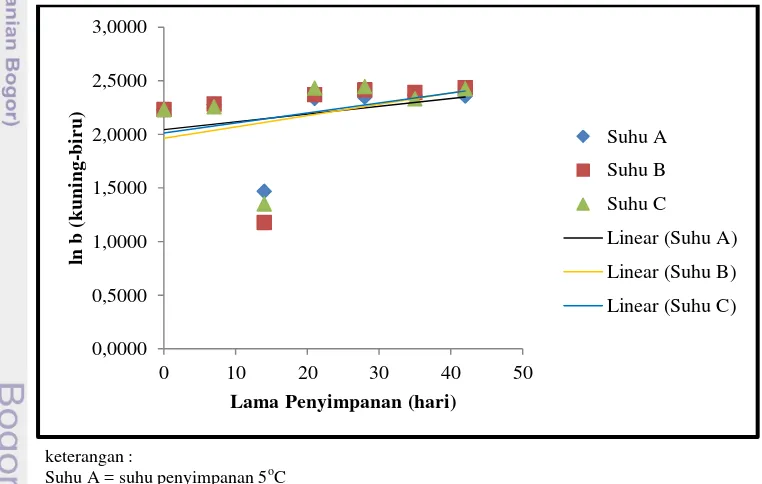
untuk warna merah dan rentang nilai –a (negatif) dari 0 – (-80) untuk warna hijau. Notasi b
menyatakan warna kromatik campuran biru-kuning dengan rentang nilai +b (positif) dari 0 – 70
untuk kuning dan rentang nilai –b (negatif) dari 0 – (-70) untuk warna biru.
3.3.5.
Analisis Total Fenol (Javanmardi et al. 2003)
Sebanyak 0.5 ml sampel ditambahkan ke dalam 0.5 ml etanol 95%, 2.5 ml akuades, dan 2.5 ml reagen Folin Ciocalteau 50%. Campuran didiamkan 5 menit, lalu ditambah 0.5 ml Na2CO3 5% dan divortex. Setelah disimpan di ruang gelap selama 1 jam, larutan diukur absorbansinya pada panjang gelombang 725 nm. Kurva standar asam galat dibuat dengan memplotkan konsentrasi asam galat sebesar 50, 100, 150, 200, 250 mg/L dengan nilai absorbansinya masing-masing, kemudian nilai total fenol sampel ditentukan dengan mensubstitusikan nilai absorbansi pada persamaan regresi linier dari kurva standar.
3.3.6.
Analisis Total Mikroba (BAM 2001)
Analisis total mikroba dilakukan dengan memipet 1 ml sampel dari pengenceran yang dikehendaki ke dalam cawan petri. Sebanyak ± 12-15 ml media PCA dituangkan ke dalam cawan petri kemudian cawan petri digerakkan secara hati-hati untuk menyebarkan sel-sel mikroba secara merata, yaitu dengan gerakan angka delapan. Setelah agar membeku, cawan diinkubasi dengan
posisi terbalik pada suhu 35 oC selama 48±2 jam. Setelah inkubasi selesai, jumlah koloni yang
15
N = 1 x n1 1 x n C x Dketerangan :
N = jumlah koloni per ml atau per gram produk
C = jumlah seluruh koloni yang dihitung
n1 = jumlah cawan pada pengenceran pertama n2 = jumlah cawan pada pengenceran kedua D = pengenceran pertama yang dapat dihitung
3.3.7.
Uji Organoleptik Ranking Sederhana dan Rating Hedonik
Uji ranking digunakan untuk membandingkan intensitas ataupun kesukaan antar sampel dan mengurutkannya. Uji dapat dilakukan berpasangan ataupun sederhana. Pada uji ranking sederhana, kepada panelis disajikan satu set sampel pada waktu bersamaan dengan nilai ranking 1 untuk sampel yang paling disukai dan ranking 5 untuk sampel yang paling tidak disukai.
Pada uji rating hedonik, panelis diminta untuk menilai atribut-atribut sensori sampel yang
disajikan, yaitu warna, aroma, rasa, dan keseluruhan. Dalam uji ini digunakan panelis tidak terlatih sebanyak 70 orang. Taraf signifikansi yang digunakan adalah 5%. Analisis data dilakukan
menggunakan ANOVA (Analysis of Variance) dengan uji lanjut Duncan. Skala yang digunakan
dalam uji ini adalah skala kategori 5 poin dengan deskripsi : sangat suka=5, suka=4, agak suka=3, agak tidak suka=2, dan tidak suka=1.
3.3.8.
Analisis Penghambatan Aktivitas Enzim Alfa Glukosidase (Matsumoto
et al. 2002)
Sebanyak 980 l buffer fosfat 0,1 M (pH 7), 500 l 4-nitrofenil α-D-glukopiranosida 20
mM, 20 l sampel dicampurkan dan diinkubasi pada suhu 37oC selama 5 menit. Reaksi enzimatis
dimulai dengan menambahkan 500 l larutan α-glukosidase. Campuran diinkubasi kembali pada
suhu 37 oC selama 15 menit dan menghasilkan senyawa p-nitrofenol. Reaksi kemudian dihentikan
dengan penambahan 2 ml larutan sodium karbonat 200 mM. Hidrolisis enzimatik dari substrat diamati berdasarkan jumlah p-nitrofenol yang dihasilkan pada sistem reaksi tersebut pada panjang gelombang 400 nm menggunakan spektrofotometer. Acarbose digunakan sebagai kontrol positif. Persentase penghambatan α-glukosidase dihitung berdasarkan formula :
16
3.3.9.
Analisis Komponen Senyawa Volatil Minuman dengan Metode GCMS
(Gas Chromatography Mass Spectrometry)
Sebanyak 3,5 gram sampel dalam vial SPME (Solid Phase Microextraction) 22 ml
diekstrak pada 80oC selama 30 menit pada headspace vial dengan menggunakan fiber SPME
jenis DVB/PDMS. diinjeksikan ke GCMS dengan kondisi berikut : suhu injektor 250oC; jenis
injektor adalah splitless, gas pembawa adalah gas helium (He) dengan laju alir 1ml/menit. Kondisi
suhu MS adalah 280oC. Kondisi oven diatur dengan suhu awal 45oC selama 1 menit kemudian
meningkat 6°C/min sampai 250°C selama 25 menit. Kolom yang digunakan adalah DB-WAX (60 m x 250 µm x 0.25 µm).
3.3.10.
Analisis Proksimat Minuman Fungsional Terpilih
Analisis proksimat minuman fungsional terpilih dilakukan terhadap kandungan berikut :
1. Kadar air dengan metode oven vakum (AOAC Official Mehod 925.45 1999)
2. Analisis kadar abu dengan metode pengabuan kering (SNI 01-2891-1992)
3. Analisis kadar protein metode Kjeldahl (AOAC Official Method 960.52 1995)
4. Analisis total gula dengan metode Luff Schoorl (SNI 01-2892-1992)
3.3.11.
Analisis Sifat Fisik Minuman Fungsional Terpilih
Analisis sifat fisik minuman fungsional terpilih dilakukan terhadap parameter berikut:
1. Analisis massa jenis
2. Analisis analisis viskositas dengan Brookfield Viscometer
17
IV.
HASIL DAN PEMBAHASAN
4.1.
Persiapan Bahan Baku
Penelitian dimulai dengan proses pengeringan daun sirih merah dan jahe dengan cara menjemur daun sirih merah yang sudah dicuci bersih dan jahe yang sudah dipotong di bawah sinar matahari mulai pukul 09.00-14.00, sedangkan jeruk nipis yang digunakan adalah dalam bentuk segar dan hanya digunakan air perasannya serta kayu manis yang digunakan sudah dalam bentuk
kering. Suhu pengeringan matahari bervariasi, yakni 29,5oC pada pukul 9, 32,5oC pada pukul 12,
dan 27oC pada pukul 16 (Asti 2009). Proses pengeringan bahan di bawah sinar matahari cukup
efektif dalam menurunkan kadar air bahan (Asti 2009) serta mudah diterapkan kepada masyarakat. Proses pengeringan pada tiga bahan baku bertujuan agar bahan baku dapat bertahan lebih lama sampai proses penelitian selesai. Bahan yang sudah kering dibubukkan menggunakan blender kering, dikemas dalam plastik yang diseal dan dimasukkan dalam toples kaca bersilika gel, kemudian disimpan untuk digunakan pada proses-proses selanjutnya. Komponen aktif pada suatu bahan pangan alami rentan sekali terhadap panas sehingga pada suhu yang tinggi kandungan
dalam bahan pangan cenderung menurun (Igual et al. 2010) sehingga proses pengeringan matahari
ini dapat meminimalisasi masalah tersebut.
Bahan yang telah kering kemudian diukur kadar airnya dengan metode oven (AOAC Official Method 925.45 1999). Hasil pengukuran kadar air dapat dilihat pada Tabel 3. Kadar air dalam basis basah yang didapatkan pada percobaan ini sudah memenuhi Standar Nasional Indonesia (SNI) rempah bubuk (SNI 01-3709-1995), yaitu maksimum kadar air adalah 12 % (bb). Standar kadar air kayu manis mengikuti SNI Casia Indonesia (SNI 01-3395-1994) dengan tingkat kadar air maksimum adalah 14% (bb). Penyerapan uap air selama 6 bulan penyimpanan bubuk jahe dan kayu manis (Herawati 2008) diduga menjadi faktor yang menyebabkan kadar air bubuk jahe dan kayu manis tidak tepat sama dengan kadar air dalam SNI. Penelitian sebelumnya mengungkapkan bahwa pengeringan dengan metode oven lebih efektif dalam menurunkan kadar air jika dibandingkan dengan metode pengeringan matahari, yaitu kadar air bahan pengeringan oven adalah sebesar 2,32% dan kadar air pengeringan matahari adalah 2,86% (Agustini 2006).
Tabel 3. Hasil pengukuran kadar air bahan baku
Sampel KA (%bk) KA (%bb)
Sirih Merah 12,96 ± 0,15 11,48 ± 0,12
Kayu Manis 16,50 ± 0,03 14,16 ± 0,03
Jahe 14,06 ± 0,06 12,32 ± 0,05
Perasan Jeruk Nipis - 87,30 ± 0,99
Keterangan : bk = basis kering bb = basis basah
18
4.2.
Proses Ekstraksi Bahan Baku
Pembuatan formula minuman mengikuti formula baku dari minuman fungsional berbahan
dasar sirih merah yang telah dilakukan sebelumnya oleh Yasni et al. (2010) yaitu dengan
mencampurkan 5 ml ekstrak air sirih merah, 4 ml esktrak air jahe, dan 3 ml esktrak air kayu manis (5:4:3 (v/v)). Ekstrak didapatkan dari proses ekstraksi bahan baku dengan air mendidih agar jumlah komponen dapat terekstrak secara maksimal dan dilakukan dalam wadah tertutup untuk meminimalkan teruapnya komponen volatil pada rempah. Berdasarkan proses ekstraksi tersebut diperoleh rendemen sirih merah 73,87%, jahe 73,33%, dan kayu manis 67,07%.
4.3.
Formulasi Minuman Fungsional
Formula minuman fungsional campuran sirih merah, jahe, dan kayu manis dengan rasio 5:3:4 (v/v) memiliki rasa pahit yang dominan. Untuk memperbaiki citarasa formula tersebut, dilakukan penambahan jeruk nipis. Bentuk jeruk nipis yang ingin ditambahkan mengacu pada kapasitas antioksidan dari ekstrak buah jeruk nipis dengan air dan/atau dari air perasan jeruk nipis (Tabel 4). Berdasarkan hasil pengukuran nilai kapasitas antioksidan, maka dipilihlah air perasan jeruk nipis sebagai alternatif perbaikan formula baku, yaitu dengan menambahkannya pada lima tingkat perbandingan (Tabel 2), dan pada tahap akhir pembuatan minuman fungsional ditambahkan sebanyak 12% (b/v) pemanis stevia.
Tabel 4. Kapasitas antioksidan bahan baku penyusun minuman fungsional
Sampel Kapasitas antioksidan (ppm AAE)
Sirih merah masak 1652,00 ± 48,855
Sirih merah gerus 423,00 ± 53,354
Kayu manis 1884,73 ± 12,856
Jahe bubuk 355,27 ± 66,854
Jahe 291,18 ± 18,642
Jeruk nipis masak 68,91 ± 12,856
Jeruk nipis peras 447,54 ± 25,070
Daun jeruk 406,18 ± 52,712
Keterangan : AAE = Ascorbic Acid Equivalent
Bahan baku yang digunakan pada penelitian ini memiliki kandungan senyawa aktif yang berguna bagi kesehatan. Sirih merah mengandung alkaloid, flavonoid, dan tanin yang berfungsi sebagai antioksidan serta dapat menurunkan kadar kolesterol dan gula darah (Azima 2003 dan
Safithri et al. 2006). Jahe mengandung zingiberen dan zingiberol yang berfungsi sebagai
antioksidan dan antihiperglikemia (Koswara 2006). Kayu manis mengandung tannin, eugenol,
sinamaldehid yang berfungsi sebagai antioksidan dan menghambat aktivitas enzim α-glukosidase
(King 2000 dan Ngadiwiyana et al. 2011). Antioksidan pada rempah biasanya tidak rusak akibat
19
adalah oksigen dan cahaya selama penyimpanan (Pokorny 2001). Berdasarkan penelitian sebelumnya, nilai kapasitas antioksidan berbagai bahan baku yang digunakan adalah 37,64% (metode rancimat) untuk jahe bubuk (Wuisan 2007); 806,78 ppm AAE untuk jahe segar (Herold2007); 75 mg/100mL untuk nilai IC50 jeruk nipis (Ghafar et al. 2010); 5,06 mg/L IC50 kayu manis
(Pebrimadewi 2011) atau pada konsentrasi 50 ppm dapat menghambat radikal bebas sebesar
28,9% (Alfarabi et al. 2010). Perbedaan ini diduga karena perbedaan metode analisis maupun
perbedaan perisapan bahan baku.
Pengukuran kapasitas antioksidan ekstrak bahan baku ditujukan untuk melihat potensi bahan baku sebagai sumber antioksidan serta untuk melihat perlakuan yang cocok diterapkan pada bahan baku untuk mendapatkan nilai kapasitas antioksidan paling tinggi. Berdasarkan nilai kapasitas antioksidan bahan baku penyusun minuman fungsional yang tertera pada Tabel 4, terlihat bahwa sirih merah yang diekstrak dengan cara dimasak menghasilkan nilai kapasitas antioksidan yang lebih tinggi dibandingkan sirih yang hanya digerus saja. Jahe yang dibubukkan memiliki nilai kapasitas antioksidan yang lebih tinggi dibanding dengan jahe yang hanya dirajang biasa. Perasan jeruk nipis memiliki kapasitas antioksidan yang lebih tinggi. Oleh karena itu, perlakuaan perebusan sirih merah, pembubukan jahe, dan perasan air jeruk nipis dipilih dalam pembuatan minuman fungsional berbahan dasar sirih merah. Formulasi minuman ini dilakukan dalam 5 tahap, yaitu (1) penentuan tiga formula minuman dengan uji ranking hedonik terhadap beberapa panelis, (2) penentuan satu formula terpilih dengan uji rating hedonik pada 70 panelis tidak terlatih, (3) perbaikan citarasa minuman dengan variasi konsentrasi pemanis, (4) perbaikan warna minuman dengan penambahan mundar, dan (5) verifikasi penentuan formula terpilih dengan menggunakan panelis terlatih berusia 30-80 tahun.
Kelima formula citarasa yang telah ditambahkan pemanis stevia sebesar 12% (b/v) kemudian diujikan kepada beberapa panelis untuk mengetahui tingkat kesukaan. Dari hasil pengujian didapatkan tiga formula yang akan diujikan pada tahap selanjutnya dan pada proses ini panelis diminta untuk mengurutkan formula yang paling disukai sampai yang paling tidak disukai. Hasil yang didapatkan pada tahap ini menunjukkan bahwa tidak ada perbedaan nyata antar sampel yang diuji karena nilai F hitung lebih rendah dari F tabel pada perhitungan daftar sidik ragamnya (Lampiran 2). Walapun demikian tetap harus dilakukan pemilihan 3 formula yang disukai untuk dilakukan uji selanjutnya. Pemilihan 3 formula ditentukan berdasarkan rata-rata dari nilai yang diperoleh setiap formula, yaitu nilai rata-rata paling rendah mewakili sampel yang paling disukai dan sebaliknya. Berdasarkan hal tersebut, dipilihlah formula 3 dengan skor 3.6, formula 4 dengan skor 2.0, dan formula 5 dengan skor 2.0 (Lampiran 2).
Tahap pengujian perbaikan formula adalah mengujikan 3 formula terpilih pada 70 orang
panelis tidak terlatih untuk mengetahui tingkat kesukaan panelis melalui uji rating hedonik
(Meilgaard et al. 1999), dengan parameter aroma, rasa, warna, dan overall. Hasil pengujian
parameter aroma adalah terlihat bahwa tidak terdapat perbedaan nyata antar sampel. Artinya, kesukaan pada parameter aroma tidak berbeda satu sama lain. Namun, bila dilihat dari nilai rata-rata, formula yang memiliki tingkat kesukaan paling tinggi menurut hasil uji Duncan adalah formula 3 dengan nilai 3.06 (agak suka).
20
adanya perbedaan nyata antar sampel. Sampel formula 3 berbeda nyata dengan sampel formula 5, tetapi tidak berbeda nyata dengan formula 4 dan formula 5. Namun, formula 3 memiliki tingkat kesukaan yang lebih tinggi dibanding dengan formula 5, yakni 2.71 (mendekati agak suka).Parameter sensori keseluruhan (overall) dari 3 formula tersebut menunjukkan tidak terdapat
ada perbedaan nyata antar sampel. Sampel yang memiliki tingkat kesukaan paling tinggi menurut hasil uji Duncan adalah formula 3 dengan nilai 3.06 (agak suka). Hasil analisis pada uji sensori ini dapat dilihat pada Lampiran 2. Uji sensori tahap pertama ini ternyata belum memberikan peningkatan kesukaan panelis terhadap citarasa minuman yaitu masih berkisar pada tingkat agak suka (skor 3). Oleh karena itu, perlu dilakukan kembali upaya perbaikan formula. Alternatif yang dilakukan adalah dengan melakukan variasi penambahan konsentrasi pemanis pada minuman.
Tahap perbaikan formula selanjutnya adalah dengan mencoba beberapa konsentrasi pemanis, yaitu sebesar 12%, 20%, dan 25%. Pemanis stevia digunakan untuk menutupi rasa pahit yang tidak disukai panelis karena pemanis stevia memiliki tingkat kemanisan 200-300 kali dari
sukrosa, tetapi kandungan kalorinya rendah (Lemus-Mondaca et al. 2011), serta tidak
menimbulkan efek tetratogenik (Widowati et al. 2011). Variasi konsentrasi pemanis dimaksudkan
untuk mendapatkan tingkat kesukaan yang meningkat seiring dengan meningkatnya konsentrasi
pemanis. Ketiga sampel lalu diuji sensori menggunakan uji rating hedonik terhadap 70 panelis tak
terlatih untuk memilih konsentrasi mana yang memiliki tingkat kesukaan paling tinggi. Hasil
penilaian dari panelis pada uji rating hedonik menunjukkan bahwa tidak ada perbedaan nyata antar
sampel pada semua parameter. Perbedaan konsentrasi pemanis pada minuman fungsional campuran sirih merah, kayu manis, jahe, dan jeruk nipis tidak menghasilkan perbedaan tingkat kesukaan yang signifikan.
Tingkat kesukaan pada parameter aroma berkisar pada skala 2-3 (agak tidak suka-agak suka), dan tingkat kesukaan paling tinggi terhadap parameter aroma adalah pada minuman berkonsentrasi pemanis 12%, yakni sebesar 3.0857. Tingkat kesukaan pada parameter aroma setelah dilakukan variasi penambahan pemanis tidak berbeda jauh dengan uji sebelumnya (3,06). Tingkat kesukaan pada parameter warna berkisar pada skala 2 (agak tidak suka), dan tingkat kesukaan paling tinggi terhadap parameter warna adalah pada minuman berkonsentrasi pemanis 12%, yakni sebesar 2.8429. Tingkat kesukaan pada parameter warna setelah dilakukan variasi penambahan pemanis tidak berbeda jauh dengan uji sebelumnya (2,71). Tingkat kesukaan pada parameter rasa berkisar pada skala 1-2 (sangat tidak suka-agak tidak suka), dan tingkat kesukaan paling tinggi terhadap parameter rasa adalah pada minuman berkonsentrasi pemanis 20%, yakni sebesar 1.9143. Tingkat kesukaan pada parameter rasa setelah dilakukan variasi penambahan pemanis sedikit meningkat dibandingkan dengan uji sebelumnya (1,77). Tingkat kesukaan pada
parameter overall berkisar pada skala 2 (agak tidak suka), dan tingkat kesukaan paling tinggi
terhadap parameter overall adalah pada minuman berkonsentrasi pemanis 25%, yakni 2.1714.
Tingkat kesukaan pada parameter overall setelah dilakukan variasi penambahan pemanis justru
lebih rendah dibandingkan dengan uji sebelumnya (3,06). Keseluruhan hasil analisis uji sensori ini dapat dilihat pada Lampiran 4.
21
minuman, yaitu masih berkisar pada tingkat agak tidak suka. Pemanis umumnya akan memberikan pengaruh paling besar terhadap parameter rasa terutama untuk menutupi rasa pahit yang pada dasarnya terkandung dalam bahan, semakin tinggi konsentrasi pemanis semakin tinggi pula tingkatkesukaan panelis terhadap pangan (Kailaku et al. 2005). Pemanis stevia dipilih karena
keamanannya bagi penderita diabetes. Penggunaan stevia dapat dipadukan dengan pemanis lain yang juga aman bagi penderita diabetes, misalnya sorbitol, agar meningkatkan penerimaan citarasa
produk. Sorbitol biasa dipadukan dengan pemanis lain untuk menutup aftertaste dari pemanis lain,
memiliki kalori yang rendah sehingga cocok untuk penderita diabetes, dan dapat mencegah reaksi pencoklatan selama proses pembuatan produk (Smith dan Hui 2004). Untuk memastikan tingkat kesukaan panelis terhadap tiga formula yang ada dengan tingkat konsentrasi pemanis sebesar 12%,
maka selanjutnya dilakukan kembali uji rating hedonik terhadap 3 formula minuman kepada 70
orang panelis tidak terlatih yang berumur 30-80 tahun. Kelompok panelis ini dipilih asumsi dapat lebih mengerti akan manfaat minuman kesehatan, sehingga penerimaan akan lebih baik.
Pada tahap uji sensori ini, hasil penilaian dari panelis menunjukkan bahwa ada perbedaan nyata antar sampel pada semua parameter. Perbedaan tingkat konsentrasi jeruk nipis pada minuman fungsional campuran sirih merah, kayu manis, jahe, dan jeruk nipis menghasilkan perbedaan tingkat kesukaan yang signifikan. Jeruk nipis diketahui memiliki rasa asam kandungan
flavonoid dan fenolik tinggi (Ghafar et al. 2010). Rasa asam jeruk nipis diharapkan dapat
membantu penerimaan minuman fungsional serta kandungan senyawa aktifnya dapat meningkatkan kapasitas antioksidan minuman. Hasil analisis uji ini dapat dilihat pada Lampiran 5.
Tingkat kesukaan dari parameter warna berkisar pada skala 3 (agak suka), dan terdapat perbedaan kesukaan antara formula 3 dan 5, walaupun tidak terdapat perbedaan signifikan dengan formula 4. Tingkat kesukaan paling tinggi terhadap parameter warna adalah pada minuman dengan tingkat konsentrasi jeruk nipis 3, yakni sebesar 3.3714. Tingkat kesukaan pada parameter aroma berkisar pada skala 3 (agak suka). Hasil uji menunjukkan adanya perbedaan kesukaan antara sampel dengan tingkat konsentrasi 3 dan dua konsentrasi lainnya, walaupun tidak terdapat perbedaan signifikan antara sampel dengan tingkat konsentrasi 4 dan 5. Tingkat kesukaan paling tinggi terhadap parameter aroma adalah pada minuman dengan tingkat konsentrasi jeruk nipis 4, yakni sebesar 3.4000.
Tingkat kesukaan dari parameter rasa berkisar pada skala 1-2 (sangat tidak suka-agak tidak suka). Hasil uji ini menunjukkan adanya perbedaan kesukaan antara sampel dengan tingkat konsentrasi 3 dan dua konsentrasi lainnya, walaupun tidak terdapat perbedaan signifikan antara sampel dengan tingkat konsentrasi 4 dan 5. Tingkat kesukaan paling tinggi terhadap parameter aroma adalah pada minuman dengan tingkat konsentrasi jeruk nipis 4, yakni sebesar 2.3857.
Tingkat kesukaan pada parameter overall berkisar pada skala 2 (agak tidak suka), dan terdapat
perbedaan kesukaan antara sampel dengan tingkat konsentrasi 3 dan dua konsentrasi lainnya walaupun tidak terdapat perbedaan signifikan antara sampel dengan tingkat konsentrasi 4 dan 5.
Tingkat kesukaan paling tinggi terhadap parameter overall adalah pada minuman dengan tingkat
konsentrasi jeruk nipis 4, yakni sebesar 2.6429. Dengan mempertimbangkan hasil uji sensori dan kapasitas antioksidan dari 3 formula tersebut (Tabel 6), maka formula 4 adalah formula terpilih.
22
sampel 472). Kulit buah mundar yang berwarna merah cerah serta rasanya yang asam diharapkandapat memperbaiki penerimaan terhadap rasa serta warna minuman sirih merah (Saleh et al. 2012).
Warna merah cerah dari ekstrak kulit buah mundar memiliki keunggulan dalam memperbaiki warna minuman dibandingkan ekstrak jeruk nipis. Formula-formula tersebut diuji kepada panelis dengan uji beda dari kontrol. Pada pengujian tersebut, formula utama yang ditambahkan dengan perasan jeruk nipis juga disajikan sebagai kontrol dan juga sebagai sampel dengan kode 405.
Uji beda dari kontrol terhadap sampel-sampel tersebut memberikan hasil yang berbeda nyata antara sampel kontrol dengan ketiga sampel lainnya pada 4 parameter yang diujikan. Jika dilihat dari parameter warna, maka sampel 489 memiliki perbedaan yang moderat dengan sampel kontrol, sedangkan sampel 414 dan 472 memiliki perbedaan yang cukup besar dengan kontrol. Pada pengolahan data lebih lanjut, sampel 489, 414, dan 472 diketahui memberikan kesan warna
yang lebih buruk dibanding dengan kontrol, yakni bernilai 0,1 – 0,2 yang mana nilai 0 mewakili
nilai lebih buruk dan nilai 1 mewakili nilai lebih baik.
Hasil pengujian parameter aroma menyatakan bahwa sampel 489 agak berbeda dengan sampel kontrol, sedangkan sampel 414 dan 472 memiliki perbedaan yang moderat dibanding dengan kontrol. Pada pengolahan data lebih lanjut, sampel 489, 414, dan 472 diketahui
memberikan kesan aroma yang lebih buruk dibanding dengan kontrol (0 – 0,1). Jika dilihat dari
parameter rasa, maka sampel 489, 414, dan 472 memiliki perbedaan yang moderat dengan sampel kontrol. Ketiga sampel tidak berbeda nyata. Pada pengolahan data lebih lanjut, sampel 489, 414, dan 472 diketahui memberikan kesan yang lebih buruk dibanding dengan kontrol (0 – 0,1). Secara
overall, terlihat bahwa sampel 489 agak berbeda dengan sampel kontrol, sedangkan sampel 414 dan 472 memiliki perbedaan yang moderat dibandingkan dengan kontrol. Pada pengolahan data lebih lanjut, sampel 489, 414, dan 472 diketahui memberikan kesan yang lebih buruk dibanding
dengan kontrol (0 – 0,1). Hasil analisis selengkapnya untuk uji beda dari kontrol ini dapat dilihat
pada Lampiran 5.
Berdasarkan beberapa upaya yang dilakukan untuk memperbaiki citarasa minuman fungsional berbasis sirih merah, formula 4 adalah formula terpilih karena dapat memberikan tingkat kesukaan terhadap citarasa yang kurang lebih mendekati minuman fungsional berbahan dasar sirih merah yang telah dibuat pada penelitian sebelumnya, yakni pada tingkat agak suka
(Yasni et al. 2010). Formula terpilih inilah yang kemudian akan dijadikan sampel penentuan umur
simpannya.
4.4.
Analisis Komponen Volatil Senyawa Minuman
Komponen volatil pada bahan penyusun pangan sangat penting untuk diketahui, karena komponen volatil akan mempengaruhi aroma produk pangan. Sebagian besar komponen volatil berbentuk fraksi minyak atsiri. Minyak atsiri adalah kelompok senyawa berbau, larut dalam alkohol, terdiri dari campuran eter, aldehida, keton, dan terpen. Kelompok senyawa kimia yang bersifat volatil ini diantaranya adalah hidrokarbon (senyawa terpena rendah), turunan oksigenasi dari senyawa terpena, dan senyawa aromatik struktur benzoid (Nychas dan Tassou 2000).
Pada penelitian ini dianalisa komponen volatil yang ada pada bubuk sirih merah serta pada minuman fungsional sirih merah, jahe, kayu manis, dan jeruk nipis. Berdasarkan data yang didapat dari hasil analisis GCMS pada bubuk sirih merah, diketahui terdapat 62 komponen volatil, dan
lima komponen volatil dengan persentase luas area terbesar adalah -curcumene 6,90%, -linalool
23
volatil pada minuman fungsional yang dapat diidentifikasi berjumlah 69 komponen dan limakomponen yang memiliki luas area terbesar adalah -curcumene (12,45%), geraniol acetate
(4,89%), p-menth-1-en-8-ol (4,74%), (-)-zingiberene (4,43%), dan β-bisabolene (4,42%).
Perbedaan jumlah komponen volatil pada ekstrak sirih merah dan minuman fungsional disebabkan oleh perbedaan komponen penyusun pada minuman fungsional yang terbuat dari 4 bahan baku. Ada dua komponen volatil utama pada minuman fungsional yang juga merupakan
komponen volatil utama pada sirih merah, yakni -curcumene dan (-)-zingiberene. Nilai
komponen -curcumene yang meningkat pada minuman terjadi karena adanya kandungan
-curcumene yang berasal dari bahan baku lain, seperti jahe (Djafar et al. 2010) dan kayu manis
(Aggarwal et al. 2005).
Komponen -curcumene merupakan kelompok sesquiterpene (Anonim 2011) yang
memiliki kemampuan antidiabetik (Rao et al. 2010). Alfa-curcumene juga diketahui memiliki
fungsi dalam menurunkan tingkat kolesterol dalam darah (Aggarwal et al. 2005). Peningkatan
jumlah -curcumene pada minuman fungsional menunjukkan adanya sinergisme antar bahan
dalam minuman tersebut sebagai komponen antidiabetik.
4.5.
Analisis Proksimat Formula Terpilih
Analisis proksimat adalah analisis yang dilakukan untuk mengetahui kandungan lima komponen utama dalam suatu bahan pangan, yaitu kadar air, kadar abu (mineral), dan kadar protein yang hasilnya kemudian dapat dicantumkan pada label produk. Kadar air dan kadar abu dapat direpresentasikan dalam basis basah ataupun basis kering.
Kadar air menunjukkan kandungan air yang terkandung dalam bahan. Kadar air dari minuman ini adalah 85,24% (bb). Hal ini menunjukkan kandungan air yang cukup besar pada produk, karena pada dasarnya produk minuman kesehatan ini didominasi oleh air. Kadar abu merujuk pada residu anorganik yang tertinggal setelah proses oksidasi dari komponen organic pada sebuah produk pangan. Kadar abu menunjukkan kandungan total mineral dalam pangan (Nielson 2010), dan dalam produk minuman kesehatan ini berjumlah 0,35% (bb) atau 2,37% (bk). Kandungan abu yang rendah menunjukkan bahwa kandungan mineral dalam minuman kesehatan ini cukup rendah, demikian pula kadar proteinnya yang berjumlah 0,41% (bb) atau 2,80% (bk). Kandungan total gula dari minuman kesehatan berbasis sirih merah ini adalah 5,05%.
4.6.
Analisis Fisik dan Kimia Formula Terpilih
4.6.1.
Massa Jenis
Massa jenis adalah perbandingan antara massa suatu zat dengan volumenya. Setiap benda akan memiliki massa jenis yang berbeda-beda. Massa jenis tidak dipengaruhi oleh bentuk dari benda, tetapi dipengaruhi oleh volume dari benda. Suhu yang turut mempengaruhi volume suatu zat juga ikut mepengaruhi massa jenis dari suatu zat atau benda (Nielsen 2010).
24
suatu beban terstandar yang diberikan pada suatu sampel cair dan kemudian diukur penambahan volume yang terjadi. Prinsip kerja hidrometer ini mengikuti prinsip Archimedes. Piknometer adalah salah satu alat untuk mengukur massa jenis dengan membandingkan bobot dengan suatu volume tetap dari alat tersebut. Hasil massa jenis (densitas) yang didapat dari piknometer ini adalah hasil perbandingan dengan densitas air (Nielsen 2010).Pengukuran massa jenis minuman fungsional dilakukan dengan alat piknometer pada suhu
ruang dan menghasilkan massa jenis minuman sebesar 1,0733 g/ml (= g/cm3). Massa jenis
minuman kesehatan berbasis sirih merah tidak jauh berbeda dengan massa jenis air, yaitu sebesar 1
g/cm3, karena komponen utama dari minuman adalah air yang berinteraksi dengan
komponen-komponen dari bahan baku. Nilai massa jenis minuman ini yang sedikit lebih tinggi dibandingkan air disebabkan adanya kandungan pati (jahe) dari bahan baku yang ikut terekstrak. Pengetahuan massa jenis dapat digunakan untuk mengetahui kandungan zat di dalam minuman yang kemudian digunakan dalam pembuatan bentuk lain dari minuman ini (oleoresin atau nanoemulsi).
4.6.2.
Viskositas
Reologi adalah suatu ilmu yang mempelajari respon suatu bahan terhadap tekanan yang diberikan. Salah satu respon yang dipelajari dalam reologi ini adalah viskositas. Viskositas sendiri didefinisikan sebagai suatu tahanan internal (berasal dari bahan) untuk mengalir. Salah satu parameter yang penting dalam menggambarkan sifat reologi suatu bahan adalah suhu. Biasanya, viskositas akan menurun seiring meningkatnya suhu. Artinya, suatu bahan akan lebih mudah mengalir atas tekanan yang diberikan kepadanya pada suhu yang lebih tinggi (Nielsen 2010).
Viskositas dari minuman fungsional diukur menggunakan alat Brookfield Viscometer.
Prinsip kerja alat ini adalah dengan memberikan beban pada bahan sebagai tekanan. Beban dapat
berupa suatu tabung silinder logam, cone, atau plate. Beban tersebut kemudian diputar dengan
kecepatan tertentu dan skala yang terbaca pada alat kemudian dikalikan dengan faktor konversi yang ada dan didapatlah nilai viskositas bahan.
Nilai viskositas dari minuman fungsional ini adalah 9,625 cP. Nilai ini lebih besar dari nilai viskositas air, yaitu 1 cP (Nielsen 2010) ataupun viskositas minuman fungsional dengan
penambahan barley
-glukan, yaitu 4,43 cP (Din 2009). Apabila dibandingkan dengan nilaiviskositas sari buah komersial yang beredar, yaitu sekitar 1,77-6,61 cP (Pratiwi 2009), kekentalan minuman fungsional ini masih lebih tinggi. Tingkat kekentalan minuman yang tinggi diduga karena adanya pengaruh dari ekstrak air dari kayu manis yang ditambahkan pada minuman. Hal ini diperkuat dengan penelitian Al-Dhubiab (2012), yakni viskositas dari ekstrak pektin kulit kayu manis adalah 1000 cP. Rincian pengukuran viskositas ini dapat dilihat pada Lampiran 9.
4.6.3.
Total Padatan Terlarut
25
Nilai TPT dari minuman fungsional berbasis sirih merah adalah 15,62 oBrix, artinya
terdapat 15,62 gram sukrosa per 100 gram sampel. Nilai ini lebih tinggi dari nilai gula yang ditambahka