PENENTUAN NILAI pH DAN ALKALINITAS PADA AIR
FILTER HM. YAMIN DI LABORATORIUM
PDAM TIRTANADI MEDAN
TUGAS AKHIR
OLEH:
RAMAHDANI
NIM 102410053
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KATA PENGANTAR
Bismillahirahmanirahim
Segala puji bagi Rabb semesta alam Allah swt yang telah melimpahkan rahmat, karunia, dan ridho-Nya serta memberikan ilmu-Nya kepada setiap hamba-Nya sebagai nur dalam kehidupan. Shalawat berangkaikan salam dihadiahkan kepada kekasih-Nya, Rasulullah saw yang telah membawa cahaya islam bagi manusia di seluruh penjuru dunia.
Alhamdulillah, berkat bantuan Sang Ilahi penulis dapat menyelesaikan tugas akhir yang berjudul “Penentuan Nilai pH dan Alkalinitas pada Air Filter HM. Yamin di Laboratorium PDAM Tirtanadi Medan”. Tugas akhir ini diajukan sebagai salah satu syarat untuk memperoleh gelar ahli madya analis farmasi dan makanan pada Fakultas Farmasi Universitas Sumatera Utara.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak, penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya. Untuk itu penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada berbagai pihak atas bimbingan dan bantuannya terutama kepada:
2. Kak Devi, Abang Zainul, Kak Teta, Abang Ali, Abang Idhul, dan Adik Azmar terima kasih atas do’a, dorongan dan pengorbanan baik moril maupun materil dalam penyelesaian tugas akhir ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan bantuan dan fasilitas selama masa pendidikan.
4. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt, selaku Ketua Program Studi Diploma-III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan perhatiaanya kepada penulis dan seluruh mahasiswa Analis Farmasi dan Makanan.
5. Bapak Dr. Edy Suwarso, S.U., Apt., selaku Dosen Pembimbing penulis yang telah membimbing dengan penuh kesabaran, tulus dan ikhlas selama penetilian dan penulisan tugas akhir ini berlangsung.
6. Bapak Dr. Maratua Pandapotan Nasution, MPS., Apt., selaku Dosen Penasehat Akademik selama penulis menjalankan proses perkuliahan. 7. Bapak dan Ibu staf pengajar Fakultas Farmasi Universitas Sumatera Utara
atas semua ilmu, didikan dan bimbingan kepada penulis selama diperguruan tinggi ini.
8. Staf administrasi di Fakultas Farmasi yang telah membantu penulis dalam kemudahan administrasi selama ini.
10. Bang Dikky, Kak Astri, Kak Clara, Kak Yuni, Rahman, Tiwi, Yani, dan seluruh teman-teman seperjuangan Analis Farmasi dan Makanan stambuk 2010 yang tidak dapat penulis sebutkan satu per satu, terima kasih telah memberikan semangat kepada penulis dalam mengarungi perjuangan ini. Salam Kompak untuk kita semua.
11. Adik-adik stambuk 2011 dan 2012 yang tidak dapat disebutkan namanya satu per satu, terima kasih buat kebersamaan, semangat, dan do’anya yang ditujukan kepada penulis.
12. UKMI AT-THIBB FF USU terima kasih telah mengizinkan penulis untuk melebur di dalamnya, memberikan motivasi, mengajari untuk selalu bekerja sama, dan saling mendo’akan. Penulis berharap semoga silahtuhrrahmi tetap terjalin.
13. Serta pihak-pihak yang telah ikut membantu penulis namun tidak tercantum namanya.
Penulis menyadari sepenuhnya bahwa Tugas Akhir ini masih terdapat kekurangan, baik dalam penulisan maupun penyajian. Penulis mengharapkan kritik dan saran yang membangun demi kesempurnaan Tugas Akhir ini.
Akhir kata semoga Allah swt melimpahkan Rahmat dan Karuni-Nya kepada kita semua dan semoga Tugas Akhir ini bermanfaat bagi kita semua.
Medan, April 2013
Penulis,
Ramahdani
Determination Of pH And Alkalinity In Water Filter HM. Yamin In The Laboratory Tirtanadi Medan
Abstract
Water is a chemical compound that is essential for the process of life, a lot of water is used for cooking, washing, bathing, and so on. In the provision of drinking water, and the pH value of the water alkalintas is one factor to be considered in the drinking water quality standards. Experiment goal is to determine the pH and alkalinity of the water filter HM.Yamin used as drinking water.
Sample taken from the water faucet filter derived from the production wellbore Tritanadi PDAM Medan. Determination of pH and alkalinity values carried by direct potentiometric and titrimetric methods in accordance with the procedures and tools used in the Laboratory Tirtanadi.
The results showed that the water filter HM. Yamin has examined the pH 7.20 where the results have not exceeded the maximum levels set by the Minister Regulation. 492/Menkes/Per/IV/2010 ie 6.5 to 8.5. And alkalinitasnya content is 120 mg / l CaCO3 where according to Effendi (2003), a good alkalinity values ranged between 30-500 mg / l CaCO3.
PENENTUAN NILAI pH DAN ALKALINITAS PADA AIR FILTER HM. YAMIN DI LABORATORIUM PDAM TIRTANADI MEDAN
Abstrak
Air merupakan senyawa kimia yang sangat penting bagi proses kehidupan, air banyak yang digunakan untuk memasak, mencuci, mandi, dan sebagainya. Dalam penyediaan air minum, pH dan nilai alkalintas air merupakan salah satu faktor yang harus dipertimbangkan dalam standar mutu air minum. Tujuan peneletiaan ini adalah untuk menentukan nilai pH dan alkalinitas pada air filter HM.Yamin yang digunakan sebagai air minum.
Sampel di ambil dari kran air filter yang berasal dari sumur bor produksi PDAM Tritanadi Medan. Penentuan nilai pH dan alkalinitas dilakukan menurut metode potensiometri langsung dan titrimetri sesuai dengan prosedur dan alat yang digunakan di Laboratorium PDAM Tirtanadi Medan
Hasil penelitian menunjukkan bahwa air filter HM. Yamin yang diperiksa memiliki pH yaitu 7,20 di mana hasil ini belum melebihi batas kadar maksimum yang ditetapkan oleh Permenkes No. 492/Menkes/Per/IV/2010 yakni 6,5-8,5. Dan kandungan alkalinitasnya adalah 120 mg/l CaCO3 di mana menurut Effendi
(2003), nilai alkalinitas yang baik berkisar antara 30-500 mg/l CaCO3.
2.3.4 Persyaratan Penyediaan Air Minum ... 10
2.4 Teknik Pengambilan Sampel Air ... 11
2.4.1 Pengambilan Sampel ... 11
2.4.2 Penentuan Titik Pengambilan Sampel ... 12
2.5 Derajat Keasaman (pH) ... 14
2.5.1 Defenisi Derajat Keasaman (pH) ... 14
2.5.2 Analisis Derajat Keasaman (pH) ... 14
2.6 Alkalinitas ... 16
2.6.1 Defenisi Alkalinitas ... 16
2.6.2 Analisis Alkalinitas Air Secara Titrimetri ... 19
DAFTAR TABEL
DAFTAR LAMPIRAN
Determination Of pH And Alkalinity In Water Filter HM. Yamin In The Laboratory Tirtanadi Medan
Abstract
Water is a chemical compound that is essential for the process of life, a lot of water is used for cooking, washing, bathing, and so on. In the provision of drinking water, and the pH value of the water alkalintas is one factor to be considered in the drinking water quality standards. Experiment goal is to determine the pH and alkalinity of the water filter HM.Yamin used as drinking water.
Sample taken from the water faucet filter derived from the production wellbore Tritanadi PDAM Medan. Determination of pH and alkalinity values carried by direct potentiometric and titrimetric methods in accordance with the procedures and tools used in the Laboratory Tirtanadi.
The results showed that the water filter HM. Yamin has examined the pH 7.20 where the results have not exceeded the maximum levels set by the Minister Regulation. 492/Menkes/Per/IV/2010 ie 6.5 to 8.5. And alkalinitasnya content is 120 mg / l CaCO3 where according to Effendi (2003), a good alkalinity values ranged between 30-500 mg / l CaCO3.
PENENTUAN NILAI pH DAN ALKALINITAS PADA AIR FILTER HM. YAMIN DI LABORATORIUM PDAM TIRTANADI MEDAN
Abstrak
Air merupakan senyawa kimia yang sangat penting bagi proses kehidupan, air banyak yang digunakan untuk memasak, mencuci, mandi, dan sebagainya. Dalam penyediaan air minum, pH dan nilai alkalintas air merupakan salah satu faktor yang harus dipertimbangkan dalam standar mutu air minum. Tujuan peneletiaan ini adalah untuk menentukan nilai pH dan alkalinitas pada air filter HM.Yamin yang digunakan sebagai air minum.
Sampel di ambil dari kran air filter yang berasal dari sumur bor produksi PDAM Tritanadi Medan. Penentuan nilai pH dan alkalinitas dilakukan menurut metode potensiometri langsung dan titrimetri sesuai dengan prosedur dan alat yang digunakan di Laboratorium PDAM Tirtanadi Medan
Hasil penelitian menunjukkan bahwa air filter HM. Yamin yang diperiksa memiliki pH yaitu 7,20 di mana hasil ini belum melebihi batas kadar maksimum yang ditetapkan oleh Permenkes No. 492/Menkes/Per/IV/2010 yakni 6,5-8,5. Dan kandungan alkalinitasnya adalah 120 mg/l CaCO3 di mana menurut Effendi
(2003), nilai alkalinitas yang baik berkisar antara 30-500 mg/l CaCO3.
BAB I PENDAHULUAN
1.1 Latar Belakang
Planet bumi sebagian besar terdiri atas air karena luas daratan memang lebih kecil dibandingkan dengan luas lautan. Makhluk hidup yang ada di bumi ini tidak dapat terlepas dari kebutuhan akan air. Air merupakan senyawa kimia yang sangat penting bagi proses kehidupan di mana fungsinya tidak dapat digantikan oleh senyawa lain. Selain itu, air merupakan sumber daya alam yang diperlukan untuk hajat hidup orang banyak yang dipergunakan untuk memasak, mencuci, mandi, dan membersihkan kotoran yang ada di sekitar rumah. Air juga digunakan untuk keperluan industri, pertanian, pemadam kebakaran, tempat rekreasi, transportasi, dan lain-lain (Wardhana, 2004).
Sebagian besar keperluan air sehari-hari berasal dari sumber air tanah dan sungai, air yang berasal dari PAM (air ledeng) juga bahan bakunya berasal dari sungai, oleh karena itu sumber daya air harus dilindungi agar tetap dapat dimanfaatkan dengan baik oleh manusia serta mahkluk hidup lainnya (Achmad, 2004).
Pengelolaan sumber daya air sangat penting, agar dapat dimanfaatkan secara berkelanjutan dengan tingkat mutu yang diingikan. Salah satu langkah pengelolaannya yang dilakukan adalah pemantuan dan interpretasi data kualitas air, mencakup kualitas fisika, kimia, dan biologi (Effendi, 2003).
Di sini penulis tertarik melakukan pemantauan kualitas air berdasarkan dua parameter dari segi kimia yaitu pH dan nilai alkalinitas air pada air filter HM.Yamin yang berasal dari sumur bor produksi PDAM Tirtanadi yang dilakukan di Laboratorium PDAM Tirtanadi dengan satu kali pengukuran di mana air ini nantinya dapat digunakan sebagai air minum oleh masyarakat. Dalam penyediaan air minum, pH dan nilai alkalintas air merupakan salah satu faktor yang harus dipertimbangkan dalam standar mutu air minum, mengingat pengaruhnya yang dapat menyangkut aspek kesehatan bagi masyarakat.
1.2 Tujuan
Untuk mengetahui apakah nilai pH dan nilai alkalinitas air filter HM. Yamin memenuhi persyaratan standar mutu air minum berdasarkan Peraturan Menteri Kesehatan Republik Indonesia No. 492/MENKES/PER/IV/ 2010.
1.3 Manfaat
BAB II
TINJAUAN PUSTAKA
2.1 Air
2.1.1 Defenisi Air
Air adalah senyawa yang setiap molekulnya mangandung dua atom hidrogen yang terikat pada satu oksigen. Air terbentuk ketika hidrogen terbakar di udara. Secara alamiah air tidak pernah dijumpai dalam keadaan betul-betul murni (Sutrisno dan Eni, 2010).
Air merupakan zat yang paling penting dalam kehidupan setelah udara. Sekitar tiga per empat bagian dari tubuh kita terdiri dari air dan tidak seorangpun dapat bertahan hidup lebih dari 4-5 hari tanpa minum air (Chandra, 2006).
Dalam jaringan hidup, air merupakan medium untuk berbagai reaksi dan proses eksresi. Air merupakan komponen utama baik dalam tanaman maupun hewan termasuk manusia (Achmad, 2004).
2.1.2 Siklus Hidrologi Air
Lingkungan air disebut juga Hidrosfir. Lingkungan air sangat erat kaitannya dengan kehidupan manusia. Sekalipun air jumlahnya relatif konstan, tetapi air tidak diam, melainakan bersirkulasi akibat pengaruh cuaca, sehingga terjadi suatu siklus yang disebut siklus hidrologi (Mulia, 2005).
tumbuhan (transpirasi), hewan dan manusia (transpirasi, respirasi). Uap air ini memasuki atmosfir. Di dalam atmosfir uap ini akan menjadi awan dan dalam kondisi cuaca tertentu dapat mendingin dan berubah bentuk menjadi tetesan-tetesan air dan jatuh kembali ke permukaan bumi sebagai hujan. Air hujan ini ada yang mengalir langsung masuk ke dalam permukaan (runoff), ada yang meresap ke dalam tanah (perkolasi) dan menjadi air tanah, baik yang dangkal maupun yang dalam dan ada juga yang diserap oleh tumbuhan (Mulia, 2005).
Air tanah akan timbul ke permukaan sebagai mata air dan menjadi air permukaan. Air permukaan bersama-sama dengan air tanah dangkal dan air yang berada dalam tubuh akan menguap kembali menjadi awan,, maka siklus hidrologis akan kembali berulang. Siklus hidrologi merupakan aspek penting untuk mensuplai daerah daratan dengan air (Mulia, 2005).
2.2 Sumber-Sumber Air
Air yang berada di permukaan bumi ini dapat berasal dari berbagai sumber. Berdasarkan letak sumbernya air dapat di bagi menjadi air angkasa (hujan), air permukaan, dan air tanah.
2.2.1 Air Hujan
Air hujan merupakan jenis air yang paling murni. Namun, dalam perjalanannya turun ke bumi, air hujan akan melarutkan partikel-partikel debu dan gas yang terdapat dalam udara, misalnya gas CO2, gas N2O3, dan gas S2O3
2. Gas S2O3 + air hujan asam sulfat
3. Gas N2O3 + air hujan asam nitrit
Dengan demikian, air hujan yang sampai di permukaan bumi sudah tidak murni dan reaksi diatas dapat mengakibatkan keasaman pada air hujan sehingga akan terbentuk hujan asam (Chandra, 2006).
2.2.2 Air Permukaan
Air permukaan merupakan salah satu sumber penting bahan baku air bersih. Faktor-faktor yang harus diperhatikan, antara lain:
1. Mutu atau kualitas baku 2. Jumlah atau kuantitanya 3. Kontinuitasnya
Dibandingkan dengan sumber air lain, air permukaan merupakan sumber air yang paling tercemar akibat kegiatan manusia, fauna, flora, dan zat-zat lain (Chandra, 2006).
Menurut Sutrisno dan Eni (2010), sumber-sumber air permukaan ada dua macam, yakni:
a. Air Sungai
Air sungai dalam penggunaanya sebagai air minum haruslah mengalami suatu pengolahan yang sempurna, mengingat bahwa air sungai ini pada umumnya mempunyai derajat pengotoran yang tinggi sekali. Debit yang tersedia untuk memenuhi kebutuhan akan air minum pada umunya dapat mencukupi.
b. Air rawa/danau
Kebanyakan air rawa ini berwarna yang disebabkan oleh adanya zat-zat organis yang telah membusuk, misalnya asam humus yang larut dalam air yang menyebabkan warna kuning coklat. Dengan adanya pembusukan kadar zat organis tinggi, maka umumnya kadar Fe dan Mn akan tinggi pula dan dalam keadaan kelarutan O2 kurang sekali (anaerob), maka unsur-unsur Fe dan Mn ini akan larut.
Pada permukaan air akan tumbuh algae (lumut) karena adanya sinar matahari dan oksigen (O2).
2.2.3 Air Tanah
Air tanah merupakan sebagian air hujan yang mencapai permukaan bumi dan menyerap ke dalam lapisan tanah dan menjadi air tanah. Sebelum mencapai lapisan tempat air tanah, air hujan akan menembus beberapa lapisan tanah dan menyebabkan terjadinya kesadahan pada air (hardness of water) (Chandra, 2006).
Menurut Sutrisno dan Eni (2010), sumber-sumber air tanah terbagi atas tiga macam, yakni:
a. Air tanah dangkal
Air tanah dangkal terjadi karena daya proses peresapan air dari permukaan tanah. Air tanah dangkal ini dapat pada kedalaman 15,00 m. Air tanah dangkal ini ditinjau dari segi kualitasnya agak baik bila digunakan sebagai sumur air minum. Kuantitas air tanah dangkal ini kurang baik dan tergantung pada musim.
b. Air tanah dalam
penyaringan alamiah dan kebanyakan mikroba sudah tidak ada lagi terdapat di dalamnya. Air tanah dalam kualitasnya lebih baik dari air dangkal, karena penyaringannya lebih sempurna dan bebas dari bakteri. Perubahan musim juga hanya sedikit mempengaruhi air tanah dalam.
c. Mata air
Mata air adalah air tanah yang ke luar dengan sendirinya ke permukaan tanah. Mata air yang berasal dari tanah dalam, hampir tidak terpengaruh oleh musim dan kualitas/kuantitasnya sama dengan keadaan air dalam. Berdasarkan keluarnya (munculnya permukaan tanah) terbagi atas:
- rembesan, di mana air ke luar dari lereng-lereng.
- umbul, di mana air ke luar ke permukaan pada suatu dataran.
2.3 Air Minum
2.3.1 Definisi Air Minum
Air minum adalah air rumah tangga yang melalui proses pengolahan atau tanpa proses pengolahan yang memenuhi syarat kesehatan dan dapat langsung diminum (Jokoa, 2010).
2.3.2 Sistem Penyediaan Air Minum
1. Menyediakan air yang kualitasnya aman dan sehat bagi pemakainya. 2. Menyediakan air yang memadai kuantitasnya, dan
3. Menyediakan air secara kontinyu, mudah dan murah untuk menunjang hygiene perseorangan maupun rumah tangga.
Sistem penyediaan air minum harus dapat menyediakan jumlah air yang cukup untuk kebutuhan suatu kota.. Unsur-unsur sistem yang modern terdiri atas: sumber air baku, fasilitas penyimpanan, fasilitas transmisi ke unit pengolahan, fasilitas pengolahan, fasiltas transmisi dan penyimpanan, dan fasilitas distribusi (Jokoa, 2010).
2.3.3 Unit Produksi Air Minum
Unit produksi sistem penyediaan air minum berfungsi untuk mengolah air baku menjadi air minum. Untuk mencapai kualitas air yang sesuai dengan standar kualitas air minum tersebut, air baku diolah dengan proses pemisahan partikel kasar, proses pemisahan tersuspensi, proses pemisahan terlarut, proses netralisasi dan proses desinfeksi (Jokob, 2010).
Menurut Jokob (2010), pengolahan air adalah usaha-usaha teknis yang dilakukan untuk merubah sifat-sifat air tersebut. Hal ini penting sekali dalam air minum, karena dengan adanya proses pengolahan ini, maka akan diperoleh mutu air minum yang memenuhi standar yang telah ditentukan. Ada dua macam pengolahan air yang sudah dikenal, yaitu:
- Pengolahan sebagian, di sini air baku hanya mengalami proses pengolahan kimia dan/atau pengolahan bakteriologis.
Pada dasarnya, pengolahan air minum dapat diawali dengan penjernihan air, pengurangan kadar bahan-bahan kimia terlarut dalam air sampai batas yang dianjurkan, penghilangan mikroba patogen, memperbaiki derajat keasaman (pH) serta memisahkan gas-gas terlarut yang dapat mengganggu estetika dan kesehatan (Mulia, 2005).
Purifikasi air merupakan salah satu cara untuk menjernihkan atau memurnikan sumber air baku guna mendapatkan air bersih. Proses ini dapat dilakukan dalam skala besar maupun skala kecil disesuaikan dengan kebutuhannya (Chandra, 2006).
Menurut Chandra (2006), purifikasi air dalam skala besar dilakukan di daerah perkotaan. Proses semacam ini biasa dilakukan di instalasi penjernihan air bersih (PAM) melalui tahap berikut:
1. Penyimpanan (storage)
Air baku diisap atau dialirkan dari sumber seperti sungai, kali, sumur, dan sebagainya ke dalam bak penampungan alami atau bak buatan yang sudah dilindungi dari pencemaran. Air yang disimpan dalam wadah penampungan tersebut akan mengalami proses purifikasi secara alami yaitu proses fisik,, kimiawi, dan biologis.
2. Penyaringan (filtration)
98-99% dalam air yang dihasilkan. Proses filtrasi dapat dilakukan melalui slow sand filter (filter biologis) yang digunakan untuk purifikasi air dalam skala kecil,
dan rapid sand filter (filter mekanis) yang digunakan untuk purifikasi air dalam skala besar terutama untuk memenuhi kebutuhan penduduk di kota besar. Air yang telah melewati proses filtrasi ini disebut sebagai air filter.
3. Klorinasi (chlorination)
Klorinasi adalah proses pemberian klorin ke dalam air yang telah menjalani proses filtrasi dan merupakan langkah yang maju dalam proses purifikasi air.
2.3.4 Persyaratan Penyediaan Air Minum
Menurut Jokob (2010), secara umum ada beberapa persyaratan utama yang harus dipenuhi dalam sistem penyediaan air bersih, antara lain:
1. Persyaratan Kualitatif
Peryaratan kualitatif menggambarkan mutu/kualitas dari air bersih. Parameter-parameter yang digunakan sebagai standar kualitas air antara lain:
- Parameter fisik, meliputi padatan terlarut, kekeruhan, warna, rasa, bau, dan suhu.
- Parameter kimia, meliputi Total Dissolved Solids, alkalinitas, flourida, logam, kandungan organik dan nutrien.
- Parameter biologi, meliputi mikroorganisme yang dianggap patogen yaitu bakteri, virus, protozoa, dan cacing parasit (Helminths).
Setelah persyaratan kualitatif terpenuhi maka air bersih juga harus mampu melayani daerah pelayanan. Banyaknya penduduk yang ada dalam suatu wilayah harus mampu terpenuhi secara kuantitasnya. Persyaratan kuantitatif ini sangat dipengaruhi sekali dengan jumlah air baku yang tersedia, serta kapasitas produksi dari instalasi pengolahan air.
3. Persyaratan Kontinuitatif
Arti kontinuitatif disini adalah bahwa air baku untuk air bersih tersebut dapat diambil secara terus menerus dangan fluktuasi debit yang relatif tetap, baik pada musim hujan maupun musim kemarau. Sehingga persyaratan kontinuitas ini erat sekali hubungannya dengan persyaratan kuantitas.
4. Mudah diperoleh oleh konsumen 5. Harga air relatif murah
2.4 Teknik Pengambilan Sampel Air 2.4.1 Pengambilan Sampel
Menurut Effendi (2003), pengambilan sampel air dapat dilakukan melalui langkah-langkah sebagai berikut:
a. Disiapkan alat pengambilan sampel yang sesuai dengan keadaan sumber air. b. Alat-alat tersebut dibilas sebanyak tiga kali dengan sampel air yang akan
diambil.
d. Jika pengambilan sampel dilakukan pada beberapa titik maka volume sampel dari setiap titik harus sama.
2.4.2 Penentuan Titik Pengambilan Sampel
Menurut Effendi (2003), titik pengambilan sampel air yang berupa air permukaan dan air tanah ditetapkan dengan ketentuan-ketentuan sebagai berikut: a. Titik pengambilan sampel air permukaan
Pengambilan sampel air permukaan dapat dilakukan terhadap air sungai maupun air waduk. Titik pengambilan sampel air sungai ditetapkan menurut ketentuan-ketentuan sebagai berikut:
1. Pada sungai dengan debit kurang dari 5 m3/detik, sampel air diambil pada satu titik di tengah sungai pada 0,5 x kedalaman sungai.
2. Pada sungai dengan debit antara 5-150 m3/detik, sampel air diambil pada dua titik, masing-masing pada jarak 1/3 dan 2/3 lebar sungai pada 0,5 x kedalaman sungai.
3. Pada sungai dengan debit lebih dari 150 m3/detik, sampel air diambil minimum pada enam titik, masing-masing pada jarak ¼, ½, dan ¾ lebar sungai, pada 0,2 x kedalaman sungai dan 0,8 x kedalaman sungai.
Titik pengambilan sampel air danau atau waduk ditetapkan menurut ketentuan-ketentuan sebagai berikut:
2. Pada danau atau waduk dengan kedalaman antara 10 m – 30 m, sampel diambil pada titik, yaitu di permukaan, lapisan termoklin, dan di dasar danau.
3. diambil pada empat titik, yaitu permukaan, lapisan termoklin (metalimnion), di atas lapisan hipolimnion, dan dasar danau/waduk.
4. Pada danau atau waduk dengan kedalaman lebih dari 100 m, titik pengambilan sampel air dapat diperbanyak sesuai dengan keperluan.
b. Titik pengambilan sampel air tanah
Sampel air tanah dapat berupa sampel air tanah bebas dan sampel air tanah tertekan. Titik pengambilan sampel air tanah bebas ditetapkan menurut ketentuan-ketentuan sebagai berikut:
1. Pada sumur gali, sampel diambil pada kedalaman 20 cm di bawah permukaan air. Pengambilan sampel sebaiknya pada pagi hari.
2. Pada sumur bor dengan pompa tangan atau mesin, sampel diambil dari kran/mulut pompa (tempat keluarnya air). Pengambilan sampel dilakukan kira-kira lima menit setelah air mulai dibuang.
Titik pengambilan sampel air tanah tertekan ditetapkan menurut ketentuan-ketentuan sebagai berikut:
1. Pada sumur bor eksplorasi, sampel diambil pada titik yang telah ditentukan sesuai dengan keperluan eksplorasi.
3. Pada sumur produksi, sampel diambil pada kran/mulut pompa (tempat keluarnya air).
2.5 Derajat Keasaman (pH)
2.5.1 Defenisi Derajat Keasaman (pH)
pH adalah merupakan istilah yang digunakan untuk menyatakan intensitas keadaan asam atau basa sesuatu larutan. Ia merupakan juga satu cara untuk menyatakan konsentrasi ion H+ (Sutrisno dan Eni, 2010).
Air murni (H2O) berasosiasi sempurna sehingga memiliki ion H+ dan ion
OH- dalam konsentrasi yang sama, dan dalam keadaan demikian pH air murni = 7 (Ghufran dan Andi, 2007).
Air dapat bersifat asam atau basa, tergantung pada besar kecilnya pH air atau besarnya konsentrasi ion hidrogen di dalam air. Air normal yang memenuhi syarat untuk kehidupan mempunyai pH antara 6,5-7,5. Untuk air minum sebaiknya memiliki pH antara 6,5-8,5 (Sunu, 2001).
Air yang mempunyai pH lebih kecil dari pH normal akan bersifat asam, sedangkan air yang mempunyai pH lebih besar dari normal akan bersifat basa. Klasifikasi nilai pH yaitu netral (pH=7), asam (0<pH<7), dan basa atau alkalis (7<pH<14) (Wardhana, 2004).
2.5.2 Analisis Derajat Keasaman (pH)
akurat dibandingkan dengan kertas lakmus dan cara calorimeter (Sutrisno dan Eni, 2010).
Penggunaan pH meter atau mengukur ion spesifik untuk mengukur konsentrasi ion hidrogen atau suatu ion yang lain dalam larutan, jelas merupakan contoh potensiometri langsung (Basset, et al., 1991).
Potensiometri adalah satu cara elektrokimia untuk analisa ion secara kuantitatif berdasarkan pengukuran potensial dari elektroda yang peka terhadap ion yang bersangkutan. Potensiometri digunakan untuk menentukan konsentrasi suatu ion, pH larutan, dan titik akhir titrasi. Alat-alat yang diperlukan dalam metode potensiometri adalah elektrode pembanding (refference electrode), elektroda indikator (indicator electrode), dan alat pengukur potensial. Komponen-komponen tersebut disusun membentuk suatu sel potensiometri (Lesna, 2011).
pH Meter adalah sebuah alat elektronik yang digunakan untuk mengukur pH (kadar keasaman atau alkalinitas) dari suatu larutan. Pada prinsipnya pengukuran suatu pH adalah didasarkan pada potensial elektrokimia yang terjadi antara larutan yang terdapat didalam elektroda gelas (membran gelas) yang telah diketahui dengan larutan yang terdapat diluar elektroda gelas yang tidak diketahui. Hal ini dikarenakan lapisan tipis dari gelembung kaca akan berinteraksi dengan ion hidrogen yang ukurannya relatif kecil dan aktif, elektroda gelas tersebut akan mengukur potensial elektrokimia dari ion hidrogen atau diistilahkan dengan potential of hidrogen (Anonim, 2012).
yang terukur. Elektroda kaca (gelas) merupakan elektroda indikator yang peka akan ion hidrogen yang paling meluas penggunaanya, dan penggunaannya bergantung pada fakta bahwa bila suatu selaput kaca dibenamkan dalam suatu larutan, terjadi suatu potensial yang merupakan fungsi linier dari konsentrasi ion hidrogen larutan itu. Untuk mengukur konsentrasi ion hidrogen dari suatu larutan, elektroda kaca itu harus digabung dengan sebuah elektroda pembanding; elektroda kalomel paling lazim digunakan (Basset, et al., 1991).
Untuk mengukur pH larutan dengan pH meter, maka pH meter harus dikalibrasi menggunakan larutan-larutan buffer, jika larutan ini belum tersedia, buffer kalium hidrogen ftalat (pH 4), dan buffer natrium tetraborat (pH 9,2) merupakan buffer yang paling sering digunakan untuk maksud kalibrasi. Setelah dikalibrasi, mulailah mengukur pH larutan yang diberikan. Selesai penetapan, jangan lupa mencuci elektroda dengan air suling, dan membiarkan mereka tetap tercelup dalam air suling (Basset, et al., 1991).
2.6 Alkalinitas
2.6.1 Defenisi Alkalinitas
Alkalinitas atau yang lebih dikenal dengan total alkalinitas adalah konsentrasi total dari unsur basa-basa yang terkandung dalam air dan biasa dinyatakan dalam mg/L atau setara dengan kalsium karbonat (CaCO3) (Ghufran
dan Andi, 2007).
karbonat, dan hidroksidanya. Alkalinitas keseluruhan biasanya dinyatakan dengan padanan kalsium karbonat dalam miligram per liter (Linsley dan Joseph, 1979).
Pada umunya, komponen utama yang memegang peran dalam menentukan alkalinitas perairan adalah ion bikarbonat, ion karbonat, dan ion hidroksil.
HCO3- + H+ CO2 + H2O
CO3- + H+ HCO3-
OH- + H+ H2O
Alkalinitas umumnya dinyatakan sebagai alkalinitas phenolftalein yaitu proses situasi dengan asam untuk mencapai pH 8,3 dimana HCO3- merupakan ion
terbanyak, dan alkalinitas total yang menyatakan situasi dengan asam menuju titik akhir indikator metal jingga (pH 4,3), yang ditunjukan oleh berubahnya kedua jenis karbonat dan ion bikarbonat menjadi CO2 (Achmad, 2004).
Bikarbonat, karbonat, dan asam karbonat merupakan sumber utama karbon anorganik di perairan. Karbon anorganik di perairan dapat berasal dari beberapa sumber, yaitu atmosfer, batuan karbonat, siklus biologi karbon, dan sumber
allocthonous (dari luar perairan). Tingginya kadar bikarbonat di perairan
disebabkan oleh ionisasi asam karbonat, terutama pada perairan yang banyak mengandung karbondioksida (kadar CO2 mengalami saturasi/jenuh).
Karbondioksida di perairan bereaksi dengan basa yang terdapat pada batuan dan tanah membentuk bikarbonat (HCO3-) (Effendi, 2003).
dapat berperan sebagai asam dengan melepaskan ion H+ seperti persamaan reaksi (b).
HCO3- + H+ H2O + CO2 (a)
HCO3- H+ + CO3 2- (b)
Bikarbonat mengandung asam (CO2) dan basa (CO3 2-) pada konsentrasi
yang sama, seperti yang ditunjukkan dalam persamaan reaksi (c). 2HCO3- CO2 + CO32- + H2O (c)
Selain karena bereaksi dengan ion H+, karbonat dianggap basa karena dapat mengalami hidrolisis menghasilkan OH-, seperti persamaan reaksi (d).
CO32- + H2O HCO3- + OH- (d)
Sifat kebasaan CO32- lebih kuat dari pada sifat keasaman CO2 sehingga
pada kondisi kesetimbangan, ion OH- dalam larutan bikarbonat selalu melebihi ion H+ (Effendi, 2003).
Menurut Effendi (2003), alkalinitas berperan dalam hal-hal sebagai berikut:
1. Sistem penyangga (buffer)
Bikarbonat yang terdapat pada perairan dengan nilai alkalinitas total tinggi berperan sebagai penyangga (buffer capacity) perairan terhadap perubahan pH yang drastis.
2. Koagulasi Kimia
alkalinitas berperan sebagai penyangga untuk mengetahui kisaran pH yang optimum bagi penggunaan koagulan. Dalam hal ini alkalinitas sebaiknya berada pada kisaran optimum untuk mengikat hidrogen yang dilepaskan pada proses koagulasi.
3. Pelunakan air (water softening)
Alkalinitas adalah parameter kualitas air yang harus dipertimbangankan dalam menentukan jumlah soda abu dan kapur yang diperlukan dalam proses pelunakan (softening) dengan metode presipitasi. Pelunakan air bertujuan untuk menurunkan kesadahan.
2.6.2 Analisis Alkalinitas Air Secara Titrimetri
Analisis titrimetri mengacu pada analisis kimia kuantitatif yang dilakukan dengan menetapkan volume suatu larutan yang konsentrasinya diketahui dengan tepat, yang diperlukan untuk bereaksi secara kuantitatif dengan larutan dari zat yang akan ditetapkan. Larutan dengan konsentrasi yang diketahui tepat itu, disebut larutan standar (Basset, et al., 1991).
Menurut Bassett, et al., (1991), untuk digunakan dalam analisis titrimetri, suatu reaksi harus memenuhi kondisi-kondisi berikut:
1. Harus ada suatu reaksi yang sederhana, yang dapat dinyatakan dengan suatu persamaan kimai, zat yang ditetapkan harus bereaksi lengkap dengan reagensia dalam proporsi yang stoikiometrik atau ekuivalen.
2. Reaksi harus praktis berlangsung dalam sekejap atau berjalan dengan sangat cepat sekali.
3. Harus ada perubahan yang menyolok dalam energi bebas, yang menimbulkan perubahan dalam beberapa sifat fisika atau kimia pada titik ekuivalen.
4. Harus tersedia suatu indikator, yang oleh perubahan sifat-sifat fisika (warna atau pembentukan endapan), harus dengan tajam menetapkan titik akhir reaksi.
Reaksi dalam analisis titrimetri digolongkan menjadi reaksi penetralan (asidimetri dan alkalimetri), reaksi pembentukan kompleks, reaksi pengendapan, dan reaksi oksidasi-reduksi (Basset, et al., 1991).
Ciri-ciri khas utama dari indikator penetralan adalah bahwa perubahan dari warna dominan asam menjadi warna dominan basa tidaklah mendadak sekaligus, tetapi berjalan di dalam suatu selang (interval) pH yang dinamakan selang perubahan-warna indikator (Basset, et al., 1991).
Penetapan Alkali total
Dua metode dapat digunakan untuk analisis ini. Dalam metode pertama, alkali total ditetapkan dengan titrasi dengan asam standar, dengan menggunakan jingga metil, jingga metil karmin indigo, atau biru bromofenol sebagai indicator. Dalam porsi larutan yang kedua, karbonat diendapkan dengan larutan barium klorida yang sedikit berlebih, dan tanpa menyaring, larutan titrasi dengan asam standar dengan menggunakan biru timol atau fenolftalein sebagai indikator. Titrasi terakhir ini memberi kandungan hidroksida, dan dengan mengurangkan ini dari titrasi pertama, diperoleh volume asam yang diperlukan untuk karbonat (Basset, et al., 1991).
BAB III
METODE PENGUJIAN
3.1 Pengambilan Sampel
1. Sampel di ambil dari kran air filter yang berasal dari sumur bor produksi PDAM Tritanadi Medan
2. Masukkan sampel ke dalam botol plastik. Isi penuh dan tutup rapat. 3. Analisis sampel dengan segera.
3.2 Alat
- Beaker glass 250 mL - Erlenmeyer 250 mL - Botol semprot - Gelas ukur 100 mL - Digital titrator - pH meter Sension 156
3.3 Bahan - Aquadest
- Brom Cresol Green - Methyl Red Powder Pillows - Buffer pH 4,01; 7,00; 10,01
3.4 Prosedur Kerja 3.4.1 Analisis pH
3.4.1.1 Kalibrasi pH meter
- Hubungkan Pottasium Chloride Electrolyte Gel Cartridge pada alat Platinum series pH
- Tekan dispenser pada elektroda sampai gelombang keluar. Bilas kelebihan gel yang keluar dari tip
- Hubungkan elektroda ke Sension 2 pH/ISE meter
- Hidupkan pH meter dengan menekan tombol power. Tekan pH mv hingga pada layar menampilkan pH
- Siapkan tiga buffer pH (buffer pH 4,01; 7,00; 10,01) di dalam beaker glass - Tekan tombol Cal, layarakan menampilkan standard 1
- Angkat elektroda dari storage salution bilas dengan aquadest dan keringkan dengan tissue
- Letakkan elektroda dalam buffer pH 10,01 tekan Read, layar akan menampilkan Stabilizing
- Apabila pembacaa telah stabil, layar akan menampilkan standard 2 - Angkat elektroda, bilas dengan aquadest dan keringkan dengan tissue - Letakkan elektroda ke dalam buffer pH 7,00 tekan Read, layar akan
menampilkan Stabilizing
- Letakkan elektroda ke dalam buffer pH 4,01 tekan Read, layar akan menampilkan Stabilizing
- Apabila pembacaan telah stabil, tekan Read untuk menyimpan hasil kalibrasi
- Apabila kalibrasi telah selesai, rendam elektroda di dalam beaker glass yang berisi aquadest selama 10 menit
- Angkat elektroda, tekan dispenser sampai fres Gel keluar dan bilas elektroda dengan aquadest lalu keringkan dengan tissue
3.4.1.2 Pengujian Sampel
- Siapkan sampel air yang akan diuji di dalam beaker glass - Masukkan elektroda ke dalam sampel air
- Tekan Read, layar akan menampilkan Stabilizing - Tunggu sampai pembacaan stabil
- Catat hasil analisa yang ditampilkan pada layar
3.4.2 Analisis Alkalinitas
- Tentukan volume sampel dan konsentrasi asam sulfat (sebagai pentiter) yang digunakan berdasarkan Tabel 3.1 di bawah ini.
Tabel 3.1 Penentuan Volume Sampel dan Konsentrasi Asam Sulfat
- Siapkan alat digital titrator dengan memasukkan tube pengeluaran ke dalam titrator cartridge, hubungkan cartridge ke titrator. Pegang digital titrator dengan ujung cartridge mengarah ke atas, tekan dan dorong tombol pengeluaran untuk mengeluarkan udara dan beberapa tetes titran, reset penghitung ke nol dan keringkan ujung tube dengan tissue.
- Sampel dari botol plastik di pindahkan ke dalam beaker gelas - Ambil sampel sebanyak 100 mL dengan menggunakan gelas ukur - Masukkan sampel tersebut ke dalam erlenmeyer
- Tambahkan satu kandungan indikator Phenolftalein Powder Pillow, aduk untuk mencampurkannya. Jika larutan berubah menjadi merah muda, titrasi dengan asam sulfat sampai tidak berwarna.
- Catat angka selama titrasi pertama (F). Hitung alkalinitas phenolftalein. Jika larutan tidak berubah warna setelah penambahan indikator, alkalinitas phenolftalein sama dengan 0.
- Tambahkan 1 kandungan indikator Brom Cresol Green - Methyl Red
Powder Pillows ke dalam larutan, kemudian aduk untuk
mencampurkannya.
- Lanjutkan titrasi dengan larutan asam sulfat sampai berubah warna dari hijau menjadi biru terang kehijauan (pada pH 5,1), warna abu-abu ungu terang (pH 4,8) atau warna merah muda terang (pH 4,5) sesuai dengan komposisi kandungan sampel (lihat Tabel 3.2).
- Hitung alkalinitas phenolftalein dan total alkalinitas berdasarkan perhitungan.
Tabel 3.2 Komposisi Kandungan Alkalintas Sampel Terhadap TAT Komposisi Kandungan Sampel Titik Akhir Titrasi
Alkalinitas kira-kira 30 mg/L Alkalinitas kira-kira 150 mg/L Alkalinitas kira-kira 500 mg/L
Silika dan phosphate Buangan industri atau sistem yang
kompleks
B = Angka yang dibutuhkan selama titrasi kedua
C = Normalitas asam sulfat yang digunakan dari sertifikat D = Normalitas asam sulfat yang digunakan dari tabel E = mg/L alkalinitas phenolftalein sebagai CaCO3
F = Angka yang dibutuhkan selam titrasi pertama Hubungan Alkalinitas
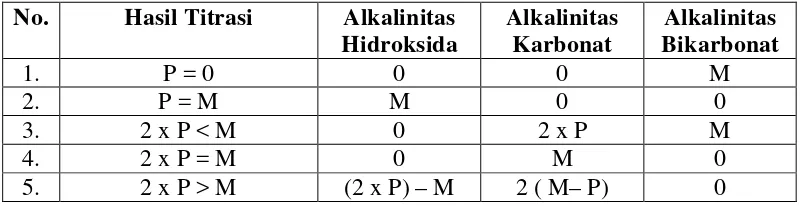
Tabel 3.3 Penentuan Konsentrasi Dari Alkalinitas
No. Hasil Titrasi Alkalinitas Hidroksida
Alkalinitas Karbonat
Alkalinitas Bikarbonat
1. P = 0 0 0 M
2. P = M M 0 0
3. 2 x P < M 0 2 x P M
4. 2 x P = M 0 M 0
5. 2 x P > M (2 x P) – M 2 ( M– P) 0
Keterangan:
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Berikut ini adalah tabel hasil uji nilai pH dan alkalinitas dari air filter HM. Yamin yang diuji pada tanggal 27 Februari 2013.
Tabel 4.1 Hasil Uji Nilai pH dan Alkalinitas Sampel Air
No Parameter Kadar Maks. U/ Air
**) Permenkes No. 492/Menkes/Per/IV/2010 tanggal 19 April 2010
4.2 Pembahasan
Pada hasil di atas dapat kita lihat bahwa nilai pH dan alkalinitas dari sampel air tersebut yaitu 7,20 dan 120 mg/L di mana ini masih memenuhi syarat mutu kualitas air minum yang ditetapkan oleh Permenkes No. 492/Menkes/Per/IV/2010 walaupun batas kadar maksimum untuk alkalinitas tidak ditetapkan, tetapi menurut Effendi (2003) nilai akalinitas yang baik berkisar antara 30-500 mg/L CaCO3.
menyebabkan beberapa senyawa kimia berubah menjadi racun yang menggangu kesehatan (Sutrisno dan Eni, 2010).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Nilai pH dan alkalinitas dari air filter HM. Yamin setelah dilakukan pengujian memberikan hasil yang memenuhi persyaratan mutu kualitas air minum sesuai dengan yang ditetapkan oleh Peraturan Menteri Kesehatan Republik Indonesia No. 492/MENKES/PER/IV/ 2010, sehingga air ini aman untuk dikonsumsi oleh masyarakat sebagai air minum.
5.2 Saran
DAFTAR PUSTAKA
Achmad, R. (2004). Kimia Lingkungan. Yogyakarta: Andi. Hal. 15, 22.
Anonim. (2012). Fungsi pH Meter. Available from: http:/www. Ilmubawang. blogspot. com/fungsi-pH-meter. html. Tanggal 28 Maret 2013.
Basset, J.C., Denny. R.C., Jeffrey, G.H., dan Mendham, J. (1991). Vogel’s Text book of Quantitave Inorganic Analysis Including Elementary Instrumental Analysis, diterjemahkan oleh Dr. A. Handayana Pudjaatmaka dan Ir.L. Setiono, Buku Ajar Vogel Kimia Analisis Kuantitatif Anorganik, 1994. Jakarta: Buku Kedokteran EGC. Halaman 261-263, 275, 359-360, 673-674, 687, 690-691.
Chandra, B. (2006). Pengantar Kesehatan Lingkungan. Jakarta: EGC. Hal. 39, 42, 45, 49-50, 55-56.
Effendi, H. (2003). Telaah Kualitas Air. Yogyakarta: Kanisius. Hal.11-12, 17-21, 95-100.
Ghufran, M., dan Andi B.T. (2007). Pengelolaan Kualitas Air dalam Budi Daya Perairan. Jakarta: Rineka Cipta. Hal. 47, 50.
Jokoa,T. (2010). Unit Air Baku dalam Sistem Penyediaan Air Minum. Yogyakarta: Graha Ilmu. Hal 9.
Jokob,T. (2010). Unit Produksi dalam Sistem Penyediaan Air Minum. Yogyakarta: Graha Ilmu. Hal 1-2, 8, 13.
Lesna. (2011). Potensiometri. Available from: http:/www. lesnacamay. blogspot.com/potensiometri. html. Tanggal 28 Maret 2013.
Linsley, R.K., dan Joseph B.F. (1979). Water Resources Engineering, 3rd edition, diterjemahkan oleh Ir. Djoko Sasongko M. Sc., Teknik Sumber Daya Air, 1991. Jakarta: Erlangga. Hal. 108.
Mulia, R.M. (2005). Kesehatan Lingkungan. Yogyakarta: Graha Ilmu. Hal. 39-40, 63.
Sunu, P. (2001). Melindungi Lingkungan Dengan Menerapkan ISO 14001. Jakarta: Gramedia. Hal.111.
Lampiran 2. Contoh Perhitungan
Analisa data untuk alkalinitas
Diperoleh: B = 122 ml D = 1,6 N C = 1,570 N
A = B x Angka Pengali x C/D = 122 x 1x 1,570/1,6 = 119,7 mg/L
= 120 mg/L Keterangan:
A = mg/L total alkalinitas sebagai CaCO3
B = Angka yang dibutuhkan selama titrasi kedua
Lampiran 1. Gambar Alat, Bahan, dan Pengujian
pH Meter Larutan Buffer
Kalibrasi pH Meter Pengujian pH Sampel
Persiapan Sampel untuk Alkalinitas Pereaksi Alkalinitas: Bromcresol Green-Methyl Red, Indikator PP, dan Asam Sulfat Cardtridge