PENENTUAN DOSIS LARUTAN KAPUR OPTIMUM
UNTUK MENETRALKAN pH AIR RESERVOIR
PDAM TIRTANADI SUNGGAL
TUGAS AKHIR
Oleh :
EVA SURYANTI 052410074
PROGRAM DIPLOMA III ANALIS FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN2008
LEMBAR PENGESAHAN
PENENTUAN DOSIS LARUTAN KAPUR OPTIMUM UNTUK
MENETRALKAN PH AIR RESERVOIR PDAM TIRTANADI
SUNGGAL
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Untuk Memperoleh Gelar Ahli Madya Pada Program Diploma III Analis Farmasi
Fakultas Farmasi Universitas Sumatera Utara
Oleh :
EVA SURYANTI 052410074
Medan, Mei 2008
Disetujui oleh: Dosen Pembimbing,
Drs. Agusmal Dalimunthe, MS,Apt. NIP 131 286 002
Disahkan Oleh: Dekan,
i
KATA PENGANTAR
Assalamua’laikum Wr. Wb.
Puji dan syukur penulis panjatkan kehadirat Allah SWT, Tuhan Semesta
Alam yang senantiasa melimpahkan rahmat dan karunia-Nya, serta shalawat
teriring salam dihadiahkan pada Baginda Rasulullah Muhammad SAW sehingga
penulis dapat menyelesaikan tugas akhir ini.
Dengan mengulurkan sepuluh jari seraya memohon ampun dan ucapan
terima kasih terbesar kepada ayahanda Sumadi dan ibunda Hanim Aryani yang
tercinta, yang telah membesarkan, mendidik, serta memberikan bimbingan dan
dukungan baik material maupun spiritual kepada penulis.
Penyusunan tugas akhir ini dilakukan berdasarkan pengamatan penulis
selama melaksanakan Praktek Kerja Lapangan (PKL) di PDAM Tirtanadi
Instalasi Pengolahan Air (IPA) Sunggal dengan judul “PENENTUAN DOSIS
LARUTAN KAPUR OPTIMUM UNTUK MENETRALKAN PH AIR
RESERVOIR PDAM TIRTANADI SUNGGAL”. Penyusunan tugas akhir ini
diajukan sebagai salah satu syarat untuk menyelesaikan pendidikan pada program
Diploma III Analis Farmasi di Fakultas Farmasi Universitas Sumatera Utara
Medan.
Dalam kesempatan ini dengan ketulusan, keikhlasan dan kerendahan hati
penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada :
1) Bapak Drs. Agusmal Dalimunthe ,MS,Apt., selaku Dosen Pembimbing
yang sudah sangat berperan dalam penyelesaian tugas akhir;
2) Bapak Prof. Dr. Jansen Silalahi M.App.Sc.Apt., selaku Koordinator
Program Diploma III Analis Farmasi, Fakultas Farmasi Universitas
Sumatera Utara;
3) Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara;
4) Ibu Poppy Anjelisa Z.Hsb.Ssi,Apt., selaku Dosen Wali selama mengikuti
kegiatan Akademik Program Diploma III Analis Farmasi, Fakultas
Farmasi Universitas Sumatera Utara;
5) Seluruh staf pengajar dan pegawai Fakultas Farmasi Universitas Sumatera
Utara yang telah turut membantu dalam penyelesaian tugas akhir ini;
6) Bapak Drs. Asan Sihaloho selaku Kepala Bagian Produksi Instalasi
Pengolahan Air PDAM TIRTANADI Sunggal yang sudah banyak
membantu dalam penulisan tugas akhir ini;
7) Bapak Iwan Setiawan selaku Kepala Bagian Pengendalian Mutu Instalasi
Pengolahan Air PDAM TIRTANADI Sunggal yang sudah banyak
memberikan bimbingan dalam penulisan tugas akhir ini.
8) Kak Asmidar selaku Analis Pengendalian Mutu Instalasi Pengolahan Air
PDAM TIRTANADI Sunggal yang sudah banyak membantu dalam
penulisan tugas akhir ini;
9) Adikku yang paling bijaksana, Ely Suhartini; terima kasih tak terhingga
iii
10)Adik-adikku yang paling aku sayangi; Eko dan Ningsih, terima kasih atas
semangat yang kalian berikan, bersama kalian hidup kakak menjadi lebih
berarti;
11)Sahabat-sahabat terbaikku Ira, Mimi, Ega, Putri, Dila, Irfan, Tedy, Diki,
Ijal, Jaya, Desi, Ika, Herna, kak Sherly, yang selalu memberikan perhatian,
doa, dan dukungan serta kebersamaan dalam penyelesaian tugas akhir ini;
12)Seluruh rekan mahasiswa Program Diploma III Analis Farmasi dan semua
pihak yang sudah membantu dalam penyelesaian tugas akhir ini yang tidak
dapat disebutkan satu persatu.
Penulis menyadari tugas akhir ini masih jauh dari kesempurnaan, untuk itu
penulis dengan senang hati akan menerima segala bentuk saran dan kritik yang
membangun demi kesempurnaan tugas akhir ini.
Akhir kata, penulis berharap semoga tugas akhir ini dapat bermanfaat bagi
siapapun yang membacanya.
Wassalamua’alaikum Wr. Wb.
Medan, Mei 2008
Penulis
DAFTAR ISI
KATA PENGANTAR ... i
DAFTAR PUSTAKA ... iv
DAFTAR TABEL ... vi
DAFTAR GRAFIK ... vii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan dan Manfaat ... 2
1.2.1. Tujuan ... 2
1.2.1. Manfaat ... 2
BAB II TINJAUAN PUSTAKA ... 3
2.1 Air ... 3
2.2.1. Sumber Air ... 6
2.2.2. Syarat-Syarat Air Minum ... 9
2.2 Proses Pengolahan Air secara Umum ... 12
2.2.1. Proses Purifikasi ... 13
2.2.2. Proses Desinfeksi ... 14
2.2.3. Proses Pengaturan pH Air ... 15
2.3. Kapur ... 16
BAB III METODOLOGI PERCOBAAN ... 18
v
3.1.1. Alat ... 18
3.1.2. Bahan ... 18
3.2 Prosedur Kerja ... 19
3.2.1 Pembuatan Larutan Kapur Jenuh ... 19
3.2.2. Persiapan Penginjeksian ... 19
3.2.3. Pemeriksaan pH ... 20
BAB IV HASIL DAN PEMBAHASAN ... 21
4.1 Hasil ... 21
4.2 Pembahasan ... 22
BAB V KESIMPULAN DAN SARAN ... 23
5.1 Kesimpulan ... 23
5.2 Saran ... 24
DAFTAR PUSTAKA
DAFTAR TABEL
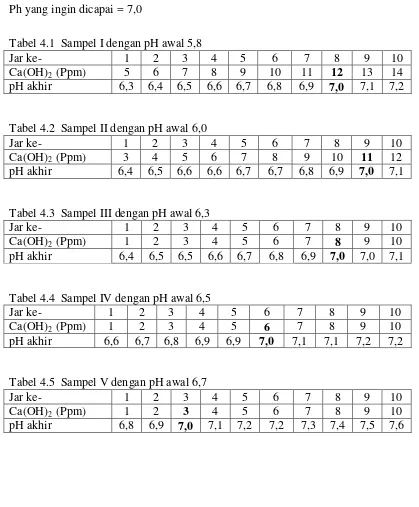
Table 4.1 Sampel I dengan pH awal 5.8
Table 4.2 Sampel II dengan pH awal 6.0
Table 4.3 Sampel III dengan pH awal 6.3
Table 4.4 Sampel IV dengan pH awal 6.5
vii
DAFTAR GRAFIK
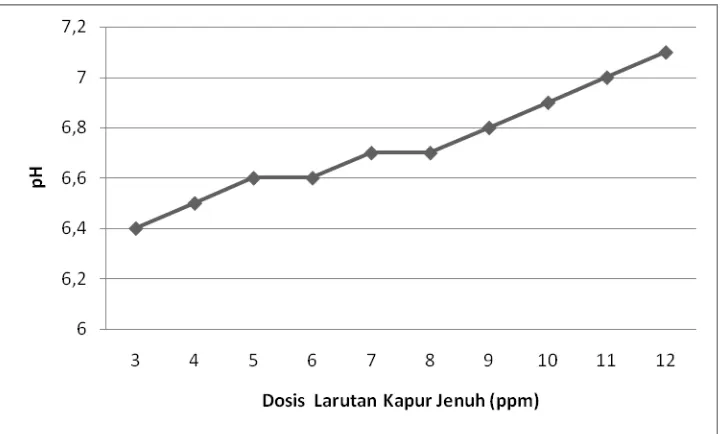
Grafik 4.1 untuk Sampel I dengan pH awal 5.8
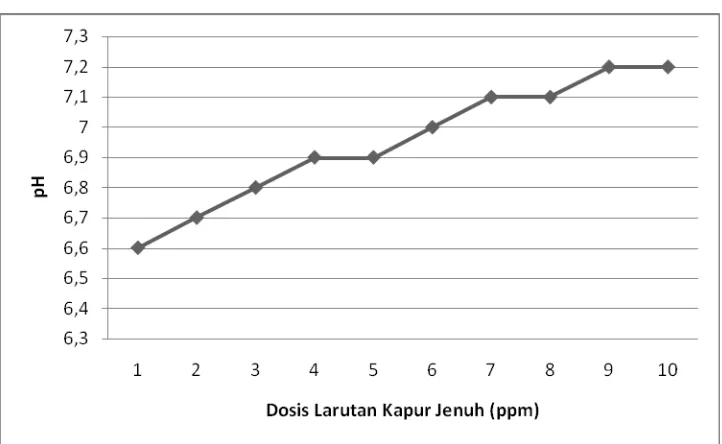
Grafik 4.2 untuk Sampel II dengan pH awal 6.0
Grafik 4.3 untuk Sampel III dengan pH awal 6.3
Grafik 4.4 untuk Sampel IV dengan pH awal 6.4
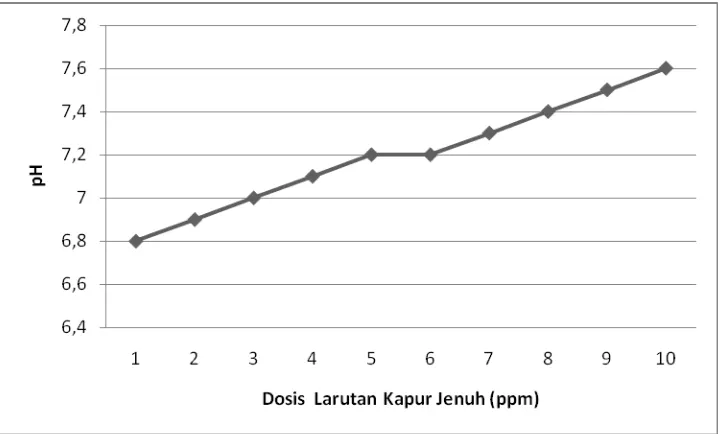
Grafik 4.5 untuk Sampel V dengan pH awal 6.7
Grafik Linearitas Ph versus Dosis Optimum Ca(OH)2 (Ppm)
BAB I
PENDAHULUAN
1.1. Latar Belakang
Air merupakan sumber daya yang paling fundamental yang dimiliki
manusia. Air merupakan zat kehidupan manusia, dimana tidak satu pun makhluk
hidup di planet bumi ini yang tidak membutuhkan air. Hasil penelitian
menunjukkan bahwa 65-75 % dari berat badan manusia dewasa terdiri dari air.
Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan
masyarakat, karena air merupakan salah satu media dari berbagai macam
penularan. Melalui penyediaan air bersih disuatu daerah, maka penyebaran
penyakit menular diharapkan bisa ditekan seminimal mungkin.
Peningkatan kualitas air minum dapat dilakukan dengan jalan mengadakan
pengolahan terhadap air yang akan diperlukan sebagai air minum dengan mutlak
diperlukan terutama apabila air tersebut berasal dari permukaan. Pengolahan yang
dimaksud bisa dimulai dari yang sangat sederhana sampai yang pada pengolahan
yang mahir/lengkap, sesuai dengan tingkat kekotoran dari sumber asal air
tersebut. Oleh karena itu, dalam praktek sehari-hari maka pengolahan air menjadi
pertimbangan yang utama untuk menentukan apakah sumber tersebut bisa dipakai
sebagai sebagai sumber persediaan atau tidak. Salah satu proses pengolahan yang
bisa diterapkan untuk mengolah air sungai menjadi air bersih yang berkualitas
baik adalah proses netralisasi pH. Proses ini merupakan proses akhir dalam
2
peran suatu bahan kimia, yang biasa dipakai adalah kapur (Ca(OH)2).
Penambahan bahan kimia ini dilakukan pada bak reservoir melalui pengendapan
terdahulu pada bak dan saturator yang bertujuan untuk mengurangi
partikel-partikel yang dapat menyebabkan kekeruhan. Penambahan larutan kapur ini
dimaksudkan untuk menetralisasi pH air karena dengan adanya kandungan
alum(tawas) dalam air yang berasal dari bak clearator akan membuat pH air
bersifat asam.
1.2. Tujuan dan Manfaat
1.2.1. Tujuan
Adapun tujuan tugas akhir ini adalah untuk menentukan dosis larutan
kapur (Ca(OH)2) optimium yang dibutuhkan untuk menetralkan pH air reservoir
PDAM Tirtanadi Sunggal.
1.2.2. Manfaat
Adapun manfaat tugas akhir ini adalah agar dapat memperkirakan berapa
dosis larutan kapur (Ca(OH)2 yang optimum untuk menetralkan pH air reservoir
PDAM Tirtanadi Sunggal.
BAB II
TINJAUAN PUSTAKA
2.1. Air
Air adalah materi esensial di dalam kehidupan. Tidak ada satu pun
makhluk hidup yang berada di planet bumi ini yang tidak membutuhkan air. Di
dalam sel hidup, baik pada tumbuh-tumbuhan ataupun pada hewan (termasuk di
dalamnya manusia) akan terkandung sejumlah air, yaitu lebih dari 75 %
kandungan sel tumbuh-tumbuhan atau lebih dari 67 % kandungan sel hewan,
terdiri dari air. Jika kandungan tersebut berkurang, misalnya dehidrasi pada
manusia yang diakibatkan muntaber, kalau tidak cepat ditanggulangi akan
mengakibatkan kematian. Tanaman yang lupa tidak disiram pun akan layu dan
kalau dibiarkan akan mati.
Secara tidak langsung yang menjadi penyebab krisis air terutama karena
terjadi penggundulan hutan, penurunan kawasan resapan air, dan pencemaran.
Yang paling mengerikan adalah akibat pencemaran. Air merupakan substrat yang
paling parah akibat pencemaran. Berbagai jenis pencemar yang banyak memasuki
badan air, berasal dari:
- Sumber domestik (rumah tangga, perkampungan, kota, pasar, jalan) dan
sebagainya;
- Sumber nondomestik (pabrik, industri, pertanian, peternakan, perikanan
serta sumber-sumber lainnya).
Secara langsung ataupun tidak langsung pencemar tersebut akan
4
ataupun keperluan lainnya. Kekeruhan air yang dapat ditimbulkan oleh adanya
bahan organik dan anorganik, seperti lumpur dan buangan dari pemukiman
tertentu yang menyebabkan air sungai menjadi keruh.
Warna air berubah bergantung kepada buangan yang memasuki badan air.
Sedangkan dari sifat pengendapannya, yang dapat menyebabkan kekeruhan
berasal dari bahan-bahan yang mudah diendapkan dan bahan-bahan yang sukar
diendapakan. Berbagai cara dan usaha telah banyak dilakukan agar kehadiran
pencemaran terhadap air dapat dihindari, dikurangi, atau minimal dapat
dikendalikan.
Air yang mengandung kekeruhan tinggi akan mengalami kesulitan kalau
diproses untuk sumber air bersih. Kesulitannya antara lain dalam proses
penyaringan. Kalaupun proses penyaringan dapat dilakukan akan memerlukan
biaya yang lebih besar dan mungkin pula mahal ( Suriawiria, 2004 ).
Menurut Abdullah (1989), air dapat dibagi atas beberapa kriteria yaitu
golongan A, B, C, dan D.
- Golongan A; yaitu air yang dapat digunakan sebagai air minum secara
langsung tanpa pengolahan terlebih dahulu;
- Golongan B; yaitu air yang dapat dipergunakan sebagai air baku untuk diolah
sebagai air minum dan keperluan rumah tangga;
- Golongan C; yaitu air yang dapat dipergunakan untuk keperluan perikanan
dan peternakan;
- Golongan D; yaitu air yang dapat dipergunakan untuk keperluan pertanian dan
dapat dimanfaatkan untuk usaha perkotaan, industri, listrik tenaga air.
Selain itu menurut Gabriel juga ada tiga penyebab utama tercemarnya
suatu perairan:
- Peningkatan konsumsi atau penggunaan air sehubungan dengan peningkatan
ekonomi dan taraf hidup masyarakat;
- Terjadinya perpindahan dan pertambahan penduduk di sekitar daerah industri;
- Kurangnya kesadaran sosial dan rendahnya pendapatan untuk memperbaiki
lingkungan hidup.
Air sering juga disebut sebagai pelarut universal karena mempunyai sifat
yang dapat melarutkan banyak zat kimia. Dalam bentuk ion, air dapat
dideskripsikan sebagai sebuah ion hydrogen (H+
Secara umum kegunaan air di dalam tubuh dan kehidupan manusia adalah
untuk proses metabolisme mengangkat zat-zat makanan dalam tubuh mengatur
keseimbangan suhu tubuh dan menjaga jangan sampai tubuh kekeringan oleh
kandungan air (dehidrasi). Oleh karena itu penyediaan air bersih salah satu
tuntutan umum bagi manusia untuk kelangsungan hidupnya dan penentu dalam
kesehatan dan kesejahteraan manusia ( Sutrisno, 2004 ).
) yang berikatan dengan sebuah
ion hidroksida.
2.1.1. Sumber Air
Pada prinsipnya, jumlah air di alam ini tetap dan mengikuti suatu aliran
yang dinamakan “ Cyclus Hydrology”. Dengan adanya penyinaran matahari,
maka semua air yang ada di permukaan bumi akan menguap dan membentuk uap
air. Karena adanya angin, maka uap air ini akan bersatu dan berada di tempat yang
6
lama makin tinggi dimana temperatur semakin rendah, dan akan membentuk
titik-titik air dan akan jatuh ke bumi sebagai hujan. Air hujan ini sebagian mengalir
kedalam tanah, jika menjumpai lapisan rapat, peresapan air akan berkurang, dan
sebagian akan mengalir diatas lapisan rapat tersebut. Jika air ini keluar ke
permukaan bumi, maka air ini akan disebut mata air.
Air yang mengalir di atas permukaan bumi umumnya berbentuk
sungai-sungai dan jika melalui suatu tempat rendah (cekung) maka air akan berkumpul
dan membentuk suatu danau atau telaga. Tetapi banyak diantaranya yang
mengalir ke laut kembali dan kemudian akan mengikuti siklus hidrologi ini
(Sutrisno, 2004).
Menurut Gabriel ( 2001 ), secara garis besar dapat dikatakan air bersumber
dari:
1. Laut; air laut
2. Darat; air tanah
3. Udara; air hujan
1. Air Laut
Air yang dijumpai di dalam alam berupa air laut sebanyak 80%, sedangkan
sisanya berupa air tanah/daratan, es, salju dan hujan.
Menurut Sutrisno (2004), air laut mempunyai sifat asin karena
mengandung garam NaCl. Kadar garam NaCl dalam air laut 3%. Dengan keadaan
ini maka air laut tidak memenuhi syarat untuk air minum.
2. Air tanah
Air tanah disebut pula air tawar oleh karena tidak terasa asin. Berdasarkan
lokasi air maka air tanah dibagi dalam dua bagian yaitu:
1. Air permukaan tanah
2. Air jauh dari permukaan tanah.
2.1. Air permukaan tanah
Termasuk air permukaan tanah antara lain sungai, rawa-rawa, danau,
waduk (danau buatan). Kesemuanya itu sangat tergantung curah hujan. Apabila
curah hujan lebat, maka air sungai, danau akan pasang.
Menurut Sutrisno ( 2004), air permukaan tanah terjadi karena daya proses
peresapan air dari permukaan tanah. Lumpur akan tertahan, demikian pula dengan
sebagian bakteri, sehingga air tanah akan jernih.
2.2. Air jauh dari permukaan tanah
Disebut juga air tertekan yaitu air yang tersimpan didalam lapisan tanah.
Menurut Sutrisno (2004), air ini terdapat setelah lapisan rapat air yang pertama.
Pengambilan air tanah dalam ini tidak semudah pada air tanah dangkal. Dalam hal
ini harus menggunakan bor dan memasukkan pipa ke dalamnya, sehingga dalam
suatu kedalaman tertentu akan didapat suatu lapisan air.
Jika tekanan air tanah air ini besar, maka air ini akan dapat menyembur
keluar dan dalam keadaan ini sumur ini disebut dengan artesis. Jika air tidak dapat
keluar dengan sendirinya, maka digunakan pompa untuk membantu pengeluaran
8
3. Air hujan
Adalah air yang mengalir di permukaan bumi. Pada umumnya air hujan
ini akan mendapat pengotoran selama pengalirannya misalnya oleh lumpur,
batang-batang kayu, daun-daun, kotoran industri kota dan sebagainya. Setelah
mengalami suatu pengotoran, pada suatu saat air hujan itu akan mengalami suatu
proses pembersihan sendiri dengan cara udara yang mengandung oksigen atau gas
O2 akan membantu mengalami proses pembusukan yang terjadi pada air
permukaan yang telah mengalami pengotoran, karena selama dalam perjalanan,
O2
2.1.2. Syarat-Syarat Air Minum
akan meresap ke dalam air hujan.
Menurut Sutrisno (2004), unsur-unsur yang dianalisa dalam penentuan air
disebut parameter kualitas air, yakni sifat-sifat fisis, kimia dan biologis. Parameter
dari kualitas air antara lain:
1. Persyaratan fisis
Dalam standar persyaratan fisis air minum tampak adannya lima unsur
persyaratan meliputi; suhu, warna, bau, rasa , dan kekeruhan.
1.1. Suhu
Temperatur dari air akan mempengaruhi penerimaan masyarakat akan air
tersebut dan dapat pula mempengaruhi reaksi kimia dalam pengolahan, terutama
apabila temperatur tersebut sangat tinggi. Temperatur yang diinginkan adalah
100C sampai 150, tetapi iklim setempat, kedalaman pipa-pipa saluran air, dan jenis
dari sumber-sumber air akan mempengaruhi temperatur ini.
1.2. Warna
Banyak air permukaan khususnya yang berasal dari daerah rawa-rawa,
sering kali berwarna sehingga tidak dapat diterima masyarakat baik untuk
keperluan rumah tangga maupun untuk keperluan industri, tanpa dilakukannya
pengolahan untuk menghilangkan warna tersebut. Bahan-bahan yang
menimbulkan warna tersebut dihasilkan dari kontak antara air dengan reruntuhan
organis seperti daun, duri pohon jarum, dan kayu yang semuanya dalam berbagai
tingkat pembusukan. Air yang mengandung bahan-bahan pewarna alamiah yang
berasal dari rawa dan hutan dianggap tidak mempunyai sifat-sifat yang
membahayakan atau toksis.
1.3. Bau dan Rasa
Adanya bau dan rasa pada air minum akan mengurangi penerimaan
masyarakat terhadap air tersebut. Bau dan rasa biasanya terjadi bersama-sama dan
biasanya disebabkan oleh adanya bahan-bahan organik yang membusuk, tipe-tipe
tetentu organisme mikroskopik, serta persenyawan-persenyawaan kimia seperti
fenol. Bahan-bahan yang menyebabkan bau dan rasa ini berasal dari berbagai
sumber. Intensitas bau dan rasa dapat meningkat, bila terhadap air dilakukan
klorinasi. Standart persyaratan air minum yang menyangkut bau dan rasa ini baik
yang ditetapkan oleh WHO maupun U.S. Public Health Service menyatakan
bahwa dalam air minum tidak boleh terdapat bau dan rasa yang tidak diinginkan.
1.4. Kekeruhan
Air dikatakan keruh apabila air tersebut mengandung begitu banyak
10
berlumpur dan kotor. Bahan-bahan yang menyebabkan kekeruhan ini meliputi:
tanah liat, lumpur, bahan-bahan organik yang tersebar, dan partikel-partikel kecil
yang tersuspensi lainnnya. Kebanyakan bangunan pengolahan air yang modern
menghasilkan air dengan kekeruhan 1 ppm atau kurang. Menurut Clair N
Sawyear, dkk; dikatakan bahwa kekeruhan pada air merupakan satu hal yang
harus dipertimbangkan dalam penyediaan air bagi umum, mengingat bahwa
kekeruhan tersebut akan mengurangi segi estetika, menyulitkan dalam usaha
penyaringan dan akan mengurangi efektifitas usaha desinfeksi.
2. Persyaratan Kimia
Air minum tidak boleh mengandung racun, zat-zat mineral atau zat-zat
kimia tertentu dalam jumlah melampaui batas yang telah ditentukan.
Dalam Peraturan Mentri Kesehatan RI No.907/MENKES/SK/VII/ 2002
tercantum sebanyak 29 macam standart. Unsur-unsur tersebut tidak dikehendaki
kehadirannya dikarenakan zat kimia yang bersifat racun dapat merusak perpipaan
ataupun karena sebagai penyebab bau/rasa yang akan menganggu estetika.
Nikel mg/L 0.02 0.02
3. Persyaratan Biologis
Air minum tidak boleh mengandung bakteri-bakteri penyakit ( pathogen )
sama sekali dan tidak boleh mengandung bakteri-bakteri golongan Coli. Sekalipun
sebaliknya mikroorganisme nonpathogen secara relative tidak berbahaya bagi
kepentingan kesehatan, namun karena golongan ini sering dalam jumlah
berlebihan dapat mempengaruhi rasa, bau esthetis dan lain-lain, timbale balik
justru dapat berakibat menyulitkan pengolahan air.
2.2. Proses Pengolahan Air Secara Umum
Pengolahan air merupakan terjemahan dari bahasa Inggris “ Water
Treatment” yaitu suatu usaha menjernikan air dan meningkatkan mutu air agar
dapat diminum. Pengolahan disebut juga usaha-usaha teknis yang dilakukan untuk
mengubah sifat-sifat suatu zat. Hal ini penting artinya bagi air minum, karena
dengan adanya pengolahan ini, maka akan didapatkan suatu air minum yang
12
Menurut Gabriel (2001), proses pengolahan air meliputi empat tahap,
yaitu:
1. Proses purifikasi (penjernihan) air
2. Proses desinfeksi
3. Proses pengaturan pH air
4. Proses pengaturan mineral air.
2.2.1 Proses purifikasi (penjernihan) air
Pemurnian air atau disebut juga water purification yaitu suatu proses
merubah keadaan air dari keruh, berbau dan berwarna, pH beraneka menjadi air
yang jernih, bebas dari keruh, bau dan warna serta pH-nya netral.
Menurut Gabriel (2001), untuk mengatasi kekeruhan dapat dilakukan
dengan berbagai cara, antara lain:
2.2.1.1. Pengendapan secara alami (sedimentasi)
Dengan cara membiarkan air yang mengandung Lumpur kasar maupun
halus akan perlahan-lahan mengendap. Proses ini memerlukan waktu 1-6 jam,
sedangkan air yang mengandung koloidal tidak mungkin terjadi pengendapan
secara alami.
Pengendapan partikel-partikel padat dari air sungai terjadi dengan gaya
gravitasi. Untuk menjaga efektivitas ruang pengendapan dan pencegahan
pembusukan lumpur endapan, maka secara periodik lumpur endapan harus kita
keluarkan (Sutrisno,2004).
2.2.1.2. Melalui proses koagulasi
Proses ini menyangkut pembentukan flok yang mengadsorbsi dan
mengikat partikel koloid dalam air sehingga membentuk flok yang lebih besar
agar mudah diendapkan dan disaring. Koagulasi dapat dilakukan dengan
penambahan bahan kimia atau sering disebut koagulan. Koagulan yang umum
digunakan adalah aluminium sulfat ( Al2(SO4)3.18H2
2.2.1.3. Proses sedimentasi aktif
O ) yang juga dikenal
dengan nama tawas. Bahan ini paling banyak dipergunakan karena relative murah
dan mudah didapat di pasaran ( Suriawiria, 2004 ).
Apabila sudah menggunakan koagulan, maka koloidal-koloidal yang ada
dalam air akan mengalami flokulasi dan dengan sendirinya akan membentuk
endapan dalam waktu 1-4 jam berikutnya. Untuk mempercepat terjadinya
sedimentasi perlu dilakukan sentrifuge.
2.2.1.4. Melalui proses filtrasi
Koloidal yang telah mengalami flokulasi namun tidak terjadi pengendapan
maka usaha selanjutnya melalui proses filtrasi. Ada dua macam filtrasi yaitu
saringan pasir cepat ( rapid sand filter) dan saringan pasir lambat (slow sand
filter). Keuntugan rapid sand filter adalah kemampuan menyaring 5- 10
m3/m2/jam, makin luas permukaan makin besar volume air yang tersaring,
berbeda halnya dengan slow rapid sand yang hanya memiliki kemampuan
menyaring sekitar 0,1-0,2 m3/m2/jam, dibutuhkan bak yang sangat besar untuk
meningkatkan volume penyaringan.
Sedangkan kejelekan dari rapid sand filter adalah perl pretreatment
(pengolahan air terdahulu misalnya proses sedimen atau proses koagulasi terlebih
dahulu) dan banyak bakteri turut melewati filter, berbeda halnya dengan slow
sand filter, tidak perlu dilakukan ptertreatmen oleh karena banyak bakteri akan
14
2.2.2. Proses Desinfeksi
Lebih dari 50 persen patogen di dalalm air akan mati dalam waktu 2 hari
dan 90 persen akan mati pada akhir 1 minggu. Oleh karena itu, waduk- waduk
penampun sebenarnya cukup efektif untuk mengendalikan bakteri. Walaupun
demikian, beberapa jenis patogen mungkin tetap hidup selama 2 tahun atau lebih,
karena itu dibutuhkan desinfeksi, yaitu suatu proses agar kuman patogen yang
berada dalam air dapat di musnahkan. Klorin telah terbukti merupakan
desinfektan yang ideal. Bila dimasukkan dalam air akan meempunyai pengaruh
yang segera dan membinasakan kebanyakan makhluk mikroskopis (Linsey, 1991).
2.2.3. Proses Pengaturan pH Air
PH adalah merupakan istilah yang digunakan untuk menyatakan intensitas
keadaan asam atau basa suatu larutan. Dalam penyediaan air, ph merupakan satu
faktor yan harus dipertimbangkan mengingat bahwa derajat keasaaman dari air
akan sangat mempengaruhi aktivitas pengolahan yang akan dilakukan, misalnya
dalam melakukan koagulasi kimia, desinfeksi. Pengaruh yang menyangkut aspek
kesehatan dari penyimpangan standar kualitas air minum dalam hal pH ini adalah
Ph air normal berkisar 6,5 – 9,2 ( Sutrisno, 2004 ).
Pembatasan pH dilakukan karena akan mempengaruhi rasa, korosifitas air
dan efisiensi klorinasi. Beberapa senyawa asam dan basa lebih toksid dalam
bentuk molekuler, dimana disosiasi senyawa-senyawa tersebut dipengaruhi oleh
pH ( Hanum, 2002 ).
Apabila pH kurang dari 6,5 atau lebih besar dari 9,2 akan mengakibatkan
pipa air yang terbuat dari logam mengalami korosi pada pipa-pipa air sehingga
pada akhirnya air tersebut akan menjadi racun bagi tubuh manusia. Dalam
penjernihan, dimana tawas merupakan pilihan utama (oleh karena ekonomis),
namun dalam hal pembentukan flok cendrung bersifat asam.
2.3. Kapur ( Adjusment pH )
Kapur merupakan bahan kimia yang paling dikenal dan digunakan untuk
penetapah pH. Kebanyakan tersedia di pasaran dalama bentuk Ca(OH)2
Penambahan larutan kapur bertujuan untuk menetralisasi pH. Karena
dengan adanya kandungan alum ( tawas) dalam air akan membuat pH air bersifat
asam. Penambahan larutan kapur ini dilakukan pada bak reservoir sebelum air
siap untuk didistribusikan, sedangkan pengendapan larutan kapur dilakukan di bak
dan saturator, keseluruhan proses ini mengandalkan proses gravitasi agar getaran
dan riak dapat diminimalisir. Saturator adalah sebuah tabung besar yang
merupakan terminal larutan kapur untuk diinjeksikan ke air hasil olahan. Air
kapur dari saturator ini juga masih membwa partikel kapur yang luput
mengendap, walupun demikian reservoir dapat juga berperan sebagai bak
pengendap akhir dari air hasil proses ( Buletin Titrtanadi No.4, 2006 ).
, biasanya
tersedia dalam bentuk gumpalan, serbuk atau tepung. Karena pada umumnya
kapur tersedia dengan mudah, harganya lebih relatif murah, dan mudah untuk
digunakan. Walaupun demikian sistem pemakain kapur dapat menimbulkan
masalah dalam pemeliharaan jika operasinya tidak memadai.
Penambahan larutan kapur ke dalam air hasil olahan untuk mengatasi
keasaman air. Di laboratorium, dosis larutan kapur yang dibutuhkan dapat
16
dibutuhkan untuk menetralkan pH air tergantung pada mutu kimiawi air. Dalam
air larutan kapur akan menghasilkan reaksi sebagai berikut :
Al2(SO4)3 2Al+++ + 3 SO4
Ion Aluminium (Al
=
+++
H
) berasal dari proses koagulasi (tawas);
2O H+ + OH
Ion Hidroksida (OH
-) kemudian bereaksi dengan ion aluminium (Al+++
2Al
)
+++
+ OH- 2Al(OH)3
Terbentuknya endapan (flok) dan dihasilkan asam yang berasal dari ion H
+
Untuk menetralkan ditambahkan larutan kapur ( Ca(OH)
) berasal dari larutan kapur bereaksi dengan ion H+
H
+
+ 2OH- H2O
Semakin banyak jumlah alum(tawas) yang ditambahkan dalam air maka
akan meningkatkan keasaman air, dan hal ini meyebabkan Ph semakin turun.
semakin tinggi tingkat keasaman air maka semakain besar dosis larutan kapur
yang dibutuhkan untuk menetralkan air hasil olahan.
Dengan demikian, perlu dicari dosis larutan kapur yang optimum
untuk menetralkan air hasil olahan agar berada dalam range pH 6,8 – 8,5 yang
merupakan standart pH di reservoir 6,5 – 8,5 (Keputusan Mentri Kesehatan RI
No.907/MENKES/SK/VII/ 2002.
BAB III
METODOLOGI PERCOBAAN
3.1. Alat dan Bahan
3.1.1. Alat-alat
Alat-alat yang digunakan dalam percobaan ini adalah:
1. Jar Test
2. Timbangan analitik
3. 10 Beaker glass 1000 ml
4. Gelas ukur 20 ml
5. Pipet volum 10 ml
6. Comparator pH
3.1.2. Bahan-bahan
Bahan-bahan yang dipakai dalam percobaan ini adalah:
1. Kapur
2. Air Reservoir PDAM Tirtanadi Sunggal
3. Aquadest
18
3.2. Prosedur Kerja
3.2.1. Pembuatan Larutan Kapur jenuh
Prosedur:
1. Ditimbang 2,5 gr kapur,
2. Dilarutkan dalam 1000 ml Aquadest dalam beaker glass,
3. Dilakukan pengadukan cepat dengan menggunakan Jar Test, diatur pada
putaran 140 rpm selama 20 menit,
4. Didiamkan selama 2 jam,
5. Diperiksa dan dicatat pH larutan kapur jenuh.
3.2.2. Persiapan Penginjeksian
Prosedur:
1. Diisi masing-masing 10 beaker glas 1000 ml dengan 1000 ml sampel air
reservoir,
2. Lalu diinjeksikan masing-masing beaker glas dengan variasi dosis larutan
kapur jenuh yang diinginkan berdasar hasil perhitungan :
3. Dilakukan pengadukan cepat dengan menggunakan Jar Test, diatur
putaran 140 rpm selama 5 menit,
4. Didiamkan selama 10 menit
5. Diperiksa dan dicatat pH sampel.
3.2.3. Pemeriksaan pH
1. Diisi kuvet dengan air sampel ± 10 ml.
2. Ditambahkan 3 tetes indikator Brom Thymol Blue.
3. Ditempatkan kuvet sampel di sebelah kanan pada tempat kuvet
comparator.
4. Ditempatkan kuvet blanko sebelah kiri pada tempat kuvet comparator.
5. Dibandingkan warna sampel dengan standart pada comparator.
i. Jika warna sampel sama atau mendekati maka nilai pH baca pada
disk comparator. Keterangan
ii. Jika warna sampel tidak sama dengan warna pada disk comparator,
maka dilihat nilai tengah median.
6. Dicatat hasil pengukuran yang diperoleh.
Standart pH di reservoir 6,5 – 8,5 (Keputusan Mentri Kesehatan RI
20
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil
Berdasarkan percobaan yang telah dilakukan diperoleh hasil
Ph yang ingin dicapai = 7,0
Tabel 4.3 Sampel III dengan pH awal 6,3
Grafik 4.1 Sampel I dengan pH awal 5,8
22
Grafik 4.3 Sampel III dengan pH awal 6,3
Grafik 4.4 Sampel IV dengan pH awal 6,5
Grafik 4.5 Sampel V dengan pH awal 6,7
Tabel pH awal versus Dosis Optimum Ca(OH)2 pH Awal
(Ppm)
5,8 6,0 6,3 6,5 6,7 Dosis Optimum Ca(OH)2 (Ppm) 3 6 8 11 12
24
4.2. Pembahasan
Berdasarkan data dan hasil percobaan di atas, diperoleh dosis larutan kapur
yang optimum untuk menetralkan pH air. Selain itu, hal ini juga menunjukkan
hubungan yang searah, yaitu semakin tingginya tingkat keasaman air maka
semakin besar dosis larutan kapur yang dibutuhkan untuk mengatasi keasaman
dan membuat pH air berada dalam range yang distandarkan yaitu pH 6,8 – 8,5.
Penambahan larutan kapur Ca(OH)2 ke dalam air olahan dimaksudkan
untuk mencapai suatu titik, dengan kata lain membuat pH air konstan, tidak turun
lagi, titik tersebut titik optimum. Titik optimum dicapai ketika larutan kapur
Ca(OH)2 ditambahkan dengan dosis tertentu bekerja semaksimal mungkin untuk
bereaksi dengan ion H+
Dengan demikian, dosis larutan kapur Ca(OH)
yang berasal dari proses koagulasi air olahan yang
merupakan penyebab keasaman. Ketika titik optimum dicapai maka pH air olahan
akan semakin meningkat sepeti terlihat pada table di atas.
2
- Sampel I dengan pH awal 5,8 dibutuhkan dosis Ca(OH)
optimum yang
dibutuhkan untuk menetralkan air reservoir pada masing-masing sampel seperti
terlampir pada table di atas adalah sebagai berikut :
2
- Sampel II dengan pH awal 6,0 dibutuhkan dosis Ca(OH)
sebesar 12 ppm
2
- Sampel III dengan pH awal 6,3 dibutuhkan dosis Ca(OH)
sebesar 11 ppm
2
- Sampel IV dengan pH awal 6,5 dibutuhkan dosis Ca(OH)
sebesar 8 ppm
2
- Sampel V dengan pH awal 6,7 dibutuhkan dosis Ca(OH)
sebesar 6 ppm
2 sebesar 3 ppm
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil dan pembahasan percobaan yang telah dilakukan dapat diambil
kesimpulan sebagai berikut :
- Bahan kimia yang sering digunakan untuk menetralkan pH air olahan adalah
kapur ( Ca(OH)2
- Penentuan dosis larutan kapur (Ca(OH) )
2
- Diperoleh hubungan yang searah antara tingkat keasaman air dengan dosis
larutan kapur, yaitu semakin tinggi tingkat keasaman air maka semakin besar
pula dosis larutan kapur yang dibutuhkan untuk mengatasi keasaman dan
membuat pH air berada dalam range yang distandarkan yaitu pH 6,8 – 8,5 ) optimum untuk menetralkan pH air
dapat dilakukan dengan menggunakan metode jar-test
- Dosis optimum ( Ca(OH)2
- Sampel I dengan pH awal 5,8 dibutuhkan dosis Ca(OH)
) yang dibutuhkan untuk menetralkan air reservoir
dengan tingkat keasaman yang berbeda dapat diperkirakan adalah sebagai
berikut:
2
- Sampel II dengan pH awal 6,0 dibutuhkan dosis Ca(OH)
sebesar 12 ppm
2
- Sampel III dengan pH awal 6,3 dibutuhkan dosis Ca(OH)
sebesar 11 ppm
2
- Sampel IV dengan pH awal 6,5 dibutuhkan dosis Ca(OH)
sebesar 8 ppm
2
- Sampel V dengan pH awal 6,7 dibutuhkan dosis Ca(OH)
sebesar 6 ppm
26
5.2. Saran
Sebaiknya penginjeksian larutan kapur (Ca(OH)2
) dilakukan sebelum air
olahan sampai ke reservoir untuk lebih menimalisir tingkat kekeruhan dan
memperkecil terjadinya korosi pada pipa-pipa distribusi.
DAFTAR PUSTAKA
Abdullah, Chaenulfifah. (1989). LAPORAN PENELITIAN EVALUASI
KUALITAS KIMIA DAN BIOLOGI DI SEKITAR PT. INDAH KILAT
PULP PERAWANG RIAU. Pekan Baru.
Buletin Titrtanadi NO.4. (2006). PDAM TIRTANADI PENGHARGAAN CIPTA
KARYA DAN CITRA PELAYANAN PRIMA. Periode 2. Medan.
Gabriel, J. F. (2001). FISIKA LINGKUNGAN. Cetakan I. Penerbit Hipokrates.
Jakarta.
Hanum,Farida. (2002). PROSES PENGOLAHAN AIR SUNGAI UNTUK
KEPERLUAN AIR MINUM. USU Digitally Library. Medan.
Ryadi, Slamet SKM. (1984). PENCEMARAN AIR. Penerbit Karya Anda.
Surabaya.
Suriawiria,Unus. (2005). AIR DALAM KEHIDUPAN DAN LINGKUNGAN
YANG SEHAT. Penerbit PT. Alumni. Bandung.
Sutrisno, Totok C, dkk. (1987). TEKNOLOGI PENYEDIAAN AIR BERSIH.