PERTUMBUHAN, KONSENTRASI KLOROFIL-A, DAN STRUKTUR
MAKROALGA
Gracilaria edulis
PADA MEDIA MENGANDUNG Cu
EMMY SYAFITRI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Pertumbuhan,
Konsentrasi Klorofil-a, dan Struktur Makroalga
Gracilaria edulis
pada
Media Mengandung Cu adalah karya saya dengan arahan dari komisi
pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan
tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya
yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan
dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis
ini.
Bogor, April 2012
Emmy Syafitri
NRP C551090021
ABSTRACT
EMMY SYAFITRI. Growth, Concentration Chlorophyll-a, and Structure of
Macroalgae
Gracilaria edulis
in the Culture Media Containing Copper.
Under supervision of TRI PRARTONO and MUJIZAT KAWAROE.
The physiological responses (specific growth rate, concentration of
chlorophyll-a, morphological and anatomical structure of the vegetative
cells) of the marine macroalga
Gracilaria edulis
at the different
concentrations of copper (0.01 as control, 0.04, 0.06 and 0,5 ppm)
delivered continuously for 28 days under controlled laboratory conditions
were investigated. Result showed that the degree of copper toxicity
depends on both factor the concentration and exposure time. Copper
concentration and day of exposure decreased significantly the specific
growth rate (SGR) of the
Gracilaria edulis
but only 0,5 ppm Cu decreased
the chlorophyll-a content when compared to control. Of the various
physiological end points measured, growth proved to be the most sensitive
response than chlorophyll-a with reductions in specific growth rate (SGR).
The reason for this could be related to a greater sensitivity of the enzymes
involved in growth than those related to chlorophyll-a or a greater energy
needs to maintain cellular integrity and metabolic processes under
sub-lethal Cu stress
.
In all cases, the main effect on vegetative cells were
structure changes in cortex and subcortex cells, compared to control,
macroalgae exposed to copper showed depigmentation and blending in
the lateral branches, heavy staining of the cell wall and severe damage of
cell membrane, while the mucilage and the cell walls was densely fibrillar,
thick and heavily stained, the cortex cell was clearly vacuolated, the
presence of endophytic on the cell wall and endophytic spores in the
mucilage. The presence vacuoles should be related to a metal
immobilization mechanism, minimizing the Cu toxicity for cells. The
epiphytic bacteria can act as a biofilter diminishing the availability of Cu for
macroalgae accumulation.
RINGKASAN
EMMY SYAFITRI. Pertumbuhan, Konsentrasi Klorofil-a, dan Struktur
Makroalga
Gracilaria edulis
pada Media Mengandung Cu. Dibimbing oleh
TRI PRARTONO dan MUJIZAT KAWAROE.
Tembaga sebagai salah satu logam berat essensial yang berfungsi
sebagai mikronutrien dalam proses metabolisme organisme fotosintetik
perairan khususnya makroalga (membantu transport elektron dalam
proses fotosintesis), namun akan bersifat toksik bila konsentrasi tembaga
meningkat dalam sel organisme. Makroalga berperanan penting dalam
keseimbangan ekosistem akuatik, karena berada pada tingkat pertama
dalam rantai makanan yang memproduksi bahan organik dan oksigen
melalui proses fotosintesis. Penelitian dilaksanakan dengan tujuan
menunjukkan respon pertumbuhan, konsentrasi klorofil-a, dan struktur
talus
Gracilaria edulis
berdasarkan tingkat konsentrasi Cu.
Gracilaria
edulis
diperoleh dari tambak budidaya rumput laut Dusun 4
Desa Selotong Kecamatan Secanggang Kabupaten Langkat Sumatera
Utara. Bibit diambil dengan cara memotong bagian ujung vegetatif
kira-kira 10-20 cm. Setelah tiba di laboratorium makroalga segera dimasukkan
ke dalam akuarium untuk proses aklimatisasi selama 14 hari. Media
menggunakan metode dasar (
bottom method
) yang telah dimodifikasi
sesuai keadaaan akuarium. Tiap akuarium dipelihara sebanyak 3 rumpun
makroalga, dan setiap rumpun beratnya 10 gram. Media uji menggunakan
air laut murni sebanyak 10 liter dengan kandungan nitrat 0,55 ppm dan
fosfat 0,07 ppm serta 0,01 ppm Cu. Pergantian air media uji dilakukan 2
kali seminggu (semistatik) untuk mempertahankan nutrien bagi makroalga
dan konsentrasi Cu (sebagai perlakuan toksisitas) tetap stabil hingga akhir
penelitian. Percobaan penelitian menggunakan rancangan acak kelompok
(RAK) dimana konsentrasi Cu (0,01 ppm, 0,04 ppm, 0,06 ppm, 0,5 ppm)
sebagai perlakuan sedangkan waktu pengamatan termasuk dalam
kelompok. Pengamatan percobaan terdiri dari: (1) parameter kualitas air;
(2) parameter respon fisiologis yang terdiri dari: bobot segar dan laju
pertumbuhan spesifik, klorofil-a dan struktur talus. Data-data yang
diperoleh dalam penelitian ini dianalisis dengan menggunakan analisis
varians (ANOVA). Apabila pengaruh perlakuan dan kelompok berbeda
nyata dengan selang kepercayaan 95 % (P<0,05), maka diadakan uji
lanjut Duncan.
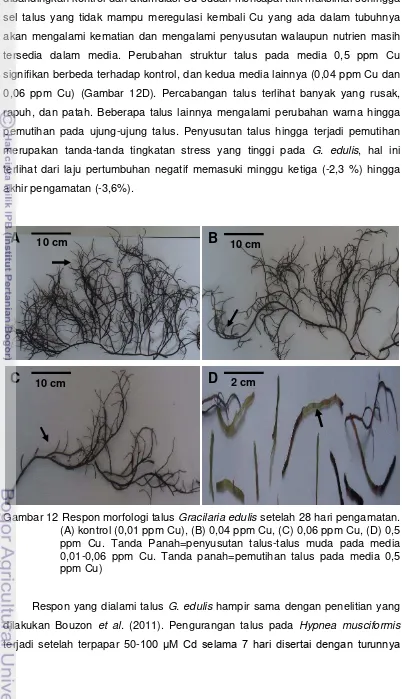
paparan. Secara morfologi tampak terhambatnya pertumbuhan talus-talus
muda pada media 0,04-0,06 ppm Cu hingga terjadi pemutihan pada
ujung-ujung talus disertai rapuhnya struktur talus pada media 0,5 ppm Cu,
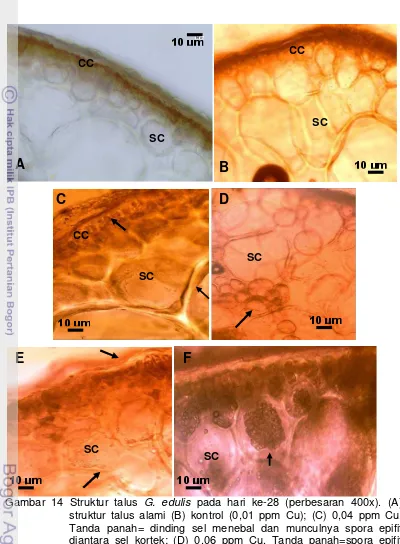
diduga munculnya lapisan alga filament yang melekat pada dinding sel
hingga terbentuknya spora endofit diantara ruang sel kortek dan sel sub
kortek. Dinding sel dan lapisan mucilage yang menebal diduga dipenuhi
noda-noda hitam hingga masuk ke dalam sitoplasma sel kortek
merupakan akibat dari proses penyerapan dan kemampuan akumulasi
makroalga terhadap logam berat Cu hingga terbentuknya vakuola dalam
sitoplasma sebagai mekanisme pertahanan
G. edulis
dalam zat toksik Cu.
Fenomena ini mengindikasikan bahwa respon pertumbuhan merupakan
respon fisiologis yang paling sensitif dibandingkan konsentrasi klorofil-a.
Hal ini diduga terganggunya kerja sistem enzim dan berkurangnya
pasokan energi yang dibutuhkan untuk proses pertumbuhan serta
kerusakan oksidatif pada lapisan lemak, protein dan asam nukleat.
Kata kunci: pertumbuhan, klorofil-a, struktur talus, tembaga, makroalga,
G.
edulis
© Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang – Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk
kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan
laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan
tersebut tidak merugikan kepentingan yang wajar IPB
PERTUMBUHAN, KONSENTRASI KLOROFIL-A, DAN STRUKTUR
MAKROALGA
Gracilaria edulis
PADA MEDIA MENGANDUNG Cu
EMMY SYAFITRI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Kelautan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
HALAMAN PENGESAHAN
Judul Tesis
: Pertumbuhan, Konsentrasi Klorofil-a, dan Struktur
Makroalga
Gracilaria edulis
pada Media Mengandung
Cu.
Nama
: Emmy Syafitri
NRP
: C551090021
Disetujui
Komisi Pembimbing
Dr. Ir. Tri Prartono, M.Sc Dr. Ir. Mujizat Kawaroe, MSi
Ketua Anggota
Diketahui
Ketua Program studi Ilmu Kelautan
Dr. Ir. Neviaty P. Zamani, M.Sc
Dekan Sekolah Pascasarjana IPB
Dr. Ir. Dahrul Syah, M.Sc.Agr
PRAKATA
Puji syukur kehadirat Allah SWT atas segala rahmat dan karunia-Nya
sehingga penulis dapat menyelesaikan tesis dengan judul “Pertumbuhan,
Konsentrasi Klorofil-a, dan Struktur Makroalga
Gracilaria edulis
Pada
Media Mengandung Cu”. Penulis berharap tesis ini dapat bermanfaat bagi
kita semua dan kemajuan ilmu pengetahuan dibidang ilmu kelautan.
Dalam kesempatan ini penulis menyampaikan terima kasih kepada semua
pihak yang telah membantu dalam penyusunan tesis ini, terutama kepada Dr. Ir.
Tri Prartono, M.Sc selaku Ketua Komisi Pembimbing dan Dr.Ir. Mujizat Kawaroe,
M.Si selaku pembimbing anggota yang telah penuh perhatian dan kesabaran
dalam memberikan bimbingan dan arahan hingga penyusunan tesis ini selesai.
Selanjutnya, ungkapan terima kasih disampaikan kepada Dr. Ir. Etty Riani, MS
selaku penguji luar komisi yang juga telah memberikan masukan untuk
menyempurnakan tesis ini. Di samping itu, ungkapan terima kasih tak terhingga
kupersembahkan kepada papa, mama, serta suami dan putraku tercinta
Kurniawan Sinaga dan Hanif Izzan Sinaga atas doa, dukungan, dan kasih
sayangnya. Terima kasih juga di ucapkan kepada seluruh teman-teman di
Program studi IKL dan pegawai sekretariat Program studi IKL, atas segala
bantuannya.
Penulis menyadari bahwa tesis ini belum sempurna, oleh karena itu
penulis mengharapkan kritik dan saran untuk perbaikan tesis ini.
Bogor, April 2012
RIWAYAT HIDUP
Penulis dilahirkan di Medan pada tanggal 27 Agustus 1981 dari ayah
Drs. Syafrinal, Apt, MSi dan ibu Emiar Wahid. Penulis merupakan putri
pertama dari dua bersaudara.
DAFTAR ISI
Halaman
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
DAFTAR LAMPIRAN ...v
1. PENDAHULUAN... 1
1.1 Latar Belakang ... 1
1.2 Kerangka Pemikiran ... 2
1.3 Perumusan Masalah ... 6
1.4 Tujuan Penelitian ... 6
1.5 Manfaat Penelitian ... 6
1.6 Hipotesis Penelitian ... 6
2.
TINJAUAN PUSTAKA ... 7
2.1 Pencemaran Logam Berat Tembaga ... 7
2.2 Peran Tembaga Bagi Makroalga ... 7
2.3 Toksisitas Tembaga bagi Makroalga ... 8
2.3.1 Pertumbuhan ... 9
2.3.2 Klorofil-a ... 10
2.3.3 Struktur Talus ... 12
2.4 Mekanisme Toksisitas dan Detoksifikasi Tembaga pada Makroalga .... 15
2.5 Penggunaan Makroalga sebagai Biota Uji Toksisitas ... 18
3.
METODE PENELITIAN ... 21
3.1 Tempat dan Waktu Penelitian ... 21
3.2 Alat dan Bahan... 21
3.3 Persiapan Penelitian ... 22
3.3.1 Penentuan Konsentrasi Toksikan Cu ... 22
3.3.2 Penyediaan Makroalga ... 22
3.3.3 Aklimatisasi Makroalga ... 23
3.3.4 Pembuatan Larutan Stok ... 23
3.4 Perlakuan Penelitian ... 24
3.4.1 Rancangan Percobaan ... 24
3.4.2Pengamatan Percobaan ... 25
3.4.2.1 Parameter Kualitas Media ... 25
3.4.2.2 Parameter Respon Fisiologis ... 25
3.4.2.2.1 Laju Pertumbuhan ... 25
3.4.2.2.2 Klorofil-a ... 25
3.4.2.2.3 Struktur Talus ... 26
3.5 Analisa Data ... 27
4.
HASIL DAN PEMBAHASAN ... 29
4.1 Hasil ... 29
4.1.1 Laju Pertumbuhan Spesifik ... 29
4.1.2 Klorofil-a ... 33
4.1.3 Struktur Talus... 35
4.1.4 Parameter Kualitas Media ... 41
4.2 Pembahasan ... 43
5.
SIMPULAN dan SARAN ... 51
5.1.Kesimpulan ... 51
5.2.Saran ... 51
DAFTAR PUSTAKA ... 53
DAFTAR TABEL
Halaman
1. Alat dan bahan untuk pemeliharaan Gracilaria edulis. ... 21
2. Alat dan bahan untuk pengukuran laju pertumbuhan,
konsentrasi klorofil-a, dan pengamatan struktur talus. ... 22
3. Konsentrasi Cu sebagai konsentrasi toksikan terhadap makroalga. ... 22
4. Kualitas air rata-rata (± STD, n=6) selama 28 hari pengamatan
DAFTAR GAMBAR
Halaman
1. Skema kerangka pemikiran. ... 5
2. Penampang melintang (4) dan potongan membujur (5)
Gracilaria edulis. ... 12
3. Transmisi elektron mikrograph sel Enteromorpha flexuosa... ... 13
4. Respon morfologi Hypnea musciformis setelah terpapar Cd
selama 7 hari (skala 1 cm)... ... 14
5. Pemutihan pada L. nigrescens setelah terpapar Cu selama 96 jam (skala 2 cm).... ... 14
6. Penampang melintang talus H. Musciformis setelah terpapar Cd selama 7 hari.... ... 15
7. Skema akuarium terkontrol pada pemeliharaan Gracilaria edulis. ... 24
8. Pengacakan dan bagan percobaan RAK. ... 24
9. Bobot segar rata-rata (gr) (± SE, n=6) Gracilaria edulis selama 28 hari pengamatan.. ... 29
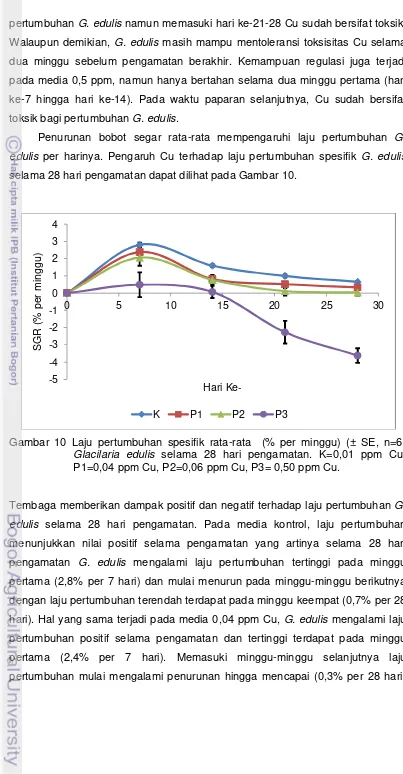
10. Laju pertumbuhan spesifik rata-rata (% per minggu) (± SE, n=6) Glacilaria edulis selama 28 hari pengamatan. ... 31
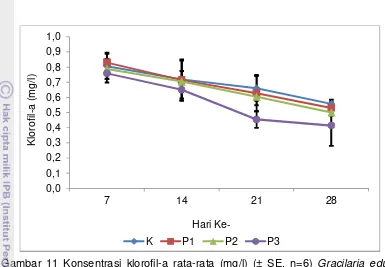
11. Konsentrasi klorofil-a rata-rata (mg/l) (± SE, n=6)
Gracilaria edulis selama 28 hari pengamatan. ... 34
12. Respon morfologi talus Gracilaria edulis setelah 28 hari pengamatan. ... 36
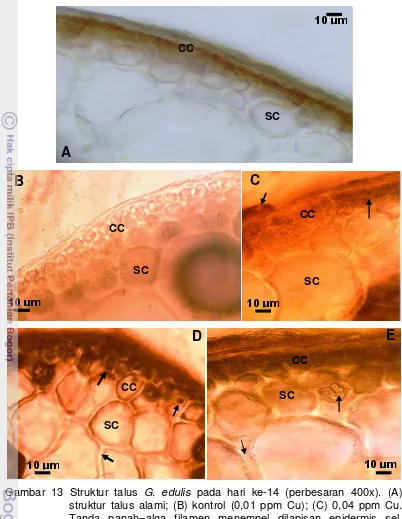
13. Struktur talus G. edulis pada hari ke-14 (perbesaran 400x). ... 38
DAFTAR LAMPIRAN
Halaman
1. Pembuatan larutan stok Cu. ... 59
2. Bobot segar rata-rata, laju pertumbuhan spesifik rata-rata, dan konsentrasi klorofil rata-rata G. edulis selama 28 hari
pengamatan. ... 60
3. Analisa ragam (ANOVA) dan uji lanjut Duncan bobot segar
G. edulis. ... 61
4. Analisa ragam (ANOVA) dan uji lanjut Duncan laju pertumbuhan spesifik G. edulis... 62
5. Analisa ragam (ANOVA) dan uji lanjut Duncan konsentrasi klorofil-a G. edulis.. ... 63
6. Kualitas air media rata-rata selama 28 hari pengamatan.. ... 64
1.
PENDAHULUAN
1.1 Latar Belakang
Peningkatan kesejahteraan hidup rakyat melalui pembangunan di bidang
industri, nampak memberikan dampak terhadap perubahan lingkungan perairan
pesisir dan laut karena buangan limbah yang dihasilkan. Salah satu limbah
berbahaya dan beracun bagi organisme adalah logam berat tembaga. Limbah
tersebut berpotensi menurunkan fungsi dan daya guna air termasuk
mengganggu kehidupan organisme akuatik. Gangguan tersebut dapat berupa
gangguan fungsi fisiologis, pertumbuhan, reproduksi, bahkan mengakibatkan
kematian.
Tembaga merupakan salah satu logam berat yang paling sering digunakan
dalam sektor industri dan menghasilkan limbah sebanyak 35x103 hingga 90x103
ton per tahun di permukaan perairan seluruh dunia (Perales-Vela et al., 2007).
Fenomena tersebut secara signifikan terjadi pada daerah pesisir yang
merupakan tempat bermuaranya limbah perkotaan, run off dari kegiatan industri,
pertambangan, dan pertanian. Limbah ini akan terus meningkat dari waktu ke
waktu seiring berkembangnya perkotaan dan kegiatan industri.
Tembaga digolongkan ke dalam logam berat essensial dan berfungsi
sebagai mikronutrien dalam proses pertumbuhan makroalga, membantu kerja
enzim (kofaktor enzim), pembawa (carrier) elektron dalam proses fotosintesis
dan respirasi (Perales-Vela et al., 2007). Makroalga adalah komponen essensial
sebagai produsen pada ekosistem akuatik yang memproduksi oksigen dan
substansi organik melalui proses fotosintesis yang sangat dibutuhkan bagi
organisme lainnya antara lain ikan dan invertebrata (Eklund dan Kautsky, 2003).
Pertumbuhan makroalga seperti Gracilaria edulis sangat dipengaruhi oleh
kualitas lingkungan perairan. Tingginya konsentrasi logam berat di perairan
dapat bersifat toksik dan pada akhirnya mampu menghambat pertumbuhan
makrolaga tersebut. Penelitian fitotoksikologi logam berat tembaga pada
makroalga khususnya Gracilaria edulis di Indonesia masih sangat sedikit. Sejauh
ini mikroalga dan tumbuhan tingkat tinggi masih mendominasi dalam uji toksisitas
logam berat dan hanya 82 artikel yang ditemukan dari tahun 1959-2000 yang
membahas mengenai respon toksisitas logam berat pada makroalga (Eklund dan
Kautsky, 2003; Melville dan Pulkownik, 2006). Berdasarkan laporan tersebut
hidup pada daerah subtropik dengan jenis Fucus spp dan Enteromorpha spp dan
respon fisiologis makroalga akibat cemaran logam berat Cu berbeda-beda
sensitifitasnya antara jenis yang satu dengan jenis lainnya tergantung daerah
atau habitat dari masing-masing organisme tersebut. Melihat kondisi tersebut
perlu dilakukan studi fitotoksikologi (pertumbuhan, klorofil-a, dan struktur talus)
pada Gracilis edulis yang hidup pada daerah tropis akibat cemaran logam berat
Cu.
1.2 Kerangka Pemikiran
Tembaga masuk ke laut melalui buangan limbah industri dan endapan
partikel atmosfer yang tercemar oleh asap pabrik mengandung tembaga.
Menurut Mukhtasor (2007) industri galangan kapal dan pengecatan antifouling
pada kapal merupakan pencemar Cu terbesar di Great Britain dan California
Selatan pada tahun 1978. Data tentang status pencemaran logam tembaga
untuk setiap wilayah perairan Indonesia belum tersedia, namun penelitian
mengenai status pencemaran tembaga telah banyak dilakukan dan diperkirakan
sudah berindikasi pencemaran.
Gracilaria spp umumnya hidup sebagai fitobentos, melekat pada substrat
padat seperti kayu, batu, karang mati dan sebagainya. Tersebar luas di daerah
pesisir (litoral dan sub litoral), sampai kedalaman tertentu, yang masih dapat
dicapai oleh oleh penetrasi cahaya matahari. Di Indonesia terdapat lebih kurang
15 jenis Gracilaria yang menyebar di seluruh kepulauan (Sjafrie, 1990) salah satu
diantaranya adalah Pulau Lancang dan Pulau Pari Kepulauan Seribu (Kadi,
1993). Perkembangan terakhir mengindikasikan bahwa populasi makroalga
khususnya Gracilaria semakin menurun. Penurunan ini diduga disebabkan oleh
terjadinya penurunan kualitas perairan akibat pencemaran logam berat di
Kepulauan Seribu mengingat perairan ini berhubungan langsung dengan Teluk
Jakarta yaitu teluk yang paling tercemar di Asia akibat limbah industri dan rumah
tangga (Lestari dan Edward, 2004).
Evaluasi kondisi lingkungan perairan Kepulauan Seribu bagian utara,
tengah, dan selatan tahun 2004 menunjukkan bahwa konsentrasi Cu telah
melebihi ambang batas toleransi bagi makroalga yaitu berkisar antara
0,076-0,209 mg/l (Sachoemar, 2008). Konsentrasi ini diperkirakan akan terus
meningkat dengan semakin meningkatnya kegiatan industri saat ini. Program
digunakan untuk memahami efek toksikan pada lingkungan sampai tingkat
populasi.
Tembaga tergolong logam berat essensial dan merupakan mikronutrien
bagi organisme fotosintetik. Walaupun demikian bila konsentrasinya meningkat
Cu akan bersifat racun seperti mengganggu proses pertumbuhan dan beberapa
proses fisiologi lainnya. Beberapa penelitian uji toksisitas Cu telah dilakukan
pada spesies indikator, seperti konsentrasi Cu terlarut yang mencapai 0,01 ppm
akan mengakibatkan kematian bagi fitoplankton; bangsa crustacea akan
mengalami kematian dalam tenggang waktu 96 jam, bila konsentrasi Cu berkisar
antara 0,17-1,00 ppm; dalam tenggang waktu yang sama, bangsa moluska akan
mengalami kematian bila Cu dalam kisaran 0,16-0,5 ppm, dan bila Cu dalam
kisaran 2,5-3,0 ppm akan dapat membunuh ikan (Palar, 2008).
Kasus di atas menunjukkan bahwa tembaga dapat mengakibatkan
kerusakan lingkungan secara biologis. Lingkungan yang sehat ditandai dengan
kondisi biologis yang seimbang dan kehidupan biota yang beranekaragam. Oleh
sebab itu, guna mengurangi dan mengendalikan terjadinya pencemaran air yang
disebabkan oleh tembaga perlu suatu penelitian untuk memahami tingkat
toksisitas tembaga terhadap organisme yang hidup di dalam perairan.
Pengetahuan tentang efek senyawa-senyawa kimia penyebab pencemaran air
pada organisme perairan sangat penting untuk mengetahui keberadaan senyawa
tersebut dalam air dan dapat digunakan sebagai bahan acuan dalam
menentukan pengawasan bagi keamanan dan kesehatan lingkungan.
Tingkat toksisitas tembaga serta pengaruhnya terhadap organisme
perairan dapat ditentukan dengan cara uji hayati (Hindarti, 1997). Hindarti (1997)
menyatakan uji hayati adalah pengujian menggunakan organisme dalam waktu
tertentu untuk mengevaluasi bahan kimia, limbah, faktor lingkungan, beserta
kombinasinya yang dapat menimbulkan pengaruh tertentu. Uji ini bertujuan
mengevaluasi pencemaran perairan, karena uji secara kimiawi dan fisika belum
mencukupi untuk menilai kondisi suatu perairan yang tercemar. Metode dalam uji
hayati terbagi menjadi dua cara yaitu bersifat letal dan subletal (Connell, 2005).
Pertimbangan Gracilaria edulis sebagai biota uji didasarkan pada tingkat
sensitifitas biota terhadap bahan pencemar, siklus hidupnya relatif panjang,
bernilai penting secara ekologis dan ekonomis, mudah diambil, tidak cepat rusak
dan mempunyai toleransi terhadap perubahan lingkungan seperti cahaya, suhu,
laboratorium untuk keperluan penelitian, dan resisten terhadap parasit dan
penyakit (Costanzo et al., 2000; Eklund dan Kautsky, 2003; Melville dan
Pulkownik, 2006).
Penelitian ini menunjukkan efek subletal Cu terhadap indikator fisiologis
pada makrolaga Gracilaria edulis dan tingkat respon fisiologisnya. Informasi ini
dapat dimanfaatkan sebagai alat (tool) atau acuan dalam melihat perairan yang
relatif tercemar dan relatif tidak tercemar logam berat tembaga. Pengembangan
uji toksisitas pada makroalga akan sangat berguna karena efek yang ditimbulkan
akan memberikan dampak awal pada rantai makanan dan akan memberikan
dampak sekunder pada tingkatan trofik yang lebih tinggi. Selanjutnya, jika
tembaga menunjukkan efek negatif terhadap pertumbuhan beserta struktur
distribusinya maka secara tidak langsung akan memberikan dampak negatif
pada ekosistem pesisir dan laut.
Efek subletal atau respon fisiologis yang akan diamati meliputi
pertumbuhan, konsentrasi klorofil-a, dan morfologi beserta anatomi makroalga
merah (Gambar 1). Respon di atas merupakan indikator sensitif dan akurat
dalam uji toksisitas logam berat tembaga. Beberapa penelitian menunjukkan
pertumbuhan merupakan respon fisiologis yang paling sensitif diantara respon
fisiologis dan biokimiawi lainnya (Li et al., 2010) diikuti konsentrasi klorofil-a.
Apabila pada waktu tertentu dan akumulasi Cu pada talus makroalga sudah
melewati ambang batas akan terjadi pemutihan pada sebagian atau keseluruhan talus. Hal ini terjadi pada konsentrasi Cu 100 μgL-1
selama 96 jam, Lessonia
nigrescens mengalami pemutihan pada ujung talusnya diakibatkan rusaknya
klorofil-a (Contreras et al., 2009).
Tembaga adalah salah satu senyawa kimia yang paling sering digunakan
untuk uji efek toksisitas pada makroalga sejak tahun 1959-2000 (Eklund dan
Kautsky, 2003) dan berdasarkan laporan tersebut makroalga yang sering diuji
adalah kelompok makroalga coklat dan hijau dengan jenis Enteromorpha spp
dan Fucus spp yang hidup di daerah sub tropis (Eklund dan Kautsky, 2003).
Penelitian terdahulu melaporkan spesies yang sama namun hidup dan tumbuh
pada daerah dengan parameter lingkungan yang berbeda dapat memberikan
respon yang berbeda pula terhadap toksikan logam berat (Hall et al., 1979).
Informasi mengenai respon fisiologis akibat cemaran logam berat tembaga pada
Gracilaria edulis yang hidup di daerah tropis jarang diketahui (Mamboya et al.,
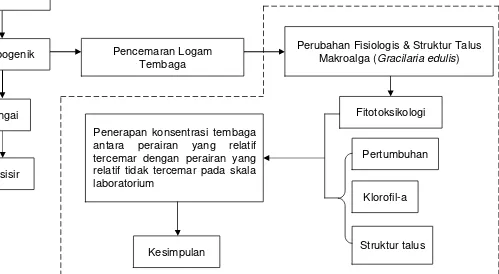
Keterangan:
: Proses
: Ruang lingkup Penelitian
Gambar 1 Skema kerangka pemikiran
Perubahan Fisiologis & Struktur Talus
Makroalga (Gracilaria edulis)
Pesisir Sungai Antropogenik Natural (Alami)
Sumber Logam Tembaga di Pesisir
Pencemaran Logam Tembaga
Fitotoksikologi
Penerapan konsentrasi tembaga antara perairan yang relatif tercemar dengan perairan yang relatif tidak tercemar pada skala laboratorium
Pertumbuhan
Laut
Klorofil-a
1.3 Perumusan Masalah
Berdasarkan latar belakang dan kerangka pemikiran di atas, maka
permasalahan penelitian ini dirumuskan sebagai berikut :
1. Apakah tembaga mempunyai pengaruh toksik terhadap pertumbuhan,
klorofil-a danstruktur talus Gracilaria edulis ?
2. Apakah tingkat konsentrasi Cu berpengaruh terhadap sifat fitotoksisitasnya ?
1.4 Tujuan Penelitian
Penelitian ini dilaksanakan dengan tujuan menunjukkan respon
pertumbuhan, konsentrasi klorofil-a, dan struktur talus Gracilaria edulis
berdasarkan tingkat konsentrasi Cu.
1.5 Manfaat Penelitian
Manfaat yang diperoleh dari penelitian ini adalah sebagai dasar
kelengkapan informasi tentang toksisitas cemaran tembaga pada biota air
khususnya organisme fotosintetik, Gracilaria edulis berdasarkan respon fisiologis
untuk kemudian dapat dijadikan dasar dalam melihat tingkat indikator kesehatan
ekosistem pesisir dan laut dan dapat memberikan informasi kepada
pembudidaya Gracilraria spp dalam mempertimbangkan lokasi budidaya
sehingga usaha budidaya Gracilaria spp dapat berhasil dengan baik.
1.6 Hipotesis Penelitian
Hipotesis penelitian ini adalah tingkat konsentrasi Cu pada kisaran 0,01-0,5
ppm selama 28 hari paparan dapat menurunkan pertumbuhan dan konsentrasi
2. TINJAUAN PUSTAKA
2.1 Pencemaran Logam Berat Tembaga
Lingkungan perairan dikatakan tercemar apabila telah terjadi
perubahan-perubahan dalam tatanan lingkungan perairan sehingga tidak sama lagi dengan
bentuk asalnya, sebagai akibat masuknya suatu zat ke dalam tatanan lingkungan
tersebut. Salah satu zat yang dapat mencemari lingkungan perairan adalah
logam berat dan apabila terlarut dalam konsentrasi tinggi, dapat berdampak
buruk pada satu atau lebih jenis organisme yang tadinya hidup normal dalam
tatanan lingkungan tersebut.
Tembaga (Cu) masuk ke dalam tatanan lingkungan perairan melalui jalur
alamiah dan non alamiah. Pada jalur alamiah, logam tembaga mengalami siklus
perputaran yang stabil, namun kandungan alamiah logam akan berubah-ubah
akibat jalur non alamiah. Jalur non alamiah berupa aktifitas manusia seperti
buangan limbah kegiatan industri, pertambangan Cu, maupun industri galangan
kapal beserta outfall dan pengecatan anti fouling pada kapal adalah jalur yang
mempercepat terjadinya peningkatan kelarutan Cu dalam perairan (Mukhtasor,
2007).
Kadar ambien total (Cu+2) yang terlarut dalam perairan laut lepas berkisar
antara 1-10 nM dan akan meningkat kadarnya mencapai 10-100 nM pada daerah
pesisir dan muara sungai (Brown dan Newman, 2003). Penelitian mengenai
status pencemaran tembaga di Indonesia telah banyak dilakukan dan
diperkirakan sudah berindikasi pencemaran. Evaluasi kondisi lingkungan
perairan Kepulauan Seribu bagian utara, tengah, dan selatan tahun 2004
menunjukkan bahwa konsentrasi Cu telah melebihi ambang batas toleransi bagi
makroalga yaitu berkisar antara 0,076-0,209 mg/l (Sachoemar, 2008).
2.2 Peran Tembaga Bagi Makroalga
Tembaga merupakan mineral essensial mikro yaitu mineral yang
diperlukan dalam jumlah sangat sedikit dan umumnya terdapat dalam tubuh
dengan konsentrasi sangat kecil. Walaupun dibutuhkan tubuh dalam jumlah
sedikit, bila kelebihan dapat mengganggu kesehatan atau mengakibatkan
keracunan (Yruela, 2005). Tembaga sebagai logam transisi, aktif dalam kegiatan
redoks pada berbagai proses fisiologi tumbuhan karena dibutuhkan untuk sistem
protein, berpartisipasi dalam transportasi elektron pada proses fotosintesis,
membantu proses respirasi pada mitokondria, merespons stress oksidatif pada
tubuh, membantu proses metabolisme dinding sel, dan membantu kerja hormon
(Yruela, 2005).
Tembaga dalam bentuk ion berperan sebagai kofaktor sistem enzim seperti
superoksida dismutase (SOD), katalase, askorbat peroksida (APX), sitokrom c
oksidase, amino oksidase, laccase, plastosianin, dan polifenol oksidase serta
bagian dari antioksidan enzim seperti askorbat, glutathione, flavonoid,
tokopherol, dan karotenoid (Collen et al., 2003; Yruela, 2005). Oleh karena itu,
tembaga sangat dibutuhkan untuk pertumbuhan dan perkembangan tumbuhan
khususnya makroalga.
2.3 Toksisitas Tembaga bagi Makroalga
Menurut Soemirat (2005) toksisitas adalah kemampuan racun (molekul)
untuk menimbulkan kerusakan apabila masuk ke dalam tubuh dan lokasi organ
yang rentan terhadapnya. Bentuk aksi penyerangan dari suatu toksikan
ditentukan oleh bentuk toksisitas yang dimiliki toksikan. Persenyawaan kimia dari
logam tembaga dapat merusak proses fisiologis makroalga seperti menghalangi
kerja enzim. Kemampuan siklus redoks Cu antara Cu+2 dan Cu+ dapat
memproduksi ROS dalam jumlah besar sehingga merusak DNA, lemak, protein,
dan biomolekul lainnya (Yruela, 2005).
Literatur telah melaporkan berbagai interaksi logam berat terhadap
biomolekul dalam tingkat sellular, diantaranya adalah : (1) berikatan pada gugus
sulfida protein sehingga menghambat sistem kerja enzim dan fungsi protein; (2)
menggantikan posisi ion-ion logam essensial yang terdapat dalam molekul terkait
seperti logam Mg; (3) menghalangi proses transportasi antar sel; dan (4)
kerusakan oksidatif pada tubuh (Yruela, 2005). Tingkatan toksisitas Cu sangat
sulit untuk diprediksi tergantung pada kondisi habitat dan jenis masing-masing
dari organisme tersebut. Karena bersifat essensial dan toksik konsentrasi Cu
dibutuhkan dalam jumlah yang kecil seperti, makroalga dapat mentoleransi <10 μg L-1
Cu dalam selnya (Lobban dan Harrison, 1997).
Beberapa toksisitas yang disebabkan Cu bila konsentrasi dalam sel
melebihi kemampuan toleransi makroalga seperti, menghambat proses
pertumbuhan, menghambat proses biosintesis klorofil-a, dan merusak elastisitas
2.3.1 Pertumbuhan
Pola pertumbuhan makroalga Gracilaria membentuk kurva sigmoidal
(pertumbuhannya meningkat dari nilai lambat, cepat dan akhirnya mendekati nilai
tetap (konstan) yang bergantung hanya pada waktu, sehingga model
pertumbuhan biomassa Gracilaria merupakan model pertumbuhan logistik
dengan carrying capacity konstan (Kartono et al., 2008). Model pertumbuhan
logistik ini menunjukkan pertumbuhan maksimum ketika biomassa Gracilaria
sama dengan carrying capacity, dan pada saat itu pertumbuhan tidak lagi terjadi.
Kematian pada makroalga disebabkan antara lain menipisnya nutrien,
kekurangan oksigen, media lingkungan yang terlalu panas, pH media yang selalu
berubah-ubah, atau kontaminasi yang berasal dari media kultivasi
(Coutteau,1996).
Pertumbuhan adalah proses perubahan ukuran meliputi panjang, berat
atau volume pada periode waktu tertentu. Pertumbuhan yang optimal
dikarenakan proses metabolisme berjalan dengan baik. Proses metabolisme
akan berjalan dengan baik bila didukung oleh kondisi lingkungan yang optimal
termasuk konsentrasi mikronutrien yang cukup bagi kelangsungan proses
pertumbuhan makroalga. Enzim memegang peranan yang sangat penting dalam
mempercepat dan memperlancar proses metabolisme. Enzim-enzim tertentu
yang terdapat pada makroalga merah memiliki gugus fungsi sulfhidril (-SH)
sebagai pusat aktifnya (Lobban dan Harrison, 1997). Enzim yang memiliki gugus
sulfhidril merupakan kelompok enzim yang mudah terhalang daya kerjanya
disebabkan gugus sulfhidril yang dikandungnya dengan mudah dapat berikatan
dengan ion-ion logam berat yang masuk ke dalam tubuh (Palar, 2008). Akibat
dari ikatan yang terbentuk, daya kerja yang dimiliki enzim menjadi sangat
berkurang atau sama sekali tidak dapat bekerja. Keadaan ini secara keseluruhan
akan merusak sistem metabolisme tubuh. Selain mempengaruhi kerja enzim,
tembaga juga mempengaruhi pasokan energi untuk proses pertumbuhan.
Pertumbuhan yang optimal, secara fisiologis hanya dapat terjadi apabila
terdapat kelebihan energi, setelah energi melalui pakan yang dikonsumsi
dikurangi dengan kebutuhan energi untuk berbagai aktivitas. Adanya perubahan
kondisi lingkungan terutama kelarutan logam berat yang tinggi akan berpengaruh
pada besaran energi yang dikonsumsi dapat lebih besar atau lebih kecil
daripada energi yang dibelanjakan terutama untuk keperluan pertumbuhan.
dalam tubuh organisme) akan menginduksi produksi ROS (reactive oxygen
species) seperti superoxide radicals (O2•¯ ), hydrogen peroxide (H2O2), singlet
molecular oxygen (1O2 (1Δg)), dan hydroxyl radicals (OH). Komponen ROS
tersebut akan menginduksi kerusakan oksidatif pada lapisan lemak, protein, dan
asam nukleat disertai menganggu fungsi kerja sel.
ROS dalam konsentrasi kecil merupakan hal yang normal pada organisme
fotosintetik, namun dalam kondisi stress produksi ROS akan meningkat sehingga
akan menjadi permasalahan dalam tubuh. Strategi untuk mencegah kerusakan
yang disebabkan oleh ROS, makroalga memproduksi enzim dan antioksidan
enzim seperti SOD (superoxide dismutase), katalase, APX (ascorbate
peroxidase), glutathione, malondialdehyde (MDA), flavonoids, tocopherols, dan
karotenoids (Bouzon et al., 2011; Manimaran et al., 2011). Pengaktifan enzim
dan antioksidan ini membutuhkan energi yang besar sehingga energi yang ada
digunakan untuk memproduksi antioksidan tersebut agar kerusakan sel tidak
terjadi dan sisa energi yang ada tidak dapat mencukupi dalam kegiatan proses
pertumbuhan.
Beberapa penelitian toksisitas Cu yang menunjukkan hubungan antara
proses pertumbuhan dengan enzim antioksidan dan cadangan energi yang ada
pada makroalga. Penelitian yang dilakukan oleh Collen et al. (2003) konsentrasi
0,2 ppm Cu+2 selama 4 hari paparan menunjukkan penurunan laju pertumbuhan
Gracilaria tenuistipitata sebesar 60% per hari disertai peningkatan produksi
enzim dan antioksidan enzim berupa SOD, APX, katalase, MDA, dan karotenoid.
Hal yang sama dilakukan oleh Huang et al pada tahun 2010, selama 14 hari
paparan dengan jenis yang sama laju pertumbuhan mengalami penurunan 60% per hari pada konsentrasi 200 μg L-1
Cu disertai cadangan total energi untuk
pertumbuhan yang semakin menurun akibat toksisitas Cu. Penelitian lain yang
dilakukan Han et al. (2008) selama 3 hari paparan konsentrasi 100 μg L-1 Cu
telah menurunkan 41% laju pertumbuhan Ulva armoricana per hari disertai
peningkatan antioksidan pada konsentrasi tersebut, namun pada konsentrasi 250 μg L-1
Cu terjadi laju pertumbuhan negatif (-1,4% per hari) disertai
kecenderungan menurunnya produksi antioksidan.
2.3.2 Klorofil-a
Komponen molekular penting pada organisme fotosintetik khususnya
klorofil-a dan d (Meeks, 1974). Klorofil-a dalam bentuk kimia mengandung satu
inti porfirin dengan satu atom magnesium terikat kelat ditengah dan satu rantai
samping hidrokarbon panjang (fitil) tergabung melalui gugus asam karboksilat
(Meeks, 1974). Faktor-faktor yang langsung mempengaruhi konsentrasi klorofil-a
adalah nutrien, intensitas cahaya, suhu, dan umur sel (Meeks, 1974). Oleh sebab
itu keberadaan Cu dalam sel makroalga tidak secara langsung berdampak
negatif terhadap konsentrasi klorofil-a.
Beberapa penelitian sebelumnya menunjukkan Cu tidak berdampak
langsung terhadap konsentrasi klorofil-a seperti, Cu 0 μgL-1–500 μgL-1 tidak
memberikan pengaruh yang signifikan terhadap jumlah konsentrasi klorofil-a
Gracilaria longissima selama 7 hari (Brown dan Newman, 2003), selama 4 jam
dengan konsentrasi Cu 0,2 ppm Cu+2 klorofil-a Gracilaria tenuistipitata tidak
mengalami perubahan dibandingkan kontrol (Collen et al., 2003), Xia et al.
(2004) juga membuktikan bahwa pada perlakuan Cu 0 μM–10 μM selama 96 jam
tidak memberikan pengaruh yang signifikan terhadap jumlah klorofil-a Gracilaria
lemaneiformis, hal serupa terjadi pada mikroalga Pavlova viridis yakni tidak
terjadi perubahan konsentrasi klorofil-a akibat terpapar 0,05–0,5 mgl- Cu+2
selama 16 hari (Li et al., 2006), dan diatom laut Odontella mobiliensis tidak
mengalami perubahan konsentrasi klorofil-a dibandingkan kontrol pada selang
konsentrasi Cu 52-213 μg L-1 selama 72 jam (Manimaran et al., 2011).
Beberapa toksisitas Cu terhadap klorofil-a apabila konsentrasinya sudah
sangat tinggi diantaranya adalah, menghambat pembentukan pigmen fotosintetik
dan memperlambat penggabungan klorofil ke tilakoid (membran fotosintetik
kloroplas) (Manimaran et al., 2011), mengakibatkan pembesaran kompleks
antena (light-harvesting antenna) dalam fotosistem (Bertrand dan Poirier, 2005)
sehingga mengakibatkan fotoinhibisi, berkurangnya konsentrasi klorofil dengan
mengganti posisi logam Fe sebagai biosintesis klorofil-a (Patsikka et al., 2002),
menghambat beberapa enzim dalam sintesa klorofil yaitu δ-aminolevulinic acid
dan protochlorophyllide (Perales-Vela et al., 2007; Manimaran et al., 2011),
ALA-dehydratase (enzim yang membantu membentuk struktur porphyrin klorofil-a)
(Fernandes dan Henriques, 1991), dan merangsang produksi ROS yaitu
peroxidation yang merusak sintesa pigmen dan membran lemak (Fernandes dan
Henriques, 1991; Perales-Vela et al., 2007; Li et al., 2010), rusaknya struktur
molekul klorofil dikarenakan posisi atom Mg yang berada di tengah cincin
penangkap cahaya akan terhambat dan akhirnya proses fotosintesis akan
terganggu (Kupper et al., 1996; Bertrand dan Poirier, 2005).
Dampak yang terlihat pada klorofil-a akibat toksisitas Cu adalah terjadinya
chorosis yaitu pemutihan sebagian talus makroalga. Chorosis adalah tanda
dimana tumbuhan mengalami stres akibat kondisi lingkungan yang tidak kondusif
sehingga dapat dijadikan indikator terhadap kondisi lingkungan tersebut
(Bertrand dan Poirier, 2005; Ayeni et al., 2010).
2.3.3 Struktur Talus
Struktur anatomi talus Gracilaria edulis dengan menggunakan mikroskop
cahaya, tampak tersusun oleh 3 bentuk sel. Susunan sel dari luar ke dalam yaitu:
epidermis, kortek (cortical), sub kortek (sub cortical), dan tengah (medula)
(Yamamoto, 1978). Terlihat bahwa susunan sel dari tepi berbentuk kecil
(epidermis dan kortek), mulai membesar pada lapisan sel sub kortek dan
semakin ke dalam bentuk selnya semakin besar, poligonal sampai agak bulat
disebut sel medula (Gambar 2).
.
Gambar 2 Penampang melintang (4) dan potongan membujur (5) Gracilaria
edulis; (a) Lapisan sel kortek, (b) lapisan sel sub kortek, (c) lapisan sel medula (Yamamoto, 1978).
Tidak banyak penelitian yang membahas toksisitas logam berat khususnya
tembaga terhadap struktur sel makroalga bila di dilihat menggunakan mikroskop
cahaya, namun beberapa penelitian telah membahas permasalahan tersebut.
Tahun 1972 penelitian sitologi yang dilakukan Nuzzi dalam Massalski et al.
(1981) menggunakan mikroskop cahaya pada diatom laut Phaeodactylum
tricormutum, terjadi perubahan-perubahan struktur sel akibat terpapar logam
berat merkuri seperti bentuk sel yang berubah menjadi lebih lonjong dan
a
c
c
b
terbentuknya banyak vakuola. Pada kondisi yang sama terjadi
ketidakseimbangan pertumbuhan sel-sel Chlorella sp yaitu berubah menjadi sel
raksasa Hal serupa terjadi pada konsentrasi 50 µg/L Cu, vakuola besar dan
beberapa vakuola kecil yang berada pada sitoplasma Enteromorpha flexuosa
(makroalga hijau) dipenuhi oleh logam Cu dan terakumulasi di dalamnya
(Gambar 3) (Andrade et al., 2004). Menurut Andrade et al. (2004) pembentukan
vakuola merupakan salah satu proses atau mekanisme dalam meminimalisasi
daya toksik Cu terhadap sel. Salah satu peran vakuola dalam sel adalah sebagai
tempat pembuangan produk samping metabolisme yang akan membahayakan
sel itu sendiri jika produk samping ini terakumulasi dalam sitosol (Campbell et al.,
2002).
Gambar 3 Transmisi elektron mikrograph sel Enteromorpha flexuosa. (1) sel
Enteromorpha flexuosa pada media kontrol, tidak terjadi akumulasi
Cu di dalam vakuola (tanda panah). (2) sel Enteromorpha flexuosa
pada media 50 µg/L Cu, terjadi akumulasi Cu di dalam vakuola
besar dan vakuola kecil (tanda panah) (Andrade et al., 2004).
Penelitian yang dilakukan Bouzon et al. (2011) pada Hypnea musciformis
(makroalga merah) bahwa kisaran 50-100 μM Cd selama 7 hari paparan,
percabangan talus (dichotomy) mulai terhambat pertumbuhannya dan tampak
hanya talus utama yang masih utuh (Gambar 4). Pemutihan talus terjadi ketika H.
musciformis terpapar 200-300 μM Cd (Gambar 4). Hal serupa terjadi pada
Lessonia nigrescens (makroalga coklat) yang terpapar 100 μg L-1 Cu selama 96
jam, ujung talus makroalga mengalami pemutihan (Contreras et al., 2009)
(Gambar 5).
Gambar 4 Respon morfologi Hypnea musciformis setelah terpapar Cd selama 7 hari (skala 1 cm). (A) kontol, (B) 50 μM Cd, (C) 100 μM Cd, (D) 200 μM Cd, (E) 300 μM Cd. Tanda panah menunjukkan degradasi warna pada percabangan talus pada media kontrol hingga terjadi pemutihan
pada media 200-300 μM Cd (Bouzon et al., 2011).
Gambar 5 Pemutihan pada L. nigrescens setelah terpapar Cu selama 96 jam
(skala 2 cm). Tanda panah dua (sebelah kiri) menunjukkan L.
nigrescens pada media kontrol dan tanda panah satu (sebelah
kanan) menunjukkan L. nigrescens pada media 100 μg L-1 (Contreras
et al., 2009).
Perubahan lain yang tampak pada Hypnea musciformis setelah terpapar 50
μM Cd secara anatomi tampak kehadiran bakteri endofit pada lapisan epidermis hingga lapisan sel kortek hingga spora endofit pada lapisan mucilage (ruang antar sel kortek). Pada konsentrasi 100 μM Cd, lapisan mucilage H. musciformis
mulai tertutupi oleh noda-noda hitam disertai penebalan pada dinding sel kortek dan sub kortek, memasuki konsentrasi 200 μM Cd, dinding sel kortek mulai terjadi kerusakan, volume sel sub kortek terlihat mengecil (keriput) disertai ruang
antar sel sub kortek yang menebal dan dipenuhi noda-noda hitam. Jumlah bakteri endofit yang semakin meningkat dan pada konsentrasi 300 μM Cd, terdapat penggumpalan noda-noda hitam di dalam sitoplasma sel kortek
menandakan Cd sudah masuk ke dalam sel dan terakumulasi pada cairan
Gambar 6 Penampang melintang talus H. Musciformis setelah terpapar Cd selama 7 hari. (A, B, C) sel H. Musciformis pada media kontrol. Tanda panah menunjukkan kehadiran alga endofit diantara sel kortikal (CC) dan spora endofit pada lapisan mucilage. (D) sel H. Musciformis pada media 50 μM Cd. Tanda panah menunjukkan alga endofit. (E) sel H. Musciformis pada media 100 μM Cd menunjukkan penipisan lapisan mucilage dan penebalan dinding sel. (F) sel H. Musciformis pada media 200 μM Cd, dinding sel rusak dan semakin menipisnya lapisan mucilage disertai meningkatnya jumlah spora endofit. (G, H) sel H. Musciformis pada media 300 μM Cd, tanda panah menunjukkan keberadaan logam Cd terjadi akumulasi pada daerah tersebut. (Bouzon et al., 2011).
Munculnya noda-noda hitam pada dinding sel dikarenakan interaksi yang
terjadi antara ion logam berat dengan senyawa-senyawa organik yang ada di
dinding sel. Alga merah akan meningkatkan produksi senyawa-senyawa organik
berupa polisakarida sulfonat (agar adalah senyawa organik pada jenis Gracilaria)
ketika logam berat memasuki sel dan mengikatnya serta mengakumulasinya
pada dinding sel (Diannelidis dan Delivopoulos, 1997).
2.4 Mekanisme Toksisitas dan Detoksifikasi Tembaga pada Makroalga
Toksisitas terjadi ketika tahapan detoksifikasi sudah tidak mampu lagi
mentoleransi keberadaan logam berat dalam talus. Beberapa mekanisme atau
tahapan yang terjadi pada talus makroalga ketika media kultivasi terlarut logam
[image:31.595.107.526.104.798.2]atas: (1) paparan/adsorbsi; (2) Absorpsi; (3) distribusi; (4) metabolisme; (5)
detoksifikasi (akumulasi/ekskresi); (6) interaksi; (7) efek toksik.
Proses adsorbsi adalah kemampuan zat menempel pada suatu
permukaan. Senyawa organik polisakarida berupa zat agar-agar disekresikan
Gracilaria untuk mengadsorbsi Cu dari media (Bouzon et al., 2011). Logam berat
atau nutrien dapat melakukan penetrasi ke dalam sel makroalga melalui seluruh
permukaan talusnya dalam bentuk kation, anion, atau senyawa organik (Bertrand
dan Poirier, 2005). Proses selanjutnya adalah absorbsi Cu ke dalam talus
makroalga yang terdiri dari tiga mekanisme yaitu transpor pasif (difusi), difusi
terfasilitasi, dan transport aktif (Lobban dan Harrison, 1997). Difusi adalah
mekanisme transpor zat mengikuti aliran cairan dari media dengan konsentrasi
tinggi ke media berkonsentrasi rendah. Mekanisme difusi dapat dilakukan
dengan dua cara, pertama dengan cara pertukaran ion (ion pada dinding sel
digantikan oleh ion-ion logam berat). Lapisan membran makroalga terdiri atas
lipid bilayer pada permukaannya yang mengandung lapisan pengikat ion-ion
yang akan diserap.
Membran sel tidak saja mengatur masuknya logam-logam ke dalam sel,
tetapi juga mengontrol mekanisme pembentukan ligan protein dalam sel
(Darmono, 1995) karena membran sel bersifat sukar dilalui (impermeabel ) oleh
ion-ion logam berat seperti Cu. Untuk dapat melintasi membran sel, ion logam
berat mengalami mekanisme difusi terfasilitasi dengan bantuan suatu enzim di
dalam membran sel yang disebut permease (Soemirat, 2005). Permease
berfungsi sebagai katalis sehingga dapat menggangu pasokan nutrien pada sel.
Proses kedua adalah pembentukan senyawa kompleks antara ion-ion logam
berat dengan gugus fungsional seperti karbonil, amino, thiol, hidroksi, fosfat, dan
hidroksi-karboksil secara bolak balik dan cepat (Lobban dan Harrison, 1997).
Membran sel juga mampu memompa ion logam berat berlawanan dengan
gradien konsentrasi (mekanisme transpor aktif) dengan menggunakan energi
yang didapat dai pemecahan ATP menjadi ADP oleh hidrolisa enzim permease.
Bila konsentrasi zat kecil, zat akan tetap berada di dalam sel (Soemirat, 2005).
Absorpsi racun ke dalam organel makroalga akan berlanjut dengan proses
distribusi zat ke seluruh organel. Distribusi ini sangat ditentukan oleh afinitas zat
terhadap organel dan spesifisitasnya. Telah dijelaskan di atas, tembaga berperan
penting dalam proses metabolisme, kovaktor sistem kerja enzim, dan berikatan
Sehingga selama fase pertumbuhan, Cu akan terdistribusi ke seluruh organel
makroalga untuk melaksanakan perannya. Namun apabila konsentrasi Cu sudah
melebihi batas toleransi pertumbuhan makroalga, Cu akan terdistribusi kedinding
sel, vakuola, dan apoplast (lapisan ruang antar sel/lapisan mucilage) (Bertrand
dan Poirier, 2005).
Tembaga yang telah terdistribusi akan mengalami proses metabolisme.
Metabolisme adalah transformasi zat akibat proses seluler. Pada umumnya
transformasi terjadi agar zat menjadi lebih polar sehingga lebih mudah
diekskresikan atau diakumulasikan (Soemirat, 2005). Transformasi atau
metabolisme terdiri atas dua fase yaitu fase I (reaksi penguraian sehingga zat
menjadi lebih reaktif terdiri dari reaksi oksidasi, reduksi, dan hidrolisis) dan fase II
(reaksi konyugasi agar mudah diekskresikan) dan reaksi tersebut terjadi di
beberapa organel yaitu retikulum endoplasma, mitokondria, dan sitoplasma
(Soemirat, 2005).
Masa pertumbuhan dengan konsentrasi Cu yang kecil akan dimanfaatkan
seluruhnya dalam proses metabolisme untuk menunjang proses pertumbuhan
makroalga. Namun apabila fase pertumbuhan selesai dan makroalga tetap
terpapar Cu dalam waktu yang lama maka proses konyugasi akan terjadi hingga
akumulasi, proses ini dinamakan detoksifikasi. Akumulasi merupakan
penumpukan zat dalam talus makroalga. Bila terjadi akumulasi, maka jumlah
yang diabsorpsi akan lebih besar daripada jumlah yang diekskresikan. Zat yang
terakumulasi adalah zat yang relatif tidak berubah karena metabolisme dan
disimpan dalam jaringan yang memiliki senyawa pengikat (chelating agent).
Logam berat terakumulasi dalam talus makroalga melalui mekanisme
spesifik yaitu proses absorpsi, transpor aktif atau difusi terfasilitasi, dan proses
pemangsaan (Neff, 2002). Konsentrasi logam berat dalam talus makroalga
merupakan fungsi dari kesetimbangan antara tingkat pengambilan (rate of
uptake) dengan tingkat pengeluaran (rate of excretion). Perbedaan dari kedua
sistem tersebut menjelaskan bahwa telah terjadi proses akumulasi logam berat
dan penyebarannya dalam talus makroalga (Neff, 2002).
Akumulasi terjadi karena logam berat dalam talus makroalga cenderung
membentuk senyawa komplek dengan zat-zat organik yang terdapat dalam talus
makroalga, sehingga logam berat terfiksasi dan tidak diekskresikan oleh
makroalga yang bersangkutan (Lobban dan Harrison, 1997). Beberapa senyawa
polisakarida, dan lemak yang terdapat di dalam makroalga relatif tinggi (Lobban
dan Harrison, 1997). Akumulasi dalam komponen sellular makroalga terjadi pada
dinding sel, phosphate-rich granules, lapisan lemak, vakuola, dan physodes,
senyawa organik spesifik pengikat logam seperti metalloprotein dan
phytochelatin (Andrade et al., 2004).
Beberapa proses detoksifikasi makroalga untuk mencapai kembali
homeostatis adalah mengakumulasi Cu pada dinding sel, mengekskresikan dan
menyimpan Cu dalam vakuola, dan mengikat Cu dengan enzim phytochelatin
(PCs) yang disintesa dari glutathione (Bertrand dan Poirier, 2005; Yruela, 2005).
Tahapan interaksi akan terjadi apabila kemampuan akumulasi dan detoksifikasi
melebihi daya toleransi makroalga sehingga Cu akan bersifat toksik bagi organel
dimulai dengan kemampuan antioksidan enzim yang sudah tidak mampu
menetralisir kerusakan oksidatif pada organel, merusak struktur enzim sehingga
menganggu proses metabolisme, mempengaruhi permeabilitas plasmalemma,
menyebabkan hilangnya ion K+ dari sel dan merubah ukuran volume sel,
menghalangi proses fotosintesis dengan melepaskan penggabungan elektron
transport ke NADP+, kerusakan permanen pada lamella kloroplas hingga
rusaknya struktur klorofil-a, dan kematian organisme (Lobban dan Harrison,
1997). Keseluruhan mekanisme toksisitas dipengaruhi oleh perubahan dalam
faktor fisika kimiawi misalnya, pH, suhu, kadar garam dan ciri-ciri fisiologi dan
perilaku dari organisme tersebut (Connel, 2005).
2.5 Penggunaan Makroalga sebagai Biota Uji Toksisitas
Penelitian toksikologi pada dasarnya bertujuan untuk mengevaluasi
konsentrasi bahan kimia dan lamanya pemaparan yang dapat menimbulkan
pengaruh tertentu (Hindarti, 1997). Uji toksisitas bertujuan untuk mengevaluasi
pencemaran perairan karena uji secara kimiawi dan fisika belum mencukupi
untuk menilai pengaruh bahan pencemar terhadap biota perairan. Karena
pengaruh-pengaruh tersebut tidak selalu berbahaya, maka prinsip dari uji
toksisitas adalah untuk mengidentifikasi bahan kimia yang dapat menimbulkan
dampak negatif bagi biota perairan seperti mortalitas dalam waktu pendek atau
panjang, respon akut, respon letal atau subletal, kerusakan sistem reproduksi,
dll.
Penggunan makroalga sebagai biota uji toksisitas logam berat pertama kali
alga merah berfilamen, Steele dan Thursby pada tahun 1970 mempublikasikan
biota uji dari alga merah yaitu C. parvula dan alga coklat dari kelompok Laminaria
dan Fucus, dan tahun 1980, Fletcher mempelajari alga hijau yaitu jenis
Enteromorpha. Dalam kurun waktu 40 tahun (1959-2000) telah tercatat 82 artikel
yang membahas mengenai uji toksisitas pada makroalga dengan total jenis yang
tercatat adalah 26 jenis berasal dari kelompok makroalga merah, 28 jenis dari
kelompok makroalga coklat, dan 11 jenis dari kelompok makroalga hijau dan
tembaga adalah komponen dari logam berat yang paling sering digunakan (41%)
dalam uji toksisitas (Eklund dan Kautsky, 2003).
Pertimbangan utama dalam pemilihan biota dalam uji toksisitas adalah
biota yang dipilih harus sensitif terhadap bahan yang akan digunakan dalam uji
toksisitas, berada dalam tingkatan trofik, kelimpahannya tinggi dalam suatu
perairan, dan tersedia sepanjang tahun, hidup pada zona intertidal (daerah yang
selalu dipengaruhi oleh pencemaran, bernilai ekonomis dan ekologis,
kemudahahan pemeliharan (ukuran yang tepat) dalam skala laboratorium,
resisten terhadap perubahan lingkungan, parasit, dan penyakit (Hindarti, 1997).
Satu spesies tertentu nampaknya tidak mungkin memenuhi semua kriteria
tersebut, namun kriteria tersebut dapat digunakan sebagai pedoman yang sangat
bermanfaat dalam menentukan pilihan biota yang akan digunakan dalam
pengujian. Makroalga adalah kelompok alga multiseluler yang dapat digunakan
sebagai biota uji dalam pengujian toksisitas berbagai bahan pencemar baik di
perairan estuarin maupun laut. Hal ini disebabkan makroalga memenuhi hampir
keseluruhan persyaratan sebagai biota uji yang telah disebutkan di atas (Eklund
3. METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan di beberapa laboratorium, yaitu Laboratorium
Fisiologi Tumbuhan Universitas Sumatera Utara, Laboratorium Kimia Dasar LIDA
Universitas Sumatera Utara, Laboratorium Kesehatan Ikan dan Lingkungan DKP
Propinsi Sumatera Utara dan berlangsung dari bulan Maret hingga Mei tahun
2011.
3.2 Alat dan Bahan
Alat dan bahan yang digunakan dalam penelitian ini dibagi menjadi dua
kategori. Alat dan bahan yang digunakan untuk pemeliharaan makroalga
Gracilaria edulis.disajikan pada Tabel 1.
Tabel 1 Alat dan bahan untuk pemeliharaan Gracilaria edulis.
Alat
Bahan Jenis Spesifikasi
Akuarium Bahan kaca uk. 40x20x20 cm3 Air laut alami filterisasi Air Pump Merk BS-410 Gracilaria edulis
Thermometer DO meter pH meter Refraktometer Colorimeter
Model gelas RST-03 (0-400 C) Merk Lutron DO-5509
Merk Hanna Merk S-Mill-E
Merk Hach model DR/890
Pecahan karang Aquades
Reagent 8039 Cadmium Reduction Reagent 8048 PhosVer 3 (Ascorbic Acid) Method
Alat dan bahan yang digunakan untuk pengukuran laju pertumbuhan,
konsentrasi klorofil-a, kualitas air, dan pengamatan histologi struktur talus
Tabel 2. Alat dan bahan untuk pengukuran laju pertumbuhan, konsentrasi klorofil-a, dan pengamatan struktur talus.
Alat
Bahan
Jenis Spesifikasi
Spektrofotometer Timbangan digital Labu ukur 100 ml Gelas beker Pipet ukur
Atomic Absorption Spectrometer Mortar Hot plate
Model Milton Roy Spectronic 20D Model WkrCB 3K0,5N
Brand 100 ml Pyrex 50 ml Pyrex 25 ml
Merk Shimadzu model AA-6300
Larutan HNO3
Aseton 80% Alkohol 70%
Tembaga bubuk (CuSO4.5H2O)
3.3 Persiapan Penelitian
3.3.1 Penentuan Konsentrasi Toksikan Cu
Studi literatur dan lapangan dilaksanakan untuk menentukan konsentrasi
Cu terlarut dalam perairan laut alami. Berdasarkan studi literatur dan latar
belakang di atas ditetapkan konsentrasi Cu yang akan diuji toksisitasnya pada
makroalga adalah Cu yang terlarut di Perairan Kepulauan Seribu (Perairan Pulau
Lancang dan Perairan Pulau Pari) dan hasil pengamatan lapangan, konsentrasi
Cu terlarut di perairan tersebut berkisar antara 0.01-0,4 ppm Cu sehingga dipilih
4 konsentrasi Cu sebagai perlakuan toksisitas logam berat terhadap Gracilaria
edulis (Tabel 3).
Tabel 3 Konsentrasi Cu sebagai konsentrasi toksikan terhadap makroalga
Toksikan Konsentrasi Cu (ppm) Keterangan
Tembaga (Cu)
0+0,01 Kontrol (air laut alami tanpa penambahan Cu) 0,01+0,03 Perlakuan 1 (air laut alami + Cu)
0,01+0,05 Perlakuan 2 (air laut alami + Cu) 0,01+0,49 Perlakuan 3 (air laut alami + Cu)
3.3.2 Penyediaan Makroalga
Bibit Gracilaria edulis diperoleh dari tambak budidaya rumput laut Dusun 4
Desa Selotong Kecamatan Secanggang Kabupaten Langkat Sumatera Utara.
Pemilihan lokasi relatif bebas dari kawasan industri sehingga diharapkan bibit
Gracilaria edulis diambil dari tanaman induk budidaya yang sehat dan segar
dengan cara memotong bagian ujung vegetatif kira kira 10-20 cm. Bagian ujung
tanaman dipilih karena bagian ini terdiri dari sel dan jaringan muda yang akan
memberikan pertumbuhan yang optimal (Indriyani dan Suminarsih, 2004).
3.3.3 Aklimatisasi Makroalga
Makroalga dicuci dibawah air mengalir untuk menghilangkan epifit yang
menempel pada talus setelah tiba di laboratorium. Setelah bersih, makroalga
segera dimasukkan ke dalam akuarium untuk proses aklimatisasi dengan tujuan
dapat beradaptasi dan hidup pada lingkungan media uji. Tiap hari dilakukan
penimbangan bobot basah makroalga, sampai hari ke-14 bobot makroalga stabil
atau tidak mengalami penurunan, kemudian dilakukan penimbangan bibit untuk
sampel uji toksisitas.
Bibit terendam seluruhnya dalam media, dengan menggunakan metode
dasar (bottom method) yang telah dimodifikasi sesuai keadaaan akuarium
(Alamsjah et al., 2009). Tiap akuarium dipelihara sebanyak 3 rumpun makroalga,
dan setiap rumpun beratnya 10 gram.
3.3.4 Pembuatan Larutan Stok
Larutan induk (stock solution) Cu dibuat dari Tembaga (II) sulfat
pentahidrat (CuSO4.5H2O) (Merck), formula pembuatan larutan induk adalah
sebagai berikut:
BM A
BM B x C………(1)
Keterangan :
Bm A = berat molekul senyawa CuSO4.5H2O
Bm B = berat molekul Cu
C = konsentrasi larutan induk yang diinginkan
3.3.5 Penyediaan Media Uji
Media uji menggunakan air laut murni sebanyak 10 liter dalam akuarium
kaca berukuran 40x20x20 cm3 dengan kandungan nitrat 0,55 ppm dan fosfat
0,07 ppm serta 0,01 ppm Cu. Nutrien dan konsentrasi Cu dalam media sudah
memenuhi dan tidak bersifat toksik pada kehidupan makroalga (Huang et al.,
sistem aerasi. Oksigen disalurkan dari aerator, lalu dimasukkan ke dalam
akuarium dengan menggunakan selang air yang diberi batu pemberat.
Pengaerasian dilakukan untuk membuat pergerakan air dalam akuarium
(Mamboya et al., 2007). Pergantian air media uji dilakukan 2 kali seminggu
(semistatik) untuk mempertahankan nutrien bagi makroalga dan konsentrasi Cu
[image:39.595.103.490.32.824.2](sebagai perlakuan toksisitas) tetap stabil hingga akhir penelitian.
Gambar 7 Skema akuarium terkontrol pada pemeliharaan Gracilaria edulis.
3.4 Perlakuan Penelitian
3.4.1 Rancangan Percobaan
Percobaan penelitian ini menggunakan rancangan acak kelompok (RAK)
terdiri atas satu faktor perlakuan kuantitatif tetap yaitu konsentrasi Cu yang
dibedakan menjadi 4 taraf yaitu 0,01 ppm sebagai kontrol, 0,04 ppm sebagai
perlakuan pertama, 0,06 sebagai perlakuan kedua, dan 0,5 sebagai perlakuan
ketiga sedangkan waktu pengamatan termasuk dalam kelompok atau blok
(Mattjik dan Sumertajaya, 2006). Bagan percobaan dapat digambarkan sebagai
berikut (Gambar 8).
P3 P1 P4 P2
P1 P4 P2 P3
P3 P1 P4 P2
Gambar 8 Pengacakan dan bagan percobaan RAK
P1 P3 P4 P2
P2 P3 P4 P1
Blok 2 (Hari ke-7)
Blok 3 (Hari ke-14) Blok 4 (Hari ke-21)
3.4.2 Pengamatan Percobaan
3.4.2.1 Parameter Kualitas Media
Kualitas air media disesuaikan dengan keadaan lingkungan tropis tempat
G. edulis hidup. Parameter kualitas air diusahakan tetap dan konstan antara
kontrol dan akuarium dengan logam berat Cu di dalamnya selama masa kultivasi
dengan salinitas berada dalam kisaran 30–31, suhu dengan kisaran 27–28 oC,
pH dengan kisaran 7–8, dan DO berada dalam kisaran 5–6 mg/l. Oleh karena itu,
parameter kualitas air pada seluruh akuarium termasuk kontrol tidak memiliki
respon toksik atau strees pada Gracilaria edulis. Pengamatan dilakukan 1 kali
dalam seminggu.
3.4.2.2 Parameter Respon Fisiologi
3.4.2.2.1 Laju Pertumbuhan
Pengamatan pertumbuhan diukur dalam beberapa tahap yaitu, (1)
menimbang bobot segar (basah) Gracilaria edulis menggunakan timbangan
digital dengan kepekaan 0,5 gram. Sebelum ditimbang, Gracilaria edulis
dikeringkan menggunakan kertas tisu agar tetesan air tidak mempengaruhi
penimbangan; (2) menghitung laju pertumbuhan spesifik (specific growth rate)
menurut Lobban dan Harrison (1997). Kedua tahapan dilakukan pada hari ke-0,
ke-7, ke-14, ke-21, dan ke-28.
SGR = ………...(1)
Keterangan :
SGR = laju pertumbuhan spesifik (SGR)
Nt = berat basah/biomassa pada waktu ke-t (gram)
No = berat basah/biomassa awal (gram)
t = waktu
3.4.2.2.2 Klorofil-a
Konsentrasi klorofil-a diukur menggunakan spektrofotometrik dan nilai yang
terbaca dikalkulasi menurut Arnon (1949) dalam Meeks (1974). Gracilaria edulis
dipotong dengan pisau dan ditimbang seberat 1 gram talus segar. Talus
kurang lebih selama 5 menit dan talus Gracilaria edulis menjadi partikel yang
sangat kecil, larutan tersebut disaring dengan kertas saring 0,22 μm dan
ditambahkan aseton sedikit demi sedikit, hingga ampas benar-benar berwarna
coklat muda. Filtrat tersebut kemudian dimasukkan ke dalam labu takar 50 ml,
dan ditambahkan aseton hingga volume ekstrak tepat 50 ml. Ekstrak ini siap
diukur dengan bantuan spektrofotometer.
Ekstrak tersebut dibaca pada panjang gelombang 663 nm dan 645 nm.
Angka digital yang ditunjukkan adalah angka skala absorban (OD/D = optical
density). Pengukuran dilakukan pada hari ke-7, ke-14, ke-21, dan ke-28.
Chl-a (mg L-1) = 12,7 x D663nm – 2,69 x D645 ………...……….. (2)
Keterangan :
Chl-a = konsentrasi klorofil-a dalam ekstrak (mg L-1)
D663nm = absorbansi pada spektrofotometri yang diperiksa pada panjang
gelombang 663 nm
D645nm = absorbansi pada spektrofotometri yang diperiksa pada panjang
gelombang 645 nm
3.4.2.2.3 Struktur Talus
Struktur talus diamati dalam 2 cara yaitu, pengamatan struktur talus secara
eksternal dan pengamatan struktur talus secara internal (dilakukan
pembedahan). cara pertama dilakukan secara visual dan dicatat perubahan yang
tampak pada masing-masing perlakuan dan pengambilan data dilakukan pada
akhir pengamatan (hari ke-28). Cara kedua membuat preparat segar atau
semipermanen dengan cara mengiris talus setipis mungkin dan diamati di bawah
mikroskop pada hari ke-14 dan ke-28. Tujuan dari pembuatan preparat segar
atau semipermanen adalah meminimalkan kerusakan dari struktur talus sehingga
kerusakan jaringan hanya dikarenakan terpaparnya logam berat Cu.
Preparat dilakukan di bawah mikroskop cahaya merk Boeco dengan micro
digital camera eyepiece (MDCE) dengan nomor produk 5A pada perbesaran100
dan 400 kali. Sel-sel talus diukur dengan mikrometer yang terpasang pada lensa
3.5 Analisa Data
Analisis terhadap laju pertumbuhan dan klorofil-a makroalga dilakukan
secara deskriptif dan melalui uji ragam (ANOVA). Persamaan umum model
rancangan tersebut adalah sebagai berikut :
Yij = μ + τi + βj + εij ………(1)
Keterangan:
Yij = nilai pengamatan pada perlakuan ke-i kelompok ke-j
μ = nilai tengah populasi
τi = pengaruh perlakuan τ taraf ke-i βj = pengaruh kelompok β taraf ke-j
εij = galat percobaan pada perlakuan ke-i kelompok ke-j
Hipotesis yang digunakan adalah :
1. Hipotesis perlakuan
H0 : pengaruh perlakuan tidak berbeda nyata
H1 : minimal ada 1 perlakuan yang memberikan pengaruh berbeda nyata
2. Hipotesis kelompok/blok
H0 : pengaruh kelompok tidak berbeda nyata
H1 : minimal ada 1 kelompok/blok yang memberikan pengaruh berbeda nyata
Apabila pengaruh perlakuan dan kelompok berbeda nyata dengan selang
kepercayaan 95 % (P<0,05), maka dilakukan uji lanjut Duncan (Mattjik dan
Sumertajaya, 2006).
4. HASIL DAN PEMBAHASAN
2.1 Hasil
4.1.1 Laju Pertumbuhan Spesifik
Laju pertumbuhan adalah persentase perbandingan antara bobot akhir dan
bobot awal per waktu sehingga laju pertumbuhan dipengaruhi oleh bobot awal
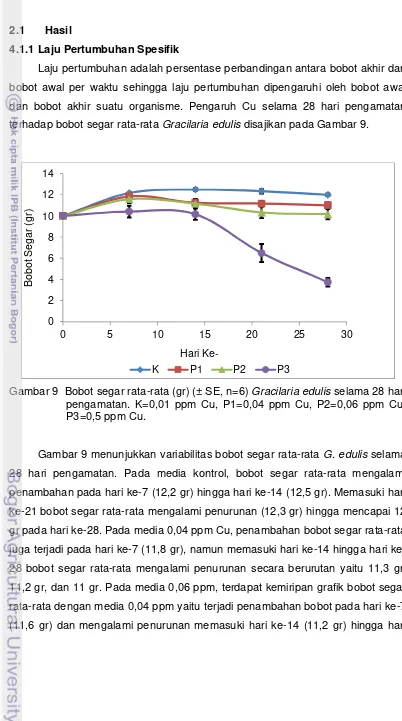
dan bobot akhir suatu organisme. Pengaruh Cu selama 28 hari pengamatan
[image:43.595.104.506.110.831.2]terhadap bobot segar rata-rata Gracilaria edulis disajikan pada Gambar 9.
Gambar 9 Bobot segar rata-rata (gr) (± SE, n=6) Gracilaria edulis selama 28 hari
pengamatan. K=0,01 ppm Cu, P1=0,04 ppm Cu, P2=0,06 ppm Cu, P3=0,5 ppm Cu.
Gambar 9 menunjukkan variabilitas bobot segar rata-rata G. edulis selama
28 hari pengamatan. Pada media kontrol, bobot segar rata-rata mengalami
penambahan pada hari ke-7 (12,2 gr) hingga hari ke-14 (12,5 gr). Memasuki hari
ke-21 bobot segar rata-rata mengalami penurunan (12,3 gr) hingga mencapai 12
gr pada hari ke-28. Pada media 0,04 ppm Cu, penambahan bobot segar rata-rata