PEMANFAATAN ADSORBEN JERAMI PADI YANG
DIAKTIVASI DENGAN HCl UNTUK MENYERAP LOGAM
Zn (II) DARI LIMBAH ELEKTROPLATING
SKRIPSI
WINDY TOBING
120822026
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATER UTARA
PEMANFAATAN ADSORBEN JERAMI PADI YANG
DIAKTIVASI DENGAN HCl UNTUK MENYERAP LOGAM
Zn (II) DARI LIMBAH ELEKTROPLATTING
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
WINDY TOBING 120822026
DEPARTEMEN MATEMATIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Pemanfaatan Adsorben Sebagai Jerami Padi yang Diaktivasi Dengan HCl
Untuk Menyerap Logam Zn (II) Dari Limbah Elektroplatting
Kategori : Skripsi
Nama : Windy Tobing Nomor Induk Mahasiswa : 120822026
Program Studi : Kimia Ekstensi S1 Departemen : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Univesitas Sumatera Utara
Disetjui di Medan, April 2015
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Dr.Andriyani, M.Si Dra.Saur Lumbanraja, M.Si NIP.196903021999032001 NIP.195506231986012002
Disetujui Oleh:
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PEMANFAATAN ADSORBEN JERAMI PADI YANG
DIAKTIVASI DENGAN HCl UNTUK MENYERAP LOGAM
Zn (II) DARI LIMBAH ELEKTROPLATTING
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Februari 2015
PENGHARGAAN
Puji dan syukur kita panjatkan kepada Tuhan Yang Maha Esa yang telah memberikan berkat dan kesempatan untuk penulis, sehingga dapat menyelesaikan penyusunan skripsi.
Dalam penulisan ini, penulis banyak mendapat bantuan dari berbagai pihak. Maka kesempatan ini penulis mengucapkan terima kasih yang sebesar-besarnya kepada, Ibu Dra. Saur Lumbanraja, M.Si selaku dosen pembimbing 1, Ibu Dr.Andriayani, M.Si selaku dosen pembimbing 2 yang telah memberikan arahan kepada penulis dalam menyelesaikan skripsi ini. Kepada Orangtua saya W.L.Tobing,ST dan E.Br Pardede yang memberikan doa dan dukungan materi maupun moril kepada penulis.Ibu Rumondang Bulan selaku Ketua Departemen, Bapak Dr. Darwin Yunus ,MS selaku ketua prodi kimia ekstensi, dan teman-teman stambuk 2012.
Medan, April 2015
Penulis
PEMANFAATAN ADSORBEN JERAMI PADI YANG
DIAKTIVASI DENGAN HCl UNTUK MENYERAP LOGAM
Zn (II) DARI LIMBAH ELEKTROPLATTING
ABSTRAK
UTILIZATION OF OF RICE STRAW ADSORBENT ACTIVATED BY HCl AT pH VARIATION FOR Zn METAL ABSORPTION ELECTOPLATING
WASTE
ABSTRACT
Have done absorption of zinc metal (Zn) from wastewater using adsorbents
elektroplatting derived from rice straw with rice straw delignification first using 3% NaOH solution at 70 ° C were analyzed by FT-IR spectrophotometry showed that the analysis of adsorbent tape uptake 3367.71 cm-1 shows the -OH groups of the
DAFTAR ISI 2.1.2.Jerami Padi Sebagai Penyerap Logam Berat dalam Air 6 2.2. Selulosa 7 2.2.1. Sifat-Sifat Selulosa 8 2.3. Pencemaran Lingkungan Akibat Limbah Indsutri 8 2.4.Toksisitas Logam Berat 10 2.5. Seng 11 2.5.1.Sifat Fisika dan Kimia Seng 13
2.5.2.Fungsi dari Seng 14
2.6 Adsorpsi 15
2.6.1.Pembagian Adsorpsi 15 2. 6.1.1.Adsorpsi Fisika 15 2.6.1.2.Adsorpsi Kimia 15 2.6.2.Faktor yang mempengaruhi adsorpsi 16 2.7. Spektrometri FT-IR(Fourier Transform Infrared) 17 2.8.Spektrofotometri Serapan Atom 18 2.8.1.Prinsip Dasar Spektrofotometri Serapan Atom 19 2.8.2.Instrumentasi SSA Nyala Berkas Tunggal 19 2.8.2.1.Tabung Katoda Berongga 20
2.8.2.2.Nyala 20
2.8.2.3.Monokromator 21
2.8.2.4.Detektor 21
2.8.2.6.Read Out 22 2.8.3.Gangguan-gangguan Spektrofotometri Serapan Atom 22 2.8.4.Aplikasi Spektrofotometri Serapan Atom 23 Bab 3. Metode Penelitian 24
3.1. Alat 24
3.2.Bahan 25
3.3. Prosedur Percobaan 25
3.3.1. Pembuatan Adsorben 25 3.3.1.1. Pembuatan Serbuk Jerami Padi 25 3.3.1.2. Pembuatan Serbuk Jerami Padi Terdelignifikasi 25 3.3.1.3. Akivasi Adsorben dengan HCl 26 3.3.1.4. Penentuan pH Adsorpsi Pada Limbah Elektroplatting 26
3.4. Bagan Penelitian 27
3.4.1. Pembuatan Adsorben 27 3.4.1.1.PembuatanSerbuk Jerami Padi 27 3.4.1.2.Pembuatan Serbuk Jerami Padi Terdelignifikasi 27 3.4.1.3.Aktivasi Adsorben Dengan HCl 28 3.4.1.4.Penentuan Variasi pH Adsorpsi Zn Pada Limbah Elektroplating 29
Bab 4. Hasil dan Pembahasan
4.1. Hasil Penelitian 30
4.1.1.Preparasi Sampel 30 4.1.2.Pembuatan Serbuk Jerami Padi Terdelignifikasi 31 4.1.3.Pengambilan Sampel 31
4.3. Pembahasan 39
Bab 5. Kesimpulan dan Saran
5.1.Kesimpulan 40
5.2.Saran 40
DAFTAR TABEL
Nomor Tabel Judul Halaman
1 Interpretasi gugus fungsi senyawa hasil analisis FT-IR 31 dari adsorben jerami padi sebelum didelignikasi
2 Interpretasi gugus fungsi senyawa hasil analisis FT-IR 32 dari adsorben jerami padi sesudah didelignikasi
3 Data Konsentrasi Awal logam Zn dari limbah elektroplatting 33
4 Konsentrasi Logam Seng dalam limbah cair elektroplattinng 34 pada variasi pH dengan menggunakan aktivasi HCl 0.2M dan sesudah penambahan adsorben jerami padi
5 Konsentrasi Logam Seng dalam limbah cair elektroplattinng 35 pada variasi pH dengan menggunakan aktivasi HCl 0.6M dan sesudah penambahan adsorben jerami padi
DAFTAR GAMBAR
Nomor
Gambar Judul Halaman
DAFTAR LAMPIRAN
Nomor Judul Halaman Lampiran
PEMANFAATAN ADSORBEN JERAMI PADI YANG
DIAKTIVASI DENGAN HCl UNTUK MENYERAP LOGAM
Zn (II) DARI LIMBAH ELEKTROPLATTING
ABSTRAK
UTILIZATION OF OF RICE STRAW ADSORBENT ACTIVATED BY HCl AT pH VARIATION FOR Zn METAL ABSORPTION ELECTOPLATING
WASTE
ABSTRACT
Have done absorption of zinc metal (Zn) from wastewater using adsorbents
elektroplatting derived from rice straw with rice straw delignification first using 3% NaOH solution at 70 ° C were analyzed by FT-IR spectrophotometry showed that the analysis of adsorbent tape uptake 3367.71 cm-1 shows the -OH groups of the
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Di Indonesia, jerami padi belum dinilai sebagai produk yang memiliki nilai
ekonomis. Petani membiarkan siapa saja untuk mengambil jerami padi dari lahan
sawahnya. Di beberapa daerah, petani bahkan senang bila sawahnya bebas dari jerami
padi. Pada sistem usaha tani yang intensif, jerami padi sering dianggap sebagai sisa
tanaman yang mengganggu pengolahan tanah dan penanaman padi. Oleh karena itu,
75 - 80% petani membakar jerami padi di tempat, beberapa hari setelah dipanen
(Makarin, 2007).
Adapun kandungan dari jerami padi ialah lignoselulosa yang terdiri dari tiga
komponen fraksi serat, yaitu selulosa 32,1%, hemiselulosa 24%, lignin 18%, dan juga
mengandung silika (Howard, 2003).
Menurut Redi dan Yang (2006) juga menyatakan bahwa komposisi jerami padi terdiri
dari 40% selulosa, 30% hemiselulosa, 15% silika dan 15% lignin.
Jerami padi dapat di fungsikan sebagai bahan adsorben logam berat. Bahan ini
relatif murah dalam menanggulangi pencemaran logam berat dalam air (Kohar dan
Setyaningrum, 2007).
Pada penelitian sebelumnya telah digunakan adsorben jerami padi untuk
pengolahan limbah logam berat Pb (II) dengan menggunakan NaOH 3% yang
diaktivasi dengan HNO3 dan pH limbah serta waktu kontak divariasikan. hidroksida.
Derajat keasaman pada limbah berfungsi untuk mempengaruhi spesies logam yang
terdapat dalam limbah (Safrianti dkk, 2012). Juga telah dilakukan penelitian untuk
pengolahan limbah Cd dengan menggunakan NaOH 2%
Menurut Maryeni pengolahan limbah elektroplating dapat dilakukan seacar fisika dan
kimia. Jenis pengolahan limbah elektroplating dilakukan tergantung dari
karakteristik senyawa-senyawa yang ada pada limbah cair. Pengolahan limbah
elektroplating yang dilakukan dengan cara netralisasi dengan asam klorida, mengatur
pH dari 8-10 limbah dengan penambahan larutan natrium hidroksida, penambahan
koagulan berupa tawas untuk mempercepat terbentuk gumpalandan endapan.
Pengolahan limbah dengan metode sedimentasi dan koagulasi didasarkan pada
prinsip bahwa logam-logam dalam limbah cair elektroplating dapat diendapkan
dengan netralisasi menggunakan kapur atau natrium hidroksida. Pengendapan
berlangsung antara pH 8.5-9.5 (Purwanto dan Huda, 2005).
Zat-zat pencemar merupakan senyawa yang tidak diinginkan dalam
lingkungan hidup. Bahan-bahan pencemar itu tergolong zat organik dan anorganik.
Diantara zat-zat pencemar anorganik maka logam berat seperti zinkum (Zn)
mendapatkan perhatian yang lebih banyak (Widowati, 2008).
Didalam tubuh manusia terdapat Zn kira-kira 2,3 g dan hanya dapat menyerap
20 - 40% Zn dari makanan sehingga dapat dicukupi dengan minuman yang diperkaya
dengan Zn. Kelebihan Zn dapat menyebabkan mual, muntah, pusing, mulas/sakit
perut, demam, diare (Widowati, 2008).
Mengingat dampak yang ditimbulkan oleh logam Zn tersebut, maka
diperlukan suatu upaya untuk mengurangi kadarnya. Adsorpsi merupakan salah satu
metode yang dapat digunakan untuk mengurangi kadar seng. Keuntungan dengan
menggunakan metode adsorpsi lebih murah tidak menimbulkan efek samping beracun
dan efektif pada konsentrasi logam yang rendah (Igwe dan Abla, 2007).
Berdasarkan hal tersebut peneliti ingin menggunakan adsorben jerami padi
tersebut untuk pengolahan limbah elektroplating yang mengandung logam Zn
dengan menggunakan NaOH 3%, kemudian diaktivasi dengan menggunakan HCl dan
1.2. Permasalahan
Bagaimana pengaruh aktivasi HCl terhadap jerami padi dalam menurunkan kadar
logam Zn dalam limbah electroplating, dan berapakah pH optimum dari limbah yang
dapat terserap oleh adsorben tersebut.
1.3. Pembatasan Masalah
1. Jerami padi diperoleh dari desa Saitnihuta, Tarutung
2. Adsorben jerami padi diperoleh dengan cara didelignifikasi kemudian
diaktivasi dengan menggunakan asam klorida
3. Penyerapan limbah elektroplating yang mengandung logam Zn diperoleh
dengan metode adsorpsi
1.3. Tujuan Penelitian
- Untuk membuat adsorben jerami padi yang teraktivasi HCl 0.2M, 0.6M dan
1M
- Untuk mengetahui daya serap adsorben yang berasal dari jerami padi yang
diaktivasi dengan HCl terhadap limbah elektroplating yang mengandung
logam Zn
- Untuk mengetahui penurunan kadar logam Zn yang terdapat pada limbah
elektroplating dengan menggunakan adsorben yang berasal dari jerami padi.
1.4. Manfaat Penelitian
Hasil Penelitian diharapkan dapat memberikan informasi mengenai peranan jerami
padi sebagai penyerap logam berat Zn dalam pengolahan limbah industri
elektroplating.
1.5. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Ilmu Dasar Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara Medan. Lokasi Pengujian limbah
dilakukan di Badan Riset dan Standarisasi Industri (BARISTAN) Medan. Pengujian
FT-IR dilakukan di Laboratorium Penelitian Fakultas Farmasi.
1.6. Metode Penelitian
Penelitian ini bersifat eksperimen laboratorium. Lokasi pengambilan sampel jerami
padi dari desa Saitnihuta Tarutung Metode Pengambilan sampel jerami padi dan
sampel limbah elektroplating dilakukan secara acak . Adsorben jerami padi dibuat
dengan cara mendelignifikasikan jerami padi dengan menggunakan NaOH 3% dan
pengeringan pada suhu 70°C hasilnya dianalisa dengan FT-IR, yang selanjutnya
diaktivasi dengan menggunakan asam klorida (HCl) dengan konsentrasi yang berbeda
yaitu 0,2 M, 0,6 M, dan 1M. Limbah elektroplating kemudian ditambahkan dengan
adsorben jerami padi kemudian disaring, filtratnya di analisa dengan menggunakan
Spektrofotometri serapan atom untuk mengetahui daya serap dan penurunan kadar
BAB 2
TINJAUAN PUSTAKA
2.1. Jerami Padi
Tanaman padi memiliki batang yang beruas-ruas. Panjang batang tergantung pada
jenisnya. Pada jenis unggul biasanya berbatang pendek atau lebih pendek daripada
jenis lokal, sedangkan jenis padi yang tumbuh di tanah rawa dapat lebih panjang lagi,
yaitu antara 1-2 meter. Biasanya setelah panen hasil, batang padi tidak dipergunakan
lagi dan dibuang begitu saja sehingga menjadi kumpulan jerami padi yang tidak
berguna lagi. Jerami tersebut kebanyakan terdiri dari batang padi, tetapi ada juga
terdapat ujung daunnya.
Setelah padi dipanen, bulir padi atau gabah dipisahkan dari jerami padi.
Perbandingannya yang dapat diperoleh antara gabah dan jerami tergantung dari
varietas padi biasanya adalah 1: 1 atau 1: 1.25.
Jerami adalah tanaman padi yang telah diambil bulirnya (gabahnya) sehingga
tinggal batang dan daunnya yang merupakan limbah pertanian terbesar. Jerami
sebagai limbah pertanian sering menjadi permasalahan bagi petani sehingga sering
dibakar untuk mengatasi masalah tersebut. Di beberapa daerah di Indonesia, jerami
diangkut seluruhnya untuk pakan ternak, pembuatan kertas dan lain-lain
2.1.1. Sifat Jerami Padi
Jerami padi terdiri atas daun, pelepah daun, dan ruas atau buku. Ketiga unsur ini
relatif kuat karena mengandung silika, dan selulosa yang tinggi dan pelapukannya
memerlukan waktu yang lama. Namun, apabila jerami padi diberi perlakuan tertentu
akan mempercepat terjadinya perubahan strukturnya (Kohar dan Setyaningrum,
2007). Kandungan dari Jerami Padi ialah lignoselulosa yang terdiri dari tiga
komponen fraksi serat yaitu selulosa 32,1%, hemiselulosa 24%, dan lignin 18%.
Disamping itu juga jerami padi mengandung silika (Howard,2003). Menurut Reddy
dan Yang (2006) bahwa komposisi dari jerami padi terdiri dari 40% selulosa, 30%
hemiselulosa, 15% silika dan 15% lignin.
2.1.2. Jerami Padi sebagai Penyerap Logam Berat dalam Air
Logam berat dalam air merupakan bahan pencemar yang membahayakan kesehatan
manusia dan ternak bila terkonsumsi atau terkena kulit. Dengan semakin tinginya
peluang tercemarnya air (air minum ataupun air mandi) maka perlu upaya mencegah
penemaran dan membersihkan air yang sudah tercemari. Bahan yang relatif murah
dan mudah digunakan untuk mengeliminasi atau mengurangi pencemaran logam
berat dalam air adalah sekam dan jerami padi. Sekam dan jerami padi diolah dengan
NaOH 1%, 2%, 3%, 4%. Perlakuan jerami padi dengan NaOH 2% dengan waktu
perendaman 1 jam menunjukkan aktivitas penyerapan Cd yang paling tinggi. Sekam
padi pada umumnya menunjukkan aktivitas penyerapan yang lebih rendah
dibandingkan dengan jerami, baik untuk Cd maupun Pb. Persentase terserap tertinggi
untuk Pb didapat dari konsentrasi jerami padi 3% dan 4% dan didiamkan selama 4
jam(Kohar dan Setyaningrum, 1999).
2.2. Selulosa
Komponen utama penyusun jaringan dinding sel tumbuhan pada umumnya adalah
selulosa. Selulosa adalah polimer alam berupa zat karbohidrat (polisakarida) yang
Selulosa mempunyai rumus molekul 2(C6H10O5)n, dengan n adalah derajat
polimerisasi. Panjang suatu rangkaian selulosa tergantung pada derajat
polimerisasinya. Semakin panjang suatu rangkaian selulosa, maka rangkaian selulosa
tersebut mempunyai serat yang lebih kuat, lebih tahan terhadap pengaruh bahan
kimia, cahaya, dan mikroorganisme.
Selulosa dapat dibedakan menjadi:
a. α Selulosa
Selulosa untuk jenis ini tidak dapat larut dalam larutan NaOH dengan kadar 17,5%
pada suhu 20ºC dan merupakan bentuk sesunguhnya yang telah dikenal sebagai
selulosa.
b. ß Selulosa
jenis dari selulosa ini mudah larut dalam larutan NaOH yang mempunyai kadar
17,5% pada suhu 20ºC dan tidak akan mengendap bila larutan tersebut berubah
menjadi larutan yang memiliki suasana asam.
c. ɤ Selulosa
untuk selulosa jenis ini mudah larut dalam larutan NAOH yang mempunyai kadar
17,5% pada suhu 20ºC tidak akan terbentuk endapan setelah larutan tersebut
dinetralkan.
Alpha selulosa sangat menentukan sifat tahanan kertas, semakin banyak kadar
alpha selulosanya menunjukkan semakin tahan lama kertas tersebut. Dan memiliki
sifat hidrofilik yang lebih besar pada gamma dan beta selulosa daripada alpha
selulosanya (Fengel dan Wegner, 1995).
2.2.1. Sifat-Sifat Selulosa
Sifat-sifat selulosa terdiri dari sifat fisika dan sifat kimia. Selulosa dengan rantai
panjang mempunyai sifat fisik yang lebih kuat, lebih tahan lama terhadap degradasi
yang disebabkan oleh pengaruh panas, bahan kimia maupun pengaruh biologis. Sifat
fisika dari selulosa yang penting adalah panjang, lebar dan tebal molekulnya. Sifat
a. Dapat terdegradasi oleh hidrolisa, oksidasi, fotokimia maupun secara mekanis
sehingga berat molekulnya menurun.
b. Tidak larut dalam air maupun pelarut organik, tetapi sebagian larut dalam larutan
alkali.
c. Alam keadaan kering, selulosa bersifat higroskopis, keras dan rapuh. Bila selulosa
cukup banyak mengandung air maka akan bersifat lunak. Jadi fungsi air disini
adalah sebagai pelunak.
d. Selulosa dalam Kristal mempunyai kekuatan lebih baik jika dibandingkan dengan
amorfnya (Fengel dan Wengner, 1995).
2.3. Pencemaran Lingkungan Akibat Limbah Industri
Pencemaran atau polusi adalah suatu kondisi yang telah berubah dari bentuk asal
kekeadaan yang lebih buruk. Pergeseran bentuk tatanan dan kondisi asal pada kondisi
yang buruk ini dapat terjadi sebagai akibat masuknya bahan-bahan pencemar atau
polutan. Bahan polutan tersebut pada umumnya mempunyai sifat racun (toksik) yang
berbahaya bagi organisme hidup. Toksisitas atau daya racun dari polutan itulah yang
kemudian menjadi pemicu terjadinya pencemaran (Palar, 2004).
Suatu lingkungan hidup dikatakan tercemar apabila telah terjadi
perubahan-perubahan dalam tatanan lingkungan itu sehingga tidak sama lagi dengan bentuk
asalnya. Perubahan yang terjadi itu memberikan dampak yang buruk terhadap
organisme yang sudah ada. Dan pada tingkat lanjut dalam arti jika lingkungan sudah
tercemar dalam tingkat tinggi, dapat membunuh bahkan memusnahkan satu atau lebih
jenis organisme. Jadi pencemaran lingkungan adalah terjadinya perubahan dalam
tatanan lingkungan dari bentuk asli kearah yang lebih buruk (Palar, 2004).
Perkembangan ekonomi di Indonesia menitik beratkan pada pembangunan di
sektor industri. Di satu sisi pembangunan akan meningkatkan kualitas hidup manusia
menurunkan kesehatan masyarakat dikarenakan pencemaran yang berasal dari limbah
industri (Widowati, 2008).
Proses industri pada akhirnya akan menghasilkan limbah baik dalam bentuk
padat maupun cair. Limbah dikatakan berbahaya jika menimbulkan dampak yang
negatif bagi kesehatan manusia. Logam berat pada limbah industri dapat berasal dari
bahan baku maupun dari bahan pendukung pada proses industri.
Pencemaran yang disebabkan oleh buangan industri baik dalam bentuk unsur
maupun persenyawaan logam berat merupakan toksik yang mempunyai daya racun
yang sangat tinggi. Polutan ini akan mencemari lingkungan, baik melalui udara,
tanah, dan air (Palar, 2004).
Pencemaran air terjadi apabila substansi kondisi (termasuk panas)
menurunkan kualitas badan air sehingga air tidak dapat memenuhi kualitas standar
atau tidak dapat digunakan untuk tujuan tertentu. Pencemaran logam berat yang ada
di lingkungan tanah, air udara dengan suatu mekanisme masuk kedalam mahluk
hidup. Logam berat yang masuk kedalam tubuh manusia akan melakukan interaksi
antara lain dengan enzim, protein, DNA, serta metabolit lainnya. Adanya logam berat
dalam tubuh jelas akan berpengaruh terhadap tubuh. Bila jumlahnya berlebih, maka
akan berbahaya bagi tubuh. Pencemaran logam berat ke lingkungan dilalui dari air.
Pencemaran air terjadi pada sumber-sumber air danau, sungai, laut dan air tanah yang
disebabkan oleh aktifitas manusia. Air dikatakan tercemar jika tidak dapat digunakan
sesuai dengan fungsinya. Pencemaran ini dapat disebabkan oleh limbah industri,
perumahan, pertanian, rumah tangga. Polutan industri antara lain polutan organik dan
polutan anorganik, sisa bahan bakar dan tumpahan minyak tanah merupakan sumber
pencemaran air terutama air tanah. Polutan dalam air mencakup unsur-unsur kimia,
pathogen, dan perubahan sifat fisika dan kimia dalam air. Banyak unsur kimia
merupakan racun yang mencemari air. Pencemaran air merupakan masalah regional
penggunaan lahan tanah atau daratan. Pencemaran air terdiri dari bermacam-macam
jenis, dan pengaruhnya terhadap lingkungan dan mahluk hidup. Salah satu penyebab
pencemaran air adalah keberadaan bahan kimia anorganik seperti Pb, Cd, Hg dalam
kadar yang tinggi menyebabkan air tidak enak untuk dikonsumsi. Pencemaran logam
berat diperairan banyak bersumber dari pertambangan, peleburan logam, dan jenis
industri lainnya. Logam berat biasanya ditemukan sangat sedikit sekali dalam air
secara alamiah yaitu kurang dari 1µg/L. Untuk menentukan kualitas air tehadap
konsentrasi logam dalam air, agak sulit karena erat hubungannya dengan partikel
tersuspensi yang terlarut didalamnya. Konsentrasi logam toksik seperti Cd, Pb, Hg,
dan As dalam perairan secara alamiah sangat kecil (Masduki, 2004).
2.4. Toksisitas Logam Berat
Logam berat mempunyai kriteria yang sama dengan logam-logam lain. Perbedaannya
terletak pada pengaruh yang dihasilkan oleh logam berat ini jika berikatan atau masuk
ke dalam tubuh organisme hidup, sehingga akan menimbulkan pengaruh-pengaruh
buruk terhadap fungsi fisiologis tubuh.
Kerja utama logam adalah menghambat kerja enzim. Efek ini timbul akibat
interaksi antara logam dengan gugus S-H pada enzim. Fungsi enzim juga dapat
terhambat oleh logam toksik melalui penggusuran kofaktor logam yang penting dari
enzim (Frank, 1994).
Umumnya, efek toksik logam merupakan akibat dari reaksi antara logam dan
komponen intrasel. Setelah masuk kedalam sel, logam dapat mempengaruhi berbagai
organel seperti retikulum endoplasma yang mengandung berbagai jenis enzim.
Logam-logam toksik ini akan merusak struktur dari enzim dan menghambat
2.5. Limbah Elektroplating
Elektroplating adalah pelapisan logam dengan menggunakan teknik elektrokimia atau
elektrolisa. Secara teknis elektroplating disebut juga sebagai pelapis listrik, yaitu
proses pengendapan logam dalam ion logam yang dialirkan oleh arus listriksearah
melalui elektroda dalam larutan elektrolit dari kutub anoda ke kutub katoda. Logam
yang akan dilapisi biasanya berbentuk produk logam, atau disebut juga sebagai benda
kerja. Dalam praktek, benda kerja atau produk logam yang akan dilapis dihubungkan
dengan katoda. Selama arus listrik searah mengalir dari anoda ke katoda maka ion
logam dalam larutan elektrolit akan menuju ke katoda dan terkumpul pada benda
kerja. Dengan proses tersebut benda kerja atau produk logam akan dilapisi dengan
logam yang dikehendaki. Umumnya produk logam bisa dilapisi dengan menggunakan
emas, nikel, tembaga, seng, kuningan, perak, krom atau logam lainnya. Produk
industri yang membutuhkan pelapisan logam antara lain adalah peralatan rumah
tangga yang terbuat dari besi, kuningan, dan aluminium. Biasanya produk seperti
meja, kursi, sendok makan dan alat dapur lainnya dilapisi dengan menggunakan
logam nikel dan krom. Tujuannya agar produk yang dihasilkan tahan korosi, lebih
memperhalus permukaan, atau untuk tujuan khusus seperti meningkatkan daya hantar
listrik atau panas dan meningkatkan mutu penampilannya.(Anonim, 2002)
Limbah industri elektroplating berasal dari bahan-bahan kimia yang
digunakan dan hasil dari proses pelapisan. Bahan-bahan kimia yang digunakan adalah
bahan beracun sehingga limbah yang dihasilkan berbahaya bagi kesehatan manusia
baik yang terlibat langsung dengan kegiatan industri maupun yang di sekitar
perusahaan.
Jenis Limbah Dan Bahayanya
1. Limbah Asam
Asam dapat menyebabkan luka pada kulit, selaput lendir, selaput mata
2. Limbah Basa
Bahan-bahan basa seperti amonium hidroksida, potassium hidroksida,
sodium
hidroksida, sodium sianida, sodium karbonat, sodium pryophospat,
sodium silikat dan trisodium phispat tidak begitubahaya bagi sistem
saluran pernafasan, tetapi dapat mengiritasi kulit.
3. Limbah Garam dan Senyawa lainnya
Sianida sangat beracun, dan dapat mematikan bila tertelan. Menyebabkan
iritasi kerongkongan, pusing-pusing, mabuk, mual, lemah dan sakit
kepala dan bahkan berhenti bernafas (Anonim, 2002)
2.6. Zink (Zn)
2.6.1.Sifat Fisika Zink
Zink merupakan salah satu unsure kimia dengan simbol Zn, nomor atom 30 dan
menempati tempat pertama pada golongan XII unsur transisi di dalam tabel periodik
unsur. Secara kimia, zink memiliki sifat yang mirip dengan magnesium (Mg) karena
memiliki ukuran atom yang hamper sama dengan bilangan oksidasi +2. Zink
memiliki warna putih kebiru-biruan, berkilau, dan bersifat diamagnetik. Logam ini
cukup mudah untuk di tempa, dan dapat dilihat pada suhu 110-150°C. zink melebur
pada suhu 410°C dan mendidih pada 906°C. dibandingkan dengan logam-logam
lainnya, zink memiliki titik lebur dan titik didih yang terendah diantara semua
logam-logam transisi. Produksi terbesar zink ada di Australia, Kanada, Peru, dan Amerika
(Vogel, 1991).
Zink sedikit kurang padat daripada besi dan berstruktur Kristal heksagonal.
Hal ini menyebabkan mutu komersial Zn tidak berkilau. Logam ini keras dan rapuh
pada berbagai suhu, namun menjadi dapat ditempa antara 100 sampai 150°C, diatas
210°C, logam ini kembali menjadi rapuh dan dapat dihancurkan menjadi bubuk
dengan cara memukul logam tersebut. Pada umumnya, zink berada di alam dalam
Zink digunakan secara luas untuk menyepuh logam-logam lain dengan listrik
seperti besi untuk menghindari karatan. Zink sulfida digunakan dalam membuat
tombol bercahaya, sinar x, kaca-kaca TV, dan bola-bola lampu (Vogel,1991).
2.6.2. Sifat Kimia Zink
Sifat kimiawi zink mirip dengan logam-logam transisi periode pertama seperti nikel
dan tembaga. Zink bersifat diamagnetik dan berwarna putih kebiru-biruan. Jari-jari
ion zink dan magnesium juga hamper identik. Oleh karenanya, garam kedua senyawa
ini akan memiliki struktur Kristal yang sama. Pada kasus ini jari-jari ion merupakan
faktor penentu, sifat-sifat kimiawi keduanya akan sangat mirip. Zink cenderung
membentuk ikatan kovalen berderajat tinggi. Zink juga akan membentuk senyawa
kompleks dengan kebanyakan berkoordinasi 4 ataupun 6 walaupun koordinasi 5 juga
diketahui ada (Shriver, 1999).
Zink memiliki konfigurasi elektron [Ar]3d104S2 dan merupakan unsure golongan 12 tabel periodik. Zink cukup reaktif dan merupakan reduktor kuat.
Permukaan logam zink murni akan dengan cepat mengusam, membentuk lapisan zink
karbonat, Zn5(OH)6CO3, dan akan bereaksi dengan karbon dioksida. Lapisan ini
membantu mencegah reaksi lebih lanjut dengan udara dan air. Zink bereaksi dengan
asam, basa dan non-logam lainnya. Zink yang sangat murni hanya akan bereaksi
secara lambat dengan air yang ada dan akan melepaskan gas hidrogen (Shriver,
1999).
Zink akan larut dengan natrium hidroksida membentuk endapan seperti gelatin yang
putih. Endapan larut dlam asam:
Zn2+(aq) + 2NaOH(l) Zn(OH)2(s)
Dengan larutan amoniak terbentuk endapan putih
Dengan larutan amonium sulfida terbentuk endapan putih
Zn2+(aq) + S2-(aq) ZnS(s)
Dengan asam sulfat pekat panas, zink akan melepaskan belerang dioksida
Zn2+(aq) + 2H2SO4(l) Zn2+
(aq) + SO2(g) + SO4(aq)2- + 2H2O(l)
Pelarutan akan terjadi dalam asam nitrat yang encer dan tidak ada gas yang
dilepaskan:
4Zn(s) + 10 H+(aq) + NO3(aq) 4Zn2+(aq)+ NH4(aq) + 3H2O(aq)
Dengan bertambah pekatnya konsentrasi asam nitrat, akan terbentuk dinitrogen
oksida (N2O), nitrogen oksida (NO):
4Zn(s) + 10 H+(aq) + 2NO3(aq) 4Zn2+
(aq)+ N2O(g) + 5H2O(l)
3Zn(s) + 8 HNO3(l) 3Zn2+(aq)+ 2NO(g) + 6NO3(aq) + 4H2O(l)
2.6.3. Fungsi Dari Zink
Zink banyak digunakan pada pelapisan baja dan besi untuk mencegah korosi dan juga
sebagai bahan pembuatan alloy. Sedangkan pada industri pengolahan bijih emas, zink
dalam bentuk serbuk digunakan pada proses sementasi emas atau prespitasi yang
dikenal sebagai proses Merill-Crowe (Sudarsono, 2003).
Zink merupakan unsur yang sangat penting untuk pertumbuhan manusia.
Metabolisme sel dipengaruhi dan ditentukan oleh zink. Zink berperan dalam fungsi
syaraf dan reproduksi. Zink juga berperan dalam menstabilisasi sruktur protein.
Selain itu, zink juga dibutuhkan dalam sintesis DNA, replika DNA, transkripsi RNA,
pertumbuhan dan aktivitas sel, pertumbuhan dan perkembangan normal selama hamil,
masa pertumbuhan anak dan pertumbuhan remaja, menjaga kesehatan kulit dan daya
tahan terhadap infeksi, serta merupakan aktifator enzim dan juga berperan dalam
Zink merupakan unsur esensial dan mempunyai banyak fungsi, namum dalam
dosis tinggi zink dapat berbahaya dan bersifat toksik. Dalam keadaan sebagai ion,
zink bebas memiliki toksisitas tinggi. Absorpsi zink berlebih mampu mengakibatkan
defisiensi dan gangguan metabolisme mineral lain seperti penurunan kadar Cu,
pengubahan Fe, pengurangan imunitas tubuh, serta pengurangan kadar high density
lipoprotein (HDL). Konsumsi seng sebesar 2 g atau lebih akan menyebabkan mual,
muntah, dan demam (Widowati, 2008).
2.7. Adsorpsi
Adsorpsi merupakan suatu proses dimana komponen pindah dari fase satu ke fase
lainnya dengan melintasi beberapa pembatas. Atau perpindahan zat dari pelarut
menuju penyerap (LaGrega, et al., 2001). Menurut Benjamin (2002), adsorpsi adalah
akumulasi dari suatu substansi pada atau di dekat permukaan. Substansi yang terserap
disebut dengan adsorbat, sedangkan bahan yang menyerap disebut dengan adsorben.
Perpindahan bahan organik atau anorganik pada sisi permukaan adsorben terjadi
dalam empat proses yaitu transpor bulk fluid, film transport, difusi intrapartikel,
physical attachment.
2.7.1. Pembagian Adsorpsi
a. Adsorpsi Fisika
Dalam adsorpsi fisika, melibatkan gaya van der waals yang menyebabkan molekul
adsorbat terikat secara lemah dengan permukaan adsorben, dan proses ini
berlangsung cepat dan bersifat reversible (Madan dan Tuli, 2007). Proses adsorpsi
fisika terjadi tanpa memerlukan energi aktivasi (energi untuk bereaksi), sehingga
proses tersebut membentuk banyak lapisan (multilayer) pada permukaan adsorben.
Kecepatan difusi dari adsorbat terhadap permukaan adsorben dan tidak tergantung
b. Adsorpsi Kimia
Adsorpsi kimia terjadi karena adanya reaksi kimia antara molekul-molekul adsorbat
dengan permukaan adsorben dan berlangsung lambat, bersifat irreversibel dan hanya
membentuk satu lapisan (monolayer) (Madan dan Tuli, 2007). Adsorpsi kimia
(chemisorptions) selalu disertai dengan pertukaran electron pada adsorben dan
tergantung terhadap temperatur ( Selwood, 1962).
2.7.2. Faktor yang mempengaruhi adsorpsi
Menurut Al-Anber (2011), beberapa faktor yang mempengaruhi adsorpsi yakni:
- Luas Permukaan adsorben, semakin luas area permukaan adsorben, maka
kapasitas adsorpsinya juga semakin meningkat.
- Ukuran partikel adsorben, semakin kecil ukuran partikel adsorben maka
akan memperlambat difusi internal.
- Waktu kontak, semakin lama waktu kontak maka proses adsorpsi semakin
baik.
- Kelarutan adsorbat dalam air atau limbah, adsorbat yang kurang larut
dalam limbah akan semakin mudah untuk diserap oleh adsorben.
- Afinitas pelarut terhadap adsorben, jika permukaan adsorben bersifat
kurang polar, maka substansi yang kurang polar akan lebih mudah
diadsorpsi.
- Ukuran molekul adsorbat dan ukuran pori adsorben, molekul adsorbat
yang berukuran besar jika masuk kedalam pori adsorben yang ukuran
lebih kecil, maka akan menurunkan kapasitas adsorpsi.
- Kemampuan ionisasi adsorbat
- pH, ionisasi adsorbat tergantung pada pH, sehingga dapat mempengaruhi
adsorpsi.
- Efek konsentrasi awal adsorbat, dengan konsentrasi tinggi, kemampuan
adsorpsi lebih sedikit, hal ini berhubungan dengan proses kompetitif difusi
- Keefektifan adsorben, adsorpsi akan semakin efektif jika adsorben yang
digunakan semakin banyak.
Total zat yang teradsorpsi adsorben disebut dengan densitas adsorbsi,
dengan simbol q. Densitas adsorpsi dapat berupa masa zat yang terserap per luas area
(mg/m2) atau per masa adsorben (mg/g) (Benjamin, 2002)
2.8. Spektrometri FT-IR (Fourier Transform Infrared)
Bila sinar inframerah dilewatkan melalui cuplikan senyawa organik, sejumlah
frekuensi diserap sedang frekuensi yang lain diteruskan/ditransmitasikan tanpa
diserap. Jika kita menggambar antara persen absorbansi atau persen transmitansi
lawan frekuensi maka akan dihasilkan suatu spectrum inframerah.
Spektrum inframerah dari alkana rantai panjang (parafin cair atau nujol)
menunjukkan pita serapan pada daerah sekitar 3000 cm-1 dan 1400 cm-1, sedangkan frekuensi lainnya tidak berinteraksi dengan cuplikan dan sebagai akibat hamper
semuanya diteruskan.
Molekul-molekul alkana hanya menyerap sinar inframerah pada frekuensi
tertentu jika didalam molekul ada transisi tenaga yang besar yaitu sebesar .
Transisi yang terjadi didalam serapan inframerah berkaitan dengan
perubahan-perubahan vibrasi didalam molekul, sebagai contoh pita didekat 3000 cm-1 (9,3 x 1013 Hz) mempunyai frekuensi yang tepat sama dengan ikatan C-H yang mengalami
vibrasi stretching/ rentangan. Itulah sebabnya pita serapan dekat 3000 cm-1 disebut serapan C-H stretching, biasanya dinyatakan dengan C-H str.
Pita-pita sekitar 1400 cm-1 sesuai dengan frekuensi vibrasi bending dari ikatan-ikatan C-H dan disebut serapan-serapan C-H bending. Sering vibrasi-vibrasi bending
dinyatakan sebagai deformasi, sehingga pita-pita deformasi C-H dapat diberi tanda
sebagai C-H def. Itulah sebabnya spektroskopi inframerah disebut spektroskopi
vibrasi. Ikatan – ikatan yang berbeda (C-C, C=C, C-O, C=O, O-H, N-H, dsb)
ikatan tersebut dalam molekul organik dengan mengidentifikasi frekuensi-frekuensi
karakteristiknya sebagai pita serapan dalam spectrum inframerah. Dalam spektrum
inframerah suatu aldehid berada dalam pita serapan 2800 cm-1 dan O-H dalam pita serapan antara 3000- 3500 cm-1(Sastrohamidjojo, 1985).
Spektrofotometri infra merah merupakan suatu metode yang mengamati
interaksi molekul dengan radiasi elektromagnetik yang berada pada daerah panjang
gelombang 0,75 – 1000 µm atau paada bilangan gelombang 13.000 – 10 cm-1. Radiasi elektromagnetik dikemukakan pertama kali oleh James Clark Maxwell, yang
menyatakan bahwa cahaya secara fisis merupakan gelombang elektromagnetik,
artinya mempunyai vektor listrik dan vektor magnetik yang keduanya saling tegak
lurus dengan arah rambatan. Saat ini telah dikenal berbagai macam gelombang
elektromagnetik dengan rentang panjang gelombang tertentu. Spektrum
elektromagnetik merupakan kumpulan spektrum dari berbagai panjang gelombang.
Berdasarkan pembagian panjang gelombang sinar inframerah dibagi atas tiga daerah,
yaitu:
a. Daerah inframerah dekat
b. Daerah inframerah pertengahan
c. Daerah inframerah jauh.
Dari pembagian daerah spektrum elektromagnetik tersebut, daerah panjang
gelombang yang digunakan spektrofotometer infra merah adalah pada daerah infra
merah pertengahan, yaitu pada panjang gelombang 2,5-50µm atau pada bilangan
gelombang 4000-200 cm-1. Dasar spektroskopi infra merah dikemukakan oleh Hooke dan didasarkan atas senyawa yang terdiri dari dua atom atau diatom yang
digambarkan dengan dua buah bola yang saling terikat oleh pegas (Silverstain, 2000).
2.9. Spektrofotometri Serapan Atom
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika menelaah
garis-garis hitam pada spektrum matahari. Sedangkan yang memanfaatkan prinsip serapan
1955. Sebelumnya ahli kimia banyak tergantung pada cara-cara spektrofotometrik
atau metode analisis spektrografik. Beberapa cara ini sulit dan memakan waktu,
kemudian segera digantikan dengan spektroskopi serapan atom atau atomic
absorption spectroskopi. Metode ini sangat tepat untuk analisis zat pada konsentrasi
rendah (Khopkar, 2002).
2.9.1. Prinsip dasar Spektrofotometri Serapan Atom
Jika cahaya dengan panjang gelombang resonansi dilewatkan nyala yang
mengandung atom-atom yang bersangkutan, maka sebagian cahaya itu akan diserap
dan jauhnya penyerapan akan berbanding lurus dengan banyaknya atom keadaan
dasar yang berada dalam nyala. Hal ini merupakan dasar penentuan kuantitatif
logam-logam dengan menggunakan SSA (Vogel, 1992).
2.9.2. Instrumentasi Spektrofotometri Serapan Atom Nyala Berkas Tunggal
Sebuah instrumen serapan atom berisi komponen dasar yang sama sebagai instrumen
yang dirancnag untuk pengukuran penyerapan molekul. Sumber, wadah sampel
(disini, sebuah reservoir api), pemilih panjang gelombang, dan detektor/ sistem
pembacaan. Kedua instrument tunggal dan ganda yang ditawarkan oleh berbagai
produsen. Kisaran kecanggihan dan biaya keduanya substansi (Skoog, A, D, 1991).
Adapun instrumentasi Spektrofotometer Serapan Atom Nyala Berkas Tunggal
dapat digambarkan dalam bagan sebagai berikut : (Underwood,A.,I, 1986).
1 3 4 5 6
7 2 9
Gambar 2.8.2. Bagan Instrumentasi Spektrofotometri Serapan Atom
Keterangan :
1. Tabung Katoda berongga
2. Nyala (Unit pengatoman analit)
3. Monokromator
Sebagai sumber cahaya radiasi digunakan lampu katoda berongga (hallow cathode
lamp) yang merupakan sumber sinar, mengeluarkan radiasi dengan frekuensi yang
sesuai dengan unsur yang dianalisis. Di dalam tungku penguapan larutan sampel yang
masuk akan dipecah menjadi tetesan-tetesan halus dan akan disemburkan dalam nyala
untuk diatomkan (Khopkar, 2002).
b. Nyala
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan menjadi
bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Konsentrasi atom-atom
dalam bentuk gas dalam nyala, baik dalam keadaan dasar maupun keadaan tereksitasi,
dipengaruhi oleh komposisi nyala (Vogel, 1992).
Kombinasi bahan bakar senyawa oksidator paling umum adalah asetilena dan
udara, yang menghasilkan suhu nyala bahan bakar 2400-2700 K. Kombinasi bahan
Tabel 2.1. Suhu Nyala Maksimum
Dalam spektroskopi serapan atom fungsi monokromator adalah untuk memisahkan
garis resonansi dari semua garis yang tak diserap yang diapancarkan oleh sumber
radiasi (Braun, 1982).
Monokromator yang dipakai harus mampu memberikan resolusi yang terbaik.
Ada dua bentuk monokromator yang dipakai pada spektrofotometri adsorpsi serapan
atom yaitu monokromator celah dan kisi difraksi (Mulja, 1995).
d. Detektor
Detektor pada spektrofotometri adsorpsi serapan atom berfungsi mengubah intensitas
radiasi yang datang menjadi arus listrik. Pada spektrofotometri serapan atom yang
umum dipakai sebagai detektor adalah tabung penggandaan foton
(PMT = Photo Multiplier Tube detector) (Mulja, 1995).
e. Penguat Arus
Penguat arus (amplifier) hanya mampu menguatkan arus bolaak-balik (AC).
f. Read Out
Read out merupakan sistem pencatatan hasil. Hasil pembacaaan dapt berupa angka
atau berupa kurva dari suatu rekorder yang menggambarkan absorbansi atau
intensitas emisi (Braun, 1982).
Read out dapat berupa galvanometer sederhana, voltmeter digital, atau
potensiometer perekam pena tinta, untuk laboratorium dengan beban yang berat,
keluaran penguat dapat didigitalkan dan diproses dengan computer
(Underwood, 1986).
2.9.3. Gangguan-gangguan Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) pada spektrofotometri serapan atom adalah
peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis
menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya
dalam sampel (Gandjar dan Rohman, 2008). Secaraluas dapat dikategorikan menjadi
dua kelompok, yakni interferensi sifat absorpsi (Khopkar, 1985).
Interferensi spektral disebabkan karena timpang asuh absorpsi antara spesies
pengganggu dan spesies yang diukur. Interferensi kimia disebabkan adanya reaksi
kimia selama atomisasi, sehingga mengubah sifat absorpsi (Khopkar, 1985).
Contoh gangguan kimia adalah terdapatnya senyawa yang sukar diuraikan
dengan nyala api, dengan adanya senyawa ini maka akan mengurangi jumlah atom
netral yang terdapat dalam nyala (Gandjar dan Rohman, 2008).
2.9.4. Aplikasi Spektrofotometri Serapan Atom
Spektrofotometri serapan atom berguna dalam penentuan sejumlah besar logam,
terutama pada tingkat rendah. Secara luas digunakan untuk dalam bidang-bidang
penentuan diberikan cukup kritis, dan siap untuk melakukan metode penelitian yang
panjang, ini penting untuk mendapatkan petunjuk khusus. Instrument utama produsen
menyediakan pedoman luas termasuk prosedur untuk semua logam biasa dalam
berbagai matriks (Ewing, 1982).
Teknik ini juga diterapkan pada penetapan 60 unsur, dan teknik ini merupakan
alat utama dalam pengkajian yang meliputi logam runutan dalam lingkungan dan
dalam sampel biologis. Teknik ini juga berguna dalam kasus-kasus dimana logam itu
berada pada kadar yang cukup di dalam sampel itu, tetapi hanya tersedia sedikit
BAB 3
METODE PENELITIAN
3.1. Alat
- Gelas Beaker 1000 ml pyrex
- Gelas Ukur 10 ml pyrex
- Hot Plate stirrer termoscientific
- Magnetic stirrer
- Erlenmeyer 500 ml pyrex
- Labu Takar 1000 ml pyrex
- Labu takar 500 ml pyrex
- Corong pyrex
- Oven
- Pipet Tetes
- Spatula
- Indikator Universal
- Botol Aquades
- Ayakan 100 mesh
- Blender
- Spektrofotometri Serapan Atom Shimadzu
3.2. Bahan
- NaOH p.a. Merck
- HNO3(p) p.a. Merck
- Aquades
- Jerami Padi
- Limbah elektroplating
- Kertas Saring Whatman no.1
- Kertas saring Whatman no. 42
3.3. Prosedur Perobaan
3.3.1. Pembuatan Adsorben
3.3.1.1. Pembuatan Serbuk jerami padi
Dicuci bersih jerami padi, kemudian dikeringkan jerami padi tersebut dibawah sinar
matahari hingga jerami padi kering. Jerami padi yang telah kering di haluskan dengan
diblender kemudian di ayak dengan ayakan ukuran 100 mesh. Maka didapatlah
serbuk jerami padi.
3.3.1.2.Pembuatan Srbuk Jerami Padi Terdelignifikasi
Direndam serbuk jerami padi dengan menggunakan larutan NaOH 3%, kemudian
diaduk selama 1-2 jam, lalu didiamkan 1-2 jam, kemudian disaring. Residu dicuci
dengan aquades hingga netral. Setelah adsorben netral dikeringkan dengan
menggunakan oven pada suhu 70°C. Serbuk jerami padi yang terdelignifikasi
3.3.1.3.Aktivasi Adsorben dengan HCl
Disiapkan larutan HCl dengan variasi konsentrasi 0,2 ; 0,6 ; 1M, masing-masing
tersebut ditambahkan 50 gram serbuk jerami padi terdelignifikasi. Campuran tersebut
diaduk dengan magnetic stirrer selama 30 menit kemudian disaring. Residu
dikeringkan dalam oven 50°C selama 24 jam, kemudian suhu dinaikkan menjadi
105°C lalu didinginkan. Selanjutnya masing-masing sampel dicuci dengan aquadest
hingga netral, kemudian dikeringkan dalam oven pada suhu 50°C selama 24 jam.
3.3.1.4. Penentuan Kadar Zn Pada Limbah Elektroplating dengan Variasi pH
Dimasukkan 50 ml limbah elektroplating kedalam beaker glass, divariasikan pada
larutan limbah elektroplating pH 4,5,6,7, dan 8 ditambahkan adsorben jerami padi
yang diaktivasi dengan HCl 0,2 M sebanyak 1 gram kedalam larutan, kemudian
diaduk selama 60 menit dengan magnetic stirer, kemudian didiamkan larutan selama
15 menit, disaring. Filtrat di analisa dengan spektrofotometri serapan atom untuk
menentukan konsentrasi logam Zn. Dilakukan hal yang sama pada adsorben jerami
3.4. Bagan Penelitian
3.4.1. Pembuatan Adsorben
3.4.1.1. Pembuatan Serbuk Jerami Padi
dicuci bersih
dikeringkan dibawah sinar matahari
selama 3 hari
digiling sampai halus dengan blender
diayak dengan ayakan 100 mesh
3.4.1.2. Pembuatan Serbuk Jerami Padi Terdelignifikasi
direndam dengan NaOH 3%
diaduk selama 1-2 jam
didiamkan selama 1-2 jam
dicuci dengan aquadest hingga netral
dikeringkan dengan oven pada suhu 70°C
dianalisa dengan spektometri FT-IR 800 gr jerami padi
500 gr serbuk jerami padi
500 gr serbuk jerami
3.4.1.3. Aktivasi Adsorben dengan HCl
dimasukkan kedalam beaker glass
ditambahkan sebanyak 250 ml larutan HCl 0,2M
diaduk selama 30 menit
disaring
dikeringkan selama 24 jam pada suhu 50°C
dinaikkan suhu menjadi `105°C
didinginkan
dicuci dengan aquades hingga netral
dikeringkan pada oven dengan suhu 50°C
selama 24 jam
Hal yang sama dilakukan untuk HCl 0,6 M dan HCl 1 M 50 gr serbuk jerami padi terdelignifikasi
residu filtrat
3.4.1.4. Penentuan Kadar Zn Pada Limbah Elektroplating dengan Variasi
pH
dimasukkan kedalam beaker glass yang
berisi limbah elektroplating
divariasikan pada pH 4
ditambahkan Adsorben yang diaktivasi
dengan HCl 0.2 M 1 gr
distirer selama 60 menit
didiamkan Selama 15 menit
disaring
ditentukan konsentrasi logam Zn
dengan spektrofotometri serapan atom
Perlakuan yang sama dilakukan dengan variasi pH 5, 6, 7, dan 8 pada limbah
elektroplatting dan dengan aktivasi HCl 0.6 M dan 1 M 50 ml Limbah Elektroplatting
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Preparasi Sampel
Dicuci bersih sampel jerami padi, kemudian dikeringkan jerami padi tersebut
dibawah sinar matahari hingga jerami padi kering. Jerami padi yang telah kering
dihaluskan menggunakan blender kemudian diayak dengan ayakan ukuran 100 mesh.
Maka didapatlah serbuk jerami padi berwarna coklat tua. Selanjutnya serbuk jerami
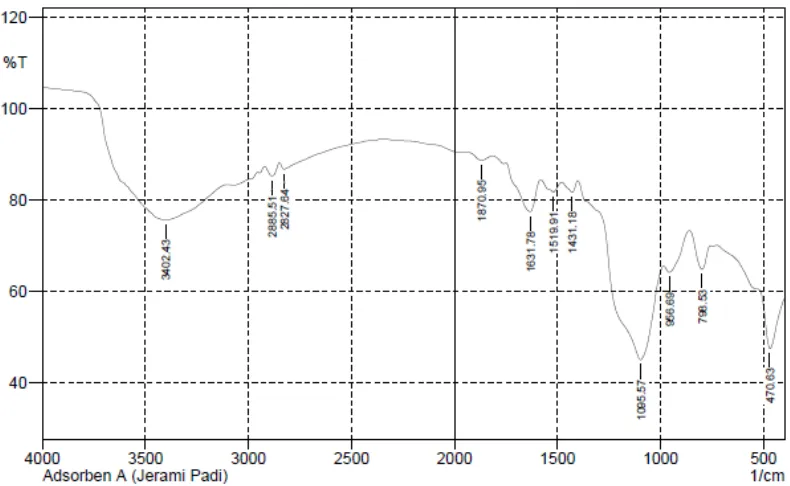
padi di analisa dengan spektrofotometri FT-IR. Berikut adalah gambar spektra FT-IR
dari serbuk jerami padi.
Dari gambar diatas maka jerami padi sebelum didelignifikasi memiliki interpretasi
sebagai berikut:
Tabel 4.1. Interpretasi gugus fungsi senyawa hasil analisis FT-IR dari adsorben jerami padi sebelum didelignifikasi
Gugus Fungsi Frekuensi (cm-1) hasil Frekuensi (cm-1) teori
-OH 3402.43 3200-3500
-CH ulur
-CH tekuk
2885.51
798.53
2885-3000
600-1000
C=C 1631.78 1600-1680
CH3 1431.18 1375-1450
-CO 1095.57 1000-1300
4.1.2. Pembuatan Serbuk Jerami Padi Terdelignifikasi
Direndam serbuk jerami padi dengan menggunkan larutan NaOH 3 %,
kemudian diaduk selama 1-2- jam, lalu didiamkan selama 1-2 jam, disaring. Residu
dicuci dengan aquades hingga pH netral. Setelah pH serbuk jerami padi netral,
dikeringkan dengan menggunakan oven pada suhu 70°C. Maka didapat hasil serbuk
jerami padi yang terdelignifikasi dengan warna coklat muda, setelah itu dianalisa
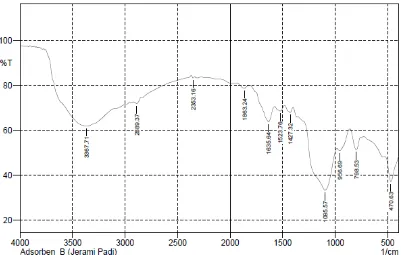
dengan menggunakan spektrofotometri FT-IR. Berikut adalah gambar spektra FT-IR
Gambar 2. Spektrum FT-IR dari adsorben jerami padi setelah didelignifikasi
Dari gambar diatas maka jerami padi sesudah didelignifikasi memiliki interpretasi
sebagai berikut:
Tabel 4.2. Interpretasi Gugus Fungsi Senyawa Hasil Analisis FT-IR dari adsorben jerami padi setelah didelignifikasi
Gugus Fungsi Frekuensi (cm-1) hasil Frekuensi (cm-1) teori
-OH 3367.71 3200-3500
-CH ulur
-CH tekuk
2889.37
798.53
2885-3000
600-1000
C-O
C=C
1095.57
1635.64
1000-1300
4.1.3. Pengambilan Sampel
Sampel limbah elektroplatting diambil dari hasil pembuangan proses elektroplating
dari Politeknik Medan Fakultas Teknik Mesin. Sampel diambil dari bak yang
disediakan untuk limbah. Proses pengambilan limbah elektroplatting dilakukan secara
acak.
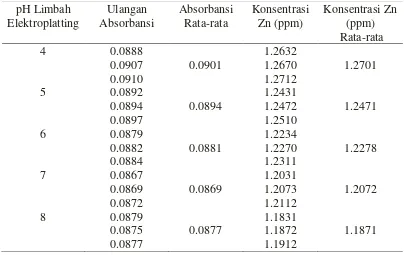
Sebelum adsorben digunakan terlebih dahulu dianalisa kadar logam Zn yang
terkandung dalam limbah elektroplatting dengan menggunakan alat spektrofotometri
serapan atom yang datanya adalah sebagai berikut:
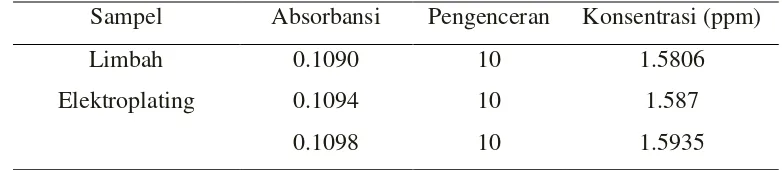
Tabel 4.3. Data Konsentrasi awal logam Zn dari limbah elektroplatting
Sampel Absorbansi Pengenceran Konsentrasi (ppm)
Limbah
Elektroplating
0.1090 10 1.5806
0.1094 10 1.587
0.1098 10 1.5935
dilakukan pengenceran terhadap limbah sebesar 10 kali sehingga diperoleh
konsentrasi sebenarnya seperti yang tertera diatas.
Adsorben jerami padi yang sudah didelignifikasi selanjutnya diaktivasi dengan
menggunakanHCl 0,2M ; 0,6M ; 1M dan diuji terhadap limbah elektroplatting yang
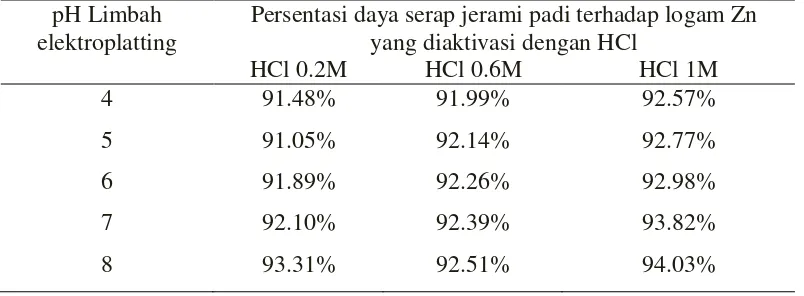
4.1.4. Persentasi Daya Serap
Adapun Persentasi kenaikan daya serap dari jerami padi terhadap logam Zn dengan
variasi pH 4 sampai 8 dari limbah elektroplatting yang diaktivasi dengan HCl 0.2M,
0.6M dan 1 M dapat ditentukan dengan rumus sebagai berikut :
% Daya Serap =
x 100%
Persentasi daya serap logam Zn dari limbah elektroplatting dengan variasi pH 4 – 8
menggunakan adsorben jerami padi yang diaktivasi dengan HCl 0.2M, 0.6M dan 1 M
ialah sebagai berikut:
Contoh perhitungan persentasi daya serap logam Zn dari limbah elektroplatting
menggunakan adsorben jerami padi yang diaktivasi dengan HCl 0.2M pada pH 4
% Daya serap =
x 100 %
= 91.48%
Data perhitungan dapat dilihat pada tabel 8.
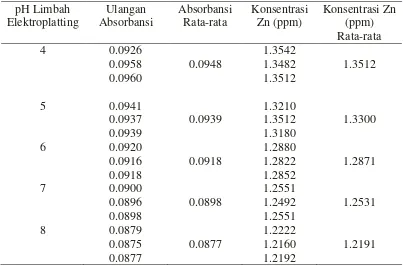
Tabel 4.8. Persentasi kenaikan daya serap dari jerami padi yang teraktivasi dengan HCl 0.2M, 0.6M dan 1M dengan variasi pH 4 sampai 8 dari limbah Elektroplatting
pH Limbah elektroplatting
Persentasi daya serap jerami padi terhadap logam Zn yang diaktivasi dengan HCl
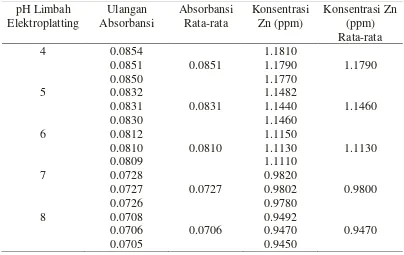
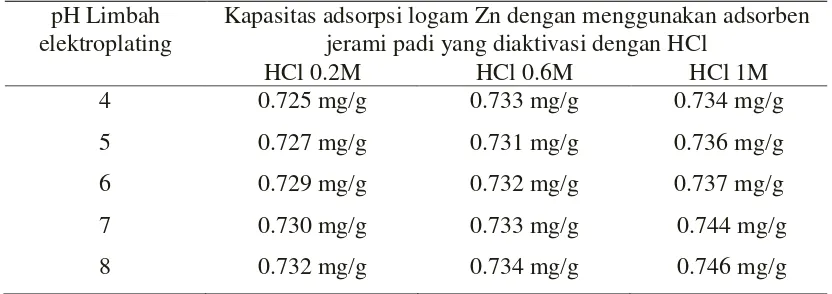
4.1.5. Menentukan Kapasitas Adsorpsi dari adsorben jerami padi
Dalam menentukan kapasitas daya serap dari jerami padi dapat diketahui dengan
rumus berikut ini :
qe =
Dengan
qe = kapasitas Adsorpsi (mg/g)
Ci = Konsentrasi awal logam (mg/L)
Ce = Konsentrasi akhir logam (mg/L)
W = masa dari adsorben (g)
V = volume larutan logam (L)
Kapasitas adsorpsi dari serbuk jerami padi yang diaktivasi dengan HCl 0.2M, 0.6M
dan 1 M yaitu sebagai berikut:
Contoh perhitungan kapasitas adsorpsi dari serbuk jerami padi yang diaktivasi dengan
HCl 0.2M pada pH 4
qe =
x 0.05L
=0.725 mg/g
Data perhitungan dapat dilihat pada tabel 9
Tabel 4.9.Kapasitas adsorpsi logam Zn dengan menggunakan adsorben jerami padi yang diaktivasi dengan HCl 0.2M, 0.6M dan 1M pada variasi pH 4 sampai 8
pH Limbah elektroplating
Kapasitas adsorpsi logam Zn dengan menggunakan adsorben jerami padi yang diaktivasi dengan HCl
4.2. Pembahasan
Sampel jerami padi yang telah bersih dan diayak dengan ukuran partikel 100 mesh,
dilakukan proses delignifikasi. Fungsi dari delignifikasi dalam penelitian ini adalah
untuk melarutkan senyawa-senyawa dalam jerami padi seperti lignin yang dapat
menghambat proses adsorpsi. Jerami padi mengandung komponen utama karbohidrat
(selulosa dan hemiselulosa), lignin, dan silika. Keberadaan lignin akan menghalangi
proses transfer ion yang menghalangi masuknya Zn ke sisi aktif adsorben. Larutan
NaOH digunakan sebagai pelarut bertujuan untuk memisahkan selulosa dan lignin.
Ion OH- dari NaOH akan memutuskan ikatan-ikatan dari struktur dasar lignin sehingga lignin akan mudah larut. Indikasi terlarutnya lignin dapat dilihat dari
berkurangnya berat sampel setelah dilakukan proses delignifikasi dan warna sampel
dapat dibedakan sebelum dan sesudah delignifikasi yang terlihat lebih cerah. Berat
serbukjerami padi sebelum di delignifikasi sebesar 800 gram setelah didelignifikasi
sebesar 500 gr, dapat diketahui bahwa telah terjadi pengurangan berat sampel sesudah
dilakukan proses delignifikasi. Hal ini mengindikasi bahwa proses delignifikasi telah
berlangsung baik.
Untuk mengetahui bahwa selulosa dan lignin sudah terpisah dapat dilihat dari
data spektrofotometri FT-IR sebelum dan sesudah didelignifikasi yang datanya pada
tabel.1 Interpretasi gugus fungsi senyawa hasil analisis FT-IR dari serbuk jerami padi
sebelum delignifikasi bahwa didapatkan pita serapan 3402.43 cm-1 gugus fungsi –OH dari selulosa, pita serapan 2885.51 dan 798.53 (–CH) dari selulosa maupun dari
lignin pita serapan 1631.78 cm-1 (C=C) dari senyawa aromatik lignin dan 1431.18 (-CH3) dari lignin. Pita serapan 1095.57 cm-1 (-CO) dari selulosa. Dan dari data tabel 2.
Interpretasi gugus fungsi senyawa hasil analisis FT-IR dari serbuk jerami padi
sesudah delignifikasi maka pita serapan 3367.71 cm-1 menunjukkan gugus dari –OH selulosa dan pita serapan 2889.37 dan 789.53 (-CH) dimana pada pita serapan
2889.37 cm-1 –CH ulur dan 789.53 cm-1 –CH tekuk. Pita serapan 1095.57 cm-1 menunjukkan adanya gugus C-O dari selulosa (Sastrohamidjojo, 1985) yang dapat
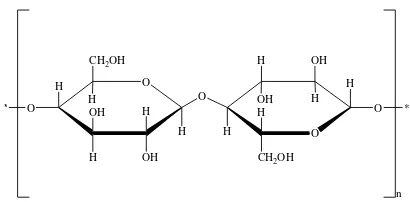
Gambar 3. Gambar struktur molekul selulosa (Fessenden dkk, 1992)
Selanjutnya adsorben diaktivasi dengan menggunakan asam klorida (HCl) dengan
variasi konsentrasi yaitu 0,2M; 0,6M; dan 1M. Aktivasi bertujuan untuk
mendekomposisikan senyawa-senyawa yang terdapat dalam sampel jerami padi.
Selanjutnya adsorben dikeringkan dengan menggunakan oven pada suhu 50ºC
kemudian suhu dinaikkan menjadi 105ºC dengan lama pemanasan 24 jam.
Pemanasan ini bertujuan untuk meningkatkan porositas dinding sel adsorben
sehingga luas permukaan yang besar diharpkan akan mengakibatkan besarnya
kapasitas adsorpsi logam zink (Zn). Pemilihan suhu 105ºC selama 24 jam karena
pada suhu yang terlalu tinggi akan mengakibatkan kerusakan permukaan struktur sel
adsorben. Selanjutnya adsorben yang telah teraktivasi digunakan untuk menurunkan
kadar logam Zn dalam limbah elektroplatting. Dari data tabel 9 maka diketahui
bahwa persentasi daya serap yang paling baik untuk menyerap logam Zn dalam
limbah elektroplattning dengan adsorben jerami padi yang diaktivasi dengan HCl
0.2M, 0.6M dan 1 M yaitu pada adsorben jerami padi yang diaktivasi dengan HCl 1M
sebesar 94.03% dan kapasitas adsorpsi sebesar 0,9479 mg/L
BAB 5
KESIMPULAN dan SARAN
5.1. Kesimpulan
Berdasarkan hasil penelistian yang telah dilakukan, maka dapat diambil kesimpulan
sebagai berikut :
1. Data hasil analisa spektrometri FT-IR diperkirakan bahwa jerami padi yang
sudah didelignifikasi dapat digunakan sebagai adsorben.
2. Aktivasi adsorben jerami padi dengan HCl dapat menurunkan kadar logam
dari Zn.
3. Daya serap adsorben jerami padi pda limbah elektroplating yang pH nya
divariasikan, pH optimum adalah pH 8 dengan daya serap 94,03% dan kadar
logam Zn sebesar 0,9470 mg/L
5.2. Saran
Diharapkan kepada peneliti selanjutnya untuk melakukan pengolahan terhadap logam
lainnya yang bersifat toksik yang terdapat dalam limbah elektroplatting dengan
DAFTAR PUSTAKA
Al-Anber, M.A. 2011. Thermodynamics Approach in the Adsorption of Heavy Metal. Editor: Juan Carlos Moreno Pirajin.
Anonim, (20s02). Buku Panduan Teknologi Pengendalian Dampak Lingkungan Industri Lapis Listrik. Kementrian Lingkungan Hidup, Jakarta.
Braun, R. D. 1982. Introduction to Chemical Analysis. New York: Mc Graw-Hill Book Company.
Ewing, W. G. 1982. Instrumental Methods of Chemical Analysis. Fifth Edition. New York: Mc Graw-Hill Book Company.
Farooq, U. 2010. Biosorption Of Heavy Metal Ion Using Wheat Based Biosorbent- A Review of the Recen Literature. Biosource Technology.
Fengel dan Wegner. 1995. Kayu Kimia Ultrastruktur dan Reaksi-reaksi. Yogya :Gajah mada University Press.
Frank, C. Lu. 1994. Toksikologi Dasar asa Organ Sasaran dan Penilaian Fisika. Edisi Kedua. Jakarta: UI Press.
Gandjar, I. G. dan Rohman, A. 2008. Kimia Farmasi Analisis. Cetakan Ketiga. Yogyakarta: Pustaka Pelajar.
Hamid, H. dan Pramudyanto, B. 2007. Pengawasan Industri dalam Pengendalian Pencemaran Lingkungan. Jakarta: Granit.
Igwe, J. C. dan Abia, A. A. 2007. Adsorption Isotherm Studies of Cd(II), Pb (II), Zn (II) on Bioremediation from Aquaeous Solution Using Unmodified and EDTA. Modified Maize Cob. Ecletica.
Khopkar, S. M. 2002. Konsep dasar Analitik. Jakarta: UI-Press.
Kohar dan Setyaningrum. Studi pendahuluan kemampuan sekam dan jerami padi yang telah diolah dengn berbagai konsentrasi larutan.
La Grega, M. D. et all. 2001. Hazardous Waste Management. Edisi Kedua. New York: Mc Graw-Hill.
Madan, R. I. dan Tuli, G. 2007. Physical Chemistry. Edisi Keempat. New Delhi: Rajenda Ravindra Printers.
Mediastika, C. E. 2007. Potensi Jerami Padi Sebagai bahan Baku Panel Akutik. Diakses tanggal 19 Oktober 2014
http://puslit2.petra.ac.id/journal/index.php/ars/article.
Mulia, R. M. 2005. Kesehatan Lingkungan. Edisi Pertama. Yogyakarta: Graha Ilmu.
Mulja, M. 1995. Analisis Instumental. Surabaya: Airlangga University Press.
Palar,H. 2004. Pencemaran dan Toksikologi Logam Berat. Jakarta: Rineka Cipta.
Sastrohamidjojo, H. 1985. Dasar-dasar Spektroskopi. Yogyakarta: Liberty.
Selwood, P. W. 1962. Adsorption Collective Paramagnetism.
New York: Academic Press.
Shriver, D. 1999. Inorganic Chemistry. Third Edition. Oxford: University press.
Skoog, A. D. 1991. Fundamentals of Analytical Chemistry. Seventh edition. USA: Sounders College Publishing.
Sudarsono, A. S. 2003. Pengantar Pengolahan dan Ekstrak Bijih Emas.
Bandung: Departemen Teknik Pertambsangan, ITB.
Underwood, A. L. 1986. Quantitative Analysis. Fifth Edition. New Jersey: Prentice-Hall.
Vogel, I, A, 1994. Kimia Analitik Kuantitatif Anorganik. Edisi Keempat. Jakarta: EGC Kedokteran.
Lampiran 1.Perhitungan Hasil
Data kadar Logam seng
Tabel 1. Penurunan persamaaan garis regresi dengan metode least square
No xi yi xi –x yi - y (xi–x)2 (yi–y)2 (xi –x)(yi–y)
1 2 0.1386 -4 -0.2488 16 0.0619 0.9952
2 4 0.2646 -2 -0.1228 4 0.0150 0.2456
3 6 0.3760 0 -0.0114 0 0.0001 0
4 8 0.5202 2 0.1146 4 0.0131 0.2292
5 10 0.6376 4 0.2502 16 0.0626 1.0008
Σ xi = 30 yi = 1.937 0 -0.0182 40 0.1527 2.4708
x = 6 y = 0.3847
y = ax + b
Dimana : a = slope
b = intersept
a = ∑ ̅ ̅
∑
y = ax + b
b = ̅ ̅
b = 0.3874 – (0.0627)(6)
b = 0.3874 – 0.3762
b = 0.0113
Maka persamaan garis regresi adalah:
Menghitung Koefisien Korelasi (r)
0,00 2,00 4,00 6,00 8,00 10,00 12,00
Lampiran 2.Gambar Proses delignifikasi
1.Perendaman serbuk jerami padi dengan larutan NaOH 3%
2.Penyaringan serbuk jerami padi yang telah didelignifikasi
Proses aktivasi serbuk jerami padi
3.Perendaman serbuk jerami padi dengan larutan HCl
6.Serbuk jeramssi padi yang diaktivasi dengan HCl 0,6M
Proses penyerapan limbah elektroplating
8.Limbah elektroplating
10.Penyaringan limbah elektroplating