STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT
PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL
SIBOLGA SEBAGAI BAHAN BAKU KOMPOS
TESIS
Oleh
SELVYA 117006012/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT
PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL
SIBOLGA SEBAGAI BAHAN BAKU KOMPOS
TESIS
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains Dalam Program Studi Ilmu Kimia Pada Fakultas Matematika Dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara
Oleh
Selvya 117006012/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
Judul Tesis : STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL SIBOLGA SEBAGAI BAHAN BAKU KOMPOS
Nama Mahasiswa : Selvya
Nomor Pokok : 117006012
Program Studi : Magister Ilmu Kimia
Menyetujui Komisi Pembimbing
Dr. Hamonangan Nainggolan, M.Sc Jamahir Gultom, Ph.D
Ketua Anggota
Ketua Program Studi Dekan
Prof.Basuki Wirjosentono, MS,Ph.D Dr.Sutarman, M.Sc
Telah diuji pada
Tanggal : 26 April 2013
PANITIA PENGUJI TESIS
Ketua : Dr. Hamonangan Nainggolan, MSc Anggota : 1. Jamahir Gultom, Ph.D
2. Prof. Basuki Wirjosentono,MS,Ph.D 3. Dr. Nimpan Bangun,MSc
PERNYATAAN ORISINALITAS
STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT
PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL
SIBOLGA SEBAGAI BAHAN BAKU
KOMPOS
TESIS
Dengan ini saya menyatakan bahwa saya mengakui semua karya Tesis ini adalah hasil kerja saya sendiri kecuali kutipan dan ringkasan yang tiap satunya telah dijelaskan sumbernya dengan benar.
Medan, 2013
Selvya
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH
UNTUK KEPENTINGAN AKADEMIS
Sebagai Sivitas Akademika Universitas Sumatera Utara, saya yang bertanda tangan di bawah ini:
Nama : Selvya
Nomor Pokok : 117006012
Program Studi : Magister Ilmu Kimia Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Eksklusif (Non-Exclusif Royalty Free Right) atas Tesis saya yang berjudul:
STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT
PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL
SIBOLGA SEBAGAI BAHAN BAKU
KOMPOS
beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non-Eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan Tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai pemilik hak cipta.
Demikian pernyataan ini dibuat dengan sebenarnya.
Medan, 2013
Selvya
RIWAYAT HIDUP
DATA PRIBADI
Nama Lengkap : Selvya
Tempat / Tgl lahir : Tanjung Morawa, 23 Mei 1969
Alamat Rumah : Griya Payaroba Indah Blok G No.9 Binjai
HP : 08126552052
Email : [email protected]
Instansi Tempat Kerja : SMA Negeri 4 Binjai
Alamat Kantor : Jl. Cut Nyak Dien No 134 Binjai
DATA PENDIDIKAN
SD Negeri 101897 Tanjung Morawa Tamat 1982
SMP Negeri 1 Tanjung Morawa Tamat 1985
SMA Negeri Tanjung Morawa Tamat 1988
D-3 Kependidikan USU Tamat 1992
i
STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL
SIBOLGA SEBAGAI BAHAN BAKU KOMPOS
ABSTRAK
Telah dilakukan penelitian pembuatan pupuk kompos dari limbah ikan tempat pelelangan (TPI) dan pasar tradisional Sibolga. Proses pengomposan menggunakan EM4 yang telah diaktifkan dengan tetes tebu.Selama pengomposan kondisi suhu
ii A STUDY ON THE USE OF FISHES WASTE FROM THE FISH
AUCTION (TPI) AND TRADITIONAL MARKET SIBOLGA AS COMPOS MATERIAL
ABSTRACT
This thesis deals with a research on composting of waste fish in the fish auction (TPI) and traditional markets in Sibolga. The Composting process used EM4 which has been enabled with drops of cane. During composting, the temperature was being maintained by compost reversal and the changing of color and odor was being observed. Testing the levels of C-Organic, Nitrogen, Phosphorus, and Potassium were performed on span days 0,2,5,10,15,20. The results showed the levels of C-Organik; 51.69%, Nitrogen; 8.25%, Phosphorus; 4.75%, and Potassium; 1.56%. From the results of testing C-Organic, Nitrogen, Phosphorus, and Potassium, it shows a high level compared with the ISO quality compost. Therefore the compost from fish waste in the fish auction (TPI) and a traditional market Sibolga can be used as fertilizer.
iii
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang member limpahan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan tesis ini.
Dengan selesai tesis ini, penulis mengucapkan terimakasih yang sebesar-besarnya kepada : Rektor Universitas Sumatera Utara, Bapak Prof. Dr. dr.Syahril Pasaribu, DMT&H, M.Sc, (CTM), SpA (K), atas kesempatan dan fasilitas yang diberikan kepada penulis untuk menjadi mahasiswa Program Magister pada Sekolah Pasca Sarjana Universitas Sumatera Utara, Dekan FMIPA Dr.Sutarman, M.Sc. Dan Bapak Prof. Basuki Wirjosentono, MS, Ph.D. Atas kesempatan yang telah diberikan kepada penulis untuk menjadi mahasiswa Program Magister pada sekolah Pascasarjana Universitas Sumatera Utara.
Terima kasih yang tak terhingga dan penghargaan setinggi-tingginya penulis ucapkan kepada Bapak Dr. Hamonangan Nainggolan, MSc dan Bapak Jamahir Gultom, Ph.D selaku komisi pembimbing yang setiap saat dengan penuh perhatian dan selalu menyediakan waktu untuk memberi bimbingan, saran dan motivasi sehingga tesis ini dapat selesai.
Seluruh Staf Pengajar, karyawan dan rekan-rekan mahasiswa angkatan 2011 pada Program Pasca Sarjana Program Studi Ilmu Kimia yang telah memberikan ilmu,bantuan moril dan motivasi bagi penulis,atas semuanya penulis ucapkan terima kasih.
iv
Penulis menyadari bahwa tesis ini masih banyak kekurangan dan masih jauh dari sempurna, oleh karena itu penulis sangat mengharapkan kritik dan saran yang sifatnya membangun dari pihak pembacauntuk kesempurnaan bagi peneliti dan kemajuan ilmu.
Medan, April 2013
v
DAFTAR ISI
ABSTRAK i
ABSTRACT ii
KATA PENGANTAR iii
DAFTAR ISI v
DAFTAR TABEL vii
DAFTAR GAMBAR viii
BAB 1 PENDAHULUAN
1.1 Latar Belakang 1
1.2 Rumusan Masalah 2
1.3 Pembatasan Masalah 2
1.4 Tujuan Penelitian 2
1.5 Manfaat Penelitian 3
1.6 Metodologi Penelitian 3
1.7 Lokasi Penelitian 3
BAB 2 TINJAUAN PUSTAKA
2.1 Limbah Ikan 4
2.2 Kompos 5
2.3 Aktivator 6
2.4 EM4 (Effektif Micrroorganisme 4) 6
2.5 Proses Pengomposan 8
vi
2.7 Kompos Matang 14
2.8 Standar Pupuk Kompos 16
BAB 3 METODE PENELITIAN
3.1 Alat-Alat Yang Digunakan 17
3.2 Bahan-Bahan Yang Digunakan 18
3.3 Prosedur Penelitian 18
3.4 Bagan Penelitian 25
BAB 4 HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian 31
4.2 Pembahasan 36
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 41
5.2 Saran 41
DAFTAR PUSTAKA DAFTARLAMPIRAN
vii
DAFTAR TABEL
Nomor Judul Halaman
Tabel 2.6 Kondisi yang optimal mempercepat proses pengomposan
13
Tabel 2.8 Standar kualitas kompos berdasarkan SNI 19-7030-2004 16 Tabel 4.1 Pengujian kadar C-Organik dari limbah ikan TPI dan
pasarTradisinal Sibolga
32
Tabel 4.2 Pengujian kadar Nitrogen dari limbah ikan TPI dan PasarTradisinal Sibolga
33
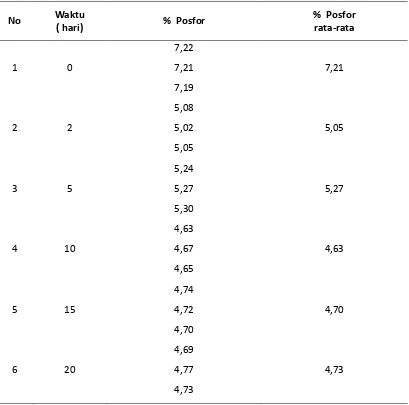
Tabel 4.3 Pengujian kadar Posfor dari limbah ikan TPI dan Pasar Tradisinal Sibolga
34
Tabel 4.4 Pengujian kadar Kalium dari limbah ikan TPI dan Pasar Tradisinal Sibolga
35
Tabel 4.2.1 Pengujian kadar C-Organik, Nitrogen, Posfor dan Kaliumdari limbah ikan TPI dan pasar tradisinal Sibolga
viii
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar 4.2.1 Kurva Perubahan kadar C-Organik Vs Waktu 36 Gambar 4.2.2 Kurva Perubahan kadar Nitrogen Vs Waktu 37 Gambar 4.2.3 Kurva Perubahan kadar Posfor Vs Waktu 38
i
STUDI PEMANFAATAN LIMBAH IKAN DARI TEMPAT PELELANGAN IKAN (TPI) DAN PASAR TRADISIONAL
SIBOLGA SEBAGAI BAHAN BAKU KOMPOS
ABSTRAK
Telah dilakukan penelitian pembuatan pupuk kompos dari limbah ikan tempat pelelangan (TPI) dan pasar tradisional Sibolga. Proses pengomposan menggunakan EM4 yang telah diaktifkan dengan tetes tebu.Selama pengomposan kondisi suhu
ii A STUDY ON THE USE OF FISHES WASTE FROM THE FISH
AUCTION (TPI) AND TRADITIONAL MARKET SIBOLGA AS COMPOS MATERIAL
ABSTRACT
This thesis deals with a research on composting of waste fish in the fish auction (TPI) and traditional markets in Sibolga. The Composting process used EM4 which has been enabled with drops of cane. During composting, the temperature was being maintained by compost reversal and the changing of color and odor was being observed. Testing the levels of C-Organic, Nitrogen, Phosphorus, and Potassium were performed on span days 0,2,5,10,15,20. The results showed the levels of C-Organik; 51.69%, Nitrogen; 8.25%, Phosphorus; 4.75%, and Potassium; 1.56%. From the results of testing C-Organic, Nitrogen, Phosphorus, and Potassium, it shows a high level compared with the ISO quality compost. Therefore the compost from fish waste in the fish auction (TPI) and a traditional market Sibolga can be used as fertilizer.
1
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Hasil penangkapan ikan dari perairan laut di pantai barat Sumatera bagian utara khususnya di wilayah pantai Sibolga adalah berjumlah cukup besar dan jenisnya cukup beragam. Dapat dikatakan bahwa hasil perikanan laut di wilayah ini sangat berperan untuk mendukung perekonomian rakyat Sibolga. Hasil penangkapan ikan dimaksud terlebih dahulu disortir sesuai dengan jenis dan kondisi fisiknya, sehingga diharapkan dapat memenuhi kehendak konsumen, baik ditempat pelelangan ikan maupun di pasar tradisional kota Sibolga, demikian juga halnya dengan ikan yang akan dijual keluar kota.
Sangat disayangkan, sesuai dengan kenyataan bahwa tidak semua ikan hasil tangkapan itu dapat dimaanfaatkan sebagai sumber daya alam yang bernilai ekonomis, karena banyaknya ikan yang harus terbuang sebagai limbah. Limbah ikan tersebut diatas ditumpuk di beberapa tempat,baik ditempat pelelangan ikan, maupun dipasar trasional Sibolga. Penanganan terhadap limbah ikan dimaksud belum maksimal, sehingga menimbulkan bau busuk atau pencemaran lingkungan.
Penanggulangan terhadap dampak pencemaran yang disebabkan oleh penumpukan ikan busuk pernah dilakukan oleh BLHPP (Badan Lingkungan Hidup, Pertamanan dan Perkotaan) Kabupaten Samosir pada tahun 2009, dengan cara mengkomposkan menjadi pupuk dengan menggunakan EM4 sebagai mikroba
2
Kompos yang dihasilkan dari proses ini diuji coba oleh BLHPP (Badan Lingkungan Hidup, Pertamanan dan Perkotaan) Kabupaten Samosir dikebun percontohan jagung milik BLHPP Kabupaten Samosir. Hasilnya cukup memuaskan dengan hasil yang jauh lebih besar dibandingkan dengan tanaman sejenis
disekelilingnya yang dimiliki oleh rakyat di wilayah Desa Pebabak Samosir. ( Gultom, J, 2009, Informasi lisan )
Oleh karena itu, penulis merasa tertarik untuk melakukan penelitian dengan
judul “Studi Pemanfaatan Limbah Ikan dari Tempat Pelelangan Ikan (TPI) dan Pasar Tradisinal Sibolga sebagai Bahan Baku Kompos“ dengan harapan limbah ikan
yang dihasilkan dari tempat pelelangan ikan dan pasar tradisional Sibolga dapat dimanfaatkan, sehingga pencemaran yang diakibatkan juga dapat diatasi.
1.2 Rumusan Masalah
1.Apakah limbah ikan dari tempat pelelangan ikan (TPI) dan pasar tradisional Sibolga dapat dimanfaatkan sebagai pupuk kompos.
2.Berapa lama waktu yang dibutuhkan untuk pembuatan kompos.
3.Berapa besar kadar C-organik, Nitrogen,Posfor dan Kalium dan di sesuaikan dengan SNI kompos.
1.3 Pembatasan Masalah
1. Limbah ikan yang digunakan dalam pembuatan pupuk kompos diambil dari tempat pelelangan ikan (TPI) dan pasar tradisional Sibolga
2. Parameter yang dianalisa adalah C-organik, Nitrogen, Posfor, dan Kalium.
1.4 Tujuan Penelitian
1. Mengolah limbah ikan dari tempat pelelangan ikan (TPI) dan pasar tradisional Sibolga sebagai pupuk kompos.
3
13. Mengetahui kadar C-organik, Nitrogen, Phosfor dan Kalium disesuaikan dengan SNI kompos.
1.5 Manfaat Penelitian
1. Memberikan sumbangan pengetahuan alternatif lain dalam pembuatan pupuk kompos.
2. Meningkatkan nilai ekonomis dari limbah ikan
3. Mengurangi beban pecemaran lingkungan yang disebabkan dari limbah ikan Sibolga.
1.6 Metodologi Penelitian
1. Penelitian ini merupakan eksperimen laboratorium
2. Limbah ikan diambil dari Tempat Pelelangan Ikan (TPI) dan Pasar Tradisional Sibolga
3. Pembuatan kompos dari limbah ikan yang difermentasi dengan EM4
4. Penentuan C-organik metode Gravimetri
5. Penentuan Nitrogen dilakukan dengan metoda Kjehldal 6. Penentuan Posfor dengan Spektrofotometer Visible
7. Penentuan Kalium dengan Spektrofotometer Serapan Atom (AAS)
1.7 Lokasi Penelitian
4
BAB 2
TINJAUAN PUSTAKA
2.1 Limbah Ikan
Produksi perikanan laut Indonesia dari tahun-ke tahun semakin meningkat dan berkembang.Disamping kekayaan ikan di kawasan Indonesia yang berlimpah serta usaha untuk meningkatkan hasil tangkapan yang terus-menerus dilaksanakan,ternyata baru mencapai nilai 35% saja yang dapat di capai.
Dari data yang dapat dikumpulkan,setiap musim masih terdapat antara 25-30% hasil tangkapan ikan laut yang akhirnya harus menjadi sisa atau ikan buangan yang disebabkan karena berbagai hal.
1. Keterbatasan pengetahuan dan sarana para nelayan di dalam cara pengolahan ikan . misalnya, hasil tangkapan tersebut masih terbatas sebagai produk untuk dipasarkan langsung (ikan segar), atau diolah menjadi ikan asin, pindang, terasi serta hasil-hasil olahannya.
2. Tertangkapnya jenis-jenis ikan lain yang kurang berharga ataupun sama sekali belum mempunyai nilai di pasaran, yang akibatnya ikan tersebut harus dibuang.
5
Limbah ikan yang dihasilkan dari kegiatan perikanan adalah berupa :
1. Ikan curah yang bernilai ekonomis rendah sehingga belum banyak dimanfaatkan sebagai pangan.
2. Bagian daging ikan yang tidak dimanfaatkan dari rumah makan, rumah tangga, industry pengalengan, atau industri pemiletan.
3. Ikan yang tidak terserap oleh pasar, terutama pada musim produksi ikan melimpah.
4. Kesalahan penanganan dan pengolahan.
Berdasarkan karakternya limbah dapat dibagi menjadi dua kelompok, yaitu limbah yang masih dapat dimanfaatkan dan sudah tidak dapat dimanfaatkan. Limbah perikanan berbentuk padatan, cairan dan gas. Limbah tersebut ada yang berbahaya dan sebagian lagi beracun. Limbah padatan memiliki ukuran bervariasi, mulai beberapa micron hingga beberapa gram atau kilogram.
2.2 Kompos
Menurut J.H.Crawford (2003) kompos didefenisikan sebagai berikut : Kompos adalah hasil dekomposisi parsial/tidak lengkap, dipercepat secara artifisial dari campuran bahan-bahan organik oleh populasi berbagai macam mikroba dalam kondisi lingkungan yang hangat, lembab, dan aerobik.
6
Beberapa kegunaan kompos adalah: 1. Memperbaiki struktur tanah.
2. Memperkuat daya ikat agregat (zat hara) tanah berpasir 3. Meningkatkan daya tahan dan daya serap air
4. Memperbaiki drainase dan pori-pori dalam tanah 5. Menambah dan mengaktifkan unsur hara
Kompos digunakan dengan cara menyebarkannya di sekeliling tanaman. Kompos yang layak digunakan adalah yang sudah matang, ditandai dengan menurunnya temperatur kompos di bawah 40oC (Djuarni, Nan.Ir,Msc.,dkk, 2006).
2.3 Aktivator
Gaur (1983) diacu dalam Nengsih (2002) mendefinisikan bahwa setiap zat atau bahan yang dapat mempercepat penguraian bahan organik disebut dengan aktivator. Aktivator mempengaruhi proses penguraian bahan organik melalui dua cara, cara pertama yaitu dengan menginokulasi strain mikroorganisme yang efektif dalam menghancurkan bahan organik (pada aktivator organik), kedua yaitu meningkatkan kadar nutrisi makanan bagi mikroorganisme tersebut. Aktivator terdiri dari dua jenis yaitu aktivator organik yang terdiri dari aktivator organik alami seperti pupuk kandang, fungi, dan tanah kaya humus dan aktivator buatan contohnya OST (Organic Soil Treatment), EM4 dan Gt 1000-Wta dan aktivator kimia seperti asam
asetat, amonium sulfat, urea, dan amoniak.
2.4 EM4 (Effective Microorganisme 4)
Teknologi EM4 (Effective Microorganisme 4) adalah teknologi fermentasi
yang dikembangkan pertama kali oleh Prof Dr Teruo Higa dari University Of The Ryukyus, Okinawa Jepang sejak tahun 1980. EM4 merupakan kultur campuran dari
beberapa mikroorganisme yang menguntungkan bagi pertumbuhan tanaman. Mikrooranisme alami yang terdapat dalam EM4 bersifat fermentasi (peragian) terdiri
7
sp.), jamur fermentasi (Saccharonzyces sp.), bakteri asam laktat (Lactobacillus sp.), dan Actinomycetes. EM4 merupakan biofertilizer yang diaplikasi sebagai inokulan
untuk meningkatkan keragaman dan populasi mikroorganisme di dalam tanah. EM4
mampu mempercepat dekomposisi limbah dan sampah organik, meningkatkan ketersediaan nutrisi tanaman, dan rnenekan aktivitas mikroorganisme patogen. Selain itu EM4 juga dapat digunakan untuk membersihkan air limbah, serta meningkatkan
kualitas air pada tambak udang dan ikan (Indriani 1999).
Bakteri fotosintetik merupakan bakteri yang dapat mensintesis senyawa nitrogen, dan gula. Jamur fermentatif berfungsi untuk memfermentasi bahan organik menjadi senyawa-senyawa organik (dalam bentuk alkohol, gula, dan asama amino) yang siap diserap oleh perakaran tanaman. bakteri asam laktat terutama golongan Lactobacillus sp. berfungsi untuk memfermentasi bahan organik menjadi senyawa-senyawa asam laktat yang dapat diserap oleh tanaman. Actinomycetes merupakan bakteri yang tumbuh dalam bentuk miselium (filamen berbentuk jalinan benang). Actinotnycetes berfungsi mengambil asam amino dan zat yang dihasilkan oleh jamur fermentatif dan mengubahnya menjadi antibiotik yang bersifat toksik terhadap patogen atau penyakit serta dapat melarutkan ion-ion fosfat dan ion-ion mikro laimya. Streptonzyces sp. menghasikan enzim steptomisin yang berguna bagi tanaman (Wididana et al. 1996 diacu dalam Nengsih 2002).
Mikroorganisme yang terdapat dalam EM4 dapat bekerja efektif menambah
unsur hara apabila bahan organik dalam keadaan cukup. Bahan organik tersebut merupakan bahan makanan dan sumber energi. Dalarn penggunaan EM4
8
2.5 Proses Pengomposan
Penguraian suatu senyawa ditentukan oleh suatu bahan, dimana pada umumnya senyawa organik mempunyai sifat yang cepat diuraikan, sedangkan senyawa anorganik mempunyai sifat sukar diuraikan.Proses biologi merupakan proses alami yang bersifat dinamis dan kontinu selama faktor-faktor yang berhubungan dengan kebutuhan hidup mikroorganisme yang berperan didalamnya terpenuhi.
Penguraian bahan organik akan berlangsung melalui jalur-jalur proses yang sudah dikenal,yang secara keseluruhan disebut dengan fermentasi. Campuran bahan yang sudah ditambah bioaktivator difermentasi dengan cara menutup dengan menggunakan terval dan membiarkannya selama 5-7 hari. Pada hari kedua atau ketiga, temperatur bahan kompos akan meningkat menjadi 40-600 C. Jika temperatur meningkat, tumpukan bahan tersebut harus dibalik, kemudian ditutup lagi. Tiga hari kemudian temperatur akan turun kembali dan berangsur-angsur stabil, bahan tersebut sudah menjadi kompos dan siap dikemas atau digunakan. (Sofian,2006).
Sumber bahan organik tanah adalah jaringan tanaman baik yang berupa serasah atau sisa tanaman yang berupa batang, akar, daun, yang kemudian dirombak oleh mikroorganisme tanah, atau sisa hewan yang berupa kotoran maupun bangkai hewan. Secara kimiawi bahan organik tanah tersusun atas karbohidrat, protein lignin dan sejumlah senyawa kecil seperti lemak, lilin dan sebagainya, salah satu hasil perombakan bahan organik adalah humus, yang mempunyai kapasitas pengikat unsur hara dan air yang sangat tinggi, memiliki kekhususan koloidal dan mampu mengikat air 80-90% dari berat keringnya, bandingkan dengan tanah liat yang hanya mampu mengikat air 15-20% saja. Humus memberi warna tanah menjadi agak kehitaman dan sangat bermanfaat bagi pertanian karena mempengaruhi struktur tanah.
9
bahan organik yang cepat lapuk. Walaupun demikian peranan oksigen yang terkandung dalam tanah sangat penting, karena berkurangnya kadar oksigen juga berpengaruh pada aktivitas mikroorganisme dalam penguraian. Ini berkaitan dengan ketersediaan unsur hara dari bahan organik yang bisa diserap tanaman.(M,Isnaini,2006)
Reaksi-reaksi yang terjadi pada proses pengomposan yaitu : Reduksi Sulfat :
CH3CHOHCOOH + SO42- 2CH3COOH + H2S + 2OH
4H2 + SO42- 2H2O + H2S + 2OH-
Reduksi karbon organik secara anaerobik : CH3COOH CH4 + CO2
4CH3OH 3CH4 + CO2 + 2H2O
C6H12O6 bakteri 3CH3COOH
C6H12O6 kapang 2CH3CH2OH + 2CO2
Reduksi karbon dioksida :
2CH3CH2OH + 2O2 2CH3COOH + CH4
4H2 + CO2 CH4 + H2O
4H2 + 2CO2 CH3COOH + 2H2O
Reduksi oksidasi sempurna :
CH3COOH + 2O2 CO2 + 2H2O
2H2 + O2 2H2O
CH4 + 2O2 CO2 + 2H2O
10
2.6 Faktor-Faktor Yang Mempengaruhi Proses Pembuatan Kompos
Setiap organisme pendegrasi bahan organik membutuhkan kondisi lingkungan dan bahan yang berbeda-beda. Apabila kondisinya sesuai, maka dekomposer tersebut akan bekerja giat untuk mendekomposisi limbah padat organik. Apabila kondisinya kurang sesuai atau tidak sesuai, maka organisme tesebut akan dorman, pindah ke tempat lain, atau bahkan mati. Menciptakan kondisi yang optimum untuk proses pengomposan sangat menentukan keberhasilan proses pengoposan itu sendiri.
11
2.6.1 Rasio C/N
Rasio C/N yang efektif untuk proses pengomposan berkisar antara 30 : 1 hingga 40 : 1. Mikroba memecah senyawa C sebagai sumber energy dan menggunakan N untuk sintesa protein. Pada rasio C/N diantara 30 s/d 40 mikroba mendapatkan cukup C untuk energi dan N untuk sintesis protein. Apabila rasio C/N terlalu tinggi, mikroba akan kekurangan N untuk sintesis protein sehingga dekomposisi berjalan lambat.
2.6.2 Ukuran Partikel
Aktivitas mikroba berada diantara permukaan area dan udara. Permukaan area yang lebih luas akan meningkatkan kontak antara mikroba dengan bahan dan proses dekomposisi akan berjalan lebih cepat. Ukuran partikel juga menentukan besarnya ruang antar bahan (porositas). Untuk meningkatkan luas permukaan dapat dilakukan dengan memperkecil ukuran partikel bahan tersebut.
2.6.3 Aerasi
Pengomposan yang cepat dapat terjadi dalam kondisi yang cukup oksigen (aerob). Aerasi secara alami akan terjadi pada saat terjadi peningkatan suhu yang menyebabkan udara hangat keluar dan udara yang lebih dingin masuk ke dalam tumpukan kompos. Aerasi ditentukan oleh posiritas dan kandungan air bahan (kelembaban). Apabila aerasi terhambat, maka akan terjadi proses anaerob yang akan menghasilkan bau yang tidak sedap. Aerasi dapat ditingkatkan dengan melakukan pembalikan atau mengalirkan udara di dalam tumpukan kompos.
2.6.4 Porositas
12
pengomposan. Apabila rongga dipenuhi oleh air, maka pasokan oksigen akan berkurang dan proses pengomposan juga akan terganggu.
2.6.5 Kelembaban (Moisture content)
Kelembaban memegang perananyang sangat penting dalam proses metabolisme mikroba dan secara tidak langsung berpengaruh pada suplay oksigen. Mikroorganisme dapat memanfaatkan bahan organik tersebut larut di dalam air. Kelembaban 40 – 60 % adalah kisaran optimum untuk metabolisme mikroba. Apabila kelembaban di bawah 40%, aktivitas mikroba akan mengalami penurunan dan akan lebih rendah lagi pada kelembaban 15%. Apabila kelembaban lebih besar dari 60%, hara akan tercuci, volume udara berkurang, akibatnya aktivitas mikroba akan menurun dan akan terjadi fermentasi anaerob yang menimbulkan bau tidak sedap.
2.6.6 Temperatur
Panas dihasilkan dari aktivitas mikroba. Ada hubungan langsung antara peningkatan suhu dengan konsumsi oksigen. Semakin tinggi temperatur akan semakin banyak konsumsi oksigen dan akan semakin cepat pula proses dekomposisi. Peningkatan suhu dapat terjadi dengan cepat pada tumpukan kompos. Temperatur yang berkisar antara 30 - 60oC menunjukkan aktivitas pengomposan yang cepat. Suhu yang lebih tinggi dari 60oC akan membunuh sebagian mikroba dan hanya mikroba thermofilik saja yang akan tetap bertahan hidup. Suhu yang tinggi juga akan membunuh mikroba-mikroba patogen tanaman dan benih-benih gulma.
2.6.7 pH
13
contoh, proses pelepasan asam, secara temporer atau lokal, akan menyebabkan penurunan pH (pengasaman), sedangkan produksi amonia dari senyawa-senyawa yang mengandung nitrogen akan meningkatkan pH pada fase-fase awal pengomposan. pH kompos yang sudah matang biasanya mendekati netral.
2.6.8 Kandungan hara
Kandungan P dan K juga penting dalam proses pengomposan dan biasanya terdapat di dalam kompos-kompos dari peternakan. Hara ini akan dimanfaatkan oleh mikroba selama proses pengomposan.
2.6.9 Kandungan bahan berbahaya
Beberapa bahan organik dapat mengandung bahan-bahan yang berbahaya bagi kehidupan mikroba. Logam-logam berat seperti Mg, Cu, Zn, Nickel, Cr adalah beberapa bahan yang termasuk kategori berbahaya untuk kehidupan mikroorganisme. Logam-logam berat akan mengalami imobilisasi selama proses pengomposan.
(http://www.ipard.com)
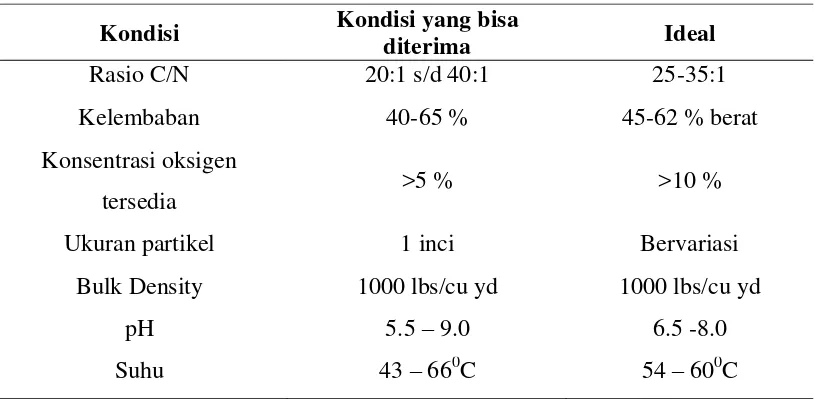
Tabel 2.6 Kondisi yang optimal untuk mempercepat proses pengomposan (Rynk, 1992)
Kondisi Kondisi yang bisa
diterima Ideal
Rasio C/N 20:1 s/d 40:1 25-35:1
Kelembaban 40-65 % 45-62 % berat
Konsentrasi oksigen
tersedia >5 % >10 %
Ukuran partikel 1 inci Bervariasi
Bulk Density 1000 lbs/cu yd 1000 lbs/cu yd
pH 5.5 – 9.0 6.5 -8.0
14
2.7. Kompos matang
Stabilitas dan kematangan kompos adalah beberapa istilah yang sering dipergunakan untuk menentukan kualitas kompos. Stabil merujuk pada kondisi kompos yang sudah tidak lagi mengalami dekomposisi dan hara tanaman secara perlahan (slow release) dikeluarkan ke dalam tanah. Stabilitas sangat penting untuk menentukan potensi ketersediaan hara di dalam tanah atau media tumbuh lainnya. Kematangan adalah tingkat kesempurnaan proses pengomposan. Pada kompos yang telah matang, bahan organik mentah telah terdekomposisi membentuk produk yang stabil.
Untuk mengetahui tingkat kematangan kompos dapat dilakukan dengan uji dilaboratorium untuk pengamatan sederhana di lapangan. Berikut ini disampaikan cara sederhana untuk mengetahui tingkat kematangan kompos :
1. Dicium/dibaui
Kompos yang sudah matang berbau seperti tanah dan harum, meskipun kompos dari sampah kota. Apabila kompos tercium bau yang tidak sedap, berarti terjadi fermentasi anaerobik dan menghasilkan senyawa-senyawa berbau yang mungkin berbahaya bagi tanaman. Apabila kompos masih berbau seperti bahan mentahnya berarti kompos belum matang.
2. Warna kompos
Warna kompos yang sudah matang adalah coklat kehitam-hitaman. Apabila kompos masih berwarna hijau atau warnanya mirip dengan bahan mentahnya berarti kompos tersebut belum matang.
3. Penyusutan
Terjadi penyusutan volume/bobot kompos seiring dengan kematangan kompos. Besarnya penyusutan tergantung pada karakteristik bahan mentah dan tingkat kematangan kompos. Penyusutan berkisar antara 20 – 40 %. Apabila penyusutannya masih kecil/sedikit, kemungkinan proses pengomposan belum selesai dan kompos belum matang.
15
4. Tes kantong plastik
Contoh kompos diambil dari bagian dalam tumpukan. Kompos kemudian dimasukkan ke dalam kantong plastik, ditutup rapat, dan disimpan didalam suhu ruang selama kurang lebih satu minggu. Apabila setelah satu minggu kompos berbentuk baik, tidak berbau atau berbau tanah berarti kompos telah matang.
5. Tes Perkecambahan berkecambah. Bandingkan jumlah kecambah yang tumbuh di dalam kompos dan di atas kapas basah. Kompos yang matang dan stabil ditunjukkan oleh banyaknya benih yang berkecambah
6. Suhu
Suhu kompos yang sudah matang mendekati dengan suhu awal pengomposan. Suhu kompos yang masih tinggi, atau di atas 50oC, berarti proses pengomposan masih berlangsung aktif.
7. Kandungan air kompos
Kompos yang sudah matang memiliki kandungan kurang lebih 55-65%. Cara mengukur kandungan air kompos adalah sebagai berikut:
• Ambil sampel kompos dan ditimbang
• Kompos dikeringkan di dalam oven atau microwave hingga beratnya konstan, kompos ditimbang kembali
• Kandungan air kompos dihitung dengan rumus sebagai berikut :
16
2.8 Standar Pupuk Kompos
Indonesia telah memiliki standar kualitas kompos, yaitu SNI 19-7030-2004 dan Peraturan Menteri Pertanian No. 02/Pert/HK.060/2/2006. Di dalam standar ini termuat batas-batas maksimum atau minimum sifat-sifat fisik atau kimiawi kompos, termasuk di dalamnya batas maksimum kandungan logam berat. Untuk memastikan apakah seluruh kriteria kualitas kompos ini terpenuhi maka diperlukan analisis laboratorium. Pemenuhan atas standar tersebut adalah penting, terutama untuk kompos yang akan dijual di pasaran. Standar itu menjadi salah satu jaminan bahwa kompos yang akan dijual benar-benar merupakan kompos yang siap diaplikasikan dan tidak berbahaya bagi tanaman, manusia, maupun lingkungan.
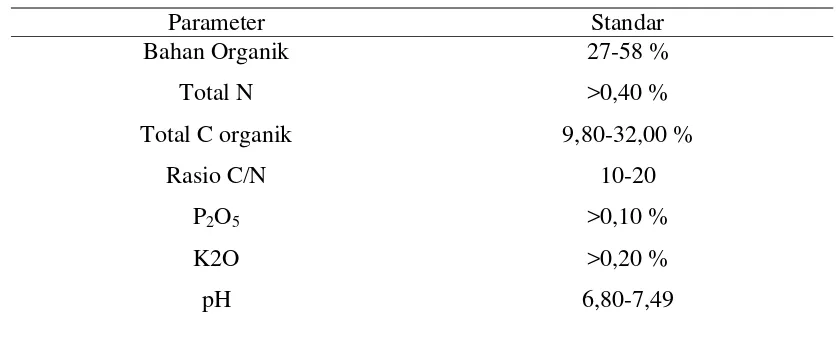
Tabel.2.8 Standar kualitas pupuk kompos berdasarkan SNI 19-7030-2004
Parameter Standar
17
BAB 3
METODE PENELITIAN
3.1 Alat-alat yang digunakan.
Alat-alat yang dipergunakan dalam penelitian ini adalah :
1. Buret Pyrex
2. Statif/klemp
3. Labu erlemeyer Pyrex
4. Beaker glass 250 ml Pyrex
5. Pipet volumentri 10 ml Pyrex
6. Pipet volumentri 5 ml Pyrex
7. Labu takar 100 ml Pyrex
8. Labu kjehldahl Pyrex
9. Pipet ukur 5 ml Pyrex
10. Thermometer
11. Spektrofotometer Visibel
12. Spektrofotometer Serapan Atom
13. Magnit stirier
14. Toples plastik
15. Timbangan teknis ohaus 16. Pisau pencacah
18
3.2 Bahan-bahan yang digunakan.
Bahan-bahan yang digunakan dalam penelitian ini adalah : 1. Limbah ikan
2. Larutan EM4
3. P.a
4. Fe . O P.a
5. NaOH P.a
6. Fenolftalein P.a
7. Metil Merah P.a
8. Metil Biru P.a
9. . O P.a
10. HCL P.a
11. P.a
12. P.a
13. Selenium P.a
14. Akuades
3.3 Prosedur Penelitian.
3.3.1 Penyediaan Sampel Limbah Ikan
Limbah ikan diambil di TPI dan Pasar Tradisionil Sibolga
3.3.2 Pengaptifan EM4
Kedalam Toples plastik di masukkan sebanyak 10 ml EM4. Selanjutnya di tambahkan
tetes tebu 10 ml dan substrat jumlah maksimum 1% { (NH4)3PO4 dan KCl} aduk
19
3.3.3 Pembuatan pupuk kompos.
Kedalam wadah plastik berpori masukkan 2 kg limbah ikan yang sudah dihaluskan dengan kadar air 15,08% , lalu dimasukkan larutan EM4 aktif hingga lembab dan
dibiarkan selama 3 minggu. Analisa kadar C, N, P, dan K dilakukan pada hari 0, 2, 5, 10, 15, 20
3.3.4 Pembuatan Pereaksi dan Larutan Standar.
3.3.4.1 Pembuatan Pereaksi untuk Penentuan Nitrogen Metode Kjeldhal a. Larutan NaOH 40%
Ditimbang sebanyak 40 gr kristal NaOH, dimasukkan kedalam gelas piala 250 ml, kemudian dilamtkan dengan aquades, dimasukkan ke dalam labu takar 100 ml, diencerkan hingga garis tanda dan dikocok sampai homogen.
b. Larutan Indikator Phenolphtalein 1%
Ditimbang kristal fenolphtalein sebanyak 1gr kemudian dilarutkan dengan alkohol 96% dimasukkan kedalam labu takar 100 ml, diencerkan hingga garis tanda, dan dikocok sampai homogen.
c. Larutan H3BO3 3 %
Ditimbang H3BO3 sebanyak 3 gr, dimasukkan kedalam gelas piala 250 ml,
dilarutkan dengan aquades, dimasukkan kedalam labu takar 100 ml,diencerkan hingga garis tanda dan dikocok sampai homogen.
d. Larutan Indikator Campuran
Sebanyak 2 ml larutan indikator metil biru 0,1% (b/v ) didalam alkohol, dicampurkan dengan 1 ml larutan indikator metil merah 0,2% (b/v) kemudian dihomogenkan.
e. Larutan H2C2O4 0,01 N
Ditimbang kristal H2C2O4.2H2O secara kuantitatif sebanyak 0,63 gr, dimasukkan
20
f. Larutan NaOH 0,01 N
Ditimbang kristai NaOH sebanyak 0,40 gr, dimasukkan ke dalam gelas piala 250 ml, dilarutkan dengan aquades, dimasukkan ke dalam labu takar 1000 ml, diencerkan hingga garis tanda, dan dikocok sampai homogen.
g. Standarisasi Larutan NaOH 0,01 N
- Di pipet 10 ml larutan H2C2O4 0,01 N dimasukkan ke dalam gelas erlemeyer
- Ditambahkan 3 tetes indikator fenolphtalein.
- Dititrasi dengan NaOH hingga terjadi perubahan warna menjadi merah lembayung.
- Dilakukan hal yang sama sebanyak 3 kali.
h. Larutan HCI 0,01 N
Sebanyak 0,83 ml HCI 37% dipipet ke dalam labu takar 1000 ml, diencerkan hingga garis tanda dengan aquades, dan dikocok sampai homogen.
i. Standarisasi HCI 0,01 N
- Dipipet 10 ml larutan HCI 0,01 N dimasukkan ke dalam gelas erlemeyer - Ditambahkan 3 tetes indikator bromtimol blue
- Dititrasi dengan NaOH yang telah distandarisasi hingga terjadi perubahan warna biru menjadi hijau kekuningan
- Dilakukan hal yang sama sebanyak 3 kali.
3.3.4.2 Pembuatan pereaksi dan larutan standar untuk penentuan Posfor dengan metode Spektrofotometri
a. Larutan HCI 25%
Dengan menggunakan gelas ukur 100 ml dituang 173,6 ml HCI(p), dimasukkan
21
b. Larutan Standar Posfor 100 ppm
Di timbang 0,2195 g krislal KH2PO4 secara kuantitatif, dimasukkan ke dalam
gelas piala 250 ml, dilarutkan dengan aquades secukupnya, diraasukkan ke dalam labu takar 500 ml, diencerkan dengan aquades hingga garis tanda dan dikocok sampai homogen.
c. Larutan Amonium Molibdat 4%
Di timbang 1,883 g kristal (NH4)6Mo7O24.4H2O, dimasukkan ke dalam gelas
piala 50 ml, dilarutkan dengan aquades secukupnya, dimasukkan kedalam labu takar 50 ml, diencerkan dengan aquades hingga garis tanda, dan dikocok sampai homogen.
d. Larutan Asam Askorbat 0,1 M
Di timbang 0,880 gr kristal C6H8O6, dimasukkan ke dalam gelas piala 50 ml,
diencerkan dengan aquades secukupnya, dimasukkan kedalam labu takar 50 ml, diencerkan dengan aquades hingga garis tanda, dan dikocok sampai homogen.
e. Larutan Kalium antimonil Tartarat 1 mg /ml
Ditimbang 0,105 gr kristal KSbOC4H4O6.½H2O, dimasukkan ke dalam gelas
piala 50 ml, dilarutkan dengan aquades secukupnya, dimasukkan kedalam labu takar 50 ml, diencerkan dengan aquades hingga garis tanda, dan dikocok sampai homogen.
f. Larutan Seri Standar Posfor dalam ekstrak HCI 0,95 N
Dipipet masing-masing 20 ml aquades dan 11,7 ml HCI 25% ke dalam labu takar 100 ml. dipipet 2 ml, 4 ml, 6 ml, 8 ml, 10 ml larutan standar 100 ppm secara kuantitatif diencerkan dengan aquades hingga garis tanda, dan dikocok sampai homogen.
g. Larutan H2SO4 5 N
Dipipet 13,72 ml H2SO4 (p),dimasukknn ke dalam labu takar 100 ml yang telah
22
h. Pembuatan Larutan Campuran Pengkompleks
Dipipet 25 ml H2SO4 5 N ke dalam labu takar 50 ml, ditambahkan 7,5 ml larutan
(NH4)6Mo7O24 4%, ditambahkan 15 ml larutan asam askorbat 0,1 M,
ditambahkan 2,5 ml larutan KSbOC4H4O6 0,1 M. dan dikocok sampai homogen.
3.3.4.3 Pembuatan Pereaksi Untuk Penentuan Kalium Dengan Spektrofotometer Serapan Atom (SSA)
a. Larutan HCl 25%
Dipipet 173,6 ml HC1 (p), dimasukkan ke dalam labu takar 250 ml, diencerkan
dengan aquades hingga garis tanda dan dikocok sampai homogen.
b. Larutan Kalium 100 ppm
Dilarutkan 1,907 g KCl p.a. dengan aquades dalam labu takar 1000 ml hingga garis tanda. Larutan ini mengandung 1 mg /l Kalium.
c. Larutan Standar Kalium 100 ppm
Sebanyak 10 ml larutan standar kalium 1000 ppm diencerkan dengan aquades dalam labu takar 100 ml hingga garis tanda.
d. Larutan Seri Standard Kalium untuk kalibrasi (0.0 - 5 - 10 - 15 - 20 ppm)
Dari larutan standar 100 ppm kalium masing-masing dipipet 0,0 ; 5 ; 10 ; 15 ; 20, ml, kemudian masing-masing diencerkan dengan aquades dalam labu takar 100 ml hingga garis tanda. Masing - masing larutan adalah 0,0; 5 ; 10 ; 15 ; 20 ppm kalium.
3.3.5 Penentuan Kadar C-Organik dengan metode Gravimetri a. Kadar Air
Ditimbang 1,00 gr sampel ke dalam botol yang sudah diketahui bobot kosongnya
Dipanaskan dalam oven dengan suhu 1050C selama 3 jam
23
b. Kadar Abu
Ditimbang 1,00 gr sampel ke dalam cawan porselin yang sudah di bobot kosongnya
Diabukan dalam tanur dengan suhu 550 0C
Dinginkan di dalam desikator selama 30 menit kemudian timbang
Kadar C-Organik dapat diketahui dengan mengurangkan berat sampel dengan kadar air dan kadar abu
3.3.6 Pengukuran Nitrogen dengan Metode Kjeldahl
- Sebanyak 1,00 gr sampel dimasukkan kedalam labu Kjehldah - Ditambahkan 0,30 gr selenium dan 25 ml H2SO4 pekat
- Didekstruksi hingga sampel berubah menjadi larutan coklat kehitaman - Dipindahkan ke dalam labu destilasi dan ditambahkan 50 ml aquades
- Ditambahkan 3 tetes indikator Fenolphtalein dan NaOH 40% sehingga berwarna merah lembayung
- Destilat ditampung dengan labu Erlemeyer yang berisi 50 ml H3BO3 3% dan 3
tetes indikator campuran
- Dipasang tabung destilasi pada alat destilasi
- Dilakukan destilasi hingga diperoleh warna hijau muda
- Destilat kemudian dititrasi dengan HCl 0,01 N sampai terbentuk merah lembayung - Dicatat volume titran dan tentukan % N
24
3.3.7 Penentuan Posfor dengan Metode Spektrofotometri 3.3.7.1 Preparasi Sampel
Sebanyak 1 ml sampel dimasukkan ke dalam gelas erlemeyer 250 ml, ditambahkan dengan 12,5 ml HCI 25%, dikocok dengan pengaduk magnit stirier selama 2 jam, disaring dengan kertas saring whatman no.40, ditampung ekstrak ke dalam labu takar 100 ml, diencerkan dengan aquades hingga garis tanda, dan di kocok sampai homogen.
3.3.7.2 Pembuatan Kurva Kalibrasi.
Dipipet 1 ml masng-masing larutan standar ke dalam tabung reaksi, ditambahkan 5 ml aquades, ditambahkan 1 ml larutan campuran, didiamkan selama 15 menit, diukur absorbansinya dengan spektrofotometer, pada λ = 400 nm, dibuat kurva kalibrasi konsentrasi terhadap absorbansi.
3.3.7.3. Penentuan Kadar Posfor.
Dipipet 1 ml sampel ke daiam tabung reaksi, ditambahkan 5 ml aquades, ditambahkan 1 ml larutan campuran, didiamkan selama 15 menit, diukur absorbansinya dengan spektrofotomeler, pada λ = 400 nm.
3.3.8. Penentuan Kalium Dengan Alat Spektrefotometer Serapan Atom (SSA)
- Sebanyak 5 ml sampel dimasukkan ke dalam erlemeyer 100 ml
- Ditambahkan 12,5 ml HCl 25% ke dalam erlemeyer 100 mlyang berisi sampel - Larutan dibiarkan selama 1 malam
- Kemudian diaduk dengan pengaduk magnit stirer seiama 2 jam sampai terbentuk suspensi
- Lalu disaring dengan menggunakan kertas saring whotman No. 40, filtrat masukkan ke dalam labu takar 100 ml sambil dicuci sebanyak 3 kali dengan aquades, lain tambahkan aquades sampai garis tanda
- Filtrat disimpan didalam botol plastik untuk penetapan kadar kalium
25
3.4. Bagan Penelitian
3.4.1. Pembuatan pupuk kompos
Dikeringkan dgn sinar matahari Di giling halus
Pembalikan
Uji penentuan C,N,P,K pada 0,2,5,10,15,20 hari
Limbah ikan dicacah
Dimasukkan dalam wadah
Ditambahkan larutan EM4 yang telah diaktifkan
Proses pengomposan
26
3.4.2. Penentuan kadar C – Organik dengan Metode Gravimetri a. Penentuan Kadar Air
Suhu 1050C ditimbang
b. Penentuan kadar Abu
Panaskan dengan Suhu 5500C Di dinginkan selama 30 menit dalam desikator
Ditimbang
Diulang prosedur yang sama sampai berat konstan
1,00 gr Sampel
Hasil
Hasil Akhir 1,00 gr Sampel
Dipanaskan 3 jam
27
c. Kadar C-Organik
C-Organik = 100% - (Kadar Air + Kadar Abu
3.4.3. Penentuan Kadar Nitrogen Pupuk Kompos dengan Metode Kjehldal
Tambahkan 0,3 g Selenium dan H2SO4 pekat
Didekstruksi hingga menjadi larutan coklat kehitaman
Dipindahkan ke dalam labu destilasi Ditambahkan 50 ml aquades
Ditambahkan 3 tetes indikator Phenolphtalein Tambahkan 30 ml NaOH 40%
Dipanaskan
Tampung di dalam gelas erlemeyer yang berisi 50 ml H3BO3 3% dan 3 tetes indikator
campuran titrasi dengan HCl 0,01N
Tentukan % Nitrogen 1,00 gr sampel
Larutan coklat
Larutan Destilat berwarna hijau
Larutan Merah Muda
28
3.4.4. Penentuan Posfor denganMetode Spektrofotometri 3.4.4.1. Pembuatan ekstrak
Ditambahkan 12,5 ml HCL 25%
Dikocok selama 2 jam dengan pengaduk dengan kecepatan 20 rpm
Disaring dengan kertas saring whatman no. 40
Kocok sampai homogen
Masukkan ke dalam labu takar 100 ml
Encerkan dengan aquades hingga garis tanda 1,00 gr sampel
Ekstrak pupuk kompos
Residu
29
3.4.4.2. Pengukuran Absorbansi Larutan Standar Posfor untuk kurva Kalibrasi larutan Standar 2 ppm
Masukkan ke dalam tabung reaksi Tambahkan 5 ml aquades
Tambahkan 1 ml larutan campuran pengkompleks
Ukur absorbansinya dengan spektorfotometer pada
λ 400 nm
3.4.4.3. Pengukuran Absorbansi untuk ekstrak pupuk kompos
Masukkan ke dalam tabung reaksi Tambahkan 5 ml aquades
Tambahkan 1 ml larutan campuran pengkompleks Diamkan selama 15 menit
Ukur Absorbansinya dengan spektorfotometer pada
λ – 400 nm 1 ml larutan
standar 2 ppm
Larutan berwarna
Hasil
1 ml larutan ekstrak pupuk
organik cair
Larutan berwarna biru
30
3.4.5 Penentuan Kalium dengan Alat Spektrofotometer Serapan Atom
Masukkan ke dalam erlenmeyer 100 ml Larutkan dengan 12,5 ml HCl 25% Didesktruksi selama 3 jam
Dinginkan, lalu disaring
Encerkan dengan aquades sampai garis tanda Dinginkan pada suhu kamar selama 12 jam
Disaring dengan kertas saring Whatman No. 40 Cawan dicuci dengan aquades
Kertas saring dicuci dengan aquades
Buat pH = 3 dengan penambahan NH4OH 20% tetes
demi tetes
Encerkan dengan aquades hingga garis tanda
Konsentrasi K diukur dengan Spektrofotometer Serapan Atom
5,00 gr sampel
Larutan biru
Filtrat (dalam labu takar 100
ml)
Endapan dibuang
31
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
Data hasil penentuan C-Organik dengan Metode Gravimetri dapat dilihat pada tabel 4.1, data hasil penentuan Nitrogen dengan Metode Kjehldal dapat dilihat pada tabel 4.2, data hasil penentuan Posfor dengan Metode Spektrometri dapat dilihat dengan pada table 4.3 dan data hasil pengukuran Kalium dengan alat Spektrofotometer Serapan Atom (SSA) dapat dilihat pada tabel 4.4.
32
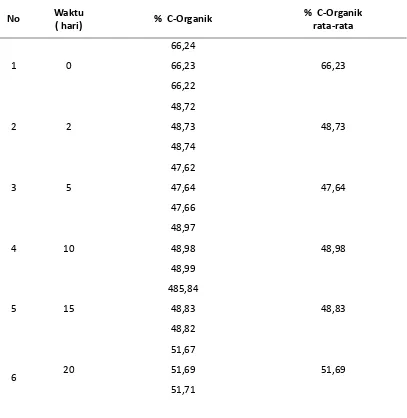
4.1.1 Data Analisa C-organik Pupuk Kompos dari Limbah Ikan TPI dan Pasar Tradisional Sibolga
35
4.1.4. Data Analisa Kalium Pupuk Kompos dari Limbah Ikan TPI dan Pasar Tradisional Sibolga
36
4.2 Pembahasan
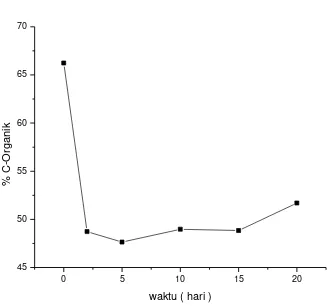
Gambar 4.2.1 Kurva Perubahan Kadar C-Organik Vs Waktu
Dari kurva gambar 4.2.1 diatas terlihat bahwa sebelum pengomposan kadar C-organik yang tersedia adalah adalah 66,23%. Pada pengomposan sampai hari ke 5 mengalami penurunan sampai 47,64% dan kembali mengalami peningkatan pada hari ke 10 sampai hari ke 20 yaitu 48,98% - 51,69%. Perubahan kadar C-organik tersebut disebabkan karena adanya aktivitas mikroorganisme untuk medekomposisi bahan karbon akan di rombak oleh mikroorganisme dan digunakan sebagai sumber energi dalam proses metabolisme dan perbanyakan sel diubah menjadi CO2 dan H2O secara
0 5 10 15 20
45 50 55 60 65 70
%
C
-O
rg
a
n
ik
37
aerob dan anaerob senyawa C-organik berubah menjadi asam organik dan alkohol terlebih dahulu kemudian diubah menjadi CO2, CH4, dan H2O (Yuwono,D,2006).
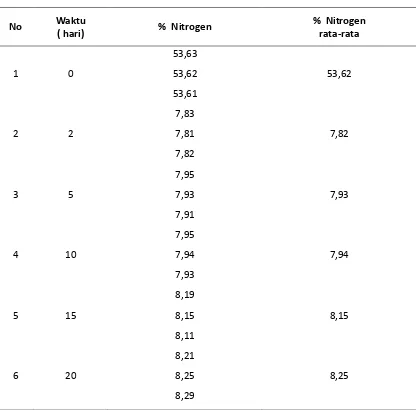
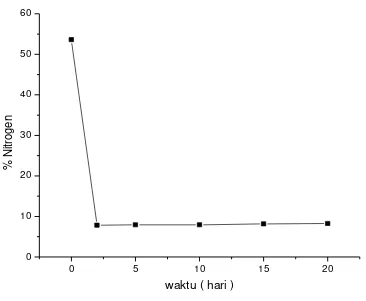
Gambar 4.2.2 Kurva Perubahan Kadar Nitrogen vs Waktu
Dari gambar 4.2.2 diatas terlihat bahwa sampel pupuk kompos dari limbah ikan TPI dan pasar tradisinal Sibolga sebelum pengomposan mengandung 53,62% kadar Nitrogen, namun mengalami penurunan dan peningkatan pada saat pengomposan. Hal ini disebabkan dalam proses pengomposan Nitrogen terlebih dahulu diubah menjadi ammonia (NH3) yang mudah menguap kemudian menjadi
nitrit (NO2-) dan nitrat (NO3-) yang merupakan bentuk Nitrogen yang stabil. Pada
pengomposan hari ke 2 kandungan Nitrogen menurun sampai kadar 7,82%, tetapi
0 5 10 15 20
0 10 20 30 40 50 60
%
N
itro
g
e
n
38
kembali mengalami peningkatan mulai hari ke 5 sampai hari ke 20, dari kadar 7,93% - 8,25% keadaan ini disebabkan karena ammonia (NH3) diubah menjadi bentuk lebih
stabil yaitu nitrit (NO2-) dan nitrat (NO3-). (Irma,2008)
Gambar 4.2.3 Kurva Perubahan Kadar Posfor vs Waktu
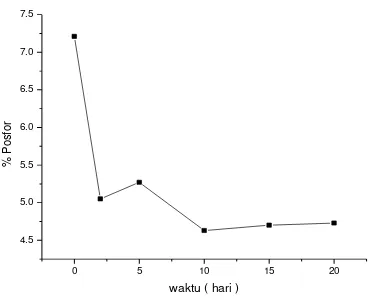
Dari gambar 4.2.3 di atas terlihat bahwa kompos dari limbah TPI dan pasar tradisional Sibolga, sebelum pengomposan mempunyai kadar posfor 7,21%. Dengan adanya proses pengomposan terjadi penurunan dan peningkatan. Dari grafik di gambarkan pada hari ke 2 posfor menurun secara tajam sampai kadar 5,05% , hari ke 5 naik pada kadar 5,27%, hari ke 10 turun pada kadar 4,63%, hari ke 15-20 naik tajam sampai ke kadar 4,73%.
0 5 10 15 20
4.5 5.0 5.5 6.0 6.5 7.0 7.5
%
Posfor
39
Hal ini terjadi karena aktivitas mikroorganisma, penguraian posfor dilakukan oleh bakteri pseudomonas sp dimana bakteri ini dapat menguraikan posfor dari posfor terikat menjadi posfor yang bebas dan sebahagian digunakan untuk metabolisme hidupnya. (Rao,N.S.S.1994)
Gambar 4.2.4 Kurva Perubahan Kadar Kalium vs Waktu
40
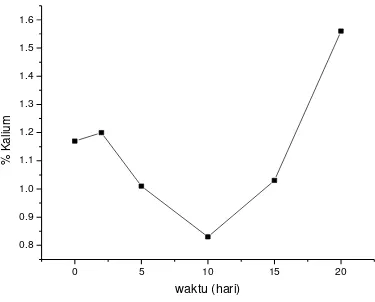
Hal ini di sebabkan karena Kalium digunakan oleh mikroorganisma untuk membentuk kofaktor enzim, lama kelamaan mikroorganisma tersebut akan mati dan akhirnya meninggalkan sisa-sisa berupa mineral Kalium. Sehingga pada akhirnya kompos akan terdekomposisi dengan kadar penumpukan mineral Kalium. (Nurwontoro,1997).
Tabel 4.2.1 Pengujian Kadar C-Organik, Nitrogen, Posfor, dan Kalium dari Pupuk Kompos dari Limbah ikan TPI dan Pasar Tradisional Sibolga.
Parameter Kompos limbah ikan
(%)
Kompos dari limbah ikan mempunyai C/N lebih rendah dari kualitas kompos SNI, hal ini di sebabkan kadar C-Organik dianalisa dgn metoda gravimetri. Penggunaan metode ini mengakibatkan ada karbon menguap sebagai CO2.Untuk
kadar Nitrogen, kompos dari limbah ikan mengandung 8,25%, hal ini menunjukkan jauh lebih baik dari kandungan kualitas kompos SNI. Begitu juga kadar Posfor kompos dari limbah ikan adalah 4,73%, ini membuktikan bahwa kompos dari limbah ikan sangai baik untuk pupuk, karena tumbuhan sangat membutuhkan Posfor dalam bentuk PO4-3, jika dibandingkan dengan kandungan kualitas kompos SNI hanya
0,1%.
41
BAB 5
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
1. Limbah ikan dari Tempat Pelelangan Ikan (TPI) dan Pasar Tradisional Sibolga dapat dimanfaatkan sebagai pupuk kompos.
2. Kadar Nitrogen, Posfor dan Kalium dari pupuk kompos Limbah Ikan Tempat Pelelangan Ikan (TPI) Pasar Tradisional Sibolga cukup tinggi dan layak digunakan untuk tanaman dan memenuhi Standar SNI 19-7030-2004.
5.2 SARAN
42
DAFTAR PUSTAKA
Anas I, Widyastuti, Muluk T. 2005. Pemanfaatan limbah pengolahan ikan Sebagai bahan pupuk organik. Penelitian Hibah Bersaing X. Bogor : Institut Pertanian Bogor.
Anonim. 2012. Kompos. Diunduh dari http : //www.kompos.go.id/htmt, (diakses tanggal 12 April 2012)
Anonim. 2012. Kompos Limbah Padat. Diunduh dari http : //www.ipard.com, (diakses tanggal 15 April 2012)
Badan Standarisasi Nasional (BSN).2004. Spesifikasi Kompos dari Sampah Organik Domestik. SNI 19-7030-2004
Cawford. J. H. Composting of Agricultural Waste, in Biotechnology Application And Researe : Paul N. Cheremisin of and R. P. Quellette (ed).
Djuarni, Nan. Ir,MSc. Ktristiawan, Setiawan, Budi Susilo. (2006). Cara Cepat Membuat Kompos. Jakarta : Agro Media
Indriani YH. 1999. Membuat Kompos Secara Kilat. Jakarta : Penerbit Swadaya Ikan mania.word pres.com/2007/12/3/pemanfaatan-limbah-ikan-sebagai-bahan pupuk-organik (diakses tanggal 15 April 2013)
Irma.2008.Pemanfaatan Hasil Pengolahan Limbah Cair Perikanan dengan Lumpur Aktif sebagai Pupuk Nitrogen Pada Tanaman Bayam.[ skripsi ] Bogor. Institut Pertanian Bogor.
Isnaini,M.2006. Pertanian Organik untuk Keuntungan Ekonomi dan Kelestarian Bumi. Yogyakarta : Kreasi Wacana.
43
Nurwanto.1997. Mikroba Pangan Hewan Nabati. Yogyakarta: Penerbit Kanisius Nurheti Yularti dan Isroi, 2009, Kompos Cara Mudah, Murah, dan cepat
Menghasilkan kompos, Yogyakarta : Andi Offset
Rao, N.S.S. 1994 Mikroba Tanah dan Pertumbuhan Bahan Tanam. EdisiKedua. Jakarta: UI Press
Ryak R. 1992. On Farm Composting Handbook. Nort theast Regional Agricultural Engineering Service PU. No. 54. Cooperative Extension Service.Ithaca, N.Y.1992 : 186 PP A. Classc in on Farm Composting. Website ; www.nreas.org
Sutedjo, M.M. 2002. Pupuk dan Cara Pemupukan. Jakarta : Penerbit Aneka Citra Sofian. 2006. Sukses Membuat Kompos Dari Sampah. Jakarta : PT. Argo Media Simamora, S, Salundik. 2006. Meningkatkan Kualitas Kompos. Jakarta : PTAgro
Media Pustaka.
Sutanto R. 2002, Penerapan Pertanian Organik Pemasyarakatan dan Pengembangannya. Yogyakarta: Kanisius.
Yuliarti.N.2009.1001 Cara Menghasilkan Pupuk Organik. Yogyakarta : Penerbit Andi.
44
Lampiran 1 : Perhitungan penentuan kadar C-Organik,N,P dan K
a. Perhitungan penentuam kadar C-Organik %C-Organik = 100% - (kadar air + kadar abu)
b. Perhitungan penentuan kadar Nitrogen % N =
Keterangan, Vs : Volume Sampel Vb : Volume Blangko
W : Normalitas Larutan Standar Fp : Faktor Pencerahan
W : Berat sampel
c. Perhitungan penentuan kadar kalium
% K
45
d. Perhitungan penentuan kadar Fosfor
% P
46
Lampiran 2: Standar kualitas kompos SNI 19-7030-2004
No Parameter Satuan Minimum Maksimum No Parameter Satuan Minimum Maksimum
1 Kadar air % 0C 50 17 Cobal (Co) mg/kg * 34
Unsur makro Unsur lain
9 Bahan organic % 27 58 25 Calsium (Ca) % * 25,50
47
Lampiran 3 : Gambar bahan - bahan kompos
48
Lampiran 5 : Gambar limbah ikan yang di haluskan