LEMAK DAGING DAN KINERJA PERTUMBUHAN IKAN PATIN Pangasius hypophthalmus YANG DIBERI PAKAN DENGAN RASIO
KARBOHIDRAT DAN LEMAK BERBEDA
RIDWAN TOBUKU
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis “Lemak Daging dan Kinerja Pertumbuhan Ikan Patin Pangasius hypophthalmus yang Diberi Pakan dengan Rasio Karbohidrat dan Lemak Berbeda” adalah benar hasil karya yang belum pernah diajukan dalam bentuk apapun kepada Perguruan Tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Pebruari 2008
RINGKASAN
Penelitian ini dilakukan untuk mengetahui rasio karbohidrat dan lemak pakan yang dapat menghasilkan laju pertumbuhan tinggi dan kadar lemak daging terendah pada ikan patin (Pangasius hypophthalmus). Enam ekor juvenil ikan patin dengan bobot awal 16,1±0,5 g dipelihara selama 60 hari dalam akuarium yang diisi air sebanyak 60 liter. Ikan diberi pakan secara at satiation mengandung karbohidrat dan lemak dengan rasio 1, 2, 3 atau 4. Lemak pakan berkisar antara 7,6% sampai 16,9% dan karbohidrat 16 sampai 31%. Protein pakan 36%, sama untuk semua pakan perlakuan.
ABSTRACT
LEMAK DAGING DAN KINERJA PERTUMBUHAN IKAN PATIN Pangasius hypophthalmus YANG DIBERI PAKAN DENGAN RASIO
KARBOHIDRAT DAN LEMAK BERBEDA
RIDWAN TOBUKU
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Ilmu Perairan
Judul : LEMAK DAGING DAN KINERJA PERTUMBUHAN IKAN PATIN Pangasius hypophthalmus YANG DIBERI PAKAN DENGAN RASIO KARBOHIDRAT DAN LEMAK BERBEDA
Nama : RIDWAN TOBUKU
NRP : C151040011
Program Studi : ILMU PERAIRAN
Disetujui, Komisi Pembimbing
Dr. Dedi Jusadi Prof. Dr. Ing Mokoginta Ketua Anggota
Diketahui
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT, karena taufik dan
rahmat-Nya sehingga tesis berjudul “Lemak Daging dan Kinerja Pertumbuhan Ikan Patin
Pangasius hypophthalmus yang Diberi Pakan Dengan Rasio Karbohidrat dan Lemak Berbeda” dapat diselesaikan.
Sejak penyusunan proposal, pelaksanaan penelitian sampai penulisan tesis ini
tidak terlepas dari bantuan dan bimbingan berbagai pihak. Pada kesempatan ini, penulis
menyampaikan terima kasih kepada:
1. Dr. Dedi Jusadi dan Prof.Dr. Ing Mokoginta selaku komisi pembimbing atas
pengarahan dan bimbingan yang telah diberikan selama penyusunan proposal,
pelaksanaan penelitian dan penulisan tesis.
2. Ketua Program Studi Ilmu Perairan, Ketua dan Staf Laboratorium Nutrisi Ikan
Departemen Budidaya Perairan Fakultas Perikanan dan Ilmu Kelautan Institut
Pertanian Bogor.
3. Almarhumah ibunda Sohadiah Bahasoan dan Almarhum ayahanda Wahab Tobuku
yang telah berjasa.
4. Istri, Siti Nurjannah dan anak-anak, Fuad, Fakhri, dan Aulia.
Akhirnya semoga tesis ini dapat bermanfaat bagi semuanya. Amin .
Bogor, Pebruari 2008
RIWAYAT HIDUP
Penulis dilahirkan di Maluku Utara, pada tanggal 03 Januari 1966 dari pasangan
Wahab Tobuku (Alm) dan Sahadiah Bahasoan (Alm). Penulis merupakan anak keempat
dari lima bersaudara. Penulis lulus SMA pada tahun 1986 dan melanjutkan program
sarjana (S1) di Universitas Hasanuddin, selesai pada Maret 2001. Pada tahun 2003
penulis diterima sebagai Staf Pengajar di Fakultas Pertanian UNDANA, dan tahun 2004
ditugaskan mengikuti pendidikan jenjang magister pada Program Studi Ilmu Perairan
DAFTAR TABEL
Daftar Tabel Halaman 1. Komposisi bahan pakan percobaan (g/100g pakan)...17
2. Komposisi proksimat pakan perlakuan (% bobot kering) ...18
3. Rata-rata konsumsi pakan (FC), retensi protein (RP), retensi lemak (RL), laju pertumbuhan harian (LPH), konversi pakan (FCR) dan kelangsungan hidup (SR) ikan patin selama 60 hari pemeliharaan...22
DAFTAR GAMBAR
DAFTAR LAMPIRAN
Daftar Lampiran Halaman
1. Prosedur analisis proksimat (Takeuchi, 1988) ...32
2. Bobot rata-rata awal dan akhir ikan uji ...35
3. Laju pertumbuhan (%) ikan patin yang diberi perlakuan pakan uji rasio karbohidrat/lemak berbeda...36
4. Komposisi proksimat daging pada akhir percobaan (bobot basah) ...37
5. Komposisi proksimat tubuh pada akhir percobaan (bobot basah) ...38
6. Komposisi proksimat hati pada akhir percobaan (bobot basah) ...39
7. Perhitungan retensi protein...40
8. Perhitungan retensi lemak ...42
9. Perhitungan nilai konversi pakan ...43
10. Analisis ragam dan Uji BNT konsumsi pakan uji selama percobaan...44
11. Analisis ragam dan Uji BNT konversi pakan ...44
12. Analisis ragam dan Uji BNT laju pertumbuhan harian ...45
13. Analisis ragam dan Uji BNT retensi protein ...45
14. Analisis ragam dan Uji BNT retensi lemak...46
15. Analisis ragam dan Uji BNT kadar lemak daging pada akhir percobaan ...46
16. Analisis ragam dan Uji BNT kadar protein daging pada akhir percobaan...47
17. Analisis ragam dan Uji BNT kadar abu daging pada akhir percobaan ...47
20. Analisis ragam dan Uji BNT kadar protein tubuh pada akhir percobaan...49
21. Analisis ragam dan Uji BNT kadar abu tubuh pada akhir percobaan ...49
22. Analisis ragam dan Uji BNT kadar air tubuh pada akhir percobaan...50
23. Analisis ragam dan Uji BNT kadar lemak hati pada akhir percobaan ...50
PENDAHULUAN
Latar Belakang
Pembesaran ikan patin pada umumnya dilakukan di keramba jaring apung
(KJA) dan kolam air tenang, serta sebagian kecil di kolam air deras, namun
kualitas daging yang dihasilkan berbeda. Ikan patin yang tumbuh dan besar di
KJA dan kolam air tenang memiliki daging dengan kandungan lemak tinggi
mencapai 7,98% bobot basah atau 30,59% bobot kering, sedangkan dari kolam air
deras sebesar 3,04% bobot basah atau 13,26% bobot kering (Suwarsito, 2004).
Suwarsito (2004) telah berupaya menurunkan kadar lemak daging ikan
patin dengan menggunakan L-karnitin. Penambahan L-karnitin dalam pakan
sebesar 0,18% telah dapat menurunkankan kadar lemak daging dari 32,25%
menjadi 7,51% bobot kering atau 7,88% menjadi 1,63% bobot basah. Namun cara
ini ternyata tidak ekonomis untuk diaplikasikan karena harga L-karnitin yang
relatif mahal. Cara lain yang mungkin dapat dilakukan untuk menurunkan kadar
lemak daging adalah dengan mengatur imbangan karbohidrat dan lemak dalam
pakan. Menurut Furuichi (1988), lemak tubuh sangat dipengaruhi oleh lemak
pakan. Hasil penelitian pada channel catfish menunjukkan bahwa deposisi lemak
tubuh berhubungan dengan kadar lemak pakan (Garlis & Wilson, 1976 dalam Takeuchi, 1988).
Lemak dan karbohidrat mempunyai sparing effect pada penggunaan atau pemanfaatan protein. Protein akan dimanfaatkan sebagai energi apabila lemak dan
karbohidrat dalam pakan harus ada pada kadar atau rasio yang tepat, karena
apabila kelebihan atau kekurangan akan memberikan dampak negatif pada ikan
yang diberi pakan tersebut. Kadar lemak pakan yang tinggi akan menyebabkan
penyimpanan lemak pada tubuh, penurunan konsumsi pakan dan pertumbuhan
serta degenerasi hati (Huisman, 1987). Begitu juga pakan berkadar karbohidrat
tinggi akan meningkatkan laju pembentukan lemak (Lehninger, 1993).
Beberapa hasil penelitian menunjukkan bahwa rasio karobohidrat terhadap
lemak pakan memberikan pengaruh signifikan pada kandungan lemak daging dan
tubuh ikan serta beberapa indikator pertumbuhan. Ikan African catfish Clarias gariepinus yang diberi pakan dengan rasio karbohidrat (KH) terhadap lemak (L) 1,66 (mengandung 27% KH dan 16% L) signifikan mempengaruhi laju
pertumbuhan, efisiensi pakan dan protein. Rasio 0,74 (14% KH/21%L)
menghasilkan pertumbuhan dan deposisi lemak terendah (Ali & Jaucey, 2004).
Hasil penelitian Shimeno et al. (1992) pada Oreochromis niloticus menunjukkan pakan dengan rasio KH/L sebesar 9 (47,7%KH/5,3%L) menghasilkan laju
pertumbuhan tertinggi 37,5% dan kadar lemak daging bagian dorsal (dorsal
muscle) 0,5% bobot basah, sedangkan rasio 2,7 (33,4%KH/12,45%L)
menghasilkan kadar lemak daging bagian dorsal terendah 0,3% bobot basah dan
laju pertumbuhan 35,6%.
Dari penelitian di atas, terlihat bahwa rasio karbohidrat terhadap lemak
selain mempengaruhi beberapa indikator pertumbuhan juga memperlihatkan
atas maka perlu dilakukan penelitian rasio karbohidrat lemak pakan untuk ikan
patin.
Tujuan Penelitian
Percobaan ini bertujuan untuk menentukan rasio karbohidrat dan lemak
yang tepat untuk menghasilkan daging dengan kadar lemak rendah dan kinerja
TINJAUAN PUSTAKA
Kebutuhan Nutrisi Ikan Patin Kebutuhan Protein
Protein adalah komponen dasar jaringan hewan sehingga merupakan
nutrien esensial untuk pertumbuhan dan pemeliharaan jaringan (Herper, 1990),
dan juga berperan dalam pembentukan komponen nitrogen lainnya seperti asam
nukleat, enzim, hormon dan vitamin (Furuichi, 1988).
Kebutuhan protein untuk ikan herbivora (plant eating) dan omivora
(plant-animal eaters) lebih rendah dibandingkan ikan karnivora (flesh-eating), dan lebih
tinggi untuk ikan yang dipelihara dengan kepadatan tinggi (recirculating
aquaculture) dibandingkan dalam sistem kolam air tenang. Begitu juga untuk ikan
pada stadia awal membutuhkan lebih tinggi kadar protein pakan daripada stadia
lanjut (Craig & Helfrich, 2002). Pada beberapa jenis ikan, peningkatan
temperatur air diikuti meningkatnya kebutuhan protein (Halver, 1989).
Selanjutnya dikatakan tingkat optimum kebutuhan protein untuk ikan dipengaruhi
oleh imbangan protein energi, komposisi dan kecernaan asam amino, dan jumlah
energi nonprotein pakan.
Hepher (1990) menyatakan bahwa kebutuhan protein untuk ikan bervariasi
berdasarkan spesies, ukuran ikan, kondisi lingkungan, serta kualitas protein dan
daya cerna pakan. Umumnya ikan membutuhkan protein 35-50%, ikan karnivora
membutuhkan protein 40-50% dan omnivora 25-35% (Craig et al. 2002). Kebutuhan protein untuk catfish antara 24-40% (NRC, 1977). Pertumbuhan
pada kadar protein pakan 35 dan 45%, dan kedua nilai pertumbuhan ini tidak
berbeda nyata (Hung et al. 2004).
Kebutuhan Karbohidrat
Karbohidrat diketahui sebagai gula atau sakarida adalah komponen
esensial semua organisme hidup, mempunyai peran sebagai cadangan energi yang
dapat dengan cepat digunakan, sebagai molekul yang dapat memfasilitasi transfer
energi dan sebagai komponen struktural (De Silva & Anderson, 1995),
membentuk senyawa lipid kompleks dan bergabung dengan protein membentuk
glikoprotein (Murray et al. 1995). Karbohidrat juga berperan sebagai sumber ribosa untuk sintesis DNA dan RNA, serta dapat diubah menjadi asam amino
non-esensial (Lehninger, 1993).
Ikan yang diberi pakan tanpa karbohidrat memiliki laju pertumbuhan yang
relatif lebih rendah jika dibandingkan dengan pakan yang diberi karbohidrat
(Wilson, 1994). Namun pemberian karbohidrat yang terlalu tinggi akan
mengakibatkan pertumbuhan ikan menurun dan tidak efektifnya pakan yang
diberikan (Zonneveld et al., 1991). Pertumbuhan fingerling catfish, lebih tinggi ketika pakannya mengandung karbohidrat dibandingkan hanya mengandung
lemak sebagai sumber energi non-protein (NRC, 1993).
Nilai metabolisme energi karbohidrat dalam pakan ikan berhubungan
dengan sumber dan jenis karbohidrat (Craig et al. 2002), namun sumber karbohidrat (glukosa, dekstrin, strach) pada kadar yang sama tidak mempengaruhi
Lee, 2004). Polisakarida, seperti starch dan dekstrin sangat baik dimanfaatkan
catfish, dan ikan ini cenderung tidak efisien dalam memanfaatkan disakarida atau
monosakarida (Robinson et al. 2001). Menurut Halver (1989), nilai kecernaan starch dan dekstrin pada rainbow trout dipengaruhi oleh konsentrasinya dalam
pakan. Kecernaan dekstrin 77,2% pada pakan dengan level dekstrin 20% dan
menurun menjadi 45,5% ketika level mencapai 60%. Selanjutnya dikatakan
bahwa ikan omonivora seperti carp mampu memanfaatkan dektrin hingga 40%
sedangkan carnivora seperti yellowtail maksimal hanya 10%.
Kemampuan ikan menggunakan karbohidrat sebagai sumber energi
berbeda diantara spesies ikan. Kebanyakan ikan perairan tropis, termasuk catfish
dapat memanfaatkan lebih banyak karbohidrat dibandingkan ikan perairan dingin
dan ikan laut (Robinson et al. 2001). Ikan omnivora umumnya mampu memanfaatkan karbohidrat lebih tinggi (kadar optimum 30-40%) sedangkan ikan
karnivora memanfaatkan karbohidrat pada kadar optimum 10-20% (Furuichi,
1988). Ikan yellowtail Seriola quinqueradiata (karnivora) memanfaatkan karbohidrat terendah diikuti oleh red sea bream Chrysophrys major (semi-karnivora) dan carp Cyprinus carpio (omnivora) (Furuichi & Yone, 1981). Ikan gurame Osphrronemus gouramy fase fingerling memiliki kemampuan memanfaatkan karbohidrat lebih rendah dibandingkan dengan fase subadult
Kebutuhan Lemak
Lemak berfungsi sebagai sumber energi yang efisien, baik secara langsung
maupun potensial tersimpan di dalam jaringan adiposa (Murray et al. 1995), sebagai penyedia asam lemak esensial serta komponen struktur sel dan
pemeliharaan integritas biomembran (Takeuchi, 1988; Sepherd & Bronage, 1992),
membantu dalam penyerapan vitamin yang larut dalam lemak dan untuk
mempertahankan daya apung tubuh (NRC, 1993), sebagai prekursor untuk
hormom-hormon steroid (Robinson et al. 2001).
Lemak tidak hanya dilihat proporsinya dalam pakan namun seharusnya
memenuhi kebutuhan asam lemak esensial karena lemak merupakan satu-satunya
sumber asam lemak esensial (Takeuchi, 1988). Ikan tidak dapat mensintesis Poly Unsaturated Fatty Acid (PUFA) asam lemak n-3 dan n-6, sehingga asam lemak ini merupakan nutrien esensial yang harus tersedia dalam pakan. Ikan dapat
menkonversi 18:2n-6 dan 18:3n-3 ke bentuk asam lemak berantai panjang, seperti
20:5n-3, 22:6n-3, 20:4n-6 yang merupakan komponen esensial membran sel
(Houlihan et al. 2002). Selanjutnya dikatakan kebutuhan asam lemak esensial spesies ikan laut dan ikan air tawar berhubungan dengan kompoisi makanan
alaminya. Menurut Jobling (1995), ekosistem perairan tawar kaya akan asam
lemak n-6 dan perairan laut kaya dengan asam lemak n-3.
Kebutuhan ikan akan asam-asam lemak esensial berbeda untuk setiap
spesies ikan (Furuichi, 1988). Perbedaan kebutuhan ini terutama dihubungkan
dengan habitatnya. Ikan yang hidup di laut lebih memerlukan asam lemak n-3,
kombinasi asam lemak n-3 dan n-6 (Hepher,1990). Ikan catfish membutuhkan
baik asam lemak n-3 maupun asam lemak n-6 (Robinson et al. 2001), namun umunya spesies ikan air tawar membutuhkan lebih banyak n-6 dibandingkan n-3
(Takeuchi, 1988).
Kadar lemak pakan dapat mempengaruhi pemanfaatan pakan untuk
pertumbuhan. Naiknya kadar lemak pakan menyebabkan berkurangnya konsumsi
pakan pada juvenil Cobia, Rachycentron canadum (Wang et al.2005), pertambahan berat dan efisiensi pakan (Robinson et al. 2001). Laju pertumbuhan ikan black catfish, Rhamdia quelen meningkat dengan meningkatnya kadar lemak pakandari 8% menjadi 14% (Salhi et al. 2004) dan ikan Chinese longsout catfish Leiocassis longirostris dari 3% sampai 18%, dan pada kadar lemak pakan 21% menurunkan laju pertumbuhan (Pei et al. 2004). Penurunan pertumbuhan ikan yang mengkonsumsi pakan mengandung lemak tinggi diakibatkan menurunnya
kemampuan mencerna dan mengabsorpsi lemak, dan berkurangnya konsumsi
pakan (NRC, 1983). Selain itu, kebutuhan protein untuk pertumbuhan optimal
semakin berkurang dengan meningkatnya lemak Kebutuhan protein optimal ikan
bagrid catfish, Pseudobagrus fulvidraco 52% kadar lemak pakan 10% dan menurun menjadi 42% pada kadar lemak pakan 19% (Kim et al. 2005). Lemak karkas tidak berbeda antara ikan Rohu (Labeo rohita) yang mengkonsumsi pakan berkadar lemak 8% dan 13%, sedangkan pakan berkadar lemak 18%
Kebutuhan Energi Ikan Patin
Energi pakan diperoleh dari tiga sumber, yaitu karbohidrat, lemak dan
protein (De Silva & Anderson, 1995). Energi dari ketiga molekul tersebut
merupakan salah satu faktor utama yang mempengaruhi konsumsi pakan (feed
intake). Selain energi, keberadaan nutrien esensial seperti asam amino, asam
lemak, vitamin dan mineral juga berperan penting. Defisiensi nutrien esensial
diketahui dapat menimbulkan dua respon, (1) meningkatnya konsumsi pakan
untuk memenuhi tingkat kebutuhan, (2) respon penghambatan terhadap konsumsi
pakan ketika defisiensi sangat besar (Holihan et al. 2002).
Ikan seperti hewan lainnya, makan untuk memenuhi kebutuhan energi
(Halver, 1989). Ketika ikan mengkonsumsi pakan mengandung energi terlalu
tinggi maka konsumsi protein dapat lebih rendah dari kebutuhan saat energinya
terpenuhi sehingga menurunkan laju pertumbuhan (Webster & Lim, 2002).
Kelebihan energi pakan dapat juga berakibat meningkatnya deposit lemak tubuh
(Halver, 1989).
Terdapat beberapa faktor yang mempengaruhi kebutuhan energi pada ikan,
yaitu aktivitas fisik, temperatur, ukuran ikan, laju pertumbuhan, spesies, dan
konsumsi pakan (Webster & Lim, 2002). Proporsi energi yang dikonsumsi
meningkat dengan meningkatnya ukuran ikan, namun efisiensi pencernaan dan
absorpsi menurun yang akhirnya memperlambat pertumbuhan akibat energi yang
hilang melalui feses meningkat (De Silva & Anderson, 1995). Selain itu, aktivitas
fisik, temperatur dan stres juga mempengaruhi kebutuhan energi pada ikan
Imbangan protein dan energi penting untuk menunjang pertumbuhan ikan.
Pakan dengan kadar protein tinggi belum menjamin pertumbuhan optimal bila
total energi pakan rendah. Pakan dengan energi yang dapat menyebabkan protein
yang dikonsumsi sebagian digunakan untuk menghasilkan energi guna mencukupi
kebutuhan energi ikan. Sebaiknya kebutuhan energi dapat tercukupi dari nutrien
protein, yakni karbohidrat dan lemak. Sehingga kecukupan energi
non-protein dapat meningkatkan fungsi non-protein dalam menunjang pertumbuhan ikan
(Furuichi, 1988). Energi non-protein dapat dipenuhi oleh karbohidrat, karena
sebagian besar enzim untuk mencerna karbohidrat tersedia pada ikan (Wilson,
1994) dan karbohidrat merupakan sumber energi yang relatif murah dan
diperlukan untuk biosintesis asam amino non essensial dan asam nukleat (NRC,
1993). Pada umumnya karbohidrat pada pakan digunakan sebagai sumber energi
bagi ikan meskipun penggunaannya lebih rendah daripada hewan domestik
lainnya (Furuichi,1988). Energi dari karbohidrat telah dibuktikan sama efektifnya
dengan energi dari lemak sebagai “protein sparing action” untuk pertumbuhan (Zonneveld et al 1991). Karbohidrat juga merupakan sumber energi utama sebagian besar hewan herbivor atau omnivor (Gallego et al, 1994), dan sumber energi ini disimpan dalam bentuk glikogen dalam hati dan otot (Stefens, 1989).
Penggunaan lemak sebagai protein sparing effect telah diuji pada berbagai spesies untuk menemukan tingkat optimum lemak pakan yang dapat
meningkatkan penggunaan protein optimal untuk pertumbuhan tanpa deposisi
lemak yang berlebihan (Halver, 1989). Umumnya sekitar 10-20% lemak dalam
dengan tidak menghasilkan deposisi lemak berlebihan (Cowey & Sargent, 1979
dalam Halver 1989). Pakan mengandung 54% kasein dan lemak 15 sampai 20% memperlihatkan pertumbuhan dan konversi pakan yang tinggi pada trout yang
mengkonsumsi lemak 20% dibandingkan 5% (Takeuchi et al. 1978 dalam Halver, 1989).
Ikan lebih efisien dalam mengkonversi pakan menjadi jaringan tubuh dan
membutuhkan lebih sedikit energi per unit protein dibandingkan mamalia dan
burung, sedangkan kebutuhan proporsi protein pada ikan lebih tinggi. Rasio
energi protein optimum telah ditemukan pada berbagai spesies ikan, dan rasio
tersebut berkisar antara 8 sampai 10 kkal DE per gram protein pakan (Halver,
1989). Sedangkan pada catfish rasio ini berkisar antara 7,4-12 kkal/g. Peningkatan
rasio DE/P pakan catfish diatas kisaran ini akan meningkatkan deposisi lemak,
dan jika energi terlalu rendah, pertumbuhan ikan akan melambat (Robinson et al, 2001).
Metabolisme Karbohidrat dan Lemak Metabolisme karbohidrat
Karbohidrat dalam makanan umumnya berbentuk senyawa polisakarida,
disakarida dan monosakarida. Karena ikan tidak memiliki kelenjar air liur
(salivary gland), maka pencernaan karbohidrat dimulai di bagian lambung.
Pencernaan karbohidrat secara intensif terjadi di segmen usus yaitu dengan
Karbohidrat diabsorpsi melalui dinding saluran pencernaan (digestive
tract) dan masuk aliran darah dalam bentuk monosakarida (glukosa, fruktosa,
galaktosa) (De Silva & Anderson, 1995), dan hewan mangsa berbentuk glikogen
(Affandi et al. 2005). Pada vertebrata, sebagaian besar monosakarida dibawa
langsung ke hati dan mengalami sintesis menghasilkan glikogen dan oksidasi
menghasilkan karbondioksida dan air (Lehninger, 1993). Pada dinding usus
galaktosa dan fruktosa diubah menjadi glukosa (Affandi, 2005). Sebagian
monosakarida dibawa ke jaringan lain dan mengalami metabolisme lebih lanjut
(Lehninger, 1993).
Glukosa memegang peranan penting sebagai sumber energi. Beberapa
jaringan (contohnya otak) hanya menggunakan glukosa sebagai sumber energi
sehingga hewan harus mempertahankan kadar glukosa darahnya pada level
tertentu (De Silva & Anderson, 1995). Bila kadar glukosa dalam darah meningkat
sebagai akibat meningkatnya proses pencernaan dan penyerapan karbohidrat,
sintesis glikogen dari glukosa oleh hati akan naik. Sebaliknya bila kadar glukosa
menurun glikogen diuraikan menjadi glukosa untuk selanjutnya mengalami proses
katabolisme menghasilkan energi (Lehninger, 1993).
Terdapat empat jalur reaksi yang berperan dalam metabolisme karbohidrat,
yakni: (1) glikolisis, yaitu katabolisme glukosa menghasilkan energi; (2)
glukoneogenesis, sintesis glukosa dari molekul lain; (3) glikogen sintesis,
pembentukan cadangan glukosa dalam bentuk glikogen; (4) glikogenolisis,
Pada hewan yang normal, bila terjadi kelebihan glukosa dalam darah,
glukosa tersebut akan diubah menjadi glikogen melalui proses glikogenesis
(Lehninger 1994). Glikogen yang terbentuk akan disimpan di dalam hati dan otot.
Kemampuan hati dan otot untuk menyimpan glikogen ini terbatas, sehingga bila
kandungan glukosa darah masih berlebih, maka akan terjadi pembentukan lemak
melalui proses lipogenesis. Sebaliknya, bila glukosa darah rendah dan biasanya
terjadi bila tidak makan dalam waktu yang cukup lama atau hanya memakan
pakan yang mengandung karbohidrat rendah, maka akan terjadi proses
pembentukan glukosa melalui proses glikogenolisis dan glukoneogenesis
(Shimeno 1974). Glikogenolisis merupakan proses perombakan glikogen menjadi
glukosa dengan melibatkan enzim fosforilase dan 1,4 glukantransferase.
Glukoneogenesis merupakan proses pembentukan glukosa dari senyawa
komponen protein dan lemak. Pada proses glukoneogenesis terdapat 3 jenis
enzim kunci yang sangat berperan yaitu fosfoenolpiruvat karboksilase, fruktosa
1,6-difosfatase, dan glukosa 6-fosfatase.
Penelitian pada kondisi laboratorium terhadap European eels Anguilla anguilla dengan berat awal 133g yang dipuasakan memperlihatkan konsentrasi glikogen hati tidak berubah dalam waktu 96 hari dan glikogen otot selama 164
hari setelah dipuasakan (Dave et al. 1975 dalam Halver, 1989). Selanjutnya dikatakan bahwa selama dipuasakan energi metabolik diperoleh dari lipid dan
sejumlah yang terbatas dari katabolisme protein. Glikogen hepatopankreas ikan
carp yang dipuasakan selama 22 hari sebesar 10,65% tidak berbeda terhadap
hepatopankreas tinggal 1,55% (Nagai & Ikeda, 1971 dalam Halver, 1989). Selanjutnya dikatakan bahwa untuk ikan karnivora, glikogen hati tidak
menyediakan sumber glukosa yang dapat digunakan segera dan glukoneogenesis
adalah proeses penting untuk hal ini.
Metabolisme lemak
Pencernaan lemak mulai terjadi di bagian lambung, akan tetapi pencernaan
di sini tidak efektif (Affandi et al. 2005). Ketidakefektifan ini disebabkan enzim lepase tidak dapat bekerja baik efektif dalam suasana pH rendah (Lehninger,
1993).
Absorpsi lemak pada berbagai spesies ikan telah banyak dipelajari. Studi
ini mengindikasikan umumnya penyerapan awal terjadi pada anterior ileum
termasuk cecum dan kebanyakan berlangsung pada intestin. Hasil pencernaan
lemak yang berupa garam empedu, monoasilgliserol, gliserol, lisofosfolipid, dan
asam lemak bebas diabsorpsi melalui difusi ke dalam epitel intestinal dan
berlangsung lambat (sekitar 10 jam atau lebih). Di dalam sel mukosa, asam lemak
bebas kembali mengalami esterifikasi dengan gliserol dan monogliserol
menghasilkan triasilgliserol, dan dengan lisofosfolipid menghasilkan fosfolipid.
Melalui saluran darah dan sitem limfa, lemak ini diangkut ke hati dalam bentuk
Sebagian besar asam lemak bebas yang mengalami katabolisme berasal
dari proses hidrolisis trigliserida oleh enzim lipase yang terdapat dalam sel
adiposa. Asam lemak ini dikeluarkan dari sel berikatan dengan serum albumin
yang kemudian bersama aliran darah dibawa ke jaringan lainnya dalam tubuh
untuk selanjutnya mengalami oksidasi (Lehninger, 1993). Oksidasi asam lemak
ini berperan penting dalam menyediakan energi untuk jaringan ikan. Pada trout,
otot merah lateral dan jantung mempunyai kemampuan yang sama dalam oksidasi
lemak, lebih tinggi dari hati, ginjal dan otot putih. Pada teleostei, oksidasi asam
lemak menyediakan energi untuk ritme kontraksi yang lambat yang merupakan
karakteristik dari otot merah dan jantung (Halver, 1989). Selanjutnya dikatakan
bahwa selama ikan dipuasakan, energi metabolik lebih banyak diperoleh dari
katabolisma lemak, dan sejumlah yang terbatas dari katabolisme protein.
Biosintesis asam lemak sebagai bagian dari biosintesis lemak adalah suatu
proses metabolisme yang penting dalam jasad hidup. Hal ini benar jika diingat
jaringan hewan mempunyai kemampuan terbatas untuk menyimpan energi dalam
bentuk karbohidrat (Lehninger, 1993). Selanjutnya dikatakan sebagian
polisakarida dirombak melalui glikolisis menjadi asetil ko-A, yang merupakan
prazat untuk biosintesis asam lemak dan trigliserida. Biosintesis asam lemak dari
asetil ko-A terjadi di hampir semua bagian tubuh hewan, terutama di jaringan hati
dan adiposa. Menurut Halver (1989), enzim yang mengkonversi asam amino
menjadi piruvat dan asam trikarboksil adalah aktif pada ikan. Karbon dari asam
amino bergabung dengan sitrat ditranspor dari mitokondria ke sitosol menjadi
ATP-sitratliase aktif dalam jaringan hati coho salmon tetapi tidak aktif pada rainbow
trout atau channel catfish.
Biosintesis lemak atau lipogenesis pada ikan sama dengan yang terjadi
pada mamalia umumnya. Jaringan hati dan adiposa bagian penting terjadinya
lipogenesis hewan mamalia terestrial dan burung (Halver, 1989). Aktivitas enzim
yang terlibat dalam lipogenesis pada coho salmon sama dengan channel catfish,
utamanya dalam jaringan hati (Likimani & Wilson, 1982) dalam Halver (1989). Aktivitas enzim-enzim tersebut juga aktif pada jaringan hati belut (eel), dan
sebagian kecil pada intestinal dan otot merah Aster & Moon (1981) dalam Halver (1989). Salah satu substrat untuk lipogenesis ialah glukosa. Bila glukosa tidak
segera dibutuhkan untuk energi, kelebihan glukosa yang masuk secara kontinu ke
dalam sel akan disimpan sebagai glikogen (Desilva & Anderson, 1995), dan bila
sel (terutama sel hati) mendekati saturasi glikogen, glukosa tambahan diubah
menjadi lemak dalam sel hati dan adipositi kemudian disimpan dalam adiposit
BAHAN DAN METODA PENELITIAN
Pakan Uji
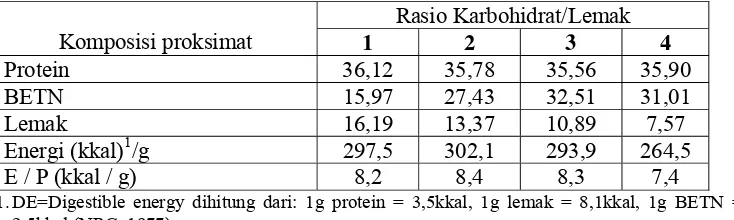
Penelitian ini menggunakan empat jenis pakan uji yang mengandung
iso-protein sekitar 36% dan rasio energi tercerna/iso-protein 7,4 – 8,4 kkal DE/g dengan
rasio karbohidrat dan lemak yang berbeda, yaitu 1, 2, 3 dan 4. Sebagai sumber
lemak digunakan minyak ikan dan minyak jagung. Sumber karbohidrat (BETN)
utama diperoleh dari dekstrin. Komposisi bahan pakan disajikan pada Tabel 1 dan
komposisi proksimat pakan pada Tabel 2.
Tabel 1. Komposisi bahan pakan percobaan (g/100g pakan)
Bahan Penyusun Rasio Karbohidrat/Lemak
Tabel 2. Komposisi proksimat pakan perlakuan (% bobot kering)
Rasio Karbohidrat/Lemak
Pemeliharaan Ikan dan Pengumpulan Data
Ikan diperoleh dari petani berukuran 7,75±3,3g dan dibesarkan pada
kondisi laboratorium selama 40 hari di Laboratorium Nutrisi Ikan, Departemen
Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, IPB sampai mencapai
ukuran yang diinginkan untuk awal penelitian. Ikan dengan berat rata-rata
16,1±0,5g diambil sebanyak 6 ekor dan dimasukkan ke dalam akuarium ukuran
50x30x40cm yang diisi air sebanyak 60 liter. Sistem pemeliharaan menggunakan
sistem resirkulasi yang dilengkapi aerasi dan filtrasi. Selama penelitian dilakukan
pergantian air sekitar 50% per hari untuk menjaga kualitas air. Pemberian pakan
secara at satiation dua kali sehari pukul 07.00 dan 17.00 WIB dan banyaknya pakan yang diberikan dicatat untuk mengetahui tingkat konsumsi pakan. Setelah
60 hari pemberian pakan percobaan, ikan dipuasakan selama 24 jam dan
ditimbang satu per satu untuk mengetahui bobot akhir. Sebanyak 2 ekor ikan dari
setiap akuarium digunakan untuk analisis proksimat tubuh dan 3 ekor diambil
daging bagian lateral untuk dianalisis proksimat daging. Selama penelitian, kadar
oksigen terlarut 4,4-6,5 ppm; suhu 29-31oC; pH 7,5-7,6. Kualitas air ini dapat
menunjang pertumbuhan air yang normal.
Analisis Kimia
Analisis proksimat yang meliputi kadar protein kasar, lemak kasar, BETN,
abu, serat kasar dan air dilakukan terhadap bahan pakan dan pakan, sedangkan
daging dan tubuh meliputi kadar protein kasar, lemak kasar, abu, dan air. Analisis
proksimat total tubuh ikan dilakukan pada awal dan akhir percobaan, dan
proksimat daging dilakukan pada akhir penelitian. Prosedur analisis proksimat
terdapat pada Takeuchi (!988)(Lampiran 1).
Analisis Statistik
Desain penelitian menggunakan Rancangan Acak Lengkap (RAL) dengan
4 perlakuan dan 3 ulangan. Uji lanjut menggunakan Uji Beda Nyata Terkecil
(BNT). Peubah yang diuji dalam penelitian ini ialah laju pertumbuhan, retensi
protein dan lemak, konversi pakan, kadar lemak, protein, air, dan abu daging
maupun tubuh, kelangsungan hidup. Laju pertumbuhan, konversi pakan, retensi
lemak dan protein, kelangsungan hidup dihitung menggunakan formula sebagai
berikut:
1. Laju pertumbuhan bobot harian (Huisman, 1976)
α = [(Wt / Wo)1/t -1] x 100%
Keterangan :
α = laju pertumbuhan bobot harian (%) Wt = bobot rata-rata ikan pada akhir penelitian
W0= bobot rata-rata ikan pada akhir penelitian
2. Konversi pakan (Feed conversion ratio)(Viola & Rappaport, 1979)
3. Retensi protein dan lemak (Viola & Rappaport, 1979)
Pertambahan bobot protein/lemak tubuh (g)
R = --- x 100% Bobot total protein/lemak yang dimakan (g)
4. Kelangsungan hidup
Jumlah ikan pada akhir penelitian (ekor)
HASIL DAN PEMBAHASAN
Hasil
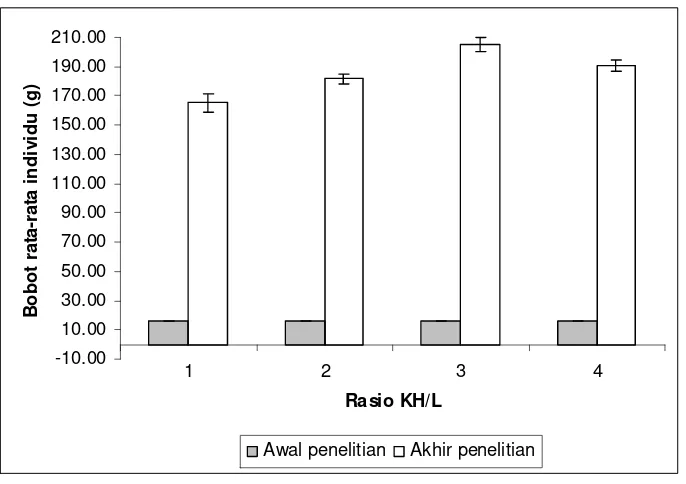
Bobot rata-rata individu pada awal dan akhir percobaan disajikan pada
Gambar 1, sedangkan bobot biomassa pada awal dan akhir penelitian disajikan
pada Lampiran 2. Pada Gambar 1 terlihat bahwa pertambahan bobot rata-rata
individu tertinggi diperoleh pada ikan yang diberi pakan dengan rasio 3 (32,51%
karbohidrat dan 10,89% lemak), diikuti oleh rasio 4 (31,01% karbohidrat dan
7,57% lemak), 2 (27,43% karbohidrat dan 13.37% lemak), dan 1 (15,97%
karbohidrat dan 16,19% lemak). Ikan patin yang mengkonsumsi pakan dengan
rasio 3 menghasilkan bobot rata-rata individu pada akhir penelitian sebesar
205,04g diikuti rasio 4, 2 dan 1 dengan bobot rata-rata berturut-turut 190,38,
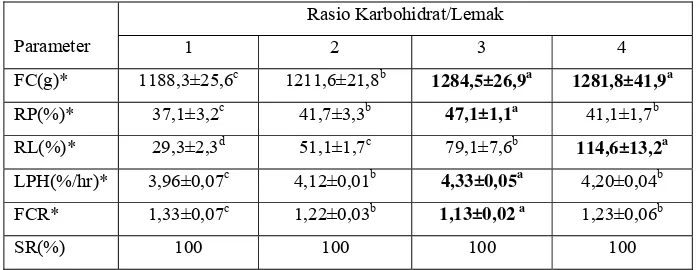
Tabel 3. Rata-rata konsumsi pakan (FC), retensi protein (RP), retensi lemak (RL), laju pertumbuhan harian (LPH), konversi pakan (FCR)
dan kelangsungan hidup (SR) ikan patin selama 60 hari pemeliharaan
Rasio Karbohidrat/Lemak
Parameter 1 2 3 4
FC(g)* 1188,3±25,6c 1211,6±21,8b 1284,5±26,9a 1281,8±41,9a
RP(%)* 37,1±3,2c 41,7±3,3b 47,1±1,1a 41,1±1,7b
RL(%)* 29,3±2,3d 51,1±1,7c 79,1±7,6b 114,6±13,2a
LPH(%/hr)* 3,96±0,07c 4,12±0,01b 4,33±0,05a 4,20±0,04b
FCR* 1,33±0,07c 1,22±0,03b 1,13±0,02 a 1,23±0,06b
SR(%) 100 100 100 100
Keterangan : huruf yang berbeda pada baris yang sama menunjukkan adanya perbedaan antar perlakuan (P<0,05).
*Data per ulangan terdapat pada Lampiran 3 - 9.
Tabel 3 memperlihatkan bahwa retensi lemak meningkat sejalan dengan
meningkatnya rasio karbohidrat/lemak, tetapi retensi protein dan laju
pertumbuhan meningkat hanya sampai pada rasio 3 dan terjadi penurunan pada
rasio 4. Sedangkan peningkatan rasio karbohidrat/lemak menyebabkan terjadi
penurunan pada nilai konversi pakan, dan penurunan ini hanya sampai pada rasio
3 dan meningkat kembali pada rasio 4. Selama penelitian berlangsung tidak terjadi
kematian ikan uji untuk setiap jenis pakan uji yang dicobakan. Rata-rata
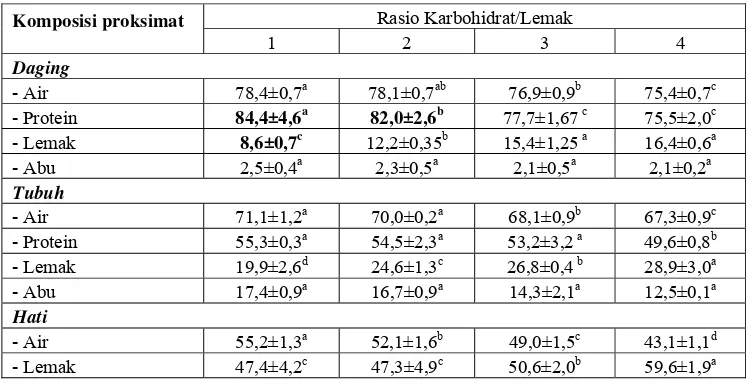
komposisi proksimat daging, tubuh dan hati ikan patin setelah 60 hari pemberian
pakan uji disajikan pada Tabel 4. Kadar air dan protein daging serta tubuh ikan
patin semakin kecil sejalan meningkatnya rasio karbohidrat/lemak pakan.
Keadaan sebaliknya terjadi pada kadar lemak, dimana semakin tinggi rasio
dan tubuh. Kadar lemak hati semakin tinggi dengan meningkatnya rasio
karbohidrat/lemak pakan dan keadaan sebaliknya terjadi pada kadar air. Rasio
karbohidrat/lemak pakan tidak menghasilkan perbedaan kadar abu daging dan
tubuh.
Tabel 4. Komposisi proksimat daging, tubuh dan hati (bobot kering)
Rasio Karbohidrat/Lemak
Keterangan : huruf yang berbeda pada baris yang sama menunjukkan adanya perbedaan antar perlakuan (P<0,05) (Lihat Lampiran 15-24).
Pembahasan
Hasil penelitian menunjukkan bahwa ikan yang diberi pakan dengan rasio
karbohidrat/lemak 3 dan 4 mengkonsumsi jumlah pakan tertinggi dibandingkan
dua perlakuan lainnya (Tabel 3). Semakin banyak pakan yang dikonsumsi,
kebutuhan energi untuk ikan tercukupi terutama yang bersumber dari karbohidrat
dan lemak sehingga pemanfaatan protein untuk pertumbuhan semakin efisien. Hal
ini dapat dilihat pada rasio 3 dimana nilai retensi protein dan laju pertumbuhan
perbedaan ukuran ikan akibat perbedaan laju pertumbuhan selama percobaan
berlangsung. Ikan yang berukuran besar membutuhkan dan mengkonsumsi pakan
lebih banyak dari pada ikan yang berukuran kecil (pemberian pakan dilakukan
secara at satiation). Pakan dengan rasio karbohidrat/lemak 4 menghasilkan retensi protein dan pertumbuhan yang lebih rendah dibandingkan rasio 3
disebabkan pemanfaatan pakan menjadi kurang efisien ketika terjadinya proses
lipogenesis yang ditunjukkan oleh nilai retensi lemak dan kadar lemak hati yang
tinggi.
Ikan patin yang diberi pakan berkadar lemak tinggi (rasio
karbohidrat/lemak 1) cenderung menggunakan banyak lemak sebagai sumber
energi yang ditunjukkan pada nilai retensi lemak yang rendah. Selain itu,
tingginya kadar lemak pakan diikuti dengan semakin menurunnya kadar
karbohidrat telah menyebabkan kebutuhan karbohidrat sebagai sumber energi
tidak tercukupi karena ikan tidak efisien dalam memanfaatkan protein yang
ditunjukkan pada nilai retensi protein dan pertumbuhan yang semakin kecil.
Menurut Lehninger (1993), jaringan tertentu pada hewan seperti otak cenderung
menggunakan glukosa yang bersumber dari protein apabila glukosa dari
karbohidrat tidak tercukupi. Sedangkan peningkatan kadar karbohidrat pakan
diikuti penurunan kadar lemak menghasilkan retensi lemak yang semakin tinggi.
Retensi lemak pada perlakuan pakan dengan kadar lemak terendah menunjukkan
nilai tertinggi dan nilai ini mencapai lebih dari 100%. Tubuh ikan membutuhkan
lemak untuk disimpan sebagai lemak sruktural. Untuk memenuhi kebutuhan
non-lemak, seperti karbohidrat menjadi asam-asam lemak dan trigliserida yang
terjadi di hati dan jaringan lemak (Linder, 1992). Selanjutnya Brauge et al. (1994) menyatakan bahwa tingginya kadar karbohidrat yang dapat dicerna merangsang
terjadinya proses lipogenesis dan meningkatkan penyimpanan lemak. Proses
lipogenesis ini memerlukan energi dan keperluan energi ini akan mengurangi
energi untuk pertumbuhan.
Jadi juvenil ikan patin memerlukan suatu kadar lemak tertentu dalam
pakan yang sekaligus juga rasio karbohidrat/lemak tertentu sehingga pemanfaatan
energi nonprotein tersebut akan maksimal. Keadaan ini akan memberikan
efisiensi protein pakan yang optimum seperti yang dihasilkan pada rasio
karbohidrat/lemak 3. Rasio 3 menghasilkan energi nonprotein yang maksimum
sehingga protein pakan dapat digunakan untuk sintesis protein tubuh lebih efisien.
Hal ini terbukti tingginya jumlah protein yang tersimpan dalam tubuh ikan yang
ditunjukkan oleh nilai retensi protein 47,06%. Nilai ini lebih tinggi dari
P. djambal yang diberi pakan rasio karbohidrat/lemak 6 (36,14% karbohidrat dan 6,25% lemak), yaitu 45,37%. Menurut Peres dan Teles (1999), terjadinya protein sparing effect oleh karbohidrat dan lemak akan mengurangi pemanfaatan protein untuk energi. Viola & Rappaport (1979) menggunakan retensi protein sebagai
indikator efektivitas pakan. Pemanfaatan protein yang semakin efisien
ditunjukkan pula oleh nilai konversi pakan yang diperoleh pada pakan dengan
nilai rasio karbohidrat/lemak sebesar 3. Efek lanjut pakan dengan rasio
karbohidrat/lemak 3 akan menghasilkan pertumbuhan harian yang tertinggi pula.
pertumbuhan yang tinggi sehingga akan dihasilkan pula konversi pakan yang
rendah.
Kadar lemak tubuh dan daging terkecil diperoleh pada ikan yang diberi
pakan uji rasio karbohidrat/lemak 1. Rendahnya kadar lemak ini akibat
kebanyakan lemak pakan dimanfaatkan sebagai sumber energi sehingga jumlah
yang disimpan semakin sedikit (nilai retensi lemak yang kecil). Nilai lemak tubuh
ini (19,9±2,6) lebih kecil dibandingkan yang diperoleh Suwarsito (2004), yakni
32,19% bobot kering tetapi lebih besar dari hasil yang diperoleh Hung et al. (2004) yakni 13,7% bobot kering pada perlakuan protein pakan 45%. Sedangkan
kadar lemak daging terkecil relatif sama dengan yang diperoleh Suwarsito (2004)
sebesar 7,51% bobot kering pada penambahan L-karnitin 0,18%.
Semakin tinggi kadar lemak pakan diikuti semakin rendah kadar
kabohidrat menghasilkan kadar lemak daging terendah dan protein daging
tertinggi. Pakan dengan rasio karbohidrat/lemak 1 menghasilkan kualitas daging
yang lebih baik dibandingkan dengan rasio 2, 3 dan 4.
Di akhir penelitian, ukuran ikan baru mencapai sekitar 200g, sedangkan
ukuran konsumsi ikan ini di atas 500g, maka pakan dengan rasio 1 belum mutlak
diaplikasikan. Untuk kepentingan budidaya pada tahap tersebut, peningkatan
pertumbuhan lebih menjadi prioritas. Dengan demikian, pakan dengan rasio
SIMPULAN
Ikan patin, P. hypophthalmus yang diberi pakan uji rasio karbohidrat/lemak 3 (mengandung 32.51% karbohidrat dan 10.89% lemak)
DAFTAR PUSTAKA
Affandi R, Sjafei DS, Raharjo MF, Sulistiono. 2005. Fisiologi ikan: Pencernaan dan penyerapan makanan. Departemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan IPB. 215 hal.
Ali MZ,. Jaucey K. 2004. Optimal dietary carbohydrate to lipid ratio in African catfish Clarias gariepinus. J. Aqua. Int. 12: 169-180.
[APHA] American Public Health Association, American Water Works Assosiation and water pollution control federation. 1975. Standart methods for the examination of water and wastewater. 14th. Ed., Washington, D.C. 1193 pp.
Brauge CF, Medale F, Corraze G. 1994. Effect of dietary carbohydrate levels on growth, body composition, and glicaemia in rainbow trout, Oncorhynchus mykiss, reared in sea water. INRA Fish Nutrition Laboratory, Hydrobiology Station, France. Aquaculture, 123:109-120.
Campbell PN and Smith AD, 1982. Biochemistry Illustrated. Illustrator by Harris S. Churchill Livingstone. Edinburg. London.
Cho CY, Cowey CB and Watanabe T. 1985. Finfish nutrition in Asia. Methodological Approach of Research and Development. Ottawa, Ont. DCR. 154 pp.
Craig S and Helfrich LA. 1992. Understanding fish nutrition, feed, and feeding. Department of Fisheries and Wildlife Science. Virginia Tech.
De Silva SS, and Anderson TA. 1995. Fish nutrition in aqualculture. Chapman & Hall Aqualculture serien 1. New York. 308 p.
Du ZY, Liu YJ, Tian LX, Wang JT, Wang Y, Liang GY. 2005. Effect of dietary lipid level on growth, feed utilizatition and body composition by juvenil Grass Carp (Ctenopharyngodon idellla). Aquacult. Nutr. 11, 139-146. Furuichi M and Yone Y. 1981. Change of blood sugar and plasma insulin level of
fishes in glucosa tolerance test. Bull. Japan. Soc. Sci. Fish 47: 761-764.
Gallego MG, Bzoca J, Akharbach H, Suarez MD, Sanz A. 1994. Utilization of different carbohydrates by the European eel (Anguilla anguila). Aquaculture 124 : 99-108.
Guyton, AC. 1994. Textbook of medical physiology. Alih bahasa Tengadi. Penerbit Buku Kedokteran ECG. Jakarta. 399 hal.
Halver JE. 1989. Fish nutrition. 2nd Ed. Academic Press, Inc. News York. 713 pp.
Hepher B. 1990. Nutrition of pond fishes. New York. Cambridge Univercity Press. 388 p.
Houlihan D, Boujard T and Jobling M. 2002. Food intake in fish. Blackwell science Lrd. 414 pp.
Huisman EA, 1976. Food conversion efficiencies at maintenance and production levels for Carp, Cyprinus carpio L and rainbow trout, Salmo gairdneri Richardson. Aquaculture 9:256-273.
Hung LT, Suhenda N, Slembrouck J, Lazard J and Moreau Y. 2004. Comparison of dietary protein and energy utilization in three Asian catfish (Pangasius bocourty, P. Hypophthalmus and P. djambal). Aquacult. Nutr. 10, 317-326.
Kim LH and Lee Sang-Ming. 2005. Effect of the dietary protein and lipid levels on growth and body composition of Bagrid catfish, Pseudobagrus fulvidraco. Aquaculture 243, 323-329.
Lee S and Lee JH. 2004. Effect of dietary glucose, dextrin and strach on growth and body composition of juvenile starry flounder Platichthys stellatus. J. Fish. Sci. 70: 53-58.
Lehninger AL. 1993. Dasar-dasar biokimia (terjemahan). Jakarta. Erlangga. 73 hal.
Linder MC. 1992. Nutrisi dan metabolisme karbohidrat, hal. 27-58. Dalam : Linder, M.C (ed). Biokimia Nutrisi dan Metabolime (terjemahan). Jakarta . UI-Press. Indonesia.
Lovell T. 1988. Nutrition and feeding of fish. Auburn Univercity. Published by Van Nostrand Academy of Sciences Washington DC. 260 pp.
Mokoginta I, Takeuchi T, Hadadi A, Jusadi D. 2004. Different capabilities in utilizing dietary carbohydrate by fingerling and subadult giant gouramy Osphronemus gouramy. J. Fish. Sci. 20: 996-1002.
Muchtadi D, Palupi SN, Astawan M. 1993. Metabolisme zat gizi Jilid I. Pustaka Sinar Harapan. Jakarta. Hal 12.
[NRC] National Research Countil. 1983. Nutrient requirement of warmwater fishes and shellfishes. Revised Edition. National Academy of Sciences Washington DC. 102 pp.
[NRC] National Research Countil. 1977. The role of chromium in animal nutrition. National Acad. Press. Washington DC. 80 hal.
Pei Z, Xie S, Lei W, Zhu X and Yang Y. 2004. Comparative study on the effect of dietary lipid level on growth and feed utilization for gibel carp(Carasius auratus Gibelio) and Chinese longsnout catfish (Leiocassis longirostris Gunther). Aquacult. Nutr. 10: 209-216.
Peres H, Teles AO. 1999. Effect of dietary lipid level on growth performance and feed utilization by European sea bass juveniles (Dicentrarchus labrax). Aquaculture 179:325–334.
Robinson EH, Menghe H Li, Bruce BM. 2001. A practical guide to nutrition feeds, and feeding of Catfish. Bull. 1113. Mississippi Agricultural & Forestry Experiment Station. Mississippi State University.
Salhi M, Bessonart M, Chediak G, Bellagamba M and Carnevia D. 2004. Growth, feed utilization and body composition of black catfish, Rhamdia quelen, fry fed diets containing different protein. Aquaculture 231, 435-444. Sa R, Pausao-Ferreira P, Oliva-Teles A. 2006. Effect of dietary protein and lipid
level on growth and feed utilization of White Sea Bream (Diplodus sargus) juvenil. Aquacult. Nutr. 12 ;310-321.
Sheperd J and Bronage N. 1992. Intensive fish farming. Blackwell Scientific Publication, Oxford, London. 404 pp.
Shimeno, S. Ming Duan-Cun, Takeda, M. 1993. Metabolic respons to dietary carbohydrate to lipid ratio in Oreochromis niloticus. J. Nippon Suisan Gakkaishi. 59, 827-833.
Suhenda N, Setijaningsih L, Suryanti Y. 2003. Penentuan rasio antara kadar karbohidrat dan lemak pada benih ikan patin jambal (Pangasius djambal). J. Penelitian Perikanan Indonesia, Vol. 9 No. 1;21-29.
Suwarsito. 2004. Pengaruh kadar L-karnitin berbeda dalam pakan terhadap kadar lemak daging dan pertumbuhan ikan patin (Pangasius hypopthalmus). Tesis. Sekolah Pascasarjana Institut Pertanian Bogor. Bogor. 55 hal.
Takeuchi T. 1988. Laboratory work-chemical evaluation of dietary nutrients, p. 179-233. In Watanabe T. (ed): Fish Nutrition and Mariculture. Tokyo. Departement of Aquatic Biosciences Tokyo Univercity of Fisheries. JICA.
Viola S and Rappaport U. 1979. The “Extra calorie effect” of oil in nutrient of carp. Bamidgeh, 31: 51-69.
Wang Ji-Teng, Liu Yong-Jian, Tian Li-Xia, Mai Kang-Sen, Du Zhen-Yu, Wang Y, Yang Hui-Jun. 2005. Effect of dietary lipid level on growth performance, lipid deposition, hepatic lipogenesis in juvenile Cobia (Rachycentron canadum). Aquaculture 249, 439-447.
Webster CD and Lim C. 2002. Nutrient requirements and feeding of finfish for aquaculture. Cabi Publishing, Walingford Oxon, UK. 412 pp.
Wilson RP. 1994. Utilization of dietary carbohidrate by fish. Aquaculture. 124: 67-80.
Lampiran 1. Prosedur analisa proksimat (Takeuchi, 1988) 1. Prosedur analisa kadar protein
A. Prosedur Oksidasi:
1. Sampel ditimbang 1,0 g (S), dimasukkan ke dalam labu kjedahl.
2. Katalis (K2SO4 + CuSO4 + H2O) rasio 9:1 ditimbang sebanyak 3 g dan
dimasukkan ke dalam labu kjedahl.
3. 10 ml H2SO4 pekat ditambahkan ke dalam labu kjedahl kemudian
dipanaskan pada suhu 400oC selama 3-4 jam sampai cairan dalam labu
berwarna hijau bening.
4. Larutan didinginkan, ditambahkan air destilasi 100 ml, kemudian larutan
dimasukkan ke dalam labu takar dan diencerkan dengan akuades hingga
volume larutan tersebut mencapai 100 ml (larutan A).
B. Prosedur Destilasi:
1. Labu erlenmeyer diisi dengan 10 ml H2SO4 0,05 N, ditambahkan 2 tetes
indikator methyl red (larutan B).
2. Larutan A diambil sebanyak 5 ml dan ditambahkan 10 ml NaOH 30% lalu
dimasukkan ke dalam labu Kjedahl. Lakukan destruksi selama 10 menit
mulai saat tetesan pertama pada larutan B.
C. Titrasi:
1. Hasil destruksi dititrasi dengan NaOH 0,05 N, dan volume titran dicatat.
2. Dilakukan juga terhadap blanko dengan prosedur yang sama.
D. Protein (%) =
2. Prosedur analisa kadar lemak (Metode ether ekstraksi)
1. Labu ekstraksi dipanaskan pada suhu 110oC selama 1 jam. Kemudian
didinginkan dalam eksikator selama 30 menit. Panaskan kembali selama 30
menit, lalu didinginkan, kemudian ditimbang. Proses tersebut diulang sampai
tidak ada perbedaan bobot labu lebih dari 0,3 mg. Bobot labu ekstraksi (A)
2. Sampel sebanyak 1 gram dimasukkan ke dalam tabung filter, lalu dipanaskan
pada suhu 90o – 100oC selama 2 – 3 jam.
3. Tabung filter ditempatkan pada no.2 ke dalam ekstraksi dari soxchlet.
Kemudian disambungkan ke kondensor labu ekstraksi pada no.1 yang telah
diisi 100 ml petroleum ether.
4. Dilakukan pemanasan ether pada labu ekstraksi dengan mengguanakan water
bath, suhu 70oC selama 16 jam.
5. Labu ekstraksi dipanaskan pada suhu 100oC, kemudian ditimbang (B).
6. x100%
3. Prosedur analisa kadar lemak (Metode Folch)
1. Bahan ditimbang sebanayak A gram dan ditambahkan C ml (20 x A)
Chloromethanol perbandingan 2 : 1.
2. Dihomogenkan selama 5 menit.
3. Hasilnya disaring menggunakan Vaccum Pump dan kertas saring.
4. Hasil penyaringan dimasukkan (dengan cara disaring menggunakan kertas
saring) ke dalam labu pemisah yang sebelumnya dimasukkan MgCL2
sebanyak (0,2xC)ml.
5. kocok perlahan selama 5 menit dan didiamkan selama semalam.
6. kemudian diambil endapan di bagian bawah dan dieveporasi dan
4. Prosedur analisa serat kasar
1. Kertas filter dipanaskan dalam oven selama 1 jam pada suhu 110oC, lalu
didinginkan dalam eksikator lalu ditimbang (X1).
2. Sampel ditimbang 0,5 g (A), dimasukkan ke dalam erlenmeyer 250 ml.
3. H2SO4 0,3 N sebanyak 50 ml dimasukkan ke dalam erlenmeyer lagi kemudian
dipanaskan selama 30 menit. Setelah itu NaOH 1,5 N sebanyak 25 ml
dimasukkan ke dalam erlenmeyer lagi kemudian dipanaskan selama 30 menit.
4. Larutran dan bahan yang telah dipanaskan kemudian disaring dalam corong
buchner dan dihubungkan pada vacuum pump untuk mempercepat filtrasi.
5. Larutan dan bahan yang ada pada corong buchner dibilas secara berturut-turut
dengan 50 ml air panas, H2SO4 0,3 N, air panas 50 ml, dan 25 ml aseton.
6. Kertas saring dan isinya dimasukkan ke dalam cawan porselen, dikeringkan
selama 1 jam kemudian didinginkan dalam eksikator dan ditimbang (X2).
7. Kemudian dipanaskan dalam tannur 600oC hingga berwarna putih, dinginkan
dalam eksikator dan ditimbang (X3).
1. Cawan porselen dipanaskan pada suhu 600oC selama 1 jam dengan
menggunakan muffle furnace, kemudian dibiarkan sampai suhu muffle
furnace turun sampai suhu 110oC, lalu cawan porselen dikeluarkan dan
didinginkan dalam eksikator selama 30 menit, lalu ditimbang (A).
2. Sampel dimasukkan ke dalam cawan porselen lalu ditimbang (B) pada suhu
600oC, sampai bahan berwarna putih.
3. Cawan porselen dikeluarkan lalu didinginkan dalam eksikator selama 30
6. Prosedur analisa analisa kadar air
1. Cawan dipanaskan pada suhu 105oC selama 3 jam.
2. Bahan seberat A gram dimasukkan ke dalam cawan dan ditimbang (X gram).
3. Cawan yang sudah berisi bahan dipanaskan dalam oven pada suhu 105oC
selama 3 jam, selanjutnya didinginkan dalam eksikator dan ditimbang (Y
gram).
4. Prosedur no.3 diulang kembali sampel berat sampel konstan (tidak berubah).
5. 100%
Lampiran 3. Laju pertumbuhan (%) ikan patin yang diberi perlakuan pakan uji rasio karbohidrat/lemak berbeda
Perlakuan
Rasio K/L Ulangan
Bobot individu awal (g)
Bobot individu akhir (g)
Laju pertumbuhan (%)
1 1 15,95 170,39 4,03
2 16,05 158,17 3,89
3 16,13 167,15 3,97
2 1 15,85 177,65 4,11
2 16,24 183,28 4,12
3 16,40 184,16 4,11
3 1 16,27 205,40 4,32
2 16,08 200,79 4,30
3 15,95 210,02 4,39
4 1 16,09 185,95 4,16
2 16,27 191,55 4,20
Lampiran 4. Komposisi proksimat daging pada akhir percobaan Jumlah 78,36±0,72 78,06±0,70 76,89±0,85 75,43±0,65
Kadar protein (bobot basah)
Jumlah 18,3±0,40 18,0±0,17 18,0±0,74 18,6±0,04
Kadar lemak (bobot basah)
Jumlah 1,86±0,17 2,68±0,12 3,55±0,30 4,04±0,04
Lampiran 5. Komposisi proksimat tubuh pada akhir percobaan Jumlah 71,08±1,21 70,02±0,22 68,08±1,98 67,25±0,86
Kadar protein Jumlah 5,74±0,58 7,40±0,38 8,55±0,67 9,28±0,99
Lampiran 6. Komposisi proksimat hati pada akhir percobaan (bobot basah)
Kadar air
Rasio Karbohidrat/Lemak Ulangan
1 2 3 4
1 55,62 52,66 50,49 44,21
2 53,76 50,30 48,87 43,20
3 56,31 53,45 47,55 41,97
Jumlah 55,23±1,32 52,14±1,64 48,97±1,47 43,13±1,12
Kadar lemak
Rasio Karbohidrat/Lemak Ulangan
1 2 3 4
1 19,78 19,7 25,21 34,39
2 24,14 24,4 24,.83 33,80
3 19,79 23,8 27,55 33,53
Lampiran 7. Perhitungan retensi protein Total protein ikan akhir 174,82 167,35 210,74 188,55
149,94 189,15 199,99 187,33 151,43 177,90 215,48 180,08 Rata-rata 476,20 534,39 626,21 555,96
Pakan ikan:
Protein pakan (% bobot basah) 36,12 35,8 35,56 35,9
Konsumsi protein 1 32,4 32,2 31,9 32,2 2 32,4 32,2 31,9 32,2 3 32,4 32,2 31,9 32,2 Rata-rata 32,4 32,2 31,9 32,2 Total konsumsi protein 1 391,7 390,0 415,6 425,9
2 388,5 382,5 400,3 399,0 3 376,0 396,5 414,6 414,7
Retensi Protein:
Lampiran 10. Analisa ragam dan Uji BNT konsumsi pakan uji
** berbeda sangat nyata pada taraf α(0,01)
Uji BNT(0,05)
Lampiran 11. Analisa ragam dan Uji BNT konversi pakan uji
Sumber db JK KT F-hitung F-tabel Keragaman 0,05 0,01 Perlakuan 3 0,0563 0,0188 8,19** 4,07 7,59 Galat 8 0,0183 0,00229
Total 11
** berbeda sangat nyata pada taraf α(0,01)
Lampiran 12. Analisa ragam dan Uji BNT laju pertumbuhan harian
** berbeda sangat nyata pada taraf α(0,01)
Uji BNT(0,05)
Lampiran 13. Analisa ragam dan Uji BNT retensi protein
Sumber db JK KT F-hitung F-tabel Keragaman 0.05 0.01 Perlakuan 3 346,18 115,39 9,86** 4,07 7,59 Galat 8 93,644 11,706
Total 11
** berbeda sangat nyata pada taraf α(0,01)
Lampiran 14. Analisa ragam dan Uji BNT retensi lemak
** berbeda sangat nyata pada taraf α(0,01)
Uji BNT(0,05)
Lampiran 15. Analisa ragam dan Uji BNT kadar lemak daging pada akhir percobaan
** berbeda sangat nyata pada taraf α(0,01)
Lampiran 16. Analisa ragam dan Uji BNT kadar protein daging pada akhir percobaan
Sumber db JK KT F-hitung F-tabel Keragaman 0,05 0,01 Perlakuan 3 146,78 48,928 5,64** 4,07 7,59 Galat 8 69,437 8,6796
Total 11
* berbeda nyata pada taraf α(0,05)
Uji BNT(0,05)
Nilai rata-rata Kelompok homogen Rasio
--- --- --- 1 84,42a I
2 81,98ab II 3 77,72cb II 4 75,50d ..I
Lampiran 17. Analisa ragam dan Uji BNT kadar abu daging pada akhir percobaan
Sumber db JK KT F-hitung F-tabel Keragaman 0,05 0,01 Perlakuan 3 0,401 0,13376 0,73ns 4,07 7,59 Galat 8 1,476 0,18445
Total 11
Lampiran 18. Analisa ragam dan Uji BNT kadar air daging pada
** berbeda sangat nyata pada taraf α(0,01)
Uji BNT(0,05)
Lampiran 19. Analisa ragam dan Uji BNT kadar lemak tubuh pada akhir percobaan
** berbeda sangat nyata pada taraf α(0,01)
Lampiran 20. Analisa ragam dan Uji BNT kadar protein tubuh pada
Lampiran 22. Analisa ragam dan Uji BNT kadar air tubuh pada
* berbeda sangat nyata pada taraf α(0,05)
Uji BNT(0,05)
Lampiran 24. Analisa ragam dan Uji BNT kadar air hati pada akhir percobaan
Sumber db JK KT F-hitung F-tabel Keragaman 0,05 0,01 Perlakuan 3 240,45 80,150 40,83** 4,07 7,59 Galat 8 15,705 1,9631
Total 11
** berbeda nyata pada taraf α(0,01)
Uji BNT(0,05)
Nilai rata-rata Kelompok homogen Rasio
--- --- --- 1 55,23a I