51
PENGARUH KONSENTRASI PELARUT DAN PRAPERLAKUAN
DENGAN LARUTAN ASAM KLORIDA TERHADAP EKSTRAKSI ASAM HUMAT
DARI KOMPOS KOTORAN SAPI
Chyntia Nabela1*, Intan Syahbanu1, Nurlina1 1
Program Studi Kimia, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H Hadari Nawawi, Pontianak
*email: chyntianabela@gmail.com
ABSTRAK
Potensi humat di Indonesia cukup tinggi karena sumber asam humat yang berasal dari lahan gambut melimpah. Asam humat dapat diperoleh dari kompos yang sudah matang. Kompos merupakan bahan organik yang terdiri dari sisa-sisa tanaman, hewan, ataupun sampah-sampah yang telah mengalami pelapukan. Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi pelarut KOH dan praperlakuan dengan larutan HCl pada proses ekstraksi asam humat dari kompos terhadap asam humat hasil ekstraksi dan karaktersitik yang diperoleh. Asam humat diekstraksi dengan pelarut KOH, dan terendapkan dengan penambahan HCl, kemudian dicuci dengan akuades dan diuji dengan AgNO3 hingga tidak terbentuk endapan,
selanjutnya dilakukan penentuan nilai keasaman, karboksil dan fenolik. Asam humat yang paling banyak didapat pada konsentrasi 0,25 M, dengan hasil tanpa praperlakuan sebesar 4,486 %, dan dengan hasil praperlakuan sebesar 6,699 %. Asam humat hasil ekstraksi dengan praperlakuan memperoleh nilai total keasaman, karboksil dan fenolik yaitu masing-masing 812,5 cmol/kg, 287,5 cmol/kg dan 525 cmol/kg.
Kata Kunci : asam humat, variasi konsentrasi, praperlakuan, nilai keasaman
PENDAHULUAN
Kompos merupakan bahan organik yang terdiri dari sisa-sisa tanaman, hewan, ataupun sampah-sampah yang telah mengalami pelapukan. Kompos memiliki peranan sangat penting bagi tanah karena dapat mempertahankan dan meningkatkan kesuburan tanah melalui perbaikan sifat kimia, fisika, dan biologinya. Hal ini dapat dikaitkan dengan kandungan senyawa kimia yang ada pada kompos. Kompos banyak mengandung asam-asam organik salah satunya yaitu asam humat (Mulyadi, 2008). Asam humat merupakan salah satu fraksi dari senyawa humat, selain asam fulvat dan humin. Asam humat adalah zat organik yang dihasilkan dari berbagai proses kimia, fisika dan biologis kandungan bahan organik yang terdapat di dalam tanah. Asam humat merupakan bahan makromolekul polielektrolit yang memiliki gugus fungsional seperti –COOH, –OH fenolat maupun –OH alkoholat. Asam humat telah banyak diteliti keterkaitannya dengan kesuburan dan pertumbuhan tanaman (Hidayah dan Muhamad, 2015).
Beberapa penelitian menyampaikan potensi asam humat dalam membantu meningkatkan kesehatan tanah dan pertumbuhan mikroorganisme tanah. Asam humat juga diketahui dapat merangsang pertumbuhan rambut akar, meningkatkan panjang akar, jumlah akar dan percabangan akar sehingga peran akar sebagai pengumpul nutrisi bagi tanaman dapat optimal (Cannelas, 2008).
Asing (2009) melakukan ekstraksi asam humat menggunakan variasi konsentrasi dari pelarut kalium hidroksida yaitu 0,1; 0,25 dan 0,5 M untuk mengekstrak asam humat, dari ketiga konsentrasi tersebut asam humat terbanyak diperoleh pada konsentrasi 0,25 M yaitu 11% sedangkan pada konsentrasi 0,1 M asam humat yang didapat hanya 3% dan pada konsentrasi 0,5 M asam humat yang didapat adalah sekitar 10,7%. Hasil penelitian tersebut menunjukkan bahwa konsentrasi pelarut yang digunakan berpengaruh pada perolehan asam humat.
Meskipun banyak penelitian yang telah dilakukan tentang isolasi asam humat dari
52 tanah gambut, namun penelitian tentang isolasi asam humat dengan kompos masih memerlukan pengamatan yang lebih jauh mengingat asam humat merupakan bahan organik alami yang sangat heterogen dan kompleks. Berdasarkan uraian tersebut maka dalam penelitian ini akan dilakukan ekstraksi asam humat dengan menggunakan variasi konsentrasi larutan kalium hidroksida dan praperlakuan dengan larutan asam klorida. Asam humat yang telah murni akan dikarakterisasi gugus fungsinya dengan metode titrasi dan spektrofotometri FT-IR.
METODOLOGI PENELITIAN Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat alat gelas, neraca analitik dan spektrofotometri FT-IR. Bahan-bahan yang digunakan adalah akuades (H2O), kalium hidroksida (KOH),
asam klorida (HCl), barium hidroksida (Ba(OH)2), perak nitrat (AgNO3), barium
asetat (Ba(CH3COO)2), natrium hidroksida
(NaOH) dan sampel kompos kotoran sapi.
Prosedur Kerja
Ekstraksi dan Pemurnian Asam Humat dengan Variasi Konsentrasi
Sebanyak 80 gram kompos yang telah dihaluskan dimasukkan ke dalam erlenmeyer yang berisi 1000 mL larutan kalium hidroksida 0,05; 0,1; 0,25 dan 0,5 M, kemudian dikocok menggunakan shaker selama 2 jam lalu didiamkan selama 24 jam. Setelah didiamkan, campuran disaring kemudian filtratnya disentrifugasi selama 15 menit dan disaring. Filtratnya kemudian diasamkan dengan asam klorida sampai pH=1, dikocok menggunakan shaker selama 2 jam dan didiamkan 24 jam. Campuran disentrifugasi selama 15 menit untuk mendapatkan fraksi asam humat (endapan).
Endapan asam humat kemudian dilarutkan dengan kalium hidroksida 0,3 M lalu disentrifugasi selama 15 menit kemudian disaring. Filtrat yang dihasilkan diasamkan kembali dengan asam klorida pekat hingga pH = 1, lalu dikocok dengan menggunakan shaker selama 2 jam kemudian didiamkan selama 24 jam, disentrifugasi pada 3950 rpm selama 15 menit lalu disaring. Residu yang didapat
dicuci dengan akuades dan diuji dengan AgNO3 sampai bebas Cl-. Residu
dikeringkan dengan oven pada suhu 105oC selama 2 jam.
Ekstraksi dan Pemurnian Asam Humat dengan Praperlakuan
Sebanyak 80 gram kompos yang telah dihaluskan dimasukkan ke dalam erlenmeyer yang berisi 1000 mL larutan asam klorida 0,1 M, kemudian dikocok menggunakan shaker selama 2 jam lalu didiamkan selama 24 jam. Setelah didiamkan, campuran disaring. Residunya dilarutkan dengan larutan kalium hidroksida 0,25 M, kemudian dikocok menggunakan shaker selama 2 jam lalu didiamkan selama 24 jam. Setelah didiamkan, campuran disaring kemudian filtratnya disentrifugasi selama 15 menit dan disaring. Filtratnya kemudian diasamkan dengan asam klorida sampai pH= 1, dikocok menggunakan shaker selama 2 jam dan didiamkan 24 jam. Campuran disentrifugasi selama 15 menit untuk mendapatkan fraksi asam humat (endapan).
Endapan asam humat kemudian dilarutkan dengan kalium hidroksida 0,3 M lalu disentrifugasi selama 15 menit kemudian disaring. Filtrat yang dihasilkan diasamkan kembali dengan asam klorida pekat hingga pH = 1, lalu dikocok dengan menggunakan shaker selama 2 jam kemudian didiamkan selama 24 jam, disentrifugasi selama 15 menit lalu disaring. Residu yang didapat dicuci dengan akuades dan diuji dengan AgNO3 sampai bebas Cl-.
Residu dikeringkan dengan oven pada suhu 105oC selama ± 2 jam.
Identifikasi Gugus Fungsional Asam Humat
Asam humat yang didapat dari proses ekstraksi diukur dengan menggunakan spektrofotometri FT-IR untuk mengetahui gugus fungsi yang dimiliki.
Penentuan Total Keasaman Asam Humat Sebanyak 20 mg asam humat dimasukkan ke dalam erlenmeyer dan ditambahkan 10 mL larutan Ba(OH)2 0,2 N
dalam kondisi atmosfer nitrogen. Erlenmeyer ditutup rapat dan dikocok dengan menggunakan shaker selama 24 jam pada temperatur kamar. Suspensi yang terbentuk disaring kemudian residu dibilas
53 dengan aquades, filtrat dan air bilasan digabung lalu dititrasi dengan larutan standar asam klorida 0,25 N hingga pH 8,4. Titrasi ini juga dilakukan pula terhadap larutan blangko yaitu larutan jenuh Ba(OH)2
0,2 N sebanyak 10 mL. Adapun total keasaman asam humat dapat dihitung dengan menggunakan persamaan sebagai berikut :
( )
( ) dimana :
Vb : volume asam klorida yang digunakan untuk titrasi blanko
Vs : volume asam klorida yang digunakan untuk titrasi sampel N : normalitas Asam klorida
Penentuan Konsentrasi Gugus karboksil (-COOH)
Sebanyak 20 mg asam humat dimasukkan ke dalam erlenmeyer dan ditambahkan 10 mL larutan Ba(CH3COO)2
0,2 M dan 40 mL aquades. Dalam waktu yang sama juga dilakukan pula terhadap larutan blangko yaitu 10 mL larutan Ba(CH3COO)2 0,2 M dan 40 mL aquades
kemudian larutan dikocok dengan menggunakan shaker selama 24 jam pada suhu kamar. Suspensi yang terbentuk disaring kemudian residu dibilas dengan aquades. Filtrat dan air bilasan digabung kemudian dititrasi dengan menggunakan larutan standar 0,25 M NaOH hingga pH 9,8. Adapun total keasaman asam humat dapat dihitung dengan menggunakan persamaan sebagai berikut :
( )
( )
dimana :
Vb : volume NaOH yang digunakan untuk titrasi blanko
Vs : volume NaOH yang digunakan untuk titrasi sampel
N : normalitas NaOH
Penentuan Konsentrasi OH Fenolik Kandungan gugus –OH fenolat merupakan selisih antara kemasaman total dengan kandungan gugus –COOH. Perhitungan kandungan gugus OH fenolat dalam cmol/kg dilakukan dengan rumusan sebagai berikut :
[OH] fenol = keasaman total – [COOH]
HASIL DAN PEMBAHASAN
Asam Humat Hasil Ekstraksi dan Pemurnian
Ekstraksi asam humat dari kompos telah dilakukan berdasarkan metode ekstraksi dengan larutan alkali. Metode ini berlaku universal untuk semua jenis tanah dan pereaksi yang digunakan tidak merusak bahan yang diisolasi serta penanganannya relatif mudah dan sederhana (Tarchitzky dkk., 1993).
Kompos yang telah halus dilarutkan dengan larutan kalium hidroksida. Larutan basa kuat digunakan untuk melarutkan asam humat, sehingga reaksi yang terjadi adalah reaksi pembentukan garam, dimana ion K+ dari KOH akan berinteraksi dengan ion negatif dari asam humat dan ion OH -akan berinteraksi dengan gugus H+ dari asam humat.
Kompos yang telah dilarutkan dikocok agar larutan tersebut homogen lalu didiamkan agar larutan dan endapan terpisah secara sempurna. Filtratnya kemudian diasamkan dengan asam klorida tujuannya adalah untuk menggumpalkan atau mengendapkan asam humat dan asam fulvat/humin akan larut dengan asam klorida. Asam humat yang telah didapat pada proses ekstraksi kemudian dicuci berulangkali dengan akuades untuk menghilangkan ion Cl-. Apabila filtrat pencucian asam humat ditambahkan larutan AgNO3dan tidak terbentuk endapan
putih AgCl, maka dapat disimpulkan bahwa asam humat sudah bebas ion Cl-. Adapun hasil ekstraksi asam humat dengan kalium hidroksida pada kompos dapat dilihat pada Tabel 1.
Tabel 1. Perolehan Asam Humat Hasil Ekstraksi Berdasarkan Variasi Konsentrasi Ekstraksi
Konsentrasi Asam Humat Hasil Ekstraksi (%)
0,05 M 1,217
0,1 M 2,935
0,25 M 4,486
0,5 M 3,451
Berdasarkan Tabel 1. dapat dijelaskan bahwa perolehan asam humat hasil ekstraksi paling tinggi terdapat pada konsentrasi 0,25 M yaitu 4,486%. Hal ini berarti pada konsentrasi 0,25 M merupakan
54 konsentrasi optimum untuk ekstraksi asam humat. Pada konsentrasi 0,5 M terjadi penurunan perolehan asam humat hasil ekstraksi. Hal ini dikarenakan pada konsentrasi tinggi peluang terjadinya interaksi akan semakin besar. Ion K+ mampu mengikat gugus ester yang mempunyai sifat hidrofilik. Hal ini juga sesuai dengan pernyataan Asing et al. (2009) bahwa penurunan perolehan asam humat hasil ekstraksi menggunakan konsentrasi KOH yang tinggi dapat disebabkan oleh peningkatan gangguan antar intermolekul yang merusak ikatan asam fulvat dengan asam humat, seperti ikatan –H atau ikatan tipe-ester sehingga mengubah rasio asam humat dan asam fulvat (Stevenson, 1982).
Pada penelitian ini konsentrasi kalium hidroksida 0,25 M digunakan kembali untuk studi pengaruh proses praperlakukan terhadap perolehan asam humat hasil ekstraksi. Praperlakuan dengan larutan asam klorida dilakukan untuk mengetahui dan membandingkan seberapa banyak asam humat yang diperoleh dengan proses ekstraksi tanpa dan dengan praperlakuan dengan larutan asam klorida.
Ekstraksi asam humat yang didahului praperlakuan dengan HCl dimulai dengan pencucian kompos dengan asam klorida (HCl) 0,1 M. Tujuan pencucian dengan larutan HCl adalah untuk menghilang pengotor dan bahan-bahan anorganik yang mungkin terkandung di dalam kompos, selain itu senyawa humat lainnya (asam fulvat dan humin) akan larut dalam HCl sehingga pada tahap pencucian dengan larutan asam, asam fulvat dan humin tereduksi.
Perolehan asam humat hasil ekstraksi yang didapat melalui proses praperlakuan dengan HCl adalah sebesar 6,699%. Hasil ini lebih banyak dari proses ekstraksi tanpa
praperlakuan dengan HCl. Asam humat hasil praperlakuan dengan larutan asam klorida lebih baik dari ekstraksi asam humat tanpa melakukan proses praperlakuan. Hal ini dikarenakan dengan melakukan pencucian dengan larutan asam klorida terlebih dahulu dapat membuat pengotor bahan organik atau anorganik hilang sebelum kompos diekstrak dengan larutan kalium hidroksida. Hal ini juga sesuai dengan pernyataan Stevenson (1994) yaitu asam klorida diyakini mampu membebaskan asam humat dari pengotor bahan-bahan organik.
Kandungan Gugus Fungsional Asam Humat
Keasaman total asam humat disebabkan oleh adanya proton yang dapat terdisosiasi atau pelepasan ion-ion H+ pada gugus-gugus karboksilat dan gugus-gugus hidroksil fenolat. Dalam penelitian ini penetapan kandungan keasaman total asam humat menggunakan metode barium hidroksida (Baryta Absorption Methods). Metode tersebut didasarkan pada pelepasan ion H+ dari gugus-gugus fungsional asam humat yang bersifat asam. Reaksi yang terjadi dimodelkan sebagai berikut (Stevenson, 1994):
2 RH + Ba(OH)2 (berlebih) → R2Ba + 2H2O
Ba(OH)2 (sisa) + 2HCl → BaCl2 + 2H2O
dimana R adalah makromolekul dan H adalah proton gugus –COOH atau -OH yang bersifat asam.
Penentuan gugus karboksilat dilakukan dengan menggunakan metode Ca-asetat. Reaksi yang terjadi merupakan suatu reaksi yang menghasilkan pembentukan dan pelepasan asam asetat (Tan,1998):
2 R-COOH + Ba(CH3COO)2 → Ba(R-COO)2
+ 2CH3COOH
CH3COOH + NaOH → CH3COONa + H2O
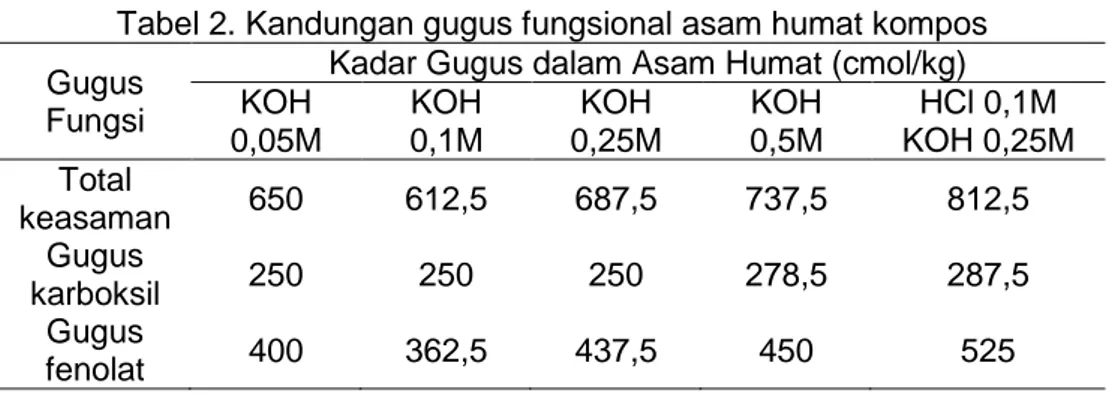
Tabel 2. Kandungan gugus fungsional asam humat kompos Gugus
Fungsi
Kadar Gugus dalam Asam Humat (cmol/kg) KOH 0,05M KOH 0,1M KOH 0,25M KOH 0,5M HCl 0,1M KOH 0,25M Total keasaman 650 612,5 687,5 737,5 812,5 Gugus karboksil 250 250 250 278,5 287,5 Gugus fenolat 400 362,5 437,5 450 525
55 Nilai keasaman total menunjukkan kapasitas pertukaran kation dan kekuatan membentuk kompleks (Stevenson, 1994). Pada penelitian ini, asam humat yang diekstraksi dengan KOH 0,25 M dengan praperlakuan HCl 0,1 M memiliki total keasaman paling tinggi. Hal ini sesuai dengan hasil perolehan asam humat yang diekstraksi dengan KOH 0,25 M dengan praperlakuan HCl 0,1 M. Keasaman total yang tinggi berarti kapasitas pertukaran kation dan kekuatan membentuk kompleksnya lebih tinggi. Keasaman yang lebih tinggi ini juga dapat dihubungkan pada terjadinya ionisasi H+ dari gugus karboksil dan gugus fenolik yang ditemukan dalam rantai alifatik atau cincin aromatis (Schnitzer, 1982).
Karakterisasi Asam Humat Hasil Isolasi dari Kompos Menggunakan FTIR (Fourier Transform Infra Red)
Berdasarkan hasil analisis dengan spektra FTIR sebagaimana diberikan pada Gambar 2, diketahui bahwa asam humat hasil variasi konsentrasi kalium hidroksida dan praperlakuan dengan asam klorida menunjukkan pola yang sama dengan struktur asam humat standar. Berdasarkan spektra tersebut muncul pita-pita utama
yang merupakan karakteristik dari spektra asam humat. Pita-pita tersebut muncul pada daerah 3354,94 cm-1 dengan adsorpsi kuat menunjukkan bahwa pada daerah ini terjadi serapan rentang (OH). Namun tidak menutup kemungkinan bahwa pada daerah ini juga terdapat rentang (-N-H) dan ikatan hidrogen. Terjadinya serapan rentang (OH) tersebut merupakan karakteristik asam humat karena adanya gugus fungsional fenolik dan alkoholik.
Pita karakteristik lain yang menunjukkan bahwa cuplikan hasil ekstraksi tersebut adalah asam humat yaitu pita serapan pada 2942,57 cm-1, pita ini terlihat sangat signifikan pada asam humat. Pita ini dapat berupa rentang vibrasi yang asimetri maupun simetri khususnya pada rentang alifatis (C-H) dalam gugus metil yang biasanya dalam bentuk keton terkonjugasi dengan struktur sebagai (CO-CH2-CO-).
Pita di daerah 1631,33 cm-1 dan 1633,65 cm-1 menunjukkan adanya gugus aromatis (C=C) ikatan rangkap terkonjugasi dengan (C=O) atau (COO). Pita ini sangat jelas bila hanya satu gugus alkil menempel pada ikatan rangkap dua. Semakin banyak gugus alkil yang menempel, intensitas absorpsi berkurang karena vibrasi terjadi dengan perubahan momen dipol yang lebih kecil.
Tabel 3. Bilangan Gelombang Utama Spektra Inframerah Asam Humat Kompos Bilangan Gelombang Standar (cm-1)* Asam Humat Ekstraksi dengan KOH 0,25 M (cm-1) Asam Humat Ekstraksi dengan Praperlakuan (cm-1)
Perkiraan Gugus Fungsi
3400 – 3300 3354,94 3354,93 Regang O-H dan N-H
2940 – 2900 2942,57 2942,57 Regang C-H
1660 – 1630 1631,33 1633,65 C-O dari amida, kuinon atau C=O dari ikatan –H konjugasi keton 1590 – 1517 1552 1517,82 Regang simetrik COO
-, N-H deformasi
dan C=N 1460 – 1400 1443,45 1445,54 COO-, C-H alifatik
1280 – 1200 1232,24 1236 C-O dan deformasi O-H dari COOH, C-O dari aril eter
56
Gambar 1. (a) Spektra Inframerah asam humat hasil ekstraksi KOH 0,25 M, (b) spektra Inframerah asam humat hasil ekstraksi HCl 0,1 M KOH 0,25 M (praperlakuan)
57 Bilangan gelombang gugus fungsional pada spektra inframerah tersebut di atas sesuai dengan spektra inframerah asam humat yang dilakukan oleh Rahmawati (2011). Data spektra inframerah asam humat yang diperoleh dalam penelitian ini, juga sesuai dengan hasil karakterisasi asam humat yang telah dilakukan oleh Stevenson (1994) yang menunjukkan bahwa karakteristik spektra serapan inframerah asam humat ditandai dengan munculnya pita serapan pada angka gelombang 3400, 2900, 1600 dan 1200 cm-1. Dengan demikian dapat dinyatakan bahwa hasil isolasi dan pemurnian yang dilakukan dalam penelitian ini menghasilkan asam humat dengan gugus-gugus fungsional sesuai dengan gugus-gugus fungsional asam humat hasil isolasi peneliti sebelumnya.
SIMPULAN
Berdasarkan penelitian yang telah dilakukan diperoleh simpulan yakni asam humat pada konsentrasi 0,25 M lebih tinggi yaitu 4,486 % dan asam humat hasil praperlakuan dengan Asam klorida yaitu 6,699 %. Selain itu, nilai keasaman gugus karboksil dan gugus fenolik yang paling tinggi dari asam humat pada praperlakuan HCl 0,1 M KOH 0,25 M yaitu keasaman total sebesar 812,5 cmol/kg, gugus karboksil sebesar 287,5 cmol/kg dan gugus fenolik sebesar 525 cmol/kg.
DAFTAR PUSTAKA
Asing J , N.C. Wong and S. Lau. 2009, Optimization Of Extraction Method And Characterization Of Humic Acid Derived From Coals and Composts. J. Trop. Agric. and Fd. Sc. 37(2)(2009): 211–223.
Canellas, L. P., L. R. L. Teixeira Junior, L. B. Dobbss, C. A. Silva, L. O. Medici, D. B. Zandonadi, and A. R. Façanha.
2008b. Humic Acids
Crossinteractions With Root And Organic Acids. Ann. Appl. Biol., 153:157-166.
Canellas, L.P., Riccardo Spaccini, Alessandro Piccolo, Leonardo B.
Dobbss, Anna L. Okorokova-Facanha, Gabriel de Araujo Santos, Fabio L. Olivares and Arnoldo R. Facanha, 2009, Relationships Between Chemical Characteristics and Root Growth Promotion of Humic Acids Isolated From Brazilian Oxisols. Soil Science., 174:611-620. Hidayah, F.F,. dan Muhamad, I,. 2015,
Pemanfaatan Biomassa dan Limbah Peternakan untuk Pembutan Pupuk Organik Berasam Humat Tinggi, Program Studi Pendidikan Kimia Universitas Muhammadiyah Semarang. Seminar Nasional Konservasi dan Pemanfaatan Sumber Daya Alam 2015.
Mulyadi, A., 2008, Karakteristik Kompos dari Bahan Tanaman Kaliandra, Jerami Padi dan Sampah Sayuran, Program Studi Ilmu Tanah Fakultas Pertanian Institut Pertanian Bogor, (Skripsi).
Rahmawati, A., 2011, Isolasi dan Karakterisasi Asam Humat dari Tanah Gambut, Prodi Tadris Kimia, Fakultas Tarbiyah IAIN Walisongo, Phenomenon, 2:117-136.
Rahmawati, S., 2003, Karakterisasi Asam Humat dari Kompos Gambut dan Kompos Daun Karet, Jurusan Tanah, Fakultas Pertanian, Institut Pertanian Bogor.
Schnitzer, M., 1986, Pengikatan Bahan Humat Oleh Koloid Mineral Tanah, dalam buku Interaksi Mineral Tanah dengan Organik Alami dan Mikroba, 1997, Huang, P. M dan Schnitzer, M. (editor), Gadjah Mada University Press, Yogakarta, 119-155.
Stevenson, F.J., 1994, Humus Chemistry: Genesis, Composition, Reaction, 2nd Ed. John Wiley & Sons, Inc. New York.
Tan, K.H., 1992, Principles of Soil Chemistry, second edition, Marcel Dekker Inc., New York.
Tarchitzky, J., Y.Chen., dan A.Banin, 1993, Humic Subtances and pH Effects on Sodium-and Calcium-Montmorillonite Flocculation and Dispersion, Soil Science Soc. Am. J, 57 : 367-372.