PROSIDING
SEMINAR NASIONAL REKAYASA KIMIA DAN PROSES 2004 ISSN : 1411 - 4216
PENGARUH KADAR AIR DAN LAJU UDARA
PADA PEMBAKARAN LIMBAH PADAT PABRIK KERTAS
Kusnarjo, Fransisca Liana Ekasari dan Indiar RosminggorJurusan Teknik Kimia FTI – ITS
Telp : (031) 5946240 E-mail : perpanmas@yahoo.com
Kampus ITS Keputih Sukolilo, Surabaya 60111
INTISARI
Penelitian ini bertujuan untuk melihat pengaruh kadar air dalam limbah padat pabrik kertas dan laju udara terhadap temperatur pembakaran limbah padat pabrik kertas yang mengandung pith dan kadar air. Pembakaran dilakukan didalam tungku pembakaran yang terbuat dari pipa besi berdiameter 10,16 cm , tinggi 40 cm dengan cerobong berdiameter 3,16 cm tinggi 50 cm. Limbah padat yang berkadar air : 10,826%; 19,993%; 31,786%; 40,634% dan 51,772% dibakar dengan laju alir udara : 3432000 l/min; 3200000 l/min; 2952000 l/min; 2688000 l/min dan 2408000 l/min. Temperature hasil pembakaran diukur menggunakan thermocouple setiap selang waktu 1 menit sampai pembakaran selesai dan abu (ash) sisa pembakaran ditimbang. Dari hasil penelitian yang telah dilakukan didapatkan kesimpulan : pada laju udara yang tetap semakin kecil kadar air didalam limbah akan semakin besar temperatur pembakaran dan pada kadar air tetap semakin besar laju udara yang digunakan akan semakin naik temperatur pembakaran yang terjadi. Semakin besar laju udara yang digunakan semakin sedikit sisa pembakaran yang dihasilkan.Temperature tertinggi yang tercapai pada pembakaran limbah pada kadar air 10,826 % sebesar 765oC dengan laju udara 3432000 l/min. Sisa pembakaran akan bertambah besar dengan naiknya kadar air dan menurunnya laju udara.
Kata kunci : limbah padat pabrik kertas , pembakaran
Abstract
The objective of this research is to study the effect of moisture and air velocity on combustion temperature while paper solid waste was combusted in the furnace with dimension 10,16 cm on diameter and 40 cm in high and chimney 3,81 cm on diameter and 50 cm in high. The paper solid waste generally containing pith and water was combusted. For this research the, water content is varied : 10,826; 19,993; 31,786; 40,634 , 51,772% and air flow varied : 3432000 l/min; 3200000 l/min; 2952000 l/min; 2688000 l/min and 2408000 l/min. . Feed entered furnace and first burning used kerosene constructively air. Temperatures combustion was measured by thermocouple every 1 minute during 40 minute until the combustion finish. Dusty ash of combustion was generated. This research the following atconstant air flow rate, the combustion temperature increase with decreasing water content in the waste and at constant water content in the waste, the combustion temperature increase with increasing air flow rate. The amount of combustion residue decrease with increasing air flow rate. The highest combustion temperature (765OC) was reached at water content of 10,826 % and air flow rate of 3432000 l/min .The amount of combustion residue increasing with increasing water content and decreasing air flow rate
Key words : paper solid waste, combustion
1. Pendahuluan
Limbah padat pabrik kertas biasanya mengandung pith dan air dan senyawa kimia jumlahnya cukup banyak sehingga untuk membuangnya mengalami kesulitan dan mengganggu lingkungan. Dari hasil analisa buangan pabrik kertas, senyawa yang terkandung didalam pith tersebut antara lain adalah hidrokarbon (C, H dan O) dan juga bahan lain seperti chlor (Cl). Untuk mengatasai hal tersebut yaitu dengan mengurangi volume dan menghilangkan kandungan bahan yang mengganggu lingkungan, agar dapat dibuang dengan
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-1
aman. Salah satu cara pengolahannya dengan cara dibakar. Ada beberapa keuntungan penanganan dengan cara tersebut yaitu memanfaatkan panas yang timbul dan abu sisia pembakaranya. Selain kandungan bahan tersebut pada limbah pabrik kertas masih mengandung banyak air sehingga volume bahan menjadi lebih besar dan sulit dilakukan pembakaran.
Dari penelitian yang terdahulu telah dilakukan penelitian yang mempelajari tentang pembakaran dengan parameter temperatur pembakaran pada berbagai bahan. Maka perlu dilakukan penelitian dengan cara pembakaran untuk menentukan temperatur pembakaran yang tepat untuk membakar limbah padat yang mengandung pith. Selain itu juga perlu mencari kadar air yang terbaik agar proses pembakaran dapat berlangsung dengan baik. Berdasarkan kandungan air dan kebutuhan udara dalam suatu pembakaran maka perlu dicari pengaruh kadar air yang tepat agar tercapai pembakaran sempurna dan jumlah panas dihasilkan terbesar.
2. Tinjauan pustaka
Agar pembakaran berlangsung dengan sempurna ada lima faktor yang perlu diperhatikan ,yaitu : a.pencampuran murni reaktan (proper mixing)
b.jumlah udara primer dan sekunder c. temperature pembakaran yang sesuai d. waktu untuk berlangsungnya reaksi e. kerapatan untuk merambatkan nyala api.
Pada umumnya dalam proses pembakaran oksigen yang diperlukan diambil dari udara yang mengandung : Oksigen, Nitrogen, Argon, Oksida Arang dan uap air Didalam literature udara yang digunakan dalam proses pembakaran adalah udara kering. Sedangkan pengaruh kelembaban udara diperhitungkan pada penentuan kebutuhan udara agar proses pembakaran dapat terjadi sacara sempurna. Dalam proses pembakaran sangat sulit mendapatkan percampuran yang baik maka tidak pernah diperoleh pembakaran yang baik sehingga untuk mendapatkan pembakaran yang sempurna dapat dilakukan dengan menyediakan udara berlebih (excess air). Kelebihan udara akan menentukan komposisi gas buang baik berupa hasil pembakaran sempurna misalnya : karbondioksida, air dan sulfurdioksida serta beberapa hasil pembakaran tak sempurna termasuk sebagian bahan bakar yang tak terbakar antara lain : karbonmonoksida, hidroksil dan aldehid, nitrogen serta senyawa-senyawa nitrogen misalnya nitrat oksida (NO), nitrogen oksida (NO2).
Biasanya pembakaran limbah padat dilakukan didalam incenerator sehingga peristiwa pembakaran yang terjadi dalam incinerator meliputi :
a. Drying
Pada umumnya, pengeringan (drying) didalam incenerator mempunyai pengertian menguapkan sejumlah kecil air atau zat cair lain dari bahan padat zat padat sehingga mengurangi kandungan zat cair di dalam zat padat itu sampai suatu jumlah tertentu.
b. Pirolisis
Pirolisis adalah peristiwa dekomposisi kimia dan fisika dari suatu bahan akibat pemanasan. Pirolisis disebut juga proses devolatilisasi. Jika suatu bahan yang mengandung karbon mengalami pirolisis, kandungan bahan volatilnya yang kaya akan unsur hidrogen akan terdistilasi, meninggalkan residu padat yang kaya akan karbon. Pada temperatur tinggi terjadi pengusiran zat-zat organik yang mudah menguap, disusul dengan pemecahan lignoselulose disertai dengan pengeluaran kalor dan peristiwa itu terjadi pada temperatur yang berbeda-beda, tergantung pada jenis bahan baku. Reaksi eksotermik tidak berjalan lama. Pemecahan hidrokarbon pada umumnya berlangsung secara endotermik. Bila temperatur ditingkatkan lagi (400O - 600OC) terbentuklah gas CO, H
2, CO2, hidrokarbon rendah menengah CmHn yang segera
meninggalkan reaktor bersama-sama dengan senyawa yang rantainya lebih panjang, yang akan mengembun pada pendinginan. Sebagai sisa pirolisis biasanya berupa arang yang kering.
c. Gasifikasi
Gasifikasi adalah proses mereaksikan gas ke dalam incenerator untuk mendorong pembentukan produk gas atau melepaskan panas di dalam incenerator. Gas yang direaksikan biasanya oksigen, uap air, atau hidrogen yang menyebabkan reaksi seperti dibawah ini :
C + O2 CO2
C + H2O CO + H2
C + ½ O2 CO
C + 2H2 CH2
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-2
Reaksi gasifikasi biasanya dikondisikan pada temperatur tinggi daripada temperatur yang diperlukan pada pirolisis. Untuk gasifikasi semua zat padat dikonversi menjadi gas.
Pembakaran adalah proses oksidasi eksotermik. Oksigen di dalam udara bereaksi dengan karbon dan hidrogen yang ada dalam bahan bakar membentuk karbon monoksida, karbondioksida dan uap air. Untuk stoikiometri pembakaran hidrokarbon murni CmHn, seperti yang terlihat pada persamaan (1)
CmHn + (m + n/4)O2 + 3.76(m + n/4)N2 → mCO2 + n/2H2O + 3.76(m + n/4) N2 ... ... (1)
Kelebihan udara (excess air) yang dibutuhkan untuk pembakaran sempurna tersebut tergantung pada
banyaknya materi yang akan dibakar dengan jumlah teoritis seperti yang terlihat pada persamaan (2). .
dibutuhkan yang O dibutuhkan yang O -proses memasuki O 100 udara kelebihan % 2 2 2 × = ... ... (2)
Jumlah panas yang dapat dihasilkan pada pembakaran dapat dihitung dengan menggunakan persamaan neraca energi seperti yang terlihat pada persamaan (3).
[Akumulasi energi pada sistim] = [energi masuk sistim] – [energi keluar sistim] + [generasi energi pada sistim] – [konsumsi energi dalam sistim] ... (3)
Sedangkan enthalpy absolute hasil reaksi dari suatu senyawa pada temperatur tertentu dapat dihitung seperti yang terlihat pada persamaan (4).
hT = ∆H°f + (hr - h298) ...………...
(4) Biasanya pada proses pembakaran tidak ada kerja sedangkan perubahan energi potensial diabaikan dan energi kinetik yang ada sangat tergantung dari penerapan particular. Dengan demikian neraca energi untuk proses pembakaran dapat dinyatakan seperti pada persamaan (5).
Q = ∆H + ∆KE
= ∆ n0 ( Ho + KEo ) - ∆ ni ( Hi+ KEi ) ... (5)
dimana :
ni : mol komponen masuk , ( mol )
no : mol komponen keluar , ( mol )
Q : perpindahan panas untuk ni mol dari bahan bakar. ( cal )
Hi dan Hj : enthalpy absolute untuk senyawa , ( cal )
Jika persamaan (4) disubstitusikan ke dalam persamaan (5) akan didapatkan jumlah panas yang dihasilkan akan mengikuti persamaan seperti yang terlihat pada persamaan (6)
(
)
[
]
[
(
)
∑
∆ + − −∑
∆ + − = P R T f i T f j H h h n H h h n Q 298 0 298 0]
... (6)apabila energi kinetic diabaikan maka persamaan (6) akan menjadi seperti persamaan (7)
(
)
(
)
∑
∆ −∑
∆ +∑
− −∑
− = P R P R T i T j f i f j H n H n h h n h h n Q 0 0 298 298 ... (7)apabila : ∆ =
∑
∆ −∑
∆ maka persamaan (7 ) akan terlihat seperti pada persamaan (8)P R f i f j R n H n H H0 0 0
(
)
(
)
(
)
∑
− −∑
− −∑
− + ∆ = p R R T i T i T i R n h h n h h n h h H Q 298 298 298 0 298 , ... (8)Persamaan diatas hanya digunakan jika enthalpy reaksi untuk reaksi yang diinginkan terdapat dalam tabel. Dengan cara lain, untuk data yang tersedia harga enthalpy pembentukan digunakan persamaan (8). Untuk
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-3
mengetahui temperatur nyala akhir dapat dilakukan dengan cara coba-coba (trial). Pada saat temperature nyala akhir ditrial perpindahan panas Q pada persamaan (8) dianggap sama dengan nol sedangkan prosesnya
dianggap adiabatic sehingga HP sama dengan HR. Hal ini dilakukan untuk memperkirakan temperature nyala
akhir Tf,. Selanjutnya enthalpy produk pembakaran dihitung mempergunakan temperatur trial. Harga HP
didapat dibandingkan dengan HR dan dilakukan iterasi pada T sampai HP sama dengan HR.
3. Metodologi penelitian
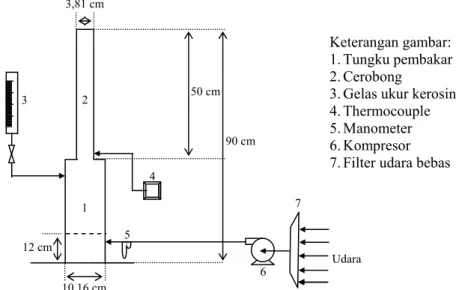
Pada penelitian ini digunakan peralatan seperti yang terlihat pada gambar 1 berupa tungku pembakaran yang dibuat dari pipa besi berukuran 10,16 cm tinggi 40 cm. dan cerobong berdiameter 3,8 cm. tinggi 50 cm. dilengkapi dengan distributor udara dan bahan bakar kerosin. Pada tungku pembakaran dipasang kasa pada jarak 12 cm. dari dasar untuk menahan bahan yang akan dibakar dan memberikan kruang untuk udara yang dihembuskan dari luar serta mengayak sisa pembakaran yang akan jatuh pada dasar tungku.. Untuk memasukkan udara digunakan kompressor udara sedangkan untuk memasukkan kerosin digunakan tabung kerosin disamping tungku pembakaran.
Sebagai alat ukur digunakan flowmeter untuk mengukur jumlah udara yang digunakan dan thermocouple untuk mengukur temperatur pembakaran yang dipasang pada dasar cerobong.
Keterangan gambar:
1.Tungku pembakar
2.Cerobong
3.Gelas ukur kerosin
4.Thermocouple
5.Manometer
6.Kompresor
7.Filter udara bebas
3 4 12 cm 50 cm 90 cm 3,81 cm 10,16 cm 7 6 5 1 2 Udara
Gambar 1. Skema peralatan penelitian
Dengan susunan alat seperti yang terlihat pada gambar 1, umpan seberat 100 gram dengan kadar air 10,826% dimasukkan dalam tungku dan diukur ketinggiannya. Kompresor dijalankan dan udara dialirkan kedalam tungku dengan laju udara 3432000 l/min dan kerosin dialirkan sebesar 25 ml sebagai bahan pembakar awal. Selanjutnya dilakukan pembakaran dengan menyalakan dengan api. Diamati temperatur menggunakan thermocouple pada interval waktu 1 menit selama 40 menit sampai umpan diperkirakan terbakar habis. Sisa pembakaran yang terjadi ditimbang untuk mengetahui berapa jumlah bahan yang telah terbakar.
Dilakukan hal sama untuk kadar air : 19,993%; 31,786%; 40,634% dan 51,772%. Hal yang sama dilakukan untuk berbagai laju udara, yaitu: 3200000 l/min; 2952000 l/min; 2688000 l/min dan 2408000 l/min.
4. Hasil dan pembahasan
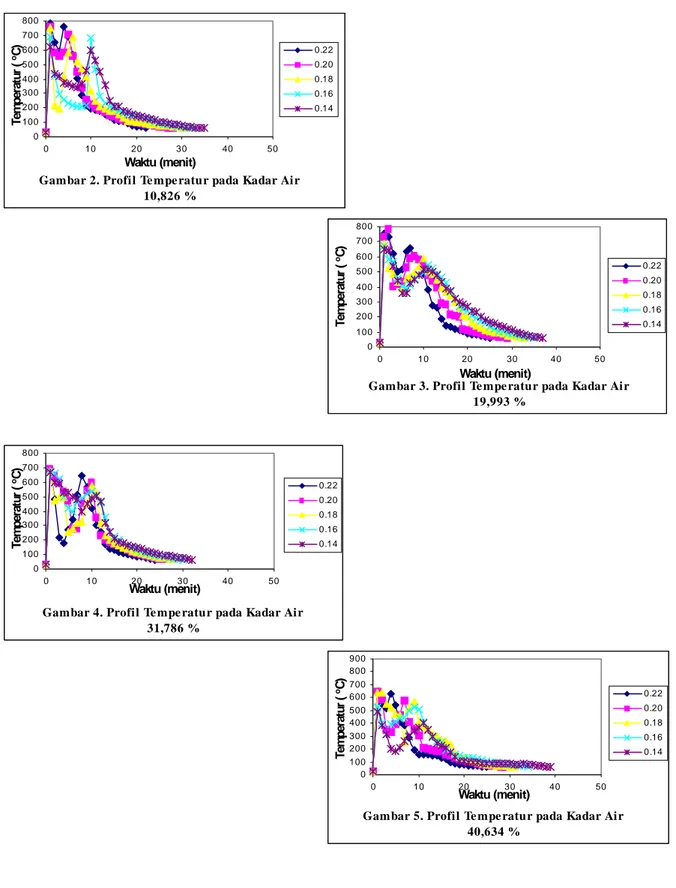
Dari hasil penelitian yang telah dilakukan seperti yang terlihat pada gambar 2 sampai dengan gambar 11 terlihat bahwa kadar air 10,826% dan laju udara sebesar 3432000 l/menit memberikan suhu pembakaran
yang tertinggi sebesar 765oC dengan waktu pembakaran selama 23 menit. Untuk kadar air lebih besar dan
laju udara lebih kecil waktu pembakaran lebih lama, suhu pembakaran lebih rendah bahkan pada kadar air 51,772% pembakaran menjadi tidak sempurna. Hal ini disebabkan reaksi pembakaran berjalan lancar dan air yang terdapat pada bahan tidak mengurangi suhu pembakaran.
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-4
Gambar 2. Profil Te mpe ratur pada Kadar Air 10,826 % 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 0.22 0.20 0.18 0.16 0.14
Gambar 3. Profil Te mpe ratur pada Kadar Air 19,993 % 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 0.22 0.20 0.18 0.16 0.14
Gambar 4. Profil Te mpe ratur pada Kadar Air 31,786 % 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 0.22 0.20 0.18 0.16 0.14
Gambar 5. Profil Te mpe ratur pada Kadar Air 40,634 % 0 100 200 300 400 500 600 700 800 900 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 0.22 0.20 0.18 0.16 0.14
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-5
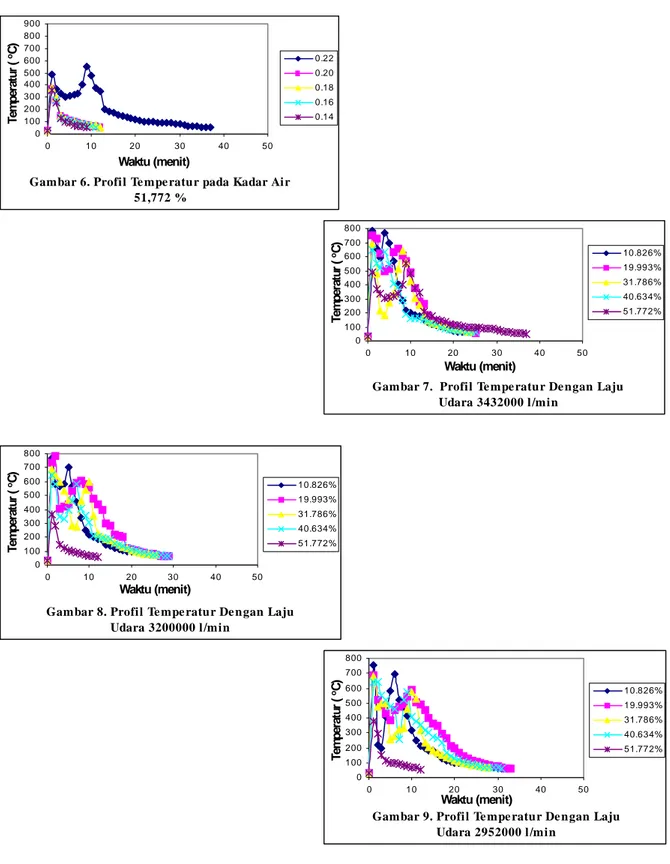
Gambar 6. Profil Te mpe ratur pada Kadar Air 51,772 % 0 100 200 300 400 500 600 700 800 900 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 0.22 0.20 0.18 0.16 0.14
Gambar 7. Profil Te mpe ratur De ngan Laju Udara 3432000 l/min 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 10.826% 19.993% 31.786% 40.634% 51.772%
Gambar 8. Profil Te mpe ratur De ngan Laju Udara 3200000 l/min 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 10.826% 19.993% 31.786% 40.634% 51.772%
Gambar 9. Profil Te mpe ratur De ngan Laju Udara 2952000 l/min 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 10.826% 19.993% 31.786% 40.634% 51.772%
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-6
Gambar 10. Profil Te mpe ratur De ngan Laju Udara 2688000 l/min 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 10.826% 19.993% 31.786% 40.634% 51.772%
Gambar 11. Profil Te mpe ratur De ngan Laju Udara 2408000 l/min 0 100 200 300 400 500 600 700 800 0 10 20 30 40 50 Waktu (menit) Temperatur ( oC) 10.826% 19.993% 31.786% 40.634% 51.772%
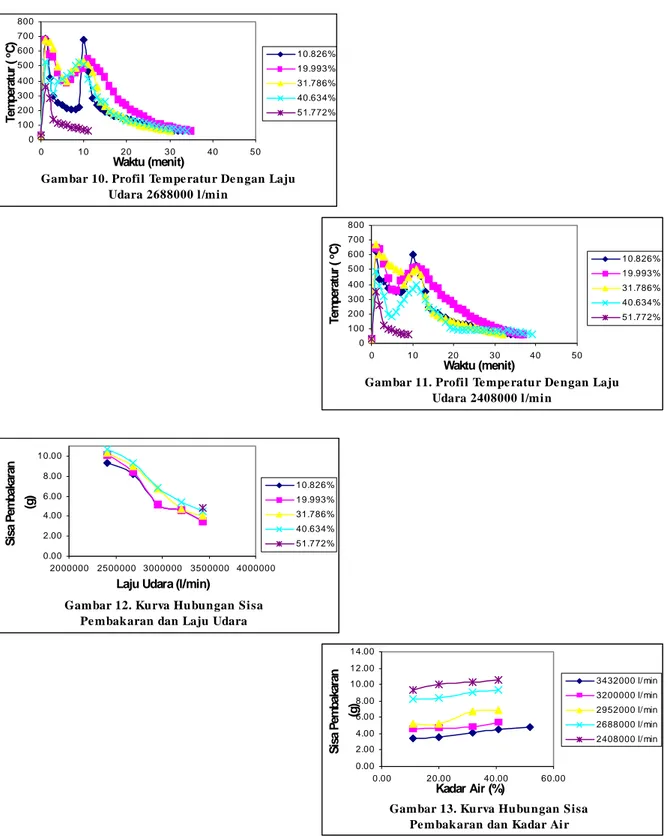
Gambar 12. Kurva Hubungan Sisa Pe mbakaran dan Laju Udara
0.00 2.00 4.00 6.00 8.00 10.00 2000000 2500000 3000000 3500000 4000000
Laju Udara (l/min)
Sisa Pembakaran (g) 10.826% 19.993% 31.786% 40.634% 51.772%
Gambar 13. Kurva Hubungan Sisa Pe mbakaran dan Kadar Air
0.00 2.00 4.00 6.00 8.00 10.00 12.00 14.00 0.00 20.00 40.00 60.00 Kadar Air (%) Sisa Pembakaran (g) 3432000 l/ min 3200000 l/ min 2952000 l/ min 2688000 l/ min 2408000 l/ min
Pada gambar 12 dan 13 menunjukkan bahwa kadar air yang rendah dengan laju udara yang terbesar memberikan sisa pembakaran yang kecil sedangkan pada kadar air yang semakin besar dan laju udara semakin rendah sisa pembakaran semakin besar.
5. Kesimpulan
Dari hasil penelitian dapat disimpulkan sebagai berikut :
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-7
a. Temperatur pembakaran akan semakin besar dengan semakin besarnya laju udara pada kadar air tetap.
Temperature tertinggi dihasilkan pada kadar air 10,826 % sebesar 765oC dengan laju udara 3432000
l/min.
b. Sisa pembakaran semakin besar dengan semakin besarnya kadar air dan semakin kecilnya laju udara.
Ucapan terima kasih
Ucapan terima kasih kami sampaikan pada Jurusan Teknik Kimia FTI-ITS yang telah membiayai presentasi makalah ini pada Seminar Rekayasa Kimia dan Proses 2004.
Daftar pustaka
Corbitt, Robert A. 1998. Handbook of Environmental Engineering. 2nd edition. New York: McGraw Hill
Companies.
Culp, Archie W. 1996. Prinsip-prinsip Konversi Energi. Jakarta: Penerbit Erlangga.
Djunaedi, Imam, dkk. 2004. Analisa Bahan Bakar dan Udara Pembakaran Arang Kayu pada Model Tungku
Peleburan Logam Alumunium. Yogyakarta: Prosiding Seminar Teknik Kimia.
Himmelblau, David M. 1989. Basic Principles and Calculations in Chemical Engineering. 5th edition.
Prentice-Hall International, Inc.
Ross, Richard P. 1980. Handbook of Industrial Waste Disposal. New York: Van Nostrand Reinhold
Company.
Sharma, Chander Mohan. 1987. Fuel and Combustion. New Delhi: McGraw Hill
Tchobanoglous, George Hilary Theisen, Rolf Eliassen. 1977. Solid Waste: Engineering Principles and
Management Issues. Kogakusha: McGraw Hill, Inc.
Daftar notasi
Cp : Kapasitas panas, cal/gmol.K
T : Temperatur, K
∆H : entalpi, cal/jam
Q : banyaknya panas, kJ/kgmol
ni : mol komponen masuk
nj : mol komponen keluar
Q : perpindahan panas untuk ni mol dari bahan bakar.
Hi dan Hj : enthalpy absolute untuk senyawa
∆Hf : enthalpy pembentukan
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK H-11-8