II. TINJAUAN PUSTAKA
A. Brokoli (Brassica oleraceaL. var. italic)
Brokoli merupakan sayuran subtropik yang termasuk dalam golongan tanaman kubis-kubisan dan sering dikenal dengan nama kubis bunga hijau. Pemanenan brokoli dilakukan pada saat bunga mencapai ukuran maksimal dan telah padat (kompak), tetapi kuncup bunganya belum mekar. Umur panen adalah 47 - 67 hari setelah tanam. Waktu panen yang paling tepat adalah pagi dan sore hari, dengan cara memotong tangkai bunga bersama sebagian batang dan daun-daunnya sepanjang 25 cm dengan menggunakan pisau. Untuk pemasaran jarak jauh sebaiknya disertakan enam helai daun. Sedangkan untuk tujuan pemasaran dekat, hanya disertakan 3 - 4 helai daun, dan ujung-ujung daunnya dipotong (Rukmana, 1994). Brokoli mempunyai tingkat taksonomi sebagai berikut:
Divisi : Spermatophyta
Sub divisi : Dycotyledonae
Famili : Cruciferae
Genus : Brassica
Spesies : Brassica oleraceaL. var italic
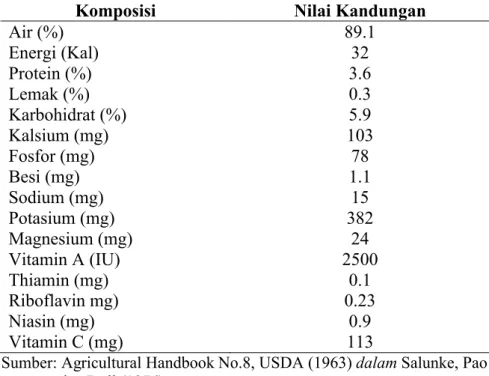
Tabel 1. Nilai nutrisi brokoli per 100 g bagian yang dapat dimakan
Komposisi Nilai Kandungan
Air (%) 89.1 Energi (Kal) 32 Protein (%) 3.6 Lemak (%) 0.3 Karbohidrat (%) 5.9 Kalsium (mg) 103 Fosfor (mg) 78 Besi (mg) 1.1 Sodium (mg) 15 Potasium (mg) 382 Magnesium (mg) 24 Vitamin A (IU) 2500 Thiamin (mg) 0.1 Riboflavin mg) 0.23 Niasin (mg) 0.9 Vitamin C (mg) 113
Sumber: Agricultural Handbook No.8, USDA (1963) dalam Salunke, Pao dan Dull (1976)
Rukmana (1994) menyebutkan kualitas brokoli dapat dilihat dari kekompakan bunga (curd density), kehijauannya, cacatnya, serta diameter bunganya. Menurut Susila (2006) pengelompokkan (grading) brokoli dilihat dari ukuran bunganya, yaitu:
- Grade 1 : diameter bunga 30 cm - Grade 2 : diameter bunga 25 - 30 cm - Grade 3 : diameter bunga 20 - 25 cm - Grade 4 : diameter 15 - 20 cm
Brokoli merupakan komoditi yang mudah rusak (perishable) karena memiliki kandungan air yang tinggi (90 %), dan kelas laju respirasi yang terlalu tinggi. Pada suhu 5 oC serta lebih tinggi dibandingkan asparagus, bayam dan jagung manis (Utama, 2001). Potensi masa simpan brokoli kurang dari 2 minggu dalam udara dengan suhu dan RH optimum (Kader, 1993). Oleh karena itu setelah dipanen brokoli harus segera ditangani dengan baik dengan melakukan pra pendinginan untuk menurunkan laju respirasi dan mencegah terjadinya pelayuan
dan pembusukan (Rokhani, 1995). Pra pendinginan dapat dilakukan dengan cara
hydrocooling atau dengan menggunakan es, jika kondisinya baik dan sirkulasi udara pada ruang penyimpanan sesuai maka brokoli dapat bertahan 10 - 14 hari pada suhu 0oC (Rokhani, 1995).
Brokoli memiliki umur simpan yang pendek, yaitu 1 - 2 hari pada kondisi suhu 20 oC, RH 60 – 70%; 2 - 6 hari pada kondisi suhu 4oC, RH 80 – 90 %; 1 - 2 minggu pada kondisi suhu 0 oC, RH 90 – 95 % dan dikemas dalam kotak
polystyrene yang diberi es (Tan, 2005 dalam Bafdal, et al., 2007). Menurut Bafdal, et al., (2007) bahwa jika 15 kg brokoli yang setelah dipanen diberi perlakuan hydrocoolingkemudian dimuat dalam kontainer yang diberi bongkahan es (ice crushed) sebanyak 3 kg dapat menjaga suhu di dalam kontainer 8.5 – 10.3 oC selama 22 jam.
B. Karakteristik Respirasi
Menurut Winarno dan Kartakusuma (1981), respirasi adalah suatu proses metabolisme dengan cara menggunakan oksigen dalam pembakaran senyawa yang lebih kompleks seperti pati, gula, protein, lemak, dan asam organik, sehingga menghasilkan molekul yang sederhana seperti CO2, air serta energi dan molekul lain yang dapat digunakan oleh sel untuk reaksi sintesa.
Energi yang dikeluarkan berupa panas akibat respirasi (dikenal sebagai panas vital atau vital heat) mempengaruhi penerapan teknologi pasca panen, seperti memperkirakan kebutuhan sistem pendingin dan ventilasi (Kader, 1993). Menurut (Hardenburg, Watada dan Wang, 1968), reaksi kimia sederhana untuk proses respirasi dapat dituliskan sebagai berikut:
C6H12O6+ 6O2 6CO2+ 6H2O + 673 kcal
Pada persamaan di atas terlihat bahwa sumber utama penghasil energi adalah glukosa. Besar kecilnya respirasi dapat diukur dengan menentukan substrat yang hilang, O2 yang diserap, CO2 yang dikeluarkan, panas yang dihasilkan, dan energi yang ditimbulkan.
Menurut Phan et al., 1986 dalam Ananta, 1997 laju respirasi buah dan sayuran dipengaruhi oleh faktor luar dan faktor dalam. Faktor dalam yang mempengaruhi respirasi adalah tingkat perkembangan organ tanaman, ukuran produk, lapisan alamiah dan jenis jaringan. Faktor luar yang mempengaruhi adalah suhu, konsentrasi gas O2 dan CO2 yang tersedia, zat-zat pengatur tumbuh dan kerusakan yang ada pada buah dan sayuran.
Laju respirasi brokoli termasuk sangat tinggi (Kader, 1987; Hardenburg, Walada dan Wang, 1968). Semakin cepat laju respirasi maka semakin besar jumlah panas yang dilepaskan per satuan waktu. Laju respirasi besarnya bervariasi tergantung jenis komoditi, akan tetapi terutama dipengaruhi oleh suhu dan komposisi gas di sekitar komoditi tersebut (Kader, 1989; Saltveit, 1989; Manapperuma and Singh, 1987 dalam Rokhani, 1995).
B.1. Pengaruh Suhu
Laju respirasi brokoli dipengaruhi secara nyata oleh suhu penyimpanan, yaitu semakin tinggi suhu penyimpanan, laju respirasinya semakin besar; juga sebaliknya, laju respirasi semakin menurun dengan semakin rendahnya suhu penyimpanan; melalui pengaturan suhu dan kelembaban serta komposisi gas ruang penyimpanan, mutu produk hortikultura yang disimpan dapat dipertahankan (Rokhani, 1995). Laju respirasi brokoli yang digambarkan sebagai laju produksi CO2 (mg/kg jam) pada suhu penyimpanan 0 oC, 4 - 5 oC, 10 oC, 15 - 16 oC, dan 20 - 21 oC adalah berturut-turut (mg/kg jam) 19 - 21, 32 – 37, 75 - 87, 161 – 186, dan 278 – 320 (Hardenburg, Watada dan Wang, 1986). Laju respirasi brokoli juga dipengaruhi oleh ukuran floret (Tian, et al. dalamFinger, et al., 1999) dan jenis kultivarnya (Finger, et al., 1999).
Respirasi membutuhkan O2dan menghasilkan zat sisa metabolisme berupa uap air, CO2, dan panas sebagai entropi (energi panas yang tidak termanfaatkan). Kuosien respirasi (respiratory quotient) merupakan perbandingan CO2 terhadap O2. Kuosien respirasi berguna untuk mendeduksi sifat substrat yang digunakan dalam respirasi sejauh mana respirasi telah berlangsung, sejauh mana reaksi
respirasi telah berlangsung, dan sejauh mana proses itu bersifat aerobik atau anaerobik (Phanet al.,1986).
Tabel 2. Sifat-sifat respirasi berdasarkan tipe substrat yang digunakan Tipe
Substrat Substrat Reaksi Respirasi
RQ (CO2/O2) Karbohidrat Glukosa C6H12 + 6O2 6CO2+ H2O 1.00
Lemak Asam palmitik C16H32O2 + 11O2 C12H22O11+ 4CO2 + 5H2O 0.36 Asam organik Malic acid C4H6O5+ 3O2 4CO2+ 3H2O 1.33 Sumber: Kays (1991)
Phan et al., (1986) menyatakan bila kuosien respirasi sama dengan satu, gulalah yang dioksidasi. Jika nilai kuosien respirasi lebih besar dari satu, menunjukkan bahwa yang digunakan dalam respirasi itu suatu substrat yang mengandung oksigen, yaitu asam-asam organik. Bila kuosien respirasi kurang dari satu, maka ada beberapa kemungkinan, yaitu (a) substrat mempunyai perbandingan oksigen terhadap karbon yang lebih kecil daripada heksosa, (b) oksidasi belum tuntas, misalnya terhenti pada pembentukan asam suksinat atau zat antara lain; (c) CO2 yang dikeluarkan digunakan dalam proses-proses sintesis, misalnya pembentukan asam oksalat dan asam malat dari piruvat.
Suhu menimbulkan efek yang menentukan dalam laju metabolisme produk pasca panen (Kays, 1991 dan Nobel, 1991). Karakter perubahan pada laju reaksi akibat suhu tersebut biasanya ditentukan dengan kuosien suhu (Q10), yaitu rasio laju reaksi tertentu pada suatu tingkat suhu (T1) terhadap laju reaksi tersebut saat suhu naik 10 oC (T1 + 10 oC). Menurut Kays (1991), pada kebanyakan produk, nilai Q10 berkisar antara 2.0 – 2.5 saat suhu 5 oC hingga 25oC. Dengan kata lain, setiap peningkatan suhu 10 oC, maka laju respirasi dapat meningkat 2.0 - 2.5 kali lipat. Namun pada skala suhu 30 - 35 oC nilai Q10 dapat menurun dan laju reaksi
cenderung terhambat dikarenakan denaturasi enzim. Sedangkan suhu buah atau sayuran umumnya lebih tinggi dari ruang penyimpanan akibat panas respirasi. Perbedaan suhu tersebut cukup kritis dalam penentuan laju metabolisme produk.
Penjelasan tentang penurunan Q10 pada suhu yang tinggi adalah bahwa laju penetrasi O2 ke dalam sel lewat kutikula atau periderma mulai menghambat respirasi saat reaksi kimia berlangsung dengan cepat. Difusi O2 dan CO2 juga dipercepat dengan peningkatan suhu, tapi Q10 untuk proses fisika ini hanya 1.1 ; jadi suhu tidak mempercepat secara nyata difusi larutan lewat air. Peningkatan suhu sampai 40 °C atau lebih, laju respirasi malahan menurun, khususnya bila tumbuhan berada pada keadaan ini dalam jangka waktu yang lama. Enzim yang diperlukan mulai mengalami denaturasi dengan cepat pada suhu yang tinggi, mencegah peningkatan metabolik yang semestinya terjadi. Pada kecambah kacang kapri, peningkatan suhu dari 25 menjadi 45 °C mula-mula meningkatkan respirasi dengan cepat, tapi setelah dua jam laju respirasinya mulai berkurang. Kemungkinan penjelasannya ialah jangka waktu dua jam sudah cukup lama untuk merusak sebagian enzim respirasi (Salisbury & Ross, 1995).
B.2. Pengaruh Komposisi Gas
Komposisi gas yang utama dalam mempengaruhi respirasi adalah oksigen, karbondioksida, dan etilen (Kays, 1991). Beberapa penelitian telah menunjukkan bahwa komposisi O2 rendah dan CO2 tinggi akan menghambat laju respirasi. Pantastico et al., 1986 menyatakan bahwa etilen dapat mempercepat proses respirasi dan pembentukannya sekaligus didorong oleh laju respirasi. Dengan mengubah konsentrasi gas O2 menjadi 3 % dari 22 % dan meningkatkan konsentrasi CO2 menjadi 4 % dari keadaan normal, buah dan sayuran tidak mengalami efek kerusakan dan memperlambat proses pematangan selama beberapa hari (Liyod Ryall et al., 1982dalamTubagus, 1993).
Komposisi udara normal terdiri atas oksigen (20.95 %), karbondioksida (0.03 %), dan nitrogen (78.08 %) serta gas-gas lain dengan jumlah yang lebih sedikit. Agar buah-buahan dan sayuran dapat disimpan dalam jangka waktu yang lebih lama maka perlu dilakukan modifikasi komposisi udara di sekitar
komoditas. Penyimpanan dengan atmosfir termodifikasi dapat dilakukan dengan penyimpanan atmosfer terkendali (controlled atmosphere, CA) atau atmosfir modifikasi (modified atmosphere, MA)
Rokhani (1996) mengemukakan bahwa pada sistem CA komposisi gas dalam ruang penyimpanan diukur secara terus menerus dan perlu menginjeksikan gas atau campuran gas tertentu untuk mempertahankan komposisi gas yang diinginkan. Sedangkan sistem MA merupakan sistem statis tanpa melakukan monitoring komposisi gas selama penyimpanan. Komposisi gas pada penyimpanan sistem MA ditentukan dari komposisi gas awal yang terdapat dalam kemasan, laju konsumsi oksigen dan laju produksi karbondioksida oleh komoditas, sifatnya permeabelitas dari kemasan dan suhu penyimpanan.
Komposisi gas yang diinginkan pada sistem CA lebih teliti dibandingkan MA. Dalam praktiknya sistem CA memerlukan gas-gas pengendali seperti oksigen, karbondioksida dan nitrogen serta sejumlah peralatan untuk pengaturan dan pengendalian komposisi gas yang secara praktis diterapkan untuk penyimpanan dalam bentuk curah.
Menurut Wang dan Hruscha (1977) dalam Tubagus (1993) bahwa pada suhu penyimpanan 10 oC dengan modified atmosphere, brokoli yang tidak dikemas dapat bertahan selama 3 hari dan setelah hari ketujuh bahan akan menguning. Selanjutnya brokoli yang dikemas dengan film tertutup dapat dipertahankan mutunya sampai 14 hari. Pada penyimpanan 20 oC brokoli yang tidak dikemas hanya bertahan selama 2 hari dengan kemasan tertutup sampai hari kedua warna dapat dipertahankan tetapi mengalami kerusakan fisik.
Menurut Ballantyne et al., (1988) dalam Tubagus (1993) melaporkan bahwa penyimpanan brokoli dengan sistem modified atmosphere(CO2 tinggi dan O2 rendah) pada suhu 0 dan 5 oC akan mengalami kondisi aerobik dan diikuti dengan pembusukan setelah 4 – 5 hari penyimpanan menggunakan plastik PE, dan 6 – 8 hari dengan menggunakan film PVC. Kondisi optimun untuk penyimpanan brokoli pada suhu 5 oC menggunakan film VA adalah kombinasi dari O22 – 5 % dan CO2 3 – 10 % dimana kondisi ini akan tercapai setelah 2 - 3 hari
penyimpanan. Pada kondisi ini kerusakan dan pembusukan akan tejadi setelah 10 hari penyimpanan.
B.3. Pola Respirasi
Buah-buahan dan sayuran dapat diklasifikasikan berdasarkan pola respirasi selama pematangan sebagi klimakterik dan non klimakterik. Istilah klimakterik dicetuskan oleh Kidd dan West (1925) dalam Pantastico (1986), yang pertama kali menguraikan gejala tersebut pada saat meneliti fisiologi pasca panen apel
Bramley Seedling (diukur dengan produksi CO2) pada suhu 12.2 oC adalah lambat dan konstan pada waktu tertentu, lalu sesudah itu meningkat sampai puncak (klimaks). Oleh karena itu mereka menamakan fenomena tersebut dengan kenaikan klimakterik. Hal ini menyimpulkan bahwa ciri dari proses klimakterik adalah kenaikan produksi CO2yang mendadak.
Menurut Biale (1954) dalam Kays (1991), buah non klimakterik akan bereaksi terhadap pemberian C2H4 pada tingkat manapun dengan kenaikan laju konsumsi O2 yang tergantung pada konsentrasi etilen sedangkan pada buah klimakterik, peningkatan konsentrasi C2H4 hanya akan menggeser pola respirasi secara horizontal. Buah klimakterik mengadakan reaksi respiratik bila C2H4 diberikan dalam keadaan pra klimakterik, dan tidak lagi peka terhadap C2H4 setelah masa kenaikan klimakterik terlampaui.
C. Teknik Pengukuran Laju Respirasi
Dalam proses respirasi beberapa senyawa penting yang dapat digunakan untuk mengukur laju respirasi adalah perubahan kandungan glukosa, jumlah ATP, CO2 yang diproduksi dan O2 yang dikonsumsi. Dari keempat cara tersebut, pengukuran dengan menghitung produksi CO2 lebih sederhana dan lebih praktis. Sedangkan menentukan jumlah O2 yang dikonsumsi dapat dilakukan dengan alat yang mempunyai kepekaan tinggi seperti kromatografi gas karena jumlahnya relatif sedikit (Winarno dan Kartakusuma, 1981).
Untuk pengukuran laju respirasi tersebut diperlukan sampel gas sebagai hasil dari kegiatan respirasi. Sampel gas dapat diperoleh dari gas di dalam
jaringan (internal) atau dari gas yang ditimbulkan oleh jaringan (eksternal). Pengukuran laju respirasi dengan mengambil sampel gas secara internal telah dilakukan oleh Saltveit (1982). Dibandingkan cara internal, pengambilan sampel gas secara eksternal lebih sederhana dan tidak merusak bahan. Terdapat dua metode dalam pengambilan sampel gas secara eksternal, yaitu metode statis atau sistem tertutup (closed system) dan metode dinamis atau sistem terbuka (open system).
Dalam metode sistem tertutup bahan ditempatkan dalam suatu wadah tertutup dimana gas CO2 yang dihasilkan terakumulasi dan gas O2 yang dikonsumsi menjadi berkurang konsentrasinya. Laju respirasi dihitung dengan mengetahui berat bahan, volume bebas wadah, dan perbedaan konsentrasi setelah waktu tertentu (Rokhani, 1996). Mannapperuma dan Singh (1990) menyatakan persamaan laju respirasi sistem tertutup pada suhu tertentu dengan satuan ml/kg-jam seperti pada persamaan (1) dan (2).
R1 (1)
R2 (2)
dimana
R = laju respirasi (ml/kg jam) x = konsentrasi gas (desimal) t = waktu (jam)
V = volume bebas (ml) W = berat produk (kg)
subskrip 1, 2 = masing-masing menyatakan gas O2dan CO2.
Dalam metode sistem terbuka, campuran gas yang diketahui konsentrasinya dialirkan melalui “respiration chamber”. Setelah kondisi kesetimbangan tercapai, produksi CO2 atau konsumsi O2 dihitung dengan mengetahui berat bahan, laju aliran dan perbedaan konsentrasi antara inlet dan
outlet gas pada “respiration chamber”. Mannapperuma dan Singh (1990) menentukan laju respirasi pada sistem terbuka berdasarkan kesetimbangan massa oksigen dan karbondioksida. Sedangkan kesetimbangan massa nitrogen digunakan untuk menghitung laju aliran gas masuk. Persamaan kesetimbangan untuk oksigen, karbondioksida, dan nitrogen ditunjukkan dalam persamaan berikut:
Kesetimbangan O2 : R1 = (Gx1– Qy1) /W (3)
Kesetimbangan CO2 : R2 = (Gx2– Qy2) /W (4)
Kesetimbangan N2 : G = Q(y3/x3) (5)
dimana
R = laju respirasi (ml/kg jam)
G = laju respirasi gas masuk (ml/jam) Q = laju aliran gas keluar (ml/jam) W = berat produk (kg)
x = konsentrasi gas masuk (desimal) y = konsentrasi gas keluar (desimal)
subskrip 1, 2, dan 3 masing-masing menyatakan gas O2, CO2, dan N2.
D. Model Pendugaan
Pengertian model menurut Mayer (1984) adalah suatu objek atau konsep yang digunakan untuk mewakili suatu hal yang menyatakan skala kecil dan mengubahnya kebentuk yang dapat dimengerti. Jadi model merupakan penggambaran suatu objek yang disusun berdasarkan tujuan tertentu. Sedangkan model matematika merupakan suatu model yang memuat konsep-konsep matematika seperti konstanta, variabel, fungsi, persamaan, dan lain-lain. Tujuan dari penyusunan model matematika adalah untuk mengenali perilaku suatu objek dengan cara mencari keterkaitan antara unsur-unsurnya untuk mengadakan
optimalisasi dalam objek dan untuk mengadakan pendugaan atau prediksi untuk memperbaiki keadaan objek. Dari model matematika dapat diperoleh gambaran yang lebih jelas mengenai objek tanpa harus mengganggu keberadaan objek. Pengembangan model matematika merupakan suatu siklus fenomena yang berdasarkan konsep model verbal.
Metode pengkorelasian yang akan digunakan adalah metode regresi linear yaitu:
Linear sederhana : R = a + bT (6)
Eksponensial : R = aebT (7)
Logaritmik : R = aTb (8)
Untuk menyatakan laju respirasi sebagai fungsi suhu dapat digunakan persamaan Arrhenius:
R = Ro e–E/RT (9)
dimana
R = konstanta penurunan konsentrasi Ro= konstanta
E = energi aktivasi T = suhu mutlak (C+273)