Produksi Sediaan Farmasi di Rumah Sakit
Menurut Keputusan Menteri Kesehatan RI No.1197/MENKES/SK/X/2004, kegiatan produksi yang dilakukan oleh Instalasi Farmasi Rumah Sakit (IFRS) merupakan kegiatan membuat, merubah bentuk, dan pengemasan kembali sediaan farmasi steril atau non steril untuk memenuhi kebutuhan pelayanan kesehatan di rumah sakit.
IFRS sebagai organisasi atau lembaga produksi bertugas untuk menyediakan dan menjamin mutu produk yang diproduksinya, termasuk juga produk yang dibeli. IFRS harus berupaya memastikan terapi obat berlangsung secara efektif, aman dan rasional, serta mengadakan pengendalian penggunaan serta system distribusi obat yang tanggap dan akurat bagi seluruh pasien.
Dalam proses produksi, IFRS melakukan kegiatan yang meliputi desain atau pengembangan produk, penetapan spesifikasi produk, penetapan kriteria dan pemilihan pemasok, proses pembelian, proses produksi, pengujian mutu, dan penyiapan produk tersebut bagi pasien. Selain itu, IFRS juga melaksanakan pengemasan kembali obat atau produk obat, untuk kemasan “selama rentang terapi: dan kemasan “dosis unit”.
Kriteria obat yang diproduksi meliputi:
- Sediaan farmasi dengan formula khusus - Sediaan farmasi dengan harga murah
- Sediaan farmasi dengan kemasan yang lebih kecil - Sediaan farmasi yang tidak tersedia di pasaran - Sediaan farmasi untuk penelitian
- Sediaan nutrisi parenteral
- Rekonstruksi sediaan obat kanker
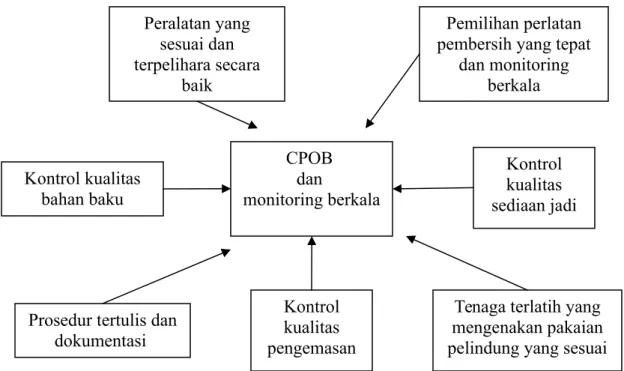
Dalam pelaksanaan seluruh proses produksi, IFRS perlu menerapkan standar system mutu ISO 9001 dan dilengkapi dengan Cara Pembuatan Obat yang Baik.(CPOB).
Gambar 1. Faktor yang berkaitan dengan Cara Pembuatan Obat yang Baik
A. Produksi Steril
Produksi steril adalah penyediaan seluruh obat steril bagi pasien yang bersifat individual. produksi steril terbagi menjadi produksi steril dan aseptic dispensing. Produksi steril adalah proses mencampur atau meracik bahan obat yang steril dan dilakukan di dalam ruangan steril. Aseptic dispensing adalah teknik aseptik yang dapat menjamin ketepatan sediaan steril yang dibuat dan bebas kontaminasi.
Kegiatan produksi obat steril yang dilakukan Sub Instalasi Produksi Farmasi adalah pembuatan nutrisi parenteral, IV admixture atau pencampuran obat-obat suntik, dan rekonstitusi sediaan berbahaya. Tujuan dari produksi steril adalah mendapatkan dosis yang tepat dan aman; 2) menyediakan nutrisi bagi penderita yang tidak dapat menerima makanan, baik secara oral, maupun enteral; 3) menyediakan obat kanker secara efektif, efisien, dan bermutu; dan 4) menurunkan biaya pengobatan.
1. Produksi sediaan nutrisi parenteral CPOB dan monitoring berkala Peralatan yang sesuai dan terpelihara secara baik Pemilihan perlatan pembersih yang tepat
dan monitoring berkala
Kontrol kualitas bahan baku
Prosedur tertulis dan dokumentasi
Kontrol kualitas pengemasan
Tenaga terlatih yang mengenakan pakaian pelindung yang sesuai
Kontrol kualitas sediaan jadi
Nutrisi parenteral adalah nutrisi steril yang diberikan kepada pasien secara intravena. Produksi sediaan nutrisi parenteral merupakan kegiatan pencampuran nutrisi parenteral yang dilakukan oleh tenaga yang terlatih secara aseptis sesuai status nutrisi dan kondisi medis pasien dengan menjaga stabilitas sediaan, formula standar, dan kepatuhan terhadap prosedur yang menyertai.
Kegiatan yang dilakukan dalam produksi sediaan nutrisi parenteral, yaitu:
a. Mencampur sediaan karbohidrat, protein, lipid, vitamin, mineral untuk kebutuhan perorangan
b. Mengemas sediaan ke dalam kantong khusus untuk nutrisi
Faktor-faktor yang perlu diperhatikan dalam produksi sediaan nutrisi parenteral adalah:
a. tim yang terdiri dari dokter, apoteker, perawat, dan ahli gizi untuk memformulasikan nutrisi yang dibutuhkan
b. Produksi dilakukan di ruangan khusus/ Clean room (Lampiran 1, Gambar 6) di dalam kabinet laminar/ Laminar Air Flow Cabinet (Gambar 2)
c. Sediaan dikemas dalam kantong khusus untuk nutrisi parenteral (Gambar 3) 2. Pencampuran obat suntik (IV admixture)
Pencampuran obat suntik yaitu mencampurkan obat steril sesuai kebutuhan pasien yang menjamin kompatibilitas, dan stabilitas obat maupun wadah dan sesuai dengan dosis yang telah ditetapkan.
Kegiatan yang dilakukan dalam pencampuran obat suntik adalah:
a. Pelarutan serbuk steril
b. Menyiapkan suntikan IV sederhana (tunggal) Contoh : memindahkan obat dari vial ke dalam syringe atau kantong infus.
c. Menyiapkan suntikan IV kompleks
Contoh : memindahkan obat yang sama dari beberapa vial ke dalam wadah akhir steril.
d. Mengemas menjadi sediaan siap pakai
Contoh : pencampuran komponen nutrisi parenteral
Proses pencampuran obat suntik harus memenuhi syarat sebagai berikut: a. Ruangan produksi merupakan ruangan ISO Class 7 (Tabel 1)
b. Proses produksi dilakukan di meja kerja kabinet laminar (laminar airflow workbench / LAFW) dengan klasifikasi ISO Class 5
c. Ruangan produksi memiliki tekanan positif dilengkapi dengan HEPA filter (Gambar 4)
d. Akses terbatas
3. Rekonstitusi sediaan farmasi berbahaya
Produksi sediaan farmasi berbahaya merupakan penanganan obat kanker secara aseptis dalam kemasan siap pakai oleh pasien yang dilakukan oleh tenaga farmasi yang terlatih dengan pengendalian keamanan terhadap lingkungan, petugas, maupun sediaan obatnya dari efek toksik dan kontaminasi, dengan menggunakan alat pelindung diri pada saat pencampuran, distribusi, maupun proses pemberian kepada pasien sampai pembuangan limbahnya. Sediaan yang termasuk dalam sediaan farmasi berbahaya adalah obat-obat kanker, seperti agen neoplastik, sitostatika; dan radiofarmaka.
Kegiatan yang dilakukan dalam rekonstitusi sediaan farmasi berbahaya adalah:
a. Melakukan perhitungan dosis secara akurat
b. Melarutkan sediaan obat kanker dengan pelarut yang sesuai
c. Mencampur sediaan obat kanker sesuai dengan protokol pengobatan d. Mengemas dalam kemasan tertentu
e. Membuang limbah sesuai prosedur yang berlaku
Hal-hal yang perlu diperhatikan pada proses rekonstitusi sediaan farmasi berbahaya:
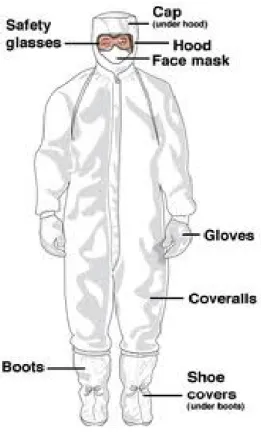
a. Operator harus mengenakan sarung tangan kemoterapi dan pakaian yang sesuai selama penerimaan, distribusi, penyimpanan, investarisasi, persiapan untuk administrasi, dan pembuangan limbah (Gambar 5).
b. Ruangan produksi dan penyimpanan harus bertekanan negatif dan buffer area ISO Class 7 atau lebih. Ruang penyimpanan terpisah dengan ruang produksi dan area lain.
c. Produksi dilakukan dalam LAC dengan klasifikasi ISO Class 5 atau Compounding Aseptic Containment Isolator (CACI).
B. Produksi Non Steril
Sub instalasi produksi farmasi mebuat perencanaan produksi obat-obat yang dibutuhkan selama satu bulan dan mencatat realisasi kerjanya, perencanaan produksi dibuat untuk bulan berikutnya berdasarkan permintaan barang dari sub instalasi apotek pegawai distribusi farmasi dan persediaan minimum produksi, selanjutnya dilaksanakan dalam kegiatan harian. Kegiatan yang dilakukan dalam produksi non steril yaitu pembuatan, pengenceran, dan pengemasan kembali. a. Pembuatan
Sub instalasi produksi farmasi memproduksi obat non steril berdasarkan master formula. Produksi obat dilakukan dengan mengisi formulir pembuatan obat. Tahapan pembuatan obat dilakukan berdasarkan urutan seperti contoh yang terdapat pada formulir pembuatan obat dan pada setiap tahap pembuatan harus diparaf oleh petugas yang mengerjakannya. Formulir pembuatan obat dibuat berdasarkan per item obat. Pengemasan dan pemberian etiket dilakukan setelah produksi obat atau pengenceran antiseptik selesai dibuat dan diperiksa kembali. Setelah selesai pengemasan, maka operator harus mengisi lembaran atau formulir pengemasan yang berisi tanggal produksi, nama obat, nomor produksi, volum dan kemasan, kemudian diparaf. Selanjutnya formulir pembuatan obat, formulir pengemasan dan etiket diparaf atau diberi cap oleh penanggung jawab sebagai tanda bahwa obat sudah diperiksa dan dapat didistribusikan.
b. Pengenceran
Pengenceran dilakukan berdasarkan urutan seperti yang terdapat pada formulir obat dan pada setiap tahap harus diparaf oleh petugas yang mengerjakannya. Pengenceran misalnya pembuatan alkohol 70% dari alkohol 95%.
c. Pengemasan kembali
Pengemasan kembali misalnya Betadine® dan Rivanol dari kemasan besar menjadi kemasan yang lebih kecil.
Penyimpanan hasil produksi dipisahkan antara obat dalam dan obat luar yang masing-masing disusun secara alfabet. Obat yang lebih dulu dikeluarkan adalah obat yang lebih dulu diproduksi dengan mempertimbangkan waktu kadaluarsanya. Setiap pengeluaran obat dicatat dalam kartu sediaan.
Instalasi produksi farmasi melayani kebutuhan barang dari sub instalasi distribusi, apotek pegawai dan apotek korpri. Pengiriman barang dilakukan setiap minggu. Sub instalasi produksi farmasi juga melayani permintaan untuk pembuatan formula khusus yang berasal dari resep dokter dan tidak ada dalam rencana produksi.
Laporan-laporan yang dibuat adalah laporan pemasukan dan pengeluaran bahan baku yang dibuat setiap bulan; laporan pembuatan dan pengeluaran produk jadi non steril, serta laporan pelayanan sitostatika. Obta-obat yang diproduksi di instalasi produksi farmasi adalah obat-obat yang lebih murah jika diproduksi sendiri dan obat yang tidak terdapat di pasaran atau merupakan formula khusus.
DAFTAR PUSTAKA
American Society of Health-System Pharmacists. Baxter. (2008). The ASHP Discussion Guide on USP Chapter <797> for Compounding Sterile Preparations. 8 September 2010. http://www.ashp.org/s_ashp/docs/files/DiscGuide797-2008.pdf.
Direktorat Jenderal Pelayanan Kefarmasian dan alat Kesehatan. (2004). Standar Pelayanan di Rumah Sakit: Keputusan Menteri Kesehatan Republik Indonesia No.1197/MENKES/SK/X/2004. Jakarta: Departemen Kesehatan RI.
Roger McFadden. (n.d.). Basic Introduction to Clean Rooms. Coastwide Laboratories, Staples. 8 September 2010.
http://www.coastwidelabs.com/Technical%20Articles/Cleaning%20the %20Cleanroom.htm.
Siregar,Charles J.P. (2004). Farmasi Rumah Sakit : Teori dan Penerapan. Jakarta: Penerbit Buku Kedokteran AGC. hal. 347-348
Stone, Patricia. Curtis, Stephen J. (1995). Pharmacy Practice (second edition). London: Farrand Press. hal. 132-139.
(n.d.). Amiparen. 8 September 2010.
http://www.otsuka.co.id/?content=product_detail&id=30&lang=id
(n.d.) Cleanroom Garments. Cole-Parmer Technical Library. 8 September 2010. http://www.coleparmer.com/techinfo/techinfo.asp?
htmlfile=CleanroomGarments.htm&ID=63.
(n.d.) Welcome to SRPREFABS Cleaning room equipments. 8 September 2010. http://www.srprefabs.com/biolo.html
(n.d.). 8 September 2010 http://www.answers.com/topic/hepa
Gambar 2. Vertical Laminar Air Flow Cabinet (kiri) dan prinsip kerjanya (kanan)
Gambar 3. Kemasan sediaan nutrisi parenteral
A. front opening B. sash
C. exhaust HEPA D. exhaust plenum
Gambar 4. HEPA Filter
LAMPIRAN
Lampiran 1. Ruangan khusus produksi sediaan steril (cleanroom)
Cleanroom merupakan tempat atau ruangan produksi produk yang terkendali. Konsentrasi partikel di udara di ruangan ini diatur dalam batas tertentu. Hal ini bertujuan untuk mengurangi kontaminasi yang dapat diakibatkan oleh faktor manusia, proses, fasilitas, dan peralatan. Kontaminasi di ruangan ini juga dikendalikan dengan melakukan pengawasan terhadap suhu, kelembaban, dan tekanan. Dalam ruang khusus produksi sediaan steril terdapat beberapa sarana antara lain termometer ruangan, barometer, pengatur kecepatan aliran udara, dan penghitung jumlah partikel.
Cleanroom didesain untuk mendapatkan dan mempertahankan aliran udara secara paralel dan kecepatannya seragam di dalam area yang terbatas (aliran laminar). Hal ini dilakukan untuk mengurangi turbulensi udara yang dapat mengakibatkan perpindahan partikel. Denah dari cleanroom dapat dilihat pada gambar di bawah ini
Cleanroom dibagi menjadi beberapa kelas berdasarkan ISO 14644-1. Pembagian ini didasarkan pada banyak jumlah partikel di udara yang berada di dalam ruangan tersebut.
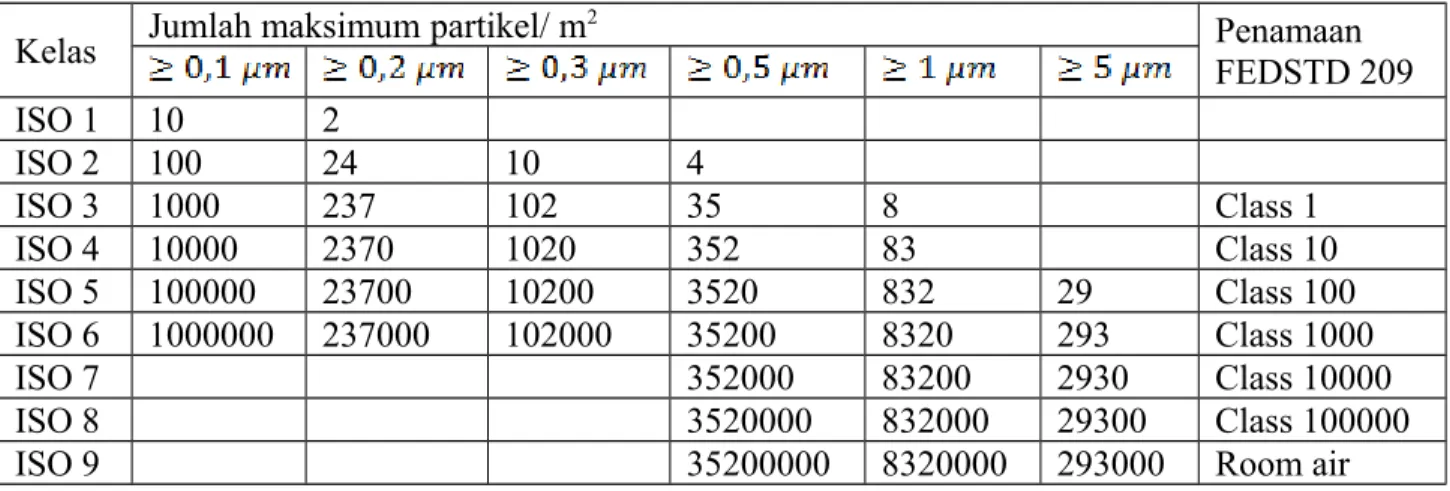
Tabel 1. Klasifikasi dan persyaratan cleanroom menurut ISO 14644-1
Kelas Jumlah maksimum partikel/ m 2 Penamaan FEDSTD 209 ISO 1 10 2 ISO 2 100 24 10 4 ISO 3 1000 237 102 35 8 Class 1 ISO 4 10000 2370 1020 352 83 Class 10 ISO 5 100000 23700 10200 3520 832 29 Class 100 ISO 6 1000000 237000 102000 35200 8320 293 Class 1000 ISO 7 352000 83200 2930 Class 10000 ISO 8 3520000 832000 29300 Class 100000
ISO 9 35200000 8320000 293000 Room air
Cleanroom dilengkapi dengan filter yang disebut High Efficiency Particulate Air Filter (HEPA). Filter ini menyaring partikel dengan ukuran 0,3 µm dengan efisiensi 99,97%.