perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user i
PENGARUH VARIASI RASIO PELARUT DAN WAKTU PERENDAMAN TERHADAP KADAR KURKUMINOID, TOTAL FENOL, DAN AKTIVITAS
ANTIOKSIDAN PADA OLEORESIN RIMPANG TEMULAWAK (Curcuma xanthorrhiza Roxb.) DENGAN PENGERINGAN CABINET DRYER
Skripsi
Oleh : HISYAM NASSER
H 0607015
FAKULTAS PERTANIAN UNIVERSITAS SEBELAS MARET
SURAKARTA 2011
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user ii
PENGARUH VARIASI RASIO PELARUT DAN WAKTU PERENDAMAN TERHADAP KADAR KURKUMINOID, TOTAL FENOL, DAN AKTIVITAS
ANTIOKSIDAN PADA OLEORESIN RIMPANG TEMULAWAK (Curcuma xanthorrhiza Roxb.) DENGAN PENGERINGAN CABINET DRYER
Skripsi
Untuk memenuhi sebagian persyaratan
guna memperoleh derajat Sarjana Teknologi Pertanian di Fakultas Pertanian
Universitas Sebelas Maret
Jurusan/Program Studi Teknologi Hasil Pertanian
Oleh : HISYAM NASSER
H 0607015
FAKULTAS PERTANIAN
UNIVERSITAS SEBELAS MARET
SURAKARTA
2011
perpustakaan.uns.ac.id digilib.uns.ac.id
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user iv KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT yang telah memberikan rahmat dan hidayah-Nya, sehingga penulis dapat menyelasaikan skripsi dengan judul “Pengaruh Variasi Rasio Pelarut dan Waktu Perendaman Terhadap Kadar
Kurkuminoid, Total Fenol, dan Aktivitas Antioksidan Oleoresin Rimpang Temulawak (Curcuma xanthorrhiza Roxb.) Dengan Teknik Pengeringan Cabinet Dryer”.
Penulisan skripsi ini merupakan salah satu syarat yang harus dipenuhi oleh mahasiswa untuk mencapai gelar Sarjana Stratum Satu (S-1) pada program studi Teknologi Hasil Pertanian, Fakultas Pertanian, Universitas Sebelas Maret Surakarta.
Penyusunan skripsi ini tidak terlepas dari bantuan berbagai pihak, untuk itu penulis mengucapkan terima kasih kepada :
1. Kedua orang tua saya Ayahanda Suratmo dan Ibunda Nur Umamah yang telah menunjuki ananda jalan hidup yang terbaik. Terimakasih karena “Hisyam Nasser” benar-benar menjadi “nama dan sekaligus pesan” dari “mama dan papa” yang luar biasa buat ananda dalam menjalani hidup ini. Kalian adalah motivator yang luar biasa, lebih dari siapapun. Terimakasih atas segalanya serta kasih sayang tanpa syarat dan tanpa batas yang Papa Mama berikan.
2. Teruntuk Adik-adikku yang luar biasa yang Kakak banggakan “Darojatun Aliyah, Fadhil Akbar Albani, dan Ibnu Hakim Arrozi” yang selalu membersamai dalam kehidupan ini. Kalian juga adalah motivator yang luar biasa dan Kakak akan slalu menjadi Kakak yang terbaik buat kalian.
3. Bapak Prof. Dr. Ir. Bambang Pujiasmanto, MS selaku Dekan Fakultas Pertanian Universitas Sebelas Maret Surakarta.
4. Bapak Ir. Kawiji, MP selaku Pembimbing Utama dan Penguji Skripsi ini, terima kasih atas segala ilmu dan masukan yang luar biasa, semoga menjadi ilmu yang bermanfaat dan berkah.
5. Bapak Edhi Nurhartadi, S.TP, MP selaku Pembimbing Pendamping dan Penguji Skripsi yang juga telah banyak membantu saya menyelesaikan skripsi ini dan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user v
memberikan ilmu kapada saya, juga inspirasi serta perhatian yang luar biasa sehingga skripsi ini dapat terselesaikan dengan baik.
6. Bapak Dimas Rahadian, S.TP., M.Sc. selaku Dosen Penguji Skripsi yang telah cermat dalam memperbaiki skripsi saya dan banyak memberikan manfaat dalam perbaikan skripsi saya sehingga skripsi ini bisa diselesaikan dengan baik.
7. Ibu Sri Liswardani, STP, Pak Slamet, Pak Giyo, Pak Joko, terima kasih banyak atas segala bantuannya mulai dari penelitian, seminar, ujian skripsi, hingga proses menjadi sarjana. Semoga Allah mengganti semua amal kebaikan selama ini. 8. Bapak dan Ibu Dosen Teknologi Hasil Pertanian Universitas Sebelas Maret
Surakarta atas segala dedikasinya dalam mengajar dan ilmu yang luar biasa. 9. Nurasri Retno Nugranti, anugerah dan warna dalam hidupku yang sudah banyak
membantu saya hampir di semua lini kehidupan saya. Terimakasih atas segalanya, juga Do’a serta perhatianmu yang sangat luar biasa sehingga saya bisa menjalani kehidupan ini dengan lebih baik.
10. Teruntuk Gandhi Ariel Efendi yang telah banyak membantu dan membersamai saya dalam berjuang menyelesaikan penelitian ini, dan juga teman- teman seperjuangan di Fakultas pertanian Khususnya Vortex (THP 07) semoga persahabatan kita senantiasa terjalin hingga tua kelak dimana pun kita berada serta menjadi kebanggaan buat keluarga, bangsa, dan juga semua orang.
11. Teruntuk organisasi BEM FP, FUSI, dan BSO Himaghita yang telah menunjukkan kepada saya indahnya perjuangan dan kebersamaan.
12. Dan semua pihak yang telah membantu kelancaran penyusunan skripsi ini dan memberi dukungan, doa serta semangat bagi penulis untuk terus berjuang.
Terima kasih banyak saya ucapkan, semoga skripsi ini bermanfaat bagi penulis khususnya dan bagi pembaca pada umumnya.
Surakarta, Januari 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user vi DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv DAFTAR ISI ... vi DAFTAR TABEL ... ix DAFTAR GAMBAR ... x DAFTAR LAMPIRAN ... xi RINGKASAN ... xii SUMMARY... ... xiii BAB I PENDAHULUAN ... 1 A. Latar Belakang ... 1 B. Perumusan Masalah ... 3 C. Tujuan Penelitian ... 3 D. Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 5
A. Temulawak... ... . 5 B. Rimpang Temulawak... 6 C. Kurkuminoid... 8 D. Antioksidan... 11 E. Senyawa Fenol... 13 F. Pengeringan ... 14 G. Ekstraksi... ... 16 H. Oleoresin... 17 I. Kerangka Berpikir ... 18 J. Hipotesis... 18
BAB III METODE PENELITIAN ... 19
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user vii
B. Bahan dan Alat ... 19
1. Bahan ... 19
2. Alat ... 19
C. Tahapan Penelitian ... 20
1. Penyiapan Bahan dan Perajangan . ... 20
2. Pengeringan... 20
3. Penepungan dan Pengayakan... 21
4. Ekstraksi dengan Variasi Waktu Perendaman... ... 21
5. Ekstraksi Dengan Variasi Rasio Pelarut ... 21
6. Penyaringan ... 22
7. Evaporasi... ... 22
8. Analisis Senyawa Aktif Oleoresin Temulawak... 22
D. Rancangan Penelitian... 24
BAB IV HASIL DAN PEMBAHASAN ... 25
A. Kadar Air... 25
B. Kadar Kurkuminoid... 26
1. Pengaruh Variasi Rasio Pelarut terhadap Kadar Kurkuminoid Oleoresin Temulawak ... 26
2. Pengaruh Waktu Perendaman terhadap Kadar Kurkuminoid Oleoresin Temulawak ... 27
3. Pengaruh Interaksi Variasi Rasio Pelarut dan Waktu Perendaman terhadap Kadar Kurkuminoid Oleoresin Temulawak ... 28
C. Total Fenol... .. 30
1. Pengaruh Variasi Rasio Pelarut terhadap Kadar Total Fenol Oleoresin Temulawak ... 30
2. Pengaruh Waktu Perendaman terhadap Kadar Total Fenol Oleoresin Temulawak ... 31
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user viii
3. Pengaruh Interaksi Variasi Rasio Pelarut dan Waktu Perendaman terhadap Kadar Total Fenol Oleoresin Temulawak . 32
D. Aktivitas Antioksidan... 34
1. Pengaruh Variasi Rasio Pelarut terhadap Aktivitas Antioksidan Oleoresin Temulawak ... 34
2. Pengaruh Waktu Perendaman terhadap Aktivitas Antioksidan Oleoresin Temulawak ... 36
3. Pengaruh Interaksi Variasi Rasio Pelarut dan Waktu perendaman Terhadap Aktivitas Antioksidan Oleoresin Temulawak ... 37
BAB V. KESIMPULAN DAN SARAN ... 41
A. Kesimpulan ... 41
B. Saran... 41
DAFTAR PUSTAKA ... 43
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user ix DAFTAR TABEL
Tabel 2.1 Kadar Komponen Senyawa Pada Simplisia Temulawak ... 8
Tabel 2.2 Karakteristik Mutu Simplisia Temulawak ... 8
Tabel 3.1 Metode Analisis Senyawa Aktif Oleoresin Temulawak ... 22
Tabel 3.2 Rancangan Percobaan Acak Lengkap Dengan Dua Faktor ... 24
Tabel 4.1 Hasil Analisis Kadar Air Simplisia Bubuk Temulawak ... 25
Tabel 4.2 Hasil Analisis Kadar Kurkuminoid Oleoresin Temulawak ... 26
Tabel 4.3 Hasil Analisis Kadar Kurkuminoid Oleoresin Temulawak ... 27
Tabel 4.4 Hasil Analisis Kadar Kurkuminoid Oleoresin Temulawak ... 28
Tabel 4.5 Hasil Analisis Kadar Total Fenol Oleoresin Temulawak ... 30
Tabel 4. 6 Hasil Analisis Kadar Total Fenol Oleoresin Temulawak ... 31
Tabel 4.7 Hasil Analisis Kadar Total Fenol Oleoresin Temulawak ... 33
Tabel 4.8 Hasil Analisis Aktivitas Antioksidan Oleoresin Temulawak ... 34
Tabel 4.9 Hasil Analisis Aktivitas Antioksidan Oleoresin Temulawak ... 36
Tabel 4.10 Hasil Analisis Aktivitas Antioksidan Oleoresin Temulawak ... 37
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user x DAFTAR GAMBAR
Gambar 2.1 Rimpang Temulawak... 8
Gambar 2.2 Rumus Bangun Kurkuminoid ... 10
Gambar 2.3 Rumus Bangun Kurkumin... 11
Gambar 3.1 Diagram Alir Pengujian Kadar Air Simplisia Temulawak ... 21
Gambar 3.2 Diagram Alir Penelitian ... 23
Gambar 4.1 Kadar Kurkuminoid ... 29
Gambar 4.2 Kadar Total Fenol ... 33
Gambar 4.2 Reaksi Radikal DPPD dengan Antioksidan ... 38
Gambar 4.3 Rasio Aktivitas Antioksidan antara Sampel dengan Asam Askorbat ... 39
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user xi DAFTAR LAMPIRAN
1. Metode Analisis ... 48 2. Hasil Analisis Kadar Air ... 49 3. Hasil Analisis Kimia Pengaruh Variasi Lama Perendaman dan Ukuran
Partikel ... 50 4. Hasil Analisis SPSS Pengaruh Variasi Ukuran Partikel dan Lama
Perendaman ... 57 5. Dokumentasi ... 66
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user xii
PENGARUH VARIASI RASIO PELARUT DAN WAKTU PERENDAMAN TERHADAP KADAR KURKUMINOID, TOTAL FENOL, DAN AKTIVITAS
ANTIOKSIDAN PADA OLEORESIN RIMPANG TEMULAWAK (Curcuma xanthorrhiza Roxb.) DENGAN PENGERINGAN
CABINET DRYER
HISYAM NASSER H0607015 RINGKASAN
Temulawak mengandung oleoresin yang sangat bermanfaat dalam industri farmasi dan makanan. Mengingat kualitas oleoresin yang ada di pasaran masih rendah, maka perlu adanya penelitian metode ekstraksi yang efisien dan efektif untuk menghasilkan oleoresin yang berkualitas tinggi. Dengan dilakukan penelitian ini diharapkan dapat diketahui teknik yang tepat dalam ekstraksi oleoresin temulawak.
Tujuan penelitian ini adalah untuk mengetahui pengaruh variasi rasio pelarut dan waktu perendaman terhadap mutu oleoresin temulawak. Mutu oleoresin rimpang temulawak ditentukan berdasarkan kadar kurkuminoid, total fenol, dan aktivitas antioksidan pada oleoresin rimpang temulawak yang dihasilkan. Ekstraksi dilakukan dengan metode maserasi dengan pelarut etanol 96%. Oleoresin temulawak dibuat dengan mengekstrak bubuk temulawak dengan metode maserasi yang kemudian dilakukan pemisahan bahan dan pelarut dengan menggunakan Rotary Vacuum
Evaporator.
Penelitian didesain dan dianalisis menggunakan Rancangan Acak Lengkap (RAL) dua faktor dengan tiga kali pengulangan. Variabel yang digunakan antara lain rasio Pelarut: 1:3, 1:5, 1:7 (b/v) dan waktu perendaman: 18, 24, 30 jam.
Hasil penelitian menunjukkan bahwa semakin besar rasio pelarut dan semakin lama waktu perendaman maka semakin besar kadar kurkuminoid, total fenol, dan aktivitas antioksidan yang dihasilkan. Kombinasi perlakuan 1:7 (b/v) 30 jam merupakan proses ekstraksi yang paling efektif dalam menghasilkan senyawa aktif temulawak dibanding dengan kombinasi perlakuan yang lain. Kadar kurkuminoid yang diperoleh sebesar 5,670 mg/100 ml, total fenol 7,080mg/100 ml, dan aktivitas antioksidan 63,149%.
Kata kunci : Oleoresin temulawak, aktivitas antioksidan, kurkuminoid, total fenol, rasio pelarut, waktu perendaman, cabinet dryer
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user xiii
THE EFFECT VARIATION OF RATIO OF SOLVENT AND TIME OF IMMERSION ON CURCUMINOID CONTENT, TOTAL PHENOL AND ACTIVITY OF ANTIOXIDANT OF CURCUMA OLEORESIN (Curcuma xanthorriza Roxb.) WITH
CABINET DRYER DRYING HISYAM NASSER
H0607015 SUMMARY
Curcuma contains oleoresin, which are very useful in pharmaceutical and food industries. Consider that quality of oleoresin sold in the market is still very low, so an experiment of extraction method to produce high oleoresin with efficiency and effectively is therefore necessary. It is expected that the results of this experiment may suggest the appropriate techniques of curcuma oleoresin extraction.
The aims of this experiment is to find out the influence variation of ratio of solvent and time of immersion to quality of curcuma oleoresin. The quality of curcuma oleoresin was determinated by curcuminoid content, total fenol, and antioxidant activity in curcuma oleoresin that produced. Extraction was carried out with maserasi method and using etanol 96% solvent. Curcuma oleorosin is made with extract the powder of curcuma uses a maceration method which is then carried out the separation of materials and solvent by using a Rotary Vacuum Evaporator.
Experiment was designed and analysed using Completely Random Design two factors with three repeatation. Observed variables were; ratio of solvent: 1:3, 1:5, 1:7 (w/v) and time of immersion: 18, 24, 30 hours.
The results showed that more increase ratio of solvent and longer time of immersion result in the increase activity of curcuminoid content, total fenol, and antioxidant activity that produced. Combination of threatment 1:7 (w/v) 30 hours is the most effective extraction process to produce active compounds of curcuma than other threatments. Curcuminoid content that obtained is 5.670 mg/100 ml, total phenol is 7.080 mg/100 ml, and Activity of antioxidant is 63.149%.
Keywords: curcuma oleoresin, antioxidant activity, curcuminoid, total phenols, ratio of solvent, length of immersion, cabinet dryer
perpustakaan.uns.ac.id digilib.uns.ac.id commit to user 1 BAB I PENDAHULUAN A. Latar Belakang
Temulawak (Curcuma xanthorriza Roxb.), termasuk salah satu tanaman rempah dan obat asli habitat Indonesia. Temulawak banyak dimanfaatkan sebagai ramuan jamu karena berkhasiat menyejukkan, meredakan rasa lelah, merangsang semangat, menghangatkan badan, mengatasi gangguan fungsi hati, hepatitis, menurunkan kadar kolestrol, mengaktifkan enzim pemecah lemak di dalam hati, mengobati gangguan pencernaan, radang sendi, bercak-bercak kulit, demam dan masuk angin. Manfaat utama temulawak yaitu sebagai bahan obat tradisional, bahan baku industri jamu dan kosmetik, bahan bumbu masak dan peternakan. Disamping itu rimpang temulawak juga bermanfaat sebagai antioksidan, antiinflamasi, antimikroba, pencegah kanker, antitumor, dan menurunkan kadar lemak darah.
Salah satu senyawa berkhasiat pada rimpang temulawak adalah kurkumin. Kurkumin mempunyai aktivitas antioksidan karena mempunyai gugus penting dalam proses antioksidan tersebut. Struktur kurkumin terdiri dari gugus hidroksi fenolik dan gugus β-diketon. Gugus hidroksi fenolik berfungsi sebagai penangkap radikal bebas pada fase pertama mekanisme anti oksidatif dan gugus β-diketon berfungsi sebagai penangkap radikal pada fase berikutnya. Bersama turunannya, desmetoksi kurkumin dan bis-desmetoksi kurkumin, bertanggung jawab terhadap efek antioksidan dari turmerik (Supriadi, 2008).
Rimpang temulawak mengandung oleoresin yang banyak dimanfaatkan dalam industri farmasi dan makanan. Meningkatnya kebutuhan oleoresin ini merupakan salah satu peluang untuk meningkatkan nilai ekonomi temulawak yaitu dengan mengambil ekstrak oleoresin temulawak. Selain itu dengan teknologi ini diharapkan komoditas temulawak yang banyak dihasilkan di Indonesia dapat termanfaatkan secara optimal. Oleoresin ini didapatkan dengan mengekstrak rimpang temulawak dengan menggunakan pelarut organik
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
2
kemudian dilakukan proses evaporasi. Oleoresin merupakan campuran minyak dan resin atau gum yang dihasilkan melalui ekstraksi menggunakan pelarut organik dari berbagai jenis rempah baik yang berasal dari buah, biji, daun, kulit maupun rimpang. Oleoresin biasanya berbentuk cairan kental, pasta atau semi padat, yang memiliki aroma dan rasa sesuai dengan bahan yang diekstrak.
Proses pembuatan oleoresin temulawak yang panjang, mulai dari pemanenan sampai menjadi ekstrak yang pekat sangat memungkinkan terjadinya degradasi senyawa aktif yang dikandung. Kurkuminoid dan aktivitas antioksidan lainnya pada temulawak sangat mudah mengalami penurunan. Penurunan senyawa tersebut dikarenakan berbagai faktor seperti cahaya, panas, oksigen, dan peroksidase.
Kandungan senyawa aktif pada temulawak khususnya kurkuminoid dan antioksidan merupakan senyawa yang penting dalam temulawak karena sifatnya sebagai antioksidan yang dapat meniadakan radikal-radikal bebas dan menghambat terbentuknya oksidasi lipida sehingga dapat mencegah penyakit degeneratif yang disebabkan oleh radikal-radikal bebas tersebut. Senyawa aktif tersebut rentan mengalami kerusakan dikarenakan adanya cahaya, panas, oksigen, dan peroksidase. Untuk itu perlu dilakukan proses penanganan yang baik agar dapat meminimalkan terjadinya penurunan terhadap senyawa aktif tersebut sehingga khasiat yang begitu banyak dari oleoresin dapat dimanfaatkan secara optimal.
Tujuan dari penelitian ini adalah untuk mengetahui pengaruh rasio pelarut dan waktu perendaman yang digunakan dengan ekstraksi maserasi dalam menghasilkan kadar kurkumin, total fenol, dan aktivitas antioksidan. Diharapkan dari penelitian ini dapat diperoleh kombinasi perlakuan yang optimal utuk menghasilkan oleoresin temulawak yang berkualitas.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
3
B. Perumusan Masalah
Dari latar belakang di atas, dapat diambil rumusan masalah sebagai berikut :
1. Bagaimana pengaruh rasio pelarut yang digunakan pada proses ekstraksi terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak?
2. Bagaimana pengaruh waktu perendaman pada proses ekstraksi terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak?
3. Bagaimana pengaruh interaksi rasio pelarut yang digunakan dan waktu perendaman pada proses ekstraksi terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan rimpang temulawak?
C. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengetahui pengaruh variasi rasio pelarut yang digunakan terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak.
2. Mengetahui pengaruh variasi waktu perendaman terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak.
3. Mengetahui pengaruh interaksi variasi rasio pelarut dan waktu perendaman yang digunakan terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak.
D. Manfaat Penelitian
Manfaat dari penelitian ini adalah:
1. Diharapkan dengan adanya penelitian ini dapat memberikan informasi tentang teknik ekstraksi dengan variasi rasio pelarut dan waktu perendaman yang digunakan yang paling efektif dan efisien terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
4
2. Diharapkan dengan adanya penelitian ini dapat memberikan informasi tentang besarnya kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak sehingga dapat menjadi acuan bagi penelitian berikutnya untuk dapat mengembangkan produk olahan oleoresin temulawak.
perpustakaan.uns.ac.id digilib.uns.ac.id commit to user 5 BAB II TINJAUAN PUSTAKA A. Temulawak
Temulawak (Curcuma xanthorrhiza Roxb.) adalah tanaman yang tumbuh berumpun. Curcuma berasal dari kata Arab : kurkum berarti kuning. Xanthorrhiza dari kata Yunani : xanthos berarti kuning dan rhiza berarti umbi akar. Jadi temulawak artinya adalah akar kuning (Anonima,2005).
Temulawak (Curcuma xanthorrhiza Roxb.) berdasarkan susunan klasifikasi sistematika tumbuhan diklasifikasikan sebagai berikut :
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Monocotyledonae
Bangsa : Zingiberales
Suku : Zingiberaceae
Marga : Curcuma
Spesies : Curcuma xanthorrhiza Roxb (Supriadi, 2008). Produksi rimpang dipengaruhi oleh tempat tumbuh. Pada dataran rendah produksi rimpang segar lebih besar daripada dataran tinggi. Produk rimpang tinggi dengan ukuran lebih besar sebaiknya temulawak ditanam di tempat yang terlindung. Tanaman temulawak masih dapat tumbuh dengan baik pada tempat yang terbuka (Supriadi, 2008).
Temulawak merupakan tumbuhan tahunan yang tumbuh tegak dengan tinggi hingga lebih dari 1 m tetapi kurang dari 2 m, berwarna hijau atau coklat gelap. Akar rimpang terbentuk dengan sempurna dan bercabang kuat, berwarna hijau gelap. Tiap batang mempunyai daun 2-9 helai dengan bentuk daun bundar memanjang sampai bangun lanset, warna daun hijau atau coklat keunguan terang sampai gelap, panjang daun 31-84 cm dan lebar 10-18 cm, panjang tangkai daun termasuk helaian 43-80 cm (Fatmawati, 2008).
Temulawak sebagai tanaman monokotil tidak memiliki akar tunggang. Akar yang dipunyai adalah rimpang. Rimpang adalah bagian
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
6
batang di bawah tanah. Rimpang disebut juga umbi akar, umbi batang, atau umbi tinggal. Rimpang temulawak berukuran paling besar di antara semua rimpang genus Curcuma dengan diameter sampai 6 cm. Rimpang temulawak terdiri atas rimpang utama (induk) dan rimpang anakan (cabang). Rimpang induknya berbentuk bulat seperti telur dan berwarna kuning tua atau coklat kemerahan. Bagian dalamnya berwarna jingga kecoklatan (Fatmawati, 2008).
Rimpang induk akan mengeluarkan rimpang kedua yang lebih kecil. Arah pertumbuhannya ke samping, berwarna lebih muda dengan bentuk yang bermacam-macam, jumlahnya sekitar 3-7 buah. Jika dibiarkan tumbuh lebih dari satu tahun, akan tumbuh banyak rimpang lagi. Rimpang ini aromanya tajam dan rasanya pahit agak pedas. Produk yang diambil dari tanaman tersebut adalah rimpang induk yang tumbuh dekat permukaan tanah dengan kedalaman 5-8 cm (Fatmawati, 2008).
Pemanenan dilakukan dengan cara membongkar rimpang dengan menggunakan garpu atau cangkul. Tanda tibanya panen adalah jika bagian-bagian tumbuhan yang ada di atas tanah sudah mulai mengering dan mati. Umur panen biasanya di atas 9 bulan. Pemanenan temulawak yang baik dilakukan berdasarkan umur tanaman untuk mendapatkan produktivitas yang tinggi yaitu pada umur 10-12 bulan setelah tanam dan biasanya daun mulai luruh atau mengering (Fatmawati, 2008).
B. Rimpang Temulawak
Khasiat temulawak terutama disebabkan oleh dua kelompok kandungan kimia utamanya yaitu kurkuminoid dan minyak atsiri kurkuminoid yang terdapat pada rimpang temulawak. Senyawa kurkuminoid terdiri dari dua kandungan senyawa yaitu kurkumin dan desmetoksikurkumin. Kurkumin sebagai suatu senyawa pada fraksi kurkuminoid mempunyai aktivitas antiinflamasi, antiviral, antitumor, antihipokolestrolemik, antihepatotoksik. Minyak atsiri pada temulawak terdiri dari 32 komponen yang secara umum bersifat meningkatkan produksi getah empedu dan mampu menekan pembengkakan jaringan (Paryanto, 2006).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
7
Menurut Sidik (1995), temulawak terdiri dari tiga fraksi yaitu fraksi pati, kurkuminoid, dan minyak atsiri. Pati merupakan komponen terbesar pada temulawak yaitu sekitar 48,18-59,64%. Makin tinggi tempat tumbuh temulawak maka kadar patinya semakin tinggi pula. Kurkuminoid merupakan zat warna kuning pada temulawak yang terdiri dari senyawa kurkumin, desmetoksi kurkumin dan bis desmetoksi kurkumin dengan kadar sekitar 2 – 3,3%. Sedangkan minyak atsiri pada temulawak yang terdiri dari isofuranogermakren, trisiklin, allo-aromadendren, germakren, xanthorrizol dengan kadar sekitar 6-10% (Nugraha, 2010).
Temulawak sebagai tanaman monokotil tidak memiliki akar tunggang. Akar yang dipunyai adalah rimpang. Rimpang adalah bagian batang di bawah tanah. Rimpang disebut juga umbi akar, umbi batang, atau umbi tinggal. Rimpang temulawak berukuran paling besar di antara semua rimpang genus Curcuma dengan diameter sampai 6 cm. Rimpang temulawak terdiri atas rimpang utama (induk) dan rimpang anakan (cabang). Rimpang induknya berbentuk bulat seperti telur dan berwarna kuning tua atau cokelat kemerahan. Bagian dalamnya berwarna jingga kecokelatan. Satu rimpang induk biasanya menghasilkan 3-4 rimpang temulawak. Rimpang temulawak biasanya berbentuk bulat seperti telur dengan warna kulit rimpang cokelat kemerahan atau kuning tua, sedangkan warna daging rimpang oranye tua atau kuning (Nugraha, 2010).
Dalam penelitiannya Rismunandar mendapatkan rimpang temulawak mengandung kurkumin 1,4-4%, sedangkan Suwiah mendapatkan kadar kurkumin dalam rimpang temulawak sebesar 1,93 %. Kadar kurkumin dan minyak atsiri sangat tergantung pada umur rimpang. Kadar kurkumin dan minyak atsiri optimum tercapai saat rimpang berumur 10-12 bulan (Paryanto, 2006).
Rimpang temulawak segar dengan umur 10-12 bulan ditunjukkan pada Gambar 2.1.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
8
Gambar 2.1 Rimpang temulawak (Anonimb,2010).
Kadar komponen senyawa dan karakteristik mutu simplisia temulawak ditunjukkan pada Tabel 2.1 dan Tabel 2.2.
Tabel 2.1 Kadar Komponen Senyawa Pada Simplisia Temulawak
Sumber: Suwiah (1991) berdasarkan bobot rimpang kering dengan bobot rimpang kering dengan kadar air 10%.
Tabel 2.2 Karakteristik Mutu Simplisia Temulawak
Sumber: Materia Medika Indonesia (1979).
C. Kurkuminoid
Fraksi kurkuminoid (C25H32O3) merupakan komponen yang memberi
warna kuning berbentuk serbuk dengan rasa pahit, larut dalam pelarut polar
Komponen senyawa Kadar (%)
Pati 27,62 Lemak 5,38 Minyak atsiri 10,96 Kurkumin 1,93 Protein 6,44 Serat kasar 6,89
Karakteristik Hasil analisis (%) Standar mutu (%)
Kadar air 10,85 <12
Kadar abu 3,92 3-7
Kadar sari air 13,08 -
Kadar sari alkohol 10,95 >5
Kadar minyak atsiri 6,48 Min 5
Kadar kurkumin 1,36 0,02-2
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
9
seperti aseton, alkohol, asam glasial, alkohol hidroksida, dan etanol. Kurkuminoid memiliki aroma yang khas dan tidak bersifat toksik. Kurkuminoid rimpang temulawak terdiri atas kurkumin dan desmetoksikurkumin. Hal ini berbeda dengan kandungan kurkuminoid pada rimpang kunyit (Curcuma domestica Vahl.) selain mengandung kedua komponen di atas, masih terdapat satu komponen lain yaitu bisdemetoksikurkumin. Sifat menarik dari bisdemetoksikurkumin ini adalah aktivitas kerjanya yang antagonis dengan kurkumin dan desmetoksikurkumin yaitu dapat menghambat sekresi empedu. Memperhatikan hal tersebut, penggunaan rimpang temulawak sebagai sumber kurkuminoid lebih menguntungkan dibandingkan dengan rimpang kunyit walaupun kandungan kurkuminoid pada rimpang temulawak lebih rendah dari rimpang kunyit. Kandungan kurkuminoid dalam rimpang temulawak kering berkisar 3,16% sedangkan kandungan kurkuminoid rimpang kunyit sebesar 6,9% (Fatmawati, 2008).
Kurkuminoid merupakan golongan senyawa yang memberikan warna kuning pada tanaman marga Curcuma, termasuk temulawak dan kunyit. Selain dapat digunakan sebagai zat warna pada makanan, minuman, dan kosmetika, komponen kurkuminoid diketahui mempunyai berbagai khasiat yang sudah dimanfaatkan secara luas sebagai senyawa obat diantaranya adalah sebagai antioksidan, antiinflamasi, antiinfeksi, dan antiviral. Pada penelitian lebih lanjut kurkumin diduga dapat dimanfaatkan sebagai antitumor dan bahkan mampu melakukan penghambatan replikasi HIV. Kurkuminoid yang terdapat pada rimpang temulawak terdiri dari 2 komponen, yaitu kurkumin dan desmetoksikurkumin. Selain itu komponen lain yang terkandung pada kurkuminoid temulawak yaitu bis-desmetoksikurkumin. Kurkumin mempunyai rumus molekul C21H20O6
dengan bobot molekul 368 g/mol, sedangkan desmetoksikurkumin mempunyai rumus molekul C20H18O5 dan bobot molekul 338 g/mol
(Supriadi, 2008). Rumus bangun kurkuminoid ditunjukkan pada Gambar
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
10
Gambar 2.2 Rumus bangun kurkuminoid (Supriadi, 2008).
Sifat kimia kurkuminoid yang menarik adalah sifat perubahan warna akibat perubahan pH lingkungan. Dalam susana asam, kurkuminoid berwarna kuning atau kuning jingga, sedangkan dalam suasana basa berwarna merah. Keunikan lain yang terjadi pada sifat kurkumin dalam suasana basa selain terjadi proses disosiasi adalah terjadi degradasi kurkumin menjadi asam ferulat dan ferulloilmetan. Degradasi ini terjadi bila kurkumin berada dalam lingkungan pH 8,5-10,0 dan dalam waktu yang relatif lama. Salah satu hasil degradasi, yaitu feruloilmetan mempunyai warna kuning coklat yang akan mempengaruhi warna merah yang seharusnya terjadi (Kiswanto, 2000).
Di dalam suatu larutan, prinsip pewarnaan dari kurkuminoid adalah tampilnya bentuk tautomeri keto-enol. Kurkuminoid merupakan zat warna yang memiliki sifat dapat larut dalam minyak dan mudah larut dalam larutan basa tetapi tidak larut dalam air pada keadaan pH asam ataupun netral. Kurkuminoid juga bersifat stabil terhadap suhu tinggi dan dalam keadaan asam tetapi tidak stabil dalam kondisi basa dan terhadap cahaya (Stankovic, 2004).
Sedangkan sifat kurkuminoid lain yang penting adalah aktivitasnya terhadap cahaya. Bila kurkumin terkena cahaya, akan terjadi dekomposisi struktur berupa siklisasi kurkumin atau terjadi degradasi struktur (Tonnesen dan Karlsen, 1985). Rumus bangun kurkumin ditunjukkan pada Gambar 2.3
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
11
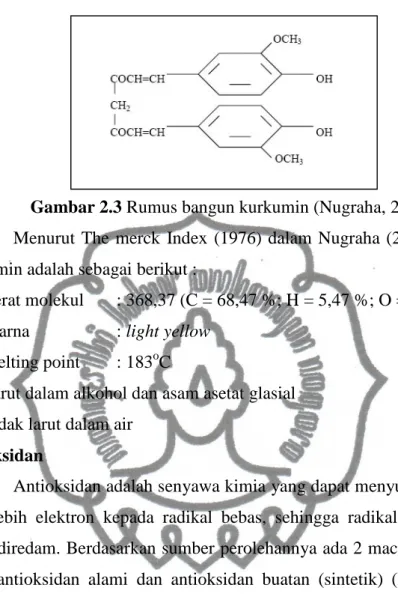
Gambar 2.3 Rumus bangun kurkumin (Nugraha, 2010).
Menurut The merck Index (1976) dalam Nugraha (2010), sifat-sifat kurkumin adalah sebagai berikut :
1. Berat molekul : 368,37 (C = 68,47 %; H = 5,47 %; O = 26,06 %). 2. Warna : light yellow
3. Melting point : 183oC
4. Larut dalam alkohol dan asam asetat glasial 5. Tidak larut dalam air
D. Antioksidan
Antioksidan adalah senyawa kimia yang dapat menyumbangkan satu atau lebih elektron kepada radikal bebas, sehingga radikal bebas tersebut dapat diredam. Berdasarkan sumber perolehannya ada 2 macam antioksidan, yaitu antioksidan alami dan antioksidan buatan (sintetik) (Dalimartha dan Soedibyo, 1999). Antioksidan alami dapat diperoleh dari ekstrak bagian tanaman rempah-rempah atau tanaman obat-obatan seperti akar, batang, daun, bunga dan biji. Senyawa yang berperan senyawa antioksidan di dalam ekstrak adalah fenol, amina aromatik, vitamin C, tokoferol, vitamin E, flavonoid dan lain sebagainya (Sukardi, 2003).
Antioksidan merupakan senyawa yang mampu menunda, memperlambat atau menghambat reaksi oksidasi pada makanan atau obat yang dapat mengakibatkan ketengikan (rancidity) pada makanan maupun kerusakan atau degradasi obat. Mekanisme kerja antioksidan secara umum menghambat oksidasi lemak atau disebut juga autooksidan yang terjadi dalam tiga tahap utama, yaitu iniasi, propagasi, dan terminasi. Pada tahap inisiasi terjadi pembentukan radikal asam lemak yaitu turunan asam lemak
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
12
yang bersifat tidak stabil dan sangat reaktif akibat hilangnya satu atom H. Pada tahap propagasi, radikal asam lemak akan bereaksi dengan oksigen membentuk radikal peroksi. Radikal peroksi lebih lanjut akan menyerang asam lemak menghasilkan hidroperoksida dan radikal asam lemak baru (tahap propagasi).
Reaksi inisiasi, radikal lipid terbentuk dari molekul lipid dan terjadi pengurangan atom hidrogen oleh radikal reaktif misalnya radikal hidrogen.
LH L* + H*
Reaksi propagasi radikal lipid diubah menjadi radikal lipid yang berbeda dan melibatkan pengurangan atom hidrogen dari molekul lipid atau penambahan atom oksigen pada radikal alkil.
L* + O2 LOO*
LOO* + LH LOOH + L*
Reaksi Terminasi, radikal bebas bergabung untuk membentuk molekul dengan membentuk pasangan antar radikal.
LOO* + LOO* LOOL + O2
LOO* + L* LOOL (Irawati,2008).
Kurkumin yang terdapat pada temulawak juga merupakan antioksidan alami yang lain dimana aktifitasnya lebih besar dibanding dengan α tokoferol jika diuji dalam minyak (Wahyudi, 2006 dalam Widiyanti, 2006). Sedangkan antioksidan sintetis merupakan antioksidan buatan yang memiliki kemampuan untuk menangkap radikal bebas. Contoh antioksidan sintetis adalah butil hidroksi anisol (BHA), butil hidroksi toluen (BHT), propil galat dan tert-butil hidoksi quinon (TBHQ) (Zapsalis,1985 dalam Widiyanti, 2006). Atas dasar fungsinya antioksidan dapat dibedakan menjadi 5 (lima) yaitu sebagai berikut :
1. Antioksidan primer yang berfungsi untuk mencegah terbentuknya radikal bebas baru karena dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, yaitu sebelum sampai bereaksi. Antioksidan primer yang ada dalam tubuh yang sangat terkenal adalah enzim superoksida dismutase. Enzim ini sangat penting karena
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
13
dapat melindungi hancurnya sel-sel dalam tubuh akibat serangan radikal bebas. Bekerjanya enzim ini sangat dipengaruhi oleh mineral-mineral seperi mangan, seng, tembaga, dan selenium yang harus terdapat dalam makanan dan minuman.
2. Antioksidan sekunder berfungsi menangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar. Contoh yang popular dari antioksidan sekunder adalah vitamin E, vitamin C, dan betakaroten yang dapat diperoleh dari buah-buahan.
3. Antioksidan tersier merupakan senyawa yang memperbaiki sel-sel dan jaringan yang rusak karena serangan radikal bebas. Antioksidan yang termasuk kelompok ini adalah jenis enzim misalnya metionin sulfoksidan reduktase yang dapat memperbaiki DNA dalam inti sel. Enzim tersebut bermanfaat untuk memperbaiki DNA pada penderita kanker.
4. Oxygen Scavanger yang mengikat oksigen sehingga tidak mendukung reaksi oksidasi, misalnya vitamin C.
5. Chelators atau Sequestrants mengikat logam yang mampu mengkatalisis reaksi oksidasi misalnya asam sitrat dan asam amino (Nugraha, 2010).
E. Senyawa Fenol
Fenol adalah senyawa yang mempunyai sebuah cincin aromatik dengan satu atau lebih gugus hidroksil. Senyawa fenol kebanyakan memiliki gugus hidroksi lebih dari satu sehingga disebut sebagai polifenol (Putra, 2009). Kurkumin merupakan molekul dengan kadar polifenol yang rendah namun memiliki aktivitas biologi yang tinggi antara lain potensi sebagai antioksidan (Jayaprakasha et al., 2006).
Senyawa fenol pada bahan makanan dapat dikelompokkan menjadi fenol sederhana dan asam folat (P-kresol, 3-etil fenol, 3,4-dietil fenol, hidroksiquinon, vanilin dan asam galat), turunan asam hidroksi sinamat (p-kumarat, kafeat, asam fenolat dan asam kloregenat) dan flavonoid (katekin, proantosianin, antisianidin, flavon, flavonol dan glikosidanya). Fenol juga dapat menghambat okidasi lipid dengan menyumbangkan atom hidrogen
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
14
kepada radikal bebas. Senyawa fenol (AH) jika berdiri sendiri tidak aktif sebagai antioksidan, substitusi grup alkil pada posisi 2, 4 dan 6 dapat meningkatkan densitas elektron gugus hidroksil, sehingga meningkatkan keaktifannya terhadap radikal lipid (Kinsella et al, 1993). Reaksi fenol dengan radikal lipid membentuk radikal fenoksil (A-) yang dapat teroksidasi lebih lanjut menghasilkan radikal bebas sebagai berikut :
F. Pengeringan
Pengeringan adalah proses pemindahan panas dan uap air secara simultan, yang memerlukan energi panas untuk menguapkan kandungan air yang dipindahkan dari permukaan bahan, yang dikeringkan oleh media pengering yang biasanya berupa panas. Bahan pangan yang dihasilkan dari produk-produk pertanian pada umumnya mengandung kadar air. Kadar air tersebut apabila masih tersimpan dan tidak dihilangkan, maka akan dapat mempengaruhi kondisi fisik bahan pangan. Contohnya, akan terjadi pembusukan dan penurunan kualitas akibat masih adanya kadar air yang terkandung dalam bahan tersebut. Pembusukan terjadi akibat dari penyerapan enzim yang terdapat dalam bahan pangan oleh jasad renik yang tumbuh dan berkembang biak dengan bantuan media kadar air dalam bahan pangan tersebut. Mikroorganisme membutuhkan air untuk pertumbuhan dan perkembangbiakannya. Jika kadar air pangan dikurangi, pertumbuhan mikroorganisme akan diperlambat. Untuk mengatasi hal tersebut, diperlukan adanya suatu proses penghilangan atau pengurangan kadar air yang terdapat dalam bahan pangan sehingga terhindar dari pembusukan ataupun penurunan kualitas bahan pangan. Salah satu cara sederhananya adalah dengan melalui proses pengeringan. Pengeringan merupakan tahap awal dari adanya pengawetan. Pengeringan akan menurunkan tingkat aktivitas air (Water
AH + ROO- A- + ROOH AH + RO- A- + ROH
A- + O2 AOO-
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
15
Activity) atau Aw yaitu jumlah air yang dapat digunakan oleh mikroorganisme untuk pertumbuhan dan perkembangbiakannya.
Prinsip utama dari pengeringan adalah penurunan kadar air untuk mencegah aktivitas mikroorganisme. Pada banyak produk, seperti sayuran, terlebih dahulu dilakukan proses pengecilan ukuran (misalnya diiris) sebelum dikeringkan. Pengecilan ukuran akan meningkatkan luas permukaan bahan sehingga akan mempercepat proses pengeluaran air. Sebelum dikeringkan, bahan pangan sebaiknya diblansir untuk menginaktifkan enzim yang dapat menyebabkan perubahan warna pangan menjadi coklat (Siswanto, 2004).
Metode pengeringan merupakan salah satu rangkaian metode pasca panen untuk mendapatkan hasil ekstrak dari tumbuh-tumbuhan. Proses pengeringan dipengaruhi oleh udara pengering dan ketebalan bahan yang akan dikeringkan. Makin tipis bahan makin cepat pengeringannya, tetapi apabila terlalu tipis akan mengakibatkan senyawa aktif yang terkandung di dalamnya menjadi mudah rusak (Septiana, 2006).
Pengeringan merupakan proses yang penting dalam pembuatan simplisia, karena disamping agar rimpang tidak membusuk, proses pengeringan juga menentukan kualitas simplisia. Tujuan pengeringan adalah menurunkan kadar air, sehingga tidak mudah ditumbuhi kapang dan bakteri, menghilangkan aktivitas enzim yang bisa menguraikan kandungan zat aktif, memudahkan proses pengolahan selanjutnya, sehingga dapat lebih ringkas, tahan lama dan mudah disimpan. Hal-hal yang perlu diperhatikan selama proses pengeringan adalah waktu pengeringan, suhu pengeringan, kelembaban udara, ketebalan bahan yang dikeringkan, sirkulasi udara dan luas permukaan bahan. Untuk memperoleh kandungan minyak yang tinggi dari rimpang sebaiknya dikeringkan sampai kadar air ±12% (Damayanti, 2008). Semakin tinggi suhu maka jumlah oleoresin yang terekstrak akan semakin banyak namun juga dapat menyebabkan kerusakan oleoresin yang tidak tahan pada suhu di atas 450 C. Sebaiknya suhu yang digunakan adalah antara 35-400 C (Ramadhan dan Phaza, 2010).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
16
Perajangan pada rimpang temulawak dilakukan untuk mempercepat proses pengeringan. Ketebalan untuk rimpang temulawak biasanya sekitar 3-5 mm (Raharjo dan Otih, 2005). Perajangan yang terlalu tebal memerlukan waktu lama dalam proses pengeringan dan kemungkinan besar bahan mudah terkontaminasi baik oleh bakteri maupun jamur. Sedangkan jika terlalu tipis dapat menyebabkan kadar minyak atsiri maupun zat aktif yang terdapat pada bahan menurun (Nugraha, 2010).
G. Ekstraksi
Salah satu tahapan penting dalam memproduksi ekstrak tanaman obat adalah proses ekstraksi. Ekstraksi merupakan istilah yang digunakan untuk mengambil senyawa tertentu dengan menggunakan pelarut yang sesuai. Metode ekstraksi tergantung pada polaritas senyawa yang akan diekstrak. Suatu senyawa menunjukkan kelarutan yang berbeda-beda dalam pelarut yang berbeda. Hal-hal yang perlu diperhatikan dalam pemilihan pelarut adalah selektivitas, kemampuan mengekstrak, toksisitas, kemudahan untuk diuapkan dan harga pelarut (Paryanto, 2006).
Metode yang pada umumnya digunakan dalam ekstraksi temulawak antara lain ekstraksi perkolasi, soxhlet dan maserasi. Pada metode perkolasi ekstraksi dilakukan dengan cara mengairkan pelarut melalui serbuk simplisia yang sudah direndam. Pada metode soxhlet, bahan berupa tepung temulawak dibungkus kertas saring kemudian dimasukkan ke dalam alat soxhlet yang telah berisi pelarut organik berupa alkohol/etanol. Kemudian bahan tersebut diekstrak oleh pelarut tersebut. Sedangkan maserasi adalah pencampuran bahan berupa tepung temulawak dengan cara merendam bahan dengan pelarut. Proses maserasi pada ekstrak temulawak menggunakan pelarut etanol 96 % dengan waktu maserasi 1 x 24 jam yang kemudian dilakukan proses penyaringan dengan menggunakan pompa vakum (Zahro, 2008). Menurut Eryanto (2009) dalam Nugraha (2010), proses maserasi yang paling baik digunakan yaitu perbandingan bahan dengan pelarut adalah 1 : 5 (b/v).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
17
H. Oleoresin
Oleoresin merupakan campuran minyak dan resin diperoleh dari hasil ekstraksi, pemekatan dan standarisasi minyak atsiri (minyak essential dan komponen non volatile dari rempah-rempah) melalui proses evaporasi dengan menggunakan alat rotary vacuum evaporator. Oleoresin biasanya berbentuk cairan kental, pasta atau padat. Menurut Aprita (2008), keuntungan penggunaan oleoresin antara lain sebagai berikut :
1. Flavor dan warna yang diperoleh lebih seragam.
2. Bahan dapat distandarisasi dengan tepat, terutama berkaitan dengan rasa, aroma dan warna. Dengan adanya standarisasi ini, kualitas produk terkontrol.
3. Bersih dan bebas dari kontaminasi mikroba serangga dan kontaminan lainnya.
4. Bebas enzim dan mengandung antioksidan alami. 5. Kadar air sangat rendah
6. Mempunyai masa simpan yang lama dalam kondisi penyimpanan normal. 7. Bahan mudah dicampur merata ke dalam bahan makanan dan minuman. 8. Menghemat ruang penyimpanan dibandingkan dengan menyimpan
rempah-rempah segar.
Oleoresin temulawak adalah sari temulawak yang mengandung komponen-komponen temulawak baik menguap (minyak atsiri) maupun tidak menguap (seperti resin dan pigmen). Oleoresin temulawak diperoleh dengan mengekstrak temulawak dengan pelarut organik. Jenis pelarut yang digunakan antara lain alkohol, heksan, etil asetat, etil alkohol, isopropil alkohol, aseton, gliserol dan gliseril. Diantara bahan-bahan tersebut alkohol banyak dipakai karena relative aman untuk makanan dan sifat polarnya banyak membantu dalam mendapatkan emulsi oleoresin yang baik (Said, 2009). Menurut Huda (2008), proses pembuatan oleoresin dilakukan dengan menggunakan rotary vacuum evaporator pada suhu 50oC setelah proses maserasi temulawak. Dalam proses rotary vacuum evaporator terjadi
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
18
pemisahan antara pelarut dengan oleoresin berdasarkan perbedaan titik didih dengan menggunakan perputaran dan pemvakuman.
I. Kerangka Berpikir
J. Hipotesis
Hipotesis dari penelitian ini adalah
1. Proses ekstraksi dengan rasio pelarut yang berbeda diduga berpengaruh terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak yang dihasilkan.
2. Variasi waktu perendaman yang digunakan diduga berpengaruh terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak yang dihasilkan.
3. Interaksi rasio pelarut dan waktu perendaman yang digunakan dalam ekstraksi diduga berpengaruh terhadap kadar kurkuminoid, total fenol, dan aktivitas antioksidan oleoresin rimpang temulawak yang dihasilkan.
Temulawak merupakan tanaman obat asli
Indonesia
Rimpang temulawak mengandung oleoresin
yang bermanfaat bagi kesehatan tubuh
Ekstraksi oleoresin yang paling sederhana
adalah menggunakan teknik maserasi
Rasio pelarut dan waktu perendaman dan yang digunakan dalam ekstraksi berpengaruh
terhadap oleoresin yang didapat
Perlu dikaji oleoresin rimpang temulawak dengan variasi rasio pelarut dan waktu perendaman terhadap kadar kurkuminoid, total
fenol, dan aktivitas antioksidan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
19
BAB III
METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Rekayasa Proses Pengolahan Pangan dan Hasil Pertanian Jurusan Teknologi Hasil Pertanian, Fakultas Pertanian, Universitas Sebelas Maret Surakarta dan Laboratorium Biologi Farmasi Universitas Islam Indonesia di Yogyakarta. Penelitian ini dilaksanakan dalam jangka waktu 4 bulan mulai bulan Juni-September 2011.
B. Bahan dan Alat
1. Bahan
Bahan utama dalam penelitian ini berupa rimpang temulawak yang dirajang dengan ketebalan 3-5 mm. Dalam proses ekstraksi temulawak pelarut yang digunakan adalah pelarut etanol 96%. Sedangkan bahan-bahan yang digunakan untuk analisis antara lain :
a. Analisis Kadar Air: xylene
b. Analisis Kadar Kurkuminoid: kurkuminoid standar dan etanol 96%. c. Analisis Total Fenol: aquadest, etanol 96%, folin ciocalteu, Na2CO3
2%.
d. Analisis Antioksidan: DPPH (2,2-dhiphenil-1-picryldhydrazyl radical) dan metanol PA.
2. Alat
Alat yang digunakan dalam pengeringan adalah cabinet dryer, untuk pembuatan bubuk simplisia menggunakan mesin penepung dan ayakan 80 mesh, dan untuk proses pembuatan oleoresin temulawak antara lain 3 buah tampah, rotary vacuum evaporator, pipet, beaker glass, pompa vakum, kertas saring dan termometer. Sedangkan alat-alat yang digunakan untuk analisis antara lain :
a. Analisis kadar air: seperangkat alat destilasi, labu destilasi, gelas ukur.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
20
pipet, gelas ukur, vortex, tabung reaksi.
c. Analisis antioksidan: spektrofotometer UV-Vis, tabung reaksi, pipet volume, vortex.
d. Analisis total fenol : labu takar 100 mL, gelas ukur, vortex, tabung reaksi, spektrofotometer UV-Vis, beaker glass, labu takar 10 mL, pengaduk, pipet.
C. Tahap Penelitian
Adapun tahapan dalam penelitian ini adalah sebagai berikut : 1. Penyiapan Bahan dan Perajangan
Rimpang temulawak yang digunakan berasal dari Batu, Wonogiri dengan umur rata-rata 10 – 12 bulan. Kemudian rimpang tersebut dicuci sampai bersih dan dilakukan proses perajangan dengan menggunakan slicer. Proses perajangan dilakukan untuk mempercepat proses pengeringan. Ketebalan rimpang temulawak mengacu pada Raharjo dan Otih (2005) sekitar 3-5 mm yang kemudian ditimbang 800 gr untuk masing-masing sampel.
2. Pengeringan
Proses pengeringan rimpang temulawak dilakukan dengan cara pengeringan cabinet dryer pada suhu 45oC. Proses pengeringan dilakukan sampai kadar air rimpang temulawak maksimal 12%. Analisis kadar air dilakukan dengan metode thermovolumetri (AOAC, 1984). Diagram alir analisis kadar air simplisia temulawak ditunjukkan pada
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
21
Gambar 3.1 Diagram alir pengujian kadar air simplisia temulawak
3. Penepungan dan Pengayakan
Proses penepungan simplisia temulawak dilakukan dengan menggunakan mesin penepung saringan berukuran kecil untuk menghasilkan bubuk temulawak. Selanjutnya bubuk temulawak dilakukan proses pengayakan dengan ayakan berukuran 80 mesh dengan menggunakan mesin pengayak.
4. Ekstraksi Dengan Variasi Waktu Perendaman
Proses ekstraksi dilakukan dengan metode yang mengacu pada Eryanto dkk (2009) yang dipadukan dengan Paryanto dan Srijanto (2004) dan Zahro (2008). Ekstrasi temulawak dilakukan dengan cara maserasi dengan suhu ruang (28-30oC). Pelarut yang digunakan dalam proses ekstraksi rimpang temulawak adalah etanol 96%. Dalam penelitian Sundari dan Sari (2009) diperoleh hasil bahwa ekstraksi oleoresin dengan etanol 96% memberikan hasil yang lebih baik daripada etanol 70%. Perolehan oleoresin dengan konsentrasi etanol yang lebih tinggi memberikan hasil yang lebih baik daripada konsentrasi etanol yang lebih rendah. Proses Ekstraksi temulawak dilakukan dengan lama perendaman 18 jam, 24 jam, dan 30 jam.
5. Ekstraksi Dengan Variasi Rasio Pelarut
Ekstrasi temulawak dilakukan dengan cara maserasi dengan variasi proporsi pelarut 1:3; 1:5; 1:7 (b/v) pada suhu ruang (28-30oC) dan
Rajangan temulawak
Simplisia kering
Pengujian kadar air dengan thermovolumetri
Pengeringan dengan menggunakan cabinet dryer 45°C
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
22
dilakukan pengadukan. Pelarut yang digunakan dalam proses ekstraksi rimpang temulawak adalah etanol 96%. Dalam penelitian Sundari dan Sari (2009) diperoleh hasil bahwa ekstraksi oleoresin dengan etanol 96% memberikan hasil yang lebih baik daripada etanol 70%. Perolehan oleoresin dengan konsentrasi etanol yang lebih tinggi memberikan hasil yang lebih baik daripada konsentrasi etanol yang lebih rendah.
6. Penyaringan
Penyaringan digunakan untuk memisahkan antara ampas atau endapan dengan filtrat. Proses penyaringan pada ekstrak temulawak dilakukan dengan pompa vakum untuk mempercepat proses penyaringan pada ekstrak temulawak.
7. Evaporasi
Proses pembuatan oleoresin temulawak menggunakan alat rotary
vacuum evaporator pada suhu 45oC dengan kecepatan yang konstan.
Proses ini dihentikan setelah pelarut etanol teruapkan semua dan didapatkan oleoresin yang berbentuk pasta. Dalam proses evaporasi ini terjadi pemisahan antara pelarut dengan oleoresin berdasarkan perbedaan titik didih dengan menggunakan perputaran dan pemvakuman. Diagram alir penelitian ditampilkan pada Gambar 3.2. 8. Analisis senyawa aktif oleoresin temulawak
Metode analisis senyawa aktif pada oleoresin temulawak ditunjukkan pada Tabel 3.1.
Tabel 3.1 Metode analisis senyawa aktif oleoresin temulawak
No Macam uji Metode
1 Kurkuminoid spektrofotometer UV-visible (AOAC, 1984) 2 Total fenol folin Ciocalteu (Nugroho, 2005)
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
23
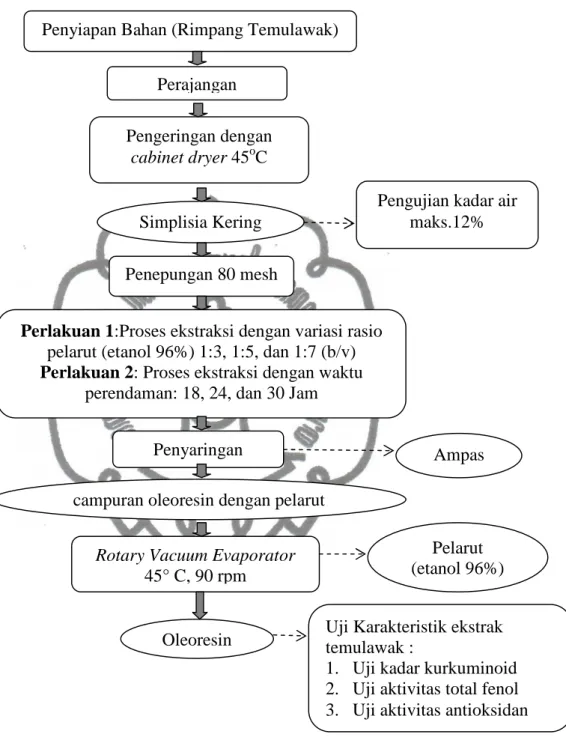
Gambar 3.2 Diagram Alir Penelitian
Penyiapan Bahan (Rimpang Temulawak)
Perajangan
Pengujian kadar air maks.12%
Uji Karakteristik ekstrak temulawak :
1. Uji kadar kurkuminoid 2. Uji aktivitas total fenol 3. Uji aktivitas antioksidan Penepungan 80 mesh
Simplisia Kering Pengeringan dengan
cabinet dryer 45oC
Penyaringan Ampas
Rotary Vacuum Evaporator 45° C, 90 rpm
campuran oleoresin dengan pelarut
Pelarut (etanol 96%)
Oleoresin
Perlakuan 1:Proses ekstraksi dengan variasi rasio
pelarut (etanol 96%) 1:3, 1:5, dan 1:7 (b/v)
Perlakuan 2: Proses ekstraksi dengan waktu
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
24
D. Rancangan Penelitian
Dalam penelitian ini digunakan Rancangan Acak Lengkap dengan dua faktor yaitu variasi rasio pelarut (1:3; 1:5; 1:7 (b/v)) dan waktu perendaman (18, 24, dan 30 jam) dengan pengulangan tiga kali tiap sampelnya. Tabel Rancangan Percobaan Acak Lengkap dengan dua faktor yaitu variasi rasio pelarut dan waktu perendaman ditunjukkan pada Tabel 3.2.
Tabel 3.2 Rancangan Percobaan Acak lengkap dengan dua faktor
Taraf Faktor Perlakuan A B C 1 A1 B1 C1 2 A2 B2 C2 3 A3 B3 C3 Keterangan: A = rasio pelarut 1:3 (b/v) B = rasio pelarut 1:5 (b/v) C = rasio pelarut 1:7 (b/v) 1 = waktu perendaman 18 Jam 2 = waktu perendaman 24 Jam 3 = waktu perendaman 30 Jam
Data yang diperoleh kemudian dianalisis dengan menggunakan two way ANOVA untuk mengetahui ada tidaknya perbedaan masing-masing perlakuan dan interaksi pada kedua perlakuan tersebut pada pada tingkat signifikansi α = 0.05, kemudian dilanjutkan dengan one way ANOVA untuk mengetahui ada tidaknya perbedaan pada masing-masing sampel dengan kedua perlakuan tersebut pada tingkat signifikansi α = 0.05.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
25
BAB IV
HASIL DAN PEMBAHASAN
A. Kadar Air
Salah satu parameter utama untuk menentukan kualitas simplisia temulawak adalah dengan menentukan kadar airnya. Dalam penelitian ini uji kadar air menggunakan metode thermovolumetri (AOAC, 1984). Dengan pengambilan sampel secara acak pada simplisia temulawak. Hasil analisis kadar air simplisia bubuk temulawak ditunjukkan pada Tabel 4.1.
Tabel 4.1 Hasil Analisis Kadar Air Simplisia Bubuk Temulawak
Sampel Kadar Air (%)
Ulangan 1 7,00
Ulangan 2 8,00
Ulangan 3 9,00
Rata-rata 8,00
Hasil penelitian menunjukkan bahwa kadar air simplisia bubuk temulawak dengan 3 kali ulangan adalah 7,00%; 8,00%; 9,00% dengan nilai rata-rata adalah 8,00%. Dari hasil tersebut menunjukkan bahwa kadar air simplisia bubuk temulawak pada keseluruhan sampel dari pengambilan secara acak berada kurang dari 12%. Sampel-sampel tersebut memenuhi karakteristik mutu simplisia temulawak yang dinyatakan Sembiring (2006) yang mengatakan bahwa kadar air simplisia temulawak maksimal 12%. Selain itu, dilihat dari standar mutu simplisia temulawak menurut RSNI/ Rancangan Standar Nasional Indonesia (2006) untuk bahan baku obat nilai kadar air simplisia temulawak maksimal adalah 10%, maka nilai kadar air pada sampel tersebut memenuhi standar yaitu kurang dari 10%. Dengan kadar air yang telah memenuhi standar, senyawa bioaktif dalam simplisia temulawak lebih dapat dipertahankan dengan teknik pengeringan yang tepat pada standar kadar air yang sama. Pada penelitian ini untuk mencapai kadar air simplisia temulawak ini sebesar 8,00% dibutuhkan waktu selama 8 jam menggunakan pengeringan Cabinet Dryer pada suhu 45°C.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
26
B. Kadar Kurkuminoid
1. Pengaruh Variasi Rasio Pelarut terhadap Kadar Kurkuminoid Oleoresin Temulawak
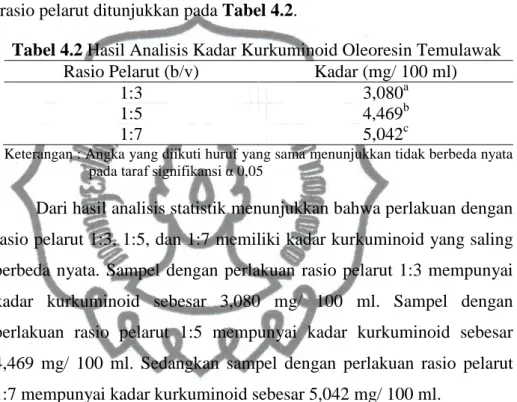
Penelitian ini menggunakan perlakuan variasi rasio pelarut dengan rasio 1:3 (b/v), 1:5 (b/v), dan 1:7 (b/v). Hasil pengujian analisis kadar kurkuminoid oleoresin temulawak dengan perlakuan variasi rasio pelarut ditunjukkan pada Tabel 4.2.
Tabel 4.2 Hasil Analisis Kadar Kurkuminoid Oleoresin Temulawak
Rasio Pelarut (b/v) Kadar (mg/ 100 ml)
1:3 3,080a
1:5 4,469b
1:7 5,042c
Keterangan : Angka yang diikuti huruf yang sama menunjukkan tidak berbeda nyata pada taraf signifikansi α 0,05
Dari hasil analisis statistik menunjukkan bahwa perlakuan dengan rasio pelarut 1:3, 1:5, dan 1:7 memiliki kadar kurkuminoid yang saling berbeda nyata. Sampel dengan perlakuan rasio pelarut 1:3 mempunyai kadar kurkuminoid sebesar 3,080 mg/ 100 ml. Sampel dengan perlakuan rasio pelarut 1:5 mempunyai kadar kurkuminoid sebesar 4,469 mg/ 100 ml. Sedangkan sampel dengan perlakuan rasio pelarut 1:7 mempunyai kadar kurkuminoid sebesar 5,042 mg/ 100 ml.
Hasil analisis ini menunjukkan bahwa semakin besar rasio pelarut yang digunakan maka semakin tinggi kadar kurkuminoid oleoresin yang dihasilkan. Hal ini kemungkinan disebabkan karena etanol merupakan pelarut yang dapat melarutkan dengan baik kandungan kurkuminoid dalam bahan sehingga semakin besar perbandingannya semakin besar juga terjadinya kontak antara partikel serbuk dengan pelarut (Paryanto, 2006).
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
27
2. Pengaruh Waktu Perendaman terhadap Kadar Kurkuminoid Oleoresin Temulawak
Dalam penelitian ini, perlakuan dengan waktu perendaman dilakukan dalam tiga variasi yaitu pada 18, 24, dan 30 jam. Hasil pengujian analisis kadar kurkuminoid oleoresin temulawak dengan variasi perlakuan waktu perendaman ditunjukkan pada Tabel 4.3.
Tabel 4.3 Hasil Analisis Kadar Kurkuminoid Oleoresin Temulawak
Waktu perendaman Kadar (mg/100 ml)
18 Jam 3,896a
24 Jam 4,106b
30 Jam 4,590c
Keterangan : Angka yang diikuti huruf yang sama menunjukkan tidak berbeda nyata pada taraf singnifikansi α 0,05
Dari hasil analisis statistik menunjukkan bahwa kadar kurkuminoid dengan variasi waktu perendaman pada masing-masing sampel berbeda nyata. Sampel dengan perlakuan waktu perendaman 18 jam mempunyai kadar kurkuminoid sebesar 3,896 mg/ 100 ml. Kemudian sampel dengan waktu perendaman 24 jam mempunyai kadar kurkuminoid 4,106 mg/ 100 ml dan pada sampel dengan waktu perendaman selama 30 jam mempunyai kadar kurkuminoid sebesar 4,590 mg/ 100 ml.
Dari data tersebut, kadar kurkuminoid tertinggi terdapat pada sampel dengan perlakuan waktu perendaman 30 jam, sedangkan kadar kurkuminoid terendah terdapat pada sampel dengan perlakuan waktu perendaman pada 18 jam. Hasil ini menunjukkan pengaruh variasi waktu perendaman terhadap kadar kurkuminoid dalam sampel yaitu dengan bertambahnya waktu ekstraksi maka semakin besar kadar kurkuminoid yang dihasilkan. Waktu ekstraksi oleoresin yang lebih lama akan menghasilkan kadar kurkuminoid yang lebih besar karena semakin lama waktu ekstraksi berlangsung, maka waktu kontak antara sampel dengan pelarut semakin lama sehingga jumlah senyawa yang terekstraksi semakin banyak. Kondisi ini akan terus berlanjut hingga tercapai kondisi kesetimbangan antara konsentrasi senyawa di dalam
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
28
bahan baku dengan konsentrasi senyawa di pelarut (Srijanto dan Paryanto, 2004).
3. Pengaruh Interaksi Variasi Rasio Pelarut dan Waktu Perendaman terhadap Kadar Kurkuminoid Oleoresin Temulawak
Dari hasil analisis statistik menunjukkan terjadi interaksi antara perlakuan variasi rasio pelarut dengan perlakuan waktu perendaman yang ditunjukkan dari nilai signifikansinya kurang dari α 0,05. Hal ini mengartikan bahwa antara masing-masing perlakuan variasi rasio pelarut dan perlakuan waktu perendaman saling mempengaruhi satu dengan lainnya terhadap kadar kurkuminoid.
Untuk mengetahui ada tidaknya perbedaan pada masing-masing sampel antara perlakuan variasi rasio pelarut dengan perlakuan waktu perendaman dapat dilanjutkan dengan one way ANOVA pada tingkat α yang sama yaitu 0,05. Hasil analisis kadar kurkuminoid oleoresin temulawak pada masing-masing sampel ditunjukkan pada Tabel 4.4 dan diagram pada Gambar 4.1.
Tabel 4.4 Hasil Analisis Kadar Kurkuminoid Oleoresin Temulawak
Sampel Kadar (mg/100 ml) 1:3 (b/v) 18 jam 2,804a 1:3 (b/v) 24 jam 3,035b 1:3 (b/v) 30 jam 3,402c 1:5 (b/v) 18 jam 4,175d 1:5 (b/v) 24 jam 4,536e 1:5 (b/v) 30 jam 4,698ef 1:7 (b/v) 18 jam 4,710ef 1:7 (b/v) 24 jam 4,746f 1:7 (b/v) 30 jam 5,670g
Keterangan : Angka yang diikuti huruf yang sama menunjukkan tidak berbeda nyata pada taraf signifikansi α 0,05
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
29
Gambar 4.1 Kadar Kurkuminoid
Dari hasil pengamatan menunjukkan bahwa semakin besar rasio pelarut dan semakin lama waktu perendaman memberikan hasil kadar kurkuminoid dengan kenaikan yang berbeda nyata, walaupun tidak signifikan. Beberapa sampel menunjukkan hasil yang tidak berbeda nyata seperti sampel 1:5 (b/v) 24 jam yang tidak berbeda nyata dengan sampel 1:5 (b/v) 30 jam dan 1:7 (b/v) 18 jam . Kemudian sampel 1:5 (b/v) 30 jam dan 1:7 (b/v) 18 jam yang juga tidak berbeda nyata dengan sampel 1:7 (b/v) 24 jam.
Pada Gambar 4.1 menunjukkan bahwa kadar kurkuminoid tertinggi yaitu pada sampel 1:7 (b/v) 30 jam dengan nilai sebesar 5,670 mg/ 100 ml. Sedangkan kadar kurkuminoid terendah terdapat pada sampel 1:3 (b/v) 18 jam sebesar 2,804 mg/ 100 ml. Rata-rata hasil kurkuminoid pada semua sampel berada pada rata-rata ini sebesar 4,197 mg/ 100 ml atau dalam satuan persen sebesar 4,19%.
Dalam penelitian lain menurut Sembiring (2006) yang mengatakan bahwa kadar kurkuminoid oleoresin temulawak berkisar 1-2 %. Adapun Srijanto (2005) melakukan ekstraksi dari temulawak secara maserasi dengan variabel waktu, perbandingan pelarut-bahan baku dan suhu serta pelarut aseton dan etanol. Kadar kurkumin tertinggi didapat pada ekstraksi dengan pelarut etanol dengan waktu 18
0 1 2 3 4 5 6 7 8 1:3 (b/v) 1:5 (b/v) 1:7 (b/v) Rasio Pelarut (b/v) Ka da r K urk um in oi d (% ) 18 jam 24 jam 30 jam
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
30
jam dan perbandingan pelarut 1:8 (b/v). Pandiangan (2011) dalam penelitiannya mendapatkan rendemen ekstrak temulawak terbesar yaitu 8,63 % diperoleh dengan pelarut etanol dengan rasio pelarut 1:5 (b/v) selama 24 jam. Sedangkan Ria (1989) mengekstrak rimpang temulawak dengan menggunakan metode maserasi untuk melihat pengaruh jumlah pelarut, lama ekstraksi dan ukuran butir bahan terhadap rendeman dan mutu oleoresin. Hasil yang diperoleh menunjukkan bahwa rendemen berkisar antara 1,86-3,06 %, kadar kurkumin terbesar diperoleh pada saat perlakuan pelarut 1:8 (b/v).
Perbedaan kandungan yang diperoleh ini dikarenakan oleh beberapa faktor, selain karena metode proses yang digunakan, individual variability bahan seperti varietas bahan, umur rimpang dan tempat tumbuh juga dapat mempengaruhi kandungan senyawa aktif yang ada di dalam rimpang temulawak (Fatmawati, 2008).
C. Total Fenol
1. Pengaruh Variasi Rasio Pelarut terhadap Kadar Total Fenol Oleoresin Temulawak
Perlakuan variasi rasio pelarut pada temulawak merupakan salah satu faktor penting karena kandungan temulawak rentan sekali mengalami kerusakan sehingga perlu menentukan rasio pelarut yang efektif dalam meminimalkan kerusakan senyawa-senyawa dalam temulawak. Hasil analisis kadar total fenol oleoresin temulawak dengan perlakuan variasi rasio pelarut ditunjukkan pada Tabel 4.5.
Tabel 4.5 Hasil Analisis Kadar Total Fenol Oleoresin Temulawak
Rasio pelarut Kadar (mg/ 100 ml)
1:3 (b/v) 5,212a
1:5 (b/v) 6,038b
1:7 (b/v) 6,789c
Keterangan : Angka yang diikuti huruf yang sama menunjukkan tidak berbeda nyata pada taraf signifikansi α 0,05
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
31
Dari hasil analisis statistik menunjukkan bahwa perlakuan rasio pelarut 1:3, 1:5 dan 1:7 (b/v) secara berurutan memiliki kadar total fenol yang meningkat dan saling berbeda nyata. Sampel dengan rasio pelarut 1:3 (b/v) memilikii kadar total fenol sebesar 5,212 mg/ 100 ml. Kemudian sampel dengan rasio pelarut 1:5 (b/v) memiliki kadar total fenol sebesar 6,038 mg/ 100 ml. Dan sampel dengan rasio pelarut 1:7 (b/v) memiliki kadar total fenol sebesar 6,789 mg/ 100 ml. Dari hasil tersebut ditunjukkan bahwa kadar total fenol terbesar yaitu pada rasio pelarut 1:7 (b/v) diikuti dengan rasio pelarut 1:5 dan 1:3 (b/v). Yang berarti bahwa rasio pelarut 1:7 (b/v) lebih efektif dalam menghasilkan kandungan senyawa fenol dalam oleoresin dibanding perlakuan lainnya. Hasil analisis ini menujukkan bahwa perlakuan variasi rasio pelarut berpengaruh dalam mengekstrak senyawa fenol pada oleoresin temulawak. Hal ini kemungkinan disebabkan karena sifat dari senyawa fenol yang larut dalam pelarut organik, dimana etanol merupakan pelarut organik yang dapat melarutkan dengan baik kandungan senyawa fenol dalam bahan sehingga semakin besar perbandingannya semakin besar juga terjadinya kontak antara partikel serbuk dengan pelarut sehingga senyawa fenol semakin banyak yang terekstrak (Paryanto, 2006).
2. Pengaruh Waktu Perendaman terhadap Kadar Total Fenol Oleoresin Temulawak
Tabel 4.6. Hasil Analisis Kadar Total Fenol Oleoresin Temulawak
Waktu perendaman Kadar (mg/ 100 ml)
18 jam 5,808a
24 jam 6,038b
30 jam 6,254 c
Keterangan : Angka yang diikuti huruf yang sama menunjukkan tidak berbeda nyata pada taraf signifikansi α 0,05
Perlakuan waktu perendaman pada temulawak juga merupakan salah satu faktor penting dalam menghasilkan oleoresin temulawak. Dan untuk mendapatkan produk oleoresin yang bermutu maka perlu menentukan waktu perendaman yang efektif sehingga dapat diperoleh
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
32
ekstrak senyawa fenol temulawak yang optimal. Hasil analisis kadar total fenol oleoresin temulawak dengan variasi waktu perendaman ditunjukkan pada Tabel 4.6.
Tabel 4.6 tersebut menunjukkan bahwa sampel dengan perlakuan
waktu perendaman 18, 24 dan 30 jam memberikan hasil dengan kenaikan kadar total fenol yang berbeda nyata. Sampel dengan waktu perendaman 18 jam mempunyai kadar total fenol terendah yaitu sebesar 5,808 mg/ 100 ml. Kemudian sampel dengan waktu perendaman 24 jam mempunyai kadar total fenol sebesar 6,038 mg/ 100 ml. Dan sampel dengan waktu perendaman 30 jam mempunyai kadar total fenol tertinggi sebesar 6,254mg/ 100 ml.
Dalam penelitian Kawiji dkk. (2008) menjelaskan bahwa semakin lama ekstraksi berlangsung maka waktu kontak antara sampel dengan etanol semakin lama sehingga jumlah senyawa fenol yang terekstraksi pada bahan semakin banyak. Dan kondisi ini akan terus berlanjut hingga tercapai kondisi kesetimbangan antara konsentrasi senyawa di dalam bahan dengan konsentrasi senyawa di pelarut (Srijanto dan Paryanto, 2004).
3. Pengaruh Interaksi Variasi Rasio Pelarut dan Waktu Perendaman terhadap Kadar Total Fenol Oleoresin Temulawak
Dari hasil analisis statistik menunjukkan adanya interaksi antara perlakuan variasi rasio pelarut dengan waktu perendaman yang ditunjukkan dari nilai sigfinikasinya kurang dari α 0,05. Hal ini menjelaskan bahwa antara masing-masing perlakuan variasi rasio pelarut dan perlakuan waktu perendaman saling mempengaruhi satu dengan lainnya terhadap kadar total fenol.
Kemudian untuk mengetahui ada tidaknya pengaruh pada masing-masing sampel dengan variasi rasio pelarut dan waktu perendaman adalah dengan one way ANOVA pada tingkat α yang sama yaitu 0,05. Hasil analisis kadar total fenol oleoresin temulawak pada