SKRIPSI
PEMBUATAN KALSIUM KARBONAT DARI BIJI
DURIAN MENGGUNAKAN H
2SO
4DAN H
2C
2O
4DISUSUN OLEH :
ANDI TRIAS PERMANA 0831310060
JURUSAN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL ”VETERAN” JAWA TIMUR
SURABAYA 2012
PEMBUATAN KALSIUM KARBONAT DARI BIJI
DURIAN MENGGUNAKAN H
2SO
4DAN H
2C
2O
4SKRIPSI
Diajukan Untuk Memenuhi Sebagian Persyaratan Dalam Memperoleh Gelar Sarjana Teknik
Jurusan Teknik Kimia
Oleh :
ANDI TRIAS PERMANA NPM. 0831310060
JURUSAN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL ”VETERAN” JAWA TIMUR
SURABAYA 2012
YAYASAN KEJUANGAN PANGLIMA BESAR SUDIRMAN UNIVERSITAS PEMBANGUNAN NASIONAL “VETERAN”
JAWA TIMUR
FAKULTAS TEKNOLOGI INDUSTRI PROGRAM STUDI TEKNIK KIMIA
KETERANGAN REVISI
Yang bertanda tangan dibawah ini:
Nama : Andi Trias Permana
NPM : 0831310060
Program Studi : Teknik Kimia
Telah mengerjakan revisi, tidak ada revisi *) Proposal / Skripsi / Kerja Praktek, dengan judul:
“PEMBUATAN KALSIUM KARBONAT DARI BIJI DURIAN MENGGUNAKAN H2SO4 DAN H2C2O4”
Surabaya, Desember 2011
Dosen Penguji yang memerintahkan revisi:
1. Ir. Dwi Heri Astuti, MT ( )
2. Ir. Siswanto ( )
Mengetahui: Dosen Pembimbing
Ir. Retno Dewati, MT 196001121987032001
Telah mengerjakan revisi sesuai dengan yang diperintahkan
*) Coret yang tidak perlu
SKRIPSI
PEMBUATAN KALSIUM KARBONAT DARI BIJI DURIAN MENGGUNAKAN H2SO4 DAN H2C2O4
Disusun Oleh:
ANDY TRIAS P. NPM. 0831310060
Telah dipertahankan dan diterima Oleh Dosen Penguji 195905201984032001
2.
Ir. Siswanto
195412121983031001
196001121987032001
Mengetahui
Dekan Fakultas Teknologi Industri
Universitas Pembangunan Nasional “Veteran” Jawa Timur
Ir. Sutiyono, MT 196007131987031001
LEMBAR PENGESAHAN
SKRIPSI
PEMBUATAN KALSIUM KARBONAT DARI BIJI DURIAN
MENGGUNAKAN H2SO4 DAN H2C2O4
Oleh :
ANDI TRIAS PERMANA 0831310060
Telah Diterima dan Disetujui Untuk Diseminarkan
Mengetahui, Dosen Pembimbing
Ir. Retno Dewati, MT. NIP. 196001121987032001
ii
KATA PENGANTAR
Dengan mengucapkan rasa syukur kepada Allah SWT dan dengan segala
rahmat serta karuniaNya sehingga penyusun telah dapat menyelesaikan Penelitian
“Pembuatan Kalsium Karbonat Dari Biji Durian Menggunakan H2SO4 dan
H2C2O4”, dimana Penelitian ini merupakan tugas yang diberikan sebagai salah
satu syarat untuk menyelesaikan program pendidikan kesarjanaan di Jurusan
Teknik Kimia, Fakultas Teknologi Industri, Universitas Pembangunan Nasional
“Veteran” Jawa Timur.
Penelitian “Pembuatan Kalsium Karbonat Dari Biji Durian Menggunakan
H2SO4 dan H2C2O4” ini disusun berdasarkan pada beberapa sumber yang berasal
dari beberapa literature, data-data, dan internet.
Pada kesempatan ini saya mengucapkan terima kasih atas segala bantuan
baik berupa saran, sarana maupun prasarana sampai tersusunya Tugas Akhir ini
kepada :
1. Bapak Ir. Sutiyono, MT, selaku Dekan FTI UPN “Veteran” Jawa Timur
2. Ibu Ir. Retno Dewati, MT, selaku Ketua Jurusan Teknik Kimia dan Dosen
Pembimbing Penelitian, FTI UPN “Veteran” Jawa Timur
3. Ibu Ir. Dwi Heri Astuti, MT, selaku Dosen Penguji.
4. Bapak Ir. Siswanto, selaku Dosen Penguji.
5. Dosen-dosen Jurusan Teknik Kimia, FTI UPN “Veteran” Jawa Timur
6. Seluruh Civitas Akademik Jurusan Teknik Kimia, FTI UPN “Veteran”
Jawa Timur
7. Kedua Orang tua dan semua saudara yang selalu mendoakan saya.
8. Semua pihak yang telah membantu, memberikan bantuan, saran serta
dorongan dalam penyelesaian penelitian ini.
iii
Saya menyadari bahwa penelitian ini masih jauh dari sempurna, karena itu
segala kritik dan saran yang membangun sangat saya harapkan dalam
sempurnanya penelitian ini.
Sebagai akhir kata, penyusun mengharapkan semoga penelitian yang telah
dilakukan ini dapat bermanfaat bagi kita semua khususnya bagi mahasiswa
Fakultas Teknologi Indusri Jurusan Teknik Kimia.
Surabaya, Maret 2012
Penyusun
iv
BAB I PENDAHULUAN I.1 Latar Belakang ... 1
I.2 Tujuan Penelitian ... 3
I.3 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA II.1 Teori Umum ... 4
II.2 Landasan Teori ... 13
II.3 Hipotesis ... 15
BAB III PELAKSANAAN PENELITIAN III.1 Bahan yang Digunakan ... 17
III.2 Alat yang Digunakan ... 17
III.3 Variabel yang Digunakan ... 18
III.4 Skema Penelitian ... 19
III.5 Prosedur Penelitian ... 20
III.6 Analisa Hasil ... 21
BAB IV HASIL PENELITIAN DAN PEMBAHASAN IV.1 Hasil Penelitian ... 22
IV.2 Pembahasan ... 23
BAB V KESIMPULAN DAN SARAN V.1 Kesimpulan ... 26
V.2 Saran ... 26
DAFTAR PUSTAKA ... vii
v
LAMPIRAN
vi
vi
DAFTAR TABEL
Tabel 1. Kandungan Pada Durian ... 6
Tabel 2. Kandungan Pada Biji Durian ... 7
Tabel 3. Spesifikasi CaCO3 ... 9
Tabel 4. Hasil Kadar CaCO3 terhadap perubahan
konsentrasi H2C2O4 dan volume H2SO4 ... 22
vii
DAFTAR GAMBAR
Gambar 1. Furnace ... 21
Gambar 2. Magnetic Hot Plate Stirrer ... 21
Gambar 3. Rangkaian Alat Titrasi ... 21
Gambar 4. Grafik hubungan antara H2C2O4 (% berat)
dan H2SO4 4 N (ml) terhadap kadar CaCO3 ... 23
i
INTISARI
Kalsium karbonat (CaCO3) dapat digunakan sebagai bahan dasar pasta
gigi, bahan kosmetik, farmasi, antibiotik dan sebagainya. Secara umum, pembuatan CaCO3 dipengaruhi oleh beberapa faktor yaitu waktu pencampuran,
suhu pencampuran, dan konsentrasi pelarut. Tujuan penelitian ini adalah untuk mengkaji penambahan H2SO4 4 N dan H2C2O4 terhadap pembuatan CaCO3.
Proses penelitian dilakukan dengan prosedur, pertama biji durian dihancurkan sampai berukuran kecil dan dikeringkan dengan bantuan oven. Setelah itu dibakar dengan suhu 500 oC selama 5 jam. Kemudian abu biji durian yang dihasilkan ditambahkan H2SO4 4 N dengan variabel volume 80 ml, 90 ml,
100 ml, 110 ml dan 120 ml sambil dipanaskan pada suhu 100 oC dan diaduk selama 10 menit yang akan menghasilkan endapan. Endapan yang diperoleh tersebut ditambahkan dengan H2C2O4 dengan variabel konsentrasi (% berat) 10%,
12%, 14%, 16% dan 18% sambil dipanaskan pada suhu 100 oC dan diaduk selama 35 menit yang akan menghasilkan endapan lagi. Kemudian endapan tersebut dipanaskan di dalam furnace pada suhu 600 oC selama 2 jam, sehingga menghasilkan CaCO3.
Berdasarkan hasil penelitian yang telah dilakukan, bahwa kadar CaCO3
(%) tertinggi pada saat volume H2SO4 4 N 100 ml dan berat H2C2O4 14%, yaitu
sebesar 96,42%.
Tugas Akhir BAB I -1 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi
BAB I
PENDAHULUAN
I.1 Latar
Belakang
Gliserol terdapat dalam bentuk lemak hewan dan tumbuhan serta
bermacam-macam minyak. Gliserol jarang ditemukan dalam bentuk bebas tetapi
biasanya terdapat sebagai trigliserida yang bercampur dengan bermacam-macam
asam lemak misalnya: asam stearat, asam oleat, asam palminat dan asam laurat,
serta sebagian lemak. Asam lemak tersebut biasanya ditemukan dalam minyak
kelapa sawit atau Crude Palm Oil (CPO), Palm Kernel Oil (PKO), Minyak
kelapa, Cotton Seet, Soybean oil, dan Olive. Minyak nabati menghasilkan gliserol
yang lebih besar dari pada beberapa lemak hewan seperti Tallow dan Lard.
Gliserol juga terdapat secara alamiah sebagai trigliserida pada seluruh sel-sel
hewan dan tumbuhan dalam bentuk lipida sebagai Lecithine Dap Caphaline.
Trigliserida ini tidak mempunyai nilai komersil.
Gliserol pertama kali dibuat pada tahun 1779 oleh Scheele, yang
memanaskan campuran Litharge dan Olive Oil dan kemudian diekstraksi dengan
air. Dengan menguapkan air, Scheele mendapatkan cairan yang rasanya manis.
Kemudian oleh Chevreul, Poluze, Bertheolot, dan lainnya dipekatkan dan didapat
Trihidrat Alkohol (gliserol).
Tugas Akhir BAB I -2 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi
Gliserol merupakan hasil samping dari pabrik biodiesel dengan bahan
baku Crude Palm Oil (CPO).
I.2 Manfaat
Dalam industri, gliserol dapat digunakan sebagai bahan pembuatan alkyl
resin, ester gum, obat-obatan dan farmasi, kosmetik, wangi-wangian, sebagai
pelapis luar daun tembakau agar tidak cepat layu atau rusak, bahan pembuatan
sabun spesial dan transparan, bahan peledak, sebagai bahan plastiliser untuk
regenerasi selulosa, sebagai solven dan pembuatan gula-gula dan ice cream,
untuk menjaga kristalisasi, sebagai minyak pelumas pada kompresor oksida
karena gliserol tahan terhadap oksida minyak mineral. Gliserol dapat digunakan
pada pompa yang terkena bensena dan bensin karena gliserol tidak larut dalam
kedua zat tersebut. Untuk pelumas biasanya ditambahkan grafit dalam gliserol,
hal ini juga dipergunakan untuk alat-alat ukur dan kran yang bertekanan tinggi,
gliserol juga digunakan untuk melunakkan daging, bahan campuran makanan agar
mudah dicerna dan tidak beracun dengan karbohidrat membentuk lemak.
Tujuan dari Pra Rancangan Pabrik Gliserol dari Hasil Samping Pabrik
Biodiesel adalah :
a). Memanfaatkan hasil samping pabrik biodiesel, sehingga menghasilkan produk
yang lebih bermanfaat untuk memenuhi kebutuhan perindustrian akan gliserol.
b). Menambah lapangan kerja di dunia industri, secara khusus industri kimia.
Tugas Akhir BAB I -3 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi
I.3 Aspek
Ekonomi
Guna memenuhi kebutuhan dalam negeri, sebagian besar masih
menggantungkan pada impor. Tetapi disisi lain selain untuk memenuhi kebutuhan
dalam negeri, tetapi juga diorientasikan untuk meningkatkan ekspor guna
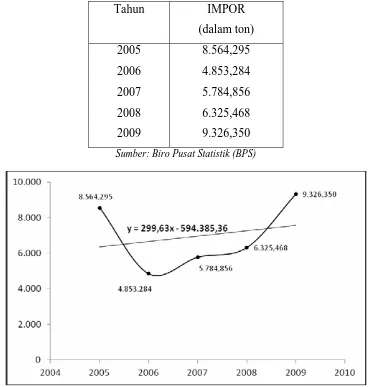
memperbesar pendapatan devisa negara. Dari tabel dibawah ini, dapat diketahui
bahwa volume impor gliserol masih jauh lebih besar dengan volume ekspornya.
Tabel I.3.1 Data Ekspor Dan Impor Produk Gliserol di Indonesia
Tahun
IMPOR
(dalam ton)
2005 8.564,295
2006 4.853,284
2007 5.784,856
2008 6.325,468
2009 9.326,350
Sumber: Biro Pusat Statistik (BPS)
Grafik I.3.1 Perkembangan Industri Gliserol
Tugas Akhir BAB I -4 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi
Dalam menentukan kapasitas pabrik gliserol ini, dititik beratkan pada
ketersediaan bahan baku gliserol dan pemenuhan kebutuhan dalam negeri
sekaligus untuk peningkatan volume ekspornya. Sedangkan kebutuhan dalam
negeri dan luar negeri akan gliserol masih cukup besar dengan melihat semakin
banyaknya didirikan industri makanan, minuman, tekstil dan farmasi yang
membutuhkan produk gliserol ini. Selain itu, jumlah industri gliserol yang masih
sangat sedikit di Indonesia. Hal ini menjadi suatu tantangan bagi produsen untuk
memproduksi gliserol, karena peluangnya yang cerah dan terbuka lebar.
I.4
Sifat Bahan Baku Dan Produk
1. Bahan baku
Hasil samping pabrik biodiesel :
Gliserol : 27,8975 %
Natrium Hidroksida (NaOH)
Asam Asetat (CH3COOH)
I.4.1 Sifat-sifat bahan pembantu dan bahan baku
1. Crude Palm Oil (CPO)
Berat jenis () : 927,07 kg/m3
Tugas Akhir BAB I -5 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi Viskositas () pada 30oC : 3,595 Cp
Indeks bias pada 40oC : 0,9226
Angka iodium : 48-56 g-I2/100g
Bilangan penyabunan : 196-206 mg-KOH/g
2. Air
Tugas Akhir BAB I -6 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi
Spesifik grafiti : 2,13
I.4.2 Sifat-sifat produk
Produk yang dihasilkan adalah gliserol 97,622% Gliserol merupakan
larutan bening, berwarna dan tidak berbau. Larutan higrokopis dengan rasa manis
dan larut dalam air, alkohol dan menyerap SO2 dan H2 dari udara.
1. Sifat-sifat fisik gliserol
Titik didih pada 1 atm : 289,0 0C
Titik leleh : 17,8 0C
Temperatur kritis : 453 0C
Tekanan kritis : 66,9 atm
Densitas liquid : 1.261 Kg/m3
Panas laten penguapan : 61.127 J/mol
Gliserol larut sempurna dalam air dan alkohol, serta sedikit larut
dalam ether, ethil asetat dan doxan
Gliserol tidak larut dalam Hidrokarbon
2. Sifat-sifat kimia gliserol
Tugas Akhir BAB I -7 Pendahuluan
Pabrik Gliserol dari L imbah Pabrik Biodiesel dengan Proses Transest erif ikasi
Rumus kimia : H2COH. HCOH. H2COH
Berat molekul : 92 kg/kmol
Gliserol sebagai alkohol trihidrat dapat membentuk ester, amina, halida,
aldehida dan senyawa tak jenuh seperti akrolein. Oksida gliserin menghasilkan
bermacam-macam produk tergantung pada kondisi reaksi, misalnya dapat
menghasilkan gliseraldehid dari oksida hidroksil.asam sitrat dapat mengkonversi
Gliserol menjadi asam gliserol.
4
Durian merupakan tanaman buah berupa pohon. Sebutan durian diduga
berasal dari istilah Melayu yaitu dari kata duri yang diberi akhiran -an sehingga
menjadi durian. Kata ini terutama dipergunakan untuk menyebut buah yang
kulitnya berduri tajam. Tanaman durian berasal dari hutan Malaysia, Sumatra, dan
Kalimantan yang berupa tanaman liar. Penyebaran durian ke arah Barat adalah ke
Thailand, Birma, India dan Pakistan. Buah durian sudah dikenal di Asia Tenggara
sejak abad 7 M. Tanaman durian termasuk famili Bombaceae sebangsa pohon
kapuk-kapukan. Yang lazim disebut durian adalah tumbuhan dari marga (genus)
Durio, Nesia, Lahia, Boschia dan Coelostegia. Ada puluhan durian yang diakui
keunggulannya oleh Menteri Pertanian dan disebarluaskan kepada masyarakat
untuk dikembangkan. Macam varietas durian tersebut adalah: durian sukun (Jawa
Tengah), petruk (Jawa Tengah), sitokong (Betawi), simas (Bogor), sunan (Jepara),
otong (Thailand), kani (Thailand), sidodol (Kalimantan Selatan), sijapang
(Betawi) dan sihijau (Kalimantan Selatan). Buah berkembang setelah pembuahan
dan memerlukan 4-6 bulan untuk pemasakan. Pada masa pemasakan terjadi
persaingan antarbuah pada satu kelompok, sehingga hanya satu atau beberapa
buah yang akan mencapai kemasakan, dan sisanya gugur. Buah akan jatuh sendiri
apabila masak. Pada umumnya berat buah durian dapat mencapai 1,5 hingga 5
Hak Cipta © milik UPN "Veteran" Jatim :
5
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
kilogram, sehingga kebun durian menjadi kawasan yang berbahaya pada masa
musim durian. Setiap buah memiliki lima ruang, yang menunjukkan banyaknya
daun buah yang dimiliki. Masing-masing ruangan terisi oleh beberapa biji,
biasanya tiga butir atau lebih, lonjong hingga 4 cm panjangnya, dan berwarna
merah muda kecoklatan mengkilap. Biji terbungkus oleh arilus (salut biji, yang
biasa disebut sebagai "daging buah" durian) berwarna putih hingga kuning terang
dengan ketebalan yang bervariasi, namun pada kultivar unggul ketebalan arilus ini
dapat mencapai 3 cm. Biji dengan salut biji dalam perdagangan disebut ponggè.
Pemuliaan durian diarahkan untuk menghasilkan biji yang kecil dengan salut biji
yang tebal, karena salut biji inilah bagian yang dimakan. Beberapa varietas unggul
menghasilkan buah dengan biji yang tidak berkembang namun dengan salut biji
tebal (disebut "sukun"). Durian terutama dipelihara orang untuk buahnya, yang
umumnya dimakan (arilus atau salut bijinya) dalam keadaan segar. Salut biji ini
umumnya manis dan sangat bergizi karena mengandung banyak karbohidrat,
lemak, protein, dan mineral. Pada musim raya durian, buah ini dapat dihasilkan
dengan berlimpah, terutama di sentra-sentra produksinya di daerah. Secara
tradisional, daging buah yang berlebih-lebihan ini biasa diawetkan dengan
memasaknya bersama gula menjadi dodol durian (biasa disebut lempok), atau
memfermentasikannya menjadi tempoyak. Selanjutnya, tempoyak yang rasanya
masam ini biasa menjadi bahan masakan seperti sambal tempoyak, atau untuk
campuran memasak ikan. Durian pun kerap diolah menjadi campuran bahan
kue-kue tradisional, seperti gelamai atau jenang. Terkadang, durian dicampurkan
dalam hidangan nasi pulut (ketan) bersama dengan santan. Dalam dunia masa
Hak Cipta © milik UPN "Veteran" Jatim :
6
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
kini, durian (atau aromanya) biasa dicampurkan dalam permen, es krim, susu, dan
berbagai jenis minuman penyegar lainnya. Bijinya bisa dimakan sebagai camilan
setelah direbus atau dibakar, atau dicampurkan dalam kolak durian. Biji durian
yang mentah beracun dan tak dapat dimakan karena mengandung asam lemak
siklopropena (cyclopropene). Biji durian mengandung sekitar 27% amilosa.
Kuncup daun (pucuk), mahkota bunga, dan buah yang muda dapat dimasak
sebagai sayuran.
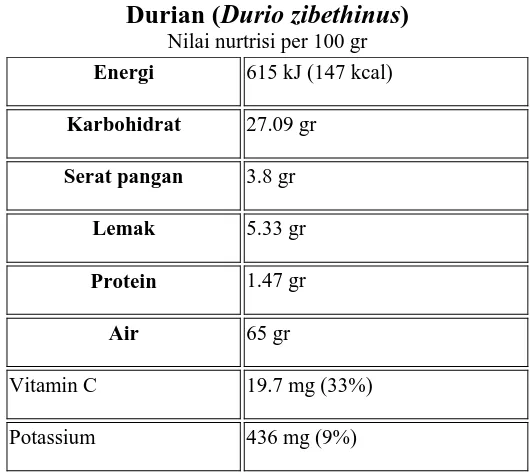
Tabel 1. Kandungan Pada Durian
Durian (Durio zibethinus) Nilai nurtrisi per 100 gr
Energi 615 kJ (147 kcal)
Karbohidrat 27.09 gr
Serat pangan 3.8 gr
Beberapa bagian tumbuhan kadang-kadang dimanfaatkan sebagai bahan
obat tradisional. Akarnya dimanfaatkan sebagai obat demam. Daunnya, dicampur
dengan jeringau (Acorus calamus), digunakan untuk menyembuhkan cantengan
(infeksi pada kuku). Kulit buahnya untuk mengobati ruam pada kulit (sakit kurap)
dan susah buang air besar (sembelit). Kulit buah ini pun biasa dibakar dan abunya
digunakan dalam ramuan untuk melancarkan haid dan menggugurkan kandungan.
Hak Cipta © milik UPN "Veteran" Jatim :
7
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
Abu dan air rendaman abu ini juga digunakan sebagai campuran pewarna
tradisional. Beberapa masyarakat di Jawa menggunakan kulit durian yang telah
dimakan sebagai pengusir (repellent) nyamuk dengan meletakkannya di sudut
ruangan. Kayu gubalnya berwarna putih dan terasnya kemerah-merahan. Ringan,
namun tidak begitu awet dan mudah diserang rayap. Biasa digunakan sebagai
perabot rumah, peti-peti pengemas, dan bahan konstruksi ringan di bawah atap,
asalkan tidak bersentuhan dengan tanah.
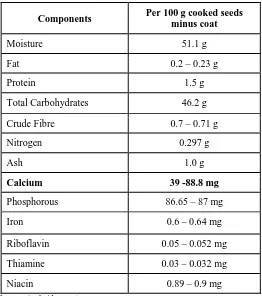
Tabel 2. Kandungan Pada Biji Durian
Components Per 100 g cooked seeds
minus coat
Moisture 51.1 g
Fat 0.2 – 0.23 g
Protein 1.5 g
Total Carbohydrates 46.2 g
Crude Fibre 0.7 – 0.71 g
Kalsium Karbonat (CaCO3)
Kalsium Karbonat yang digunakan dalam industri cat, karet dan kertas
harus mempunyai mutu yang tinggi, terutama kemurnian dan kehalusannya
(0,15-0,25 µ). Industri makanan, kosmetik, farmasi dan antibiotic dan mempunyai
Hak Cipta © milik UPN "Veteran" Jatim :
8
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
persyaratan yang lebih berat, misalnya kadar CaCO3 setelah dipanaskan pada suhu
200 oC selama 4 jam, tidak boleh kurang dari 98% dan zat pengotornya tidak
boleh lebih dari 2%, tidak menampakkan warna hijau pada tes nyala, adanya
logam berat tidak boleh lebih dari 30 bagian perjuta, magnesium dan garam alkali
tidak boleh lebih dari 5 mg pada setiap gr contoh dan bahan-bahan yang tidak
larut dalam asam tidak boleh lebih dari 10 mg/5 kg. Kalsium karbonat adalah
padatan putih yang hanya sedikit larut dalam air. Kalsium karbonat terurai bila
dipanaskan menghasilkan kalsium oksida dan karbondioksida. Senyawa ini
dijumpai di alam sebagai mineral kalsit dan argonit. Batuan mengandung kalsium
karbonat larut perlahan-lahan dalam air hujan asam dan mengakibatkan kesadahan
sementara. Di laboratorium, kalsium karbonat di endapkan dari air kapur dengan
karbondioksida, digunakan dalam pembuatan kapur dan merupakan bahan mentah
untuk proses solvey. Kalsium karbonat terdapat secara alami dalam 2 struktur
kristal, kalsit dan argonit. Kalsit secara thermodynamic stabil pada semua tekanan
dan suhu. Argonit polimorf itu menstabilkan dan tidak dapat berubah ke kalsit
ketika dipanaskan pada udara kering sampai 400 oC, laju meningkat dengan suhu
perubahan lebih cepat ketika kontak dengan air atau larutan yang mengandung
kalsium karbonat dan terjaga pada suhu kamar. Bentuk kristal dan kalsit adalah
sistem heksagonal. Ada lebih dari 60 kristal yang dibawa oleh kalsit dalam
kontras antara 10-15 untuk isostruktural karbonat lainnya. Argonit dalam sistem
ortorombik. Umumnya berbentuk kristal asikular atau prisma. Pada bentuk
komersial dari kalsium karbonat persipilasi dimana argonit tidak mendominasi,
kristal mempunyai sisi pararel dan panjang sampai rasio luas. Kalsium karbonat
Hak Cipta © milik UPN "Veteran" Jatim :
9
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
bila dipanaskan akan pecah dan menjadi serbuk remah yang lunak yang
dinamakan calsium oksida (CaO). Hal ini terjadi karena pada reaksi tersebut
setiap molekul dari kalsium akan bergabung dengan 1 atom oksigen dan molekul
lainnya akan berikatan dengan oksigen menghasilkan CO2 yang akan terlepas ke
udara sebagai gas karbondioksida. dengan reaksi sebagai berikut:
CaCO3 CaO + CO2
Reaksi ini akan berlanjut apabila ditambahkan air, reaksinya akan berjalan dengan
sangat kuat dan cepat apabila dalam bentuk serbuk, serbuk kalsium karbonat akan
melepaskan kalor. Molekul dari CaCO3 akan segera mengikat molekul air (H2O)
yang akan menbentuk kalsium hidroksida, zat yang lunak seperti pasta.
Sebagaimana ditunjukkan pada reaksi sebagai berikut:
CaCO3 + H2O Ca(OH)2 + CO2
Tabel 3. Spesifikasi CaCO3
Properti Kalsit Argonit
Densitas (kg/m3) (Kirk and Othmer, 1968)
Asam Sulfat (H2SO4)
Asam sulfat mempunyai rumus kimia H2SO4, merupakan asam mineral
(anorganik) yang kuat. Zat ini larut dalam air pada semua perbandingan. Reaksi
hidrasi (pelarutan dalam air) dari asam sulfat adalah reaksi eksoterm yang kuat.
Jika air ditambahkan ke asam sulfat pekat, terjadi pendidihan. Senantiasa
menambah asam kepada air dan bukan sebaliknya. Sebagian dari masalah ini
Dipanaskan, T = 600 oC
Hak Cipta © milik UPN "Veteran" Jatim :
10
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
disebabkan perbedaan isi padu kedua cairan. Air kurang padu dibanding asam
sulfat dan cenderung untuk terapung di atas asam. Reaksi tersebut membentuk ion
hidronium:
H2SO4 + H2O H3O+ + HSO4
-Hal ini disebabkan karena asam sulfat bersifat mengeringkan, asam sulfat
merupakan agen pengering yang baik, dan digunakan dalam pengolahan
kebanyakan buah-buahan kering. (http://id.wikipedia.org/wiki/asam_sulfat)
Asam sulfat adalah mineral yang sangat penting, diantaranya adalah
sebagai bahan penunjang bagi industri-industri baja, super phospat, industri
farmasi, cat, baterai, tekstil, pembuatan pupuk, pengolahan kulit dan pemurnian
produk petroleum serta industri semen. Umumnya asam sulfat diproduksi dengan
kadar 93-98% berat. Dengan kadar tersebut asam sulfat tampak terang seperti
minyak dan mempunyai berat jenis 1,4-1,8 kg/l, serta mudah bercampur dengan
air dalam segala keadaan. Asam sulfat merupakan asam kuat yang mempunyai
afinitas sangat besar terhadap air. Bila dicampur dengan air, akan menimbulkan
panas, karena terjadi reaksi eksotermis.
Sifat fisik:
a. Sangat korosif
b. Merupakan bahan pengikat pengoksida
c. Merupakan liquida berminyak
d. Merupakan sulfonating agent terhadap zat organik
Hak Cipta © milik UPN "Veteran" Jatim :
11
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
e. Sebagai oksidasi
f. Hydroskopis (mudah menyerap air)
g. Tidak berwarna sampai coklat kehitaman
Sifat kimia:
f. Kelarutan : larut dalam air pada berbagai perbandingan
g. Konduktansi : 1,04 gm (25 oC)
h. Viscositas : 0,2454 Pas (20 oC)
Kegunaan H2SO4:
‐ Sebagai bahan pembuatan pupuk
‐ Sebagai zat warna
‐ Industri penggilingan minyak bumi
‐ Industri cat
‐ Sebagai reagent dalam elektroplating
Hak Cipta © milik UPN "Veteran" Jatim :
12
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
‐ Sebagai katalis dalam reaksi kimia
(Kirk and Othmer, 1968)
Asam Oksalat (H2C2O4)
1. Asam Oksalat Anhidrat
Asam oksalat anhidrat mempunyai kristal rombik pyramid, tidak berbau dan
berwarna putih. Produk yang ditemui secara komersial adalah dyhidratnya
yaitu (COOH) 2H2O, yang berbentuk kristal monokline dengan perbandingan
71,42% anhidrat asam oksalat dan 28,58% air. Sedangkan sifat fisik dan
kimia dari asam oksalat adalah sebagai berikut:
Sifat fisik:
a. Berbentuk seperti jarum
b. Berwarna putih
e. Panas dekomposisi : 826,78 kJ/mol
Hak Cipta © milik UPN "Veteran" Jatim :
13
2. Asam Oksalat Dyhidrat
Sifat kimia:
‐ Sebagai pembersih kerak pada radiator mobil.
‐ Membersihkan noda tinta pada pakaian.
‐ Sebagai bahan pengecatan wol, pelenturan kulit dan pengecatan fiber dan
printing dari cotton di dalam industri tekstil.
(Kirk and Othmer, 1968)
II.2. Landasan
Teori
Pada pembuatan CaCO3, ada beberapa cara untuk mengikat kandungan
Ca2+ yang kemudian bisa didapatkan hasil menjadi CaCO3, antara lain:
1. Larutan Ammonia
Tidak ada endapan, karena kalsium hidroksida larut cukup banyak. Dengan
zat pengendap yang telah lama dibuat, mungkin timbul kekeruhan karena
terbentuknya kalsium karbonat.
Hak Cipta © milik UPN "Veteran" Jatim :
14
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
2. Larutan Ammonium Karbonat
Ca2+ + CO32- CaCO3
Dengan mendidihkan, endapan menjadi berbentuk Kristal. Endapan kuat
dalam air mengandung asam karbonat berlebihan misalnya, air soda yang
baru dibuat), karena pembentukan kalsium hidrogen karbonat yang larut.
CaCO3 + H2O + CO2 Ca2+ + 2HCO3
-Dengan mendidihkannya lagi, endapan akan muncul kembali. Hal ini
dikarenakan karbondioksida keluar selama proses terjadi. Ion-ion barium dan
strontium bereaksi serupa. Endapan larut dalam asam, termasuk asam asetat:
CaCO3 + 2H+ Ca2+ + H2O + CO2
CaCO3 + 2CH3COOH Ca2+ + H2O + CO2 + 2CH3COO
-Kalsium karbonat larut sedikit dalam larutan garam dari asam kuat.
3. Larutan Asam Sulfat
Adanya endapan putih kalsium sulfat.
Ca2+ + SO42- CaSO4
CaSO4 larut dalam air (0,61 gr Ca2+; 2,06 gr CaSO4 atau 2,61 gr CaSO4.2H2O
l-1; Ks = 2,3 x 10-4). Endapan melarut dalam asam sulfat pekat, panas:
CaSO4 + SO42- [Ca(SO4)2]
2-Hak Cipta © milik UPN "Veteran" Jatim :
15
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
Meskipun pelarutan dalam ammonium sulfat mungkin tak sempurna, ion-ion
kalsium dapat terdeteksi dalam filtrat dengan oksalat, setelah dinetralkan
dengan ammonia.
4. Larutan Ammonium Oksalat
Adanya endapan putih kalsium oksalat.
Ca2+ + (COO)22- Ca(COO)2
Pengendapan dipermudah dengan menjadikan larutan bersifat basa dengan
ammonia. Endapan praktis tidak larut dalam air (6,35 mg Ca(COO)2 l-1; Ks =
2,6 x 10-9) dan tidak larut dalam asam asetat.
5. Larutan Kalium Kromat
Tidak terjadi endapan dari larutan encer, tidak pula dari
larutan-larutan pekat dengan adanya asam asetat.
6. Larutan Kalium Heksanoferat (II)
Adanya endapan putih garam campuran.
Ca2+ + 2K+ + [Fe(CN)6]4- K2Ca[Fe(CN)6]
Dengan adanya ammonium klorida, akan menjadi lebih pekat. Dalam hal ini,
alium digantikan oleh ion-ion ammoniu. Uji ini dipakai untuk membedakan
kalsium dari strontium.
(G. Svehla, 1990)
Hak Cipta © milik UPN "Veteran" Jatim :
16
BAB I I
TI N JAU AN PU STAK A
Pembuat an K alsium K arbonat D ari Biji D urian M enggunakan H2SO4 dan H2C2O4
Pada pembuatan CaCO3 ini, digunakan larutan asam sulfat yang akan
membentuk CaSO4, yang selanjutnya menggunakan larutan asam oksalat untuk
membentuk CaC2O4, sehingga reaksi yang terjadi adalah:
1. Ca2+ + O2 CaO
2. CaO + H2SO4 CaSO4 + H2O
3. CaSO4 + H2C2O4 CaC2O4 + H2SO4
4. CaC2O4 CaCO3 + CO2 (dipanaskan 600 oC)
Selain itu, faktor-faktor yang mempengaruhi hasil penelitian untuk diperoleh hasil
yang optimum, adalah: waktu pencampuran, suhu pencampuran dan konsentrasi
Asam Oksalat (H2C2O4) sebagai pelarut. Berdasarkan penelitian yang pernah
dilakukan sebelumnya yang menggunakan bahan baku kulit jeruk, didapatkan
hasil yang optimum untuk waktu pencampuan (35 menit) dan suhu pencampuran
(100 oC).(Atik Widiati, 2005)
II.3. Hipotesis
Dilihat dari kandungan Ca (kalsium) dalam biji durian, maka biji durian
memungkinkan untuk diproses dan dimanfaatkan dalam pembuatan kalsium
karbonat (CaCO3). Penambahan asam oksalat dan asam sulfat sangat
mempengaruhi kadar kalsium karbonat (produk) yang dihasilkan.
Hak Cipta © milik UPN "Veteran" Jatim :
17
BAB I I I
PEL AK SANAAN PENEL I TI AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
BAB III
PELAKSANAAN PENELITIAN
III.1. Bahan yang Digunakan
1. Biji durian
2. Aquadest
3. Asam sulfat (H2SO4) 4 N
4. Asam oksalat (H2C2O4)
III.2. Alat yang Digunakan
1. Beaker glass
9. Timbangan neraca
10. Pipet
16. Magnetic Hot Plate Stirrer
Hak Cipta © milik UPN "Veteran" Jatim :
18
BAB I
PENDAHU L U AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
III.3. Variabel yang Digunakan
a. Variabel tetap
Berat abu : 10 gr
Suhu pengeringan biji durian dalam oven : 110 oC
Suhu pembakaran biji durian dalam furnace : 500 oC
Waktu pembakaran biji durian dalam furnace : 2 jam
Suhu di dalam furnace (pelepasan CO2) : 600 oC
Asam Sulfat (H2SO4) 4 N
‐ Temperatur pelarutan : 100 oC
‐ Waktu pelarutan : 10 menit
Asam Oksalat (H2C2O4)
‐ Temperature pelarutan : 100 oC
‐ Waktu pelarutan : 35 menit
b. Variable berubah
Konsentrasi H2C2O4 (% berat) : 10, 12, 14, 16, 18
H2SO4 4 N (ml) : 80, 90, 100, 110, 120
Hak Cipta © milik UPN "Veteran" Jatim :
19
BAB I
PENDAHU L U AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
III.4. Skema Penelitian
Endapan Abu Biji Durian Pembakaran
T = 500 oC t = 300 menit
Pemanasan dan Pengadukan T = 100 oC
t = 10 menit
Pemanasan dan Pengadukan T = 100 oC
Hak Cipta © milik UPN "Veteran" Jatim :
20
BAB I
PENDAHU L U AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
III.5. Prosedur Penelitian
1. Biji durian dipisahkan dari dagingnya dan kemudian dihancurkan sampai
berukuran kecil.
2. Biji durian yang sudah berukuran kecil tersebut dikeringkan dengan bantuan
oven untuk mengurangi kadar airnya, serta memudahkan pembakaran.
3. Setelah biji durian tersebut dikeringkan, dibakar dengan suhu 500 oC selama
5 jam hingga diperoleh abunya. Jika pada abu biji durian ada yang masih
kasar, maka harus ditumbuk dahulu sampai halus.
4. Kemudian timbang 10 gr abu biji durian yang kemudian ditambahkan asam
sulfat (H2SO4) 4 N dengan volume masing-masing 80 ml, 90 ml, 100 ml, 110
ml dan 120 ml.
5. Panaskan di atas thermostat pada suhu 100 oC sambil diaduk selama 10
menit, dan kemudian saring dengan kertas saring untuk diambil endapannya.
6. Endapan yang diperoleh didiamkan sampai terbentuk endapan putih (CaSO4).
7. Selanjutnya endapan tersebut ditambahkan asam oksalat (H2C2O4) dengan
konsentrasi berat 10%, 12%, 14%, 16% dan 18%.
8. Panaskan di atas thermostat pada suhu 100 oC sambil diaduk selama 35
menit, dan kemudian saring dengan kertas saring untuk diambil endapannya.
Hak Cipta © milik UPN "Veteran" Jatim :
21
BAB I
PENDAHU L U AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
9. Endapan yang diperoleh didiamkan sampai terbentuk endapan putih
(CaC2O4).
10. Endapan CaC2O4 tersebut dipanaskan di dalam furnace pada suhu 600 oC
selama 2 jam, sehingga menghasilkan CaCO3.
Hak Cipta © milik UPN "Veteran" Jatim :
22
BAB I
PENDAHU L U AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
III.6. Analisa Hasil
10 gr kalsium karbonat dilarutkan dengan menggunakan ammonium
oksalat 4% (jenuh) sebanyak 25 ml, yang kemudian diencerkan dengan aquadest
sebanyak 100 ml. Setelah itu diambil 10 ml dan ditambahkan dengan ± 10 ml
H2SO4 25%. Panaskan dengan suhu 70 oC, kemudian titrasi dengan KMnO4 0,1 N
sampai terjadi perubahan warna menjadi kemerah-merahan.
Gambar 1. Furnace Gambar 2. Magnetic Hot Plate Stirrer
Hak Cipta © milik UPN "Veteran" Jatim :
23
BAB I
PENDAHU L U AN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
Gambar 3. Rangkaian Alat Titrasi
Hak Cipta © milik UPN "Veteran" Jatim :
22
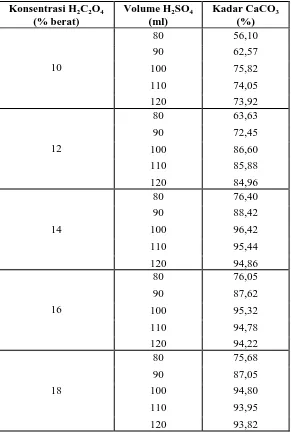
Tabel 4. Hasil Kadar CaCO3 terhadap perubahan
konsentrasi H2C2O4 dan volume H2SO4
Hak Cipta © milik UPN "Veteran" Jatim :
23
BAB I V
HASI L DAN PEM BAHASAN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
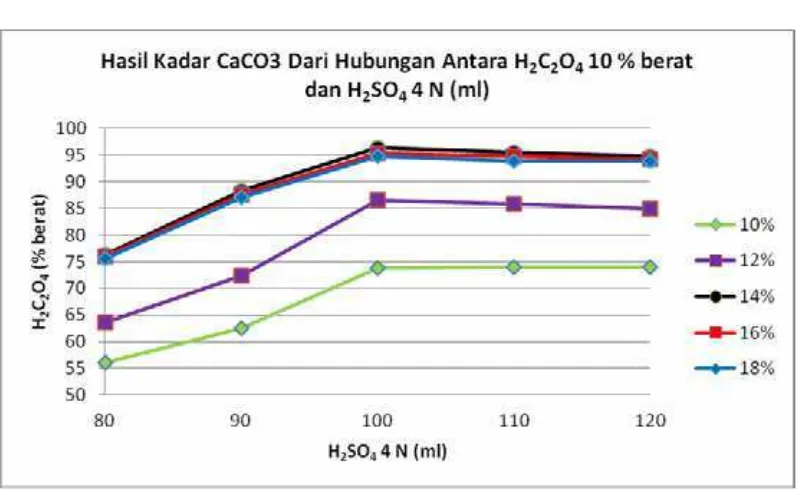
Gambar 4. Grafik hubungan antara H2C2O4 (% berat) dan
H2SO4 4 N (ml) terhadap kadar CaCO3
IV.2. Pembahasan
Dari hasil analisa pada suhu 100 oC dan waktu pencampuran 35 menit,
terlihat bahwa kadar kalsium karbonat (% CaCO3) tertinggi pada saat volume
asam sulfat 100 ml dan asam oksalat 14%, yaitu sebesar 96,42%.
Terlihat pada setiap garis grafik kadar kalsium karbonat mengalami
peningkatan dalam setiap kenaikan jumlah volume asam sulfat dan mengalami
penurunan setelah volume asam sulfat melewati 100 ml. Hal ini dikarenakan pada
penambahan volume asam sulfat 100 ml, merupakan ukuran optimum yang
digunakan untuk mengikat Ca membentuk CaSO4. Pada penambahan asam
oksalat, kadar kalsium karbonat akan mengalami kenaikan sampai mencapai hasil
optimum pada penambahan 14% asam oksalat dan mengalami penurunan ketika
Hak Cipta © milik UPN "Veteran" Jatim :
24
BAB I V
HASI L DAN PEM BAHASAN
Pembuatan K alsium K arbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
penambahan asam oksalat melebihi 14% berat. Hal ini dikarenakan Ca hanya
membutuhkan asam oksalat dengan kadar 14% berat untuk membentuk CaCO3,
atau dapat dikatakan jumlah Ca yang akan diikat sebanding atau ekuivalen dengan
14% asam oksalat. . (Day & Underwood, page 154)
Jika dibandingkan dengan penelitian sebelumnya yang telah dilakukan
yang menggunakan bahan baku dari kulit jeruk dengan variabel yang berbeda (Atik
Widiati, 2005), hasil CaCO3 yang diperoleh sebesar 93,27%. Sedangkan yang
menggunakan bahan baku biji durian sebesar 96,42%. Dapat dilihat bahwa produk
bahan baku biji durian mempunyai kandungan CaCO3 yang lebih besar
dibandingkan dengan menggunakan bahan baku kulit jeruk. Hal ini dikarenakan
kandungan Ca yang ada pada kulit jeruk lebih sedikit dibandingkan dengan biji
durian. Disini juga dapat dilihat, bahwa kandungan kalsium karbonat mengalami
peningkatan dalam setiap kenaikan jumlah volume asam sulfat dan mengalami
penurunan setelah volume asam sulfat melewati 100 ml dan mencapai hasil
optimum pada penambahan 14% asam oksalat. Hal ini memperlihatkan, bahwa
dengan menggunakan berbagai macam bahan baku yang mempunyai kandungan
kalsium, hasil optimum kandungan CaCO3 tetap diperoleh dengan kondisi volume
asam sulfat 100 ml dan asam oksalat 14%.
Hak Cipta © milik UPN "Veteran" Jatim :
26
BAB V
KESI M PU L AN DAN SARAN
Pembuatan Kalsium Karbonat Dari Biji Durian M enggunakan H2SO4 dan H2C2O4
BAB V
KESIMPULAN DAN SARAN
V.1. Kesimpulan
1. Biji durian dapat dimanfaatkan menjadi kalsium karbonat, dengan cara
mengambil kandungan kalsiumnya kemudian direaksikan dengan asam sulfat
dan asam oksalat.
2. Kondisi optimum yang diperoleh pada proses pembuatan CaCO3 dari 10 gr
biji durian adalah sebesar 96,42% saat dilarutkan dalam 100 ml H2SO4 4 N
dan 14% berat H2C2O4.
V.2. Saran
Penelitian terhadap biji durian ini diharapkan memberikan inspirasi bagi
peneliti lainnya untuk melakukan penelitian terhadap bahan baku lainnya. Yang
dimungkinkan untuk bisa diproses menjadi kalsium karbonat.
Hak Cipta © milik UPN "Veteran" Jatim :
viii
DAFTAR PUSTAKA
Achmad Djaeni S., Prof. Dr. MSc., 2000, “Ilmu Gizi”, Dian Rakyat, Jakarta.
Hawlexx G. G., “The Condensat Chemical Dictionary”, 9th edition.
Hendro Sunarjono, Drs., 1990, “Ilmu Produksi Tanaman Buah-Buahan”, Sinar Baru, Bandung.
http://venuskomputer.wordpress.com, 2004.
http://isjd.pdii.lipi.go.id, 2001.
http://id.wikipedia.org/wiki/durian, 1995.
Day & Underwood, 1986, “Quantitative Analysis”, 4th edition.
Othmer, Kirk, 1968, “Encyclopedia of Chemical Thecnology”, volume 4, 2nd edition.
Svehla, G., 1990, “Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro VOGEL”, PT. Kalman Medika Pusaka, Jakarta.
Tim Penulis, PS., 1994, “Peluang Usaha dan Pembudidayaan Buah Durian”, PT. Penebar Swadaya, Jakarta.
Widiati, Atik, 2005, “Pembuatan Kalsium Karbonat Dari Kulit Buah Jeruk Siam Dengan Menggunakan Asam Sulfat Dan Asam Oksalat”, UPN Veteran Jatim, Surabaya.
Hak Cipta © milik UPN "Veteran" Jatim :