xiv INTISARI
Empat puluh tahun terakhir, insektisida digunakan dalam pengendalian vektor Demam Berdarah Dengue (DBD) di Indonesia. Sebagai akibatnya, Ae. aegypti di beberapa daerah Indonesia, menjadi resisten terhadap insektisida. Enzim esterase memegang peran pendetoksifikasian insektisida sehingga semua insektisida yang masuk akan dihidrolisis menjadi senyawa yang kurang beracun .
Tujuan penelitian ini adalah mengetahui profil esterase non-spesifik nyamuk Ae. aegypti (subjek penelitian) dari Simpang III Sipin (daerah endemis DBD) dan Sijenjang (daerah non-endemis DBD), dengan metode elektroforesis. Penelitian ini termasuk penelitian non-eksperimental dengan rancangan deskriptif dan analitik.
Zymogram dianalisis secara kualitatif, yaitu dengan membandingkan intensitas warna pola pita zymogram nyamuk subjek penelitian dengan kontrol, menghitung kecepatan gerak (jarak) esterase non-spesifik dalam medan listrik (Rf) dan analisis menggunakan Chi-square (p < 0,05).
Dari analisis menggunakan Chi-square (p < 0,05), menunjukkan adanya perbedaan aktivitas esterase non spesifik nyamuk dari Sijenjang dengan Simpang III Sipin. Untuk hasil perhitungan Rf pita 1, 2 dan 3, antara nyamuk dari Sijenjang dengan Simpang III Sipin dan kontrol hanya pita 3 yang terdapat perbedaan, namun ketiganya tidak menunjukkan perubahan yang berarti pada komposisi protein penyusun esterase non-spesifik pada nyamuk perlakuan maupun kontrol. Hasil analisis kualitatif diperoleh intensitas warna pola pita nyamuk Ae. aegypti dari Simpang III Sipin lebih pekat dan Sijenjang intensitas warnanya lebih terang dibandingkan kontrol.
xv ABSTRACT
The use of insecticide to control Dengue Haemorrhagic Fever (DHF) vector in Indonesia during the last 40 years resulted in the resistency of the insect toward insecticides, including Ae. aegypti in some areas in Indonesia. Esterase enzyme has its main part in this insecticide detoxification became untoxic substance.
This study was aimed to the profile description of non-specific esterase of Ae. aegypti (research subject) from Simpang III Sipin (DHF endemic area) and Sijenjang (DHF non-endemic area) by using electrophoresis method. This study was non experimental research with descriptive and analytical design.
Zymogram was analyzed qualitative. The former was carried out by comparing the stained intensity the banding pattern of zymogram between the research subject mosquito and the controlled ones, by calculating the moving speed (distance) of esterase in electric current (Rf), and analyzed by Chi-square (p < 0.05).
Ae. aegypti from Simpang III Sipin and Sijenjang had different activities of esterase based on the used of Chi-square (p<0.05). The result of Rf calculation on the first, second and third band between Sijenjang with Simpang III Sipin mosquito and the controlled mosquito, only on the third band showed difference, but it was proof that there was no change on the composition of the protein in non-specific esterase both to the treated mosquito and the controlled ones. The banding pattern of Ae. aegypti from Simpang III Sipin showed high intensity and from Sijenjang showed low intensity, if its compared to the control.
PROFIL ESTERASE NON SPESIFIK NYAMUK Aedes aegypti
DARI DAERAH ENDEMIS DAN NON ENDEMIS DBD KOTA
JAMBI DENGAN METODE ELEKTROFORESIS
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh : Victoria Hapsari NIM : 028114117
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
iv
i asked for strength…
and GOD gave me difficulties to make me strong
i asked for wisdom…
and GOD gave me problem to solve
i asked for courage…
and GOD gave me obstacle to overcome
i
asked
GOD
for
favors
and GOD gave me opportunities
i received nothing i wanted…
but i received everything i needed
Lord knows
Dreams are hard to follow
But don't let anyone
Tear them away
Hold on
There will be tomorrow
In time
You'll find the way
(
Mariah Carey _Hero)
Syukur dan terima kasih kepada Tuhan Maha Pengasih atas terselesaikannya skripsi “Profil Isoenzim Esterase Non Spesifik Nyamuk Aedes aegypti Dari Daerah Endemis Dan Non Endemis DBD Kota Jambi Dengan Metode Elektroforesis” ini, guna memenuhi salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm) program studi Ilmu Farmasi.
Semua keberhasilan ini tidak lepas pula dari bantuan berbagai pihak, yang telah berjasa membantu hingga terselesaikannya skripsi ini. Untuk itu, penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Ibu Rita Suhadi, M.Si, Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Dr. Budi Mulyaningsih, M.S., Apt., selaku dosen pembimbing dan dosen penguji skripsi yang telah meluangkan waktu dan perhatian dengan penuh kesabaran membimbing sampai selesainya skripsi ini.
3. Bapak Drs. Mulyono, Apt., dan Bapak Dr. Sabikis, Apt., selaku dosen penguji skripsi yang telah banyak memberi masukan kepada penulis.
4. Kepala BAPEDA Propinsi Daerah Istimewa Yogyakarta, Kepala Badan Kesbang dan Linmas Kota Jambi, dan Kepala Dinas Kesehatan Kota Jambi yang telah mengijinkan penulis melakukan penelitian di Kota Jambi dan memberikan data yang dibutuhkan penulis.
5. Bapak Purwono selaku laboran Bagian Parasitologi Fakultas Kedokteran Universitas Gajah Mada yang membantu pelaksanaan penelitian skripsi.
Nicholas Aryo Bimo Wuryanto dan Moses Amor Deo Wuryanto yang selalu mendoakan, memberi dorongan serta kasih selama pengerjaan skripsi ini.
7. Yusuf Firmanta dan keluarga, atas kasih, kesetiaan serta bantuan yang telah diberikan hingga terselesaikannya skripsi ini.
8. Semua teman, sahabat tercinta, atas persahabatan, pengertian dan dukungannya selama ini serta bantuan infomasi yang sangat membantu.
9. Semua pihak yang telah membantu dalam penelitian ini dan tidak dapat disebutkan satu per satu.
Penulis menyadari bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan. Oleh karena itu, segala saran dan kritik yang bersifat membangun sangat penulis harapkan.
Yogyakarta, Juli 2007
Penulis
viii DAFTAR ISI
Hal.
HALAMAN JUDUL………..………... i
HALAMAN PERSETUJUAN...………... ii
HALAMAN PENGESAHAN………..………... iii
HALAMAN PERSEMBAHAN..………... iv
PERNYATAAN KEASLIAN KARYA……… v
KATA PENGANTAR... vi
DAFTAR ISI………... viii
DAFTAR TABEL………... xi
DAFTAR GAMBAR………... xii
DAFTAR LAMPIRAN………... xiii
INTISARI……….. xiv
ABSTRACT……….. xv
BAB I PENGANTAR………. 1
A. Latar Belakang………... 1
B. Permasalahan………...……….………... 4
C. Keaslian Karya…...………...………... 5
D. Manfaat Penelitian………...…….………... 5
E. Tujuan Penelitian……….………... 6
ix
A. Demam Berdarah Dengue ...………... 7
B. Nyamuk Ae. aegypti...………... 8
1. Kedudukan Taksonomi Nyamuk Ae. aegypti... 8
2. Morfologi Nyamuk Ae. aegypti... 9
3. Siklus hidup Nyamuk Ae. aegypti... 12
C. Pengendalian Vektor………...… 14
D. Insektisida... 15
E. Mekanisme Resistensi Serangga Terhadap Insektisida... 19
F. Enzim Esterase Non-Spesifik……… 21
G. Elektroforesis... 24
H. Landasan Teori... 27
I. Keterangan Empiris... 27
BAB III METODOLOGI PENELITIAN... 28
A. Jenis dan Rancangan Penelitian………... 28
B. Subjek Penelitian………. 28
B. Definisi Operasional………... 29
C. Bahan dan Alat Penelitian……...………... 30
1. Bahan Penelitian……….. 30
2. Alat Penelitian……….. 30
E. Jalannya Penelitian………... 30
F. Analisis Hasil……….………...…... 35
x
BAB V. KESIMPULAN DAN SARAN... 46
A. Kesimpulan... 46
B. Saran... 46
DAFTAR PUSTAKA... 48
LAMPIRAN... 53
xi
DAFTAR TABEL
Halaman Tabel I. Jumlah bahan yang digunakan dalam pembuatan gel
bawah... 32 Tabel II. Jumlah bahan yang digunakan dalam pembuatan gel
atas... 33 Tabel III. Enzim esterase non-spesifik dan jumlah pita yang
dihasilkan dari kelompok nyamuk Ae. aegypti yang berasal dari Kelurahan Simpang III Sipin (daerah endemik DBD), Kelurahan Sijenjang (daerah non-endemik DBD), dan Salatiga sebagai kontrol...
42
Tabel IV. Kecepatan gerak (jarak) isoenzim esterase non-spesifik dalam medan listrik (Rf) setiap pita yang terdapat pada zymogram hasil elektroforesis untuk setiap kelompok nyamuk Ae. aegypti yang berasal dari Kelurahan Simpang III Sipin (daerah endemik DBD), Kelurahan Sijenjang (daerah non-endemik DBD), dan Salatiga sebagai
kontrol...
xii
DAFTAR GAMBAR
Halaman Gambar 1. Telur nyamuk Ae. aegypti... 9 Gambar 2. Perbedaan gigi sisir pada larva Ae. aegypti dengan Ae.
albopictus dan Ae. Scutellaris...
10
Gambar 3. Larva nyamuk Ae. aegypti... 10 Gambar 4. Pupa nyamuk Ae. aegypti... 11 Gambar 5. Perbedaan toraks nyamuk Ae. aegypti (A) dan Ae.
albopictus (B)... 12 Gambar 6. Siklus hidup nyamuk Ae. aegypti... 13 Gambar 7. Reaksi metabolisme atau detoksifikasi cypermetrin
dalam tubuh serangga atau mamalia oleh enzim esterase.. 22 Gambar 8. Zymogram isoenzim esterase non-spesifik dari kelompok
nyamuk Ae. aegypti daerah endemis (3), daerah non endemis (2), dan kontrol (1) yang ditandai dengan E1
xiii
DAFTAR LAMPIRAN
Halaman Lampiran 1. Surat Ijin Penelitian dari BAPEDA Yogyakarta... 53 Lampiran 2. Surat Ijin Penelitian dari KESBANGLIMAS Kota
Jambi... 54 Lampiran 3. Surat pernyataan pemberantasan nyamuk di Kota Jambi
tahun 2005-2006... 55 Lampiran 4. Data kasus penyakit DBD di Kota Jambi tahun
2003-2005... 56 Lampiran 5. Perhitungan kecepatan gerak isoenzim esterase
non-spesifik dalam medan listrik (Rf)... 58 Lampiran 6. Perhitugan analisis data frekunsi elektromorf dengan
menggunakan analisis Chi-square (perhitungan tabel kontingensi 2x2 (rxc) untuk pola zymogram
xiv INTISARI
Empat puluh tahun terakhir, insektisida digunakan dalam pengendalian vektor Demam Berdarah Dengue (DBD) di Indonesia. Sebagai akibatnya, Ae. aegypti di beberapa daerah Indonesia, menjadi resisten terhadap insektisida. Enzim esterase memegang peran pendetoksifikasian insektisida sehingga semua insektisida yang masuk akan dihidrolisis menjadi senyawa yang kurang beracun .
Tujuan penelitian ini adalah mengetahui profil esterase non-spesifik nyamuk Ae. aegypti (subjek penelitian) dari Simpang III Sipin (daerah endemis DBD) dan Sijenjang (daerah non-endemis DBD), dengan metode elektroforesis. Penelitian ini termasuk penelitian non-eksperimental dengan rancangan deskriptif dan analitik.
Zymogram dianalisis secara kualitatif, yaitu dengan membandingkan intensitas warna pola pita zymogram nyamuk subjek penelitian dengan kontrol, menghitung kecepatan gerak (jarak) esterase non-spesifik dalam medan listrik (Rf) dan analisis menggunakan Chi-square (p < 0,05).
Dari analisis menggunakan Chi-square (p < 0,05), menunjukkan adanya perbedaan aktivitas esterase non spesifik nyamuk dari Sijenjang dengan Simpang III Sipin. Untuk hasil perhitungan Rf pita 1, 2 dan 3, antara nyamuk dari Sijenjang dengan Simpang III Sipin dan kontrol hanya pita 3 yang terdapat perbedaan, namun ketiganya tidak menunjukkan perubahan yang berarti pada komposisi protein penyusun esterase non-spesifik pada nyamuk perlakuan maupun kontrol. Hasil analisis kualitatif diperoleh intensitas warna pola pita nyamuk Ae. aegypti dari Simpang III Sipin lebih pekat dan Sijenjang intensitas warnanya lebih terang dibandingkan kontrol.
xv ABSTRACT
The use of insecticide to control Dengue Haemorrhagic Fever (DHF) vector in Indonesia during the last 40 years resulted in the resistency of the insect toward insecticides, including Ae. aegypti in some areas in Indonesia. Esterase enzyme has its main part in this insecticide detoxification became untoxic substance.
This study was aimed to the profile description of non-specific esterase of Ae. aegypti (research subject) from Simpang III Sipin (DHF endemic area) and Sijenjang (DHF non-endemic area) by using electrophoresis method. This study was non experimental research with descriptive and analytical design.
Zymogram was analyzed qualitative. The former was carried out by comparing the stained intensity the banding pattern of zymogram between the research subject mosquito and the controlled ones, by calculating the moving speed (distance) of esterase in electric current (Rf), and analyzed by Chi-square (p < 0.05).
Ae. aegypti from Simpang III Sipin and Sijenjang had different activities of esterase based on the used of Chi-square (p<0.05). The result of Rf calculation on the first, second and third band between Sijenjang with Simpang III Sipin mosquito and the controlled mosquito, only on the third band showed difference, but it was proof that there was no change on the composition of the protein in non-specific esterase both to the treated mosquito and the controlled ones. The banding pattern of Ae. aegypti from Simpang III Sipin showed high intensity and from Sijenjang showed low intensity, if its compared to the control.
BAB I PENGANTAR
A. Latar Belakang
Demam Berdarah Dengue (DBD), adalah penyakit yang kemungkinan
besar menyebabkan kematian, pertama kali dilaporkan pada tahun 1950-an saat
epidemik dengue di Filipina dan Thailand. Penyakit ini sekarang endemik pada
lebih dari 100 negara di Afrika, Amerika, Timur Tengah, Asia Tenggara dan
Pasifik Barat. Asia Tenggara dan Pasifik Barat merupakan wilayah yang paling
serius terpengaruh. Sebelum tahun 1970, hanya 9 negara yang terjangkit epidemik
DBD, angka menjadi bertambah lebih dari 4 kali lipat pada tahun 1985. World
Health Organization (WHO) menaksir sekitar 50 juta kasus infeksi dengue dari seluruh dunia setiap tahunnya (Anonim, 2002a).
Di Indonesia, penyakit dengue merupakan masalah kesehatan masyarakat
utama setiap tahunnya dan penyebab siklus epidemik di daerah perkotaan.
Penyakit ini merupakan penyebab utama anak-anak dirawat inapkan dan
meninggal. Secara terus-menerus epidemik telah dicatat terjadi diantara bulan
Januari dan Juni. Selama epidemik di tahun sebelumnya, kasus terbesar dicatat
lebih dari 40.000 pada tahun 1988, 1996, 1998, 2001, 2003 dan 2004, pada tahun
1998 mencapai 72.133 kasus dan tahun 2004 mencapai 69.017 kasus. Pada tahun
2004, ditegaskan bahwa kasus dengue dilaporkan dari Propinsi Aceh, Jambi,
Banten, Jawa Barat, Jawa Tengah, Yogyakarta, Jawa Timur, Kalimantan Selatan,
Penyakit DBD ditularkan oleh nyamuk Aedes aegypti. Virus dengue
dipindahkan dari satu orang ke orang lain bersama air liur nyamuk pada waktu
nyamuk menghisap darah (Sungkar, 2005). Mengingat sampai saat sekarang
belum diketemukan vaksin untuk membunuh virus dengue, penanggulangan
penyakit ini berupa perawatan penderita dan pengendalian vektornya (Munif,
1997a). Pengendalian Ae. aegypti sebagai vektor utama DBD dapat dilakukan
dengan berbagai metode di antaranya dengan sanitasi lingkungan, yang bertujuan
untuk mengurangi habitat larva (source reduction), pemberantasan dengan
menggunakan insektisida baik ditujukan pada nyamuk dewasa maupun larvanya
(Munif, 1997b).
Selama 40 tahun terakhir, bahan kimia telah digunakan secara luas untuk
mengontrol nyamuk dan serangga lainnya sebagai kepentingan kesehatan
masyarakat. Sebagai akibatnya, Ae. aegypti dan vektor dengue lainnya di beberapa
negara telah menjadi resisten terhadap insektisida yang umum digunakan termasuk
temephos, malathion, fenthion, permethin, propoxur dan fenitrothion (Anonim,
1999). Seperti yang dilaporkan oleh Georghiou dan Mellon (1983) cit.
Mardihusodo (1995), resistensi vektor terhadap insektisida telah terus menerus
menyebar dan mempengaruhi program pengendalian penyakit di banyak negara.
Data mengenai pemberantasan penyakit DBD dari Dinas Kesehatan Kota
Jambi (2006a), menunjukan bahwa telah dilakukan pengendalian vektor DBD,
yaitu nyamuk Ae. aegypti, dengan pengasapan menggunakan insektisida Cynoff.
untuk sebagian hama rumah tangga (Anonim, 1993). Pada semua piretroid
mempunyai beberapa ciri umum, yaitu molekul asam, ikatan utama ester dan
molekul alkohol (Shafer, Meyer and Crofton, 2005).
Esterase adalah enzim yang memecah ikatan ester dengan cara hidrolisis
(Poedjiadi, 1994). Isoenzim esterase non-spesifik telah banyak dipelajari secara
luas, sebab dapat digunakan sebagai indikator perbedaan geografis dan pada
beberapa spesies berkaitan dengan mekanisme terjadinya resistensi terhadap
insektisida (Tabachnick & Powell, 1979 cit Marvdashti, 1985).
Aplikasi insektisida pada nyamuk akan menyeleksi gen-gen resistensi yang
mengatur derajat resistensi yang terkait dengan enzim esterase yang
mendetoksifikasi bahan insektisida tersebut. Peningkatan aktivitas enzim esterase
akan menaikkan dosis letal menjadi subletal yang tidak lagi mematikan serangga
yang menjadi sasaran (Mardihusodo, 1996).
Elektroforesis gel poliakrilamida telah digunakan untuk penelitian variasi
esterase pada populasi Aedes albopictus Skuse dari beberapa daerah endemis dan
non endemis DBD di Indonesia. Hasil dari elektroforesis setiap populasi Ae.
albopictus menunjukkan pola pita isoenzim esterase yang berbeda (Mulyaningsih, 2002). Dari penelitian sebelumnya dengan menggunakan elektroforesis lapis tipis,
Yasutomi (1983) cit Mardihusodo (1996) melaporkan aktivitas esterase pada 4
spesies nyamuk Culex pipiens, Cx. pipiens fatigan, Cx. tritaeniorrhynchus, dan Ae.
terhadap insektisida dibandingkan dengan koloni nyamuk yang masih rentan pada
spesies yang sama.
Berdasarkan data Dinas Kesehatan Kota Jambi (2006b), dari tahun
2003-2005 terdapat 7 Kelurahan yang termasuk daerah non-endemis DBD yaitu
Kelurahan Teluk Kenali, Sijenjang, Tanjung Raden, Pasir Panjang, Jelmu,
Kampung Tengah, dan 1 daerah endemis DBD yaitu Kelurahan Simpang III Sipin.
Dari 7 Kelurahan yang termasuk daerah non-endemis, diambil secara acak 1
Kelurahan sebagai daerah non-endemis, yaitu Kelurahan Sijenjang. Selama 3
tahun berturut-turut, Kelurahan Simpang III Sipin yang merupakan daerah
endemis DBD, telah terjadi 37 kasus, sedangkan Kelurahan Sijenjang, tidak
terdapat kasus DBD.
Dengan adanya kenyataan tersebut di atas maka perlu dilakukan penelitian
profil esterase non-spesifik dengan menggunakan metode elektroforesis untuk
nyamuk Ae. aegypti yang berasal dari daerah endemis dan non-endemis DBD Kota
Jambi. Dari gambaran profil isoenzim esterase non-spesifik ini diharapkan dapat
memprediksi mekanisme dan tingkat resistensi nyamuk tersebut terhadap
insektisida yang biasa digunakan dalam pengendalian vektor penyakit DBD.
B. Permasalahan
Bagaimanakah gambaran profil esterase non-spesifik dari masing-masing
populasi nyamuk Ae. aegypti yang berasal dari daerah endemis dan non-endemis
C. Keaslian Penelitian
Berdasarkan sumber-sumber informasi yang diperoleh, penelitian ilmiah
tentang profil esterase non-spesifik dengan menggunakan metode elektroforesis
pada nyamuk Aedes sudah pernah dilakukan di beberapa daerah, namun penelitian
tentang penentuan profil esterase non spesifik pada nyamuk Ae. aegypti yang
berasal dari daerah endemis dan non-endemis DBD Kota Jambi dengan metode
elektroforesis belum pernah dilakukan.
D. Manfaat Penelitian Manfaat dari penelitian ini adalah:
1. Manfaat teoritis, menambah khasanah ilmu pengetahuan dan kesehatan
terutama mengenai gambaran profil esterase non-spesifik pada nyamuk Ae.
aegypti dalam kaitannya dengan pemilihan insektisida yang efektif untuk usaha pengendalian vektor penyakit DBD.
2. Manfaat praktis, memberikan data dasar gambaran profil esterase non-spesifik
dari masing-masing populasi nyamuk Ae.aegypti yang berasal dari daerah
endemis dan non endemis DBD Kota Jambi, dalam hal ini dapat memberikan
gambaran secara tidak langsung mengenai status resistensinya terhadap
E. Tujuan Penelitian
Tujuan penelitian ini adalah untuk memperoleh data dasar gambaran profil
esterase non-spesifik, masing-masing populasi nyamuk yang berasal dari daerah
BAB II
PENELAAHAN PUSTAKA
A. Demam Berdarah Dengue
Penyakit Demam Berdarah Dengue (DBD) atau Dengue Haemorrhadic Fever (DHF) merupakan penyakit akibat infeksi virus dengue yang masih menjadi masalah kesehatan masyarakat. Penyakit ini ditemukan hampir di seluruh dunia terutama negara-negara tropik dan subtropik baik sebagai penyakit endemik maupun epidemik. Kejadian Luar Biasa pertama penyakit ini terjadi di Jakarta dan Surabaya pada tahun 1968 dengan ditemukannya 54 kasus dan 24 (44%) kasus diantaranya meninggal dunia. Setelah itu, jumlah kasus akibat terinfeksi virus dengue yang dilaporkan meningkat secara tajam. Pada tahun 1994, penyakit akibat infeksi virus dengue ini telah menyebar ke seluruh propinsi di Indonesia dan bahkan sejak tahun 2001 telah menjadi suatu penyakit endemik di beberapa kota besar dan kecil, bahkan di daerah pedesaan (Djunaedi, 2006).
Nyamuk Ae. aegypti adalah salah satu nyamuk vektor yang paling efisien untuk arbovirus, karena nyamuk ini sangat antropofilik dan hidup dekat manusia dan sering hidup di dalam rumah. Wabah dengue juga dapat terjadi dengan adanya nyamuk Ae. albopictus, Ae. polynesiensis, dan banyak spesies kompleks Ae. scutellaris. Setiap spesies ini mempunyai distribusi geografisnya masing-masing, namun mereka adalah vektor epidemia yang kurang efisien dibanding Ae. aegypti (Anonim, 1999).
yang dikenal dengan nama PSN (Pemberantasan Sarang Nyamuk) atau 3M (Menguras, Menutup dan Mengubur/Menyingkirkan tempat penampungan air). Pencegahan terhadap serangan infeksi virus dengue dengan memanfaatkan vaksin dengue nampaknya belum menunjukkan yang diharapkan (Djunaedi, 2006).
B. Nyamuk Ae. aegypti
Nyamuk Ae. aegypti telah dikenal sejak lama oleh orang sebagai penyebar virus dengue penyebab penyakit DBD. Nyamuk ini ditemukan pertama kali di Mesir (Egypt) pada tahun 1762 oleh Linnaeus. Nyamuk Ae. aegypti sekarang ditemukan di negara-negara yang terletak di antara garis 45 Lintang Utara dan garis 35 Lintang Selatan (Wulandari, 2001).
1. Kedudukan taksonomi nyamuk Ae. aegypti
Menurut Gandahusada, Ilahude dan Pribadi (1998), Ae. aegypti termasuk dalam:
Filum : Arthropoda Kelas : Hexapoda/Insekta Anak kelas : Pterygota
Bangsa : Diptera Anak bangsa : Nematocera Suku : Culicidae Anak suku : Culicinae Marga : Aedes
2. Morfologi nyamuk Ae. aegypti a. Telur
Telur Aedes berbentuk lonjong dengan kedua ujung sedikit lancip dan berdinding yang menggambarkan anyaman kain kasa (Gandahusada, et al., 1998). Pada waktu diletakkan telur bewarna putih, 15 menit kemudian telur menjadi abu-abu dan setelah 40 menit menjadi hitam.
Di bawah mikroskop susunan permukaan telur tampak seperti sarang tawon. Telur diletakkan satu persatu di dinding tempat penampungan air (TPA) 1-2 cm di atas permukaan air. Air di dalam tempat tersebut adalah air jernih dan terlindung dari cahaya matahari langsung. Tempat air di dalam rumah lebih disukai dari pada di luar rumah, dan tempat air yang lebih dekat rumah lebih disukai dari pada yang lebih jauh dari rumah. Telur dapat bertahan sampai 6 bulan (Sungkar, 2005).
Gambar 1. Telur Ae. aegypti (Mortimer, 1998)
b. Larva
khas yaitu pelana yang terbuka pada segmen anal, sepasang bulu pada sifon, dan gigi sisir yang berduri lateral pada segmen abdomen ke-7 (Sungkar, 2005).
Larva Ae. aegypti bergerak sangat lincah dan sangat sensitif terhadap rangsang getaran dan cahaya. Bila ada rangsangan, larva segera menyelam selama beberapa detik kemudian muncul kembali ke permukaan air. Larva mengambil makanannya di dasar TPA sehingga disebut pemakan makanan di dasar (bottom feeder). Pada saat larva mengambil oksigen dari udara, larva menempatkan sifonnya di atas permukaan air sehingga abdomennya terlihat menggantung pada permukaan air (Sungkar, 2005).
Gambar 2. Perbedaan gigi sisir pada larva Ae. aegypti dengan Ae. albopictus dan Ae. Scutellaris (Mardihusodo, 1990)
Gambar 3. Larva Ae. aegypti (Anonim, 2002c)
c. Pupa
bagian distal abdomen ditemukan sepasang kaki pengayuh yang lurus dan runcing. Jika terganggu, pupa akan bergerak cepat untuk menyelam selama beberapa detik kemudian muncul kembali ke permukaan air (Sungkar, 2005).
Gambar 4. Pupa Ae. aegypti (Anonim, 2002c)
d. Nyamuk dewasa
Bagian tubuh nyamuk dewasa terdiri atas kepala, toraks dan abdomen (Sungkar, 2005). Ae. aegypti dewasa berukuran lebih kecil jika dibandingkan dengan ukuran nyamuk rumah (Culex quinquefasciatus), mempunyai warna dasar yang hitam dengan bintik-bintik putih pada bagian-bagian badannya terutama pada kakinya (Gandahusada, et al., 1998).
gambaran lyre, sedangkan nyamuk Ae. albopictus terdapat satu garis longitudinal..
Gambar 5. Perbedaan toraks nyamuk Ae. aegypti (A) dan Ae. albopictus (B)(Grantham, 1999)
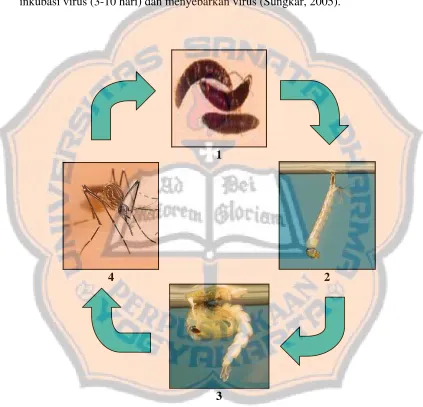
3. Siklus hidup nyamuk Ae. aegypti
Nyamuk Ae. aegypti dalam siklus hidupnya mengalami metamorfosa lengkap (holometabola), sebagaimana serangga lain dalam Ordo Diptera. Stadium yang dialami meliputi stadium telur, larva, pupa dan dewasa (Wulandari, 2001).
Nyamuk betina meletakkan telurnya pada dinding tempat perindukannya. Seekor nyamuk betina dapat meletakkan rata-rata sebanyak 100 butir telur tiap kali bertelur (Gandahusada, et.al, 1998). Telur dapat bertahan sampai berbulan-bulan pada suhu -2°C sampai 42°C. namum bila kelembaban terlampau rendah, maka telur akan menetas dalam waktu 4 hari (Soedarmono, 1988).
menjadi kaku dan kuat sehingga nyamuk mampu terbang untuk menghisap darah manusia dan kawin sehari atau 2 hari sesudah keluar dari pupa. Umumnya nyamuk betina akan mati dalam 10 hari, tetapi masa tersebut cukup bagi nyamuk untuk inkubasi virus (3-10 hari) dan menyebarkan virus (Sungkar, 2005).
1
4 2
3
Gambar 6. Siklus hidup nyamuk Aedes. aegypti (Mortimer, 1998; Anonim, 2002c; Grantham, 1999)
Keterangan : 1. telur 2. larva 3. pupa 4. dewasa
DBD, yaitu Kelurahan Simpang III Sipin dan 7 Kelurahan yang merupakan daerah non endemis, yaitu Kelurahan Teluk Kenali, Sijenjang, Tanjung Raden, Pasir Panjang, Ulu Gedong, Jelmu dan Kampung Tengah. Pada penelitian kali ini, Kelurahan Sijenjang ditetapkan sebagai daerah non endemis. Dari kedua daerah yang telah ditetapkan sebagai daerah endemis dan non endemis tersebut, telur dan larva Ae. aegypti kemudian dikoleksi.
C. Pengendalian Vektor
Obat dan vaksin untuk memberantas DBD hingga saat ini belum tersedia. Dengan demikian pengendalian DBD tergantung pada pengendalian nyamuk sebagai vektornya. Pengendalian vektor DBD dapat dilakukan dengan 4 cara, yaitu pengelolaan lingkungan, perlindungan diri, pengendalian biologis, dan pengendalian dengan bahan kimiawi (Anonim, 2004).
1. Pengendalian lingkungan
Pengelolaan lingkungan meliputi berbagai perubahan yang menyangkut upaya pencegahan atau mengurangi perkembangbiakan vektor sehingga dapat mengurangi kontak antara vektor dengan manusia. Metode ini dilakukan antara lain dengan cara mengeringkan genangan air, menimbun wadah-wadah yang dapat menampung air dan perbaikan desain rumah untuk mengurangi kesempatan masuknya nyamuk, misalnya dengan memasang kawat nyamuk di jalan angin atau jendela rumah (Anonim,2004).
2. Perlindungan diri
diri, seperti menggunakan obat nyamuk baik semprot, bakar maupun memakai obat oles anti nyamuk, penggunaan kelambu saat tidur dan pemasangan kawat kasa atau kawat nyamuk (Anonim, 1999).
3. Pengendalian biologis
Pengendalian ini dilakukan dengan tujuan untuk menurunkan populasi serangga secara alami tanpa menggangu ekologi. Termasuk dalam pengendalian serangga secara biologik adalah menggunakan predator (binatang pemangsa serangga), misalnya dengan memelihara ikan untuk memberantas larva nyamuk, menyebarkan parasit penyebab penyakit pada serangga (Soedarto, 1989).
4. Pengendalian dengan bahan kimia
Pengendalian ini menggunakan bahan kimia yang berkhasiat membunuh serangga (insektisida) atau hanya menghalau serangga saja (Repellant). Contoh cara ini adalah menaburkan bubuk AbateR pada tempat-tempat penampungan air untuk membunuh larva nyamuk, penggunaan insektisida bentuk spray untuk membunuh nyamuk dewasa (Gandahusada, et al., 1998).
Semua usaha untuk mengontrol harus tertuju melawan nyamuk. Ini penting untuk mengambil tindakan mengontrol untuk mengurangi nyamuk dan tempat mereka berkembangbiak. Bagaimanapun, usaha harus intensif sebelum musim penjangkitan (selama dan setelah musim penghujan) dan pada saat epidemia (Anonim, 2002b ).
D. Insektisida
penyakit yang merugikan bagi kehidupan tanaman dan manusia (Sastroutomo, 1991). Menurut Sudarmono (1991), ada bermacam-macam golongan insektisida, baik yang berasal dari bahan alami maupun yang berasal dari bahan sintetik. Ada beberapa cara insektisida membunuh jasad sasaran atau serangga hama :
1. fisis
2. merusak enzim 3. merusak syaraf
4. menghambat metabolisme
Menurut Untung (2001), insektisida dapat dikelompokkan dalam beberapa cara menurut cara masuknya dalam tubuh serangga dan menurut sifat kimianya. Untuk pengelompokan menurut cara masuknya ke tubuh serangga, dapat dibagi menjadi 3 kelompok, yaitu:
1. Racun perut
Insektisida memasuki tubuh serangga melalui saluran pencernaan makanan (perut). Insektisida lama umumnya merupakan racun perut. Namun ada juga insektisida modern yang beraksi pada serangga melalui perut yaitu kelompok insektisida sistemik, yang dapat diserap oleh tanaman dan ditranslokasikan dalam jaringan tanaman. Serangga yang mencucuk tanaman dan kemudian menghisap cairan tanaman yang sudah mengandung insektisida akan mati.
2. Racun kontak
3. Fumigan
Fumigan merupakan insektisida yang mudah menguap menjadi gas dan masuk ke dalam tubuh serangga melalui sistem pernapasan serangga atau sistem trachea yang kemudian diedarkan ke seluruh jaringan tubuh.
Berdasarkan data yang didapat dari Dinas Kesehatan Kota Jambi (2006a), insektisida yang digunakan untuk tahun 2005 dan 2006 adalah Cynoff. Cynoff mengandung Cypermethrin, merupakan insektisida golongan piretroid sintetik yang biasa digunakan secara luas sebagai pengendali hama profesional untuk sebagian hama rumah tangga. Cypermethrin tersedia dalam bentuk Emulsifiable Concentrate (EC), Ultra Low Volume (ULV) dan Wettable Powder (WP). Pyrethroids menyebabkan efek yang merugikan pada sistem saraf pusat (Anonim, 1993).
yaitu allerthrin yang dimunculkan pada tahun 1949. Generasi II, yaitu diantaranya tetramethrin (1965), kemudian diikuti oleh resmethrin (1967) yang memiliki 20 kali lebih efektif dari piretrum. Generasi III menjadi piretroid agrikultural pertama karena aktivitas insektisida yang luar biasa dan sifat fotostabilnya. Generasi IV, diantaranya yaitu Cypermethrin (Ware, 1999).
Terdapat 2 tipe piretroid, yaitu: tipe I, mempunyai koefisien suhu negatif (semakin rendah suhu lingkungan, maka semakin beracun untuk serangga sasaran), sedangkan tipe II memiliki koefisien suhu positif. Piretroid mempunyai mekanisme aksi yang hampir sama dengan DDT. Piretroid bekerja dengan menjaga saluran natrium pada membran saraf tetap terbuka. Piretroid mempengaruhi sistem saraf pusat dan tepi pada serangga. Awalnya menstimulasi sel saraf untuk memproduksi impuls berulang-ulang dan akhirnya menyebabkan kelumpuhan. Efek tersebut menyebabkan aksi mereka pada saluran natrium, sebuah lubang kecil yang dilalui oleh ion natrium untuk masuk ke axon dan menyebabkan rangsangan (Ware, 1999).
E. Mekanisme Resistensi Serangga Terhadap Insektisida
Menurut Small (1998) cit Widiarti (2005), mekanisme resistensi yang berperan pada serangga terhadap sebagian besar insektisida secara umum dikategorikan menjadi 2 yaitu tidak sensitifnya tempat sasaran (target site) dan resistensi metabolik. Proses terjadinya resistensi terhadap insektisida pada tubuh serangga termasuk nyamuk secara garis besar dipengaruhi oleh 3 faktor (Georghiou & Taylor, 1976 cit Faisya, 1998) yaitu:
1. faktor genetik
Ada sejumlah gen khusus yang diketahui sebagai pengendali resisten (R-gen), baik yang sifatnya dominan atau resesif dimana gen tersebut terdapat pada nyamuk dan serangga lainnya.
2. faktor biologis
Faktor biologis meliputi faktor biotik (adanya pergantian generasi, perkawinan monogami dan poligami) dan perilaku serangga (terjadinya migrasi, isolasi, monofagi dan polifagi, adanya perilaku serangga di luar kebiasaannya dalam melakukan perlindungan terhadap bahaya).
3. faktor operasional
Resistensi serangga dibagi dalam resistensi bawaan dan resistensi didapat (Gandahusada, et al., 1998).
1. Resistensi bawaan
Dari suatu populasi serangga ada anggota-anggota yang pada dasarnya sudah resisten terhadap suatu insektisida. Sifat ini turun temurun sehingga selanjutnya terjadi populasi yang resistensi seluruhnya. Resistensi bawaan juga terjadi karena perubahan gen (yang menyebabkan mutasi). Mutan ini dan keturunannya resistensi semuanya. Menurut mekanismenya resistensi bawaan dibagi dalam resistensi fisiologis bawaan dan resistensi kelakuan bawaan.
Resistensi fisiologis bawaan disebabkan oleh 1) daya absorbsi insektisida yang sangat lambat, sehingga serangga tidak mati; 2) daya penyimpanan insektisida dalam jaringan yang tidak vital, seperti jaringan lemak, sehingga alat-alat vital terhindar dan serangga tidak mati; 3) daya ekskresi insektisida yang cepat, sehingga tidak sampai membunuh serangga; 4) detoksikasi insektisida oleh enzim menyebabkan serangga tidak mati. Resistensi kelakuan bawaan disebabkan oleh 1) perubahan habitat serangga, sehingga terhindar dari pengaruh insektisida, keturunannya mempertahankan habitat yang baru ini; 2) avoidance, sifat menghindarkan diri dari pengaruh insektisida sehingga tidak terbunuh, tanpa mengubah habitat.
2. Resistensi yang didapat
Resistensi kelakuan yang didapat disebakan serangga dapat menghindarkan diri sebagai akibat dosis subletal insektisida.
Liu, Xu, Zhu dan Zhang (2006), melaporkan pada referensi mereka bahwa yang memicu resistensi piretroid pada nyamuk adalah pengaturan mekanisme molekular detoksifikasi metabolik dan peningkatan kekurangpekaan tempat target.
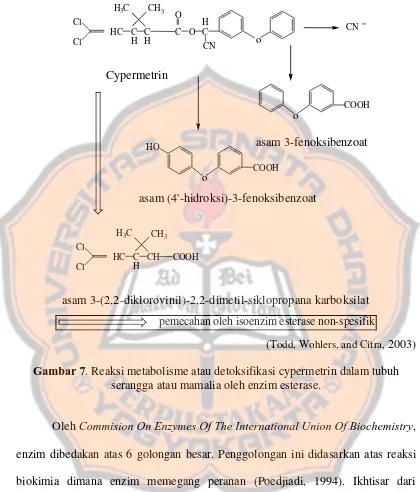
Meskipun belum ada laporan yang lengkap mengenai metabolisme cypermetrin oleh serangga, data-data yang ada menunjukkan bahwa jalur metabolisme cypermetrin memiliki kesamaan jalur pada mamalia. Dari metabolisme cypermetrin dalam tubuh serangga akan dihasilkan senyawa-senyawa yang tidak mempunyai efek membunuh, diantaranya yaitu: asam 3-fenoksibenzoat, asam (4’-hidroksi)-3-fenoksibenzoat dan asam 3-(2,2-diklorovinil)-2,2-dimetil-siklopentana karboksilat, sehingga dapat menurunkan toksisitas dari cypermetrin dalam tubuh nyamuk. Perkiraan reaksi metabolisme atau detoksifikasi cypermetrin pada tubuh serangga dapat dilihat pada Gambar 7.
F. Enzim Esterase Non Spesifik
H3C CH3
pemecahan oleh isoenzim esterase non-spesifik
(Todd, Wohlers, and Citra, 2003) Gambar 7. Reaksi metabolisme atau detoksifikasi cypermetrin dalam tubuh
serangga atau mamalia oleh enzim esterase.
Oleh Commision On Enzymes Of The International Union Of Biochemistry, enzim dibedakan atas 6 golongan besar. Penggolongan ini didasarkan atas reaksi biokimia dimana enzim memegang peranan (Poedjiadi, 1994). Ikhtisar dari klasifikasi internasional dari enzim akan disajikan berikut ini (Montgomery, Conway dan Spector, 1992):
1. Oksidoreduktase, enzim-enzim yang mengkatalisis berbagai macam reaksi oksidasi-reduksi.
3. Hidrolase, yang mengkatalisis pemutusan ikatan antara karbon dengan berbagai atom lain sambil mengikat molekul air.
4. Liase, yang mengkatalisis pemecahan ikatan antara karbon dengan karbon, karbon dengan belerang serta beberapa jenis ikatan antara karbon dengan nitrogen (tidak termasuk ikatan peptida).
5. Isomerase, kelompok enzim yang mengkatalisis reaksi rasemisasi isomer optik atau geometrik dan reaksi-reaksi oksidasi-reduksi intramolekul tertentu.
6. Ligase, yang mengkatalisis pembentukan ikatan antara karbon dengan oksigen, belerang, nitrogen dan atom-atom lain.
Enzim pada hakekatnya merupakan katalis efektif, yang bertanggung jawab bagi terjadinya reaksi kimia terkoordinasi yang terlibat dalam proses biologi dari sistem kehidupan. Sebagai suatu katalis, suatu enzim tidak dirusak dalam suatu reaksi dan karena itu tetap tidak berubah dan dapat digunakan kembali. Suatu ciri yang menonjol dari enzim sebagai katalis adalah spesifitas substrat, yang menentukan fungsi biologinya (Amstrong, 1995).
yang terdapat dalam hati dapat memecah ester sederhana, misalnya etil butirat menjadi etanol dan asam butirat (Poedjiadi, 1994).
Pada semua piretroid mempunyai beberapa ciri umum, yaitu molekul asam, ikatan utama ester dan molekul alkohol (Shafer, Meyer dan Crofton, 2005). Beberapa insektisida diantaranya organofosfat dan karbamat mengandung ikatan ester, oleh karena itu insektisida organofosfat dapat dihidrolisis oleh esterase (Scott, 1995 cit Dewi, 2006). Aktivitas enzim esterase non-spesifik dapat bertambah oleh adanya perubahan gen esterase. Perubahan genetik pada gen esterase ini menyebabkan peningkatan aktivitas enzim esterase. Hal ini menyebabkan kemampuan menghidrolisis insektisida tinggi sehingga semua insektisida yang masuk akan dihidrolisis menjadi senyawa yang kurang beracun. Oleh karena itu akan menaikkan dosis letal insektisida tersebut dan tidak lagi mematikan serangga yang menjadi sasaran (Walsh, 2001 cit Dewi, 2006).
G. Elektroforesis
perpindahan tersebut bergantung pada muatan listrik bersangkutan (Anonim, 2007a).
Gel yang digunakan biasanya merupakan polimer bertautan silang (crosslinked) yang porositasnya dapat diatur sesuai dengan kebutuhan. Untuk memisahkan protein atau asam nukleat berukuran kecil (DNA, RNA, atau oligonukleotida), gel yang digunakan biasanya merupakan gel poliakrilamida, dibuat dengan konsentrasi berbeda-beda antara akrilamida dan zat yang memungkinkan pertautan silang (cross-linker), menghasilkan jaringan poliakrilamida dengan ukuran rongga berbeda-beda (Anonim, 2007a).
Syarat dasar dari larutan penyangga yang digunakan adalah komposisi dan pHnya tidak mengubah sifat kimia dan biologi bahan yang dipisahkan, dan interaksi antara molekul protein harus minimal. Tidak diperkenankan untuk campuran yang dipisahkan mengubah cukup besar pH gel selama jalannya pemisahan. Oleh karena itu, direkomendasikan pH larutan sampel harus ditambahkan ±0,5 pH dari pH larutan penyangga, sebelum sampel diaplikasikan ke gel. Dalam penyangga alkali protein bermigrasi ke arah anoda; pada gel vertikal, untuk itu katode berada di atas. Elektroforesis harus dihentikan saat indikator pewarna mencapai 0,5-1 cm sebelum ujung gel (Gaspar, Kalasz, Kerese, Takacs, and Tyihak, 1984).
mempunyai pH berlainan (pH 8,9) mengganggu perbedaan muatan ini lalu menyebabkan pemisahan protein menjadi jalur yang berbeda (Anonim, 2007b).
Pemisahan protein memakai elektroforesis telah dipergunakan secara luas dalam mencoba membedakan strain dan spesies serangga. Ion bermuatan akan bermigrasi tergantung atas densitas muatan proteinnya. Satu sel atau bermacam-macam jaringan individu pada spesies yang sama mengandung enzim-enzim yang mempunyai protein yang berbeda tetapi mempunyai aktifitas enzimatik yang sama. Diketahui dengan baik bahwa enzim tertentu yang berbeda aktifitasnya cenderung mempunyai perbedaan tingkat variasi genetik (Ansori, 2000).
H. Landasan Teori
Berdasarkan rumusan masalah, tujuan penelitian, dan penelaahan pustaka dapat diajukan landasan berpikir sebagai berikut:
1. Faktor penyebab terjadinya resistensi pada serangga atau nyamuk secara garis besar terdiri atas faktor genetik, biologis (faktor biotik dan perilaku serangga), dan operasional insektisida (hal-hal yang terkait dengan bahan kimia yang dipergunakan dalam pengendalian vektor dan aplikasi insektisida tersebut di lapangan).
2. Peningkatan aktivitas enzim esterase dalam tubuh nyamuk akan menaikkan dosis letal menjadi subletal yang tidak lagi mematikan serangga yang menjadi sasaran.
3. Perbedaan profil esterase non spesifik nyamuk Ae. Aegypti yang berasal dari daerah endemis dan non-endemis DBD menggambarkan adanya perbedaan respon nyamuk tersebut terhadap insektisida.
I. Keterangan Empiris
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian tentang profil esterase non-spesifik pada nyamuk Ae. aegyti
yang berasal dari daerah endemis dan non endemis DBD di Kota Jambi dengan
metode elektroforesis ini termasuk penelitian non eksperimental dengan rancangan
deskriptik dan analitik.
B. Subjek Penelititan
Pada penelitian ini digunakan nyamuk Ae. aegypti yang dikoleksi dari
beberapa daerah endemis dan non endemis DBD di Kota Jambi, yang ditetapkan
berdasarkan data endemisitas DBD terbaru dari Dinas Kesehatan Kota Jambi.
Untuk koleksi nyamuk Ae. aegypti dilakukan dengan mengumpulkan telurnya
menggunakan ovitrap, diletakkan di dalam rumah atau pekarangan pemukiman
penduduk dan mengumpulkan larvanya dari tempat-tempat penampungan air yang
berada dan atau sengaja diletakkan di dalam rumah atau di sekitar pekarangan
pemukiman penduduk. Telur dan larva yang didapatkan kemudian
dikembangbiakan di Laboratorium Parasitologi Fakultas Kedokteran Umum
Universitas Gadjah Mada. Setelah dewasa, nyamuk tersebut akan
diidentifikasikan untuk memisahkan nyamuk Ae. aegypti dengan jenis nyamuk
lainnya. Nyamuk Ae. aegypti yang berasal dari Kota Jambi adalah nyamuk dari
Ae. aegypti dari Salatiga yang dikembangbiakan di Laboratorium Parasitologi Fakultas Kedokteran Umum, Universitas Gadjah Mada Yogyakarta.
C. Definisi Operasional
1. Resistensi adalah hasil dari mekanisme tubuh yang dapat menghalang-halangi atau mencegah invasi, multipliksi dari bibit penyakit kedalam tubuh atau
mencegah terjadinya kerusakan jaringan yang diakibatkan oleh racun yang
dikelurkan oleh bibit penyakit.
2. Resistensi nyamuk terhadap insektisida adalah kemampuan suatu populasi nyamuk untuk bertahan terhadap pengaruh insektisida yang biasanya
mematikan.
3. Daerah endemis DBD adalah daerah yang setiap tahunnya selama 3 tahun berturut-turut terdapat kasus DBD.
4. Daerah non endemis DBD adalah daerah yang selama 3 tahun berturut-turut tidak terjadi kasus DBD.
5. Elektroforesis adalah pergerakan zat bermuatan listrik akibat adanya pengaruh medan listrik.
6. Zymogram adalah hasil elektroforesis pada gel yang menggambarkan aktivitas isoenzim esterase non-spesifik yang terkandung dalam tubuh nyamuk
D. Bahan dan Alat Penelitian 1. Bahan penelitian
Digunakan bahan: Tris, glisin, akrilamida, HCl, N,N’-metilen
bis(akrilamida) (BIS), ammonium peroksidisulfat, ribloflavin, α-naftil asetat,
aseton, akuades, Fast Blue B, buffer fosfat, N,N,N’,N’-Tetrametiletilendiamin (TEMED), homogenat nyamuk, sukrosa, triton-X, dan bromphenol blue.
2. Alat penelitian
Digunakan alat Mini-Protean II Dual Slab Cell (Bio-Rad), sentrifugasi,
freezer, plat(lempeng) kaca sebagai cetakan, erlenmeyer, pompa vakum, gelas ukur, tempat inkubasi, pisau pemisah gel, sisir, syringe, gelas ukur, tabung
ependrof, pellet pastle, pipet tetes, aspirator, sarang nyamuk, dan mikropipet.
E. Jalannya Penelitian
Pada penelitian penentuan profil isoezim esterase non-spesifik kali ini
dilakukan dengan metode elektroforesis (O’Farrell, 1975 cit.Dharmawan, 1993),
tahap-tahap penelitiannya meliputi:
1. Penyiapan larutan
a. Larutan penyangga elektroda disiapkan dengan cara :
Dibuat larutan stok, yaitu 0,005 M Tris-0,0384 M Glisin pH 8,3 (terdiri
atas 0,05 M Tris (hidroksimetil) nitro metana sebanyak 6 gram dengan 0,384
M Glisin sebanyak 28,8 gram) dilarutkan dengan akuades sampai volume 1
liter. Bila akan digunakan larutan ini diencerkan 10 kali dengan akuades.
Larutan a adalah 1,5 M Tris-HCl (pH 8,9) yang dibuat dengan cara
sebanyak 18,3 gram Tris dilarutkan dalam akuades dengan volume tertentu dan
ditambah HCl hingga pH 8,9 dan volumenya 100 ml.
Larutan c adalah 30% akrilamida, yang dibuat dengan cara sebanyak
29,2 gram akrilamida 97,3% ditambah 0,8 gram N,N’-metilen bis(akrilamida)
(BIS) 2,7% dilarutkan dengan akuades sampai volume 100 ml.
Larutan g adalah ammonium peroksidisulfat 10%, yang dibuat dengan
cara sebanyak 1 gram ammonium peroksidisulfat, dilarutkan dalam akuades
sampai volume 10 ml (selalu dibuat baru).
c. Larutan gel atas yang terdiri atas larutan b, d dan e
Larutan b adalah 0,5 M Tris-HCl pH 6,8 yang dibuat dengan cara
sebanyak 6,055 gram Tris, dilarutkan dengan sejumlah akuades dan ditambah
HCl hingga pH 6,8 dan volumenya 100 ml.
Larutan d adalah akrilamida 12,5% yang dibuat dengan cara sebanyak
10 gram akrilamida 80% ditambah 2,5 gram bis-akrilamida 20% dan
dilarutkan dengan akuades sampai volumenya 100 ml.
Larutan e adalah riboflavin, yang dibuat dengan cara sebanyak 4 mg
riboflavin dilarutkan ke dalam akuades sampai volumenya 100 ml.
2. Pemasangan cetakan gel
Dua buah lempeng kaca diletakkan di atas meja dan permukaannya
dibersihkan dengan tissue yang telah dibasahi dengan etanol. Sekat plastik
dipasang pada sisi kanan dan kiri salah satu lempeng kaca. Sekat silikon dipasang
Lempeng kaca yang lain ditutupkan ke atasnya sehingga sekat plastik terletak
diantaranya. Pasangan ini ditegakkan di atas meja secara horizontal.
3. Penyiapan gel bawah
Pada penelitian ini gel bawah yang digunakan terdiri atas 10% akrilamida
0,375 M Tris-HCl pH 8,9 yang dibuat dengan cara :
Tabel I. Jumlah bahan yang digunakan dalam pembuatan gel bawah Banyaknya yang dibutuhkan untuk volume Bahan
Larutan a, c, akuades dan larutan g dicampur dalam Erlenmeyer atau gelas
ukur atau botol vakum bila akan dilakukan diaerasi. Larutan digojog dengan
hati-hati, kemudian dilakukan dierasi dengan pompa vakum. Diaerasi dihentikan bila
gelembung-gelembung yang terbentuk jumlahnya telah menjadi sedikit. Larutan
ditambah TEMED dan digojog lagi dengan hati-hati, kemudian segera dituang
dalam celah diantara lempeng kaca yang sudah disiapkan sampai kira-kira 2,5 cm
sebelum batas atas lempeng kaca. Akuades ditambahkan ke atas gel untuk
4. Penyiapan gel atas
Gel atas dibuat pada hari berikutnya setelah gel bawah selesai
dipersiapkan. Komposisi gel atas dengan menggunakan 5% akrilamida 0,617 M
Tris-HCl pH 6,7 adalah seperti yang tercantum pada Tabel II.
Larutan b, d, e dan akuades dicampur dalam botol vakum atau beker glass
atau Erlenmeyer dan dilakukan diaerasi menggunakan pompa vakum. Larutan
ditambah TEMED, dan dengan hati-hati digojog, selanjutnya dituang ke atas gel
bawah setelah akuades di atasnya diambil. Sisir plastik dimasukkan dalam gel atas
untuk membuat sumuran tempat sampel. Bila polimerasi sudah terjadi dengan
sempurna (gel atas tampak putih), selanjutnya sisir plastik diambil dan kelebihan
akuades yang ada dalam masing-masing sumuran dibersihkan menggunakan
syringe.
Tabel II. Jumlah bahan yang digunakan dalam pembuatan gel atas Banyaknya yang dibutuhkan untuk volume Bahan
5. Penyiapan homogenat nyamuk
Tabung ependrof diletakkan di atas hancuran es batu, kemudian ditetesi 75
memasukkan nyamuk ke dalam lemari es, dan dimasukkan dalam tabung ependrof
tersebut, dihancurkan sampai halus dengan alat pellet pestle. Selanjutnya ke dalam
tabung ependrof tersebut dimasukkan 75μl Triton-X 5% dan didiamkan selama 30
menit pada suhu 4°C. Homogenat disentrifugasi dengan kecepatan 6000 rpm
selama 4 menit. Tabung efendrof yang berisi homogenat diletakkan kembali di
atas hancuran es, kemudian supernatan diambil dan dimasukkan ke dalam tabung
efendrof baru. Supernatan ditambahkan 1 tetes indikator bromophenol blue dan
dimasukkan dalam sumuran. Sebelumnya cetakan gel dipasang terlebih dahulu
pada tempat elektroda.
6. Elektroforesis
Larutan penyangga dituang pada ruang bagian atas dan bawah tempat
elektroda. Larutan penyangga di bagian atas harus menutupi seluruh permukaan
sumuran gel atas yang telah berisi homogenat. Elektroforesis dilakukan kira-kira
selama 2,5 jam pada tegangan 120 volt, kuat arus 30 mA, pada ruang dengan
temperatur 4°C. Elektroforesis dianggap sudah cukup, bila mobilitas buffer
penanda telah melewati 70-90% panjang gel. Setelah selesai, gel diambil dengan
memisahkannya dari lempeng kaca dan dilanjutkan dengan proses pengecatan.
7. Pengecatan
Larutan substrat terdiri atas 20 mg α-naftil asetat dan 2 ml aseton. Untuk
pencucian digunakan larutan penyangga 0,1 M buffer fosfat, pH 6,8 sebanyak 50
ml. Pada akhir elektroforesis gel dicuci dengan buffer fosfat selama 5 menit untuk
yang baru (25 ml) untuk inkubasi. Larutan substrat dimasukkan dan ditutup
rapat-rapat. Inkubasi dilakukan dengan kondisi temperatur ruang antara 20-30°C selama
10 menit, sambil kadang-kadang digoyang.
Untuk pengecatan digunakan larutan yang terdiri atas akuades 10 ml,
garam Fast Blue B sebanyak 45 mg dan 0,2 M buffer fosfat pH 6,8 sebanyak 10 ml. Pada akhir inkubasi, larutan substrat dibuang dan larutan untuk pengecatan
dimasukkan dan inkubasi dilanjutkan kembali. Setelah gambaran pola esterase
non-spesifik terbentuk dengan jelas dan baik, larutan untuk pengecatan dibuang
dan gel dicuci dengan air beberapa kali sampai bersih untuk menghentikan reaksi.
Gel segera difoto untuk mendapatkan gambar yang baik.
F. Analisis Hasil
Zymogram yang terbentuk dianalisis secara kualitatif. Analisis secara
kualitatif dilakukan dengan membandingkan intensitas warna pola pita antara
nyamuk subjek penelitian atau nyamuk uji dengan kontrol dan dilakukan juga
analisis dengan menghitung kecepatan gerak (jarak) esterase dalam medan listrik,
dihitung harga Rf-nya dengan rumus:
=
serta dianalisis juga dengan menggunakan tes Chi-square untuk mengetahui
BAB IV
HASIL DAN PEMBAHASAN
Pertama-tama zymogram yang dihasilkan dari elektroforesis dianalisis
dengan membandingkan intensitas warna dari pola pita hasil reaksi aktivitas enzim
esterase non-spesifik dari nyamuk Ae. aegypti yang diamati secara visual (melihat
warna). Pada Gambar 8 dapat dilihat zymogram dan intensitas warna pola pita
hasil elektroforesis yang ditandai dengan E1 sebagai pita pertama, E2 sebagai pita
kedua dan E3 sebagai pita ketiga.
Gambar 8 menunjukkan bahwa esterase non-spesifik dari nyamuk Ae.
aegypti Salatiga yang digunakan sebagai kontrol, menghasilkan intensitas warna yang berbeda dengan kelompok nyamuk uji. Pada pita kelompok nyamuk kontrol
menunjukan intensitas warna yang pekat. Semakin pekat warna yang dihasilkan
menunjukkan bahwa nyamuk tersebut mempunyai aktivitas enzim esterase
non-spesifik yang tinggi. Intensitas warna pada kelompok nyamuk kontrol ini
digunakan sebagai pembanding untuk kelompok nyamuk yang berasal dari
Kelurahan Simpang III Sipin berada di Kecematan Kota Baru sebagai daerah
endemis DBD dan Kelurahan Sijenjang berada di Kecamatan Jambi Timur sebagai
daerah non endemis DBD.
Dari Gambar 8, dapat dilihat perbedaan intensitas warna antara daerah
endemis dan non endemis yang kemudian dibandingkan dengan kelompok
nyamuk kontrol yang berasal dari Salatiga. Pada daerah endemis intensitas warna
yang dihasilkan lebih pekat dibandingkan dengan daerah non endemis. Jika
dibandingkan dengan kontrol, intensitas warna pola pita dari daerah endemis lebih
pekat, sedangkan daerah non endemis jika dibandingkan dengan kontrol, intensitas
warna pola pita lebih terang.
Dari analisis diatas dapat diketahui bahwa populasi nyamuk dari daerah
endemis telah mengalami resistensi terhadap insektisida, sedangkan populasi
nyamuk dari daerah non endemis kecenderungan masih rentan terhadap
insektisida. Populasi nyamuk kontrol cenderung lebih rentan terhadap insektisida
dilihat dari intensitas warna pola pita yang dihasilkan dari populasi nyamuk dari
daerah endemis lebih pekat dibandingkan nyamuk kontrol.
Sama halnya dengan hasil penelitian dari Rosario, Miranda-Miranda,
Vasquez dan Estrada (1997), bahwa saat peningkatan enzim esterase non-spesifik
uji esterase menunjukkan kesamaan dengan profil protein. Sejak semua produksi
protein berlebih ditunjukkan dengan menghidrolisis ester pada naftil asetat. Selain
itu, dari penelitian Scharf, Hemingway, Reid, Small dan Bennett (1996) untuk
mengetahui resistensi Blattella germanica terhadap 4 golongan insektisida, yaitu
piretroid, organofosfat, karbamat, dan siklodien dengan menggunakan metode
biokimia dan elektroforesis. Telah diindikasikan bahwa adanya intensitas warna
pita yang lebih pekat pada Blattella germanica yang dikoleksi dari lapangan
daripada kelompok pembandingan yang masih rentan, terdapat juga peningkatan
esterase atau esterase mempunyai spesifikasi tinggi terhadap hidrolisis naftil
asetat.
Pada penelitian dengan metode elektroforesis ini, setelah gel dilepas dari
cetakan dan dicuci dengan larutan buffer fosfat, gel diinkubasi dengan larutan
substrat yang mengandung α-naftil asetat. Penginkubasian ini bertujuan untuk
mengikat enzim oleh larutan substrat. Selanjutnya ditambahkan larutan yang
digunakan untuk membentuk warna akhir. Larutan tersebut mengandung garam
fast blue B (O-dianisidine tetrazotized), akuades dan larutan buffer fosfat. Setelah warna timbul pada gel, dibilas dengan aquades untuk menghentikan reaksi. Warna
adalah reaksi pembentukan warna yang terjadi pada analisis secara kualitatif
(pengamatan visual):
O C CH3
di-α-naftol tetrazo-О-dianisidine
Berdasarkan data dari Dinas Kesehatan Kota Jambi (2006a),
dengan menggunakan Cynoff. Data dari Dinas Kesehatan menyebutkan, untuk
Kecamatan Kotabaru pada tahun 2005 dan tahun 2006 dilakukan fogging 15 kali
dan 13 kali, sedangkan untuk Kecamatan Jambi Timur dilakukan fogging 11 kali
dan 2 kali. Cynoff mengandung bahan aktif Cypermethrin, merupakan insektisida
golongan piretroid sintetik yang mempunyai gugus utama ester. Sasaran target
untuk DDT dan piretroid pada saluran membran saraf dan resistensi spesies
tergantung pada perubahan ikatan insektisida terhadap saluran natrium pada
membran (Mourya, et.al, 1993). Menurut Mardihusodo (1996), esterase
non-spesifik telah lama dikenali sebagai enzim yang penting dalam pendetoksifikasian
kimia insektisida yang berhubungan dan salah satu mekanisme resistensi
insektisida yang diketahui tejadi pada nyamuk. Oleh sebab itu, resistensi yang
didapat dari kelompok nyamuk yang berasal dari daerah endemis DBD di Kota
Jambi, kemungkinan disebabkan pendetoksifikasian berlebih dari kimia insektisida
yang dipaparkan secara berlebih juga.
Enzim pendetoksifikasi, yang merupakan dasar terjadinya resistensi saat
peningkatan level dan perubahan aktivitas dari esetrase atau oksidase, mencegah
insektisida untuk mencapai tempat aksinya. Enzim-enzim tersebut diketahui untuk
mendetoksifikasi semua gugus utama pada insektisida. Genetik dan dasar
molekular dari resistensi insektisida pada nyamuk melalui mekanisme
detoksifikasi enzim telah dipelajari secara luas. Peningkatan aktivitas detoksifikasi
enzim esterase dihubungkan dengan penjelasan tentang struktur gen yang sesuai (
Seperti yang telah disebutkan pada Bab II, mekanisme resistensi serangga
terhadap insektisida dapat disebabkan oleh resistensi metabolik. Cypermetrin yang
masuk ke dalam tubuh nyamuk akan segera dimetabolisme atau didetoksifikasi
oleh enzim yang bersangkutan sebelum berikatan dengan reseptor pada sistem
saraf sehingga tidak lagi mempunyai daya membunuh. Semakin tinggi aktivitas
enzim pendetoksi semakin nyamuk resisten terhadap insektisida. Perkiraan reaksi
metabolisme atau detoksifikasi dari cypermetrin dalam tubuh nyamuk telah
dijelaskan pada Bab II.
Zymogram yang didapatkan dari elektroforesis juga dihitung kecepatan
gerak (jarak) esterase dalam medan listrik (Rf) dan juga dianalisis dengan
menggunakan Chi-square untuk mengetahui adanya perbedaan frekuensi elektromorf yang menunjukkan adanya perbedaan aktivitas esterase non-spesifik.
Pada Tabel III, ditemukan perbedaan jumlah pita zymogram kelompok
nyamuk Ae. aegypti yang berasal dari daerah non-endemis (Kelurahan Sijenjang) dibandingkan dengan kelompok nyamuk Ae. aegypti yang berasal dari daerah
endemis (Kelurahan Simpang III Sipin), dan kontrol. Pada daerah non-endemis
hanya terdapat 2 pita, sedangkan pada daerah endemis dan kontrol terdapat 3 pita.
Esterase non-spesifik dan hasil zymogram dari elektroforesis dapat dilihat pada
Tabel III.
Untuk mengetahui adanya perbedaan aktivitas esterase, hasil pengamatan
jumlah pita yang dihasilkan pada elektroforesis ini dianalisis dengan menggunakan
dan dapat dikatakan adanya perbedaan aktivitas esterase non-spesifik antara
kelompok nyamuk Ae. aegypti dari daerah endemis dan daerah non-endemis. Hasil
serupa juga dijumpai pada penelitian yang dilakukan oleh Ernaningsih (1999)
dengan menggunakan analisis Chi-square, yaitu ditemukannya perbedaan
frekuensi elektromorf yang menandai adanya perbedaan aktivitas esterase
non-spesifik pada nyamuk Culex quinquefasciatus yang berasal dari daerah endemik
dan daerah non-endemik (p < 0,05). Pita-pita zymogram dari nyamuk yang berasal
daerah endemik, non-endemik dan kontrol yang didapat kemudian dihitung harga
Rf-nya.
Tabel III. Esterase non-spesifik dan jumlah pita yang dihasilkan dari kelompok nyamuk Ae. aegypti yang berasal dari Kelurahan Simpang III Sipin (daerah endemik DBD), Kelurahan Sijenjang (daerah non-endemik DBD), dan Salatiga sebagai kontrol
Daerah endemik Daerah
non-endemik Kontrol
Enzim
Dari Tabel IV, dapat dilihat tidak ada perbedaan yang signifikan antara
harga Rf pada pita 1 (E1) dan 2 (E2) yang dihasilkan pada kelompok nyamuk Ae.
kontrol. Untuk pita 3 (E3) pada daerah non-endemis tidak ditemukan, sehingga
harga Rf tidak dapat dihitung, tetapi juga tidak ada perbedaan yang signifikan
antara harga Rf antara daerah endemis dan kontrol.
Tabel IV. Kecepatan gerak (jarak) esterase non-spesifik dalam medan listrik (Rf) setiap pita yang terdapat pada zymogram hasil elektroforesis untuk setiap kelompok nyamuk Ae. aegypti yang berasal dari Kelurahan Simpang III Sipin (daerah endemik DBD), Kelurahan Sijenjang (daerah non-endemik DBD), dan Salatiga sebagai kontrol
Kecepatan gerak (jarak) (cm)
Pita Daerah
endemik
Daerah
non-endemik Kontrol
1 (E1) 0,18 0,18 0,2
2 (E2) 0,36 0,36 0,36
3 (E3) 0,94 - 0,96
Elektroforesis biasanya digunakan untuk menentukan komposisi protein
suatu produk makanan. Sebagai contohnya, perbedaan yang terdapat didalam
komposisi protein dari protein jenuh kacang kedelai dan weiyang dihasilkan
melalui teknik pemisahan yang berlainan. Elektroforesis dapat juga digunakan
untuk menentukan kemurniaan suatu ekstrak protein (Anonim, 2007c). Dari data
diatas (Tabel IV), diketahui tidak adanya perubahan komposisi dari protein
penyusun esterase non-spesifik pada kelompok nyamuk Ae. aegypti baik yang
berasal dari daerah endemis, daerah non-endemis maupun kontrol.
Metode elektroforesis yang digunakan untuk mengetahui gambaran profil
dan no-endemis DBD dari Kota Jambi, tidak hanya dapat digunakan untuk
mengetahui gambaran profil esterase non-spesifik pada serangga yang telah
terpapar insektisida golongan organofosfat atau karbamat, tetapi juga dapat
digunakan untuk insektisida golongan piretroid. Seperti pada penelitian yang
dilakukan oleh Ganesh, Vijayan, Urmila, Gopalan, and Prakash (2002) untuk
mengetahui adanya peranan esterase dan monooksigenase pada resistensi
Anopheles stephensi Giles (1908) terhadap deltametrin dari Mysore, digunakan elektroforesis gel poliakrilamida dan menunjukkan adanya perbedaan profil
isoenzim pada analisis A-esterase dan B-esterase. Elektroforesis gel akrilamida
juga digunakan untuk mengetahui adanya toleransi piretroid pada Culex pipiens
pipiens var molestus dari Marin, California (McAbee, et.al, 2003).
Mutasi apa saja pada gen yang bertanggung jawab dalam penurunan
sensitifitas tempat target, menyebabkan adanya resistesi silang untuk semua jenis
aksi insektisida pada tempat targetnya. Resistenasi silang antara DDT dan piretroid
telah dikatahui pada banyak nyamuk vektor. Resistensi silang juga ditemukan
antara organofosfat dan piretroid, misalnya Rodrigues et.al (2002) menemukan
bahwa Ae. aegypti yang resistensi terhadap temefos juga memberikan resistensi pada deltametrin, kemungkinan dikaitkan dengan peningkatan aktivitas GST. Juga
telah dilaporkan resistensi multipel (beberapa mekanisme resistensi terdapat dalam
1 populasi), karena pemaparan yang berulang-ulang atau terus menerus oleh
insektisida dari gugus kimia yang berbeda (Overgaard, 2006). Berdasarkan data
yang diterima dari Dinas Kesehatan Kota Jambi, hanya disebutkan pemakaian
tahun-tahun sebelumnya tidak tercantum insektisida yang digunakan. Pada
penelitian kali ini dimungkinkan telah terjadi resistensi silang antara insektisda
yang digunakan dalam program pemberantasan vektor penyakit DBD di Kota
46 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari hasil penelitian profil esterase non-spesifik dengan menggunakan metode elektroforesis ini dapat disimpulkan:
1. Adanya perbedaan profil esterase non-spesifik pada populasi nyamuk Ae. aegypti yang berasal dari daerah endemis DBD, Kelurahan Simpang III Sipin, dengan daerah non-endemis DBD, Kelurahan Sijenjang.
2. Adanya variasi aktivitas esterase antara populasi nyamuk Ae. aegytpi yang berasal dari Kelurahan Simpang III Sipin dengan Kelurahan Sijenjang (p < 0,05) yang ditandai dengan perbedaan frekuensi elektromorf.
3. Tidak adanya perbedaan kecepatan gerak (jarak) esterase antara populasi nyamuk Ae. aegypti dari Kelurahan Sijenjang dengan Kelurahan Simpang III Sipin, kecuali pada pita 3.
B. Saran
46
DAFTAR PUSTAKA
Amstrong, F.B., 1995, Buku Ajar Biokimia, ed. III, Penerbit Buku Kedokteran EGC, Jakarta, 100
Anonim, 1993, Extoxnet: Extension Toxicology Network, http://pmep.cce.cornell.edu/profiles/extoxnet/carbaryl_dicrotophos/cyper met-ext.html, diakses pada tanggal 18 April 2007
Anonim, 1999, Dengue Haemorragic Fever: Diagnosis, Treatment, Prevention, and Control, Edisi II, diterjemahkan oleh Monica Ester, , Penerbit Buku Kedokteran EGC, Jakarta, 10-11, 15, 17-18, 20-21, 88
Anonim, 2002a, Dengue and Dengue Haemorrhagic Fever, http://www.who.int/mediacentre/factsheets/fs117/en, diakses pada tanggal 9 April 2007
Anonim, 2002b, Fact Sheet on Dengue Fever and Dengue Haemorrhagic Fever, http://www.who.int/mediacentre/factsheets, diakses pada tanggal 18 April 2007
Anonim, 2002c, A Color Photo Atlas Of Mosquitoes Of Southaestern, Departemen Of Medical Entomology, Australia, http://www.arbovirus.health.nsw.gov.au/areas/arbovirus/mosquit/photos, diakses pada tanggal 28 Mei 2007
Anonim, 2004, Prevention and Control of Dengue and Dengue Haemorrhagic Fever, No.29, WHO Genewa, 3-22, 59-72
Anonim, 2005a, CD Risk Assessment: DF, DHF and DSS in Indonesia, February
2005,
http://www.who.int/diseasecontrol-emergencies/guidelines/Dengue-ind-risk%20assess.pdf, diakses pada tanggal 18 April 2007
Anonim, 2005b, DHF/DBD, http:/www.infeksi.com/artikel, diakses pada tanggal 18 April 2007
Anonim, 2005c, Demam Berdarah, http://www.pemkot-malang.go.id/britaku/data/upimages/siklus-tular.gif, diakses pada tanggal 21 Januari 2007
Anonim, 2006a, Data Penyemprotan Insektisida Cynoff di Kota Jambi, Dinas Kesehatan Kota Jambi
Anonim, 2006b, Data Kasus Demam Berdarah Dengue Periode 2003-2005 di Kota Jambi, Dinas Kesehatan Kota Jambi
Anonim, 2006c, Elektroforesis, http://id.wikipedia.org/wiki/Elektroforesis, diakses pada tanggal 9 Maret 2007
Anonim, 2006d, Elektroforesis Gel, http://id.wikipedia.org/wiki/Elektroforesis_gel, diakses pada tanggal 9 Maret 2007
Anonim, 2007a, Biologi Molekuler, http://id.wikipedia.org/wiki/Biologi_molekular, diakses pada tanggal 9 Maret 2007
Anonim, 2007b, Elektroforesis gel poliakrilamid (PAGE), http://pkukmweb.ukm.my/~mamot/STKM2022/PAGE.htm, diakses pada tanggal 9 Maret 2007
Ansori, I., 2000, Elektroforesis Beberapa Enzim Anopheles maculatus di Sumatera Selatan, Majalah Kesehatan Sumatera Selatan, Th. 32, No. 3, 38
Dewi, A.A.I.A.G., 2006, Penentuan Status Resistensi Nyamuk Aedes aegypti yang Berasal dari Wilayah Denpasar Timur (Bali) Terhadap Insektisida Organofosfat Secara Biokemis, Skripsi, Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta
Dharmawan, R., 1993, Metoda Identifikasi Spesies Kembar Nyamuk Anopheles, Sebelas Maret University Press, Surakarta
Djunaedi, D., 2006, Demam Berdarah:Epidemiologi, Imunopatologi, Patogenesis, Diagnosis, dan Penatalaksanaannya, UMM Press, Malang, 11-14, 18, 64, 82, 105-108
Ernaningsih, 1999, Culex quinquefasciatus Say (Diptera: Culicidae) dari Daerah Endemik Filariasis Bancrofti: Perbedaan Rasio Dorsal-Ventral Genital Jantan dan Analisis Isoenzim. Thesis. Fakultas Kedokteran Universitas Gadjah Mada, Yogyakarta