Dibiayai oleh DIPA UPI sesuai Jengan
Surat Perjanjian Pelaksanaan Penelitian Fundamental dengan SK Rektor UPI Nomor: 2784/H.40/PL/2009
Tanggal 07 Mei 2009 Oleh:
Dr. rer. nat. Omay Sumarna, MSi.
Dr. rer. nat. Ahmad Mudzakir, MSi.
Kurnia, Ph.D.
Mengungkap Karakter Fisikokirnia dan Kinerja Fotovoltaik Garam Fatty Imidazolinium sebagai Fungsi Struktur Kation dan Anion (Studi Eksplorasi Kristal Cair Ionik Baru Berbasis Minyak Nabati sebagai
Elektrolit Redoks pada Se/ Surya Tersensitisasi Zat Wanta)
LAPURAN HAS!L PENELITIAN
FAKULTAS PENDIDIKAN MATEMATIKA DAN IPA UNIYERSITAS PENDIOIKAN INDONESIA
2009~==~
Dibiayai oleh DIPA UPI sesuai dengan
Surat Perjanjian Pelaksanaan Penelitian Fundamental dengan SK Rektor UPI Nomor: 2784/H.40/PL/2009
Tanggal 07 Mei 2009 Oleh:
Dr. rer. nat. Ornay Sumarna. MSi.
Dr. rer. nat. Ahmad Mudzakir. MSi.
Kurnia. Ph.D.
Mengungkap Karakter Fisikokimia dan Kinerja Fotovoltaik Garam
Fatty Imidazolinium
sebagai Fungsi Struktur Kation dan Anion(Studi Eksplorasi Kristal Cair Ionik Baru Berbasis Minyak Nabati sebagai
Elektrolit Redoks pada Se/ Surya Tersensitisasi Zat Warna)
LAPORAN HASIL PENELITIAN
NVV)IVJ,SfldN3d
Daftar Pustaka . . . .. . . .. . . .. 61
Lampiran
-
64Daftar Larnpiran v111
I Pendahuluan I
II Tinjauan Pustaka . 4
Ill Tujuan dan Manfaat Penelitian IS
IV Desain dan Metode Penelitian 15
V Hasil dan Pembahasan 24
VI Kesimpulan dan Saran 60
Halaman Pengesahan . . . .. .. . . .. .. . . . .. . .. . . .. . . .. . .
11Ringkasan dan Summary .. .. .. .. .. . .. . 111
Prakata v
Daftar Gambar .. v1
Daftar Tabel vu
Daftar lsi .
ha!
Daftar Isi
Bandung, 30 November 2009 e a Peneliti,
: Rp. 39.931.500,- (Tiga Puluh Sembilan Juta Sembilan Ratus Tiga Puluh Satu Ribu Lima Ratus Rupiah) : Rp. 39.928.000,- (Tiga Puluh Sembilan Juta Sembilan
Ratus Dua Puluh Delapan Ribu Rupiah) a. Tahun Kedua
: 10 bulan 6. Masa Penelitian
7. Biaya yang Diperlukan a. Tahun Pertama
5. Kerja Sama dengan Institusi Lain
3. Jumlah Tim Peneliti : 3 orang
4. Lokasi Penelitian : Laboratorium Penelitian dan Laboratorium Kimia Instrumen Jurusan Pendidikan Kimia FPMIPA UPI
d. Pangkat/Golongan : Penata/III-d e. Jabatan Fungsional : Lektor
f. Fakultas/Jurusan : PMIP A/Pendidikan Kimia g. Perguruan Tinggi : Universitas Pendidikan Indonesia h. Pusat Penelitian : LP Universitas Pendidikan Indonesia
: Dr. rer. nat. Omay Sumama, M.Si : Laki-Laki
: 196404101989011001 2. Ketua Peneliti
a. Nama Lengkap b. Jenis Kelamin c. NIP
Halaman Pengesahan Laporan Akhir 1. Judul Penelitian
Mengungkap Karakter Fisikokimia dan Kinerja Fotovoltaik Garam Fatty Imidazolinium sebagai Fungsi Struktur Kation dan Anion (Studi Eksplorasi Kristal Cair Janik Baru Berbasis Minyak Nabati sebagai Elektrolit Redoks pada Se! Surya Tersensitisasi Zat
Warna)
Analisis terhadap uji sifat fisikokimia menggunakan Differential Scanning Calorimetry (DSC) menunjukkan terdapatnya fase kristal cair pada Ol-Imz I dengan rentang 82,58- l 5 l ,500C. Analisis sifat fisikokimia lainnya menggunakan Thermal Gravimetry I Differential Thermal Analysis (TGIDT A) menunjukkan bahwa ketiga senyawa memiliki kestabilan termal yang tinggi masing-masing dengan titik dekomposisi 368,6°C/38,6%
(Pal-lmz I); 375,5°C/45,6% (St-Imz I); dan 361,6°C/57% (01-Imz I). Analisis menggunakan cyclic voltammetry (CV) menunjukkan ketiga senyawa memiliki lebar jendela elektrokimia sebesar ± 2 V. Hasi! analisis Electrochemical Impedance
Spectroscopy (EIS) menunjukkan bahwa tahanan 01-lmz I paling kecil yaitu 0.066 kohm.cm2 pada 25°C, sedangkan St-Imz I dan Pal-lmz I masing-masing berharga 3,839 dan 1,566 kohm.cm2. Data hasil uji sifat fisikokimia menunjukkan bahwa senyawa 01- Imz I berpotensi digunakan sebagai elektrolit redoks pada OSSC.
Hasil karakterisasi struktur menggunakan FTIR dan 1H-NMR menunjukkan kesesuaian dengan senyawa yang diharapkan.
Pada penelitian ini telah berhasil disintesis tiga senyawa fatty imidazolinium iodida dengan struktur kation berbeda yakni palmitil imidazolinium (Pal-Imz), stearil imidazolinium (St-Imz), dan cis oleil imidazolinium (01-lmz). Ketiga senyawa disintesis dari asam lemak dan dietilentriamin (DETA) menggunakan metode green melalui penggunaan iradiasi gelombang mikro.
Ringkasan dan Summary Ringkasan
Penelitian nu bertujuan untuk mendapatkan deskripsi yang menggambarkan kebergantungan karakter fisikomia garam fatty imidazolinium pada struktur kation (perbedaan panjang dan kejenuhan gugus alkil), dan penjelasan rasional yang mendasari kebergantungan karakter fisikomia tersebut. Hasil penelitian ini dapat dijadikan pijakan dasar (teoritis dan empiris) bagi pengembangan sistem kristal cair ionik baru berbasis garam fatty imidazolinium sebagai elektrolit redoks pada Sel Surya Tersensitisasi Zat Warna (DSSC).
Analysis of physicochemical properties using Differential Scanning Calorimetry (DSC) shows existence of mesophase by 01-Imz I at 82,58-l 5 l ,50°C. Physicochemical analysis using Thermal Gravimetry-Differential Thermal Analysis (TG-DTA) show that these compounds have high thermal stability with decomposition temperatures for each
I
compounds are 368,6°C for Pal-Imzl; 375,5°C for St-Imzl; and 36 l ,6°C for 01-Imz I.
Analysis using cyclic voltammetry (CV) show that these compounds have electrochemical windows approximately 2 V. Analysis using Electrochemical Impedance Spectroscopy (EIS) show that resistance of 01-Imz is lowest (0,066 kohm.cm/) at 25°C, the resistance value of St-Imz I and Pal-Imz I are 3,839 and 1,566 kohm.cm", respectively. Data of physicochemical properties shows that 01-Imz I is very potential for redox electrolyte in dye-sensitized solar cell (DSSC).
Characterization using Infrared Spectroscopy (FTIR) and Proton Nuclear Magnetic Resonance (
1H-NMR) is suitable with expected compounds.
The research produce three compunds of fatty imidazolinium iodide with different cation structure, i.e. palmitic imidazolinium iodide (Pal-Irnzl), stearic imidazolinium iodide (St- Imzl), and cis-oleic imidazolinium iodide (01-Imzl). All compounds are synthesized from fatty acid and dietilentriamina (DET A) using green method with irradiation microwave and methylation with methyl iodide.
Summary
The aim of the research is to get description of physicochemical character dependency of
fatty imidazolinium salts on cation structure (length difference and bond saturation of
alkyl chain) and their rational explanation. The research result can be made to basic
stepping (theoretical and empirical) for new ionic liquid crystal system development
based on fatty imidazolinium salts as the redox in dye sensitized solar cells (DSSC).
Tim Peneliti
Bandung. 30 November 2009 Laboratorium
·~
Penelitian dan Laboratorium Kimia Instrumen Jurdik Kimia UPI,Laboratorium Polimer PP Fisika UPI Bandung, Laboratorium Kimia PP Kimia UPI Serpong, dan Laboratorium Kimia Fisika Material Jurusan Kimia !TB secara khusus diucapkan rasa terimakasih yang setinggi-tingginya. Tanpa bantuan rnereka, sangat sulit bagi tim peneliti merampungkan dan menunaikan semua kewajiban ilmiahnya.
Kegiatan penelitian yang telah dilakukan mustahil dapat terlaksana tanpa bantuan berbagai pihak. Untuk itulah tirn peneliti menyampaikan ucapan terimakasih dan penghargaan setinggi-tingginya kepada semua pihak.
yang langsung maupun tidak langsung, turut serta memperlancar kerja tim. Kepada ketua dan staf laboran diKegiatan penelitian fundamental yang telah ini mungkin belum dapat berdampak ekonomi dalam jangka pendek. Walaupun dernikian, hasil penelitian ini merupakan modal ilmiah untuk kegiatan penelitian terapan yang berdampak ekonomi dalam jangka panjang. Laporan kegiatan penelitian ini selain diharapkan dapat memperlancar pertanggungjawaban administrasi tim peneliti terhadap berbagai pihak terkait, juga sebagai pertanggungjawaban ilmiah tim peneliti terhadap komunitas kimiawan di Indonesia.
Prakata
Dengan memanjatkan puji dan syukur kepada Illahi Rabbi, yang hanya dengan rahmat-
Nya, laporan penelitian fundamental yang berjudul "Mengungkap Karakter Fisikokimia
dan Kinerja Fotovoltaik Garam Fatty Imidazolinium sebagai Fungsi Struktur Kation dan
Anion (Studi Eksplorasi Kristal Cair Ionik Baru Berbasis Minyak Nabati sebagai
Elektrolit Redoks pada Se! Surya Tersensitisasi Zat Warna" ini dapat terselesaikan tanpa
adanya rintangan yang cukup berarti.
56 58 54 55 37 39 40 42 49 50 51 35 34 34 32 31 28 26 ha!
3
6 8 9 1 112 16 17
1924 26 Struktur Kation Imidazolium 3 dan
Fatly Jmidazolinium 4Struktur Kation N,N-dialkilimidazoliurn
1Contoh Se! Surya Tersensitisasi Zat Wama
Prinsip Kerja Se! surya tersensitisasi zat wama
(DSS( ')Struktur Garam 1-Alkil-3-Metil-lmidazolium 2
Struktur Kation lmidazolium 3 dan
Fatty JmidazoliniumSkema Desain Penelitian
Skema Sintesis Garam
Skema Metode Karakterisasi Struktur
Struktur Kation Imidazolium
3dan
Fatly imidazolinium 4Reaksi Sintesis
Fatty Imidazolin(Bajpai. Divya dan Tyagi, 2008)
Mekanisme Reaksi Pembentukan Fauy
Imidazolindari Asam Lemak dan Dietilentriamin (Wahyuningrum, 2006)
Kurva Dehidrasi Reaksi Sintesis Palmitil lmidazolin Menggunakan Gelas Schott-Duran
(i) Campuran Asam Lemak, Deta, dan Kalsium Oksida Sebelum Diiradiasi (ii) Setelah Diiradiasi
(i)
Pelarutan
Fatty ImidazolinDengan Etil Asetat (ii)
Penyaringan (iii) Evaporasi,
danIiv)Palmitil Imidazolin Reaksi Metilasi-Kuartenerisasi
Fatty imidazolinedengan Metil lodida Mekanisme Reaksi Metilasi-Kuartenerisasi
Fatty imidazolineoleh Meti
IIodida
Senyawa Falty Imidazolinium
lodida (dari kiri
kekanan: Pal- Imz I, St-Imz I, dan 01-Imz
I)Perbandingan Spektra FTIR (i) Stearil Imidazolin dan (ii) Stearil Imidazolinium Iodida
Spektra FTIR (i) Pal-Imz
Idan (ii) 01-Imz I Spektra H-NMR Oleil Cis Imidazolinium Iodida Spektra H-NMR Stearil Imidazolinium lodida Kurva DSC Senyawa Oleil cis lmidazolinium Iodida Kurva DSC Senyawa Stearil Imidazolinium lodida Asetat Konformasi Molekul
(i)Kation Steril lmidazolinium dan (ii) Kation Oieil cis Imidazolinium (Chem3D Ultra Versi
9)Conteh Kurva Hasil Pengukuran EIS
Kurva EIS dari Senyawa (i)
Pal-Irnz L(ii) St-lmz
I.dan (iii) 01- Imz
ILarutan Fauy
imidazoliniutnlodida dalam n-Butanol
Cyclic Voltammogramdari
(i)Pal-Irnz
I. (ii)01-lmz I. dan (iii)
St-Imz IGambar 5.19.
Gambar 5.20.
Gambar 5.17.
Gambar 5.18.
Gambar 5.11.
Gambar 5.12.
Gambar 5.13.
Gambar 5.14.
Gambar 5.15.
Gambar 5.16.
Garn bar 5.10.
,,Gambar 5.9.
Gambar 5.7.
Gambar 5.8.
Gambar 5.6.
Gambar 5.5.
Gambar 5.4.
Gambar 5.3.
Gambar 1.1.
Gambar 2.1.
Gambar 2.2.
Gambar 2.3.
Gambar 2.4.
Gambar 2.5.
Gambar 4.1.
Gambar 4.2.
Gambar4.3.
Gambar 5.1.
Gambar 5.2.
Daftar Gambar
52 47
48 64
52 46 35 38
41 44 33 30 32
29
hal 2i 27 Metode Uji Karakter Fisikokimia
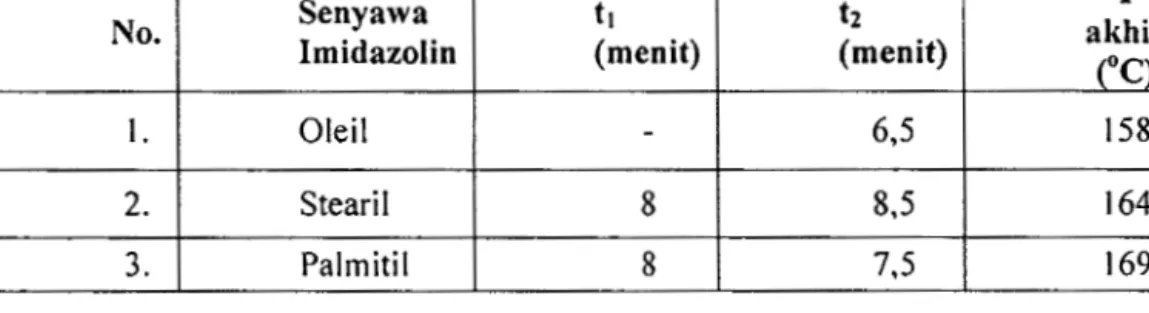
Waktu Reaksi Yang Dibutuhkan Berdasarkan Asumsi Kesetaraan Energi
Rcntang Waktu Untuk Dua Kali Dehidrasi l lingga Ternperatur Rel a ti f Konstan
Temperatur Akhir Reaksi Pada Kondisi Penelitian dan Literatur Perbandingan Rand em en Fatty I midazolin Penelitian dan Literatur
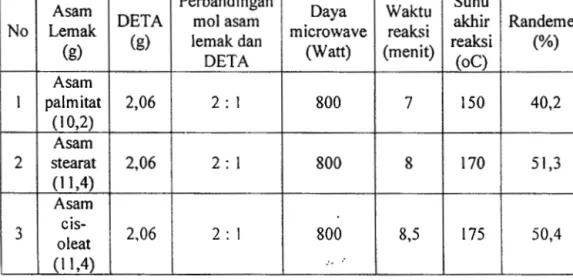
Komposisi Pereaksi, Daya Yang Digunakan, Durasi dan Suhu Reaksi, Serta Randemen Yang Diperoleh Pada Sintesis Fatly Imidazolin Menggunakan Microwave Oven
Sintesis Fatty lmidazolinium
Analisis Spektra FTIR Stearil lmidazolinium Iodida Analisis Spektra H-NMR Oleil Cis Imidazolinium Iodida Data Spektra Inframerah (dalam cm") Garam Fatty lmidazolinium pada Daerah 3200-2000 cm-1
Harga Pergeseran Kimia Proton 1H-NMR (dalam ppm) Kation- Kation dalam Garam Fatty lmidazolinium
Titik Leleh Berbagai Garam lodida'
Melting Temperature. Clearing Temperature dan Titik Dekomposisi Garam lodida dari Fatty fmidazolinium
Data Uji Tahanan (Studi Konduktivitas Ionik) Ketiga Senyawa Fatty imidazo/inium Iodida Menggunakan Instrumen EIS Data Uji Tahanan Cairan Ionik pada Penelitian Sebelumnya Tabel 5.14.
Tabel 5.13.
Tabel 5.11.
Tabel 5.12.
Tabel 5. I 0.
Tabel 5.6.
Tabel 5.7.
Tabel 5.8.
Tabel 5.9.
Tabel 5.5.
Tabel 5.3.
Tabel 5.4.
Tabel 5.2.
Tabe! 4.1.
Tabel 5.1.
Daftar Tabel
hal Lampiran 1. Struktur Molekul dan Konformasi Molekul Palmitil 64
Imidazolinium Iodida
Lampiran 2. Struktur Molekul dan Konformasi Molekul Stearil 65 lmidazolinium Iodida
Lampiran 3. Struktur Molekul dan Konformasi Molekul Cis oleil 66 Imidazolinium Iodida
Lampiran 4. Perbandingan Analisis FTIR dari Palmitil Imidzolin dan 67 Palmitil Imidazolinium lodida
Lampiran 5. Perbandingan Analisis FTIR dari Stearil Imidzolin (biru) dan 68 Stearil Imidazolinium Iodida (hitam)
Lampiran 6.
Perbandingan Analisis FTIR dari Cis oleil Imidzolin (merah) 69 dan Cis oleil lmidazolinium Iodida (biru)Lampiran 7. Spektra 1 H-NMR dari Palmitil Imidazolinium lodida 70 Lampiran 8. Spektra 1H-NMR dari Stearil Imidazolinium Iodida 71 Lampiran 9. Spektra 1H-NMR dari Cis oleil Imidazolinium lodida 72 Lampiran I 0. Kurva DSC dari Stearil Imidazolinium Iodida 73
.Lampiran 11. Kurva DSC dari Cis oleil Imidazolinium lodida 74
Lampiran 12. Kurva TG/DTA dari Palmitil Imidazolinium Iodida 75 Lampi ran 13. Kurva TG/DT A dari Stearil Imidazolinium Iodida 76 Lampiran 14. Kurva TG/DT A dari Cis oleil Imidazolinium Iodida 77 Lampiran 15. Kurva CV dari Palmitil Irnidazoliniurn Iodida dalam n-butanol 78 Lampiran 16. Kurva CV dari Stearil lmidazolinium lodida dalam n-butanol 79 Lampiran 1 7. Kurva CV dari Cis oleil Irnidazolinium Iodida dalam n-butanol 80 Lampiran 18. Kurva EIS dari Palmitil Imidazolinium lodida 81 Lampiran 19. Kurva EIS dari Stearil Imidazolinium lodida 82 Lampiran 20. Kurva EIS dari Cis oleil Imidazolinium Iodida 83 Lampiran 21. Naskah Publikasi pada "Internasional Seminar on Science and 84
Technology 2009", Bukit Tinggi, 24-25 October 2009
Lampiran 22. Buram Naskah Publikasi pada "Indonesian Journal of 94 Chemistry", Jurusan Kimia FMIPA UGM
Lampiran 23. Susunan Personalia Penelitian 103
Daftar Lampiran
Hingga saat ini telah dihasilkan tiga generasi sel surya yang masing-rnasing memiliki kelebihan dan kekurangan. Generasi pertama_ sel surya terbuat dari silikon kristal tunggal dan silikon multi kristal. Keunggulan dari tipe pertama ini adalah memiliki efisiensi yang cukup tinggi, sedangkan kelemahannya adalah biaya produksinya yang mahal sehingga tidak memenuhi salah satu kriteria sumber energi alternatif yaitu biaya produksi mu rah. Generasi kedua dari sel surya adalah tipe lapis ti pis (thin film solar cell). Keunggulan dari tipe ini diantaranya biaya produksi yang lebih murah dibandingkan dengan tipe sebelumnya dan divais yang dihasilkan bersifat lentur sehingga dapat dideposisikan terhadap piranti apapun. Sedangkan kelernahannya adalah efisiensi yang dihasilkan lebih rendah dibandingkan dengan tipe sebelumnya.
2006).
mampu untuk menutupi kebutuhan energi di seluruh dunia saat ini (Yuliarto, Sumber energi untuk sel surya yang melimpah dan terbaharui merupakan salah satu alasan dilakukannya pengembangan akan sel surya ini. Suplai energi surya dari sinar matahari yang diterima oleh permukaan bumi sangat besar yaitu mencapai 3 x I 024 joule pertahun. Jumlah energi sebesar itu setara dengan I 0.000 kali konsumsi energi di seluruh dunia saat ini. Dengan kata lain, dengan menutup 0,1% permukaan bumi dengan divais sel surya yang rnemiliki efisiensi 10% sudah
"' I. Pendahuluan
Krisis energi yang dialami oleh seluruh negara di dunia menyebabkan beberapa perubahan yang signifikan pada berbagai aspek kehidupan masyarakat. llmu Pengetahuan dan Teknologi (IPTEK) merupakan salah satu aspek yang dapat menjawab permasalahan krisis energi tersebut. Beberapa penelitian telah dilakukan oleh dalam upaya mencari sumber energi alternatif Salah satu piranti energi alternatif yang hingga saat ini menarik perhatian ban yak peneliti adalah Sel Surya (Solar Cell).
Berkaitan dengan kelernahan tersebut, beberapa usaha telah dilakukan untuk menggantikan sistem elektrolit redoks tersebut dengan semikonduktor tipe-p berbasis material anorganik, konduktor organik, atau padatan elektrolit polimer (Kang, et al., 2004). Walaupun elektrolit non-cairan dirasakan dapat mengatasi masalah kebocoran, tetapi masalah lain rnuncul yaitu dengan menurunnya efisiensi konversi. Rendahnya efisiensi dapat dihubungkan dengan relatif Tipe set surya fotokimia merupakan jenis sel surya exciton yang terdiri dari sebuah lapisan partikel nano (biasanya Ti02) yang diendapkan dalam sebuah perendam (dye). Jenis ini pertama kali diperkenalkan oleh Graetzel pada tahun 1991 sehingga jenis set surya ini sering juga disebut dengan sel Graetzel atau dye- sensitized solar cells (DSSC). Sel Graetzel ini dilengkapi dengan pasangan redoks yang diletakkan dalam sebuah elektrolit (bisa berupa padatan atau cairan). Sistem elektrolit redoks yang biasa digunakan umumnya disusun dari pasangan redoks '3- /l dalam pelarut organik seperti asetonitril atau · 3-metoksi propinitril (O' Regan dan Graetzel, 1991 ). Pelarut organik tersebut dapat mengalami kebocoran atau ketidakstabilan disebabkan peningkatan suhu selama proses iluminasi, yang berpengaruh buruk pada kestabilan elektrolit jika digunakan pada rentang waktu yang cukup lama.
Penelitian agar harga sel surya menjadi lebih murah selanjutnya memunculkan generasi ketiga dari jenis sel surya yaitu .. +ipe sel surya polimer atau disebut juga dengan sel surya organik dan tipe sel surya fotoelektrokimia. Berbeda dengan tipe sel surya generasi pertama dan kedua yang menjadikan pembangkitan pasangan electron dan hole dengan datangnya photon dari sinar matahari sebagai proses utamanya, pada sel surya generasi ketiga ini photon yang datang tidak harus menghasilkan pasangan muatan tersebut melainkan membangkitkan exciton.
Exciton inilah yang kernudian berdifusi pada dua permukaan bahan konduktor (yang biasanya di rekatkan dengan organik semikonduktor berada di antara dua keping konduktor) untuk menghasilkan pasangan muatan dan akhirnya menghasilkan efek arus foto (photocurrentv.
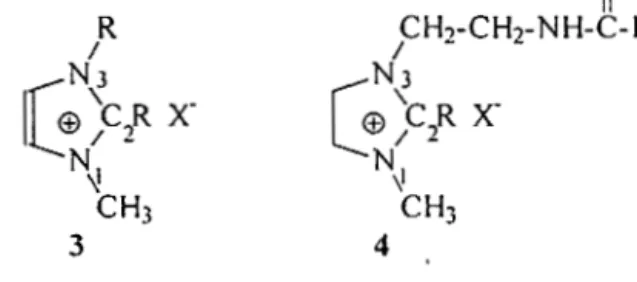
Gambar 1.1. Struktur Kation Imidazolium 3 dan Fatly Imidazolinium 4
CH1-Cl-h-NI 1-C-R
I - -
G
e N1'
C,R X.
I -
N,
(' l l.1 -I
Kation fatty imidazolinium 4 mempunyai struktur dan fungsi yang sangat mirip dengan kation imidazolium 3, berbeda hanya pada gugus substituen pada N3
[dengan adanya gugus arnida, -C(O)(NH)] pada 4 dan adanya ikatan rangkap pada sistem lingkar 3. Garam fatty imidazolinium ini dapat disintesis dari asam lemak (Bajpai, dan Tyagi, 2006; Tyagi. el al .. 2007). sehingga dimungkinkan untuk mendapatkan garam ini dari minyak nabati terbarukan lokal.
0 I
Walaupun dernikian, efisiensi konversi sel surya berbasis cairan ionik masih lebih rendah dibandingkan pelarut organik konvensional. Hal ini berkaitan dengan tingginya kekentalan cairan ionik yang mempersulit terjadinya difusi
r
dan'3-
(Yamanaka, et al., 2005). Karena usaha untuk mereduksi kekentalan belum juga berhasil, rnaka diperlukan cara lain untuk mempercepat transport muatan pada material ini. Untuk rnempercepat laju ini yaitu melalui terbentuknya struktur "self assembly" dan peningkatan konsentrasi lokal
r
dan 13-, rnaka penggunaan kristal cair ionik (ionic liquid crystals) sangat rne_mungkinkan (Yamanaka, et al., 2005).Sementara ini kristal cair ionik yang dikernbangkan adalah sistem kristal cair ionik berbasis garam imidazoliurn yang secara ekonomis rnasih kurang menguntungkan.
kurangnya kontak antara partikel nano yang mengadsorpsi zat warna dengan padatan konduktor atau polimer dalam lapisan mesopori. Dalam kaitan ini beberapa peneliti menggunakan cairan ionik sebagai alternatif karena performa fotovoltaiknya yang cukup tinggi sekaligus kestabilan fisiknya yang memadai yang menjadikan cairan ionik dapat memiliki kontak yang tinggi dengan zat warna pada partikel nano (Kang, et al., 2004).
II. Tinjauan Pustaka
Pada bagian ini akan dipaparkan state of art dalam bidang cairan ionik, sel surya
_,
(dan sistem elektrolit redoks pada DSSC), dan kristal cair ionik. Signifikansi penelitian dan hasil yang sudah dilaksanakan berkaitan dengan sintesis, karakterisasi, dan aplikasi cairan ionik sebagai elektrolit redoks pada Sel Surya Tersensitisasi Zat Warna (DSSC) juga akan dikernukakan pada bagian ini.
...
akan mendorong kation mengatur dirinya (self-organize) mernbentuk pita polimer berikatan hidrogen (hydrogen bonded ribbon polymer). Hal ini akan menstabilkan pembentukan mesophase pada rentang suhu yang cukup lebar. Terdapatnya kemiripan struktur sekaligus terdapatnya perbedaan pokok tersebut membuat kajian karakteristik fisikokimia dan kinerja fotovoltaik terhadap garam 4 ini akan sangat menarik. Kontribusi besar bagi studi eksplorasi material ini sebagai elektrolit redoks pada DSSC juga bisa diberikan.
Dalam kerangka studi eksplorasi bagi pengembangan kristal cair ionik baru sebagai elektrolit redoks pada Sel Surya Tersensitisasi Zat Warna (DSSC), adanya gugus amida ini diduga justru akan memperbesar kemungkinan fatty imidazolinium membentuk mesophase melalui pembentukan kristal cair ionik supramolekular (supramolecular ionic liquid crystals). Gugus amida primer tak tersubstitusi (-C(O)NH2) dikenal sebagai sinton pembentukan struktur supramolekular pada crystal engineering (Lee, el al.. 2003). Pembentukan kristal cair ionik supramolekular pada kation imidazolium 3 misalnya sebagian besar terstabilkan oleh interaksi ionik dan ikatan hidrogen lemah (interaksi sekunder) kation-anion. Masuknya gugus amida pada struktur kation 3 dapat memperkaya terbentuknya ikatan hidrogen lemah dan akan menstabilkan pembentukan kristal cair ionik supramolekular (Lee, et al., 2003). Dengan demikian dapat diduga bahwa dengan masuknya gugus amida pada struktur fatty imidazolinium 4 juga
Cairan ionik adalah material yang hanya terdiri atas spesies ionik (kation dan
~. anion), tidak mengandupg rnolekul netral tertentu, dan rnempunyai titik leleh
I~ e-
relatif rendah, terletak pada suhu < I 00-150 °C, walaupun umumnya pada suhu kamar (Hagiwara, et al., 2000). Berbeda dengan gararn cair (molten salt) yang biasanya mempunyai titik leleh dan viskositas tinggi, juga sangat korosif, cairan ionik umumnya berwujud cair pada suhu karnar, rnempunyai viskositas relatif lebih rendah dan relatif tidak mempunyai sifat korosif (Toma. el al., 2000). Cai ran ionik mempunyai rentang cair yang sangat lebar; tidak menguap (non volatile);
tidak terbakar (non flammables; stabilitas panas, kimia, dan elektrokirnia yang tinggi (dalam bebarapa kasus mernpunyai stabilitas terrnal sarnpai 400 °C); nilai tekanan uap yang dapat diabaikan; kemarnpuan rnelarutkan banyak senyawa organik dan anorganik: serta sifat kedapatlarutan (miscibility) yang beragam dengan pelarut air dan pelarut organik (Davis. el al., 2003).
Cairan Ionik
Sejalan dengan makin kuatnya tuntutan dunia industri atas penyediaan material baru yang handal, aman, dan ramah untuk berbagai keperluan, maka perhatian komunitas sains internasional pada penggunaan cairan ionik sebagai generasi baru pelarut green, material elektrolit, dan fluida teknik pada tahun-tahun terakhir ini narnpak semakin besar (Earle, et al., 2000; Ohno, 200 I; dan Brennecke, et al., 200 I). Karena keunikan sifat fisikokimianya serta kemudahannya dikombinasi untuk mendapatkan sifat fisikokirnia tertentu, cairan ionik juga berperan besar dalarn rnemacu perkernbangan berbagai bidang ilmu. Dalam bidang elektrokimia, riset cairan ionik diarahkan sebagai material elektrolit pada baterei, pelapisan logarn dan sistem sensor (Blomgren, 2003; Bhatt, 2003; dan Buzzeo, et al., 2004).
Cairan ionik juga diarahkan sebagai pelarut green pada sintesis kimia, katalisis dan biokatalisis (Olivier, et al., 2002; Vidis, et al.. 2005; dan Miao, et al., 2005).
Bidang teknik proses rnenggunakan cairan' ionik sebagai fluida teknik seperti
·• sebagai cairan pengemban panas, pelurnas, surfaktan dan kristal cair (Blake, et al., 2002; Ye, et al., 200 I; Merrigan. et al.. 2000; Awad, et al .• 2004; Hollbrey, 1999;
dan Gordon, et al .. 1998).
Se/ Surya Generasi Pertama (Tipe Silikon). Tipe pertama yang berhasil dikembangkan adalah tipe wafer (berlapis) silikon kristal tunggal. Tipe ini dalam perkembangannya mampu menghasilkan etisiensi yang sangat tinggi. Masalah terbesar yang dihadapi dalam pengernbangan silikon kristal tunggal untuk dapat diproduksi secara kornersial adalah harga yang sangat tinggi sehingga rnembuat panel sel surya yang dihasilkan menjadi tidak efisien sebagai surnber energi Sel Surya
Hingga saat ini terdapat beberapa jenis sel surya yang berhasil dikembangkan oleh para peneliti untuk mendapatkan divais sel surya yang memiliki efisicnsi yang tinggi atau untuk mendapatkan divais sel surya yang murah dan mudah dalam pernbuatannya,
Gambar 2.1. Struktur Kation N.N-dialkilimidazolium 1 1
Sistem kation pada cairan ionik (dan kristal+cair ionik) umurnnya merupakan kation organik dengan sifat ruah, seperti N-alkilammoniurn, P-alkilposfoniurn, N- alkil-piridinium, S-alkilsulfonium, N-alkilpirolidinium, N,N-dialkilpirazolium dan N,N-dialkilimidazolium (Olivier, et al., 2002). Fraksi terbesar fokus riset selama ini diarahkan pada kation N,N-dialkilimidazolium 1. karena begitu beragamnya sifat fisikokimia yang dapat disediakan (Olivier, et al., 2002). Bank data dari Royal Society of Chemistry (RSC), American Chemical Society (ACS), dan publikasi dari Elsevier menunjukkan hal ini. Dari sekitar 83 publikasi RSC pada tahun 2002 yang berkaitan dengan cairan ionik, 74-nya rnenyangkut garam imidazoliurn, dan persentase yang sama didapatkan dari data publikasi pada ACS dan Elsevier (Davis, et al., 2003).
Metode yang paling sering dipakai dalam pembuatan silikon jenis lapisan tipis ini adalah dengan CVD (Chemical Vapour Deposition) dari gas silan dan hidrogen.
Lapisan yang dibuat dengan metode ini menghasilkan silikon yang tidak memiliki arah orientasi kristal atau yang dikenal sebagai amorphous silikon (non kristal).
Se/ Surya Generasi Kedua (Tipe Lapis Tipis atau Thin Film). Generasi kedua sel surya adalah sel surya tipe lapisan ti pis (thin film). Ide pembuatan jenis sel surya lapisan tipis adalah untuk mengurangi biaya pembuatan sel surya mengingat tipe ini hanya menggunakan kurang dari 1% dari bahan baku silikon jika dibandingkan dengan bahan baku untuk tipe silikon wafer. Dengan penghematan yang tinggi pada bahun baku seperti itu rnernbuat harga per KwH energi yang dibangkitkan menjadi bisa lebih murah.
Modifikasi untuk membuat lebih rendah biaya pembuatan juga dilakukan dengan membuat pita silikon (silicon ribbon) yaitu dengan membuat lapisan dari cairan silikon dan membentuknya dalam struktur .~1,1Iti kristal. Meskipun tipe sel surya pita silikon ini memiliki efisiensi yang lebih rendah ( 13-15%), tetapi biaya produksinya bisa lebih dihemat mengingat silikon yang terbuang dengan menggunakan cairan silikon akan lebih sedikit.
Tipe sel surya yang kedua adalah tipe wafer silikon polikristal. Saat ini, hampir sebagian besar panel sel surya yang beredar di pasar komersial berasal dari screen printing jenis silikon polikristal ini. Wafer silikon polikristal dibuat dengan cara membuat iapisan tipis dari batang silikon dengan metode wire-sawing. Masing- masing lapisan memiliki ketebalan sekitar 250-50 micrometer. Jenis sel surya tipe ini memiliki harga pembuatan yang lebih murah meskipun tingkat efisiensinya lebih rendahjika dibandingkan dengan silikon kristal tunggal (Yuliarto, 2006).
alternatif. Sebagian besar silikon kristal tunggal komersial memiliki efisiensi pada kisaran 16-17%, bahkan silikon sel surya hasil produksi Sunl'ower memiliki efisiensi hingga 20% (Yuliarto, 2006).
Berbeda dengan tipe sel surya generasi pertama dan kedua yang menjadikan pernbangkitan pasangan electron dan hole dengan datangnya photon dari sinar matahari sebagai proses utarnanya, pada sel surya generasi ketiga ini photon yang datang akan membangkitkan exciton. Exciton inilah yang kernudian berdifusi pada dua perrnukaan bahan konduktor (yang biasanya di rekatkan dengan organik Garn bar 2.2. Contoh Sel Surya Tersensitisasi Zat Warna (Ekins, 2006)
Se/ Surya Generasi Ketiga (Tipe Se/ Surya Fotokimia). Peneliti.an agar harga sel surya menjadi lebih murah selanjutnya memunculkan generasi ketiga dari jenis sel surya ini yaitu tipe sel surya polimer atau disebut juga dengan sel surya organik dan tipe sel surya foto elektrokimi~ .. Sel surya organik dibuat dari bahan semikonduktor organik seperti polifenilena vinilena dan fulerena.
1:
Efisiensi tertinggi saat ini yang bisa dihasilkan oleh jenis sel surya lapisan ti pis ini adalah sebesar 19,5% yang berasal dari surya sel CIGS. Keunggulan lainnya dengan menggunakan tipe lapisan tipis adalah semikonduktor sebagai lapisan surya sel bisa dideposisi pada substrat yang lentur sehingga menghasilkan divais sel surya yang fleksibel.
Selain menggunakan material dari silikon. set surya lapisan ti pis juga dibuat dari bahan sernikonduktor lainnya yang memiliki efisiensi sel surya tinggi seperti kadmium tellurida (Cd'Te) dan tembaga indium galium selenida (copper indium gallium selenide, CJGS).
Gambar 2.3. Prinsip Kerja Sel surya tersensitisasi zat warna (DSS() (Ekins; 2006)
rr:)1~1 .1·.!, '"'·' <.'
~ u-" ... •1
"" ~~· 'U .;·
., ... ·,
~.
J ·., ..
I c' •'
.,
l., !
seperti asetonitril atau 3-metoksi propinitril (O'Regan dan Graetzel, t991).
Prinsip kerja dari DSSC yaitu ketika set surya DSSC dikenai cahaya matahari, maka molekul zat warna akan mengalami eksitasi dan elektron akan diinjeksikan pada pita konduksi Ti02• Dari pita konduksi, elektron kemudian akan menuju external load dan kemudian sampai ke elektroda lawan Pt untuk beregenerasi dengan adanya etektrolit redoks (Graetzel, ~093). Sistem elektrolit redoks yang biasa digunakan umumnya disusun dari kopel redoks 13-;r datam pelarut organik
~
semikonduktor berada di antara dua keping konduktor) untuk menghasilkan pasangan muatan dan akhirnya menghasilkan efek-arus foto (photocurrent).
Tipe set surya photokimia merupakan jenis set surya exciton yang terdiri dari sebuah tapisan partiket nano (biasanya titanium dioksida) yang di endapkan dalam sebuah perendam (dye). Jenis ini pertama kali diperkenatkan oleh Graetzel (O'Regan dan Graetzel, 1991), sehingga jenis set surya ini sering juga disebut dengan set Graetzel atau Dye-Sensitized Solar Cells (DSSC). Set Graetzel ini dilengkapi dengan pasangan redoks yang diletakkan dalam sebuah etektrolit (bisa berupa padat atau cairan).
Kristal Cair lonik
Sifat dari cairan ionik dapat disesuaikan dengan mengubah struktur kation dan anionnya: Sifat-sifat cairan ionik seperti sifat termal, kestabilan elektrokirnia, daya hantar ionik, dan kekentalan yang bisa diatur tergantung dari kation maupun anion yang menyusunnya menjadikan cairan ionik dikenal sebagai tailored-made solvents (Gordon, 2003). Titik leleh cairan ionik garam l-alkil-3-metil-
imidazolium 2 misalnya akan menurun sejalan dengan meningkatnya panjang gugus alk.il R. Setelah harga minimum dicapai (biasanya pada gugus heksil, heptil, atau oktil) titik leleh akan mulai meningkat sejalan dengan meningkatnya panjang gugus R (Gordon, 1998).
Walaupun elektrolit non-cairan dirasakan dapat mengatasi masalah kebocoran, tetapi masalah lain muncul yaitu dengan menurunnya efisiensi konversi.
Rendahnya etisiensi dapat dihubungkan dengan relatif kurangnya kontak antara partikel nano yang mengadsorpsi zat warna dengan padatan konduktor atau polimer dalam lapisan mesopori. Dalam kaitan ini cairan ionik dapat dijadikan sebagai alternatif karena performa fotovoltaiknya yang cukup tinggi sekaligus kestabilan fisiknya yang memadai yang me~j~dikan cairan ionik dapat memiliki kontak yang tinggi dengan zat warna pada partikel nano (Kang, et al., 2004).
Pelarut organik dapat mengalami kebocoran atau ketidakstabilan disebabkan peningkatan suhu selama proses iluminasi, yang- berpengaruh buruk pada kestabilan elektrolit jika digunakan pada rentang waktu yang cukup lama.
Berkaitan dengan kelemahan ini, beberapa usaha telah dilakukan untuk menggantikan sistem elektrolit redoks tersebut dengan tipe semikonduktor tipe p berbasis material anorganik, konduktor organik, atau padatan elektrolit polimer (Kang, et al., 2004 ).
Penggunaan kristal cair ionik sebagai elektrolit redoks pada DSSC didasari oleh fakta bahwa efisiensi konversi set surya berbasis cairan ionik masih lebih rendah dibandingkan pelarut organik konvensional. Hal ini berkaitan dengan tingginya kekentalan cairan ionik yang mempersulit terjadinya difusi
r
dan 13- (Yamanaka, et al., 2005). Karena usaha untuk mereduksi kekentalan belum juga berhasi I, maka diperlukan cara baru untuk mempercepat transport muatan pada material ini.Metode umum yang dapat dilakukan untuk mendapatkan kristal cair ionik adalah dengan menempatkan gugus alkil R relatif panjang pada struktur kation cairan ionik. Kristal cair ionik mendapatkan perhatian cukup besar karena penampakan konduktansi ioniknya yang anisotropik sekaligus memungkinkan terbentuknya material molekular (Goossens, et al., 2008).
Pada garam 2 dengan gugus alkil R panjang akan teramati adanya fasa kristal cair (mesophase). Kestabilan mesophase secara cepat akan meningkat dengan meningkatnya panjang gugus R. Walaupun panjang minimum gugus R hingga mesophase teramati ternyata bergantungjuga pada anion, tetapi nampaknya mulai gugus R dodesil hal ini dapat dipenuhi (Goossen, et al., 2008). Tanpa pengecualian, garam 2 dengan gugus R relatif panjang akan menunjukkan fasa kristal cair smektit (smectic mesophases). Pada kondisi ini, molekul-rnolekul mengatur dirinya rnembentuk lapisan karena terjadinya interaksi elektrostatis antar konstituen pembentuk kristal cair ionik. Fasa nematik jarang ditemui pada sistem kristal cair ionik (Holbrey, et al., 1999).
Gambar 2.4. Struktur Garam l-Alkil-3-Metil-lmidazolium 2
Dalam kerangka studi eksplorasi bagi pengembangan kristal cair ionik baru sebagai elektrolit redoks pada Sel Surya Tersensitisasi Zat Warna (DSSC), adanya gugus amida ini diduga justru akan memperbesar kemungkinan fatty imidazolinium membentuk mesophase melalui pembentukan kristal cair ionik supramolekular tsupramolecular ionic liquid crystals). Gugus amida primer tak tersubstitusi (-C(O)NH2) dikenal sebagai sinton pembentukan struktur supramolekular pada crystal engineering (Lee. et al .. 2003). Pernbentukan kristal cair ionik supramolekular pada kation imidazoliurn 3 misalnya sebagian besar terstabilkan oleh interaksi ionik dan ikatan hidrogen lemah (interaksi sekunder) kation-anion. Masuknya gugus amida pada struktur kation 3 dapat mernperkaya Gambar 2.5. Struktur Kation Imidazolium 3 dan Fatty Imidazolinium 4
Fatty Imidazolinium sebagai Sistem Kation Baru pada Kristal Cair Ionik Kation fatty imidazolinium 4 mempunyai struktur dan fungsi yang sangat mirip dengan kation imidazolium 3, berbeda hanya pada gugus substituen pada N3
[dengan adanya gugus amida, -C(O)(NH)] pada 4 dan adanya ikatan rangkap pada sistem lingkar 3. Garam fatty imidazolinium ini dapat disintesis dari asam lemak (Bajpai, dan Tyagi, 2006; Tyagi, et al., 2007), sehingga dimungkinkan untuk mendapatkan garam ini dari minyak nabati terbarukan Iokal.
Laju transport muatan pada kopel redoks r/13- konsentrasi tinggi sebenarnya merupakan reaksi pertukaran. Dengan demikian, untuk meningkatkan kerapatan arus pada sirkuit pendek Use). reaksi pertukaran ini haruslah dipercepat lajunya.
Kristal cair ionik dapat mempercepat laju ini melalui terbentuknya struktur "self assembly" dan peningkatan konsentrasi lokal
r
dan 13- (Yamanaka, et al., 2005).ionik berbasis kation 1-metil,3-okti 1-1.2.3-benzotriazolium yang di lakukan salah satu anggota pengusul (Mudzakir, et al., 2008) menunjukkan bahwa bahwa material ini memang masih memiliki banyak kelemahan. Pada studi tersebut tiga cairan ionik berhasil disintesis, yakni l-metil,3-oktil-1.2.3-benzotriazolium bromida (IL-Br) l-metil,-3-oktil-1,2.3-benzo-triazolium ditiosianatoargentat (IL- [Ag(SCN)i]".) dan l-metil,-3-oktil-l ,2,3-benzotriazo-lium tiosianat (I L-SCN).
Analisis menggunakan Electrochemical Impedance Spectroscopy (EIS) menunjukkan bahwa lL-SCN merupakan cairan ionik yang rnerniliki daya hantar ion yang paling baik dengan nilai hambatan 0.345 kQ.cm2, sedangkan IL-Br memiliki nilai hambatan 2,148 kn.cm~ dan IL-[Ag(SCN]2]4sekitar 7,366 kn.cm2
Analisis Cyclic Voltammetry menunjukkan bahwa IL-SCN merupakan cairan Studi karakter fisikokimia (kestabilan elektrokimia dan daya hantar ionik) cairan
\
Hasil yang sudah Dilaksanakan
Pengembangan cairan ionik sebagai material pelarut ionik (dalam proses pelarutan dan rekonstitusi selulosa), elektrolit (dalam selsurya tersensitisasi zat warna), dan fluida teknik (sebagai pelumas dan pemodifi~a~i organik suhu tinggi) sejak tahun
..
2005 telah menjadi salah satu area penelitian Rumpun Riset Cairan lonik, Kelompok Bidang Kajian (KBK) Kimia Material. di mana salah satu anggota kelompok pengusul berkiprah di dalamnya.
terbentuknya ikatan hidrogen lemah dan akan menstabilkan pembentukan kristal cair ionik supramolekular (Lee, et al., 2003). Dengan -dernikian dapat diduga bahwa dengan masuknya gugus amida pada struktur fatty imidazolinium 4 juga akan mendorong kation mengatur dirinya (self-organize) membentuk pita polimer berikatan hidrogen (hydrogen bonded ribbon polymer). Hal ini akan menstabilkan pembentukan mesophase pada rentang suhu yang cukup lebar. Terdapatnya kemiripan struktur sekaligus terdapatnya perbedaan pokok tersebut membuat kajian karakteristik fisikokimia dan kinerja fotovoltaik terhadap garam 4 ini akan sangat menarik. Kontribusi besar bagi studi eksplorasi material ini sebagai elektrolit redoks pada DSSC juga bisa diberikan.
Kajian metode sintesis cairan ionik melalui reaksi alkilasi-kuartenerisasi terhadap 1-alki 1-im idazol in dan 1-alki!-1,2,3-benzotriazol tel ah dimapankan oleh Rum pun Riset Cairan lonik sejak tahun 1998. Penelitian yang diusulkan akan merupakan kelanjutan kerja pengusul. Dengan rnernvariasikan panjang, kejenuhan, dan geometri gugus alkil pada kation (berakibat pada tingkat sirnetri dan struktur kation) dan struktur anion (berakibat pada berubahnya tingkat distribusi muatan negatif terdelokalisasi) maka kebergantungan karakter fisikokirnia dan kinerja fotovoltaik garam fatly imidazolinium pada struktur kation dan anion akan bisa Studi penggunaan kation fatty imidazolinium sebagai pemodifikasi organik pembentuk organobentonit (bentonit terrnodifikasi) sebagai lumpur pengeboran (drilling muds) telah dilakukan anggota pengusul (Supriatna, el al., 2008). Studi pendahuluan (studi TGA/DT dan studi rheologi) terhadap oleil-imidazolinium menunjukkan bahwa kation ini memiliki kestabilan termal yang cukup tinggi (mengalami dekomposisi pada suhu di atas 350°C) dan kestabilan elektrokimia yang sangat baik (sekitar 5 V,jauh lebih besar dari kestabilan elektrokimia cairan ionik 1-metil,-3-oktil-1,2,3-benzotriazolium tiosianat). Garam fatty imidazolinium juga merupakan senyawa dengan sifat kationik kuat, memungkinkan senyawa ini bertindak sebagai inhibitor karena teradsorpsi kuat pada permukaan negatif logam, plastik fiber. gelas, dan mineral (Bajpai, dan Tyagi, 2006~ Tyagi, et al., 2007). Studi pendahuluan ini cukup menjadi bukti awal bahwa garam fatty imidazolinium berbasis minyak nabati memungkinkan untuk digunakan sebagai elektrolit redoks pada DSSC.
ionik yang memiliki kestabilan elektrokimia yang tinggi dengan nilai potential window sekitar 2,5 V, sedangkan IL-Br memiliki potential- window sekitar 2 Y dan IL-[Ag(SCN]2]4 sekitar 1,5 Y. Terbentuknya struktur polirner koordinasi dalam IL-[Ag(SCN]i]oc ternyata tidak meningkatkan kestabilan elektrokimia dari cairan ionik tersebut. Pembentukan polimer koodinasi dari anion (Cd2(SCN)u]/- dan [Cu2(SCN)6]oc 2- diduga akan memberikan hasil lebih baik (Chen, et al., 2002).
IV. Desain dan Metode Penelitian
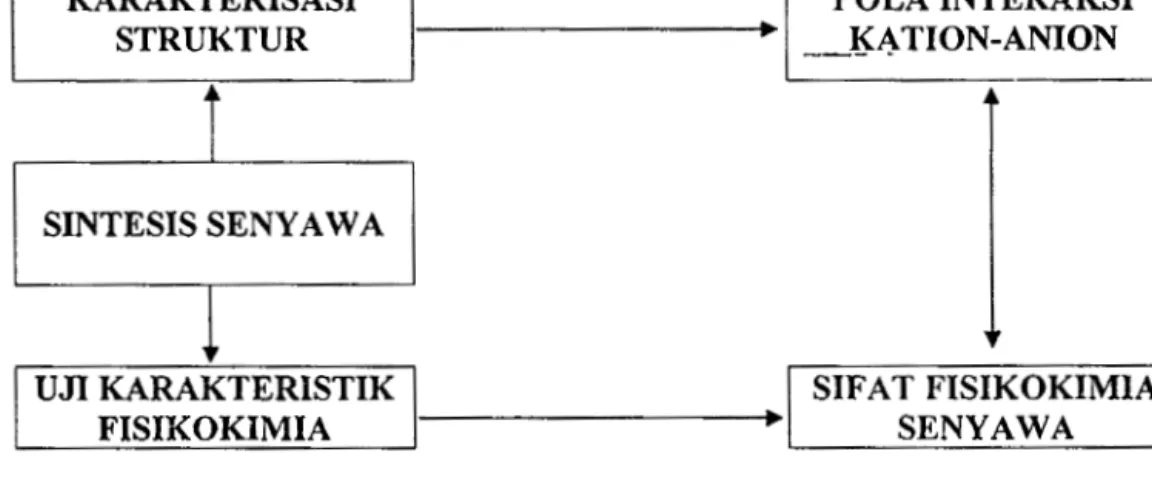
Penelitian dilakukan berdasarkan desain berikut:
B. Manfaat Penelitian
Hasil penelitian ini dapat dijadikan pijakan dasar (teoritis dan empiris) bagi pengembangan sistem kristal cair ionik baru berbasis garai:n fatty imidazolinium sebagai elektrolit redoks pada Sel Surya Tersensitisasi Zat Warna (DSSC).
Pijakan dasar yang didapatkan tidak saja diperlukan untuk menggali karakter fisikokimia material baru ini, tetapi juga untuk dapat mengkombinasikan karakter yang ada dengan kebutuhan di dunia industri.
Kedua tujuan tersebut didapatkan dengan mengkorelasikan uji karakter fisikokimia (uji sifat termal, kestabilan elektrokimia, transisi fasa, dan daya hantar ionik) dengan hasil karakterisasi struktur garam hasil sintesis.
III. Tujuan dan Manfaat Penelitian A. Tujuan Penelitian
Penelitian dilakukan dengan tujuan untuk mendapatkan:
I. deskripsi yang menggambarkan kebergantungan karakter fisikornia garam fatty imidazolinium pada struktur kation (perbedaan panjang dan
kejenuhan gugus alkil), dan
2. penjelasan rasional yang mendasari kebergantungan karakter fisikomia garam fatty imidazolinium pada struktur kation (perbedaan panjang dan kejenuhan gugus alkil).
terungkap. Kelanjutan dari apa yang telah pengusul lakukan melalui usulan ini merupakan hal yang penting untuk sampai pada aspek terapan.
I
Sintesis Garam. Garam fatty imidazoliniunj dengan berbagai gugus alkil dan jenis anion disintesis berdasarkan tiga tahap reaksi: pembentukan.fatry imidazolin 7 dari asam lemak 5 dan dietilinetriamina 6 melalui reaksi siklisasi, dan metilasi- kuartenerisasi terhadap fatty imidazolin 7.
Pada tahun pertama, total jumlah garam telah berhasil disintesis adalah tiga, dengan memvariasikan tigs substitusi gugus alkil pada kation dengan gugus palmitil (CH3(CH2)14CHr), stearil (-CH3(CH2)16CH2-). dan oleil cis
[cis-ro-S-Cl-l,
(CH2)16CH2-] dengan anion iodida (T). Terhadap setiap garam hasil sintesis telah dilakukan karakterisasi struktur dan uji karakter fisikokimia. Berdasarkan analisis korelasi antara data karakterisasi struktur dengan uji karakter fisikokirnia, maka penjelasan bagi perubahan karakter ftsikokimia material kristal cair ionik hasil sintesis sebagai fungsi struktur kation dan anion dapat diungkap.
Gambar 4.1. Skema Desain Penelitian
SIFAT FISIKOKIMIA SENYAWA UJI KARAKTERISTIK
FISIKOKIMIA SINTESIS SENY AW A
POLA INTERAKSI --~~TI ON-ANION KARAKTERISASI
STRUKTUR
Tahap Kedua: Metilasi-Kuartenerisasi Terhadap Fatty lmidazolin
Pada tahap ini dilakukan metilasi dan pembentukan garam kuartener fatty imidazolinium dari reaksi antara fatly imidazolin 7 dengan metil iodida (CH3l) seperti yang dikembangkan anggota pengusul (Mudzakir, 2004 ).
0 II
R--C-oH
5
Tahap Pertama: Pembentukan Fatty lmidazolin
Untuk keperluan ini digunakan berbagai asam lemak 5 dengan R berbeda
i
(panjang, kejenuhan, dan geometri) dan dietilinetriamina 6 melalui reaksi siklisasi seperti yang dikembangkan Bajpai dan Tyagi (2006) dan Tyagi, et al. (2007).
a
'l Garn bar 4.2. Skema Sintesis GaramCH3 N I 0 R-< ") r
II Nr:_;
R-C-NH---..,..- 8
0 II
R-C-01-1
5
+
HN....___/'-
H2N~ NH2
6
Siklisasi
R N
~ 1)
Metilasi dan ~ ~R-C-NH---..,..- Kuartenerisasi
7
Sintesis Fatty Imidazolinium Iodida
I rnol fatty imidazoline ditambahkan rnetilen klorida hingga larut dan kemudian dimasukkan ke dalam labu dasar bulat leher tiga. Ke dalarn labu dasar bulat ditambahkan 1,5 mo! rnetil iodida, selanjutnya campuran di retluks pada suhu konstan 40°C sarnbil diaduk dengan magnetic stirrer kurang lebih selama 4 jam.
Kernudian hasilnya didinginkan hingga rnencapai suhu ruangan, dan selanjutnya Campuran reaksi dibiarkan hingga mencapai suhu ruanngan. Kemudian campuran dipindahkan ke dalam labu dasar bulat leher tiga. Etilasetat ditambahkan sebanyak 80 mL dan campuran kernudian dipanaskan sampai rnendekati titik didih (40°C) etilasetat, kurang lebih dibutuhkan waktu 30 rnenit. Campuran disaring dalam keadaan panas rnenggunakan corong buchner yang dihubungkan dengan pornpa vakurn. Kemudian filtrat dipekatkan dengan evaporator dengan cara mernisahkan pelarut etil asetat. Prociuk merupakan serni-padatan berwarna coklat kekuningan.
Sintesis Fatty Imidazolina
Ke dalam gelas kimia pyrex ukuran 500 mL, dimasukkan 2,06 gram (20 mmol) dietilenatriamina, 40 mmol asam lemak (asm palmitat, asam stearat, atau asam oleat-cis) dan 20 gram kalsium oksida (CaO) secara hati hati dan diaduk hingga merata. Campuran pereaksi diiradiasi rnenggunakan microwave dengan daya 800W selarna waktu tertentu dan suhu akhir dicatat. Pertama kali, dilakukan penentuan waktu optimal reaksi dengan cara mengukur suhu dari campuran setiap
'
I menit. Setelah rnenunjukkan dua suhu rnaksimum, maka kemudian reaksi dihentikan. Setelah waktu optimal reaksi diketahui, untuk reaksi selanjutnya microwave di set pada waktu tersebut.
CH3
I
N
R---.< ~ r
0 \®
II N
R--C-NH~
8 N
0 R-._f'j \ +
CH3lII N •
R--C-NH~
7
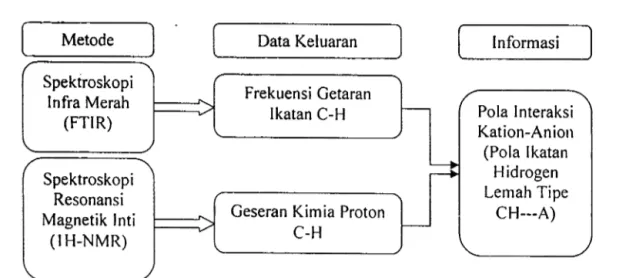
Gambar 4.3. Skerna Metode Karakterisasi Struktur
Metode Data Keluaran lnformasi
Spektroskopi
Frekuensi Getaran Infra Merah
lkatan C-H Pola lnteraksi
(FTIR)
Kation-Anion (Pola lkatan
Spektroskopi Hidrogen
Resonansi Lemah Tipe
Magnetik Inti Geseran Kimia Proton CH---A)
(IH-NMR) C-H
Karakterisasi Struktur
Karakterisasi struktur garam hasil sintesis akan dilakukan dengan metode spektroskopi infra merah (FTIR) dan spektroskopi resonansi magnetik inti
e
H-NMR). Kedua metode ini akan berperan besar mengungkap pola interaksi sekunder kation-anion yang terjadi pada bahan. Frekuensi getaran tarik dan ulur ikatan CH pada kation serta pergeserannya karena pengaruh perubahan struktur kation dan anion akan direkam melalui metode spektroskopi infra merah (FTIR).
Harga pergeseran kimia proton-proton pada kation serta perubahannya karena pengaruh perubahan struktur kation dan anion akan direkam melalui metode spektroskopi resonansi magnetik inti (1 H-NMR). Pergeseran harga frekuensi getaran ikatan CH dan perubahan harga pergeseran kimia proton pada kation akan mengungkap pola interaksi kation-anion dalam bentuk pola ikatan hidrogen lemah tipe CH···A yang terjadi antara CH pada kation dengan anion A. Metode karakterisasi struktur dan keluaran yang diharapkan dapat digambarkan berdasarkan skema berikut:
dikeringkan dengan menggunakan evaporator pada suhu 80°C kurang lebih selama 2 jam.
Penentuan struktur darifatty imidazolinium yang telah disintesa tidak cukup hanya dengan mengetahui gugus-gugus fungsi Y~.ng diketahui dengan FTIR, narnun untuk lebih jelasnya digunakan spektroskopi NMR (nuclear magnetic resonance).
Pada penelitian ini hanya menggunakan 1 H-NMR, dalam hal ini untuk mengetahui pergesaran dari ikatan C-H pada garam fatty imidazolinium yang telah disintesa.
Pengujian struktur rnenggunakan 1H-NMR
dilakukan di Pusat Penelitian Kimia Lembaga llmu Pengetahuan Indonesia (LIP() kawasan PUSPIPTEK Serpong- Tangerang. Hasil dari pengujian 1H-NMR berupa spektra NMR yang terdiri dari puncak-puncak, dimana luas puncak rnenunjukkan jumlah H dengan lingkungan kimia tertentu, sedangkan pada arah sum bu x rnenunjukkan banyaknya jenis atom H yang memiliki lingkungan kimia yang berbeda. Berbeda halnya dengan spektra FTIR yang dibandingkan dengan spektra bahan awal, pada 1 H-NMR spektrafatty imidazolinium dibandingkan dengan spektra [atty imidazolinium pada penelitian sebelurnnya yaitu yang telah dilakukan oleh Divya dan Tyagi. 2008. Pelarut yang digunakan dalam pengujian ini adalah CDCl:i.
Pada penentuan struktur atau gugus fungi dari fatty imidazolinium dilakukan analisis menggunakan Fourier Transform Infra Red (FTIR) di Laboratorium lnstrumen Jurusan Pendidikan Kimia FPMIPA UPI Bandung. Analisis tersebut bertujuan untuk menentukan gugus fungsi suatu senyawa. Walaupun sebuah molekul yang paling sederhana sekalipun dapat memberikan spektrum yang sangat rumit, namun dari hal itu dapat diambil keuntungan dengan membandingkan spektrum senyawa yang tidak diketahui terhadap spektrum cuplikan yang asli. Suatu kesesuaian puncak demi puncak merupakan bukti yang kuat tentang identitasnya (Silverstein, 1984). Hal itu pula yang diterapkan pada penelitian ini yaitu dengan membandingkan spektra sebelum dan sesudah sintesis, adanya kesesuaian ataupun perbedaan puncak yang teramati dapat menjelaskan struktur senyawa yang dihasilkan.
Pengujian karakter kestabilan termal ini dilakukan di Pusat Penelitian Fisika Lembaga llmu Pengetahuan Indonesia (UPI) Bandung. Spefikasi instumen yaitu TG/DTA 200 Seiko SSC tipe 5200H, metode uji yang digunakan adalah metode standar J IS K 7120 .. llS K 7121. Rangkaian a lat dikondisikan pada ternperatur kamar, perningkatan suhu dari 30°C - 550°C. dialiri gas nitrogen dengan laju 260mL/menit. dan laju pemanasan iheating rate) I 0°C/menit.
Tahapan studi karakter stabilitas termal dilakukan dengan tujuan untuk mengetahui suhu dekomposisi dari ketiga senyawa fatty imidazolinium yang disintesis. Analisis terhadap karakter stabilitas tennal menggunakan teknik termogravimetri. Terrnogravimetri adalah teknik untuk mengukur perubahan berat dari suatu senyawa sebagai fungsi dari suhu ataupun waktu. Pada prinsipnya, sampel dengan berat beberapa miligram dipanaskan pada laju konstan (berkisar l- 200C/menit), kernudian pemanasan dihentikan setelah sampel terdekomposisi seluruhnya atau hingga berat tertentu (tidak menunjukkan lagi dekomposisi).
Karakter Fisikokimia dan Metode (Instrumen) Data Keluaran Kinerja Fotovoltaik
Sifat Terrnal Thermogravimetric Analysis Titik Leleh dan
(TGA) Titik Dekornposisi
Ga ram
Daya Hantar Ionik Electrochemical Impedance Daya Hantar lonik Spectroscopy (EIS) Gararn
Kestabilan Elektrokimia Cyclic Voltammetry (CV) Jendela Potensi Elektrokimia Ga ram Transisi Fasa Differential Scanning Transisi Fasa
Calorimetry (])SC) Gararn Tabel 4.1. Metode Uji Karakter Fisikokimia
Uji Karakter Fisikokimia
Uji karakter fisikokimia bahan dilakukan dengan berbagai rnetodedan instrumen.
Tabet 2 berikut memperlihatkan metode dan instrumen yang digunakan untuk mengukur karakter fisikokimia yang relevan dan data keluaran yang diharapkan.
Untuk mendapatkan informasi kemungkinanfatty imidazolinium dapat digunakan sebagai elektrolit redoks pada set surya tersensitisasi zat warna maka dilakukan studi sifat kestabilan elektrokimia terhadap fatty imidazolinium hasil sintesis.
Studi ini dilakukan menggunakan instrumen cyclic voltammetry dengan merk EPSILON di Laboratorium Analitik Departemen Kimia FMIPA ITB. Program yang dijalankan pada alat ini yaitu BASi Epsilon-EC-Ver. l .60.70_XP dan kurva yang didapat diplot menggunakan program OriginPro 7.0. Pada analisis ini, elektroda platina digunakan sebagai elektroda kerja, kawat platina sebagai elektroda pembantu, dan elektroda Ag/AgCI sebagai elektroda pembanding.
Sampel yang dianalisis harus berwujud cairan, oleh karena itu sampe! dilarutkan terlebih dahulu dalam pelarut n-butanol dengan konsentrasi yang diketahui.
Larutan sampel disimpan di botol kecil dan ketiga elektroda dibiarkan kontak dengan sampel. Pengukuran dilakukan dibawah atrnosfer gas nitrogen untuk menghindari noise pada kurva cyclic akibat adanya uap air, gas oksigen dan pengotor lainnya. Arus yang dialirkan diset pada I OOmA dan disesuaikan dengan Untuk menentukan daya hantar ionik dari fatty imidazolinium dilakukan analisis menggunakan alat Electrochemistry Impedance Spectrometry (EIS) di Laboratorium Kimia Fisik dan Material Departemen Kimia FMIPA ITB. Analisis tersebut bertujuan untuk menentukan seberapa besar arus yang dapat dihantarkan melalui pengukuran tahanan dari fatty imidazolinium. Data yang didapat dari pengukuran menggunakan instrumen EIS ini yaitu berupa kurva EIS dan nilai tahanan media (R1) serta tahanan antar muka (R2). Tahanan media yaitu tahanan yang diukur ketika arus melewati larutan, sedangkan tahanan antar muka yaitu tahanan yang diukur ketika arus melewati area permukaan (batas antara logam atau elektroda dan larutan). Daya hantar ionik dari sampel ditentukan dari seberapa besar harga RI (tahanan media). Semakin besar harga RI, maka semakin kecil daya hantar ionik dari senyawa tersebut dan sebaliknya. Spesifikasi instrumen EIS yang digunakan yaitu Potensiostat Produksi Radiometer (Tacussel - Radiometer, Voltalab PGZ 301).
Untuk mengetahui melting temperature dan clearing temperature digunakan instrumen Differential Scanning Calorimetry . (DSC). Pera Iatan DSC didisain berbeda dengan DTA sehingga memungkinkan pengukuran kuantitatif perubahan entalpi yang timbul dalam sampel sebagai fungsi dari suhu maupun waktu. Pada prinsipnya, material kristal cair akan diberikan kalor dengan laju tertentu.
Perubahan fasa pada material akan ditandai dengan munculnya puncak pada rentang suhu tertentu. Pada kristal cair ionik diharapkan akan memunculkan dua puncak pada kurva, yaitu puncak yang menunjukkan perubahan dari fasa padatan menuju fasa kristal cair dan puncak yang menunjukkan perubahan dari fasa kristal cair menuju fasa cairan isotropik biasa. Dari puncak-puncak tersebut dapat diketahui melting temperature dan clearing temperature untuk kristal cair ionik yang telah disintesis serta harga semikuantitatif dari perubahan entalpi dari setiap transisi fasa. Pengujian terhadap karakter transisi fasa dilakukan di Laboratorium lJji Bahan - Pusat Teknologi Bahan Bakar Nuklir (LUB-PTBN) BA TAN kawasan PUPIPTEK Serpong-Tangerang,
Tahapan studi karakter transisi fasa dilakukan dengan tujuan untuk mengetahui rentang suhu keadaan mesofase dari kristal cair ionik berbasis/atty imidazolinium.
Setiap kristal cair ionik memiliki keadaan transisi antara keadaan padatan dan keadaan cairannya yang disebut sebagai keadaan mesofase (fase kristal cair). Pada keadaan mesofase, kristal cair akan memperlihatkan wujudnya sebagai cairan, namun molekulnya masih memiliki orientasi tertentu layaknya suatu padatan I kristal. Suhu dimana kristal cair memasuki keadaan mesofase disebutjuga sebagai melting temperature, sedangkan suhu ketika perubahan dari keadaaan mesofase menuju keadaan cairan isotropik biasa disebut sebagai clearing temperature.
kurva pada cyclic voltammogram yang dihasilkan. Batas oksidasi dan reduksi
diset pada - I sampai IV. -·- -
Dengan demikian dapat diduga bahwa dengan masuknya gugus amida pada struktur fatty imidazolinium 4 juga akan mendorong kation mengatur dirinya (se(f Dalarn kerangka studi eksplorasi bagi pengernbangan kristal cair ionik baru sebagai elektrolit redoks pada Sel Surya Tersensitisasi Zat Warna (DSSC), adanya gugus arnida ini diduga justru akan memperbesar kemungkinan fatty imidazolinium membentuk mesophase melalui pembentukan kristal cair ionik suprarnolekular tsupramolecular ionik liquid crystals). Gugus amida primer tak tersubstitusi (-C(O)NH2) dikenal sebagai simon pembentukan struktur supramolekular pada crystal engineering (Lee, el al., 2003). Pembentukan kristal cair ionik supramolekular pada kation imidazolium 3 misalnya sebagian besar terstabilkan oleh interaksi ionik dan ikatan hidrogen lemah (interaksi sekunder) kation-anion. Masuknya gugus amida pada struktur kation 3 dapat mernperkaya terbentuknya ikatan hidrogen lemah dan akan menstabilkan pembentukan kristal cair ionik supramolekular (Lee, et al., 2003).
Gambar 5.1. Struktur Kation lmidazolium 3 dan Fatty imidazolinium 4 0 II
CH.,-CH2-NH-C-R
I -
G
(£) N3 N\l'c.,R
1 -x
CH3 4V. Hasil dan Pembahasan
Kation fatty imidazolinium 4 mempunyai struktur dan fungsi yang··sangat mirip dengan kation imidazolium 3. berbeda hanya pada gugus substituen pada N3
[dengan adanya gugus arnida, -C(O)(NH)] pada 4 dan adanya ikatan rangkap pada sistern lingkar 3. Garam fatty imidazolinium ini dapat disintesis dari asam lemak (Bajpai dan Tyagi, 2008) dengan metode gelombang mikro yang lebih green, sehingga dimungkinkan untuk mendapatkan garam ini dari rninyak nabati terbarukan lokal.
5.1 Sintesis Fatty Imidazoline
Gararn fatly Imidazolinium dapat disintesis dari asam lernak (Bajpai. Divya dan Tyagi, 2008). trigliscrida. dan met ii ester dari asam lernak (Earl. G. W dalam Tyagi, 2007). Sccara umurn, tahapan reaksi/ sintesis dapat dibagi kedalam tiga tahapan, yakni, sintesis imidazolin dengan menggunakan microwave oven, Karakterisasi stuktur ketiga senyawa hasil sintesis menggunakan Fourier Transform Infra Red (FTIR) dan Nuclear Magnetic Resonance Proton (NMR-1 H).
Sedangkan karakter fisikokimia yang diuji yaitu konduktivitas ionik menggunakan Electrochemical Impedance Spectroscopy (EIS), potensi jendela elektrokimia menggunakan Cyclic Voltammetry (CV), dan transisi fasa (Differential Scanning Calorimetry). Ketiga karakter fisikokimia tersebut menjadi tolak ukur kelayakan suatu senyawa untuk digunakan sebagai elektrolit redoks pada sel surya tersensitisasi zat warna.
Pada penelitian ini telah disintesis tiga senyawa berbasis garam fatty imidazolinium dengan memvariasikan gugus alkil pada kation dengan palmitil [CH3-(CH2)wCH2-], stearil [CH3-(CH2)wCH2-], dan oleil cis [c.o-9-CH3-(CH2)w CHi-] dan iodida sebagai anion. Senyawa palmitil imidazolinium iodida (pal- lmzl) berupa padatan lembek berwarna kuning kecoklatan, senyawa stearil imidazolinium iodida (st-imzl) berupa padatan lembek berwarna kuning kecoklatan namun lebih coklat dibanding palrnitil, sedangkan senyawa oleil cis imidazolinium iodida (cis-ol-imzl) berupa pa~aJan lembek berwarna coklat lebih lembek dibandingkan palmitil dan stearil.
organize) membentuk pita polimer berikatan hidrogen (hydrogen bonded ribbon polymer). Hal ini akan menstabilkan pembentukan mesophase pada-rentang suhu yang cukup lebar. Terdapatnya kemiripan struktur sekaligus terdapatnya perbedaan pokok tersebut membuat kajian karakteristik fisikokimia dan kinerja fotovoltaik terhadap garam 4 ini akan sangat menarik. Kontribusi besar bagi studi eksplorasi material ini sebagai elektrolit redoks pada DSSC juga bisa diberikan.
Gambar 5.3. Mekanisme Reaksi Pembentukan Fattv Imidazolin dari Asam Lemak dan Dietilentriamin (Wahyuningrurn. 2006)
'
Iri....: I
~ I ...--- _I_
I I
, __
...-·- I
I
-'--
...- -'-·
IAdapun mekanisme reaksi yang terjadi adalah seperti yang digambarkan pada gambar 5.2.
Garn bar 5.2. Reaksi Sintesis Fatty Imidazolin (Bajpai, Divya dan Tyagi, 2008)
, 11 " '· •••
r,
l '''
l•.•Ir.
!
dd1ul1 .. 1I. ..
1-;. "l·
''·''" h:m.1~
pemisahan lmidazolin dari substrat, dan kuartenerisasi (Bajvai, Divya dan Tyagi, 2008).