Nama : M. Fajar Ridwan
NIM : 03031181520016
Shift : Selasa, 13.00-15.00 Kelompok : 3
RESUME JURNAL
1. Laju Korosi Baja dalam Larutan Asam Sulfat dan dalam Larutan Natrium Klorida
Pada tahun 2014, Gusti mempublikasikan penelitian yang berjudul Laju Korosi Baja Dalam Larutan Asam Sulfat dan Dalam Larutan Natrium Klorida. Pada kehidupan sehari-hari, korosi dapat dijumpai pada berbagai jenis peralatan, misalnya peralatan konstruksi yang memakai komponen logam. seperti seng, tembaga, kuningan, aluminium, besi baja bahkan stainless steel, semuanya dapat terserang oleh korosi. Di negara maju sekalipun, masalah ini secara ilmiah belum tuntas terjawab sehingga saat ini selain merupakan masalah perlakuan permukaan yang merupakan kajian dan perlu dilakukan secara fisika, korosi juga mengangkut kinetika reaksi yang menjadi wilayah kajian para ahli kimia. Korosi juga menjadi masalah ekonomi karena menyangkut umur, penyusutan dan kehilangan berat serta pemakaian suatu bahan maupun peralatan dalam kegiatan industri.
Di negara Indonesia permasalahan korosi perlu mendapat perhatian serius mengingat dua pertiga wilayah nusantara terdiri dari lautan dan terletak di daerah tropis dengan curah hujan tinggi dan kandungan senyawa klorida yang tinggi. Salah satu faktor yang mempengaruhi korosi dalam lingkungan air adalah keberadaan elektrolit. Contohnya adalah asam sulfat dan natrium klorida yang mana merupakan elektrolit kuat (Amantyo, 2006). Jenis logam yang banyak digunakan untuk bahan konstruksi bangunan adalah berbahan baja. Penelitian ini menguji bagaimana laju dari korosi baja dalam perendaman di dalam asam kuat berupa larutan asam sulfat dan di dalam larutan garam berupa natrium klorida.
asam sulfat 1 M dibuat dari asam sulfat dengan cara mengencerkan sebanyak 2,8 mL asam sulfat dalam labu ukur 50x mL sampai tanda batas dari labu ukur. Kemudian larutan asam sulfat 0,01 M, 0,02 M, 0,03 M, 0,04 M, 0,05 M dan 0,06 M dibuat dengan cara mengnencerkan larutan asam sulfat 1 M dengan volume tertentu pada labu ukur 50 mL kemudian diencerkan sampai tanda batas labu ukur.
Larutan media korosif berupa natrium klorida 1 M dibuat dengan cara mengencerkan sebanyak 2,9175 gram NaCl di dalam labu ukur 50 mL sampai tanda batas dari labu ukur. Kemudian larutan natrium klorida 0,01 M, 0,02 M, 0,03 M, 0,04 M, 0,05 M dan 0,06 M dibuat dengan cara mengencerkan larutan natrium klorida 1 M dengan volume tertentu pada labu ukur 50 mL kemudian diencerkan sampai tanda batas. Setelah proses korosi berjalan dalam waktu tertentu, baja tersebut diangkat dari media korosi, dicuci secara hati-hati dengan menggunakan sikat yang halus dan lembut kemudian baja yang telah dicuci dibiarkan mengering selama ± 15 menit dan lalu baja tersebut ditimbang sebagai berat akhirnya.
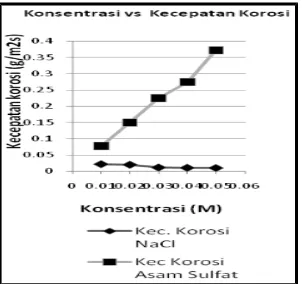
Gambar 1.1. Konsentrasi NaCl dan H2SO4 vs Kecepatan korosi
(Sumber: Gusti, 2014)
Dari Gambar 1.1. dapat diketahui bahwa pengaruh larutan asam sulfat terhadap kecepatan korosi baja sangat tinggi sekali dibandingkan kecepatan korosi pada larutan natrium klorida. Dari grafik tersebut dapat terlihat bahwa terjadi peningkatan kecepatan korosi seiring dengan meningkatnya konsentrasi dari larutan asam sulfat. Hal ini menunjukkan bahwa larutan asam sulfat merupakan media yang sangat korosif. Asam sulfat sebagai zat pengoksidator kuat
dissosiasi dari akan air membentuk senyawa berupa ferihidroksida yang dapat bereaksi kembali dengan ion Fe2+ dan menghasilkan endapan berupa suatu senyawa, senyawa tersebut yaitu ferosoferioksida (Fe3O4) yang berwarna kuning kemerahan merahan yang mana senyawa tersebut memiliki sifat magnetik, artinya senyawa ini merupakan bagian dari golongan transisi pada periode keempat. .
Dari reaksi diatas dapat dijelaskan bahwa semakin besar konsentrasi asam sulfat maka semakin banyak atom-atom yang terlepas dari besi sehingga kecepatan korosi semakin besar. .Natrium klorida merupakan media korosif, tetapi ion halogen sendiri menghambat korosi pada hingga tingkat tertentu dalam larutan. Berdasarkan grafik dan pengamatan dapat diketahui bahwa kecepatan korosi pada medium larutan NaCl lebih rendah jika dibandingkan dengan larutan asam sulfat. Nilai korosi terbesar pada larutan NaCl adalah 0,01 M kemudian menurun Dari pengamatan yang ada diduga pada larutan dengan konsentrasi 0,01–0,05 M telah terbentuk suatu lapisan pasif dimana lapisan ini akan berperan menghalangi masuknya ion-ion korosif ke dalam permukaan baja, sehingga juga akan menghalangi kecepatan korosi dari baja dalam larutan garam natrium klorida..
Bentuk lapisan pasif yang menghalangi ion-ion korosif masuk ke dalam permukaan baja adalah berupa lapisan oksida dari besi yang menempel pada permukaan baja. Selaput pasif tipis yang kemudian menyelimuti anoda akan menghalangi serangan ion-ion korosif pada permukaan baja. Hal berupa selaput tipis dari lapisan-lapisan garam inilah yang diduga sebagai penyebab laju korosi pada baja dalam larutan garam berupa larutan natrium klorida (Asdim, 2001)..
2. Kecepatan Korosi Oleh 3 Bahan Oksidan Pada Plat Besi
Pada tahun 2006, Caniago mempublikasikan penelitian yang berjudul Kecepatan Korosi Oleh 3 Bahan Oksidan Pada Plat Besi. Penelitian ini bertujuan untuk menentukan kecepatan tingkat korosi dari suatu bahan yang disebabkan oleh 3 jenis bahan oksidan (garam, udara, asam)..Penelitian ini dimaksudkan untuk memberikan kontribusi kepada Iptek dalam salah satu pemanfaatan teknologi nuklir. Sedangkan manfaat dapat ditunjukan pada sinar γ untuk mengukur seberapa besar tingkat korosi pada logam secara dini untuk diambil tindakan yang
diperlukan dalam mengatasi kerugian yang lebih besar pada sistem kontruksi besi..
Pada proses pengkorosian besi penyebab utamanya adalah terjadi reduksi oksigen pada molekul asam oleh molekul logam. Mekanisme korosi pada
permukaan logam yang bersentuhan atau berkontak langsung dengan oksidan dapat dipandang sebagai anoda, pada bagian ini terjadi reaksi. Elektron yang dihasilkan melakukan pertukaran dengan oksigen, atau mengalami reduksi. Ion H+ berperan sebagai pereduksi oksigen. Makin besar kosentrasi dari H+ (makin asam) dan reaksi yang terjadi inipun berlangsung semakin cepat. Sebaliknya makin kecil kosentrasi dari ion H+ (makin basa) maka reaksi berlangsung semakin lambat. Besi tidak terkorosi pada pH > 9. Ion Fe2+ yang terbentuk pada anoda mengalami oksidasi berlanjut membentuk Fe3+ yang selanjutnya akan membentuk suatu senyawa oksidasi terhidrasi, Fe203 x H2O, yang disebut sebagai korosi besi..
Katoda adalah bagian yang mendapat banyak suplai oksigen, sehingga korosi terjadi pada bagian ini. Pada proses pengkorosian besi bisa dilakukan secara alamiah atau secara buatan. Secara alamiah, bila oksigen yang terdapat dalam udara dapat bersentuhan dengan permukaan logam besi yang lembab,
konsentrasi oksigen lebih rendah. Besi mempunyai potensial elektroda φ sebesar -0,44 volt. Hal ini disebabkan karena Fe harus melepaskan ketiga elektronnya agar berlangsung reaksi katoda sehingga terjadi ion Fe3+. Bila reaksi terjadi dalam air yang diperkaya dengan oksigen akan didapat hasil korosi yang tidak larut dalam air yang selanjutnya disebut dengan karat atau hasil dari korosi (Supomo, 2003)..
Penelitian ini dilaksanakan di laboratorium Fisika Eksperimen Jurusan Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam. Dalam penelitian ini digunakan metode eksperimen, bahan yang digunakan adalah plat besi. Plat besi tersebut dipotong dengan ukuran yang sama. Kemudian plat tersebut dikorosikan pada media korosi berupa oksidan yaitu air (H2O), asam sulfat (H2SO4), dan air garam (NaCl), dimana dari ketiga oksidan ini akan dilihat tingkat dari korosinya..
Peralatan yang digunakan dalam penelitian ini adalah perangkat alat pendeteksi tabung Geiger Muller, Sumber radiasi sinar γ (Co-60), dan Digit Counter. Lempengan besi dengan ukuran (2x3 cm, ketebalan 3 mm) diletakkan di atas gelas yang berisi media yang berbeda-beda disusun dalam sebuah kotak kayu yang terlebih dahulu dibasahi dengan ketiga oksidan. Sebagai sampel pengontrol adalah logam yang bebas korosi, yang diukur intsnsitas sinar γ sebelum dan sesudah melewati sampel dan dihitung daya serap sinar γ pada plat besi tersebut dinyatakan sebagai data Ao. Sedangkan sampel uji, digunakan plat besi yang telah mengalami korosi dengan waktu pengoksidasian yang berbeda, yaitu: ± 5 hari, 10 hari, 15 hari, 20 hari, dan 25 hari. Data yang diambil sama dengan data pada sampel kontrol yaitu data dari intensitas sinar γ sebelum (Io) dan sesudah melewati sampel (I) kemudian menghitung daya yang akan diserapnya masing-masing..
Demikian untuk oksidan H2S04, peningkatan nilai rata-rata intensitas dimulai dari 286,8 (waktu korosi 5 hari) dan berakhir pada 300.7 (waktu korosi 25 hari).
Peningkatan intensitas sinar γ yang menembus pada bahan bersesuaian dengan semakin lamanya waktu oksidasi, dengan demikian dapat dikatakan bahwa oksidasi meyebabkan kerenggangan molekul-molekul pada besi sehingga sinar γ berpeluang lolos. Perbandingan dari suatu karakteristik bahan (hubungan Intensitas dengan lama korosi) yang mengalami korosi dengan 3 jenis oksidan (air, natrium klorida, dan asam sulfat) dapat dilihat pada gambar 2.1 berikut:
Gambar 2.1. Karakteristik Bahan yang Mengalami Korosi (Sumber: Caniago, 2006)
Dari gambar 2.1. ini terlihat bahwa semakin lama besi terkorosi maka intensitas sinar γ yang melewati plat besi mengalami kenaikan. Dampaknya adalah intensitas sinar γ yang diserap oleh plat besi yang mengalami penurunan yang bersesuaian dengan seiring lamanya proses korosi yang dialami pada bahan yang diujikan. Semakin tinggi intensitas sinar γ, maka semakin kecil pula intensitas yang diserap oleh plat besi. Besi mengalami korosi terbesar (kecepatan tingkat korosinya paling besar) berturut-turut dengan oksidan H2SO4 kecepatan korosi rata-rata dari besi 0,00198 dB/hari, pada larutan NaCI kecepatan korosi rata-rata yang diterima sebesar 0,00165 dB/hari dan H2O kecepatan korosi rata-rata yang diterima sebesar 0,00157 dB/hari. Intensitas sinar γ paling banyak melewati plat besi dengan oksidan H2SO4 dengan interval 286,8 sampai 300,7..
material logam dapat dilakukan dengan menembakkan sinar γ pada logam itu, bila itensitas sinar γ banyak melewati logam (sedikit diserap oleh logam) maka rendah.
DAFTAR PUSTAKA
Amantyo, H.. 2006. Ilmu Bahan. Jakarta: Bumi Aksara.
Asdim. 2001. Pengaruh Senyawa n-Alkilamin Terhadap Korosi Baja Dalam Larutan Asam Sulfat. Padang: Universitas Andalas.
Caniago, Z.. 2014. Kecepatan Korosi Oleh 3 Bahan Oksidan Pada Plat Besi. Jurnal Gradien Vol. 2(2): 161-166.
Gusti, D.. 2014. Laju Korosi Baja Dalam Larutan Asam Sulfat dan Dalam Larutan Natrium Klorida. Jurnal Teknik Kimia. Vol. 3(6): 28-31. Supomo..2003..Buku Ajar Korosi. Surabaya: Institut Teknologi Sepuluh