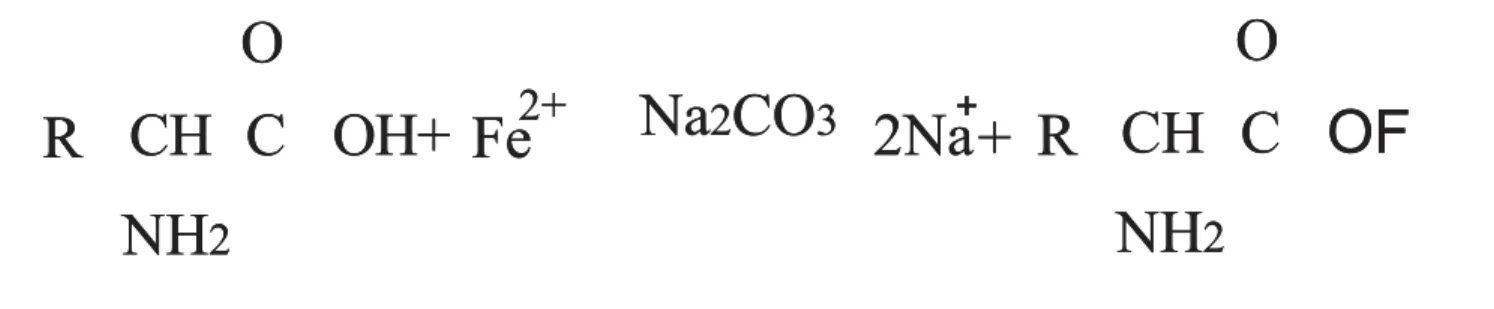UJI LOGAM BERAT
UJI LOGAM BERAT
Diajuakan untuk memenuhi persyaratan Diajuakan untuk memenuhi persyaratan
Praktikum Biokimia Pangan Praktikum Biokimia Pangan
Oleh : Oleh : Nama
Nama : : Shinta Shinta SelvianaSelviana
NRP :123020011
NRP :123020011
Kel
Kel /Meja /Meja : : A/5 A/5 (Lima)(Lima) Asisten
Asisten :Noorman Adhi Tridhar:Noorman Adhi Tridhar Tgl
Tgl . . Percobaan Percobaan :14 :14 Mei Mei 20142014
LABORATORIUM BIOKIMIA PANGAN
LABORATORIUM BIOKIMIA PANGAN
JURUSAN TEKNOLOGI PANGAN
JURUSAN TEKNOLOGI PANGAN
FAKULTAS TEKNIK
FAKULTAS TEKNIK
UNIVERSITAS PASUNDAN
UNIVERSITAS PASUNDAN
BANDUNG
BANDUNG
2014
2014
I PENDAHULUAN
I PENDAHULUAN
Bab ini akan menguraikan mengenai : (1) Latar Bab ini akan menguraikan mengenai : (1) Latar Belakang percobaan, (2) Tujuan Percobaan, (3) Prinsip Belakang percobaan, (2) Tujuan Percobaan, (3) Prinsip Percobaan, dan (4)Reaksi Percobaan.
Percobaan, dan (4)Reaksi Percobaan.
1.1.
1.1. Latar Belakang Latar Belakang PercobaanPercobaan
Protein merupakan zat makanan yang amat penting bagi Protein merupakan zat makanan yang amat penting bagi tubuh, karena zat ini di samping berfungsi sebagai bahan tubuh, karena zat ini di samping berfungsi sebagai bahan bakar dalam tubuh juga berfungsi sebagai
bakar dalam tubuh juga berfungsi sebagai zat pembangun danzat pembangun dan pengatur. Protein adalah sumber asam-asam amino yang pengatur. Protein adalah sumber asam-asam amino yang mengandung unsur-unsur C, H, O, dan N yang tidak dimiliki mengandung unsur-unsur C, H, O, dan N yang tidak dimiliki oleh lemak atau karbohidrat (Winarno, 1992).
oleh lemak atau karbohidrat (Winarno, 1992). Keistimewaan lain dari protein ini
Keistimewaan lain dari protein ini adalah strukturnya yangadalah strukturnya yang mengandung N, di samping C, H, O (seperti juga karbohidrat mengandung N, di samping C, H, O (seperti juga karbohidrat dan lemak), S, dan kadang-kadang P, Fe, dan Cu (sebagai dan lemak), S, dan kadang-kadang P, Fe, dan Cu (sebagai senyawa kompleks dengan protein). Dengan demikian maka senyawa kompleks dengan protein). Dengan demikian maka salah satu cara terpenting yang cukup spesifik untuk salah satu cara terpenting yang cukup spesifik untuk menentukan jumlah protein secara kuantitatif adalah dengan menentukan jumlah protein secara kuantitatif adalah dengan penentuan kandungan N yang ada di dalam bahan makanan penentuan kandungan N yang ada di dalam bahan makanan atau bahan lain. Protein dalam bahan makanan sangat atau bahan lain. Protein dalam bahan makanan sangat penting dalam proses kehidupan organisme yang heterotrof penting dalam proses kehidupan organisme yang heterotrof seperti hewan dan manusia (Sudarmadji, 1989).
seperti hewan dan manusia (Sudarmadji, 1989).
Sebagai zat pembangun, protein merupakan bahan Sebagai zat pembangun, protein merupakan bahan pembentuk jaringan-jaringan baru yang selalu terjadi dalam pembentuk jaringan-jaringan baru yang selalu terjadi dalam tubuh. Protein juga mengganti jaringan tubuh yang rusak dan tubuh. Protein juga mengganti jaringan tubuh yang rusak dan yang perlu dirombak. Fungsi utama protein bagi tubuh ialah yang perlu dirombak. Fungsi utama protein bagi tubuh ialah untuk membentuk jaringan baru dan mempertahankan untuk membentuk jaringan baru dan mempertahankan jaringan
jaringan yang yang telah telah ada. ada. Protein Protein juga juga digunakan digunakan sebagaisebagai bahan bakar apabila keperluan energy tubuh tidak terpenuhi bahan bakar apabila keperluan energy tubuh tidak terpenuhi oleh karbohidrat dan lemak. Protein ikut pula mengatur oleh karbohidrat dan lemak. Protein ikut pula mengatur berbagai proses tubuh. Protein mengatur keseimbangan berbagai proses tubuh. Protein mengatur keseimbangan cairan dalam jaringan dan pembuluh darah, yaitu dengan cairan dalam jaringan dan pembuluh darah, yaitu dengan menimbulkan tekanan osmotic koloid yang dapat menarik menimbulkan tekanan osmotic koloid yang dapat menarik cairan dari jaringan kedalam pembuluh darah. Sifat amfoter cairan dari jaringan kedalam pembuluh darah. Sifat amfoter protein yang dapat bereaksi dengan asam dan basa, dapat protein yang dapat bereaksi dengan asam dan basa, dapat mengatur keseimbangan asam-basa dalam tubuh.dalam mengatur keseimbangan asam-basa dalam tubuh.dalam
setiap sel hidup, protein merupakan bagian yang sangat setiap sel hidup, protein merupakan bagian yang sangat penting. Pada sebagian besar jaringan tubuh, protein penting. Pada sebagian besar jaringan tubuh, protein merupakan komponen terbesar setelah air. Diperkirakan merupakan komponen terbesar setelah air. Diperkirakan separuh atau 50% dari berat kering sel dalam jaringan seperti separuh atau 50% dari berat kering sel dalam jaringan seperti misalnya hati dan daging terdiri dari protein, dan dalam misalnya hati dan daging terdiri dari protein, dan dalam tenunan segar sekitar 20%. Protein dalam tubuh manusia, tenunan segar sekitar 20%. Protein dalam tubuh manusia, terutama dalam jaringan, bertindak sebagai bahan membrane terutama dalam jaringan, bertindak sebagai bahan membrane sel, dapat membentuk jaringan pengikat misalnya kolagen dan sel, dapat membentuk jaringan pengikat misalnya kolagen dan elastin serta membentuk protein yang
elastin serta membentuk protein yang inert inert seperti rambut dan seperti rambut dan kuku. Disamping itu protein dapat bekerja sebagai enzim, kuku. Disamping itu protein dapat bekerja sebagai enzim, bertindak sebagai plasma, membentuk antibodi, membentuk bertindak sebagai plasma, membentuk antibodi, membentuk kompleks dengan molekul lain, serta dapat bertindak sebagai kompleks dengan molekul lain, serta dapat bertindak sebagai bagian sel yang bergerak (protein otot). Kekurangan protein bagian sel yang bergerak (protein otot). Kekurangan protein dalam waktu lamadapat mengganggu berbagai proses dalam dalam waktu lamadapat mengganggu berbagai proses dalam tubuh dan menurunkan daya tahan tubuh dan menurunkan tubuh dan menurunkan daya tahan tubuh dan menurunkan daya tahan tubuh terhadap penyakit (Winarno, 1992).
daya tahan tubuh terhadap penyakit (Winarno, 1992). Beberapa ciri utama molekul protein yaitu :
Beberapa ciri utama molekul protein yaitu : Berat molekulnya besar
Berat molekulnya besar (ribuan sampai jutaan, sehingga (ribuan sampai jutaan, sehingga merupakan suatu makromolekul),
merupakan suatu makromolekul), umumnya terdiri atas 20umumnya terdiri atas 20 macam asam amino
macam asam amino. Asam amino berikatan (secara kovalen). Asam amino berikatan (secara kovalen) satu dengan yang lain dalam variasi urutan yang satu dengan yang lain dalam variasi urutan yang bermacam-macam, membentuk suatu rantai polipeptida. Ikatan peptida macam, membentuk suatu rantai polipeptida. Ikatan peptida merupakan ikatan antara gugus
merupakan ikatan antara gugus -karboksil dari asam amino-karboksil dari asam amino
yang satu dengan gugus
yang satu dengan gugus -amino yang lainnya.-amino yang lainnya. TerdapatnyaTerdapatnya ikatan kimia lain
ikatan kimia lain yang yang menyebabkan menyebabkan terbentuknyaterbentuknya lengkungan-lengkungan rantai polipetida menjadi struktur tiga lengkungan-lengkungan rantai polipetida menjadi struktur tiga dimensi protein. Sebagai contoh misalnya ikatan hidrogen, dimensi protein. Sebagai contoh misalnya ikatan hidrogen, ikatan hidrofob (ikatan apolar), iakatan ion atau ikatan ikatan hidrofob (ikatan apolar), iakatan ion atau ikatan elektrostatik dan ikatan Van der Waals (Wirahadikusumah, elektrostatik dan ikatan Van der Waals (Wirahadikusumah, 1989).
1989).
1.2.
1.2.
Tujuan PercobaanTujuan PercobaanTujuan Uji Logam Berat adalah untuk mengendapkan Tujuan Uji Logam Berat adalah untuk mengendapkan protein dengan menambahkan ion logam berat dan untuk protein dengan menambahkan ion logam berat dan untuk mengetahui kereaktifan logam berat tertentu dalam suatu mengetahui kereaktifan logam berat tertentu dalam suatu protein.
protein. . .
1.3.
1.3.Prinsip PercobaanPrinsip Percobaan
Prinsip percobaan Uji Logam Berat adalah Prinsip percobaan Uji Logam Berat adalah berdasarkan pada pH tertentu (asam atau basa) yang berdasarkan pada pH tertentu (asam atau basa) yang menyebabkan protein akan bermuatan negatif (anion) menyebabkan protein akan bermuatan negatif (anion) sehingga dapat bereaksi dengan ion logam positif.
sehingga dapat bereaksi dengan ion logam positif.
1.4.
1.4.Reaksi percobaanReaksi percobaan
Gambar 1. Reaksi Uji Logam Berat Gambar 1. Reaksi Uji Logam Berat
R
R
C
C
H
H
C
C
O
O
H
H
NH
NH
22O
O
+
+
Fe
Fe
2+2+Na
Na
22CO
CO
332Na
2Na
+++
+
R
R
CH
CH
C
C
OF
OF
NH
NH
22O
II METODE PERCOBAAN II METODE PERCOBAAN
Bab ini akan menguraikan mengenai : (1) Bahan yang Bab ini akan menguraikan mengenai : (1) Bahan yang Digunakan, (2) Pereaksi yang Digunakan, (3) Alat yang Digunakan, (2) Pereaksi yang Digunakan, (3) Alat yang Digunakan, dan (4) Metode percobaan
Digunakan, dan (4) Metode percobaan
2.1. Bahan yang Digunakan 2.1. Bahan yang Digunakan
Bahan yang di gunakan dalam uji logam berat adalah Bahan yang di gunakan dalam uji logam berat adalah sampel H ( Cocoa) sampel E (sari kacang hijau), sampel M ( sampel H ( Cocoa) sampel E (sari kacang hijau), sampel M ( ektra joss) sampel A (Smoke Beef)
ektra joss) sampel A (Smoke Beef)
2.2. Pereaksi yang Digunakan 2.2. Pereaksi yang Digunakan
Pereaksi yang di gunakan dalam uji logam berat Pereaksi yang di gunakan dalam uji logam berat adalah Na
adalah Na22COCO331%1%, CuSo, CuSo44, AgNO, AgNO33, HgCl, HgCl2,2,FeClFeCl2,2,PbClPbCl
2.3. Alat yang Digunakan 2.3. Alat yang Digunakan
Alat
Alat yang yang di di gunakan gunakan dalam dalam uji uji pengaruh pengaruh pH pH adalahadalah tabung reaksi sejumblah sampel , pipiet tetes , dan indikator tabung reaksi sejumblah sampel , pipiet tetes , dan indikator pH.
pH.
2.4. Metode Percobaan 2.4. Metode Percobaan
Metode percobaan yang digunakan dalam Uji Metode percobaan yang digunakan dalam Uji konsentrasi su
2 ml 2 ml pro
proteintein 3 t3 tetetes es NaNa22COCO33
10 tetes
10 tetes
Lar. Logam
Lar. Logam
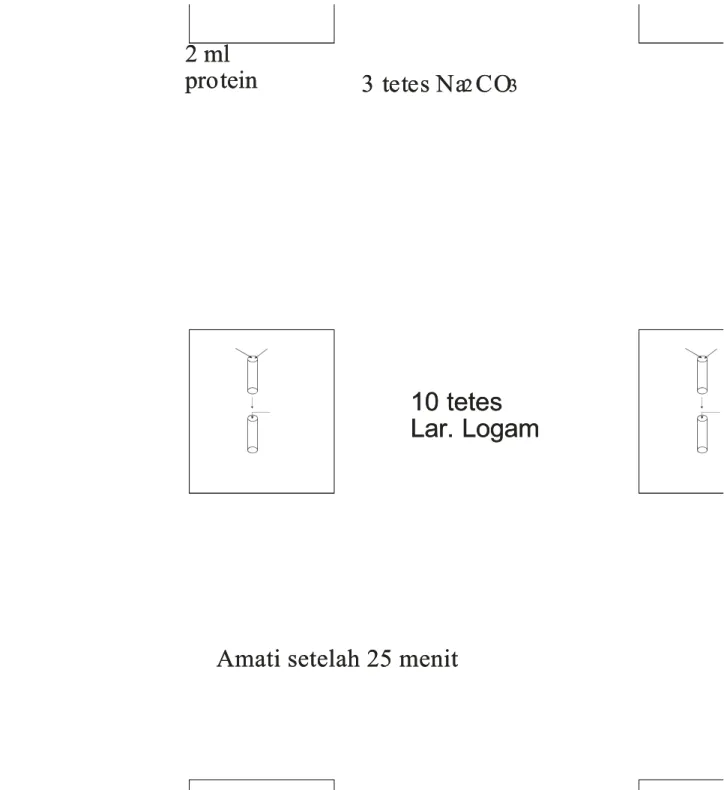
Amati setelah 25 menit Amati setelah 25 menit
Gambar 2. Metode Percobaan Uji Logam Berat Gambar 2. Metode Percobaan Uji Logam Berat
III HASIL PENGAMATAN III HASIL PENGAMATAN
Bab ini akan menguraikan mengenai : (1) Hasil Bab ini akan menguraikan mengenai : (1) Hasil Pengamatan dan, (2) Pembahasan.
Pengamatan dan, (2) Pembahasan.
3.1. Hasil Pengamatan 3.1. Hasil Pengamatan
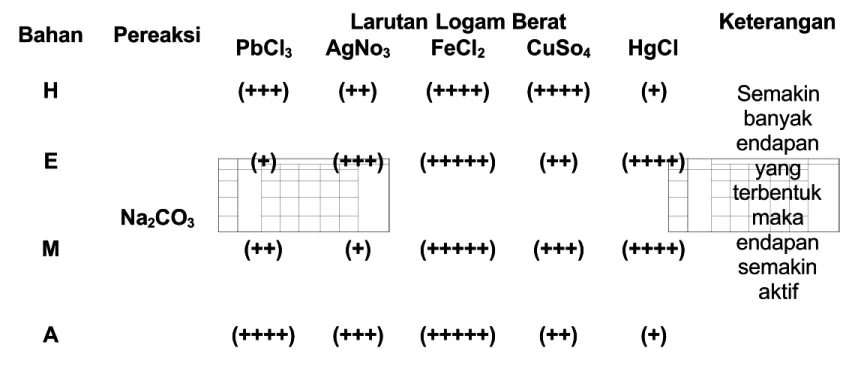
Tabel 1. Hasil Pengamatan Uji Logam Berat Tabel 1. Hasil Pengamatan Uji Logam Berat
Bahan Pereaksi
Bahan Pereaksi Larutan Larutan Logam Logam Berat Berat KeteranganKeterangan PbCl
PbCl33 AgNoAgNo33 FeClFeCl22 CuSoCuSo44 HgClHgCl
Semakin Semakin banyak banyak endapan endapan yang yang terbentuk terbentuk maka maka endapan endapan semakin semakin aktif aktif H H Na Na22COCO33 (+++) (+++) (++) (++) (++++) (++++) (++++) (++++) (+)(+) E E (+) (+) (+++)(+++) (+++++) (+++++) (++) (++) (++++)(++++) M M (++) (++) (+)(+) (+++++) (+++++) (+++) (+++) (++++)(++++) A A (++++) (++++) (+++)(+++) (+++++) (+++++) (++) (++) (+)(+) Sumber : Hasil I :
Sumber : Hasil I : Shinta dan Fitriani, Kelompok A, Meja 5,Shinta dan Fitriani, Kelompok A, Meja 5, 2014
2014
Hasil II : Laboratorium Biokimia Pangan, 2014 Hasil II : Laboratorium Biokimia Pangan, 2014
Gambar 3. Hasil Pengamatan Uji Logam Berat Gambar 3. Hasil Pengamatan Uji Logam Berat
3.2 Pembahasan 3.2 Pembahasan
Hasil dari percobaan Uji Logam Berat didapatkan hasil Hasil dari percobaan Uji Logam Berat didapatkan hasil bahwa Fe>Pb>Cu>Hg>Ag, semakin banyak endapan yang bahwa Fe>Pb>Cu>Hg>Ag, semakin banyak endapan yang terbentuk maka endapan semakin aktif.
terbentuk maka endapan semakin aktif.
Sebagian besar protein dapat diendapkan dari larutan air Sebagian besar protein dapat diendapkan dari larutan air dengan penambahan asam tertentu, seperti misalnya, asam dengan penambahan asam tertentu, seperti misalnya, asam triklorasetat dan asam perklorat. Penambahan asam ini triklorasetat dan asam perklorat. Penambahan asam ini menyebabkan terbentuknya garam protein yang tidak larut. menyebabkan terbentuknya garam protein yang tidak larut. Zat pengendap lainnya adalah asam tungstat, fosfotungstat, Zat pengendap lainnya adalah asam tungstat, fosfotungstat, dan metafosat. Protein dapat juga diendapkan dengan kation dan metafosat. Protein dapat juga diendapkan dengan kation tertentu seperti Zn
Protein mempunyai titik isolistrik yang berbeda-beda Protein mempunyai titik isolistrik yang berbeda-beda dengan yang lainnya. Titik isolistrik protein mempunyai arti dengan yang lainnya. Titik isolistrik protein mempunyai arti penting karena pada umumnya sifat fisika dan kimia erat penting karena pada umumnya sifat fisika dan kimia erat hubungannya dengan pH isolistrik ini. Pada pH di atas titik hubungannya dengan pH isolistrik ini. Pada pH di atas titik isolistrik protein bermuatan negatif, sedangkan di bawah titik isolistrik protein bermuatan negatif, sedangkan di bawah titik isolistrik protein bermuatan positif. Oleh karena itu untuk isolistrik protein bermuatan positif. Oleh karena itu untuk mengendapkan suatu protein dengan ion logam, diperlukan mengendapkan suatu protein dengan ion logam, diperlukan pH larutan di atas titik isolistrik, sedangkan pengendapan oleh pH larutan di atas titik isolistrik, sedangkan pengendapan oleh ion negatif memerlukan pH di bawah titik isolistrik. Ion-ion ion negatif memerlukan pH di bawah titik isolistrik. Ion-ion positif yang dapat mengendapkan protein antara lain ialah positif yang dapat mengendapkan protein antara lain ialah Ag
Ag++, Ca, Ca++++, Zn, Zn++++, Hg, Hg++++, Fe, Fe++++, Cu, Cu++++, dan Pb, dan Pb++++ (Poedjiadi, 2005). (Poedjiadi, 2005). Tembaga adalah logam merah muda, yang lunak, dapat Tembaga adalah logam merah muda, yang lunak, dapat ditempa, dan liat. Ia melebur pada 1038
ditempa, dan liat. Ia melebur pada 103800C. Karena potensialC. Karena potensial elektrode standarnya posotif, (+0,34V untuk pasangan elektrode standarnya posotif, (+0,34V untuk pasangan Cu/Cu
Cu/Cu2+2+), ia tak larut dalam asam klorida dan asam sulfat), ia tak larut dalam asam klorida dan asam sulfat encer, meskipun dengan adanya oksigen ia bisa larut sedikit. encer, meskipun dengan adanya oksigen ia bisa larut sedikit. Garam-garam tembaga(II) umumnya berwarna biru, baik Garam-garam tembaga(II) umumnya berwarna biru, baik dalam bentuk hidrat, padat, maupun dalam larutan air
dalam bentuk hidrat, padat, maupun dalam larutan air (Svehla,(Svehla, 1985).
1985).
Perak yang direaksikan dengan natrium karbonat akan Perak yang direaksikan dengan natrium karbonat akan menghasilkan endapan putih kekuningan membentuk perak menghasilkan endapan putih kekuningan membentuk perak karbonat (Svehla, 1985).
karbonat (Svehla, 1985).
Merkurium adalah logam cair yang putih keperakan pada Merkurium adalah logam cair yang putih keperakan pada suhu biasa, dan mempunyai rapatan 13, 534 g ml
suhu biasa, dan mempunyai rapatan 13, 534 g ml-1-1 pada pada 25
2500C. Ia tak dipengaruhi oleh asam klorida atau asam sulfatC. Ia tak dipengaruhi oleh asam klorida atau asam sulfat encer (2M), tetapi mudah bereaksi dengan asam nitrat encer (2M), tetapi mudah bereaksi dengan asam nitrat (Svehla, 1985).
(Svehla, 1985).
Besi yang murni adalah logam berwarna putih-perak, yang Besi yang murni adalah logam berwarna putih-perak, yang kukuh dan liat. Ia melebur pada 1535
kukuh dan liat. Ia melebur pada 153500C. Jarang terdapat besiC. Jarang terdapat besi komersial yang murni; biasanya besi mengandung sejumlah komersial yang murni; biasanya besi mengandung sejumlah kecil karbida, silisida, fosfida, dan sulfida dari besi, serta kecil karbida, silisida, fosfida, dan sulfida dari besi, serta sedikit grafit. Zat-zat pencemar ini memainkan peranan sedikit grafit. Zat-zat pencemar ini memainkan peranan penting dalam kekuatan struktur besi. Asam
penting dalam kekuatan struktur besi. Asam klorida encer atauklorida encer atau pekat dan asam sulfat encer dapat melarutkan besi (Svehla, pekat dan asam sulfat encer dapat melarutkan besi (Svehla, 1985).
1985).
Timbel adalah logam yang berwarna abu-abu kebiruan, Timbel adalah logam yang berwarna abu-abu kebiruan, dengan rapatan yang tinggi (11,48 g ml
dengan rapatan yang tinggi (11,48 g ml-1-1pada suhu kamar). Iapada suhu kamar). Ia mudah melarutkan dalam asam nitrat yang pekatnya (8M), mudah melarutkan dalam asam nitrat yang pekatnya (8M), dan terbentuk juga nitrogen oksida. Dengan natrium karbonat dan terbentuk juga nitrogen oksida. Dengan natrium karbonat
akan membentuk endapan putih campuran timbel karbonat akan membentuk endapan putih campuran timbel karbonat dan timbel hidroksida (Svehla, 1985).
IV KESIMPULAN DAN SARAN IV KESIMPULAN DAN SARAN
Bab ini akan menguraikan mengenai : (1) Kesimpulan Bab ini akan menguraikan mengenai : (1) Kesimpulan dan (2) Saran.
dan (2) Saran.
4.1 Kesimpulan 4.1 Kesimpulan
Hasil dari percobaan Uji Logam Berat didapatkan hasil Hasil dari percobaan Uji Logam Berat didapatkan hasil bahwa Fe>Pb>Cu>Hg>Ag, semakin banyak endapan yang bahwa Fe>Pb>Cu>Hg>Ag, semakin banyak endapan yang terbentuk maka endapan semakin aktif.
terbentuk maka endapan semakin aktif. ..
4.2 Saran 4.2 Saran
Sebaiknya praktikan memahami terlebih dahulu Sebaiknya praktikan memahami terlebih dahulu metodeyang akan dilakukan. Saat mengambil sampel metodeyang akan dilakukan. Saat mengambil sampel berbedasebaiknya menggunakan pipet berbeda agar sampel berbedasebaiknya menggunakan pipet berbeda agar sampel tidakbercampur dan alat yang digunakan harus dalam tidakbercampur dan alat yang digunakan harus dalam keadaanbersih.
Daftar Pustaka Daftar Pustaka
Anonim.
Anonim. 2011.2011. AlbuminAlbumin. www.google.com/Korantempo. 26. www.google.com/Korantempo. 26 Maret 2011.
Maret 2011. Anonim. 2011.
Anonim. 2011. ProteinProtein.. http://ms.wikipedia.org/wiki/Proteinhttp://ms.wikipedia.org/wiki/Protein.. 26 26 Maret 2011.
Maret 2011. Almatsier,
Almatsier, Sunita. Sunita. 2001.2001. Prinsip Dasar Ilmu GiziPrinsip Dasar Ilmu Gizi. Penerbit. Penerbit PT. Gramedia Pustaka Utama. Jakarta.
PT. Gramedia Pustaka Utama. Jakarta. deMan, John. 1997.
deMan, John. 1997. Kimia Makanan.Kimia Makanan. Penerbit ITB. Bandung.Penerbit ITB. Bandung. Poedjiadi, Anna. 2005.
Poedjiadi, Anna. 2005. Dasar-Dasar Biokimia.Dasar-Dasar Biokimia. PenerbitPenerbit Universitas Indonesia. Jakarta.
Universitas Indonesia. Jakarta. Sudarmadji, Slamet, dkk. 1989.
Sudarmadji, Slamet, dkk. 1989. Analisa Bahan Makanan danAnalisa Bahan Makanan dan Pertanian.
Pertanian. Edisi kedua, cetakan pertama. PenerbitEdisi kedua, cetakan pertama. Penerbit Liberty, Yogyakarta.
Liberty, Yogyakarta. Svehla, G. 1985.
Svehla, G. 1985. Analisis Kualitatif Makro dan SemimikroAnalisis Kualitatif Makro dan Semimikro .. Edisi kelima. Penerbit PT. Kalman Media Pusaka, Edisi kelima. Penerbit PT. Kalman Media Pusaka, Jakarta.
Jakarta.
Winarno, F.G. 1992.
Winarno, F.G. 1992. Kimia PanganKimia Pangan dan Gizi.dan Gizi. Cetakan keCetakan ke delapan. Penerbit PT. Gramedia Pustaka Utama. delapan. Penerbit PT. Gramedia Pustaka Utama. Jakarta
Jakarta
Wirahadikusumah, Muhammad. 1989.
Wirahadikusumah, Muhammad. 1989. Biokimia: Protein,Biokimia: Protein, Enzim, dan Asam Nukleat