BAB 2
TINJAUAN PUSTAKA
2.1. Fisiologi Nyeri
Nyeri dapat didefinisikan sebagai pengalaman sensori dan emosional yang tidak menyenangkan yang diakibatkan oleh adanya kerusakan jaringan atau potensial terjadi kerusakan jaringan (International Association for study of Pain). Dari definisi di atas dapat diketahui adanya hubungan pengaruh obyektif (aspek fisiologi dari nyeri) dan subyektif (aspek komponen emosi dan kejiwaan). Individualisme rasa nyeri ini sulit dinilai secara obyektif, walaupun dokter telah melakukan observasi atau menggunakan alat monitor . Baku emas untuk mengetahui seseorang berada dalam keadaan nyeri ataupun tidak adalah dengan menanyakan langsung.
Dalam keadaan fisiologi , stimulus dengan intensitas rendah menimbulkan sensasi rasa nyeri ringan/kurang menyakitkan yang diaktifkan oleh serabut saraf A beta, sedang stimulus dengan intensitas tinggi menimbulkan sensasi nyeri berat yang diaktifkan oleh serabut saraf A delta dan serabut saraf C . Pada keadaan pasca operasi , sistem saraf sensori ini mengalami hipersensitifitas yang akan menyebabkan juga perubahan fungsi sensori di kornu dorsalis medula spinalis sehingga dengan stimuli yang rendah menyebabkan rasa nyeri yang nyata.
18,19,20,21,22
Nyeri karena pembedahan mengalami sedikitnya dua perubahan,pertama karena pembedahan itu sendiri,menyebabkan rangsang nosiseptif.Kedua, setelah pembedahan karena terjadinya respon inflamasi pada daerah sekitar operasi
dimana terjadi pelepasan zat –zat kimia oleh jaringan yang rusak dan sel – sel inflamasi. Zat – zat tersebut antara lain prostaglandin, histamin, serotonin, bradikinin, substansi P, Leukotrin dimana zat – zat tersebut berperan sebagai tranduksi dari nyeri. 18,19,23,24
2.2. Mekanisme Nyeri
Nyeri merupakan suatu bentuk peringatan akan adanya bahaya kerusakan jaringan. Pengalaman sensoris pada nyeri akut disebabkan oleh stimulus noksius yang diperantarai oleh sistem sensorik nosiseptif. Sistem ini berjalan mulai dari perifer melalui medulla spinalis, batang otak, thalamus dan korteks serebri. Apabila telah terjadi kerusakan jaringan, maka sistem nosiseptif akan bergeser fungsinya dari fungsi protektif menjadi fungsi yang membantu perbaikan jaringan yang rusak.
Nyeri inflamasi merupakan salah satu cara untuk mempercepat perbaikan kerusakan jaringan. Sensitifitas akan meningkat, sehingga stimulus non noksius atau noksius ringan yang mengenai bagian yang meradang akan menyebabkan nyeri. Nyeri inflamasi akan menurunkan derajat kerusakan dan menghilangkan respon inflamasi.22,23
2.2.1. Sensitisasi Perifer
Cedera atau inflamasi jaringan akan menyebabkan munculnya perubahan lingkungan kimiawi pada akhir nosiseptor. Sel yang rusak akan melepaskan komponen intraselulernya seperti adenosine trifosfat, ion K+, pH menurun, sel
inflamasi akan menghasilkan sitokin, chemokine dan growth factor. Beberapa komponen diatas akan langsung merangsang nosiseptor (nociceptor activators) dan komponen lainnya akan menyebabkan nosiseptor menjadi lebih hipersensitif terhadap rangsangan berikutnya (nociceptor sensitizers).
Komponen sensitisasi, misalnya prostaglandin E
23,24
2 akan mereduksi ambang
aktivasi nosiseptor dan meningkatkan kepekaan ujung saraf dengan cara berikatan pada reseptor spesifik di nosiseptor. Berbagai komponen yang menyebabkan sensitisasi akan muncul secara bersamaan, penghambatan hanya pada salah satu substansi kimia tersebut tidak akan menghilangkan sensitisasi perifer. Sensitisasi perifer akan menurunkan ambang rangsang dan berperan dalam meningkatkan sensitivitas nyeri di tempat cedera atau inflamasi.23,24
2.2.2. Sensitisasi Sentral
Sama halnya dengan sistem nosiseptor perifer, maka transmisi nosiseptor di sentral juga dapat mengalami sensitisasi. Sensitisasi sentral dan perifer bertanggung jawab terhadap munculnya hipersensitivitas nyeri setelah cedera. Sensitisasi sentral memfasilitasi dan memperkuat transfer sinaptik dari nosiseptor ke neuron kornu dorsalis. Pada awalnya proses ini dipacu oleh input nosiseptor ke medulla spinalis (activity dependent), kemudian terjadi perubahan molekuler neuron (transcription dependent).
Sensitisasi sentral dan perifer merupakan contoh plastisitas sistem saraf, dimana terjadi perubahan fungsi sebagai respon perubahan input (kerusakan jaringan). Dalam beberapa detik setelah kerusakan jaringan yang hebat akan terjadi aliran sensoris yang masif kedalam medulla spinalis. Reaksi ini akan
menyebabkan jaringan saraf didalam medulla spinalis menjadi hiperresponsif.Reaksi ini menyebabkan munculnya nyeri akibat stimulus non noksius dan daerah yang jauh dari jaringan cedera juga menjadi sensitif rangsangan nyeri.
2.3. Nosiseptor (reseptor nyeri)
23
Nosiseptor adalah reseptor ujung saraf bebas yang ada di kulit, otot, persendian, viseral dan vascular. Nosiseptor-nosiseptor ini bertanggung jawab pada kehadiran stimulus noxious yang berasal dari kimia, suhu (panas, dingin), atau perubahan mekanikal. Pada jaringan normal, nosiseptor tidak aktif sampai adanya stimulus yang memiliki energi yang cukup untuk melampaui ambang batas stimulus (resting). Nosiseptor mencegah perambatan sinyal acak (skrining fungsi) ke CNS untuk interpretasi nyeri.19,22,25,26
Saraf nosiseptor bersinap di dorsal horn dari spinal cord dengan lokal interneuron.Saraf ini yang memproyeksikan informasi nosiseptif ke pusat yang lebih tinggi pada batang otak dan thalamus. Berbeda dengan reseptor sensorik lainnya, reseptor nyeri tidak bisa beradaptasi. Kegagalan reseptor nyeri beradaptasi untuk proteksi karena hal tersebut bisa menyebabkan individu untuk tetap pada kerusakan jaringan yang berkelanjutan. Setelah kerusakan terjadi, nyeri biasanya minimal. Mula datang nyeri pada jaringan karena iskemi akut berhubungan dengan kecepatan metabolisme. Sebagai contoh, nyeri terjadi pada saat beraktifitas kerena iskemi otot skeletal pada 15 sampai 20 detik.
19,22,27
Tipe nosiseptor spesifik bereaksi pada tipe stimulus yang berbeda. Nosiseptor C tertentu dan nosiseptor A-delta bereaksi hanya pada stimulus panas
atau dingin, dimana yang lainnya bereaksi pada stimulus yang lain. Beberapa reseptor A-beta mempunyai aktivitas nociceptor-like. Serat–serat sensorik mekanoreseptor bisa diikutkan untuk transmisi sinyal yang akan menginterpretasi nyeri ketika daerah sekitar terjadi inflamasi. Allodynia mekanikal (nyeri atau sensasi terbakar karena sentuhan ringan) dihasilkan mekanoreseptor A-beta.
Nosiseptor viseral, tidak seperti nosiseptor kutaneus, tidak didisain hanya sebagai reseptor nyeri karena organ internal jarang terpapar pada keadaan yang merusak. Banyak stimulus yang merusak (memotong, membakar, kepitan) tidak menghasilkan nyeri bila dilakukan pada struktur viseralis. Selain itu, inflamasi, iskemi, regangan mesenterik, dilatasi, atau spasme viseralis bisa menyebabkab spasme berat. Stimulus ini biasanya dihubungkan dengan proses patologis, dan nyeri yang dicetuskan untuk mempertahankan fungsi.
19,22,27.
19,22,27
2.4. Perjalanan Nyeri (Nociceptive Pathway)
Perjalanan nyeri termasuk suatu rangkaian proses neurofisiologis kompleks yang disebut sebagai nosiseptif (nociception) yang merefleksikan 4 proses komponen yang nyata yaitu transduksi, transmisi, modulasi dan persepsi, dimana terjadinya stimuli yang kuat diperifer sampai dirasakannya nyeri di susunan saraf pusat (cortex cerebri).
2.4.1. Proses transduksi
19,27,28,29,
Proses dimana stimulus noxious diubah ke impuls elektrikal pada ujung nervus. Suatu stimuli kuat (noxion stimuli) seperti tekanan fisik kimia, suhu dirubah menjadi suatu aktifitas listrik yang akan diterima ujung-ujung saraf perifer (nerve ending) atau organ-organ tubuh (reseptor meisneri, merkel, corpusculum paccini,
golgi mazoni). Kerusakan jaringan karena trauma baik trauma pembedahan atau trauma lainnya menyebabkan sintesa prostaglandin, dimana prostaglandin inilah yang akan menyebabkan sensitisasi dari reseptor-reseptor nosiseptif dan dikeluarkan zat-zat mediator nyeri seperti histamin, serotonin yang akan menimbulkan sensasi nyeri. Keadaan ini dikenal sebagai sensitisasi perifer.
2.4.2. Proses transmisi
19,27,28,29,
Proses penyaluran impuls melalui saraf sensori sebagai lanjutan proses transduksi melalui serabut A-delta dan serabut C dari perifer ke medulla spinalis, dimana impuls tersebut mengalami modulasi sebelum diteruskan ke thalamus oleh tractus spinothalamicus dan sebagian ke traktus spinoretikularis. Traktus spinoretikularis terutama membawa rangsangan dari organ-organ yang lebih dalam dan visceral serta berhubungan dengan nyeri yang lebih difus dan melibatkan emosi. Selain itu juga serabut-serabut saraf disini mempunyai sinaps interneuron dengan saraf-saraf berdiameter besar dan bermielin. Selanjutnya impuls disalurkan ke thalamus dan somatosensoris di cortex cerebri dan dirasakan sebagai persepsi nyeri.
2.4.3. Proses modulasi
19,27,28,29,
Proses perubahan transmisi nyeri terjadi disusunan saraf pusat (medulla spinalis dan otak). Proses terjadinya interaksi antara sistem analgesik endogen yang dihasilkan oleh tubuh kita dengan input nyeri yang masuk ke kornu posterior medulla spinalis merupakan proses ascenden yang dikontrol oleh otak. Analgesik endogen (enkefalin, endorphin, serotonin, noradrenalin) dapat menekan impuls
nyeri pada kornu posterior medulla spinalis. Dimana kornu posterior sebagai pintu dapat terbuka dan tertutup untuk menyalurkan impuls nyeri untuk analgesik endogen tersebut. Inilah yang menyebabkan persepsi nyeri sangat subjektif pada setiap orang.
2.4.4. Persepsi
19,27,28,29,
Hasil akhir dari proses interaksi yang kompleks dari proses tranduksi, transmisi dan modulasi yang pada akhirnya akan menghasilkan suatu proses subjektif yang dikenal sebagai persepsi nyeri, yang diperkirakan terjadi pada thalamus dengan korteks sebagai diskriminasi dari sensorik
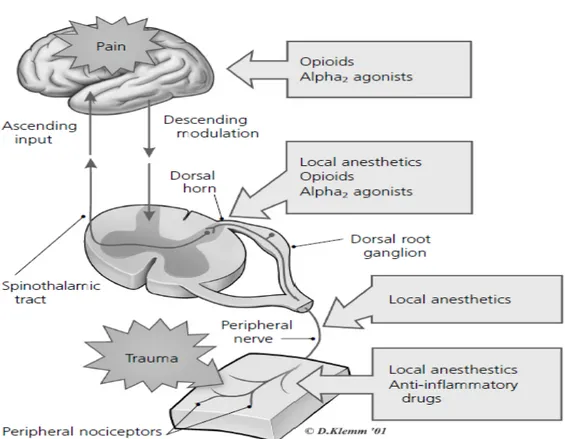
Gambar 2.1 Pain Pathway
2.5. Tramadol Hidrochloride
Tramadol Hidrochloride telah digunakan secara klinis di Jerman sejak 1970. Tramadol Hidrochloride adalah obat analgesi sintetik. Mekanisme pastinya tidak diketahui tetapi mirip dengan morpin. Seperti morpin, Tramadol Hidrochloride berikatan ke reseptor opioid di otak ,ini merupakan suatu yang penting untuk transmisi sensasi dari nyeri .
2.5.1. Farmakodinamik
Tramadol Hidrochloride adalah suatu analgesi sentral yang memiliki afinitas kuat terhadap mu reseptor dan memiliki afinitas yang lemah terhadap kappa dan delta reseptor.Tramadol meningkatkan fungsi dari spinal descending inhibitory pathway dengan menghambat reuptake neural dari norepinefrine dan 5-hydroxytryptamine (serotonin) dan merangsang pelepasan 5- 5-hydroxytryptamine di presinap. Pada pasien dengan nyeri pasca operasi, pemberian tramadol secara iv atau i.m. memiliki keberhasilan yang hampir sama dengan meperidin. Analgesi dimulai dalam satu jam dan mencapai puncak dalam dua jam. Tramadol telah terbukti efektif pada beberapa eksperimen dan memiliki efek samping seperti mual, muntah,mulut kering. Tramadol telah berhasil dalam pengobatan nyeri pasca operasi pada dosis tertentu, baik secara intravena maupun intramuskular. Mual dan muntah adalah efek samping yang sering dilaporkan. Dua enantiomer dari rasemik tramadol secara komplementer meningkatkan efektivitas analgesi dan meningkatkan profil tolerabilitas dari tramadol. Pada beberapa studi perbandingan, pemberian tramadol parenteral dosis tertentu efektif untuk nyeri pasca operasi sedang sampai parah. Peristiwa-peristiwa buruk yang paling umum (sampai dengan 20-25%) adalah mual, pusing, mengantuk, berkeringat, muntah dan mulut kering. Yang penting, tidak seperti opioid lainnya, tramadol tidak memiliki efek yang relevan secara klinis pada parameter pernafasan atau jantung pada dosis yang telah dianjurkan pada orang dewasa.32
2.5.2. Farmakokinetik
Tramadol Hidrochloride memiliki bioavaibilitas 68 % dengan konsentrasi puncak serum dalm waktu 2 jam. Tramadol Hidrochloride memiliki waktu paruh 5- 8 jam dan di ekskresi melalui ginjal. Dosis yang di rekomendasisikan 2,5 mg/KgBB sampai 5 mg/KgBB tiap 4 – 6 jam per hari. Dosis maksimal yang direkomendasikan 400mg/KgBB.
2.6.
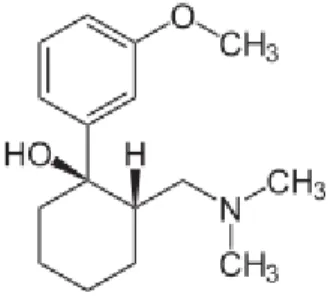
Gambar 2.2. Rumus bangun Tramadol hydrochloride
Klonidine
Klonidine adalah α2 adrenergik agonis yang diperkenalkan lebih dari dua decade sebagai obat anti hipertensi. Studi klinis telah menunjukkan bahwa Klonidine menurunkan pemakaian anestesi selama operasi dan meningkatkan analgesi setelah operasi. Klonidine dengan cepat dan hampir sepenuhnya terserap setelah pemberian dengan waktu max konsentrasi plasma 1,5-2 jam dan eliminasi dengan waktu paruh 8 jam sampai 12.
2.6.1.
33
Farmakodinamik
Klonidine dan agonis α 2 adrenergik lainnya bekerja dengan cara melakukan aktivasi reseptor α pada dua sinaps yang lokasi,yaitu presinaptik dan postsinaptik. Reseptor –reseptor ini terletak di pusat (susunan saraf pusat) dan
perifer (diluar SSP) yang jika dirangsang masing masing memberikan efek yang berbeda.34
Klonidine terutama bekerja pada sistem saraf pusat yang mengakibatkan berkurangnya pengaruh simpatis dan menurunnya tahanan perifer,tahanan vaskuler ginjal, denyut jantung dan tekanan darah. Yang penting adalah tidak adanya perubahan pada aliran darah ginjal dan kecepatan filtrasi glomerolus. Refleks postural yang normal tidak dipengaruhi, oleh karena itu gejala gejala ortostatiknya ringan dan jarang terjadi. Selama terapi jangka panjang, curah jantung akan kembali ke keadaan semula sedangkan tahanan perifer akan turun. Pada sebagian besar pasien yang diberikan klonidin akan terjadi penurunan denyut jantung , tetapi obat ini tidak mempengaruhi respon hemodinamik yang normal.35
Klonidine adalah agonis reseptor adrenergic α yang mempunyai afinitas lebih besar terhadap α2 daripada α 1 dengan rasio seleksi α2 :α1 = 200:1. Struktur agonis dari klonidin juga mengikat reseptor nonadrenergik lain yang dinyatakan sebagai reseptor klonidine, menghasilkan beberapa efek yang dianggap berasal dari reseptor α2 adrenergik. Sehingga klonidine merupakan agonis α2 adrenergik kerja langsung yang awalnya dikenal sebagai obat antihipertensi. Cara kerjanya dengan merangsang reseptor α2 di otak yang akan menurunkan curah jantung dan resistensi pembuluh darah perifer sehingga menurunkan tekanan darah.36
Klonidine mempunyai spesifisitas terhadap reseptor presinaptik α2 pada pusat vasomotor dibatang otak. Ikatan ini menurunkan kadar kalsium presinap dan menghambat pelepasan norepinefrin. Hasil akhirnya menurunkan tonus simpatetik. Selain itu lokus seruleus merupakan kelompok sel noradrenergic
terbesar di otak dan berperan penting untuk modulasi kesadaran dan tempat terbesar aksi hipnotik-sedatif dari agonis α2 adrenoreseptor dengan menstimulasi α2 adrenoreseptor. Klonidine adalah analgesi yang bekerja sentral pada locus seruleus di brainstem dan di spinal cord. Sebagai non-opioid analgesi, klonidine sebagai analgesi tanpa efek samping opioid, seperti
2.6.2.
depresi pernafasan,mual dan muntah. klonidine juga memiliki efek sedasi, mengurangi salivasi, menurunkan kebutuhan anesthesi, stabilisasi haemodinamik.
Farmakokinetik
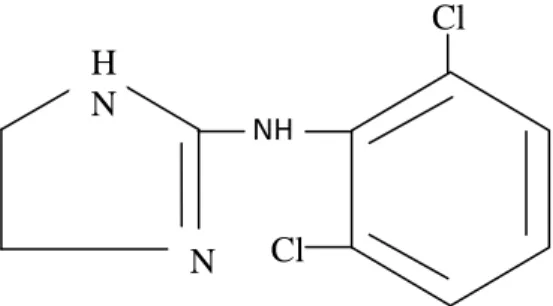
Formula klonidine C9H9C12N3 (N-2(2.6-dichlorophenyl)-4.5-dihydro-1H-imidazol-2-amine) dengan masa molekul 230.093g/mol. Bioavailabilitas klonidine 75-95% dengan ikatan protein 20-40%. Waktu paruhnya 9-12 jam dengan ekskresi melalui urin.37,38
Gambar 2.3.Rumus bangun klonidine H N N NH Cl Cl
2.7. KerangkaTeori Tramadol • Afinitas kuat terhadap µ reseptor • Meningkatkan fungsi desending inhibitory pathway • Efek samping (+) Klonidin • Aktivasi α2 agonis • Meningkatkan pelepasan β Tramadol
Kerusakan jaringan, saraf perifer, inflamasi NYERI Transmisi Modulasi Persepsi Rangsangan Noksius Pembedahan Analgesik non preemtif Analgesik preemtif
2.8. Kerangka Konsep
VAS
Tramadol Tramadol
Klonidin