AKUMULASI LOGAM BERAT TEMBAGA (Cu) DAN TIMBAL (Pb)
PADA POHON MANGROVE (Rhizopora mucronata)
DI PERAIRAN KARANGSONG, INDRAMAYU
MEILITA SYARIFAH
MANAJEMEN SUMBER DAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Akumulasi Logam Berat Tembaga (Cu) dan Timbal (Pb) Pada Pohon Mangrove (Rhizopora mucronata) di Perairan Karangsong, Indramayu adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juni 2013 Meilita Syarifah NIM C24090012
ABSTRAK
MEILITA SYARIFAH. Akumulasi Logam Berat Tembaga (Cu) dan Timbal (Pb) pada Pohon Mangrove (Rhizopora mucronata) di Perairan Karangsong, Indramayu. Dibimbing oleh AGUSTINUS M SAMOSIR dan SULISTIONO.
Mangrove memiliki banyak fungsi ekonomis dan ekologis salah satunya dapat menyerap, mengangkut dan menimbun materi termasuk zat-zat toksik. Tujuan dari penelitian ini adalah menganalisis kandungan logam berat Cu dan Pb dalam sedimen, akar dan daun pohon mangrove Rhizopora mucronata. Konsentrasi Cu di sedimen telah melebihi baku mutu menurut RNO. Kandungan Cu dan Pb pada akar lebih besar dibandingkan pada daun, begitu pula dengan nilai faktor biokonsentrasinya, BCF tertinggi yaitu BCF Pb pada akar sebesar 1,3116, sementara BCF Cu pada akar sebesar 0,5609. Hal tersebut mengindikasikan daya akumulasi akar jauh lebih tinggi daripada daun. Nilai Faktor Translokasi (TF) tertinggi dicapai oleh Pb yaitu sebesar 0,4075 sedangkan terendah pada Cu sebesar 0,3341. Translokasi logam dari akar ke daun untuk logam esensial (Cu) lebih rendah dibandingkan pada logam non esensial (Pb), hal tersebut menunjukkan bahwa mangrove menggunakan logam tersebut untuk aktivitas metabolisme dan pertumbuhan. Kemampuan mangrove dalam mengakumulasi logam berat ini masuk kedalam kategori rendah menurut indeks faktor konsentrasi. Kata kunci: Indramayu, Logam berat, Mangrove, Rhizopora mucronata.
ABSTRACT
MEILITA SYARIFAH. Accumulation Of Heavy Metal Cu and Pb in the Mangrove Tree (Rhizopora mucronata) in Karangsong Estuary, Indramayu. Supervised by AGUSTINUS M SAMOSIR and SULISTIONO.
Mangrove has many economical and ecological functions, one of its abilities is to absorb, transport and store substances including toxic materials. This research aim is to analyze the concentration of Cu and Pb in root, leave and substrat of mangrove Rhizopora mucronata and its bioaccumulation level. The concentration of Cu found in sediment exceed standar quality by RNO, which means the sediment has been contaminated by Cu. The content of Cu in the roots and leaves of mangrove is greater than Pb, so does the highest level of bioconcentration factor (BCF) was reached by BCF Pb in root at 1.3116 while BCF Cu in roots at 0,5609. This indicates that the potention of accumulation of roots is much higher than the leaves. The highest Translocation Factor (TF) was attained by Pb which is 0.4075 and the lowest is 0.3341 in Cu. Metal translocation from roots to leaves for essential metals (Cu) is lower than in non-essential metals (Pb), it shows that the mangrove use Cu for metabolic activity and growth. The ability of mangrove in accumulating this metals are still low in category according to Concentration Factor Index.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Manajemen Sumber Daya Perairan
AKUMULASI LOGAM BERAT TEMBAGA (Cu) DAN TIMBAL (Pb)
PADA POHON MANGROVE (Rhizopora mucronata)
DI PERAIRAN KARANGSONG, INDRAMAYU
MEILITA SYARIFAH
MANAJEMEN SUMBER DAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi Akumulasi Logam Berat Tembaga (Cu) dan Timbal (Pb) pada Pohon Mangrove (Rhizopora mucronata) di Perairan Karangsong, Indramayu.
Nama Meilita Syarifah
NIM C24090012
Disetujui oleh
Drlrjo.:
Ir Agustinus M Samosir, MPhil
Pembimbing I Pembimbing II Diketahui oleh
,
(t~2-~
~Dr ir M Mukhlis Kamal, MSc Ketua Departemen Tanggal Lulus:0 3 0
9
2
0
1
3
Judul Skripsi : Akumulasi Logam Berat Tembaga (Cu) dan Timbal (Pb) pada Pohon Mangrove (Rhizopora mucronata) di Perairan Karangsong, Indramayu.
Nama : Meilita Syarifah NIM : C24090012
Disetujui oleh
Ir Agustinus M Samosir, MPhil Pembimbing I Dr Ir Sulistiono, MSc Pembimbing II Diketahui oleh Dr Ir M Mukhlis Kamal, MSc Ketua Departemen Tanggal Lulus:
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah yang dilaksanakan sejak bulan januari 2013 dengan judul Akumulasi Logam Berat Tembaga (Cu) dan Timbal (Pb) pada Pohon Mangrove (Rhizopora mucronata) di Perairan Karangsong, Indramayu.
Pada kesempatan ini penulis mengucapkan terimakasih kepada Bapak Ir. Agustinus M Samosir, M.Phil selaku pembimbing I dan Bapak Dr. Ir Sulistiono, M.Sc selaku pembimbing II yang telah memberikan arahan dan masukan dalam penulisan karya ilmiah ini. Selain itu, penulis mengucapkan terimakasih kepada staff Laboratorium Biologi Makro 1, staff Laboratorium Pengujian Teknik Industri, serta Bapak Toyib dan keluarga. Ungkapan terima kasih juga disampaikan kepada Ayah, Ibu serta seluruh keluarga atas segala doa dan kasih sayangnya, tak lupa juga kepada seluruh staff Tata Usaha dan civitas MSP, teman-teman tim Indramayu, Cutra, Allsay, Nana, Iqra, teman-teman-teman-teman MSP 45, MSP 46, MSP 47, MSP 48, Niken, Fitri, Yulia, Deasy, Selvia, Nolalia, Alin, Panji, Arfianto, Rio, Devi, Tini, Anissa, Hilman, teman-teman Asrama Putri Darmaga, Ika, Teh Widya, Teh Imas, Maimuna, Desi Ratnassari, Zhulmi, Happy, Endang, Susan, atas segala doa, semangat, dukungan dan bantuannya.
Penulis menyadari masih banyak kekurangan dalam skripsi ini, oleh karena itu kritik dan saran yang membangun sangat diharapkan demi perbaikan di masa mendatang. Semoga skripsi ini bermanfaat.
Bogor, Juli 2013 Meilita Syarifah
DAFTAR ISI
DAFTAR ISI ... v DAFTAR TABEL ... vi DAFTAR GAMBAR ... vi DAFTAR LAMPIRAN ... vi PENDAHULUAN ... 1 Latar Belakang ... 1 Perumusan Masalah ... 1 Tujuan Penelitian ... 2 Manfaat Penelitian ... 2 METODE ... 2 Lokasi Penelitian ... 2 Pengumpulan Data ... 3 Analisis Data ... 4HASIL DAN PEMBAHASAN ... 5
Hasil ... 5
Pembahasan ... 11
SIMPULAN DAN SARAN ... 16
Simpulan ... 16
Saran ... 16
DAFTAR PUSTAKA ... 17
LAMPIRAN ... 19
DAFTAR TABEL
1. Indeks faktor biokonsentrasi ... 5
2. Kisaran suhu, pH, salinitas air di lokasi penelitian ... 6
3. Rata-rata kandungan logam berat Cu dan Pb pada akar dan daun ... 8
4. Matrix koefisien korelasi pada logam Cu ... 9
5. Matrix koefisien korelasi pada logam Pb ... 10
6. Akumulasi logam berat Cu dan Pb pada berbagai spesies mangrove ... 10
7. Nilai Faktor Konsentrasi (BCF) Cu dan Pb pada akar dan daun ... 11
8. Translokasi Logam berat Cu dan Pb di Karangsong, Indramayu ... 11
DAFTAR GAMBAR
1. Perumusan masalah ... 22. Peta lokasi penelitian ... 3
3. Komposisi tekstur sedimen di Karangsong, Indramayu ... 6
4. Basal area di Karangsong, Indramayu ... 6
5. Konsentrasi logam berat Cu pada sedimen ... 7
6. Konsentrasi logam berat Pb pada sedimen ... 7
7. Distribusi logam berat Cu pada sedimen, akar dan daun ... 9
8. Distribusi logam berat Pb pada sedimen, akar dan daun ... 9
DAFTAR LAMPIRAN
1. Alat dan bahan ... 192. Hasil pengukuran parameter fisika kimia ... 20
PENDAHULUAN
Latar Belakang
.
Seperti yang dilansir harian Seputar Indonesia (2012), dikatakan bahwa telah terjadi pencemaran di Sungai Prajagumiwang, yaitu sungai yang bermuara di pesisir Karangsong. Pencemaran ini disebabkan antara lain oleh limbah industri dan limbah rumah tangga. Karangsong merupakan salah satu kawasan pesisir yang banyak dimanfaatkan oleh masyarakat sekitar, sehingga terdapat berbagai aktivitas seperti pemukiman, pelayaran, wisata, industri, pertambakan, dan perikanan. Kondisi tersebut semakin meningkatkan ancaman terjadinya pencemaran karena masuknya limbah secara langsung ke perairan yang dapat menyebabkan kerusakan ekosistem estuari. Salah satunya pencemaran oleh logam berat.
Mangove merupakan salah satu ekosistem pesisir yang mempunyai peranan penting di daerah estuari. Mangrove memiliki banyak fungsi ekologi seperti tempat mencari makan, memijah dan berkembang biak bagi udang dan ikan serta kerang dan kepiting. Selain itu, ekosistem mangrove juga berfungsi sebagai perangkap sedimen, pencegah erosi dan pelindung pantai dari abrasi (Harty 1997 in Hamzah dan Setiawan 2010). Selain itu mangrove juga banyak memiliki fungsi ekonomis diantaranya yaitu beberapa jenis mangrove pada bagian tubuhnya dapat diolah untuk konsumsi, sedangkan mangrove jenis Rhizopora sp sampai saat ini pemanfaatannya untuk konsumsi belum ada.
Salah satu jenis mangrove dominan di pesisir Karangsong yaitu Rhizopora mucronata. Mangrove jenis ini memiliki akar penyangga, selain fungsinya untuk membantu tegaknya pohon, akar jenis ini juga dapat menahan dan memantapkan sedimen tanah, sehingga mencegah tersebarnya bahan pencemar ke area yang lebih luas. Oleh karena itu akar mangrove jenis ini dapat lebih optimal dalam menyerap logam berat. Organ akar dan daun pada mangrove berperan dalam penyerapan, pengangkutan dan penimbunan zat-zat, termasuk materi toksik, oleh karena itu penelitian ini dilakukan untuk mengetahui akumulasi logam berat pada bagian tubuh mangrove sehingga dapat dirumuskan manfaat dan kegunaannya dalam mengakumulasi logam berat.
Perumusan Masalah
Pemanfaaatan kawasan pesisir Karangsong oleh masyarakat dapat menyebabkan masuknya limbah ke perairan termasuk logam berat. Logam berat yang masuk ke perairan tersebut semakin lama akan mengendap dan terakumulasi pada sedimen, sehingga kemudian dapat terserap oleh mangrove dan terdistribusi ke seluruh bagian tubuh mangrove salah satunya yaitu pada bagian akar dan daunnya. Oleh karena itu salah satu manfaat lain yang dimiliki oleh mangrove yaitu dapat mengurangi konsentrasi bahan pencemar yang terdapat di lingkungan.
2
Gambar 1 Perumusan masalah
Tujuan Penelitian
Penelitian ini bertujuan untuk menganalisis kandungan logam berat Tembaga (Cu) dan Timbal (Pb) dalam sedimen, akar, serta daun pohon mangrove Rhizopora mucronata dan untuk mengetahui kemampuan vegetasi tersebut dalam mengakumulasi logam berat Cu dan Pb sehingga dapat dijadikan akumulator bahan pencemar logam berat di kawasan hutan mangrove.
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan gambaran akumulasi logam berat Cu dan Pb secara kuantitatif pada sedimen, akar, serta daun pohon Rhizopora mucronata di kawasan perairan karangsong, Indramayu, sebagai sumber informasi bagi masyarakat serta pengelola yang membutuhkan mengenai peranan Rhizopora mucronata dalam mengurai pencemaran logam berat dan untuk kepentingan pengelolaan sumberdaya pesisir, serta sebagai dasar kebijakan oleh pemerintah khususnya daerah dalam pengelolaan sumber daya pesisir.
METODE
Lokasi Penelitian
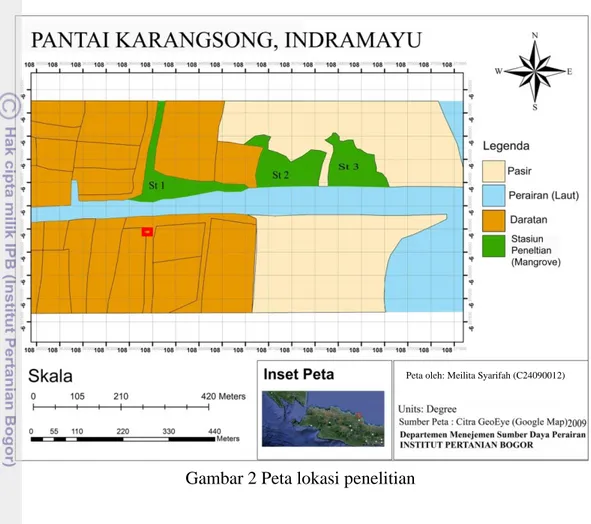
Lokasi pengambilan contoh di Perairan Karangsong, Indramayu (Gambar
2). Penelitian ini dilakukan pada bulan Januari hingga Maret 2013. Identifikasi mangrove dilakukan di Laboratorium Biologi Makro 1, Departemen Manajemen Sumber Daya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian
Sumber logam berat : Alamiah Aktivitas manusia Pencemaran Logam Berat Akumulasi di Kawasan estuari
Akumulasi pada sedimen, akar dan daun mangrove (Rhizopora mucronata)
Pengelolaan
Faktor Lingkungan : Fisika kimia air
3 Bogor. Analisis kandungan logam berat di lakukan di Laboratorium Pengujian, Departemen Teknologi Industri, Fakultas Teknologi Pertanian, Institut Pertanian Bogor. Alat dan bahan yang digunakan terlampir pada Lampiran 1.
Gambar 2 Peta lokasi penelitian
Pengumpulan Data
Daerah penelitian dibagi menjadi tiga Stasiun, Stasiun satu paling dekat dengan pelabuhan dan tempat pemukiman, sedangkan Stasiun tiga paling dekat ke laut lepas. Setiap Stasiun dilakukan tiga kali ulangan. Pengukuran yang dilakukan secara insitu yaitu pengukuran parameter fisika kimia perairan yang terdiri dari suhu, pH, dan salinitas. Pengukuran suhu, pH, dan salinitas dilakukan dengan menggunakan termometer, pH stick dan refraktometer.
Sedangkan untuk mengetahui luas tutupan basal dilakukan pengukuran lingkar batang pohon mangrove dalam transek 10m x10m. Selanjutnya dilakukan pengambilan sampel pohon mangrove, yaitu terdiri dari sedimen, akar dan daun mangrove Rhizopora mucronata. Pada pengambilan sampel dipilih mangrove tingkat pohon, dengan karakteristik diameter batang > 4 cm dan tinggi > 2 meter. Sampel didapatkan dengan memotong bagian akar dan daun yang terdapat pada pohon, serta pengambilan sampel sedimen. Pada setiap Stasiun dilakukan tiga kali ulangan, sehingga jumlah sampel yang analisis sebanyak masing - masing 9 sampel sedimen, 9 sampel daun, dan 9 sampel akar. Pada setiap ulangan diambil
4
sampel dari lima pohon mangrove. Selanjutnya sampel dimasukkan ke dalam plastik klip, dan diberi label sesuai dengan Stasiunnya. Kemudian sampel disimpan di dalam cool box. Untuk identifikasi sampel lebih lanjutnya dilakukan di laboratorium. Sedangkan analisis kandungan logam berat dilakukan dengan menggunakan AAS setelah sebelumnya terlebih dahulu dilakukan preparasi sampel akar, daun dan sedimennya.
Analisis Data
Analisis Deskriptif
Nilai suhu, pH, dan salinitas yang didapatkan dibandingkan dengan KepMen LH No 50 th 2004 yaitu baku mutu perairan yang optimal bagi pertumbuhan mangrove. Baku mutu logam berat dalam sedimen di Indonesia belum ditetapkan, oleh karena itu sebagai acuan konsentrasi logam berat Cu dan Pb pada sedimen yang didapatkan dari hasil laboratorium dibandingkan dengan baku mutu dari Reseau National d’Observation (RNO) in Rochyatun et al. (2003). Sedangkan konsentrasi logam berat Cu dan Pb pada akar dan daun dibandingkan konsentrasi logam berat Cu da Pb yang normal bagi tumbuhan menurut Allaway (1968) in Greenland (1981).
Basal Area
Basal area untuk mengetahui ada tidaknya pengaruh logam berat terhadap luasan area yang ditumbuhi mangrove. Rumus Basal Area menurut Mueller-Dombois & Ellenberg (1974) in Sambas 2012:
𝐵𝐴 = (½ D)² π Keterangan:
BA : Basal Area (m2) D : Diameter batang (m)
Faktor Biokonsentrasi
Perbandingan antara konsentrasi logam di akar atau daun dengan konsentrasi di sedimen dikenal dengan Bioconcentration Factor (BCF). Rumus Faktor biokonsentrasi menurut MacFarlane et al. 2007 in Hamzah dan Setiawan 2010:
BCF = 𝐶𝑏 𝐶𝑚 Keterangan :
BCF : Faktor Biokonsentrasi
Cb : Konsentrasi dalam biota (akar/daun) (ppm) Cm : Konsentrasi dalam media/sedimen (ppm)
5 Untuk mengetahui tingkat kemampuan akumulasi mangrove terhadap logam berat, maka berikut di bawah ini merupakan tabel indeks faktor biokonsentrasi menurut Van Esch 1977 in Suprapti 2008:
Tabel 1 Indeks faktor biokonsentrasi
Nilai BCF Keterangan
BCF < 100 Sifat akumulasi rendah BCF = 100-1000 Sifat akumulasi sedang BCF > 1000 Sifat akumulasi tinggi
Faktor Translokasi
Selain itu juga dihitung perbandingan antara konsentrasi logam pada daun dan akar yang dikenal sebagai Translocation Factors (TF). Nilai TF dihitung untuk mengetahui perpindahan akumulasi logam dari akar ke tunas (MacFarlane et al. 2007 in Hamzah dan Setiawan 2010). Berikut merupakan rumus perhitungan BCF: TF = 𝐵𝐶𝐹 𝐷𝑎𝑢𝑛 𝐵𝐶𝐹 𝐴𝑘𝑎𝑟 Keterangan: TF : Faktor Translokasi BCF : Faktor Biokonsentrasi Koefisien Korelasi
Koefesien Korelasi digunakan untuk mengetahui keeratan hubungan antara logam berat yang terdapat pada sedimen dengan akar, sedimen dengan daun dan daun dengan akar. Analisis korelasi yang digunakan yaitu Pearson Correlation.
HASIL DAN PEMBAHASAN
Hasil Kondisi Lingkungan
Beberapa pengukuran yang dilakukan untuk melihat kondisi lingkungan di lokasi penelitian yaitu pengukuran fisika kimia air, fraksi sedimen dan luas tutupan basal. Parameter fisika kimia yang diukur secara insitu yaitu suhu air, salinitas dan pH air sedimen. Suhu yang terukur nilainya semakin meningkat di setiap Stasiun, sehingga Stasiun 3 memiliki nilai rata - rata suhu tertinggi yaitu sebesar 34,6667 0C. Nilai pH rata - rata tertinggi yaitu pada Stasiun 3 sebesar 7,6667. Begitu pula dengan nilai salinitas yang juga semakin tinggi di Stasiun 3.
6
Tabel 2 Kisaran suhu, pH, salinitas air di lokasi penelitian
No Parameter Satuan Stasiun
1 2 3
1 Suhu 0C 25-29 25-33 33-36
2 pH - 7 7 7-8
3 Salinitas ‰ 20-30 23-35 25-30 Hasil pengukuran diatas jika kita bandingkan dengan baku mutu yang ada yaitu menurut pada KEPMEN LH No 50 th 2004, maka suhu, pH dan salinitas memenuhi baku mutu perairan yang optimal bagi pertumbuhan mangrove yaitu berturut-turut sebesar 28- 320C, 7-8,5 dan 34 0/00.
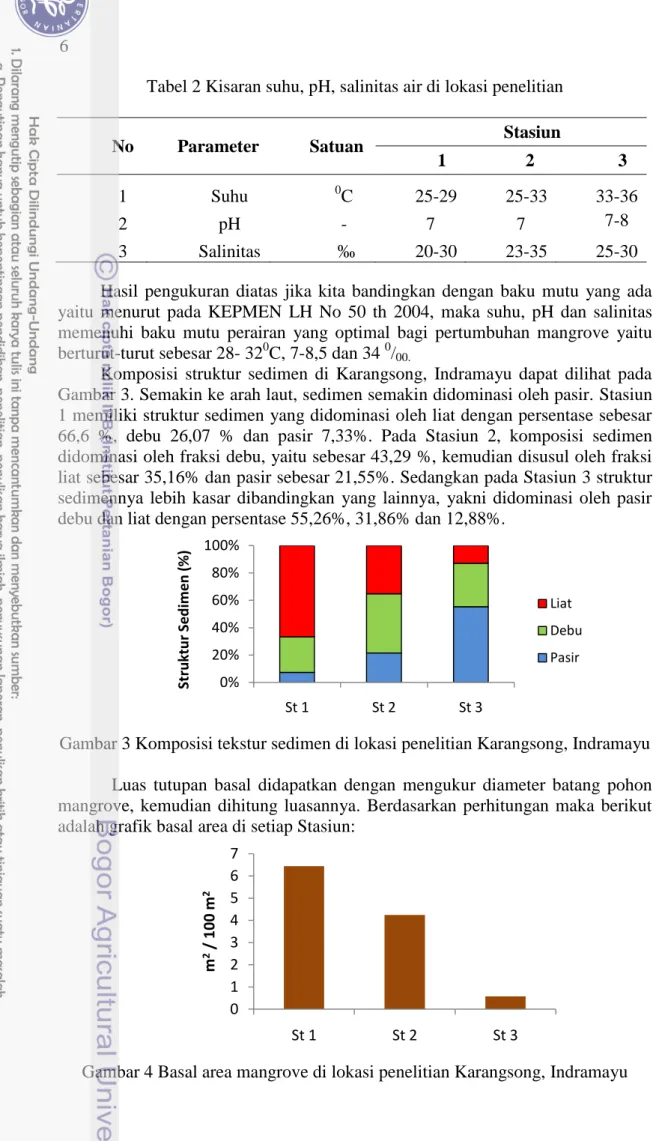
Komposisi struktur sedimen di Karangsong, Indramayu dapat dilihat pada Gambar 3. Semakin ke arah laut, sedimen semakin didominasi oleh pasir. Stasiun 1 memiliki struktur sedimen yang didominasi oleh liat dengan persentase sebesar 66,6 %, debu 26,07 % dan pasir 7,33%. Pada Stasiun 2, komposisi sedimen didominasi oleh fraksi debu, yaitu sebesar 43,29 %, kemudian disusul oleh fraksi liat sebesar 35,16% dan pasir sebesar 21,55%. Sedangkan pada Stasiun 3 struktur sedimennya lebih kasar dibandingkan yang lainnya, yakni didominasi oleh pasir debu dan liat dengan persentase 55,26%, 31,86% dan 12,88%.
Gambar 3 Komposisi tekstur sedimen di lokasi penelitian Karangsong, Indramayu Luas tutupan basal didapatkan dengan mengukur diameter batang pohon mangrove, kemudian dihitung luasannya. Berdasarkan perhitungan maka berikut adalah grafik basal area di setiap Stasiun:
Gambar 4 Basal area mangrove di lokasi penelitian Karangsong, Indramayu
0% 20% 40% 60% 80% 100% St 1 St 2 St 3 St ru ktur S e dim e n (%) Liat Debu Pasir 0 1 2 3 4 5 6 7 St 1 St 2 St 3 m 2/ 1 0 0 m 2
7
Grafik diatas menunjukan luas tutupan basal mangrove di lokasi penelitian, total basal area pada Stasiun 1, 2 dan 3 beturut - turut adalah 6,4370 m2, 4,2486 m2 dan 5,790 m2. Basal area tertinggi dicapai pada Stasiun 1 dan luas tutupan basal semakin menurun nilainya ke arah Stasiun 3.
Kandungan Logam Berat Cu dan Pb pada Sedimen
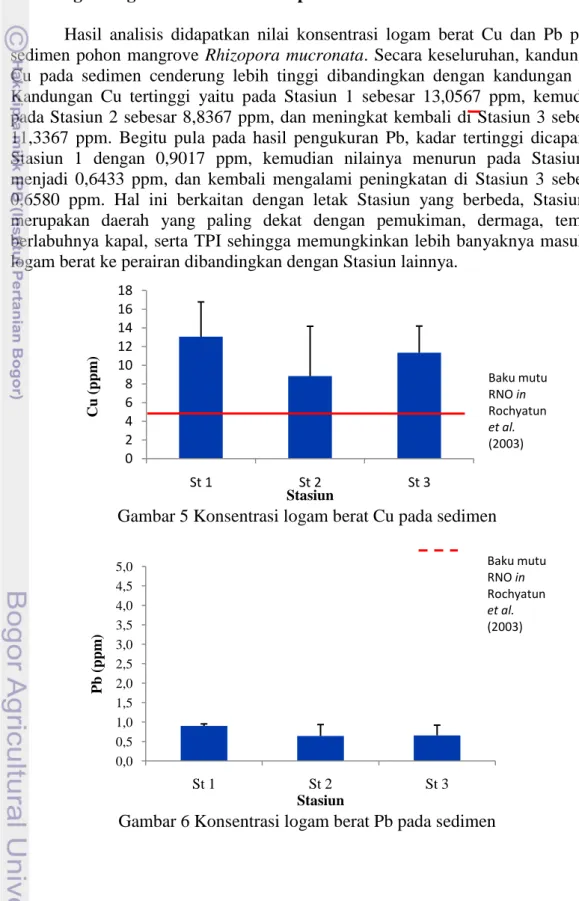
Hasil analisis didapatkan nilai konsentrasi logam berat Cu dan Pb pada sedimen pohon mangrove Rhizopora mucronata. Secara keseluruhan, kandungan Cu pada sedimen cenderung lebih tinggi dibandingkan dengan kandungan Pb. Kandungan Cu tertinggi yaitu pada Stasiun 1 sebesar 13,0567 ppm, kemudian pada Stasiun 2 sebesar 8,8367 ppm, dan meningkat kembali di Stasiun 3 sebesar 11,3367 ppm. Begitu pula pada hasil pengukuran Pb, kadar tertinggi dicapai di Stasiun 1 dengan 0,9017 ppm, kemudian nilainya menurun pada Stasiun 2 menjadi 0,6433 ppm, dan kembali mengalami peningkatan di Stasiun 3 sebesar 0,6580 ppm. Hal ini berkaitan dengan letak Stasiun yang berbeda, Stasiun 1 merupakan daerah yang paling dekat dengan pemukiman, dermaga, tempat berlabuhnya kapal, serta TPI sehingga memungkinkan lebih banyaknya masukan logam berat ke perairan dibandingkan dengan Stasiun lainnya.
Gambar 5 Konsentrasi logam berat Cu pada sedimen
Gambar 6 Konsentrasi logam berat Pb pada sedimen
0 2 4 6 8 10 12 14 16 18 St 1 St 2 St 3 Cu (pp m ) Stasiun Baku mutu RNO in Rochyatun et al. (2003) 0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0 St 1 St 2 St 3 P b (pp m ) Stasiun Baku mutu RNO in Rochyatun et al. (2003)
8
Baku mutu logam berat dalam sedimen di Indonesia belum ditetapkan, oleh karena itu sebagai acuan digunakan baku mutu dari Reseau National d’Observation (RNO). Menurut RNO in Rochyatun et al. (2003), kadar normal Cu dalam sedimen yang tidak terkontaminasi adalah 5 ppm sedangkan kadar normal Pb dalam sedimen yang tidak terkontaminasi berkisar antara 10-70 ppm. Jika dibandingkan, maka konsentrasi Cu telah melewati baku mutu yang ada, sedangkan Pb masih dibawah baku mutu.
Kandungan Logam Berat Cu dan Pb pada Akar dan Daun
Tabel berikut menunjukkan besarnya kandungan logam berat Cu dan Pb
pada akar dan daun mangrove Rhizopora mucronata diketiga Stasiun. Hasil analisis menggambarkan besarnya akumulasi Cu oleh akar dan daun dibandingkan dengan Pb. Akumulasi Cu pada akar tertinggi pada Stasiun 3 yaitu sebesar 5,5767, sedangkan akumulasi tertinggi Pb pada akar yaitu sebesar 0,8440 ppm pada Stasiun 2. Pada daun, Cu tertinggi terakumulasi sebanyak 2,8333 ppm, sedangkan kandungan Pb tertinggi yang terakumulasi di daun yaitu sebesar 0,3910 ppm.
Tabel 3 Rata-rata kandungan logam berat Cu dan Pb pada akar dan daun
No Parameter Satuan Stasiun
1 2 3 Akar 1 Cu ppm 3,6367 4,7267 5,5767 2 Pb ppm 0,7517 0,8440 0,7150 Daun 1 Cu ppm 1,4000 2,8333 0,7367 2 Pb ppm 0,3910 0,3700 0,2230
Menurut Allaway (1968) in Taryana (1995) konsentrasi logam berat Cu yang normal bagi tumbuhan adalah 4 - 15 ppm, sedangkan konsentrasi Pb yang masih dapat ditolerir oleh tumbuhan adalah 0,1 - 10 ppm (Allaway 1968 in Saepulloh 1995). Jika dibandingkan, maka kandungan logam berat Cu dan Pb pada daun Rhizopora mucronata masih dibawah konsentrasi umum pada tanaman menurut Allaway (1968). Akan tetapi menurut Zimdahl (1976) in Saepulloh (1995) logam Pb pada tanaman cenderung bersifat racun. Konsentrasi Pb sebesar 1 ppm mempunyai efek yang sangat besar terhadap proses - proses tumbuhan, termasuk proses fotosintesis dan respirasi.
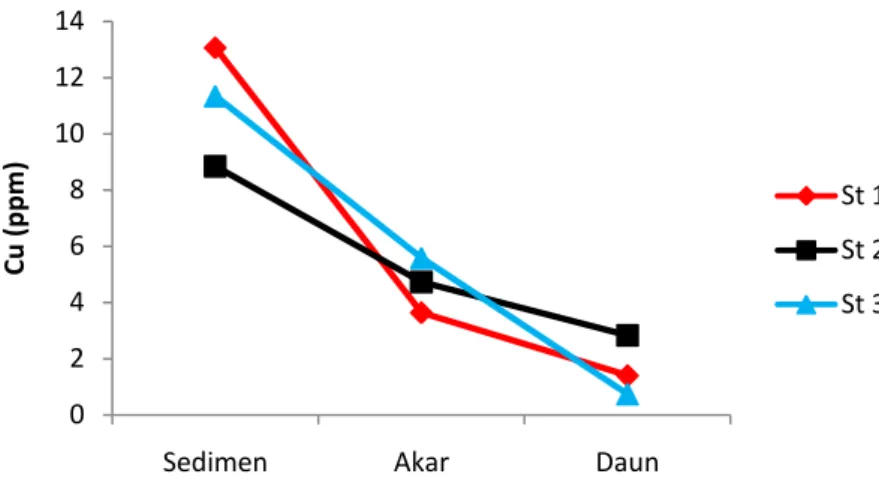
Gambar 7 disajikan untuk melihat lebih jelas perbandingan kandungan logam berat pada sedimen dan yang terakumulasi pada tumbuhan yaitu bagian akar dan daun, sehingga kita dapat menggambarkan distribusi logam berat pada tumbuhan mangrove.
9
Gambar 7 Distribusi logam berat Cu pada sedimen, akar dan daun
Gambar 8 Distribusi logam berat Pb pada sedimen, akar dan daun
Pada Gambar 4 dan 5, ketiga Stasiun menggambarkan hasil yang sama, yakni akumulasi logam berat tertinggi pada sedimen, kemudian konsentrasinya mengalami penurunan di akar dan semakin kecil ketika sampai di daun. Hal tersebut berhubungan dengan berbedanya kemampuan tumbuhan khususnya bagian akar dan daun dalam mengakumulasi logam berat yang ada pada sedimen. Pada akumulasi Pb juga terjadi demikian, akan tetapi konsentrasi Pb pada akar Stasiun 2 dan 3 justru melebihi konsentrasi pada sedimen. Yakni 0,4330 ppm pada sedimen, 0,8440 ppm pada akar dan 0,3700 ppm terakumulasi didaun.
Analisis korelasi digunakan untuk mengetahui hubungan antara konsentrasi logam berat pada sedimen dengan akar dan sedimen dengan daun di kedua logam berat yang diamati. Hasil analisis dapat dilihat pada tabel dibawah ini:
Tabel 4 Matrix koefisien korelasi pada logam Cu
Sedimen Akar Daun
Sedimen 1 * * Akar -0,4694 1 * Daun -0,7439 -0,2410 1 0 2 4 6 8 10 12 14
Sedimen Akar Daun
Cu (p p m ) St 1 St 2 St 3 0,0 0,2 0,4 0,6 0,8 1,0
Sedimen Akar Daun
Pb (p p m ) St 1 St 2 St 3
10
Tabel 5 Matrix koefisien korelasi pada logam Pb
Sedimen Akar Daun
Sedimen 1 * *
Akar -0,2905 1 *
Daun 0,5547 0,6350 1
Berdasarkan hasil analisis korelasi diatas didapatkan korelasi kandungan logam Cu pada sedimen dengan akar, sedimen dengan daun dan daun dengan akar secara berturut - turut -0,4694, -0,7439 dan -0,2410. Sedangkan korelasi ditemukan pada kandungan logam Pb di sedimen dengan daun dan pada akar dengan daun yakni berturut - turut 0,5547 dan 0,6350.
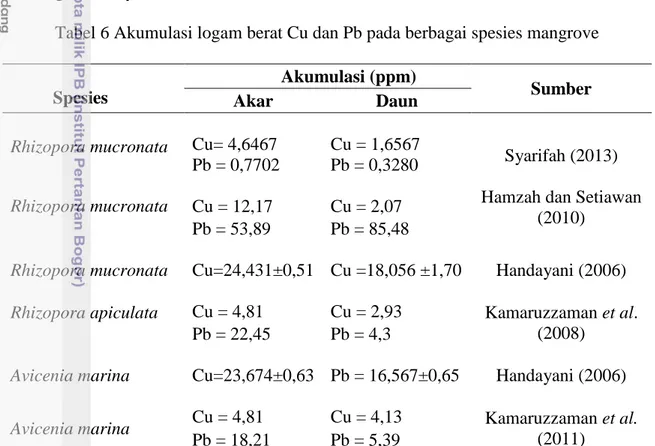
Tabel 6 Akumulasi logam berat Cu dan Pb pada berbagai spesies mangrove
Spesies Akumulasi (ppm) Sumber Akar Daun Rhizopora mucronata Rhizopora mucronata Cu= 4,6467 Pb = 0,7702 Cu = 12,17 Cu = 1,6567 Pb = 0,3280 Cu = 2,07 Syarifah (2013) Hamzah dan Setiawan
(2010) Pb = 53,89 Pb = 85,48
Rhizopora mucronata Cu=24,431±0,51 Cu =18,056 ±1,70 Handayani (2006)
Rhizopora apiculata Cu = 4,81 Cu = 2,93 Kamaruzzaman et al.
(2008) Pb = 22,45 Pb = 4,3
Avicenia marina Cu=23,674±0,63 Pb = 16,567±0,65 Handayani (2006)
Avicenia marina Cu = 4,81 Cu = 4,13 Kamaruzzaman et al.
(2011) Pb = 18,21 Pb = 5,39
Tabel diatas memperlihatkan kandungan logam berat Cu dan Pb yang diakumulasi oleh berbagai jenis spesies mangrove tanpa memperhatikan tingkatan mangrove nya maupun ukuran diameter batangnya. Jika membandingkan dengan hasil penelitian ini, maka spesies Rhizopora mucronata dapat mengakumulasi logam berat Cu dan Pb dengan baik seperti spesies lainnya.
Faktor Biokonsentrasi (BCF) dan Faktor Translokasi (TF)
Faktor Konsentrasi atau BCF pada daun dan akar dihitung untuk mengetahui seberapa besar daya akumulasi nya terhadap logam berat Cu dan Pb yang terdapat di sedimen. Berdasarkan hasil perhitungan didapatkan nilai BCF seperti pada Tabel 7, dimana BCF setiap lpgam berat berbeda nilainya pada bagian akar maupun daun.
11 Tabel 7 Nilai Faktor Konsentrasi (BCF) Cu dan Pb pada akar dan daun
Stasiun Rata-Rata 1 2 3 BCF Cu Akar 0,2890 0,8565 0,5371 0,5609 Daun 0,1134 0,4197 0,0645 0,1992 BCF Pb Akar 0,8281 1,8048 1,3018 1,3116 Daun 0,4350 0,6911 0,4092 0,5118
Berdasarkan tabel diatas, dapat kita lihat bahwa nilai Faktor konsentrasi rata-rata tertinggi yaitu BCF Pb pada akar sebesar 1,3116, kemudian disusul oleh BCF Cu pada akar sebesar 0,5609, BCF Pb pada daun sebesar 0,5118 dan BCF Cu pada daun sebesar 0,1992.
Faktor translokasi akan semakin tinggi nilainya jika faktor konsentrasi di daun lebih besar dibandingkan dengan di akar. Hasil perhitungan TF disetiap Stasiun dapat dilihat pada tabel dibawah ini:
Tabel 8 Translokasi Logam berat Cu dan Pb di Karangsong, Indramayu
Parameter Stasiun Rata-Rata
1 2 3
TF Cu 0,3923 0,4899 0,1202 0,3341
Pb 0,5253 0,3829 0,3143 0,4075
Rata-rata TF tertinggi dicapai oleh logam berat Pb yaitu sebesar 0,4075, sedangkan nilai TF untuk logam berat Cu adalah sebesar 0,3341. Faktor Translokasi dapat dipengaruhi oleh sifat essensial atau tidaknya logam tersebut dalam tumbuhan.
Pembahasan
Akumulasi logam berat Cu dan Pb pada sedimen, akar dan daun Rhizopora
mucronata
Sedimen mengandung logam berat Cu dan Pb tertinggi, kemudian disusul oleh akar dan daun. Tingginya logam berat pada sedimen dikarenakan logam berat yang mempunyai sifat mudah mengikat bahan organik dan mengendap di dasar perairan dan bersatu dengan sedimen sehingga kadar logam berat dalam sedimen lebih tinggi dibandingkan dalam air (Hutagalung 1991). Dari pernyataan diatas dapat kita simpulkan bahwa bahan organik pun menjadi faktor penting tingginya logam berat pada sedimen. Seperti yang dilaporkan pada hasil penelitian Bar-Tal
12
et al (1988) in Kamaruzzaman et al. (2011) bahwa jumlah bahan organik yang ditemukan di tanah mempengaruhi bioavailability Pb dan Cu di sedimen.
Tumbuhan mangrove dapat menyerap logam berat dan menyimpannya dalam jaringan tubuh, seperti daun, batang dan akar, sehingga dapat mengurangi tingkat pencemaran di tanah sedimen dan air. Peran tumbuhan mangrove dalam mengeliminasi logam berat dikenal dengan istilah fitoremidiasi. Proses remediasi terjadi karena tumbuhan dapat melepaskan senyawa kelat, seperti protein dan glukosida, yang berfungsi mengikat logam dan dikumpulkan di jaringan tubuh. (Stomp et al., 1993, Schnoor dkk., 1995; Jones dkk., 2000 in Setiawan 2008). Proses absorbsi logam berat pada tumbuhan seperti halnya pada hewan yang disebut difusi, sedangkan istilah pada tumbuhan adalah translokasi, yaitu transpor terjadi dari sel menuju ke jaringan vaskuler, kemudian didistribusikan ke seluruh bagian tumbuhan.
Bagian tumbuhan mangrove yang paling banyak menyerap logam berat Cu dan Pb adalah akar. Akar berinteraksi secara langsung dengan sedimen sehingga sangat memungkinkan baginya untuk mengakumulasi logam berat dengan konsentrasi yang tinggi. Menurut Andani dan Purbayanti (1981) in Taryana (1995), jika konsentrasi suatu ion jenuh lebih tinggi ditemukan didalam akar daripada di pucuk, itu merupakan bukti kuat untuk lokalisasi ekstraseluler. Tanaman dengan keadaan stress sering kali mengalokasikan sebagian besar hasil fotosintesisnya ke organ penyimpanan yang terdapat dibawah tanah. Cu dan Pb banyak diakumulasikan dalam akar kemungkinan besar karena akar mempunyai toleransi inheren yang lebih tinggi terhadap toksin dibandingkan dengan daun atau pucuk. Menurut Tyler (1976) in Taryana (1995) Cu merupakan salah satu logam yang memperlihatkan akumulasi didalam akar.
Kandungan logam berat Cu pada akar lebih tinggi dibandingkan dengan Pb, hal tersebut wajar terjadi mengingat kandungan logam berat Cu pada sedimen juga lebih tinggi, sehingga sangat memungkinkan konsentrasi logam Cu yang terserap oleh akar lebih tinggi daripada Pb. Pada Stasiun 2 dan 3 akumulasi logam berat Pb pada akar lebih besar dibandingkan dengan akumulasi di sedimen. Hal tersebut menunjukkan penumpukan logam berat pada bagian akar mangrove sehingga konsentrasinya lebih tinggi daripada di sedimen.
Akumulasi logam berat Cu dan Pb pada daun memiliki konsentrasi lebih
rendah dibandingkan dengan logam berat yang terakumulasi pada akar. Selain akar, daun juga merupakan salah satu organ tumbuhan yang dijadikan tempat mengakumulasi logam berat. Selain dapat dijadikan sebagai tempat lokalisasi dalam usaha penanggulangan (ameliorasi) untuk meminimumkan pengaruh toksin pada tumbuhan, pada daun juga dapat terjadi proses eksresi secara aktif melalui kelenjar pada tajuk atau secara pasif dengan akumulasi pada daun tua yang diikuti dengan absisi daun (gugurnya daun) (Fitter dan Hay 1991 in Rohmawati 2007). Besarnya akumulasi Cu dan Pb pada daun mencerminkan faktor translokasinya, jika kandungan logam berat pada daun tidak jauh berbeda dengan akar atau bahkan lebih tinggi daripada akar maka akan menghasilkan nilai faktor translokasi yang tinggi. Artinya mobilisasi logam tersebut dari akar ke daun sangat baik, sehingga distribusi logam berat pada akar dan daun merata, bahkan sangat memungkinkan konsentrasinya lebih tinggi pada daun. Proses masuknya Cu dan Pb ke dalam jaringan tanaman melalui penyerapan oleh akar, kemudian disalurkan melalui xylem ke semua bagian tanaman sampai ke daun, akan tetapi proses
13 masuknya logam Pb bisa juga dengan cara penempelan partikel Pb pada daun dan masuk kedalam jaringan daun melalui celah stomata (Dahlan 1986 in Saepulloh 1995). Hal tersebut wajar saja terjadi mengingat Pb bisa dihasilkan dari asap buangan kendaraan seperti kapal dan proses industri di daerah Karangsong. Seperti yang disebutkan oleh Suharto (2005) bahwa senyawa Pb dalam keadaan kering dapat terdispersi di dalam udara sehingga kemudian terhirup pada saat bernapas dan sebagian akan menumpuk di kulit dan atau terserap oleh daun tumbuhan. Begitpula menurut Defew et al (2004), logam berat yang masuk ke dalam lingkungan perairan akan mengalami pengendapan, pengenceran, dan dispersi, kemudian diserap oleh organisme yang hidup di perairan.
Faktor konsentrasi (BCF) tertinggi logam Cu dan Pb yaitu terdapat pada akar daripada di daun, maka dapat kita simpulkan bahwa akar memiliki kemampuan akumulasi yang lebih baik terhadap logam berat yang terdapat pada sedimen dibandingkan dengan daun. Meskipun demikian, kemampuan akumulasi akar ini masih tergolong rendah jika kita bandingkan dengan indeks faktor biokonsentrasi menurut Van Esch 1977 in Suprapti 2008, karena nilai BCF < 100.
Nilai faktor translokasi logam Pb lebih besar daripada Cu. Nilai TF suatu logam berat menggambarkan mobilitas logam tersebut dari akar ke daun. Faktor Translokasi dapat dipengaruhi oleh sifat essensial atau tidaknya logam tersebut dalam tumbuhan. Translokasi logam dari akar ke daun untuk logam esensial (Cu) lebih rendah dibandingkan pada logam non esensial (Pb). Rendahnya nilai TF pada logam esensial menunjukkan bahwa mangrove menggunakan logam tersebut untuk aktivitas metabolisme dan pertumbuhan.
Sumber Pencemar Logam Berat Cu dan Pb dan Pengaruhnya terhadap Tumbuhan
Kandungan logam berat Cu yang terukur pada sedimen, akar dan daun nilainya lebih tinggi daripada logam berat Pb. Kadar Cu tertinggi mencapai 13,0567 ppm sedangkan kadar Pb tertinggi hanya mencapai 0,9017 ppm. Kandungan Cu yang tinggi ini dapat bersumber dari alam maupun limbah dari aktivitas manusia. Sumber alamiah Cu seperti adanya erosi dari batuan mineral, dari debu atau partikulat Cu yang ada dilapisan udara kemudian dibawa turun oleh air hujan. Sedangkan Cu yang berasal dari aktivitas manusia yakni berupa limbah industri seperti industri pengolahan kayu, limbah rumah tangga dan lain-lain (Palar, 1994). Beberapa industri yang terdapat di sekitar Karangsong dan sepanjang Sungai Prajagumiwang adalah industri batik yang menghasilkan limbah cair pewarnaan batik yang mengandung Cu, industri pembuatan kapal yang menggunakan cat yang mengandung Cu sebagai anti fouling. Selain itu, Cu termasuk logam esensial bagi tumbuhan, sehingga tumbuhan memang menyerap logam Cu dari lingkungannya untuk kebutuhan fisologis dan metabolismenya, akan tetapi dalam jumlah yang sedikit. Cu sangat berguna untuk pertumbuhan jaringan tumbuhan terutama jaringan daun dimana terdapat fotosintesis (Kamaruzzaman et al. 2008). Cu juga mempunyai fungsi sebagai salah satu mikronutrien yang diperlukan didalam mitokondria dan kloroplas, enzim yang berhubungan dengan transpor elektron II, proses fotosintesis dan metabolisme karbohidrat dan protein serta sebagai dinding sel lignin (Verkleij dan Schat 1990
14
in Hamzah dan Setiawan 2010). Menurut Jaqob dan Uexkull (1963) in Napitupulu (2008), tembaga diserap oleh akar tanaman dalam bentuk Cu2+, berperan dalam proses oksidasi, reduksi dan pembentukan enzim. Sumber logam berat Pb di perairan Karangsong secara alami tersebar pada batuan dan lapisan kerak bumi, sumber lainnya yaitu dari bahan bakar kendaraan dan cat (Darmono 1995). Karena Pb bukan merupakan logam esensial maka terakumulasi lebih sedikit di tumbuhan.
Apabila jumlah logam berat tersebut melebihi batas normal yang dapat ditolerir oleh tumbuhan maka akan mempengaruhi perubahan morfologi proses kimia, biokimia, fisiologi, dan struktur tumbuhan. Beberapa gejala yang terlihat secara morfologi yaitu seperti klorosis, perubahan warna, nekrosis dan kematian seluruh bagian tumbuhan (Luncang 2005 in Panjaitan 2009). Secara biokimia Pb dapat menghambat sistem enzim dalam mengkonversi asam amino, dan bila tumbuhan keracunan Pb maka dapat mengurangi laju pertumbuhan tumbuhan (Saepulloh 1995). Penambahan konsentrasi Cu, Hg atau Ag akan mengakibatkan kehilangan K+ dan perubahan menjadi kasar (Puckket 1976 in Taryana 1995).
Kondisi Lingkungan
Hasil pengukuran parameter fisika kimia pada ketiga Stasiun menunjukkan nilai yang sesuai dengan baku mutu yang ditetapkan KEPMEN LH No 50 th 2004 untuk pertumbuhan optimal bagi mangrove. Parameter suhu, pH, dan salinitas air yang diukur secara insitu tersebut sebenarnya memiliki pengaruh besar terhadap konsentrasi logam berat di perairan. Hasil penelitian WALDICHUK (1974) in Hutagalung (1984) menunjukkan kenaikan suhu, penurunan pH dan salinitas perairan menyebabkan tingkat bioakumulasi semakin besar. Seperti yang disebutkan oleh Hutagalung (1984) bahwa penurunan pH air menyebabkan toksisitas logam berat makin besar. Kelarutan logam dalam air dikontrol oleh pH air, ketika pH naik maka akan terjadi perubahan kestabilan dari bentuk karbonat menjadi hidroksida yang membentuk ikatan dengan partikel pada badan air, sehingga akan mengendap membentuk lumpur (Palar 2004). Begitu pula menurut Novotny dan Olem (1994) dalam Sarjono (2009) menyebutkan hal yang sama mengenai pengaruh pH pada konsentrasi logam berat. Hasil pengukuran menunjukkan Stasiun 1 dengan Ph terendah yaitu 7 sebanding dengan konsentrasi logam berat Cu dan Pb yang tertinggi di semua Stasiun. Pengaruh suhu pada konsentrasi logam berat yaitu ketika suhu air laut rendah atau suhu yang lebih dingin akan meningkatkan adsorpsi logam berat ke partikulat untuk mengendap di dasar laut. Sementara saat suhu air laut naik, senyawa logam berat akan melarut di air laut karena penurunan laju adsorpsi ke dalam partikulat. Stasiun 1 memiliki nilai suhu terendah sehingga logam berat akan mengendap ke sedimen, hal ini dibuktikan dengan tingginya kandungan logam Cu dan Pb pada Stasiun 1. Salinitas juga ikut mempengaruhi akumulasi logam berat di permukaan sedimen, disebutkan bahwa peningkatan salinitas dapat menggangu proses oksidasi dan beberapa logam berat seperti Cr, Cu, Pb dan Zn dapat melewati lapisan oxic dan kembali ke kolom air, sehingga menurunkan konsentrasi di daerah yang lebih dekat kelaut (Du Laing et al. 2008 in Kamaruzzaman et al. 2011). Salinitas
15 terendah terukur pada Stasiun 1, begitupun hasil analisis logam dimana kadar tertinggi juga dicapai pada Stasiun 1.
Tipe substrat pada Stasiun 1 didominasi liat, Stasiun 2 didominasi oleh debu dan pada Stasiun 3 didominasi oleh pasir. Perbedaan fraksi sedimen yang mendominasi menggambarkan letak Stasiun, dimana Stasiun 3 yang paling dekat ke laut. Logam berat yang terlarut dalam air akan berpindah ke dalam sedimen jika berikatan dengan materi organik bebas atau materi organik yang melapisi permukaan sedimen dan penyerapan langsung oleh permukaan partikel sedimen, sehingga kadar logam berat dalam sedimen lebih besar daripada di air. Materi organik dalam sedimen dan kapasitas penyerapan logam sangat berhubungan dengan ukuran partikel dan luas permukaan penyerapan, sehingga konsentrasi logam dalam sedimen biasanya dipengaruhi ukuran partikel dalam sedimen (Wilson et al. 1985 in Arisandi 2001).
Hasil analisis logam berat Cu dan Pb pada sedimen di ketiga Stasiun menunjukkan nilai yang tinggi di Stasiun 1 dengan tipe substrat liat, hal tersebut sesuai dengan hasil penelitian Kamaruzzaman et al. (2011) yang menunjukkan bahwa semakin kecil ukuran fraksi sedimennya, maka semakin besar akumulasi logam berat dalam sedimen tersebut dan pada akhirnya akan meningkatkan akumulasi logam berat dalam akar. Begitu pula menurut Bernhard (1981) in Erlangga (2007) konsentrasi logam berat tertinggi terdapat dalam sedimen yang berupa lumpur, tanah liat, pasir berlumpur dan campuran dari ketiganya dibandingkan dengan yang berupa pasir murni. Hal serupa dikatakan Zanganeh et al (2008) yang mengatakan bahwa partikel halus akan memiliki daya adsorpsi logam yang lebih tinggi. Jadi, pada tanah, semakin halus teksturnya semakin tinggi kekuatannya untuk mengikat logam berat. Oleh karena itu, tanah yang bertekstur liat memiliki kemampuan untuk mengikat logam berat lebih tinggi daripada tanah berpasir.
Telah diketahui bahwa kandungan logam berat tertinggi terdapat pada Stasiun 1, dengan basal area yang teringgi pula, jika kita kaitkan maka kandungan logam berat belum mempengaruhi pertumbuhan mangrove.
Implikasi Manajemen
Hasil penelitian menunjukkan bahwa sedimen di perairan Karangsong telah tercemar Cu, begitupun bagian tumbuhan mangrove yang mengandung logam berat Cu dan Pb. Hal tersebut dapat menimbulkan berbagai macam resiko diantaranya resiko bagi masyarakat yang secara langsung memanfaatkan tumbuhan mangrove untuk konsumsi, resiko bagi hewan ternak yang mengkonsumsi daun mangrove, resiko bagi biota perairan terutama biota yang termasuk deposit feeder atau filter feeder yang berinteraksi langsung dengan sedimen, kemudian resiko bagi organisme yang memanfaatkan serasah daun mangrove, sehingga hal tersebut dapat mengganggu sistem ekologi mangrove di perairan Karangsong, akan tetapi sisi positif nya yakni pengurangan konsentrasi logam berat di perairan.
Mangrove sendiri dapat dijadikan sebagai akumulator logam berat, hal tersebut di buktikan dengan adanya kandungan logam berat dalam bagian akar dan daun mangrove. Telah kita ketahui bahwa tumbuhan memiliki mekanisme
16
tersendiri untuk menghadapi konsentrasi toksik yang berada dalam tubuhnya begitupun dengan mangrove, akan tetapi walaupun mangrove dapat mengakumulasi logam berat, jika konsentrasi logam berat tersebut sudah melewati kadar normal yang dapat ditolerir oleh mangrove maka hal tersebut justru akan menyebabkan kerusakan pada mangrove itu sendiri, baik kerusakan yang dapat dilihat secara morfologi maupun dengan terganggunya proses fisologi dan biokimia seperti terhambatnya pertumbuhan dan bahkan tidak menutup kemungkinan bahan toksik tersebut dapat mengakibatkan kematian di seluruh bagian tumbuhan. Jika kemungkinan terburuk itu terjadi, maka akan timbul permasalahan baru dikarenakan semakin berkurangnya jumlah mangrove yang ada mengingat banyaknya manfaat yang dimiliki mangrove secara ekologis, ekonomis dan sosial.
Oleh karena itu, langkah pengelolaan yang efektif agar mencegah terjadinya pencemaran perairan, biota perairan dapat terus hidup dan mangrove tetap lestari adalah dengan mengurangi masukan bahan pencemar ke dalam lingkungan perairan. Hal ini dapat dilakukan dengan beberapa cara diantaranya pelaksanaan peraturan pemerintah tentang jumlah dan jenis limbah yang boleh dibuang ke perairan, terutama limbah hasil industri, pelaksanaan persyaratan perizinan seperti izin membuka lahan industri, pemantauan atau monitoring yang dilakukan oleh pemerintah secara berkesinambungan, pemanfaatan tumbuhan lain selain mangrove untuk mengakumulasi logam berat seperti eceng gondok, dan yang terakhir adalah sosialisasi kepada masyarakat untuk meningkatkan kesadaran tentang bahaya membuang limbah ke sungai.
SIMPULAN DAN SARAN
Simpulan
1. Kandungan logam berat Cu pada akar dan daun pohon Rhizopora mucronata lebih besar daripada Pb, akan tetapi masih lebih rendah daripada sedimen. Hal tersebut mengindikasikan daya akumulasi akar yang lebih besar daripada daun.
2. Pohon mangrove Rhizopora mucronata dapat dijadikan akumulator logam berat Cu dan Pb, walaupun kemampuannya masih tergolong rendah.
Saran
Penelitian serupa perlu dilakukan dengan menganilisis kandungan logam berat pada bagian batang mangrove dengan spesies dan jenis logam yang berbeda.
17
DAFTAR PUSTAKA
Arisandi P. 2001. Mangrove jenis api-api (Avicennia marina) alternatif pengendalian pencemaran logam berat pesisir. Lembaga Kajian Ekologi dan Konservasi Lahan Basah. [internet]. 02 Des 2001; [08 Mei 2013]; http://terranet.or.id
Darmono. 1995. Logam dalam Sistem Biologi Makhluk Hidup. Jakarta: UI Press Defew, L. H., M.M. James, and M.G. Hector. 2004. An Assessment Of Metal
Contamination In Mangrove Sediments And Leaves From Punta Mala Bay, Pacific Panama. Marine pollution bulletin. 50: 547-552
Effendi H. 2003. Telaah Kualitas Air bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Yogyakarta: Kanisius.
Erlangga. 2007. Efek pencemaran perairan sungai kampar di provinsi riau terhadap ikan baung (Hemibagrus nemurus). [tesis]. Sekolah Pascasarjana: Institut Pertanian Bogor.
Greenland DJ, Hayes NHB. 1981. The Chemistry of Soil Processes. John Wiley and Sons Ltd, New York.
Hamzah F, Setiawan A. 2010. Akumulasi logam berat Pb, Cu, dan Zn di hutan mangrove Muara Angke, Jakarta Utara. Jurnal Ilmu dan Teknologi Kelautan Tropis. Vol. 2, No. 2 : 41-52
Handayani T. 2006. Bioakumulasi Logam Berat dalam Mangrove Rhizopora mucronata dan Avicenia marina di Muara Angke Jakarta. Jurnal Teknologi Lingkungan. Vol.7 No.3: 266-270
Hutagalung HP. 1991. Pencemaran laut oleh logam berat. Puslitbang Oseanologi. Status Pencemaran Laut di Indonesia dan Teknik Pemantauannya. LIPI. Jakarta.
Kamaruzzaman BY, Ong MC, Jalal KCA, Shahbudin S, Nor OM. 2008. Accumulation of lead and copper in rhizophora apiculata from setiu mangrove forest, Terengganu, Malaysia. Journal of Environmental Biology: 821-824
Kamaruzzaman BY, Sharlinda RMZ, John AB, Waznah SA. 2011. Accumulation and distribution of lead and copper in Avicenia marina and Rhizopora apiculata from balok mangrove forest, Pahang, Malaysia. Sains Malaysiana 40(6)(2011): 555–560
[KepMen LH] Keputusan Menteri Lingkungan Hidup. No. 51 Tahun 2004. Baku mutu air laut.
Napitupulu M. 2008. Analisis logam berat seng, kadmium, dan tembaga pada berbagai tingkat kemiringan tanah hutan tanaman industri PT. Toba Pulp Lestari dengan metode spektrometri serapan atom (SSA). [tesis]. Universitas Sumatera Utara. Medan.
Palar H. 1994. Pencemaran dan Toksikologi Logam Berat. Jakarta: Rineka Cipta. 289 hal.
Panjaitan GY. 2009. Akumulasi logam berat tembaga (Cu) dan timbal (Pb) pada pohon Avicennia marina di hutan mangrove. [skripsi]. Departemen Kehutanan. Fakultas Pertanian: Universitas Sumatera Utara.
18
Rochyatun E, Edward, Rozak A. 2003. Kandungan logam berat Pb, Cd, Cu, Zn, Ni, Cr, Mn & Fe dalam air laut dan sedimen di perairan Kalimantan Timur. Oseanologi dan Limnologi di Indonesia. ISSN 0125 -9830. No. 35 : 51 - 71
Rohmawati. 2007. Daya akumulasi tumbuhan Avicennia marina terhadap logam berat (Cu, Cd, Hg) di pantai Kenjeran Surabaya. [skripsi]. Jurusan Biologi. Fakultas Sains dan Teknologi: Universitas Islam Negeri Malang.
Rusdianti K, Sunito S. 2012. Konversi lahan hutan mangrove serta upaya penduduk lokal dalam merehabilitasi ekosistem mangrove. Jurnal Sosiologi Pedesaan. Departemen Sains Komunikasi dan Pengembangan Masyarakat, Fakultas Ekologi Manusia: IPB. hlm. 1-17
Saepulloh C. 1995. Akumulasi logam berat (Pb, Cd Ni) pada jenis Avicennia marina di hutan lindung mangrove Angke-Kapuk DKI Jakarta. [skripsi]. Jurusan Manajemen Hutan. Fakultas Kehutanan: Institut pertanian Bogor. Setyawan AD. 2008. Biodiversitas Ekosistem Mangrove di Jawa; Tinjauan Pesisir
Utara dan Selatan Jawa Tengah. Cetakan Pertama. Pusat Penelitian dan Pengembangan Bioteknologi dan Biodiversitas. Surakarta: LPPM Universitas Sebelas Maret. 71-79.
Sarjono A. 2009. Analisis Kandungan Logam Berat Cd, Pb, dan Hg pada Air dan Sedimen di Perairan Kamal Muara, Jakarta Utara [Skripsi]. Bogor (ID): Institut Pertanian Bogor
Suharto. 2005. Dampak Pencemaran Logam Timbal (Pb) terhadap Kesehatan Masyarakat. Majalah Kesehatan Indonesia No 165/Nty. UNAir Surabaya. Tersedia pada : http://www.pdpersi.co.id (23 Maret 2013)
Suprapti NH. 2008. Kandungan Chromium pada Perairan, Sedimen dan Kerang Darah (Anadara granosa) di Wilayah Pantai Sekitar Muara Sungai Sayung, Desa Morosari Kabupaten Demak, Jawa Tengah. [Jurnal]. Laboratorium Ekologi dan Biosistematik, Biologi. FMIPA. Universitas Dipenogoro, Semarang. Vol. 10, No.2. Hal 53-56. [26 Oktober 2012].
Taryana AT. 1995. Akumulasi logam berat (Cu, Mn, Zn) pada jenis Rhizopora stylosa Griff di hutan tanaman mangrove Cilacap BKPH Rawa Timur, KPH Banyumas Barat perum perhutani unit 1 Jawa Tengah. [skripsi]. Jurusan Manajemen Hutan. Fakultas Kehutanan: Institut pertanian Bogor. [Wetlands International]. 1999. Profil Empat Desa Pesisir: Singajaya, Pabean Udik
dan Brondong, di Kab. Indramayu.. Bogor (ID) PHKA/WI-IP. Bogor Zanganeh AHP, Lakhan, V.C, and Vazyari, M. 2008. Geochemical Associations
and Grain Size Partitioning of Heavy Metals in Nearshore Sediments Along the Iranian Coast of the Caspian Sea. Di dalam: Sengupta M and Dalwani R, editor. Proceedings of The 12th World Lake Conference [internet]. Hlm 198-202. Tersedia pada:http://wldb.ilec.or.jp/data/ilec. [diunduh 23 Maret 2013]
19
LAMPIRAN
Lampiran 1 Alat dan bahan
Nama Alat Fungsi
Termometer Mengukur suhu sedimen
Refraktometer Mengukur salinitas
pH stick Mengukur pH sedimen
Gunting/pisau Memotong tangkai/daun mangrove Sendok Plastik Plastik klip Kertas label Buku floristik Mengambil sedimen Menyimpan sampel
Menandai sampel sesuai Stasiun Menentukan jenis mangrove
Alat tulis Mencatat data
Data Sheet Mencatat data
Cool Box Menyimpan sampel
Plastik klip AAS Sedimen Akar Daun Menyimpan sampel
Menganalisis konsentrrasi logam berat Sampel untuk dianalisis
Sampel untuk dianalisis Sampel untuk dianalisis
Refraktometer pH stick AAS
Daun Sedimen Akar
20
Lampiran 2 Hasil pengukuran parameter fisika kimia
Stasiun suhu salinitas 1 7 25 24 1 7 29 20 1 7 29 30 2 7 25 35 2 7 33 23 3 8 35 25 3 8 36 28 3 7 33 30
Lampiran 3 Hasil logam berat Cu dan Pb pada akar, daun mangrove, dan sedimen
No Parameter Satuan Stasiun 1 Stasiun 2 Stasiun 3
1.1 1.2 1.3 2.1 2.2 2.3 3.1 3.2 3.3
Sedimen
1 Cu ppm 16,42 9,05 13,7 14,49 8,14 3,88 12,83 13,14 8,04
2 Pb ppm 0,954 0,903 0,848 0,897 0,321 0,712 0,816 0,805 0,353
No Parameter Satuan Stasiun 1 Stasiun 2 Stasiun 3
1.1 1.2 1.3 2.1 2.2 2.3 3.1 3.2 3.3 Akar 1 Cu ppm 5,8 3,75 1,36 4,57 1,65 7,96 2,45 7,37 6,91 2 Pb ppm 0,861 0,865 0,529 0,672 1,2 0,66 0,376 0,985 0,784 Daun 1 Cu ppm 1,48 1,37 1,35 2,45 3,48 2,57 1,26 0,471 0,479 2 Pb ppm 0,385 0,387 0,401 0,433 0,374 0,303 0,161 0,257 0,251
21
RIWAYAT HIDUP
Penulis dilahirkan di Sukabumi pada tanggal 08 Mei 1992 sebagai putri ke 2 dari pasangan Iwan Irwanto dan Siti Fauziah. Pendidikan formal pernah dijalani penulis berawal dari TK Tarbiyatul Falah (1995-1997), SDN II Cicurug (1997-2003), SMPN 1 Cicurug (2003-2006), SMAN 1 Cicurug (2006-2009). Pada tahun 2009 penulis diterima di Institut Pertanian Bogor (IPB) melalui jalur USMI, kemudian diterima di Departemen Manajemen Sumber Daya Perairan, Fakultas Perikanan dan Imu Kelautan, Institut Pertanian Bogor.
Selain mengikuti perkuliahan, penulis berkesempatan menjadi Asisten Mata Kuliah Ekosistem Perairan Pesisir (2011/2012), Asisten Mata Kuliah Ekologi Perairan Pesisir dan Laut Tropis (2012/2013) dan Asisten Mata Kuliah Sumberdaya Perikanan (2011/2012). Penulis juga aktif di organisasi kemahasiswaan Badan Eksekutif Mahasiswa (BEM) Fakultas Perikanan dan Ilmu Kelautan (2010/2011) sebagai anggota divisi Komunikasi dan Informasi (Kominfo), dan juga sebagai anggota Himpunan Mahasiswa Manajemen Sumber Daya Perairan (Himasper) serta turut aktif mengikuti seminar maupun berpartisipasi dalam berbagai kepanitiaan di lingkungan kampus IPB.
Sebagai salah satu syarat untuk memperoleh gelar sarjana pada program studi Manajemen Sumber Daya Perairan, Fakultas Perikanan dan Imu Kelautan, Institut Pertanian Bogor, penulis menyusun skripsi dengan judul “Akumulasi
Logam Berat Cu (Tembaga) dan Timbal (Pb) pada Pohon Mangrove ( Rhizopora mucronata) di Perairan Karangsong, Indramayu”.