BAB I PENDAHULUAN 1.1. Latar Belakang
Belerang atau Sulfur adalah unsur kimia dalam SPU yang memiliki lambang S dannomor atom 16. Belerang merupakan unsur non-logam yang tidak berasa. Belerang, dalam bentuk aslinya, adalah sebuah zat padat kristalin kuning. Di alam, belerang dapat ditemukan sebagai unsur murni atau sebagai mineral-mineral sulfida dan sulfat. Belerang adalah unsure penting untuk kehidupan dan ditemukan dalam 2 asam amino.
Belerang atau sulfur didapatkan dalam 2 bentuk yaitu sebagai senyawa sulfida dan sebagai belerang alam. Sebagai senyawa sulfida didapatkan dalam bentuk galena-PbS, chalkopirit-CuFeSz dan Pirit- FeS. Kesemuanya terbentuk akibat proses hidrothermal, kecuali yang tersebut terakhir dapat pula terjadi karena proses sedimenasi dalam kondisi tertentu. Sedang belerang alam unsur tersebut berbentuk kristal bercampur lumpur atau merupakan hasil sublimasi. Endapan belerang ini terbentuk oleh kegiatan solfatara, fumarola atau sebagaiakibat dari gas dan larutan yang mengandung belerang keluar dari dalam bumi melalui rekahan-rekahan, serta selalu berkaitan dengan rangkaian gunung api aktif.Dengan demikian belerang alam dapat dikelompokkan menjadi tipe sublimasi dan tipe lumpur. Belerang berrvarna kuning, kekerasan 1,5-2,5, berat jenis: 2,05' bila dibakar berwarna biru, menghasilkan gas SO2 yang berbau tidak enak' Tempat Diketemukan Seperti telah diuraikan di atas, endapan belerang berkaitan dengan gunung api yang masih aktif.
Belerang di Indonesia banyak terdapat bebas di daerah gunung berapi. Selain terdapat sebagai unsure bebas, juga terdapat dalam bentuk senyawa logam dalam bijih belerang. Belerang digunakan terutama untuk membuat asam sulfat. Pada industri ban, belerang digunakan untuk vulkanisasi karet yang bertujuan agar ban bertambah ketegangannya serta kekuatannya. Selain itu belerang juga digunakan dalam pembuatan pupuk, bubuk mesiu, korekapi, insektisida, dan fungisida.
1.2. Tujuan
Adapun tujuan dibuatnya makalah ini adalah sebagai berikut : 1. Untuk mengetahui kelimpahan belerang di alam.
2. Untuk mengetahui sifat belerang.
3. Untuk mengetahui teknik penambangan belerang. 4. Untuk mengetahui carapengolahan belerang.
BAB II
KETERDAPATAN BELERANG 2.1. Keterdapatan Belerang
Endapan belerang berkaitan dengan gunung api yang masih aktif. Tempat diketemukan endapan belerang antara lain:
Daerah Istimewa Aceh: G. Lamo Mete, P. We, Kab. Aceh besar (merupakan endapan fumarola, kadar S = 30%); Meluak Gayolestan,Kec. Blangkejeraen, Kab. Aceh Tenggara (merupakan endapan solfatara): G. Seulawah, Kab. Aceh Barat (kadar S = 45-50%);Bumiteulong, Kab. Aceh Tengah
Sumatera Utara: G. Sorik Merapi, Kab. Taput (enis danau kawah kadar S =20-93%)
Sumatara Barat: LembangJaya Kab. Solok
Jambi: Sungai Tutung, Air Hangat, Kec. Air Hangat Kab. Kerinci (terdapat sekitar mata air panas, umumya menempel pada batuan lempung tufaan); G. Kunyit, Kec. Gunungraya Kab. Kerinci (terdapat disekitar mata air panas pada umumnya menempel pada batuan lempung tufaan).
Gambar 01. Peta Keterdapatan Belerang
Jawa Barat: G. Papandayan (tipe sublimasi, kadar S = 9O-95%); G.Kraha (tipe sublimasi, kadar S = 25-60%): G. Galunggung (tipe endapan lumpur),
pupuk); G. Ciremai, G. Tangkuban Prahu;G. Wayang. G. Matang, Kawah Saat, Kawah Mas.
Jawa Tengah: G. Dieng (tipe danau kawah dan endapan lumpur,kadar S =32%): G. Telaga Terus
Jawa Timur: G. Arjuna, G. Welirang, K. Ijen (tipe sublimasi, kadar S=20-80%); G.Ijen
Sulawesi Utara: G. Soputan, Kawah Masem (tipe sublimasi, kadar S= 46-56%) Ronasui, Tomboan (tipe sublimasi kadar S = 70%): G.Ambang (tipe sublimasi kadar S =70%); G. Ambang (tipe sublimasi,kadar S = 83-99%); G. Mahawu (tipe danau kawah dan endapan lumpur, kadar S =70%
Maluku: Wuslah, P. Damar (tipe sublimasi dan endapan lumpur kadar S = 55-79%).
2.2. Genesa Belerang
Deskripsi Mineral Belerang : Nama Mineral : Belerang Rumus kimia : S
Berat Jenis (BD) : 2,1
Sistim Kristal : Ortorombik Belahan : Tidak sempurna
Warna : Kuning belerang sampai coklat kekuningan Goresan : Putih
Kekerasan : 1,5-2,5 Skala Mosh
Di Indonesia semua endapan belerang mempunyai hubungan erat dengan kegiatan gunung berapi. Endapan tersebut dapat merupakan endapan sedimen, kerak belerang, atau endapan hidrothermal-metasomatik. Mengenai asal mula belerang ada beberapa pendapat yang membahasnya diantaranya adalah :
1. Menurut Bischof, belerang berasal dari H2S yang merupakan hasil reduksi CaSO4 oleh karbon dan methan. Reaksinya adalah sebagai berikut :
CaSO4 + 2C ---> CaS + 2CO2 CaSO4 + CH4 ---> CaS + CO2 + 2H2O CaS + CO2 + H2O ---> CaCO3 + H2S 2H2S + O2 ---> 2H2O + 2S
Terbentuknya H2S menjadi belerang bisa dengan 2 cara yaitu oksidasi oleh air, tanah dan reaksi antara H2S dengan CaSO4.
2H2S + O2 ---> 2H2O + 2S (O2 dan air tanah) 3H2S + CaSO4 ---> 4S + Ca(OH)2 + 2H2O
2. Pendapat yang mengatakan bahwa belerang berasal dari dome. Belerang disini dibentuk oleh bakteri de sulpho vibrio desulfuricans umpamanya sulfat oleh bakteri diubah menjadi sulfit. Selanjutnya sulfid diubah lagi menjadi belerang contohnya seperti yang terdapat di Gulf-Coast di Amerika Serikat.
3. Pendapat yang menerangkan bagaimana terdapatnya belerang pada gipsum, dikatakan bahwa belerang pada gipsum diendapkan langsung dari poly sulfit (suatu solut yang mengandung sangat banyak belerang ).
Gambar 02. Endapan Belerang
Endapan belerang ini terbentuk oleh kegiatan solfatara, fumarola atau sebagaiakibat dari gas dan larutan yang mengandung belerang keluar dari dalam bumi melalui rekahan-rekahan, serta selalu berkaitan dengan rangkaian gunung api aktif. Dengan demikian belerang alam dapat dikelompokkan menjadi:
1. Tipe sublimasi, yang di dapatkan dari hasil sublimasi uap solfatara dengan kadar belerang (S) adalah sekitar 70 – 99,9 %
2. Tipe lumpur, terdapat di dekat danau kawah dengan kadar belerang (S) adalah sekitar 40 – 60 %
3. Tipe kerak, terdapat di sekitar kawah dengan kadar belerang (S) antara 20 -50 %
BAB III EKSPLORASI
3.1. Eksplorasi
Menurut Sukandarrumidi (1999), eksplorasi merupakan penyelidikan lapangan untuk mengumpulkan data/ informasi selengkap mungkin tentang keberadaan sumber daya alam di suatu tempat. Menurut SNI, eksplorasi adalah kegiatan penyelidikan geologi yang dilakukan untuk mengidentifikasi,menetukan lokasi, ukuran, bentuk, letak, sebaran, kuantitas dan kualitas suatu endapan bahan galian untuk kemudian dapat dilakukan analisis/kajian kemungkinan dilakukanya penambangan.
Penyelidikan terhadap deposit belerang yang dapat dilakukan adalah: 1. Penyelidikan geologi daerah belerang,
2. Pengeboran dan sumur eksplorasi,
3. Sampel diperiksa di laboratorium secara analisa kimia untuk menentukan kadar belerang dan diadakan mikroskopi bijih.
3.2. Teknik Penambangan
Teknik penambangan belerang antara lain sebagai berikut: 1. Tambang Terbuka
2. Tambang Manual 3. Metode Frasch
Berikut dijelaskan tentang teknik penambangan bahan galian belerang, seperti yang telah disebutkan diatas.
3.2.1. Tambang Terbuka
Penambangan endapan belerang dapat dikerjakan dengan cara tambang terbuka, dimana penggalian endapan belerangnya dapat dilakukan dengan alat shovel, dragline, excavator, atau dapat pula dengan cara tambang semprot.
Gambar 03. Shovel Gambar 04. Dragline
Gambar 05. Dump Truck 3.2.2. Tambang Manual
Bila jumlah endapan belerang sedikit, maka penambangannya dapat dilakukan dengan cara manual dengan menggunakan peralatan antara lain berupa cangkul, linggis, ganco dan keranjang serta dilaksanakan dengan sistem padat karya.
Gambar 08. Keranjamg Pikul 3.2.3. Metode Frasch
Sedangakan untuk endapan belerang yang ditutupi oloh lapisan tanah penutup yang sangat tebal. Maka cara penambanganya dapat dilakukan dengan cara Frasch yaitu dengan pemboran kemudian dimasukkan air 3350 F ke dalam endapan belerang, untuk kemudian melalui pipa-pipa kondensasi dipompakann keluardan ditampung dan diendapkan. Tahap berikutnya disublimasi untuk mendapatkan belerang yang bersih.
Menurut Juliantara (2013)
Pengambilan sulfur sendiri memiliki beberapa proses, tergantung sumber dari sulfur itu sendiri. Berikut adalah beberapa cara pengambilan sulfur, antara lain:
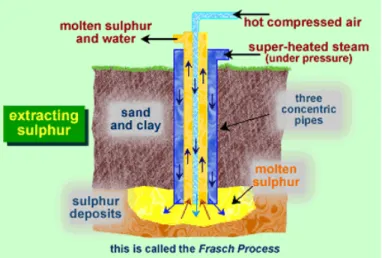
1. Proses Frasch
Sulfur yang diperoleh dari proses ini dilakukan dengan pencairan sulfur di bawah tanah/laut dengan air panas, lalu memompanya ke atas permukaan bumi. Pada proses ini digunakan 3 buah pipa konsentris 6’, 3’, dan 1’. Air panas dengan suhu 3250C dipompakan ke dalam batuan sulfur melalui bagian pipa 6’, sehingga sulfur akan meleleh (2350F). Lelehan sulfur yang lebih berat dari air akan masuk ke bagian bawah antara pipa 3’ dan 1’, dan dengan tekanan udara yang dipompakan melalui pipa 1’, air yang bercampur dengan sulfur akan naik ke atas sebagai crude S, kemudian diolah menjadi crude bright atau refined S.
Gambar 09. Diagram Frasch 2. Pengambilan dari gunung berapi
Deposit Sulfur di gunung berapi dapat berupa batuan, lumpur sedimen atau lumpur sublimasi, kadarnya tidak begitu tinggi (30-60%) dan jumlahnya tidak begitu banyak (600-1000 juta ton).
Di gunung Talaga Bodas di dapat dalam bentuk lumpur dengan kadar S (30– 70%) dan jumlah deposit 300 juta ton. Tempat – tempat lainnya adalah : kawah Ijen, Gunung Welirang, Gunung Dieng dan Gunung Tangkuban Perahu. Pemanfaatan sulfur melalui cara ini diperlukan adanya peningkatan kadar sulfur terlebih dahulu dengan cara flotasi dan benefication.
Cara flotasi yaitu dengan cara menambahkan air dan frother yang nantinya akan membuat sulfur terapung dan dapat dipisahkan. Cara benefication lebih rumit dibandingkan dengan flotasi yaitu awalnya sulfur ditambahkan dengan air dan reagen, kemudian reagen dipanaskan dalam autoklaf selama 1/2-3/4 jam pada tekanan 3 atm. Nantinya setiap partikel kecil dari sulfur akan terkumpul, lalu dilakukan pencucian dengan air untuk menghilangkan tanah. Setelah itu dipanaskan kembali dalam autoklaf sehingga sulfur akan terpisah sebagai lapisan S dengan kadar 80-90%.
Salah satu yang paling menarik yaitu di Kawah Ijen. Beberapa penambang mengambil belerang dengan cara melinggis bongkahan belerang di kaldera Gunung Ijen di Desa Ampelgading, Kecamatan Licin, Banyuwangi, Jawa Timur,
Selasa (20/10). Berdasar data di Dinas Energi Sumber Daya Mineral (ESDM) Provinsi Jatim, kapasitas produksi belerang Gunung Ijen mencapai 1.736,318 ton. Belerang ini muncul dari perut bumi karena aktivitas magma yang mendorong air dari sumber mata air keluar ke permukaan bumi dengan membawa belerang.
Gambar 10. Penyemprotan Belerang Gambar 11. Reduksi Ukuran
Gambar 12. Pemuatan Belerang Gambar 13. Pengangkutan Belerang. Penambang menggunakan cara yang sangat sederhana untuk “menangkap” belerang. Mereka memasang pipa yang terbuat dari besi (pawon) berdiameter 16 – 20 cm. Setiap pipa panjangnya 1 m. agar mudah memasang dan menggantinya jika rusak. Pipa tersebut dipasang sambung menyambung mulai dari tebing atas dimana titik solfatara yang suhunya mencapai 200o C sekaligus sebagai sumber belerang hingga dasar tebing yang jauhnya antara 50 - 150 m. Melalui pipa tersebut gas belerang dialirkan kemudian tersublimasi di ujung pipa bagian bawah dan siap ditambang. Apabila salah satu pipa rusak karena korosif, maka uap
belerang tidak mengalir sempurna dan terlepas ke udara bebas dan tidak sempat tersublimasi. Kendala lainnya adalah ketika suhu solfatara naik melampaui 200o C, maka uap belerang tidak sempat tersublimasi karena terbakar.
3. Pengambilan Sulfur dari Gas Buang
Tak dapat dipungkiri bahwa saat ini Indonesia memiliki banyak industri yang semakin berkembang. Semakin banyak industri tersebut maka semakin banyak pabrik pengolahan dan tentu semakin banyak gas buang yang dihasilkan. Sulfur adalah salah satu unsur yang dapat diperoleh dari gas buang tersebut. Sulfur diperoleh dari flue gas asal pembakaran batu bara atau pengilangan minyak bumi. Sulfur ini tidak boleh dibuang langsung ke udara karena dapat menimbulkan pencemaran. Oleh karena itu gas buang tersebut terlebih dahulu harus diabsorpsi dengan menggunakan etanolamin dan sebagainya, kemudian dipanaskan kembali untuk mendapatkan gasnya dan kemudian diproses lebih lanjut.
3.3. Pengolahan
Pengelolaan dan Pemanfaatan belerang di Indonesia telah dilakukan dalam waktu yang lama tepatnya sejak jaman kolonial Belanda. Pengelolaan masih dilakukan dengan bentuk dan cara kerja yang sederhana tanpa didukung oleh teknologi yang memadai dan tepat guna. Berdasarkan beberapa artikel yang serupa tentang penambangan belerang di Kawah Ijen menunjukan bahwa proses penambangan belerang dan sumber daya manusia yang berproses didalamnya masih sangat minim dan tradisional. Sumber daya manusia berasal dari masyarakat sekitar yang tentunya mayoritas berekonomi lemah dan kurangnya pengetahuan dan pendidikan yang memadai.
Cara pengolahan belerang tergantung dari jenis endapannya dan hasil yang diinginkan.
1. Untuk belerang yang berbentuk kristal dapat langsung dimasukkan kedalam autiklat dimasukkan/ditambahkan solar, air dan NaOH, kemudian dipanaskan dengan memasukkan uap air panas dengan tekanan 3 atmosfer selama 30-60 menit. Pemisahan akan terjadi karena belerang mempunyai
titik lebur yang lebih rendah dibandingkan dengan mineral-mineral pengotornya. Hasilnya yang berupa belerang cair dialirkan melalui filter dan kemudian dicetak.
Gambar 14. Belerang Cair
2. Untuk belerang jenis lumpur, pengolahannnya perlu dilakukan secara floatasi terlebih dahulu sebelum dimasukkan kedalam autoklaf. Tujuan dari floatasi adalah untuk meningkatkan kadar belerang dan memisahkan senyawa-senyawa besi sulfat dan silikat dari larutan. Cara pengolahan lain untuk belerang jenis ini dengan cara pelarutan dan penghabluran dengan menggunakan pelarut karbon disulfida, dimethyl disulfit atau larutan hidrokarbon berat lainnya.
3. Untuk pengolahan belerang secara sederhana dapat dilakukan dengan jalan memanaskan bongkah-bongkah belerang didalam wajan besi atau alumunium yang berdiameter 80-100 cm diatas tungku sederhana yang terbuat dari tanah liat/andesit. Pemanasan dilakukan dengan kayu atau kompor minyak tanah sambil diaduk-aduk, sesudah belerang mencair kemudian disaring dengan kantong-kantong yang terbuat dari kain. Selanjutnya ditampung dalam tabung-tabung bambu sebagai alat cetaknya.
Gambar 16. Pengolahan Belerang Secara Sederhana 3.4. Dampak Penambangan Belerang
Usaha di bidang pertambangan adakalanya menimbulkan sebuah dampak. Dampak pertambangan tidak saja merupakan masalah pada sektor tambangnya, akan tetapi juga menyangkut mengenai masalah lingkungan hidup dan masyarakat disekitarnya. Di dalam pengelolaan lingkungan berasaskan pelestarian kemampuan agar hubungan manusia dengan lingkungannya selalu berada pada kondisi optimum, dalam arti manusia dapat memanfaatkan sumber daya dengan dilakukan secara terkendali dan lingkungannya mampu menciptakan sumbernya untuk dibudidayakan. Sebagai contoh kita berbicara mengenai dampak penambangan belerang di Gunung Ijen Desa Tamansari, Kecamatan Licin Kabupaten Banyuwangi maka dapat dikaji dari sisi yaitu dampak positif dan dampak negatif.
a. Terserapnya tenaga kerja, yakni masyarakat sekitar Kawah Ijen sebagai penambang belerang maupun tenaga tehnis di perusahaan penambangan belerang tersebut. Dengan ini juga mengurangi tingkat pengangguran yang ada di sekitar daerah tersebut.
b. Menambah Pendapatan Asli Daerah (PAD) dengan kewajiban pengusaha penambang belerang dalam hal ini PT. Candi Ngrimbi untuk membayar retribusi dan iuran-iuran lain.
c. Kualitas lingkungan di tempat penambangan meningkat dengan tajam dan alam sekitar menjadi tertata lebih baik, dengan kelengkapan infrastruktur dari penambangan. Karena itu kegiatan penambangan dapat menjadi daya tarik, sehingga penduduk banyak yang berpindah mendekati lokasi penambangan tersebut. Sering pula dikatakan bahwa bahwa kegiatan penambangan telah menjadi lokomotif ekonomi bagi masyarakat Tamansari.
d. Memperlancar transportasi, karena yang tadinya jalan penduduk setempat hanya merupakan jalan setapak, maka diupayakan pengusaha untuk membuat jalan aspal agar dapat dilewati alat berat dan dump truck yang mengangkut belerang.
e. Bagi para penambang, pekerjaan rutin mereka sebagai penambang belerang yang setiap hari bergelut dengan asap belerang telah merubah f. Memudahkan para wisatawan Ijen, karena para penambang belerang
selain sebagai penambang terkadang juga ikut memandu jalan para turis naik ke Kawah Ijen.
3.4.2. Dampak Negatif
a. Berkurangnya sumber daya alam belerang.
b. Resiko akibat penambangan belerang bagi penambang yakni para penambang belerang rawan terserang infeksi saluran pernafasan atas (ISPA). "Sifat dari belerang atau sulfida itu adalah racun atau toksik. Karena itu sulfida yang berbentuk gas juga beracun karena menyerang saluran pernafasan dan paru-paru.
c. Berubahnya organ paru-paru para penambang yakni lebih bertambah besar dari ukuran organ paru-paru manusia biasanya, akibat sering menghirup asap belerang.
d. Pencemaran udara atau polusi bagi masyarakat di sekitar tempat pengolahan belerang.
e. Adanya para pendatang dan wisatawan telah mengakibatkan terjadinya akulturasi kebudayaan yang mengancam eksistensi kebudayaan asli daerah setempat.
3.5. Reklamasi
Reklamasi adalah kegiatan yang bertujuan memperbaiki atau menata kegunaan lahan yang terganggu sebagai akibat kegiatan usaha pertambangan, agar dapat berfungsi dan berdaya guna sesuai peruntukannya. Dalam hal ini yaitu reklamasi tambang belerang dimanfaatkan sebagai kawasan tempat wisata, dimana reklamasi dapat berupa pemandian air panas yang berada di Obyek Wisata Belerang Baturraden, Kab. Purwokerto, juga dapat berupa pemandangan alam seperti yang ada di Obyek Wisata Kawah Belerang Garuda Jaya Kec. Dukupuntang Kab. Cirebon, dan obyek wisata lainnya.
BAB IV
PEMANFAATAN DAN PEMASARAN 4.1. Pemanfaatan
Belerang banyak digunakan dalam industri kimia yaitu untuk pembuatan asam sulfat (H2SO4) yang diperlukan untuk pembuatan pupuk, penghalusan minyak bahan-bahan kimia berat dan keperluan lain untuk metalurgi. Di samping belerang dimanfaatkan dalam industri cat, industri karet, industri tekstil, industri korek api, bahan peledak, industri ban, pabrik kertas, industri gula yang digunakan dalam proses sulfinasi, industri rayon, film celulosa, ebonit, cairan sulfida, CS2, bahan anti seranggaltikus,bahan pengawet kayu, obat-obatan dan lain-lain. Beberapa persyaratan yang harus dipenuhi yaitu:
1. Komponen Produksi Pupuk (Kadar S : 99,88%)
Belerang yang ditemukan secara langsung dari sumber alam memang tidak dapat digunakan secara langsung. Belerang harus dirubah dalam bentuk asam sulfat dengan metode proses pembakaran khusus. Setelah itu asam sulfat bisa menjadi campuran pembuatan beberapa jenis pupuk pertanian seperti ammonium sulfat dan fosfat. Hal ini seperti manfaat batubara sebagai barang tambang yang digunakan dalam industri pupuk.
2. Bahan Pembuatan Korek Api (kadar S :98%)
Bubuk belerang yang mengandung asam sulfat ternyata menjadi bahan pokok dalam pembuatan korek api. Proses ini akan membuat lapisan bubuk belerang memiliki warna yang lebih gelap dan mengkilap serta bisa memicu panas tinggi yang menyebabkan munculnya api. Kemudian, manfaat hutan yang menghasilkan kayu pinus, digunakan sebagai batang korek apinya.
Gambar 19. Korek Api 3. Belerang dalam Proses Industri ban (S =99,997)
Proses pengolahan karet murni membutuhkan belerang untuk membentuk karet agar mudah dibentuk. Pembakaran yang dihasilkan dari belerang mampu membuat panas yang cukup tinggi sehingga karet hitam yang diproduksi bisa menjadi lebih elastis dan mudah dibentuk. Proses ini bahkan sudah dilakukan dengan bahan belerang murni tanpa pengolahan.
4. Belerang untuk Produksi Asam Sulfat (99.8%)
Produksi asam sulfat biasanya mempergunakan manfaat oksigen, untuk proses pemberian lapisan pada tambang belerang. Hal ini akan membuat belerang bisa diolah menjadi bahan khusus yang bisa dimanfaatkan untuk komponen bahan kimia pada beberapa industri seperti tekstil, produk kimia dan bahan peledak.
Gambar 21. Asam Sulfat Proses Pembuatan Asam Sulfat
Proses pembuatan asam sulfat akan dilakukan dengan cara proses kontak, dengan digunakan katalisator vanadium (V )oksida, V2O5.
Tiga langkah utama dalam proses kontak, yaitu: 1. Pembakaran belerang menajdi belerang dioksida.
Proses produksi asam sulfat di awali dengan peleburan sulfur (S) yang digunakan sebagai bahan baku utama dengan menggunakan steam yang dialirkan pada coil-coil di Sulfur Melter pada tekanan 4 Kg/cm2. Kemudian sulfur cair dipompakan dari Sulfur Melter melalui pipa-pipa dan disemprotkan ke dalam Furnace. Di dalam Furnace terjadi pembakaran belerang dengan udara.
Reaksi: S(s) + O2(g) → SO2(g)
Udara yang digunakan disuplai oleh Main Blower yang sudah mengalami proses pengeringan. Proses pengeringan udara dilakukan di Drying Tower dengan menggunakan asam sulfat sirkulasi dengan konsentrasi 93%-98%. Proses pengeringan udara tersebut dimaksudkan untuk mencegah korosi oleh gas pada pembakaran dan untuk menghilangkan kandungan air dalam udara.
Proses pembakaran belerang cair menjadi SO2 dengan temperature pembakaran kurang lebih 750-770oC. Gas hasil pembakaran di Furnace kemudian dialirkan ke Boiler melalui tube-tube untuk diambil panasnya guna menghasilkan steam yang digunakan untuk mencairkan belerang di Sulfur Melter, sebagian gas yang lain dialirkan ke Heat Exchanger bersama dengan gas keluar dari Boiler yang telah diambil panasnya. Di dalam Heat Exchanger gas didinginkan dengan menggunakan udara yang di suplai oleh Blower. Setelah itu aliran gas mengalami proses penyaringan dan penstabilan suhu gas di Hot Gas Filter.
2. Oksidasi SO2 menjadi SO3.
Dari Hot Gas Filter aliran gas masuk ke Converter. Converter ini terdiri dari empat bed katalis V2O5. Aliran gas masuk ke setiap bed diatur pada temperature 425-440oC. Dengan bantuan katalis ini aliran gas tersebut (SO2) diubah menjadi gas SO3. Reaksi ini merupakan reaksi eksoterm sehingga gas tersebut harus didinginkan pada tahap-tahap katalis.
Aliran gas keluar bed I dan bed II didinginkan dalam 1st and 2nd Heat Exchanger. Sedangkan aliran gas dari bed III langsung masuk ke bed IV karena perbedaan temperature gas keluar dan bed III dan bed IV sudah kecil.
Reaksi: 2SO2(g) + O2(g) ↔ 2SO3(g) ∆H = -196,6 kJ/mol
Dari converter aliran gas SO3 masuk ke dalam SO3 Cooler A untuk didinginkan. Kemudian didinginkan lebih lanjut ke SO3 Cooler B setelah itu aliran gas tersebut masuk ke Absorbing Tower.
3. Reaksi SO3 dengan air menjadi H2SO4.
Di Absorbing Tower terjadi proses penyerapan gas SO3 dengan menggunakan sirkulasi asam sulfat dengan konsentrasi 98-99% yang diatur di AT Pump Tank. Asam resirkulasi tersebut kemudian diencerkan dengan menambahkan air dan setelah itu baru dialirkan kembali ke dalam AT Pump Tank. Asam sulfat yang dihasilkan pada AT Pump Tank setelah mencapai level maksimum yang ditentukan, kemudian ditransfer dan ditampung di Sulphuric Acid Storage Tank.
Gambar 22. Diagram Alir Pembuatan Asam Sulfat cara Kontak
Untuk meningkatkan produksi, laju pembentukan gas SO3 merupakan hal yang penting. Oleh karena itu, perlu ditinjau asas Le Chatelier dari reaksi kesetimbangan tersebut. Reaksi (2) merupakan reaksi eksoterm yang menyangkut perubahan 2 mol gas SO2 dengan 1 mol gas O2 menjadi 3 mol SO3 sehingga hasilnya akan maksimum jika:
1. Tekanan diperbesar
Reaksi akan bergeser ke kanan jika tekanannya dinaikkan. Pada kenyataannya reaksi ini dapat berlangsung dengan baik pada tekanan 1 atmosfer (1 atm). Kenaikan tekanan menyebabkan kenaikan jumlah produk yang kurang berarti dibandingkan dengan biaya yang dikeluarkan. Oleh karena itu, proses kontak dilakukan pada tekanan 1 atm.
2. Reaksi berlangsung pada suhu rendah
Reaksi (2) akan bergeser ke kanan jika suhu diturunkan. Akan tetapi, jika suhu diturunkan reaksi akan berjalan lambat. Hal ini sesuai dengan azas laju reaksi, ketika suhu semakin turun, reaksi akan berlangsung semakin lambat. Untuk mengatasi hal ini, maka ditambahkan katalis V2O5. Penambahan katalis menyebabkan jalannya reaksi berubah, tetapi dengan energi pengaktifan lebih rendah.
Tahap 1: SO2(g) + V2O5(s) → SO3(g) + V2O4(s) Tahap 2: V2O4(s) + ½ O2(g) → V2O5(s)
Reaksi total : SO2(g) + ½ O2(g) → SO3(g)
Proses reaksi SO3 dengan air berlangsung eksoterm sehingga suhu dalam proses reaksi akan naik. Kenaikan suhu mengakibatkan gas SO3 terurai kembali menjadi SO2 dan O2. Untuk mencegah hal tersebut, proses reaksi SO3 dengan H2O tidak dilakukan secara langsung, tetapi melalui pengenceran SO3 dalam H2SO4. Larutan uap SO3 dalam H2SO4 encer ini dikenal dengan H2SO4 pekat atau oleum. Kadar asam sulfat dalam oleum ini mencapai 98% dan lebih dikenal sebagai asam sulfat berasap.
Kegunaan Asam Sulfat
Secara umum asam sulfat digunakan untuk: a. Industri pupuk (ZA, SP 36, SP 18)
b. Bahan kimia (Asam Fosfat, Tawas, PAC, Serat Rayon, Alkohol, Detergen) c. Industri makanan (bumbu masak (MSG), Lysine, dll)
d. Industri Tekstil, spiritus, utilitas pabrik, dan pertambangan
Asam sulfat merupakan komoditas kimia yang sangat penting, produksi asam sulfat suatu negara merupakan indikator yang baik terhadap kekuatan industri negara tersebut. Kegunaan asam sulfat, yaitu:
1. Penggunaan utama (60% dari total produksi di seluruh dunia) asam sulfat adalah dalam "metode basah" produksi asam fosfat, yang digunakan untuk membuat pupuk fosfat dan juga trinatrium fosfat untuk deterjen.
2. Asam sulfat digunakan dalam jumlah yang besar oleh industri besi dan baja untuk menghilangkan oksidasi, karat, dan kerak air sebelum dijual ke industri otomobil.
3. Kegunaan asam sulfat lainnya yang penting adalah untuk pembuatan aluminium sulfat. Alumunium sulfat dapat bereaksi dengan sejumlah kecil sabun pada serat pulp kertas untuk menghasilkan aluminium karboksilat yang membantu mengentalkan serat pulp menjadi permukaan kertas yang keras. Aluminium sulfat juga digunakan untuk membuat aluminium hidroksida. Aluminium sulfat dibuat dengan mereaksikan bauksit dengan asam sulfat: Al2O3 + 3 H2SO4 → Al2(SO4)3 + 3 H2O
4. Asam sulfat juga memiliki berbagai kegunaan di industri kimia. Sebagai contoh, asam sulfat merupakan katalis asam yang umumnya digunakan
untuk mengubah sikloheksanonoksim menjadi kaprolaktam, yang digunakan untuk membuat nilon.
4.2. Pemasaran Belerang
Belerang murni hasil pengolahan dari PT. Candi Ngrimbi berupa belerang dalam bentuk bubuk, bongkahan, dan cake dengan kemurnian mencapai 99,8% dan spesifikasi yang berbeda-beda. Belerang ini kemudian dipasarkan di pasar domestik maupun ekspor melalui distributor yang telah bekerja sama dengan perusahaan ini. Belerang dari kawah ijen termasuk belerang yang memiliki kwalitas terbaik di dunia sehingga dalam pemasarannya PT. Candi Ngrimbi tidak mengalami kesulitan. Negara pengimpor belerang dari Indonesia antara lain Jepang, Thailand, Korea, Filipina, dan Vietnam. Belerang yang diimpor oleh negara-negara tersebut terutama digunakan dalam industri pupuk dan kosmetik.
Gambar 23. Kemasan Bongkahan Gambar 24. Kemasan Bubuk
Untuk belerang yang di jual untuk masyarakat umum biasanya digunakan sebagai perawatan kulit untuk menghilangkan jerawat, panu, kudis, kurap, juga untuk berbagai masalah kulit lainnya seperti ketombe, alergi, dan mengurangi jumlah minyak berlebihan. Dengan harga Bongkah Rp. 4500/kg dan Bubuk Rp. 5000/kg.
Asam Sulfat Pemasaran Asam sulfat :
1. asam sulfat (H2SO4) analis/liter Rp. 825.000 2. asam sulfat (H2SO4) teknis/100ml Rp.13.000
BAB V PENUTUP 5.1. Kesimpulan
1. Belerang merupakan unsur non-logam yang tidak berasa. Belerang, dalam bentuk aslinya, adalah sebuah zat padat kristalin kuning.
2. Semua endapan belerang mempunyai hubungan erat dengan kegiatan gunung berapi. Endapan tersebut dapat merupakan endapan sedimen, kerak belerang, atau endapan hidrothermal-metasomatik.
3. Penambangan endapan belerang dapat dikerjakan dengan cara tambang terbuka,tambang semprot,tambang manual,proses frasch.Menurut Juliantara (2013), pengambilan sulfur sendiri memiliki beberapa proses yaitu; frasch, pengambilan dari gunung api, pengambilan sulfur dari gas buang.
4. Untuk pengolahan belerang tergantung dari jenis endapannya dan hasil yang diinginkan seperti ; Untuk belerang yang berbentuk Kristal, Untuk belerang jenis lumpur, Untuk pengolahan belerang secara sederhana. 5. Belerang banyak digunakan dalam industri kimia yaitu untuk pembuatan
asam sulfat (H2SO4) yang diperlukan untuk pembuatan pupuk, larutan asam sulfat, bahan pembuat korek api, dan campuran dalam pembuatan ban.
5.2. Saran
Kegunaan belerang yang pokok dalam pencampuran industri kimia di indonesia sangat tidak di dukung dengan keamanan dan keselamatan kerja dalam penambangannya. Mestinya pemerintah dan perusahaan terkait melengkapi K3 dan memperhatikan K3 untuk pekerjanya, mengenai perundang undangan pun masih belum jelas.