SB/O/BF/07
RESPON FISIOLOGI IKAN NILA, Oreochromis niloticus, YANG
DISTIMULASI DENGAN DAUR PEMUASAAN
DAN PEMBERIAN PAKAN KEMBALI
Farida Nur Rachmawati; Untung Susilo dan Yulia Sistina 1)
1)Laboratorium Fisiologi Hewan Fakultas Biologi Unsoed; [email protected]
ABSTRAK
Penelitian tentang respon fisiologi ikan Nila, Oreochromis niloticus, yang distimulasi dengan daur pemuasaan dan pemberian pakan kembali telah dilakukan secara eksperimental menggunakan rancangan dasar rancangan acak lengkap (RAL) dengan 5 perlakuan dan masing-masing perlakuan diulang sebanyak 5 kali. Perlakuan yang dicobakan yaitu : ikan diberi pakan setiap hari (P0/kontrol); ikan dipuasakan selama 4 hari (P1); ikan dipuasakan selama 8 hari (P2); ikan dipuasakan 4 hari dan diberi pakan 4 hari (P3) dan ikan dipuasakan 8 hari dan diberi pakan 8 hari (P4). Hasil percobaan menunjukkan bahwa kadar Hb ikan yang dipuasakan dan diberi pakan kembali tidak berbeda nyata (P>0,05) , sedangkan kadar glukosa darah , nilai hematokrit dan nilai osmolaritas plasma menunjukkan perbedaan yang nyata antar perlakuan (P<0,05). Oleh karena itu dapat disimpulkan bahwa ikan Nila yang dipuasakan dan diberi pakan kembali akan mengalami perubahan profil darah yang meliputi, kadar glukosa darah, nilai osmolalitas plasma dan hematokrit sebagi respon fisiologi ikan dalam menjaga kondisi homeostasis tubuhnya..
Kata kunci : respon fisiologi, profil darah, pemuasaan, Oreochromis niloticus
PENDAHULUAN
Ikan nila (Oreochromis nilaticus) merupakan salah satu jenis ikan komersial penting yang menyokong kebutuhan protein hewani bagi masyarakat. Ikan ini mudah dibudidayakan, akan tetapi tingginya harga pakan dari waktu ke waktu berdampak pada meningkatnya biaya produksi. Oleh karena itu perlu dilakukan alternatif dengan membatasi pemberian pakan pada usaha budidaya ikan nila,
sehingga dapat meningkatkan
produktivitasnya.
Pembatasan pakan baik secara tunggal maupun periodik mampu
meningkatkan kecepatan pertumbuhan ikan (compensatory growth), yang merupakan fase percepatan pertumbuhan yang diperoleh setelah ikan diberi pakan kembali.
Pemuasaan pada ikan merupakan salah satu faktor lingkungan yang memicu perubahan fisologis pada ikan. Dalam kondisi puasa ikan pada umunya mengalami stres, sehingga berpengaruh terhadap aktifitas fisiologi hewan. Stres merupakan respon bertahan pada hewan terhadap penyebab stres (stressor). Berbagai sumber stres baik berupa faktor lingkungan (suhu, cahaya, pemeliharaan,
penangkapan dan transport) maupun faktor biotik seperti infeksi mikroorganisme akan mempunyai dampak negatif terhadap perubahan fisiologis tubuh hewan. Perubahan tersebut meliputi , gangguan pertumbuhan, produktivitas dan semua aktivitas yang merupakan akibat dari mekanisme homeostasis dalam tubuh yang terganggu.
Karakteristik darah dapat digunakan untuk mengevaluasi respon fisiologi pada ikan [1]. Respon stres pada hewan dapat dilihat dari perubahan kadar hormon kortisol, glukosa darah, Hemoglobin, dan hematokrit. Dalam kondisi stres terjadi penurunan jumlah eritrosit, , nilai hematokrit dan kadar hemoglobin, sedangkan jumlah leukosit cenderung meningkat [2].
Didalam budidaya perikananan masalah penangkapan, transport benih dan pemeliharaan merupakan aktivitas yang dapat menimbulkan stres pada ikan baik teleostei [3] dan elasmobranchii [4]. Berkaitan dengan hal tersebut, ikan akan mengalami hiperaktivitas yang merupakan respon bertahan terhadap stres, dan jika berlebihan maka ikan akan mati [5]. Timbulnya respon stres tersebut menunjukkan terjadinya adaptasi terhadap perubahan yang tidak terduga dan untuk mengembalikan pada kondisi homeostasis.
Pemuasaan pada ikan juga dapat memicu timbulnya stres pada hewan. Pada
kondisi stres, terjadi perubahan yang nyata terhadap parameter hematologi. Pada Scyliorhinus canicula, perlakuan stres menurunkan jumlah eritrosit, nilai hematokrit dan kadar hemoglobin serta meningkatkan kadar glukosa darah [2].
Jumlah eritrosit muda dalam darah perifer ikan traira, Hoplias malabaricus menurun secara signifikan selama 30 hari pertama pemuasaan yang menunjukkan bahwa proses senescence terjadi pada eritrosit yang telah ada dan bahwa sel darah tidak diganti selama ikan tersebut tidak diberi pakan. Selama periode pemberian pakan kembali, jumlah leukosit dan trombosit pulih, namun jumlah eritrosit tetap menurun [6]. Pada ikan kerapu bebek, Cromileptes altivelis yang tidak diberi pakan selama 1 hari kemudian diberi pakan selama 2 atau 3 hari menunjukkan peningkatan jumlah leukosit sebagai indikasi peningkatan sistem kekebalan [7]. Peningkatan kekebalan tubuh yang berkaitan dengan pertumbuhan cepat akan sangat bermanfaat dalam budidaya ikan nila.
Studi profil darah ini menunjukan bahwa pembatasan pakan dapat menghasilkan perubahan kapasitas sistem kekebalan dan mobilisasi simpanan energi tubuh untuk menopang aktivitas selama periode pembatasan pakan. Namun demikian, respon fisiologi ikan nila pada
kondisi puasa dan diberi pakan kembali belum dilaporkan.
Tujuan dari penelitian ini adalah mengamati respon fisiologi ikan Nila yang meliputi nilai hematokrit, osmolalitas plasma, kadar glukosa darah dan Hb pada kondisi puasa dan pemberian pakan kembali.
BAHAN DAN CARA KERJA
Penelitian dilakukan pada skala laboratorium di laboratorium Fisiologi Hewan Fakultas Biologi Unsoed, Purwokerto.
Materi penelitian yang digunakan terdiri atas ikan nila berukuran 10 – 15 gram, akuarium, osmometer, “ Blood Glucose Test Meter “ GlucoDr” (Allmedicus), senfrifugasi mikro-hematokrit , pakan ikan, dan peralatan pemeliharan ikan.
Penelitian dilakukan secara eksperimental menggunakan rancangan dasar berupa rancangan acak lengkap (RAL) dengan 5 perlakuan yang diulang sebanyak 5 kali. Perlakuan yang dicobakan adalah sebagai berikut :
1. ikan diberi pakan setiap hari (kontrol)
2. ikan dipuasakan selama 4 hari 3. ikan dipuasakan selama 8 hari
4. ikan dipuasakan selama 4 hari dan diberi pakan kembali selama 4 hari
5. ikan dipuasakan selama 8 hari dan diberi pakan kembali selama 8 hari.
Ikan nila yang digunakan dalam penelitian ini diperoleh dari petani ikan desa Bobosan, kecamatan Purwokerto Utara. Ikan diaklimasi di laboratorium selama 5 hari. Pada hari terakhir aklimasi ikan dipuasakan selama 24 jam dan ditimbang bobotnya, selanjutnya ikan ditempatkan pada akuarium percobaan.
Akuarium yang digunakan
berukuran 60 x 40 x 70 cm sebagai unit percobaan dengan padat penebaran 10 ekor. Sistem pemeliharaan menggunakan sistem air statis dengan tinggi air ± 40 cm.
Parameter yang diukur dalam penelitian adalah kadar hb, glukosa darah, nilai hematokrit dan nilai osmolalitas plasma.
Sampel darah untuk keperluan pengamatan profil darah diambil dari pembuluh darah kaudal menggunakan spuit 1ml yang telah dibilas dengan EDTA. Darah lalu ditampung dalam tabung ependorf yang telah diisi larutan EDTA 5 µl untuk 0,5 ml darah. Nilai hematokrit ditentukan setelah sampel darah dalam kapiler gelas disentrifugasi selama 5 menit dengan kecepatan 3000 rpm menggunakan senfrifugasi mikro-hematokrit, hasil sentrifugasi kemudian dibaca dengan mikro-hematrokrit reader ([8]. Nilai osmotik plasma darah diukur dengan menggunakan vapour osmometer Wescor
dan nilai osmolalitas plasma akan dinyatakan dalam unit mOsm/kg. Kadar glukosa darah diukur menggunakan kit Gluko Dr, dan nilai glukosa darah akan diperoleh dalam unit mgr/dl.
Data yang diperoleh berupa kadar glukosa darah, Hb, nilai hematokrit dan nilai osmotik plasma selanjutnya dianalisa dengan program SPSS.
HASIL DAN PEMBAHASAN
Respon fisiologi ikan nila yang dipuasakan dan diberi pakan kembali dapat diamati dengan melihat profil darah yang meliputi nilai hematokrit, osmolalitas plasma, kadar Hb dan glukosa darah (Gambar1, 2, 3 dan 4)
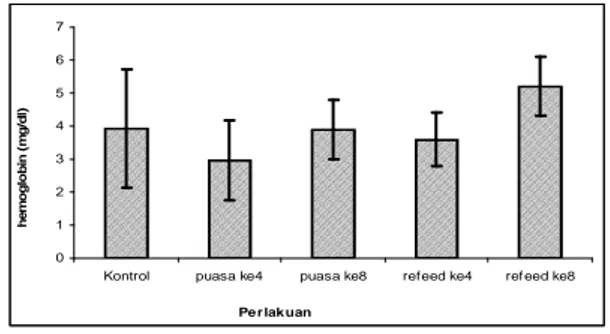
Kadar Hb ikan nila pada penelitian ini berkisar antara 2,98 – 5,20 g/dl, masing-masing yaitu pada perlakuan kontrol 3,94 g/dl, ikan yang dipuasakan selama 4 hari sebesar 2,98 g/dl, ikan yang dipuasakan selama 8 hari sebesar 3,91 g/dl, ikan yang diberi pakan kembali selama 4 hari sebesar 3,6 g/dl dan pada ikan yang diberi pakan kembali selama 8 hari sebesar 5,2 g/dl.
Hasil analisis ragam menunjukkan bahwa nilai rata-rata Hb masing-masing perlakuan tidak berbeda nyata (P>0.05). Hal ini menunjukkan bahwa kadar Hb selama pemuasaan tidak mengalami perubahan, demikian juga pada saat ikan diberi pakan kembali.
Kadar Hb ikan nila pada penelitian ini sangat rendah yaitu berkisar antara 2,98 – 5,20 g/dl. Hal ini diduga perlakuan pemuasaan yang diberikan pada penelitian ini secara terus menerus (4 hari dan 5 hari), menurunkan status kesehatan ikan yang tercermin pada penurunan kadar Hb. Sementara kadar Hb yang rendah pada kontrol, disebabkan ikan masih dalam masa aklimasi.
Hasil yang sama juga dijumpai pada ikan sidat, Anguilla anguilla, yang diberi perlakuan pemuasaan antara 47 hingga 96 hari [9], dan pada ikan traira, Hoplias malabaricus yang dipuasakan selama 240 hari kemudian diberi pakan kembali selama 30 hari [6] kadar Hb mengalami penurunan.
Berbeda dengan hasil penelitian pada ikan lele dumbo yang dipuasakan secara periodik (2/3 dan 2/5) selama 4 minggu pemeliharaan, kadar Hb lebih tinggi berkisar antara 6,47 – 7,67 g/dl [10]. 0 1 2 3 4 5 6 7
Kontrol puasa ke4 puasa ke8 refeed ke4 ref eed ke8
Pe rlak uan h e m o g lo b in ( m g /d l)
Gambar 1. Nilai rata-rata kadar Hb ikan nila yang dipuasakan dan diberi pakan kembali
nilai osmolalitas plasma ikan Nila yang berbeda nyata antar perlakuan (P<.0,05). Nilai osmolalitas plasma ikan Nila selama penelitian masing-masing adalah 4,63 mosm/kg (kontrol), 4,732 mosm/kg (puasa selama 4 hari), 4,165 mosm/kg (puasa selama 8 hari), 4,623 mosm/kg (pemberian pakan kembali selama 4 hari) dan 1,787 mosm/kg (pemberian pakan kembali selama 8 hari). 0 100 200 300 400 500 600 700 800
kontrol puasa ke4 puasa ke8 ref eed ke4 ref eed ke8
pe r lak uan O s m o la li ta s (m O s /k g )
Gambar 2. Rata-rata nilai osmolalitas plasma darah ikan nila yang dipuasakan dan diberi pakan kembali
Pada saat ikan dipuasakan selama 4 hari terjadi peningkatan nilai osmolalitas plasma yang menunjukkan adanya respon fisiologi ikan dalam mengatur konsentrasi osmotik tubuhnya, kemudian mengalami penurunan pada saat ikan dipuasakan selama 8 hari (Gambar 2). Yang menarik dalam penelitian ini adalah pada saat ikan diberi pakan kembali setelah dipuasakan selama 8 hari terjadi penurunan nilai osmolalitas plasma hampir 50%. Diduga hal ini terjadi karena periode pemuasaan yang terlalu lama (8 hari) mempengaruhi konsentrasi osmotik plasma ikan, sehingga pemberian pakan kembali
selama 8 hari berikutnya belum mapu memperbaiki konsentrasi osmotik tubuh ikan.
Perubahan nilai osmolalitas plasma pada ikan dipengaruhi oleh beberapa faktor, antara lain : suhu, salinitas dan status nutrisi. Pada saat ikan dipuasakan maka status nutrisi ikan mengalami penurunan yang selanjutnya berpengaruh terhadap konsentrasi osmotik tubuhnya yang tercermin dalam nilai osmolalitas plasma. 0 20 40 60 80 100 120 140
kontrol puasa ke4 puasa ke8 refeed ke4 ref eed ke8
Perlakuan K a d a r g lu k o s a ( m g /d l)
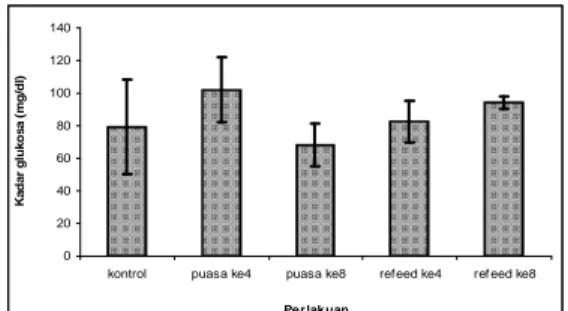
Gambar 3. Nilai rata-rata glukosa darah ikan nila yang dipuasakan dan diberi pakan kembali.
Fenomena yang sama juga diamati pada kadar glukosa darah ikan Nila yang diberi perlakuan puasa dan pemberian pakan kembali menunjukkan hasil yang berbeda nyata antar perlakuan (P <0.05).
Kadar terendah dijumpai pada perlakuan puasa selama 8 hari yaitu sebesar 68 mg/dl, kemudian mengalami peningkatan berturut-turut pada perlakuan kontrol sebesar 79,07 mg/dl, pemberian pakan kembali selama 4 hari sebesar 82.63 mg/dl, pemberian pakan kembali selama 8
hari sebesar 94,29 mg/dl dan tertinggi dijumpai pada perlakuan puasa selama 4 hari yaitu sebesar 102.1 mg/dl (gambar 3.)
Kadar glukosa mencerminkan ketersediaan energi pada ikan. Perlakuan pemuasaan selama 8 hari berturut-turut menurunkan kadar glukosa darah ikan karena selama puasa ikan akan menggunakan cadangan glikogen untuk menyediakan energi. Sehingga kondisi tersebut akan mengakibatkan kadar glukosa darah menurun.
Hasil penelitian ini menunjukkan bahwa ikan yang dipuasakan selama 4 hari terjadi peningkatan kadar glukosa darah, kemudian menurun pada pemuasaan selama 8 hari. Penurunan ini terjadi karena ikan berusaha memobilisasi glukosa dari cadangan glikogen. Fenomena yang sama juga terjadi pada channel catfish, Ictalurus punctatus (Rafinesque), glukosa darah dan glikogen hati lebih rendah pada ikan yang tidak diberi pakan pada minggu ke 2 dan 4. Jadi dapat disimpulkan bahwa pemuasaan menyebabkan penurunan glukosa darah ikan [11]. Hasil yang sama juga dijumpai pada ikan sidat, Anguilla anguilla yang dipuasakan selama 47 hari, kadar gkukosa mengalami peningkatan akan tetapi kemudian menurun setelah dipuasakan selama 164 hari [12].
Peningkatan kadar glukosa darah merupakan efek sekunder dari stres yang diperantarai oleh pelepasan kortikosteroid
dan katekolamin. Dalam keadaan stres terjadi peningkatan glukokortikoid yang berakibat pada peningkatan kadar glukosa darah untuk mengatasi kebutuhan energi yang tinggi pada saat stres. [13].
Perubahan metabolisme karbohidrat pada ikan gilthead sea bream, Sparus aurata, yang tercermin sebagai peningkatan kapasitas transport juga teramati bila ikan dipaparkan pada pemuasaan selama dua minggu [14]. Ikan catfish, Rhamdia hilarii (ikan omnivora) yang tidak diberi pakan juga menunjukkan penurunan level kadar gula darah secara progresif hingga 50 % setelah hari ke 30, dibandingkan dengan ikan yang diberi pakan [15].
Dengan demikian dapat dijelaskan bahwa ikan yang diberi pakan kembali setelah dipuasakan dalam waktu tertentu akan mengembalikan kondisi homeostasis tubuhnya dengan meningkatkan kadar glukosa yang mengalami penurunan pada saat dipuasakan.
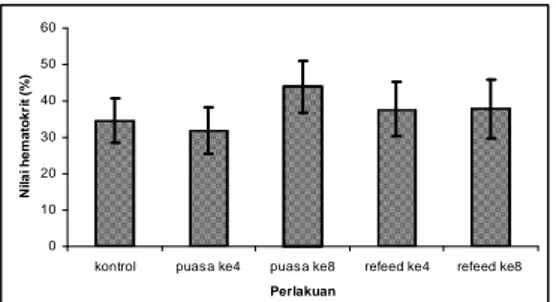
Sejalan dengan kadar glukosa darah ikan Nila, perlakuan pemuasaan dan pemberian pakan kembali mengakibatkan terjadinya perbedaan yang nyata nilai hematokrit antar perlakuan (P<0,05).
0 10 20 30 40 50 60
kontrol puasa ke4 puasa ke8 refeed ke4 refeed ke8
Perlakuan N il a i h e m a to k ri t (% )
Gambar 4. Rata-rata nilai hematokrit ikan Nila yang dipuasakan dan diberi pakan kembali
Kadar terendah dijumpai pada perlakuan puasa selama 4 hari yaitu sebesar 31,87%, kemudian mengalami peningkatan berturut-turut pada perlakuan kontrol sebesar 34,64%, pemberian pakan kembali selama 4 hari sebesar 37,77%, pemberian pakan kembali selama 8 hari sebesar 37,84% dan tertinggi dijumpai pada perlakuan puasa selama 8 hari yaitu sebesar 102.1 mg/dl (gambar 4.)
Fenomena yang sama juga dijumpai pada ikan sidat yang dipuasakan selama 47 hari , kadar hematokrit mengalami peningkatan [9], sedangkan penelitian terhadap ikan traira, Hoplias malabaricus yang dipuasakan selama 240 hari kemudian diberi pakan kembali selama 30 hari mengalami penurunan [6]..
Periode pemuasaan yang panjang akan mempengaruhi status nutrisi ikan yang selanjutnya berpengaruh terhadap nilai hematokrit ikan. Pada saat ikan dipuasakan terjedi penurunan jumlah sel darah merah, yang berpengaruh terhadap nilai heamtokrit. Dengan demikian pada saat ikan diberi pakan kembali, ikan
mengalami fase pemulihan yang tercermin dari peningkatan nilai hematokrit
Dari hasil penelitian dapat disimpulkan bahwa ikan Nila yang dipuasakan dan diberi pakan kembali akan mengalami perubahan profil darah yang meliputi, kadar glukosa darah, nilai osmolalitas plasma dan hematokrit sebagi respon fisiologi ikan dalam menjaga kondisi homeostasis tubuhnya.
DAFTAR PUSTAKA
Jenkins, J.A. 2003. Palid Sturgeon in The Lower Missisipi Region : Hematology and Genome Information. USGS Open File Report 03-406, 32 p.
Torres, P., L. Tort. J. Planas and R. Flos. 1986.
Effects of Confinement Stress and Additional Zinc Treatment on Some Blood Parameters in The Dogfish Scyliorhinus canicula. Comp. Biochem. Physiol. 83 C.
1 : 89 – 92.
Swift, D.J. 1983. Blood Componenet Value
Changes in The Atlantic Mackerel
(Scomber scombrus L.) Subejected to Capture, Handling and Confinement.
Comp Biochem. Physiol. 76A : 795 – 802
Clift, G. and G.D. Thurman. 1984. Pathological
and Physiological effects of Stress During Capture and Transport in The Juvenile dusky shark, Carcharhinus obscurus.
Comp. Biochem. Physiol. 78A : 167 –
173.
Black, E.C. (1958). Hyperactivity as a lethal factor
in fish. J. Fish. Res. Bd. Can. 15 : 573 –
586.
Riosa, F.S., Oba, E.T., Fernandes, M.N., Kalinin, A.L. and F.T. Rantin, 2005. Erythrocyte Senescence and Haematological Changes Induced by Starvation in the Neotropical
Fish Traira, Hoplias malabaricus
(characiformes, Erythrinidae).
Comparative Biochemistry and
Physiology, Part A. 140 : 181 -187
Simanjuntak, S.B.I. & Yuwono, E., 2006, Pengaruh restriksi pakan terhadap hematologi dan
histologi hati ikan kerapu bebek,
Cromileptes altivelis. Ichtyos, Jurnal
Penelitian Ilmu-ilmu Perikanan dan Kelautan, 5, 1: 33-36.
Kang, J.C., S.G Kim and S.W. Jang. 2005. Growth and Hematological Changes of Rockfish,
Sebastes schegeli (Hilgendorf) Exposed to
dietary Cu and Cd. Jornal of the World Aquaculture Society 36 (2) : 188 -195 Sjobeck, M.L.J., G. Dave., A.Larsson., K. Leander
and U.Lidman. 1975. Metabolic and Hematological effects of Starvation in The European eel, Anguilla anguilla L ---II. Hematology. Comparative Biochemistry and Physiology Part A : Physiology 52(3) : 431 - 434
Fatmawati, W.2010. Laju Metabolisme dan Profil
Darah Ikan Lele Dumbo, Clarias
gariepinus, yang Diinduksi dengan Pemuasaan secara Periodik. Skripsi (tidak dipublikasikan). Fakultas Biologi Unsoed, Purwokerto.
Shoemaker, C.A., Klesius, P.H., L im, C., and M. Yildirim, 2003. Feed Deprivation of Channel Catfish, Ictalurus punctatus (Rafineque), Influences Organosomatic
Indices, Chemical Composition and
Susceptibility to Flavobacterium
columnare. J.Fish Dis. 26 (9) : 553 – 561
Dave, G., M.L J. Sjobeck., A. Larsson., K. Leander and U.Lidman. 1975. Metabolic and Hematological effects of Starvation in The European eel, Anguilla anguilla L ---I. Carbohydrate, Lipid,Protein and Inorganik
ion Metabolism. Comparative
Biochemistry and Physiology Part A : Physiology 52(3) : 423 430.
Li, P., B. Ray and D.M. 2009. Gatlin. Effect of Handling and Transport On Cortisol Response And Nutrient Mobilization Of Golden Shiner, Notemigonus crysoleucas.
Journal of the World Aquaculture Society 40 (6) : 803 -809.
Sangiao-Alvarellos, S., J.M. Guzman, R. Laiz-Carrion, J.M. Miguez, M.P. Martin del Rio, J.M. Mancera and J.L. Soengas, 2005. Interactive Effects of high Stocking
Density anf Food deprivation on
Carbohydrate Metabolism in several
Tissue of Gilthead Sea Bream, Sparus aurata. J. Exp. Biol. 303 (A) : 761 – 775 Machado, C.R., Garafalo, M.A., Roselino, J.E.,
Kettelhut, I.C. and R.H. Migliorini, 1988. Effects of Starvation, Refeeding and
Insulin on Energy-linked Metabolic
Processes in Catfish (Rhamdia hilarii)
Adapted to a Carbohydrate-rich Diet. Gen.
Comp. Endocrinol. 71 (3) : 429 – 437
. .