Beberapa Senyawa Fenol dari Tumbuhan Morus macroura Miq.
Nunuk H. Soekamto1), Sjamsul A. Achmad1), Emilio L. Ghisalberti2), Norio Aimi3), Euis H. Hakim1), dan Yana M. Syah1)
1)
Departemen Kimia, Institut Teknologi Bandung, Jalan Ganesa 10, Bandung 40132, Indonesia
2)
Department of Chemistry, University of Western Australia, Nedlands, Western Australia 6907
3)
Faculty of Pharmaceutical Sciences, Chiba University, 1-33, Yoyio-cho, Inage-ku, Chiba 263-8522, Japan
Diterima Oktober 2002, disetujui untuk dipublikasikan Januari 2003
Abstrak
Tiga senyawa turunan stilben, yaitu lunularin (1), oksiresveratrol (2), dan andalasin A (3), bersama-sama dengan turunan 2-arilbenzofuran, morasin M (4), turunan kumarin, umbeliferon (5), dan β-resolsilaldehid (6), telah diisolasi dari Morus macroura Miq. (Moraceae), suatu tumbuhan langka yang berasal dari Sumatera Barat dan endemik Indonesia. Struktur molekul senyawa-senyawa tersebut telah ditetapkan berdasarkan data fisika dan spektroskopi.
Kata kunci: Andalasin A, lunularin, Morus macroura Miq, morasin M, oksiresveratrol, β-resolsilaldehid, dan umbeliferon.
Abstract
Three stilbene derivatives, namely lunularin (1), oxyresveratrol (2), and andalasin A (3), together with 2-arylbenzofuran derivative, moracin M (4), coumarin derivative, umbelliferon (5), and β-resolcylaldehyde, were isolated from Morus macroura Miq. (Moraceae), a rare spesies found in West Sumatera and endemic to Indonesia. The structures of all these compounds were elucidated based on physical and spectroscopic data.
Keywords: Andalasin A, lunularin, Morus macroura Miq, moracin M, oxyresveratrol, β-resolcylaldehyde, dan umbelliferon.
1. Pendahuluan
Morus merupakan salah satu marga dalam suku
Moraceae. Beberapa jenis tumbuhan Morus, seperti M.
alba, M. bombycis, M. lhou, dan M. multicaulis, telah
lama digunakan sebagai obat tradisional Cina, misalnya batuk, asma, hipertensi, influenza dan rematik1). Disamping itu, beberapa spesies Morus atau
murbei mempunyai nilai ekonomi yang tinggi, karena daunnya adalah makanan ulat sutera, sedangkan buahnya dapat dimakan, dan kayunya digunakan sebgai bahan bangunan2).
Di Indonesia, hanya terdapat dua spesies
Morus, yaitu M. alba dan M. macroura, yang
terakhir merupakan spesies yang langka dan endemik untuk Indonesia, dan terutama terdapat di daerah Sumatera Barat dan dikenal dengan nama daerah “Andalas” atau Kertey3). Beberapa jenis senyawa
fenol telah ditemukan pada tumbuhan M .macroura, seperti morasin B, morasin P, mulberosida C, dan mulberofuran4,5). Pada kesempatan ini akan diuraikan
hasil penelitian terhadap spesies yang berhubungan dengan penemuan senyawa-senyawa turunan stilben, yaitu lunularin (1), oksiresveratrol (2), dan andalasin A (3), bersama-sama dengan turunan 2-arilbenzofuran, morasin M (4), turunan kumarin, umbeliferon (5), dan β-resolsilaldehid (6). Struktur senyawa-senyawa tersebut di atas telah ditetapkan berdasarkan data
spektroskopi UV, IR, MS, dan NMR, termasuk NMR satu dan dua dimensi seperti, spin decoupling, DEPT, HMQC, dan HMBC.
2. Percobaan 2.1 Umum
Penentuan titik leleh senyawa–senyawa hasil penelitian ini dilakukan menggunakan alat penetapan titik leleh mikro. Spektrum UV dan IR diukur masing-masing dengan spektrofotometer Varian Cary 100 conc dan ONE Perkin Elmer. Spektrum 1H dan 13C NMR diukur menggunakan Bruker AM 500, yang
bekerja pada 500 MHz (1H NMR) dan 125 MHz
(13C NMR) menggunakan puncak pelarut terdeuterasi.
Spektrum massa FABMS diperoleh menggunakan spektrometer massa JEOL JMS-AM20. Kromatografi cair vakum (KCV) dilakukan dengan menggunakan Si gel Merck 60 GF254, kromatografi radial dengan
menggunakan Si gel Merck 60 GF254 dan analisis
kromatografi lapis tipis (KLT) pada pelat berlapis Si gel Merck Kieselgel 60 F254, 0,25 mm.
2.2 Pengumpulan Bahan Tumbuhan
Bahan tumbuhan berupa kayu batang dan kayu akar Morus macroura dikumpulkan pada bulan Mei 1997 dari Desa Paninjauan, Kecamatan Sepuluh Koto, Kabupaten Tanah Datar, Sumatera Barat. Bahan tumbuhan ini diidentifikasi oleh Herbarium Jurusan 35
Biologi Universitas Andalas, dan dikonfirmasikan oleh Herbarium Bogoriense, Pusat Penelitian dan Pengembangan Biologi, LIPI, Bogor, dan spesimennya tersimpan di kedua herbarium tersebut.
2.3 Ekstraksi dan Isolasi
Serbuk kayu batang Morus macroura (8,2 kg) dimaserasi dengan metanol. Setelah pelarut diuapkan pada tekanan rendah, diperoleh ekstrak metanol berupa residu berwarna coklat. Ekstrak metanol ini dilarutkan kembali dalam aseton, dan fraksi yang larut dalam aseton (108,7 g) difraksinasi empat kali berturut-turut menggunakan kromatografi cair vakum (KCV) dengan heksan, heksan-etil asetat, etil asetat, dan metanol dengan kepolaran yang terus ditingkatkan. Penggabungan fraksi-fraksi yang diperoleh yang dipantau dengan KLT, menghasilkan empat fraksi utama. Fraksi utama kedua (13,1 g) difraksinasi lebih lanjut dengan campuran CHCl3-MeOH dengan kepolaran yang terus
ditingkatkan, menghasilkan enam fraksi gabungan. Fraksi gabungan kedua (2,0 g) difraksinasi kembali menghasilkan sejumlah fraksi yang digabung pula menjadi lima fraksi utama. Campuran fraksi pertama dan kedua, setelah mengalami fraksinasi berulang kali, menghasilkan endapan kuning yang pada kristalisasi dari n-heksan-etil asetat menghasilkan umbeliferon (5) (10,8 mg) berupa kristal kuning, dengan titik leleh 182-183o C, yang homogen pada KLT menggunakan
tiga sistem eluen yang berbeda. Selanjutnya fraksi gabungan ketiga (2,1 g) dari hasil fraksinasi fraksi utama kedua (13,1 g) difraksinasi lebih lanjut menggunakan kromatografi kolom cair vakum (KCV) dengan campuran eluen 30-40 % EtOAc dalam n-heksana, menghasilkan lima fraksi utama. Fraksi utama keempat (1,7 g) difraksinasi kembali menggunakan cara KCV dengan eluen 30-50 % EtOAc dalam n-heksan, menghasilkan sejumlah fraksi yang digabung pula menjadi lima fraksi utama. Fraksi utama ketiga (1,0 g) difraksinasi menggunakan kromatografi radial dengan eluen 5-10 % MeOH dalam CHCl3, menghasilkan lima fraksi gabungan.
Selanjutnya fraksi gabungan ketiga, setelah mengalami fraksinasi berulang kali, menghasilkan endapan putih yang pada kristalisasi dari MeOH-CHCl3, menghasilkan morasin M (4) (15,0 mg) berupa
kristal putih, yang homogen pada KLT menggunakan tiga sistem eluen yang berbeda, dengan titik leleh 245-247o C.
Fraksi utama ketiga (29 g), difraksinasi menggunakan KCV dengan eluen 15-70 % aseton dalam benzena, menghasilkan lima fraksi gabungan. Fraksi gabungan keempat (17,4 g), difraksinasi kembali menggunakan KVC dengan eluen aseton-benzena (5-50 %), menjadi lima fraksi utama. Selanjutnya fraksi utama ketiga (7,11 g), difraksinasi sebanyak 1,0 g menggunakan kromatografi radial dengan eluen 10-20 % MeOH dalam CHCl3,
menghasilkan sejumlah fraksi yang digabung menjadi lima fraksi gabungan. Dari fraksi gabungan kedua
diperoleh endapan berwarna kuning yang setelah dikristalisasi menggunakan pelarut MeOH/CHCl3,
menghasilkan oksiresveratrol (2) yang berupa kristal kuning (388 mg), dengan titik leleh 95-96o C, yang
homogen pada KLT menggunakan tiga sistem eluen yang berbeda.
Serbuk kayu akar Morus macroura (7,9 kg) dimaserasi dengan metanol. Hasil maserasi diuapkan pada tekanan rendah, menghasilkan ekstrak metanol berupa residu berwarna coklat sebanyak 462,5 g. Ekstrak metanol ini dipartisi ke dalam pelarut n-heksana, CH2Cl2, dan EtOAc, sehingga diperoleh
fraksi n-heksan 11,4 g, fraksi CH2Cl2 35 g, dan fraksi
EtOAc 207,7 g. Fraksi yang terlarut dalam CH2Cl2 (35
g) difraksinasi menggunakan (KCV) dengan n-heksan, n-heksan-etil asetat, etil asetat, dan metanol dengan kepolaran yang terus ditingkatkan, menghasilkan delapan fraksi utama. Fraksi utama ketiga (13,1 g), difraksinasi lebih lanjut menggunakan KCV dengan pelarut (n-heksan-CH2Cl2, CH2Cl2, CH2Cl2-aseton),
menghasilkan sepuluh fraksi gabungan. Fraksi gabungan kelima (353 mg) difraksinasi kembali menggunakan kromatografi radial dengan n-heksan-EtOAc menghasilkan lima fraksi utama. Fraksi utama ketiga melalui kristalisasi dengan EtOAc-n-heksan menghasilkan senyawa β-resolsilaldehid (6), yang berupa kristal transparan berbentuk jarum dengan titik leleh 134-135o C.
Fraksi yang terlarut dalam CH2Cl2 (35 g)
difraksinasi, dan fraksi utama keempat (4 g) difraksinasi lebih lanjut menggunakan KCV dengan eluen CH2Cl2, CH2Cl2-aseton yang ditingkatkan
kepolarannya, menghasilkan lima fraksi utama. Fraksi utama ketiga (1,6 g) difraksinasi kembali menggunakan KCV dengan eluen n-heksan-CHCl3,
CHCl3, MeOH- CHCl3, menghasilkan delapan fraksi
gabungan. Fraksi gabungan ketujuh (1,0 g) difraksinasi menggunakan kromatografi radial dengan eluen 60-80 % CH2Cl2 dalam n-heksan, menghasilkan
lima fraksi utama. Selanjutnya fraksi utama keempat, setelah mengalami fraksinasi berulang kali menggunakan kromatografi radial, menghasilkan endapan putih yang pada kristalisasi dari CH2Cl2
-n-heksan menghasilkan lunularin (1) (135 mg) berupa kristal putih mengkilap, yang homogen pada KLT menggunakan tiga sistem eluen yang berbeda, dengan titik leleh 105-106o C.
Sejumlah 42,8 g fraksi EtOAc (207,7 g), difraksinasi menggunakan KCV dengan eluen 50-80 % etil asetat dalam n-heksan, menjadi tiga fraksi utama. Fraksi utama ketiga (18,2 g) dari jumlah keseluruhan (24,2 g), dipartisi menggunakan pelarut benzen-n-heksan-MeOH, menghasilkan fraksi yang terlarut dalam benzen + n-heksan (810 mg) dan fraksi yang terlarut dalam MeOH (14 g). Fraksi yang terlarut dalam MeOH (14 g) ini, difraksinasi menggunakan KCV dengan eluen 60-75 % EtOAc dalam heksan, menghasilkan empat fraksi utama. Fraksi utama kedua (2,5 g), difraksinasi lebih lanjut menggunakan 12,5-20 % MeOH dalam CH2Cl2 : n-heksan (1 : 1), dan setelah
dilakukan KLT terhadap fraksi-fraksi yang diperoleh empat fraksi gabungan. Fraksi gabungan keempat (260 mg), difraksinasi kembali menggunakan kromatografi radial dengan eluen MeOH : diisopropil eter : n-heksan (15 : 55 : 30), menghasilkan empat fraksi utama. Selanjutnya fraksi utama ketiga (90 mg), difraksinasi menggunakan kromatografi radial dengan MeOH : diisopropil eter : n-heksan (17,5 : 52,5 : 30), menghasilkan tiga fraksi gabungan, dan dari fraksi gabungan pertama diperoleh senyawa andalasin A (3) (22 mg) yang berupa serbuk yang berwarna coklat, dengan titik leleh 179-181o C.
3. Data Hasil Percobaan
Lunularin (1): Diperoleh sebagai kristal
berwarna putih mengkilap, t.l. 105-106o C; UV
(MeOH) λmax (log ε): 276 (2,94), 223 (3,43) nm;
(MeOH + NaOH) λmax (log ε): 281 (3,15), 205 (4,57)
nm; IR (KBr) υmax: 3307 (OH), 2920, 2847 (C-H alifatik), 1609, 1594, 1513, 1455 (C=C aromatik) cm -1; 1H NMR (aseton-d6, 500,0 MHz) δ: 7,08 (1H, t, H-5), 7,06 (2H, d, J = 6,4 Hz, H-2’, 6’), 6,70 (1H, dd, J = 1,7 dan 4,0 Hz, H-6), 6,68 ( 1H, m, H-2), 6,74 (2H, d, J = 8,6 Hz, H-3’, 5’), 6,64 (1H, ddd, J = 8,1; 2,5; & 1,1 Hz, H-4), 2,78 (4H, s, H-7, 8); 13C NMR (aseton-d6, 125,0 MHz) δ: 158,2 (C-3), 156,4 (C-4’), 144,5 1); 133,5 1’), 130,2 2’,6’), 130,0 (C-5), 120,5 (C-2), 116,2 (C-6), 115,9 (C-3’,5’), 113,6 (C-4), 38,9 (C-8), 37,7 (C-7).
Oksiresveratrol (2): Diperoleh sebagai kristal
berwarna kuning, t.l. 95-960 C; UV(MeOH): λ
max (log
ε) 327 (3,90), 301 (3,80), 239 (sh), 218 (3,93) nm; (MeOH + NaOH): (log ε) 346 (4,02), 301 (3,91), 239 (sh) nm; IR (KBr) υmax 3200 (OH), 1613, 1591, 1518, 1480, 1456 (C=C aromatik) cm-1; 1H NMR (aseton-d6, 500,0 MHz) δ: 7,40 (1H, d, J = 8,5 Hz, H-6), 7,33 (1H, d, J = 16,5 Hz, 7), 6,88 (1H, d, J = 16,5 Hz, H-8), 6,51 (2H, d, J = 2,3 Hz, H-2’ & H-6’) 6,42 (1H, d, J = 2,4 Hz, H-3), 6,37 (1H, dd, J = 2,4 Hz & J = 8,5 Hz, H-5), 6,22 (1H, t, J = 2,2 Hz, H-4’); 13C NMR (CD3OD, 125,76 MHz) δ: 159,5 (C-3’ & C-5’), 159,1 (C-4), 156,9 (C-2), 141,6 (C-1’), 128,2 (C-8), 126,2 (C-7), 124,3 (C-6), 117,2 (C-1), 108,4 (C-5), 105,4 (C-2’ & C-6’), 103,6 (C-4’), 102.2 (C-3).
Andalasin A (3): Diperoleh sebagai serbuk
berwarna coklat, t.l. 179-181o C; UV (MeOH) λ max
(log ε): 328 (4,69), 301 (4,57), 219 (4,68) nm; (MeOH + NaOH) λmax (log ε): 352 (4,66), 347 (4,69), 310
(4,50), 240 (4,57), 205 (5,06) nm, IR (KBr) υmax: 3391
(OH), 1592, 1520, 1456 (C=C aromatik) cm-1; 1
H-NMR (aseton-d6, 500,0 MHz) δ: 7,48 (1H, d, J = 8,2 Hz, H-6b), 7,35 (1H, d; J = 8,3 Hz, H-6a), 7,23 (1H, d, J = 16,4 Hz, 7a), 6,77 (1H, d; J = 16,4 Hz, H-8a), 6,53 (2H, brs, H-10a, 14a), 6,40 (1H, d; J = 2,3 Hz, H-3a), 6,35 (1H, dd, J = 8,3 & 2,3 Hz, H-5a), 6,29 (1H, dd; J = 8,2 & 2,5 Hz, H-5b), 6,28 (1H, d, J = 2,5 Hz, H-3b), 6,26 (2H, d, J = 2,2 Hz, H-10b, 14b), 6,07 (1H, dd, J = 2,2 & 2,2 Hz, H-12b), 4,86 (1H, dd, J = 8,5 & 6,8 Hz, H-7b), 3,67 (1H, dd; J = 13,7 & 8,5 Hz, H-8b), 3,38 (1H, dd; J = 13,7 & 6,8 Hz, H-8b); 13 C-NMR (aseton-d6, 125,0 MHz) δ: 158,9 (C-4a), 158,8 (C-11b, 14b), 157,1 (C-2b), 156,7 (C-2a, 11a, 13a), 156,1 4b), 145,2 9b), 138,5 9a), 130,7 (C-6b), 128,0 (C-6a), 125,6 (C-8a), 123,7 (C-7a), 121,8 (C-1b), 117,1 (C-1a), 116,9 (C-12a), 108,3 (C-5a), 108,2 (C-10b, 14b), 107,3 (C-5b), 106,4 (C-10a, 14a), 103,4 3a), 103,3 3b), 100,9 12b), 38,2 (C-8b), 36,4 (C-7b).
Morasin M (4): Ditemukan berupa kristal
berwarna putih, t.l. 245-2470 C; UV (MeOH): λ max (log ε) 328 (sh), 315 (4,55), 217 (4,51) nm, (MeOH + NaOH) 347 (sh), 333 (4,67) cm-1; IR (KBr) υ max: 3271 (OH), 1617, 1578, 1508, 1485, 1439 (C=C aromatik) cm-1; 1H NMR (aseton-d6, 500,0 MHz) δ: 7,34 (1H, d. J = 8,4 Hz, H-4), 6,90 (1H, d, J = 2,1 Hz, H-7), 6,89 (1H, m, H-3), 6,75 (2H, d, J = 2.2 Hz, H-2’ & 6’), 6,72 (1H, dd, J = 2,1 Hz & J = 8,4 Hz, H-5), 6,23 (1H, t, J = 2,2 Hz, H-4’); 13C NMR (CD 3OD, 125,76 MHz) δ: 160,0 (C-3’ & C-5’), 157,3 (C-7a), 156,9 (C-6), 156,1 (C-2), 133,8 (C-1’), 123,0 (C-3a), 122,0 (C-4), 113,2 (C-5), 103,9 (C-2’ & C-6’), 103,5 (C-4’), 102,2 (C-7), 98,5 (C-3).
Umbeliferon (5): Diperoleh sebagai kristal
berwarna kuning, t.l. 182-183o C; UV (MeOH): λ max
(log ε) 324 (4,16), 215 (4,09) nm, (MeOH + NaOH) (log ε) 368 (4,27), 230 (3,99) nm; IR (KBr) υmax: 3432
(OH), 1681 (C=O keton), 1604, 1566, 1454 (C=C aromatik) cm-1; 1H NMR (DMSO-d6, 500,0 MHz) δ: 7,92 (1H, d, J = 9.5 Hz, H-4), 7,51 (1H, d, J = 8,5 Hz, H-5), 6,77 (1H, dd, J = 2,2 Hz & J = 8,5 Hz, H-6), 6,70 (1H, d, J = 2,2 Hz, H-8), 6,19 (1H, d, J = 9,5 Hz, H-3; 13C NMR (DMSO-d 6, 125,65 MHz) δ: 161,2 7), 160,4 2); 155,4 8a), 144,5 4), 129,7 5), 113,1 6), 111,43 3), 111,2 4a), 102,1 (C-8); FABMS m/z: [MH]+ 163 (30), 154 (100), 135 (31), 136 (65), 137 (67), 107 (16), 77 (13).
β-Resolsilaldehid (6): Diperoleh sebagai kristal transparan berbentuk jarum, t.l. 134-135o C;
UV (MeOH) λmax (log ε) 321 (3,69), 279 (3,85), 231
(3,66), 212 (3,92) nm; (MeOH + NaOH) 331 (3,14), 249 (2,72), 206 (3,38) nm; IR (KBr) υmax: 3125 (OH), 1633 (C=O), 1615, 1581, 1497, 1444 (C=C aromatik) cm-1; 1H NMR (aseton-d6, 500,0 MHz) δ: 9,75 (1H, d, J = 0,6 Hz, H-formil), 7,59 (1H, d, J = 8,5 Hz, H-6), 6,54 (1H, dd, J = 2,0 Hz & J = 8,5 Hz, H-5), 6,34 (1H, d, J = 2,0 Hz, H-3; 13C NMR; (aseton-d6, 125,0 MHz) δ: 195,7 (C-formil), 166,3 (C-4); 165,2 (C-2), 137,1 (C-6), 115,8 (C-1), 109,6 (C-5), 103,1 (C-3). 4. Pembahasan
Pada ekstrak aseton kayu batang M. macroura telah ditemukan senyawa turunan stilben, oksiresveratrol (2), turunan 2-arilbenzofuran, morasin M (4), dan turunan kumarin, umbeliferon (5). Sedangkan dari ekstrak CH2Cl2 kayu akar M. macroura telah diisolasi senyawa turunan stilben,
lunularin (1) dan β-resolsilaldehid (6), dan pada ekstrak EtOAc telah berhasil diisolasi senyawa dimer
stilben, andalasin A (3). Keenam senyawa ini diperoleh melalui beberapa tahap fraksinasi, diikuti dengan pemilihan fraksi utama berdasarkan analisis kromatografi lapis tipis (KLT) dan kromatografi partisi.
Andalasin A (3), C28H24O8 diperoleh sebagai
serbuk berwarna coklat dengan t.l. 179-181o C.
Spektrum IR (2) menunjukkan pita serapan untuk gugus hidroksil (3391 cm-1) dan cincin aromatik
(1615, 1592, 1520, 1456 cm-1), sedangkan spektrum
UV menyatakan serapan pada λmax 328 nm (log ε
4,69), 301 (4,57), 219 (4,68) nm. Data ini menunjukkan bahwa senyawa (3) merupakan senyawa turunan stilben. Spektrum 1H NMR menunjukkan
adanya sederet sinyal dari tiga proton pada δ 7,35 (1H, d, J = 8,3 Hz) untuk H-6a, δ 6,40 (1H, d, J = 2,3 Hz) untuk H-3a, dan δ 6,35 (1H, dd, J = 8,3 & 2,3 Hz) untuk H-5a, yang merupakan proton-proton aromatik dari sistem ABX pada cincin A, begitu pula tiga proton aromatik pada δ 7,48 (1H, d, J = 8,2 Hz) untuk H-6b, pada δ 6,29 (1H, dd; J = 8,2 & 2,5 Hz) untuk H-5b, dan pada δ 6,28 (1H, d, J = 2,5 Hz) untuk H-3b, yang merupakan proton aromatik sistem ABX pada cincin C. Adanya sinyal pada δ 6,26 (2H, d, J = 2,2 Hz) untuk dua proton ekivalen H-10b dan H-14b dan pada δ 6,07 (1H, dd, J = 2,2 & 2,2 Hz) untuk
H-12b, menunjukkan adanya satu unit fenil disubstitusi-3,5 pada cincin D, dan adanya satu sinyal pada δ 6,53 (2H, brs) untuk H-10a dan H-14a, menunjukkan adanya cincin fenil trisubstitusi-3,4,5 pada cincin B. Adanya trans 1,2-disubstitusi vinil ditunjukkan oleh sinyal pada δ 7,23 dan 6,77 (masing-masing 1H, d, J
= 16,4 Hz) untuk H-7a dan H-8a, sedangkan sinyal
pada δ 4,86 (1H, dd, J = 8,5 & 6,8 Hz) untuk H-7b, 3,67 (1H, dd; J = 13,7 & 8,5 Hz),dan 3,38 (1H, dd; J
= 13,7 & 6,8 Hz) yang keduanya untuk H-8b,
menunjukkan bahwa terdapat unit 2,2 disubstitusi etana. Spektrum 13C NMR menunjukkan adanya dua
puluh delapan atom karbon, termasuk delapan oksiaril. Dari data tersebut di atas, dapat disimpulkan bahwa senyawa (3) merupakan dimer dari oksiresveratrol yang sesuai dengan andalasin A yang telah dilaporkan sebelumnya.6 (Tabel 1). Dengan cara yang sama, dari
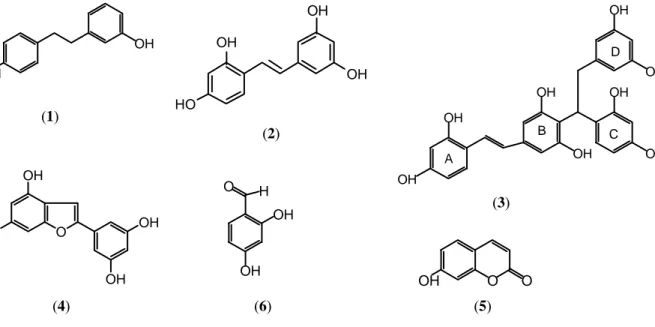
data yang ada, disimpulkan bahwa senyawa (1), (2), (4), (5) dan (6), masing-masing adalah lunularin (1), oksiresveratrol (2), morasin M ( 4), umbeliferon (5), dan β-resolsilaldehid (6). seperti tercantum pada Gambar 1. Memperhatikan struktur senyawa-senyawa tersebut yang telah ditemukan pada satu spesies M.
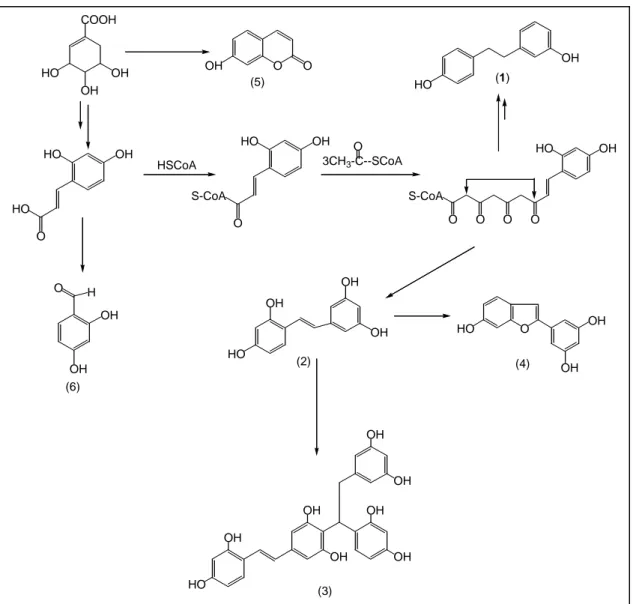
macroura, dapat disarankan hubungan biogenesis
senyawa-senyawa tersebut (Gambar 2).
(1) (2) (3) (4) (6) (5)
Gambar 1. Struktur senyawa-senyawa hasil isolasi.
OH OH O OH OH HO OH O O OH O H OH OH OH OH OH OH OH OH OH A B C D OH O H OH OH OH
Tabel 1. Data 13C NMR senyawa (3) dan andalasin A6).
Posisi
Karbon multiplisitas, J dlm HzδH senyawa (3)
δH (andalasin A) multiplisitas, J dlm Hz δc(seny. (3)) δc(Andalasin A) 1 - - 117,1 117,3 2 - - 156,7 156,6 3 6,40 (d; 2,3) 6,42 (d; 2,4) 103,4 103,5 4 - - 158,9 159,0 5 6,35 (dd; 8,3 & 2,3) 6,36 (dd; 8,4 & 1,9) 108,3 108,2 6 7,35 (d; 8,3) 7,36 (d; 8,5) 128,0 128,1 7 7,23 (d; 16,4) 7,24 (d;16,5) 123,7 123,9 8 6,77 (d; 16,4) 6,78 (d; 16,4) 125,6 125,8 9 - - 138,5 138,6 10 6,53 (brs) 6,54 (s) 106,4 106,6 11 - - 156,7 156,8 12 - - 116,9 117,0 13 - - 156,7 156,8 14 6,53 (brs) 6,54 (s) 106,4 106,6 1’ - - 121,8 122,0 2’ - - 157,1 157,2 3’ 6,28 (d; 2,5) 6,27 (d; 2,2) 103,3 103,4 4’ - - 156,1 156,2 5’ 6,29 (dd; 8,2 & 2,5) 6,31 (dd; 8,8 & 2,5) 107,3 107,5 6’ 7,48 (d; 8,2) 7,49 (d; 8,2) 130,7 130,8 7’ 4,86 (dd; 8,5 & 6,8) 4,86 (dd; 8,3 & 7,1) 36,4 36,5 8’ 3,67 (dd; 13,7 & 8,5) 3,38 (dd; 13,7 & 6,8) 3,67 (dd; 13,7 & 8,5) 3,39 (dd; 13,7 & 6,8) 38,2 38,3 - 9’ - - 145,2 145,3 10’ 6,26 (d; 2,2) 6,26 (d; 2,2) 108,2 108,3 11’ - - 158,8 158,9 12’ 6,07 (dd; 2,2 & 2,2) 6,08 (dd; 2,2 & 3,3) 100,9 101,0 13’ - - 158,8 158,9 14’ 6,26 (d;2,2) 6,26 (d; 2,2) 108,2 108,3 5. Kesimpulan
Pada penelitian terhadap tumbuhan M.
macroura ini, telah ditemukan tiga senyawa turunan
stilben, yaitu lunularin (1), oksiresveratrol (2), dan andalasin A (3), bersama-sama dengan satu turunan 2-arilbenzofuran, morasin M (4), satu turunan kumarin, umbeliferon (5), dan β-resolsilaldehid (6). Senyawa (1), (2), (4), (5), dan (6), ditemukan dari kayu batang, sedangkan senyawa (3) ditemukan dari kayu akar M.
macroura.
6. Ucapan Terima Kasih
Terima kasih disampaikan kepada Ditjen Pendidikan Tinggi, Depdiknas atas beasiswa BPPS, UNESCO program Basic Science yang memberikan dana penelitian di University of Western Australia, dan Herbarium Bogoriense, Pusat Penelitian dan Pengembangan Biologi, LIPI, Bogor yang telah membantu mengidentifikasi spesimen tumbuhan.
COOH HO OH OH HO OH HO O HO OH S-CoA O HSCoA 3CH3-C--SCoA S-CoA O O O O HO OH OH OH OH HO O OH OH HO OH HO O O OH OH HO OH OH OH OH OH OH (1) (2) (5) (4) (3) O H OH OH O (6)
Gambar 2. Saran biogenesis senyawa-senyawa hasil isolasi dari M. macroura.
Daftar Pustaka
1. Kimura, T., “International collation of traditional and folk medicine”, Vol. 1, Part. 1, World Scientific, Singapore, 12, (1996).
2. Venkataraman, K., “Wood Phenolics in the Chemotaxonomy of the Moraceae”,
Phytochemistry, 11, 1571, (1972).
3. Heyne, K, “Tumbuhan Berguna Indonesia II”, Badan Litbang Kehutanan, Jakarta, 659, (1987). 4. Hakim, E.H., Achmad, S.A., Makmur, L.,
Manjang, Y., Juliawati, L.D., Kusuma, S., Supratman, U., & Tamin, R., “Sejumlah Senyawa Fenolik dari Tumbuhan Morus Macroura Miq.
(Moraceae)”, Prosidings Seminar Kimia Bersama
ITB-UKM Kedua, Bandung, 2, 21, (1995).
5. Achmad, S.A., Aimi, N., Ghisalberti, E.L., Hakim, E.H., Jasmansyah, Juliawaty, L.D., Makmur, L., Manjang, Y., Supratman, U., Suyatno, Tamin, R., & Yelminda, A., “Some New Compounds from Indonesian Moraceae”,
Proceedings, International Seminar on Tropical Rainforest Plants, Padang, 25, (2001).
6. Syah, Y.M., Achmad, S.A., Ghisalberti, E.L., Hakim, E.H. Iman, M.Z.N. Makmur, L., & Mujahidin, D. “Andalasin A, a new stilbene dimer from Morus macroura”, Fitoterapia, 71, 630, (2000).