1 BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Hasil Penelitian
Penelitian ini dilakukan di Instalasi Bedah Sentral RSUD Dr. Moewardi Surakarta danpemeriksaanlaboratoriumdilaksanakan di Laboratorium RSUD DR. Moewardi Surakarta yang dimulai padabulan September 2016 sampai Desember 2016. Sample penelitian ini ada 32 pasien yang bersedia diikut sertakan dalam penelitian yaitu pasien yang menjalani pembedahan elektif dengan anestesi umum di Instalasi Bedah Sentral RSUD Dr. Moewardi yang telah memenuhi kriteria inklusif dan eksklusi. Cara mendapatkan sampel yang digunakan dalam penelitian ini yaitu dengan mendatangi pasien di Instalasi Bedah Sentral RSUD Dr. Moewardi Surakarta, setelah itu dilakukan identifikasi identitas (nama, jenis kelamin, umur, nomor rekam medik), berat badan, dan monitoring vital sign (tekanan darah, nadi, suhu badan)
Sebelum tindakan sampel T0 diambil sampel darah vena sebanyak 5 ml untuk memperoleh data dasar dan dimasukkan ke dalam tabung Vacutainer,
dikocok perlahan.
Kemudian pada masing-masing kelompok, subjek diinjeksikan midazolam 0,07 mg/kgBB sebagai premedikasi dan fentanyl 2 µg/kgBB intravena sebagai analgetik fasilitas intubasi. Dilakukan induksi anestesi menggunakan propofol 1,5 mg/kgBB IV dan dilumpuhkan dengan atracurium 0,5 mg/kgBB IV sebelum intubasi. Diambil sampel T1 darah vena sebanyak 5 ml untuk memperoleh data dasar dan dimasukkan ke dalam tabung
Vacutainer, dikocok perlahan.
2 sampel darah kemudian dibawa ke Laboratorium RSUD DR. Moewardi Surakarta untuk diolah.
1. Karateristik Dasar Subyek Peneltian
Berdasarkan hasil penelitian pada 32 pasien yang bersedia diikut sertakan dalam penelitian yaitu pasien yang menjalani pembedahan elektif dengan anestesi umum di Instalasi Bedah Sentral RSUD Dr. Moewardi, didapatkan karakteristik subyek penelitian sebagai berikut.
Tabel 4.1 Karakteristik Subyek Penelitian
Karateristik
Kelompok
p Sevofluran Isofluran
Jenis Kelamin* 0,465
Laki-laki 11 (68,8%) 9 (56,3%)
Perempuan 5 (31,3%) 7 (43,8%)
Umur** 43,88 + 14,56 44,06 + 12,66 0,968
Berat Badan*** 56,44 +5,74 57,19 +8,29 0,558
Tekanan Darah
Sistolik*** 119,13 +25,72 125+22,91 0,316
Diastolik*** 72,56 +22,26 77,69 +24,42 0,985
Denyut Jantung** 101+6,79 103,13 + 5,70 0,345
Suhu (0C)*** 37,88 +0,69 37,62 +0,82 0,385 Laju Nafas*** 20,63 +3,91 21,56 +2,94 0,593
Ket : * Data Kategori (Jumlah, Prosentase) Uji Chi Square
** Data numerikdistribusi normal (Mean + SD ) Uji Independen Sampel T test
*** Data numerikdistribusi tidak normal (Mean + SD ) Uji Mann Whitney
(Sumber : Hasil Olah Data 2016)
Berdasarkan tabel 4.1 diketahui bahwa mayoritas pasien pada
3 berarti bahwa tidak terdapat perbedaan yang signifikan karakteristik responden berdasarkan jenis kelamin antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan jenis kelamin pada kedua kelompok homogen.
Umur pasien kelompok Sevofluran rata-rata 43,88 + 14,56tahun, sedangkan pada kelompok Isofluran rata-rata 44,06 + 12,66 tahun. Nilai p=0,968 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan karakteristik responden berdasarkan usia antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan umur pada kedua kelompok homogen.
Berat badan pasien kelompok Sevofluran rata-rata 56,44 +5,74 kg, sedangkan pada kelompok Isofluran rata-rata 57,19 +8,29 kg. Nilai p=0,558 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan karakteristik responden berdasarkan berat badan antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan berat badan pada kedua kelompok homogen.
Tekanan darah sistolik kelompok Sevofluran rata-rata 119,13 +25,72 , sedangkan pada kelompok Isofluran rata-rata 125+22,91. Nilai p=0,316 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang
signifikan karakteristik responden berdasarkan tekanan darah sistolik antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan tekanan darah sistolik pada kedua kelompok homogen.
4 Denyut jantung pasien kelompok Sevofluran rata-rata 101+6,79, sedangkan pada kelompok Isofluran rata-rata 103,13 + 5,7. Nilai p=0,345 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan karakteristik responden berdasarkan denyut jantung antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan denyut jantung pada kedua kelompok homogen.
Suhu tubuh pasien pada kelompok Sevofluran rata-rata 37,88+0,69 0
C, sedangkan pada kelompok Isofluran rata-rata 37,62+0,82 0C. Nilai p=0,385 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan karakteristik responden berdasarkan suhu tubuh antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan suhu pada kedua kelompok homogen.
Laju nafas pasien kelompok Sevofluran rata-rata 20,63+3,91, sedangkan pada kelompok Isofluran rata-rata 21,56+2,94. Nilai p=0,593 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan karakteristik responden berdasarkan laju nafas antara kelompok Sevofluran dengan kelompok Isofluran, jadi karakteristik responden berdasarkan laju
nafas pada kedua kelompok homogen.
Berdasarkan uraian diatas diketahui bahwa pada karateristik dasar
subyek penelitian mendapatkan nilai p >0,05, hal ini menyatakan bahwa tidak ada perbedaan yang signifikan karakteristik dasar subyek penelitiaan, atau dapat dikatakan sampel pada kelompok yang diberi Sevofluran memiliki karateristik dasar yang tidak berbeda dengan sampel pada kelompok yang diberi Isofluran.
2. Perbedaan Isofluran Dibanding Sevofluran Terhadap Kadar Gula Darah Pasien Yang Menjalani Anestesi Umum.
5 uji normalitas data penelitian tersebut berdistribusi normal (p>0,05), sehingga uji beda dilakukan dengan uji statistik pair sampel t test untuk kelompok berpasangan independent sampel t test untuk kelompok tidak berpasangan.
Tabel 4.2 Uji Beda Kadar Gula Darah Antara Kelompok Sevofluran Dan Isofluran
Gula Darah (mg/dL)
Kelompok
P** Sevofluran Isofluran
T0 68,63+16,25 66,00+23,71 0,717
T1 81.44+17,12 79,44+27,52 0,807
T2 77,88+25,52 91,19+32,12 0,204
P* 0.102 0.000
T1-T0 12,81+10,99 13,44+11,76 0,878
T2-T0 9,25+21,25 25,19+17,74 0,028
Ket : * Antar kelompok berpasangan(antara T0 dan T2) Uji paired sampel t test
** Antar kelompok tidak berpasangan Uji Independen Sampel T test T0 : kadar gula darah sebelum perlakuan
T1 : kadar gula darah setelah perlakuan 15 menit T2 : kadar gula darah setelah perlakuan 30 menit
(Sumber : Hasil Olah Data 2016)
Berdasarkan tabel 4.2 diketahui bahwa kadar gula darah sebelum perlakuan T0 pada pasien kelompok Sevofluran rata-rata 68,63+16,25 mg/dL, sedangkan pada kelompok Isofluran rata-rata 66,00+23,71 mg/dL.
Nilai p=0,717 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan kadar gula darah sebelum perlakuan antara kelompok
Sevofluran dengan kelompok Isofluran.
6 Kadar gula darah 30 menit setelah perlakuan (T2) pada pasien kelompok Sevofluran rata-rata 77,88+25,52 mg/dL, sedangkan pada kelompok Isofluran rata-rata 91,19+32,12 mg/dL. Nilai p=0,204 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan kadar gula darah pada T2 antara kelompok Sevofluran dengan kelompok Isofluran.
Selisih kadar gula darah antara 15 menit setelah perlakuan dan sebelum perlakuan (T1-T0) pada pasien kelompok Sevofluran rata-rata 12,81+10,99 mg/dL, sedangkan pada kelompok Isofluran rata-rata 13,44+11,76 mg/dL. Nilai p=0,878 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan selisih kadar gula darah pada T1-T0 antara kelompok Sevofluran dengan kelompok Isofluran.
Selisih kadar gula darah antara 30 menit setelah perlakuan dan sebelum perlakuan(T2-T0)pada pasien kelompok Sevofluran rata-rata 9.25+21.25 mg/dL, sedangkan pada kelompok Isofluran rata-rata 25.19+17.74 mg/dL. Nilai p=0,028 (p<0,05) yang berarti bahwa terdapat perbedaan yang signifikan selisih kadar gula darah pada T2-T0 antara kelompok Sevofluran dengan kelompok Isofluran. Dengan kata lain
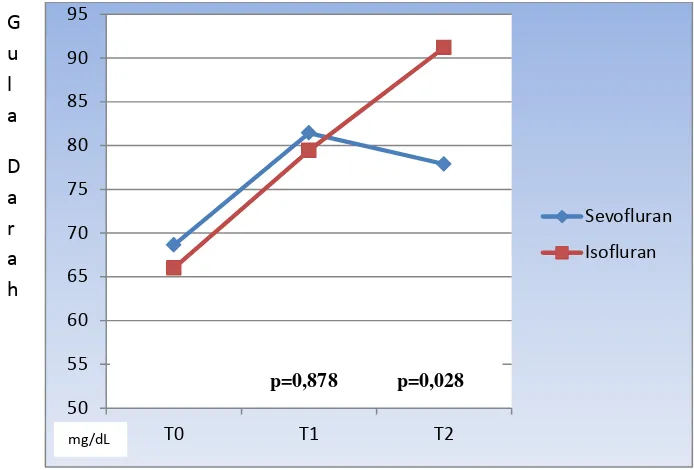
7 Gambar 8. Perbandingan Peningkatan Kadar Gula Darah
Berdasarkan gambar 8 diketahui bahwa kelompok isofluran terjadi peningkatan kadar gula darah dari waktu ke waktu, sedangkan pada kelompok sevofluran peningkatan kadar gula darah terjadi pada waktu 15 menit setelah pemberian maintenance T1 kemudian mengalami penurunan pada waktu 30 menit setelah pemberian maintenance (T2). Selisih peningkatan T2-T0 menunjukan perbedaan yang signifikan antara kelompok sevofluran dengan isofluran dengan nilai p-0,028 pada 30 menit setelah pemberian maintenance. Dengan demikian penggunaan sevofluran lebih efektif dalam menghambat peningkatan kadar gula darah dibandingkan dengan isofluran pada waktu 30 menit setelah pemberian
maintenance (T2).
B.Pembahasan
Hasil penelitian ini menunjukkan bahwa terdapat peningkatan kadar gula darah setelah pemberian maintenance selama 15 menit baik pada kelompok sevofluran maupun isofluran. Dimana Selisih kadar gula darah setelah maintenance 15 menit dan sebelum maintenance(T1-T0) pada pasien
50 55 60 65 70 75 80 85 90 95
T0 T1 T2
Sevofluran Isofluran G u l a D a r a h mg/dL
8 kelompok Sevofluran rata-rata 12,81+10,99 mg/dL, sedangkan pada kelompok Isofluran rata-rata 13,44+11,76 mg/dL. Nilai p=0,878 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan selisih kadar gula darah pada T1-T0 antara kelompok Sevofluran dengan kelompok Isofluran.
Peningkatan kadar gula darah setelah 15 menit pemberian maintenance agen inhalasi dimungkinkan karena berbagai hal diantaranya respon stress operasi, seperti perubahan kardiovaskular, perubahan cairan dan elektrolit, perubahan respon imun, perubahan metabolit, obat−obatan anestesi intravena, nyeri dan emosi yang semuanya mempengaruhi katekolamin, glukagon, insulin, kortisol serta metabolisme lemak dan karbohidrat. (Wani et al, 1993; Heger, 2008)
Kadar gula darah menunjukkan perbedaan yang signifikan antara kelompok sevofluran dengan isofluran pada waktu 30 menit setelah
maintenance (T2). Dimana selisih kadar gula darah T2-T0 pada pasien kelompok Sevofluran rata-rata 9,25+21,25 mg/dL, sedangkan pada kelompok Isofluran rata-rata 25,19+17,74 mg/dL. Nilai p=0,028 (p>0,05) yang berarti
bahwa terdapat perbedaan yang signifikan selisih kadar gula darah pada T2-T0 antara kelompok Sevofluran dengan kelompok Isofluran. Hal ini menunjukkan bahwa penggunaan sevofluran lebih efektif dibandingkan dengan isofluran dalam menghambat peningkatan kadar gula darah.
Hasil penelitian juga menunjukkan bahwa pasien kelompok Sevofluran sebelum perlakuan (T0) kadar gula darah rata-rata 68,63+16,25 mg/dL, sedangkan setelah perlakuan (T2) meningkat menjadi77,88+25,52 mg/dL, terjadi peningkatan rata-rata sebesar 9.25+21.25 mg/dL. Nilai p=0,102 (p>0,05) yang berarti bahwa tidak terdapat perbedaan yang signifikan kadar gula darah sebelum dan sesudah perlakuan pada kelompok Sevofluran.
9 sebesar 25,19+17,74 mg/dL. Nilai p=0,000 (p<0,05) yang berarti bahwa terdapat perbedaan yang signifikan kadar gula darah sebelum dan sesudah perlakuan pada kelompok isofluran.
Anestesi inhalasi banyak digunakan dalam praktik anestesi umum karena kemudahan dalam pemberian dan kemudahan dalam mengawasi efeknya. Agen anestesi utama yang sering digunakan saat ini adalah isofluran, desfluran, dan sevofluran. Sevofluran merupakan agen anestesi inhalasi yang paling banyak digunakan pada anak-anak (Ebert et al, 2009). Dosis anestesi inhalasi biasanya ditetapkan dalam MAC (minimum alveolar concentration) (Saifee et al, 2007). Beberapa agen inhalasi dapat memberikan efek proteksi miokard sehingga mencegah timbulnya iskemia yang diperlukan oleh banyak pasien yang menjalani anestesi umum (Campagna et al, 2003).
Saho et al (1997) menyebutkan pelepasan insulin yang distimulasi oleh glukosa ditekan oleh anestesi inhalasi pada model in vitro dan in vivo. Dari penelitian tersebut, anestesi sevofluran dapat mengurangi sekresi insulin yang diinduksi glukosa. Demikian juga, sekresi insulin basal yang diinhibisi oleh anestesi inhalasi. Sekresi insulin basal menurun selama anestesi sevofluran.
Oyama et al (1989) menyebutkan sekresi insulin basal menurun dengan anestesi sevofluran-nitro oksida. Anestesi sevofluran mempunyai efek inhibisi cepat yang reversibel pada sekresi insulin yang distimulasi glukosa, seperti pada anestesi inhalasi lain. Dalam hal ini, sevofluran juga dapat menginduksi resistensi insulin. Suatu studi hewan menunjukkan bahwa isoflurane menyebabkan hiperglikemia dalam derajat yang sama, namun, suatu studi observasi menunjukkan hasil yang bertolak belakang.Dengan Isofluran, cenderung terjadi penurunan aksi insulin dan glucagon sehingga utilisasi glukosa akan menurun (Allison SP, et al, 1998).
10 banyak jalur bagi anestesi inhalasi untuk menjalankan mekanisme tersebut. Anestesi inhalasi bekerja dengan mengaktivasi reseptor neurotransmiter inhibisi seperti GABAA dan glisin, serta mengaktivasi kanal ion kalium sehingga menyebabkan influk kalium dan terjadi hiperpolarisasi pada level presinapsis dan postsinapsis. Selain itu, anestesi inhalasi juga bekerja dengan menghambat transmisi eksitasi melalui inhibisi terhadap asetilkolin nikotinik neuronal, reseptor glutamat (NMDA dan AMPA), kanal ion natrium, dan kalsium sehingga mencegah timbulnya depolarisasi neuron (Perouansky et al, 2009).
Sevofluran merupakan cairan volatil yang stabil, jernih, dan tidak berwarna pada suhu ruangan serta tidak mudah terbakar atau meledak. Sevofluran memiliki bau yang paling tidak menusuk di antara ketiga agen inhalasi utama (isofluran, desfluran, dan sevofluran). Bau sevofluran tercium menyenangkan seperti bau kloroform. Sevofluran diberikan ke pasien secara inhalasi melalui mesin anestesi langsung menuju ke sistem pernafasan dan diserap oleh sirkulasi pulmonal (Saber et al, 2009).
Peningkatan yang cepat dan tidak tajam pada konsentrasi obat anestesi
di alveoli menyebabkan sevofluran sebagai pilihan yang paling bagus untuk induksi anestesi yang cepat dan lembut pada anak-anak dan pasien dewasa. Pada kenyataannya, induksi inhalasi dengan sevofluran 4-8% dalam 50% campuran nitrit oksida dan oksigen dapat dicapai kira-kira dalam 1-3 menit. Demikian juga, daya larut dalam darah yang rendah mengakibatkan penurunan konsentrasi obat anestesi di alveoli yang cepat yang tidak terus-menerus dan timbulnya lebih cepat dibandingkan isofluran (walalupun tidak dipindahkan lebih awal dari unit perawatan post anestesi) (Morgan et al, 2013).
12 BAB V
PENUTUP
A. Kesimpulan
Terdapat perbedaan bermakna pengaruh isofluran dibanding sevofluran terhadap kadar gula darah pasien yang menjalani anestesi umum. Isofluran lebih meningkatkan kadar gula darah pasien yang menjalani anestesi umum dibanding sevofluran.
B. Saran
1. Perlu penelitian lebih lanjut mengenai perbedaan pengaruh isofluran dan sevofluran terhadap kadar gula darah pasien yang menjalani anestesi umum di waktu yang berbeda (misal 45, 60, 75, 90, dan 120 menit) setelah pemberian maintenance.
2. Penggunaaan anestesi inhalasi sevoflurane perlu dipertimbangkan dibandingkan dengan isoflurane pada pasien dengan diabetes mellitus, mengingat pengaruhnya yang menghambat kenaikan kadar gula darah
lebih baik.
3. Perlu penelitian secara multicenter untuk penerapan dari hasil penelitian
13 DAFTAR PUSTAKA
Allison SP, et al, Some effects of anaesthesia and surgery on carbohydrate and fat metabolism. Br. J. Anaesth. 1998, 81: 273-7.
Akavipat P., Polsayom N., Pannak S., Punkla W. 2009. Blood glucose level in neurosurgery. Acta Med Indones-Indones J Intern Med. 41(3): 121-125.
Antognini J.F., Cartens E. 2002. In vivo characterization of clinical anaesthesia and its components. Br J Anaesth. 71: 148-163.
Aronoff SL, Berkowitz K, Shreiner B, Want Laura (2004). Glucose metabolism and regulation: Beyond insulin and glucagon. Diabetes Spectrum, 17 (3): 183-190
Bakta IM, Suastika IK (1999). Gawat darurat di bidang penyakit dalam.
Jakarta: EGC.
Behdad S., Mortazavizadeh A., Ayatollahi V., Khadiv Z., Khalilzadeh S.
2014. The Effects of Propofol and Isoflurane on BloodGlucose during Abdominal Hysterectomy in DiabeticPatients. Diabetes Metab J. 38:
311-316.
Behne M., Wilke H.J., Harder S. 2003.Clinical pharmacokinetics of sevoflurane.ClinPharmacokinet. 36 (1): 13-26.
14 Bolosco M, Barvais L, Engelman E, Fery F (2014). Perioperative management of
hyperglycemia: The diabetologist’s point of view. Acta Anaesth Belg, 65: 167-74
Branco RG, Garcia PCR, Piva JP, Casartelli CH, Seibel V, Tasker RC (2005). Glucose level and risk of mortality in pediatric septic shock. Pediatr Crit Care Med;6:470-2
Braz LG, Braz JR, Mo’dolo NS, do Nascimento P, Brushi BA, Carvalho LR. Perioperative cardiac arrest and its mortality in children. A 9-year survey in a Brazilian tertiary teaching hospital. Paediatr Anaesth. 2006; 16(8):860–6.
Bryan A, Oscar D, Guillamondegui, Sloan B, Fleming, Robert O, et al, Increased risk of adrenal insufficiency following etomidate exposure in critically injured patients. Arch Surg 2008 ; 143(1).
Butterworth JF, Mackey DC, Wasnick JD. Postanesthesia care. Dalam: Morgan GE, Mikhail M, penyunting. Clinical anesthesiology. Edisi ke-5. New York: McGraw Hill; 2013. hlm. 1257-75.
Budiarto, Eko. 2004. Biostatika Untuk Kedokteran dan Kesehatan Masyarakat. Jakarta: EGC.
Campbell, Reece, Mitchell (2004). Biologi. Edisi Kelima Jilid 3.Jakarta: Erlangga.
Campagna J.A., Miller K.W., Phil D., Forman S.A. 2003. Mechanisms of actions of inhaled anesthetics.N Engl J Med. 348: 2110-24.
15 Collins VJ. Opiate and narcotic drugs. In: Collins VJ. Physiologic and pharmacologic bases of anesthesia. 1st ed. Pennsylvania: Williams & Wilkins, 1996: 544-81.
Dahlan S. 2011. UjiChi-Square (Hipotesis Komparatif Kategorik Tidak Berpasangan Tabel 2x2). Statistik untuk Kedokteran dan Kesehatan. Jakarta: Salemba Medika. P: 30-34.
Dasgupta A., Sarma D. Saikia U.K. 2012. Hypomagnesemia in type 2 diabetes mellitus. Indian Journal of Endocrinology and Metabolism. 16(6): 1000-1003.
Deckardt K., Weber I., Kaspers U., Hellwig J., Tennekes H., van
Ravenzwaay B. 2007. The effects of inhalation anaesthetics on common clinical pathology parameters in laboratory rats. Food and Chemical Toxicology. 45: 1709–1718.
Desborough JP. The Stress Response to Trauma and Surgery, Endocrine and Metabolic Disorders in Anaesthesia and Intensive Care. Br. J. Anaesth. 2000; 85:109-17.
Dilger J. 2002. The effects of general anaesthetics on ligand-gated ion channels.
J Anaesth. 125: 309-318.
Dorland, W. A. N. 2010. Dorland’s Illustrated Medical Dictionary (29th ed.). Hartanto, H. et al, (ahli bahasa), Jakarta: EG
16 Edmont I., Edger I. 2009. Inhaled anesthesia: uptake and distribution. In: Miller
R.D. Miller’s Anesthesia Seventh Edition. USA: Elsevier.
Edomwonyi NP, Ekwere IT, Egbekun R, Eluwa B. Anesthesia-related complicationsin children. MEJ Anesth. 2006;18(5):915.
Garcia P.S., Kolesky S.E., Jenkins A. 2010. General anesthetic action on GABAA receptors.Current Neuropharmacology. 8: 2-9.
Ghozali I. 2005.Aplikasi Analisis Multivariat dengan Program SPSS.
Semarang: Badan Penerbit Universitas Diponegoro, pp: 89-95.
Guyton AC, Hall JE. Buku ajar fisiologi kedokteran (terjemahan). Edisi 9. Jakarta: EGC, 1996: 1063-76, 1203-37.
Handoko T, Suharto B. Insulin, glukagon dan anti diabetik oral. Dalam:
Ganiswara SG. Farmakologi dan terapi. Edisi 4. Jakarta: Gaya Baru, 1995: 467-81.
Hager P. Systemic stress response and hyperglicaemia after abdominal surgery in rat and man.(dissertation).Stockholm:Karolinska institutet;2008.
Hutagalung H (2004). Karbohidrat. Fakultas Kedokteran USU.
James P, McFadden R (2004). Understanding the processes behind the regulation of blood glucose. NT, 100 (16): 56-58
17 Krinskley JS (2003). Association between hyperglycemia and increased hospital mortality in a heterogenous population of critically illpatients. Mayo clin proc;78:1471-8
Liamis G., Liberopoulos E., Barkas F., Elisat M. 2014. Diabetes mellitus and electrolyte disorders. World J Clin Cases. 2(10): 488-496.
Lopes C., Franks N., Lieb W. 2003. Actions of general anesthetics and arachnoid pathway inhibitors on K+ currents activated by volatile anesthetics. Br J Pharmacol. 125: 309-18.
McAnulty G, et al, Anaesthetic management of patients with diabetes mellitus. Br. J. Anaesth. 2000; 85: 80-90.
Morgan GE, Mikhail MS. Clinical Anesthesiology. 2nd edition. Los Angeles: Appleton and Lange, 1996: chapter 34.
Myles PS, Buckland MR, Morgan DJ, Weeks AM. Serum lipid and glucose concentrations with a propofol infusion for cardiac surgery. J Cardiothorac
Vasc Anesth 1995; 9 (4): 378 – 8.
Morgan, E.G., Mikhail M.S., Butterworth J.K., Mackey D.C., Wasnick D.J. 2013. Inhalation anesthetics. In: Clinical anesthesiology 5th edition. Ohio: The McGraw-Hill Companies.
Narahashi T., Aistrup G.L., Lindstrom J.M. 2003. Ion channel modulation as the basis for general anesthesia. Toxicol Lett. 367: 607-14.
18 Perry E., Wlker M., Grace J., Perry R. 2001. Acetylcholine in mind: a neurotransmitter correlate of consciousness? Trends Neurosci. 22: 273-280.
Saber AT., Hougaard K.S. 2009. Isoflurane, sevoflurane, and desflurane.The Nordic Expert Group for Criteria Documentation of
Health Risks from Chemicals.Vol 43(9): 1-115.
Saho S, Kadota Y, Sameshima T, Miyao J, Tsurumaru T, Yoshimura N (1997).
The Effects of Sevoflurane Anesthesia on Insulin Secretion and Glucose
Metabolism in Pigs. Anesth Analg 84 (6): 1359-1365.
Saifee O., Solt K. 2007. Intravenous and inhalation anesthetics. In: Dunn P.F.
Clinical Anesthesia Procedurs of the Massachusetts General Hospital 7th
edition. USA: Lippincott William & Wilkins. Pp: 184-189.
Sjamsul hidayat, R. Dan Wim de Jong. (2005). Buku Ajar ilmu bedah, edisi revisi, Jakarta: EGC.
Sarif, Abdul Majid, Eko Suryani, 2012. Perbedaan Kejadian Mual Muntah Pasca Operasi Dengan Penggunaan Isofluran dan Halotan Sebagai Anestesi Inhalasi.Jurnal JIK, STIKES Hang Tuah Surabaya, PPNI dan AIPTINEKES.
Sastroasmoro S. 2008. Pemilihan Subyek Sampel. In: Sastroasmoro S. dan Ismael S. (ed). Dasar-Dasar Metodologi Penelitian Klinis. Ed. 3. Jakarta: Sagung Seto, p: 88.
19 Supranto J. 2000. Teknik Sampling Untuk Survei dan Eksperimen. Jakarta: Rineka
Cipta.
Stoelting RK, Hillier SC. Pharmacology and physiology in anesthetic practice. 4th ed. Philadelpia: Lippincott William & Wilkins, 2006: 163 – 7.
Tanaka K., Kawano T., Tomino T., Kawano H., Okada T., Oshita S. 2009.
Mechanisms of Impaired Glucose Tolerance and Insulin Secretion during
Isoflurane Anesthesia. Anesthesiology. 111: 1044-51.
Traynelis S.F., Wollmuth L.P., McBain C.J., Menniti F.S., Vance K.M., Ogden K.K. 2010.Glutamate receptor ion channels; structure, regulation, and fuction.Pharmacological Review.62(3).
Tumbelaka A.R., Riono P., Wirjodiarjo M., Pudjiastuti P., Firman K. 2007. Pemilihan Uji Hipotesis. In: Sastroasmoro S. dan Ismael S. (ed). Dasar-Dasar Metodologi Penelitian Klinis. Ed.3. Jakarta: Sagung Seto, pp: 279-301.
White PF. Optimizing Anesthesia for Inguinal Herniorrhaphy: General,Regional, or Local Anesthesia? Anesthesia & Analgesia 2001; 93: 1367-9.
Villars P.S., Kanusky J.T., Dougherty T.B. 2004.Stunning the neural
nexus: mechanisms of general anesthesia .AANA Journal. 72(3): 197-205.
Wakabayashi K. 2010. Stress, anesthesia, and blood hormone level. Gunma: Shibayagi’s Academic Information.
20 Zuurbier C.J., Keijzers J.M., Koeman A., Van Wezel H.B., Hollman M.W. 2008. Anesthesia’s Effects on Plasma Glucose and Insulin and Cardiac Hexokinase at Similar Hemodynamics and Without Major