62 liuku II
ID0200050
PPNY-ISATAN Yogyakarta 25-27 April 1995
PENENTUAN MOLBSDENUM D ALAM URANIUM DENG AN
METODE POLAROGRAFI
A.Punvanto, Iswani GS.PPNY-BATAN, Jl. Babarsari P.OBox 1008 Ycgyakarta 55010
A B S T R A K
PENENTUAN MOLIBDENUM DALAM URANIUM DENGAN METODE POLAROGRAFL Telah dipelajari pemisahan dan penentuan molibdenum (VI) daiam cupiikan uranium dioksida (UOi) dengan metode polarografi. Penenluan didasarkan pada reduksi eleklrokimia dari kompleks molibdenum (VI) -kuinolinolat (Movl OzQi). Untuk menghilanganpengaruh matrik kompleks tersebut diekstraksi ke dalatn kloroform. Setelah kloroform diuapkan pada suhu kamar, residu dilanttkan dengan N,N-Dimetil formamida (DMF). Polarogram Mo(VI) muncul puncak gelombang reduksipada potensial -0,48 volt
terftadap Ag/AgCl/KC! jemih dalam eicktrolit pendukung 1,0 M bufer asetat (1M CH3COOH -IM CHICOONHA). Ekstraksi dilakukan dalam media HjSOiOJ N, (pH) optimumpada 2.0dansenyawaan kompleks dipakni 4% oksin dalam H^SOA 0,5 N, ekstraksi dilakukan dua kali dengan kloroform 10 ml selama 5 menit, perbandingan fase air-organik 5:1. Dengan cara ini dicobakan terhadap Mo(Vl) konsentrasi 4,8 - 12,0 \ig dcngart adanya uranium 200 mg, prosen perolehan kembali sebesar 95%. Kandungan Mo(Vi) dalam cuplikan UO2 (dUarutkan dalam HNO} suprapitre) dengan cara adisi standar sebesar 5,26± 0.41
ABSTRACT
DETERMINATION OF MOLYBDENUM IN URANIUM BY DIFFERENTIAL PULSE POLAROGRAPHY. The seoaralion an determination ofMo(VI) in uranium dioxide (UOT) samples by pola-rography method were studied. The determination of Mo(VI) was based on electrochemislry reduction ofmolybdenum (VI) qxdnolinolat complex (Mo O2O2). To decrease the matrbc influence, this comptex was extracted into chloroform. After chloroform phase was evaporate at room temperature, residues were dissolved with N.N-Dimethyl formamida (DMF). Potenlial wave reduction ofMo(Vl) at -0,48 volt versus Ag/AgCI/KCl saturated in snporling electrolyte bujfer acelate 1 M (1M CH3COOH -1M CH-JCOONHA). Extraction was done in 0,3 MH2SO4 media at optimumpHo/2,0 and4% oxine in 0,5 M H2SO4 was usedas complex compound. Extractions two times with 10 ml chloroformfor 5 minules each ratio oforganic to water was 1:5. This methode was used lo determine Mo(VI) in concentration range of 4,8-12 \xg in thepresence oflOO mguranium. It wasfound recovery o/Mo(VI) was 95 %. Mo(VI) contents in UO2 samples determinated by standard addition was 5,26 ± 0.41 \xg/g
PENDAHULUAN
P
ada proses pemurnian uran.ium menjadi uranium murni nuklir, diperlukan analisis uji kualitas. Perlu diketahui adanya unsur-unsur minor dan kelumit yang terdapat dalam uranium. Molibdenum adalah salah satu unsurpengotoryang perlu diperhatikan dalam bahan bakar uranium karena Mo(VI) dapat membentuk senyawa fluorida yang mudah menguap, dan merygikan pada saat instalasi pengkayaan(4). Pada penentuan unsurpengotor Mo(VI) dalam uranium, dipelajari pengaruh unsur mayor uranium dan dipelajari cara pemisahannya. Pemisahan Mo(VI) dari.matrik Iainnya terutama uranium, dilakukan dengan cara
Sebagai pengompleks dipakai oxin (8-hidroksikuinolin) dalam suasana asam berikut diekstraksi ke dalam kloroform, molibdenum berada dalam fase kloroform. Prinsip penentuan didasarkan pada reduksi elektrokimia kompleks M o ( V I ) - kuinolinolat (MovlO2Q2) dibuat
p o l a r o g r a m n y a dalam media N,N-dimetiI formamida (DMF) dalam elektrolit pendukung Tetralmtyl amm^jerklorat dengan adanya asam asetat.0,01* DaTam percobaan ini dipakai elektrolit bufer asetat 1 M dalam media DMF, keluar dua puncak pada potensial -0,36 volt dan -0,48 volt terhadap elektroda pembanding Ag/AgCl/KC!jenuh.
l'rosiiliiig Pertemttan tlan Ilmialt
PI'NY-BATAN Yo&yakarla 25-27 April I99S liuktt II
dibanding dengan oksinat iain menjadi sukar larut dalam pelarut organik dan berbagai konsentrasi asam anorganik (S). Dalatn percobaan ini dipakai
pelarut dimetil formamida (DMF), dan kompleks ini mudah sekali iarut.
Menurut Boltz, De Vries dan Meion (3>
kompleks asam molibdo-posporik dalam bufer asetat pH 3,5 ( campuran dari 1 M asam asetat, 0,1 M Na asetat, 0,1 KCl ) menghasilkan dua gelombang dengan potensial puncak -0,45 volt dan -0,65 voli terhadap kalomel jenuh. Tinggi kedua geiombang tersebut berbanding langsung dengan konsentrasi Mo, tetapi arus difusi tidak mudah ditentukan.
Oleh karena itu dalam penelitian ini akan dikembangkan metode penentuan. Mo(VI) secara polarografi dengan raenggunakan elektrolit pendukung bufer asetat 1,0 M, dalam media dimetil formamida. Tujuan dari penelitian ini adalah. untuk analisis unsur pengotor dalam uranium dioksida, sebagai uji kualitas hasil proses pemumian.
TATA - KERJA
Bahan Kimia : 2. UO2(NO3)2.6H2O 3. CHjCOOH 4. CH3COONH4 5. CHCI3 6. Dimetil formamida 7. 8-Hidroksi kuinolin 8. H2SO„9. Kalium hidrogen pthalat 10. Akuatridest
Alat-alat:
Polarography Stand E 505, Polar-ecord E 506. Sel polarograph dilengkapi elektroda kerja tetes merkuri (DME), elektroda pembanding dan elektroda pembantu: Ag/AgCI/KCl jenuh Cara kerja
1. Dicoba beberapa eJektrolit pendukung untuk membuat polarogran Mo(VD dengan adanya Dicoba pembuatan polarogram M»(VI) pada konsentrasi tertentu, tanpa dan dengan adanya U(VI) dalam elektrolit pendukung :
a. 0,5 M K2H ptalat, pH 4,55 tanpa dan dengan
0,02 M kalium-askorbat atau dengan 0,02 M natrium-sitrat.
b. l M CH3COOH -1 M CH3COONR,, pH 4,6 c. lMCH3COOH-lMCH3COONH4,dengan
adanya dimetil formamida, pH larutan menjadi 5,8
2. Mempelajari konsentrasi Mo(VI) terhadap tinggi puncak dalam media DMF, elektroiit pendukung 1 M buferasetat.
Disiapkan 5 buah beker gelas 50 ml, dipipet 10 ^l M^(VI) 2,5.10"3M ke dalam beker, ditambah
40 ml H2SO4 0,3 N, pH ditepatkan 2,0, ditambah akuatrides sampai tanda tera. Diektraksi dua kali dengan lOm! 1% oksin-kloroform selama 5 menit. Fase kloroform diuapkan pada suhu kamar, setelah kering ditambah 10 ml DMF, 5 ml bufer asetat 5 M. Dipindahkan kuantitatif ke dalam labu takar 25 ml, ditambah akuatridest hinggabatas.
Dibuat polarogramnya, dibuat kurva konsentrasi terhadap tinggi puncak (arus puncak = Ip).
3. Optimasi pH ekstraksi.
Dilakukan variasi pH larutan untuk ekstraksi terhadap campuran Mo-U konsentrasi Mo(VI) 9,6 }ig dan U(VI) 200 mg.
Dipipet40 nlMo(VI)2,5.10'3M, ditambah 1 ml
U(VI) 200 mg/ml^O ml H2SO4 0,3N, 10 ml
oksin 4% dalam H2SCK, 0,5 N.
Divariasi pH larutan : 1,0 ; 1,5 ; 1,75 ; 2,0 dan 2,25 dengan NaOH/ftSOo, kemudian diekstraksi dua kali dengan 10 ml kloroform. Fase kloroform diuapkan pada suhu kamar. Residu ditambah 10 ml DMF, 5 ml bufer asetat 5 M, volume ditepatkan 25 ml dengan akuatrides, berikut dibuat polarogramnya. 4 . . Optimasi volume N,N-Dime£il fonnamid
• (DMF)
Disiapkan 5 buah beker gelas 50 ml, dipipet 10 (.tl Mo(VI) 2,5 .10"3M dimasukkan ke dalam
beker, ditambah 40 ml H2SO4 0,3 N, pK
ditepatkan 2,0, ditafnbah akuatrides sampai tandatera. Diektraksi duakali dengan lOml 1% oksin-kloroform selama 5 menit. Fase kloroform diuapkan suhu kamar, ditambah DMF dengan volume bervariasi: 5; 7,5; 10; 15 dan 20 ml. Larutan djpindah kuantitatif dalam labu takar 25 ml, ditarnbah akuatrides hingga batas.
Masing-masing dibuat polarogramnya, diukur tinggi puncak, dibuat kurva volume DMF terhadap tinggi puncak.
Buku II
Prosiding I'ertemuan ilan llmiah I'l'NY-BATAN Yo»yakarta 25-27 April 1995
5. Mencari efisisiensi ekslraksi
Dibuat variasi konsentrasi Mo(VI) diekstraksi, dibandingkan tanpa ekstraksi, dihitung prosen perolehan kembali.
a. Tanpa ekstraksi
Konsentrasi Mo(VI): 2,4; 3,6; 4,8; 6,0 dan 7,2 p.g dalam beker 50 ml, ditambah 10 ml 2% oksin-DMF, 5 ml bufer asetat 5M, dan akuatrides hingga volume 25 ml.Dibuat polarogramnya, diukur tinggi puncak, dihkung persamaan regresinya.
b. Dengan ekstraksi
Konsentrasi Mo(Vl): 2,4; 3,6; 4,8; 6,0 dan 7,2 p.g dengan adanya U(VI) 200 mg dalam beker 50 ml, ditambah 40 ml H2SO4 0,3 N,
pH ditepatkan 2,0. Dipindahkan ks dalam labu takar 50 ml,ditambah akuatrides hingga batas tera. Diekstraksi dua kali dengan 10 ml dari 1% oksin-kloroform selama 5 menit. Fase kloroform yang mengandung Mo dipisahkan dengan fase air. Fase kloroform diuapkan suhu kamar, residu dilarutkan dengan 10 ml DMF, ditambah 5 ml elektrolit pendukung bufer asetat 5 M dan ditambah akuatrides hingga volume 25 ml. Dibuat polarogramnya, diukur tinggi puncak dan dibuat kurva pH terhadap arus puncak. 6. Pengaruh beberapa kation pengotor terhadap
polarografi Mo(VI) dalam elektrolit 1,0 M bufer asetat, media DMF.
Dipipet 5 ml larutan 5,0 M bufer asetat, 10 ml 2% oksin dalam DMF ditambah akuatrides hingga 25 ml, kemudian dibuat polarogramnya. Ditambah Mo(VI) 2,4 ^g, dan dibuat nolarogramnya.
Ditambah volume tertentu (jil) dari larutan induk kation pengotor U(VI) sehingga konsentrasi U(VI): 10,20 30,40,50,60,80 dan 100 mg, setiap penambahan dibuat polarogramnya
Dengan cara yang sama dibuat untuk: P, Ti, Zn, V, Sn, = 1 -100 pg, Fe, Cd,Cu dan Pb = 1-10 jig. Setiap penambahan dibuat polarogramnya, diukur tinggi puncak dan potensial puncak, dibandingkan antara Mo murni dan setelah ditambahkan unsur pengotor.
7. Penyediaan larutan standar a. Kompleks Mo-oksikuinolin.
Dilarutkan 200 mg ammonium molibdat [(NH4)6MO7O24.4H2O3 dalam 50 ml
akuatrides. Diekstraksi 5 X dengan. 10 ml 1% oksin-kloroform. Fase kloroform
diuapkan, residu dicuci 3 X dengan metanol, dikeringkan daiatn freezy drying.
b. Larutan standar { Movl O2 Ch) D i t i m b a n g
43,39 mg kristal kering, dilarutkan dengan pelarut N.N-Dimetilformamida hingga volume 100 ml. ( 100 jal = 10 g Mo) 8. Anaiisis cuplikan UO2 dari hasia.proses
pemurnian instaiasi Teknologi Proses a. Preparasi cuplikan.
Ditimbang cuplikan ± 1,000 gram daiam beker, dilarutkan dengan 2 ml HNO3
suprapure sambil dipanaskan, ditambah akuatrides, diuapkau sampai kering diulangi 3 kali untuk menurunkan keasaman. Ditambah 40 mi H2SO4 0,3 N, pHditepatkan
2.0, ditambah 10 ml larutan 4% oksin dalam H2SO4 0,5 N, Diekstraksi dua kali dengan kloroform @ 10 ml. Fase organik dipisahkan, diuapkan suhu kamar.
b. Analisis dengan polarograph
Residu diiarutkan dengan 10 ml DMF, ditambah 1 Mbuferasetathinggavolume25 ml. Larutan dalam sel polarograph dialiri gas N2 10 nienit dan dibuat polarogramnya, dari potensial awal 0,00 volt sampai -1,10 volt. Diadisi dengan larutan standar Movq
O2 Q2 volume tertentu. Dicatat tinggi
puncak sebelum dan setelah diadisi, dihitung konsentrasi Mo(VI) dalam cuplikan.
HASIL DAN PEMBAHASAN.
1. Polarogram Mo dalam beberapa elektrolit pendukung diperoleh hasil ditunjukkan pada tabel 1.
Tabel 1. Potcnsial puncak polarogram MoVI) dan U(VI) daiam beberapa elektrolit pendukung. No 1 2 3 4 Elcktrolit pendukung 0,5 MK2HptaIatph 4,55 0,5 M K2H ptalat 0,02 M K-askorbat ph 4,5 0,5 M K2H ptala; 0,02 MNa-silratph 4,5 IMCH3COOH-Hasil Vs Ag/AgCl Mo(VI) -0,51 -0,58 -0,96 -0,60 U(VI) -0,395 -0,395 -0,395 -0,41 Pustaka Vs SCE Mo(VI) -0,58 ;O,65 U(VI) -0,45 -0,45
Prosiding ferlenutan dan Ilmiah
l'PNY-BATAN Yogyakarfa 25-27Aiirit 1995 Bnku l[ 65
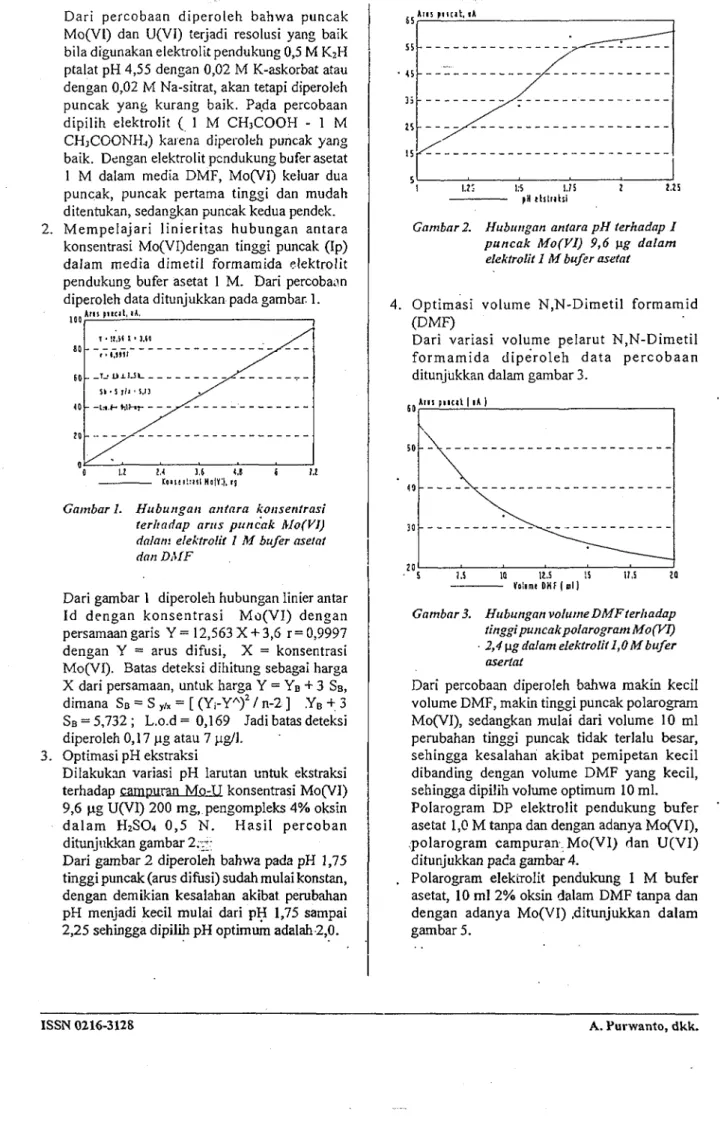
Dari percobaan diperoleh bahwa puncak Mo(VI) dan U(VI) terjadi resolusi yang baik bila digunakan elektrolit pendukung 0,5 M K2H ptalat pH 4,55 dengan 0,02 M K-askorbat atau dengan 0,02 M Na-sitrat, akan tetapi diperoleh puncak yang kurang baik. Pada percobaan dipilih elektrolit ( 1 M CH3COOH - 1 M
C H J C O O N H J ) karena diperoieh puncak yang baik. Dengan elektrolit pcndukung bufer asetat 1 M dalam media DMF, Mo(VI) keluar dua puncak, puncak pertama tinggi dan mudah ditentukan, sedangkan puncak kedua pendek. 2. Mempelajari linieritas hubungan antara
konsentrasi Mo(VI)dengan tinggi puncak (Ip) dalam media dimetil formamida elektrolit pendukung bufer asetat 1 M. Dari percobaim diperoleh data ditunjukkan pada gambar 1.
100
T • !!.S< I • 3.1«
!.< }.( l.l IX
Gainbar 1. Hubungan antara konsentrasi terhadap arus puncak Mo(VI) dalam elektrolit 1 M bufer aselat dan DMF
Dari gambar 1 diperoleh hubungan linier antar Id dengan konsentrasi Mo(VI) dengan persamaan garis Y = 12,563 X + 3,6 r = 0,9997 dengan Y = arus difusi, X = konsentrasi Mo(VI). Batas deteksi dihitung sebagai harga X dari persamaan, untuk harga Y = YB + 3 SB,
dimana SB = S ylx = [ (Y|-YA)2 / n-2 ] YB + 3
SB = 5,732 ; L.o.d = 0,169 Jadi batas deteksi
diperoleh 0,17 jig atau 7 ng/1. 3. Optimasi pH ekstraksi
Dilakukan variasi pH larutan untuk ekstraksi terhadap campuran Mo-U konsentrasi Mo(VI) 9,6 ng U(V1) 200 mg, pengompleks 4% oksin dalam H2SO4 0,5 N . Hasil percoban ditunjukkan gambar 2:rr;
Dari gambar 2 diperoleh bahwa pada pH 1,75 tinggi puncak (arus difiisi) sudah mulaikonstan, dengan demikian kesalahan akibat perubahan pH menjadi kecil mulai dari pH 1,75 sampai 2,25 sehbgga dipilih pH optimum adalah-2,0.
Alli p n t l t ,
55
1:5 I./S pH ttsltiisi
2.25
Gambar 2. Hubungan antara pH terhadap I puncak Mo(VI) 9,6 p.g dalam elektrolit 1 M bufer asetat
4. Optimasi volume N,N-Dimetil formamid (DMF)
Dari variasi volume pelarut N,N-Dimetil formamida diperoleh data percobaan ditunjiikkan dalam gambar 3.
,„Atis j i i c i t | lA )
50
1.5 10 12.5 !5 — Voiini( O H F ( j i l )
Gambar 3. Hubungan volume DMFterhadap tinggi puncak polarogramMo(VI) • 2,4\ig dalam elektrolit 1,0M bufer
asertat
Dari percobaan diperoleh bahvva makin kecil volume DMF, maktn tinggi puncak polarogram Mo(VI), sedangkan mulai dari volume 10 ml perubahan tinggi puncak tidak terlalu besar, sehingga kesalahan akibat pemipetan kecil dibanding dengan volume DMF yang kecil, sehingga dipilih volume optimum 10 ml. Polarogram DP elektrolit pendukung bufer asetat 1,0 M tanpa dan dengan adanya Mo(VI), .polarogram campuran Mo(VI) dan U(VI)
ditunjukkan pada gambar 4.
Polarogram elektrolit pendukung 1 M bufer asetat, 10 ml 2% oksin dalam DMF tanpa dan dengan adanya Mo(VI) .ditunjukkan dalam gambar 5.
66 Buku 11
Proxiclin<> Pertenuian dan llniiah PI'NY-BATAN Yogyukarta 25-27April 1995
Ans difisi, i 0,S IA 0 0.1 0.2 0.3 0.* 0.S 0.6 0.? • PotHSiil | Yoll j 0.9 1 120 100 80 60 40
Gambar 4. a. Polarogram bufer asetai 1,0 M b. Mo(VI) 9,6 p.g dulam larutan
(a)
c. Campuran Mo(Vlj dan U(VI) 23,8 mg
*rn (il.lill.S IAI
i^ liitiutMU.ItH *•
-0 -0.1 -0.! -0.3 -0,4 -0.5 O.i -0./ -0.6 -0.9
• P o i e i t i i l l ' i l l ]
Gambar 5. a, Polarogram elektrolit bufer asetai 1,0 M, 10 ml larutnn 2 % oksin dalam DMF
b. Mo(VI) 3.6 \i.g dalam elektrolit 00
Tabel2. Analisis dan efisicnsi ekstraksi molibdenum (VI) konsentrasi 2,4 - 12 Hg dengan adanya uranium 200 mg
Konsentrasi awal Mo+S 2,4 4,8 7,2 9,6 12,0 Mg 200 200 200 200 200 Kons Mo (VI) diperolch 1,5 5,0 6,6 9,0 •11,9 1,6 4,5 5,6 9,7 12,1 Hg) 2,4 4,4 6,4 10,1 11,0 Proscn pcrolchan 1 64,3 104*5 91,0 93,5 99,7 <ctnba! 67,6 93,4 77,7 101,3 100,9' 100,0 91,4 88,5 105,4 92,0
5. Mencari efisisiensi ekstraksi
Dibuat variasi konsentrasi Mo(V!) dengan adanya uranium dilakukan ekstraksi, dibaivdingkan tanpa ekstraksi, dihitung prosen perolehan kemb'ali, diperoleh hasil percobaan ditunjukkan pada tabel 2.
Dari tabel 2, diperoleh bahwa ekstraksi kurang berhasil untuk Mo(VI) < 2,4 \ig, untuk jumlah Mo > 4,8 }ig didapat prosen perolehan kembali rerata sebesar 95 %-.
6. Analisis cuplikan UO2
Analisis Mo(VI) dalam cupiikan UO2 dengan
teknik standar adisi diperoleh data ditunjukkan padatabel3.
Tabel3. Konsentrasi Mo(VI) dalam cuplikan UO2 dengan teknik standar adisi dibandingkan dengan kurva standar.
No 1 2 3 4 5 Berat Sampcl (gram) 1,0013 1,0040 1,0015 1,0027 1,0034 Hasil Analisis ( [xg 1 g ) Kurva standar 5,34 5,90 4,51 7,24 7,22 Rerata = 5,94 Deviasi = l,09 Standar adisi 5,44 5,72 5,33 4,62 5,20 Rerata = 5,26 Deviasi = 0,41
Dari percobaan diperoleh bahwa analisis Mo(VI) dalatn cuplikan UO2 dengan standar adisi adalah 5,26 + 0,41 ng/g, dengan kurva standar diperoleh 5,9 ± 1,09 pg/g, kedua cara memberikan hasil yang hampir sama, dengan standar adisi penyimpangannya lebih kecil.
KESIMPULAN
Penentuan molibdenun (VI) sebagai kompleks Mo-oksin dalara kloroform dapat ditentukan secara elektrokimia metode polaro-grafi dengan elektrolit pendukung 1 M CH3COOH -1 M CH3COONH4 dalam media N,N-Dimetil formamida. Dengan cara ini diperoleh batas penentuan yang rendah.
Ekstraksi terhadap campuran Mo(VI) -U(VI) kondisi optimum pada pH 2,0. Pengomplek digunakan 4% oxin dalam H2SO4 0,5 M, solven
ekstraksi kloroform, perbandingan fase ojrganik-air adalah 1:5. Volume DMF berpengaruh terhadap
Prositling l'ertenman etan Hm'uih
Pi'NY-JSATAN Yogyakarla 25-27April 1995 Buku II 67
puncak polarogram, dipcroleh volumeoptimum 10
tni. 'f
Dari beberapa kation pengotor yang dipelajari, ada gangguan dari Pb(II) bila konsentrasi Pb 2 kali konsentrasi Mo, menurut pustaka(5) dapat ditekan dengan penambahan pirokatekol 0,01 %.
Puncak uranium dan Mo dalam bufer asetat pH 4,5 terpisah dcngan resolusi yang baik, sehingga tidak rnengganggu. Matrik lain : P, Zn, Ti, Pb, V, Sn hingga 100 jig, kemudian Fe, Cd dan Cu hingga 10 ug belum berpengaruh terhadap 2,4 (ig Mo(VI). Kandungan Mo(VI) dalam cuplikan UO2 dengan cara standar adisi adaiah 5,26 ± 0,41 ji/g, dengan kurva standar diperoleh 5,9 ± 1,09 \i/g, kedua cara memberikan hasil yang hampir sama, akan tetapi dengan standar adisi penyimpangannya lebihkecil.
DAFTAR PUSTAKA
1. PAULA BOSSERMAN DONALLD T. SAWYER, and ALBERT L.PAGE., "Differential Pulse Polarographic Determination of Molybdenum at Parts-per-Billion Levels", Departement of Chemistry, University of California, Riverside, California 92521. Analytical Chemistry, Vol.50, No.9, August 1978. 2. PROPST R.C., "Polarographic
determination of uranium in the presence of molybdenum", DP-236, Analytical Chemistry Division, Atomic Energy Division, The USA Energy Commission, September 1957.
•'• 3. KOLTHOF I.M., and LINGANE J.J., " Inorganic Polarography" Volume II, Interscience Publishers, New York 1952. 4. RIDWAN M, dkk,; "Pengantar Ilmu
Pengetahuan Dan Teknologi Nuklir" , BATAN, Jakarta 1978. •
5. GUNANJAR, "Penentuan Fe, Cu dan Mo dalam yellovv cake dengan metode polarografi". Proceedings Bahan Murni, Fisika, Reaktor dan Instrumentasi". Yogyakarta 1982.
6. Anonim, "The Determination of Small Quantities of Molyb-denum in Water,Effluent,Plants, Salts and Other Samples". Metrohm Application-Bulletin No.l20e,August 1979
7. Anonim, "Direct Polarographic Determination of Trace Amounts of
Molybdcnum in Water". Metrohm AppIica1i;Sn-Bu[[etinNo.l45,January 1980. 8. ARTHUR I. VOGEL.,"Texbook of Quantitatif inorganic Analysis" Third Edition, London 1961.
juampiran
Polarogram DP larutan blanko hasil ekstraksi, dan poiarogram Mo(VI) 10 mikrogram dalam elektrolit pendukung bufer asetat 1,0 M dalam media DMF, ditunjukkan pada gambar 6.
160 140 120 100 80 60 40 20 0 A n s ifilssi, 1 0,6 \ 0.1 0.2 0.3 0.4 0.5 O.t 0.1 0.8 0.9 I PotensUl Ivotl]
Gambar6. a. Polarogram larutan blanko hasii ekstraksi
b. Polarogram Mo(VI) 10 mg, dalam media DMF, elektrolit pendukung bufer asetat 1,0 M. Tabe! 4. Kondisi operasi alat polarograph
No 1 2 3 4 5 6 7 8 9 10 11-Paramctcr/kondisi alat Elektroda kerja Elektroda pembanding Elektroda pembantu Elektrolit pendukung Lama deaerasi Potensial awal Potensial akhir PotensiaJ puncak I Potensial puncak 11 Waktu tetes (t drop) Sensitivitas Kcterangan Tetes merkuri Ag/AgCI/KCljenuh Ag/AaCl/KCljenuh 1 M bufer asetat lOmenit Ovolt -1,10 volt -0,48 volt -0,68 volt 0,4 detik 6.10'9A/mm(0,l)
6,1 liiiku II
Prosirfing Pertcnntiui dtui Ilmiali I'PNV-BATAN Yofjynkaria 2S-27April 1995
TANYA JAWAB
Muzakky
1. Mengapa anda memilih volume optimum gambar 3. DMF 10 ml, padahal puncak terbaik pada 15 ml, mohon dijelaskan Apakah meioda atida ini dapai menganalisis Mo dalcm hasil belah U teriradiasi, yang lebih menarik di masa mendatang, khnsusnya olah idang iiranium ?
A.Punvanto
2.
Pada pelarut DMF 5 ml, puncak Mo tinggi runcing, ada dua puncak overlap, kemungkinan puncak yang terlalu tinggi tersebut adalah arus maxima, bukan arus difusi sehingga puncak polarogram tersebut bukan yang terbaik. Puncak yang baik pada volume DiMF 10 -15 ml, pada volume tersebut diperoleh satu puncak yang baik, mudah ditentukan arus potensial puncaknya. Untuk menentukan Mo dalam hasil belah U teriradiasi, tentu diperlukan metode yang lebih baik dan khusus, mengingat faktor keselamatan. Metode penentuan Mo dalam
uranium yang kami lakukan ini memerlukan periakuan ekstraksi, apabila cuplikan U teriradiasi tentu ekstraksinya lcbih khusus lagi.
Wuryanto
Mengapa pada pcnambhan DMFpada arus puncak Mo(VI) tnrun tajam dan innlai tetap pada volume 10 ml. Fenomena apayaugtcrjadi? A. Punvanto
Makin banyak volume DMF, ?.rus puncak (Ip) makin turun. Ha! ini kemungkinan disebabkan
oleh pembentukan kompleks Mo(VI) dengan DMF, disamping pembentukan kompleks dengan oxin. Pada volume DMF 5 ml, terjadi puncak yang tinggi runcing diikuti puncak berikutnya yang lebih kecil. Pada volume DMF 10 dan 15 ml, diperoleh puncak yang baik, mudah dievaluasi Ep & Ip (hanya timbul
satu puncak), pada volume DMF 20 ml, juga terjadi dua puncak. Kemungkinan lain pengaruh H2O pada penggunaan bufer asetat terhadap pembentukan komplek Mo dengan oxin, yaitu Mo lebih cenderung dikelilingi oleh molekul H2O dari pada membentuk komplek dengan oxin. Hal ini perlu dikaji iebih lanjut.