LAPORAN HASIL ANALISIS BUTIR SOAL SEBAGAI PENENTU KUALITAS SOAL PADA MATERI SISTEM PERIODIK UNSUR
Dosen Pengampu : Yuli Rahmawati, M.Sc, Ph.D.
Disusun oleh :
Afwu Hayyi Amyyana (3315130926) Dian Nisa Fitriani (3315133600) Fahri Abdurachman (3315133598) Muhammad Sahrul Fakhri (3315133597)
PENDIDIKAN KIMIA 2013
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI JAKARTA
KATA PENGANTAR
Assalamualaikum Wr.Wb
Segala puji bagi Allah SWT yang telah melimpahkan kenikmatan serta hidayah-Nya terutama nikmat sehat, islam dan iman sehingga kami dapat menyelesaikan makalah laporan ini dengan judul “Laporan Analisis Butir Soal Sebagai penentu Kualitas Soal Pada Materi Sistem Periodik Unsur”. Makalah ini disusun sebagai tugas akhir pemenuhan mata kuliah Perencanaan, Pengelolaan dan Evaluasi Pembelajaran (PPEP).
Dalam proses pembelajaran ini, kami mengucapkan terimakasih kepada Ibu Yuli Rahmawati selaku dosen pengampu mata kuliah PPEP, Ibu Lilis selaku guru kimia SMAN 21 dan siswa-siswa X MIA 3 SMAN 21 Jakarta serta rekan-rekan mahasiswa yang telah banyak membantu untuk menyelesaikan makalah ini.
Penulis menyadari bahwa makalah ini masih belum sempurna. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun untuk perbaikan makalah ini.
Semoga makalah ini dapat bermanfaat bagi penulis khususnya dan pembaca umumnya.
Wassalamualaikum Wr.Wb
Jakarta,19 Desember 2015
DAFTAR ISI
I. PENDAHULUAN ... 2
A. Pengertian Tes ... 2
B. Tujuan ... 3
C. Deskripsi (Cakupan Kegiatan Analisis Tes)... 3
D. Konteks ... 4
II. VALIDITAS ... 5
A. Validitas Isi (Kisi-Kisi) ... 5
B. Validitas Konstruksi ... 5
C. Validitas Item ... 5
D. Validitas Bandingan ... 5
III. RELIABILITAS ... 9
A. Reliabilitas KR-20 ... 9
B. Reliabilitas Tes Uraian ... 9
IV. ANALISIS BUTIR SOAL ... 11
A. Analisis Tingkat Kesukaran ... 11
B. Analisis Daya Pembeda ... 11
C. Distraktor ... 11
V. PEMBAHASAN ... 15
A. Analisis Tes Pilihan Ganda ... 15
1. Validitas Isi ... 15
2. Validitas Konstruksi ... 15
3. Validitas Bandingan ... 16
4. Reliabilitas KR-20 ... 16
5. Validitas Item ... 16
6. Analisis Tingkat Kesukaran ... 17
7. Analisis Daya Pembeda ... 18
8. Distraktor ... 20
B. Analisis Tes Uraian ... 24
1. Validitas Isi ... 24
2. Validitas Konstruksi ... 24
3. Reliabilitas Tes Uraian ... 25
VI. KESIMPULAN ... 26
I. PENDAHULUAN
A. Pengertian Tes
Tes adalah suatu pertanyaan atau tugas/seperangkat tugas yang direncanakan untuk memperoleh informasi tentang trait/atribut pendidikan atau psikologik yang setiap butir pertanyaan atau tugas tersebut mempunyai jawaban atau ketentuan yang dianggap benar (Ebel dan Frisbie : 1996). Tes dapat dibedakan menjadi:
1. Tes Tertulis
Dimana pertanyaan-pertanyaan atau soal-soal yang diajukan dan jawaban yang harus diberikan siswa dilakukan secara tertulis. Tes tertulis juga dapat dibedakan menjadi:
• Tes Objektif (Tes Melengkapi, Tes Isian, Tes Benar Salah, Tes Pilihan Ganda dan Tes Menjodohkan)
• Tes Uraian 2. Tes Lisan
Yakni tes membawa pertanyaan-pertanyaan atau soal-soal yang diajukan dan jawaban yang harus diberikan siswa dilakukan secara lisan.
3. Tes Perbuatan
Yakni tes yang pertanyaan-pertanyaannya dapat diajukan dalam bentuk tulisan atau lisan akan tetapi jawaban yang harus diberikan siswa dilakukan dalam bentuk perbuatan.
Ciri tes yang baik adalah : 1. Validitas
Sebuah tes hasil belajar disebut valid bila tes tersebut dapat tepat mengukur apa yang hendak diukur dengan kata lain sebuah tes dikatakan telah memiliki validitas apabila tes tersebut secara tepat, benar atau shahih telah dapat mengukur apa yang seharusnya diukur melalui tes tersebut.
2. Reliabilitas
dinilai.
3. Objektivitas
Sebuah tes dikatakan memiliki objektivitas apabila dalam melaksanakan tes itu tidak ada factor subjektif yang mempengaruhinya.
4. Praktibilitas
Sebuah tes dikatakan memiliki praktibilitas yang tinggi bila tes tersebut bersifat praktis, mudah dilaksanakan, dalam pengertian mudah untuk pengadministrasiannya, mudah pemeriksanaannya dan dilengkapi dengan petunjuk yang jelas dalam cara mengerjakannya.
5. Ekonomis
Pelaksanaan tes tersebut tidak membutuhkan ongkos atau biaya yang mahal, tenaga yang banyak, dan waktu yang lama.
B. Tujuan
1. Untuk menguji ketepatan soal Sistem Periodik Unsur berdasarkan tingkat pemahaman siswa.
2. Untuk mengukur hasil belajar siswa dalam materi Sistem Periodik Unsur. 3. Untuk mengelompokkan jenis soal berdasarkan tingkat kesukaran.
4. Untuk melatih soft skill dalam pembuatan soal yang baik.
C. Deskripsi
Pembuatan soal menjadi hal wajib yang harus dikerjakan oleh seorang pendidik untuk mengetahui tingkat pencapaian kompetensi peserta didik. Banyak hal yang harus diperhatikan dalam pembuatan soal agar soal memiliki kualitas yang baik. Penyusunan dan pengembangan soal dimaksudkan untuk memperoleh tes yang valid sehingga hasil ukurnya dapat mencerminkan secara tepat hasil belajar atau prestasi belajar yang dicapai oleh masing-masing individu peserta tes. Untuk mengetahui kualitas soal yang telah dibuat, dilakukan analisis butir soal yang terdiri dari Kualitas item, yang direpresentasi oleh tingkat kesukaran, daya pembeda, validitas dan reliabilitas, dan khusus untuk tes pilihan ganda tidak kalah pentingnya adalah keefektifan pengecoh atau distraktor.
Dilaksanakan pada tanggal 21 Oktober 2015.
D. Konteks
II. VALIDITAS
A. Validitas Isi (Kisi-Kisi)
Terlampir dalam lampiran 1. Validitas Isi, Konstruksi dan Hasil Revisi
B. Validitas Konstruksi
Terlampir dalam lampiran 1. Validitas Isi, Konstruksi dan Hasil Revisi
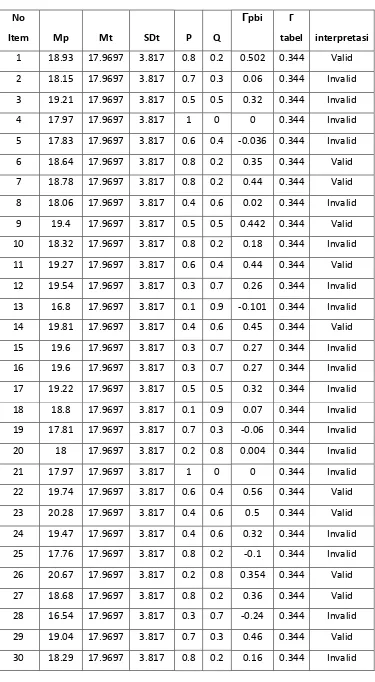
C. Validitas Item
Terdapat pada Tabel 2.1. Validitas Item
D. Validitas Bandingan
∑ xy Γxy =
√(∑ x2)(∑ y2)
Γxy =
1069.56
= 0.32
165358
Γtabel = 0.32
Sehingga, Γxy < Γtabel, Korelasi Tidak Signifikan
III. RELIABILITAS
A. Reliabilitas KR-20 (Pilihan Ganda)
Terdapat pada Tabel 3.1. Reliabilitas KR-20
Tabel 3.1. Reliabitias KR-20
∑pq 5.52
S2 (Standar Deviasi) 18.37
Γ11 0.72
Γ11 Reliabilitas Tinggi
B. Reliabilitas Tes Uraian
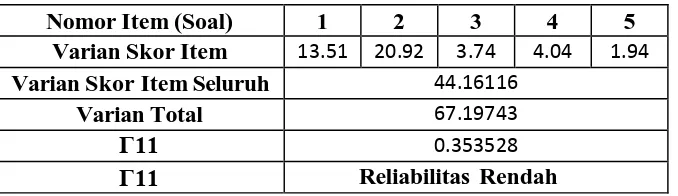
Terdapat pada Tabel 3.2. Reliabilitas Tes Uraian
Tabel 3.2. Reliabitias Tes Uraian
Nomor Item (Soal) 1 2 3 4 5
Varian Skor Item 13.51 20.92 3.74 4.04 1.94
Varian Skor Item Seluruh 44.16116
Varian Total 67.19743
Γ11 0.353528
IV. ANALISIS BUTIR SOAL
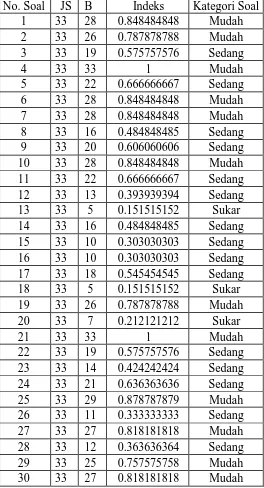
A. Analisis Tingkat Kesukaran
Terdapat pada Tabel 4.1. Analisis Tingkat Kesukaran
B. Analisis Daya Pembeda
Terdapat pada Tabel 4.2. Analisis Daya Pembeda
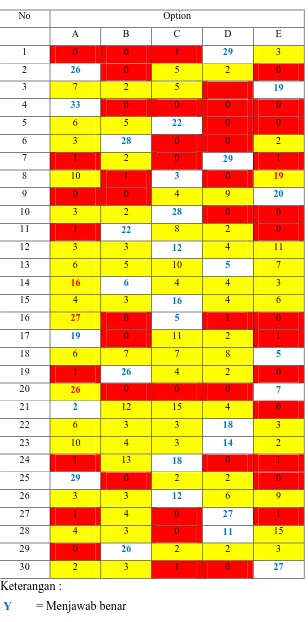
C. Distraktor
Tabel 4.1. Analisis Tingkat Kesukaran
Banyaknya Siswa yang Menjawab (JS)
Tabel 4.2. Analisis Daya Pembeda
Banyak Siswa Menjawab Benar Di Kelas Atas = BA
Tabel 4.3. Distraktor
X = Distractor sangat baik = Distractor tidak berfungsi
V. PEMBAHASAN
Tes yang dianalisis dibuat dengan tujuan untuk mengkaji dan menelaah tes agar diperoleh soal yang bermutu, untuk mengetahui apakah tes atau soal yang digunakan untuk mengevaluasi sudah mampu mengukur apa yang sebenarnya ingin diukur melalui tes atau soal tersebut dan untuk mengetahui sejauh mana data yang dihasilkan oleh tes atau soal dapat berguna bagi proses pembelajaran.
Materi yang diuji dalam tes adalah materi sistem periodik unsur. Testee yang kami pilih adalah siswa kelas X MIA 3 pada SMA Negeri 21 Jakarta, dengan jumlah testee sebanyak 33 siswa. Soal yang diujikan berupa tiga puluh butir soal pilihan ganda dan lima butir soal uraian.
Untuk analisis tes pilihan ganda ini, cakupan kegiatannya meliputi validitas isi, validitas konstruksi, validitas item, validitas bandingan, analisis tingkat kesukaran dan analisis daya pembeda. Sedangkan untuk analisis tes uraian meliputi reliabilitas tes uraian. Berikut hasil analisis tes tersebut.
A. Analisis Tes Pilihan Ganda 1. Validitas Isi
Berdasarkan materi yang diujikan, yakni sistem periodik unsur kami membuat tiga puluh butir soal pilhan ganda. Sebagai alat untuk menunjang validitas isi maka dibuat kisi-kisi soal yang terlampir pada lampiran 1. menentukan atau mengetahui validitas isi maka dilakukan validitas konstruksi dengan cara meminta bantuan dosen pengampu, untuk menelaah apakah konsep materi yang diajukan telah memadai atau belum sebagai bahan tes uji.
2. Validitas Konstruksi
Kami menggantinya dengan “Unsur-unsur dalam satu golongan yaitu F, Cl, Br, dan I mempunyai sifat-sifat yang benar dari atas ke bawah, kecuali….
A.energi ionisasi makin kecil D.nomor massanya makin besar B.jari-jari atomnya semakin besar E.muatan intinya makin besar C.afinitas elektronnya makin besar
3. Validitas Bandingan
Berdasarkan hasil tes uji, didapatkan validitas dengan korelasi tidak signifikan nilai Γxy < Γtabel dimana nilainya sebesar 0,32 yang dihasilkan dari perbandingan nilai UTS dengan nilai soal uji. Sehingga disimpulkan validitas bandingan memiliki kriterium rendah, dan soal kurang dapat mengukur kemampuan siswa. Hal ini dikarenakan kurangnya kesiapan siswa dalam melaksanakan uji soal yang mana rentang waktu antara UTS dengan uji soal hanya 1 minggu. Akibatnya, banyak siswa yang merasa jenuh oleh ritme evaluasi pembelajaran secara berkala dalam waktu yang singkat.
4. Reliabilitas KR-20
Berdasarkan hasil tes uji, didapatkan koefisien reliabilitas pilihan ganda sebesar 0,72 yang menunjukan bahwa tes hasil belajar telah memiliki reliabilitas yang tinggi (reliable) dan dapat mengukur ketetapan soal pilihan ganda terhadap kemampuan siswa.
5. Validitas Item
Berdasarkan hasil tes uji, terdapat sebelas butir soal valid dan sembilan belas soal invalid. Banyaknya soal invalid menunjukkan bahwa butir soal tersebut belum mampu Pada soal nomor 15, Ibu Lilis meminta kami mengganti soal dikarenakan tingkat
kesukaran yang terlalu tinggi dan belum dipelajari sampai hubungan antara sistem periodik unsur dengan larutan. Soal tersebut berbunyi: “Unsur-unsur A,B, dan C terletak pada periode 3 sistem periodik. Oksida unsur A dalam air menghasilkan larutan yang mempunyai pH<7, sedangkan unsur B dengan air bereaksi menghasilkan gas hidrogen. Percobaan lain menunjukkan bahwa unsur C dapat bereaksi baik dengan larutan asam maupun basa. Susunan unsur-unsur tersebut dalam sistem periodik dari kiri ke kanan adalah …
memberikan ketepatan dalam mengukur kemampuan siswa. Berdasarkan materi yang diujikan, yakni sistem periodik unsur, kami menganalisa setiap soal secara kuantitatif dan kualitatif. Secara kuantitatif test tersebut memiliki Γ Tabel 0.34 yang dijadikan sebagai standart penentu apakah suatu soal tersebut dikatakan valid ataupun invalid. Selain itu, analisa ini juga dapat ditinjau dari segi kualitatif. Berdasarkan kesimpulan kelompok kami, 11 soal valid yang tersedia didalam tabel terdiri dari beberapa submateri, diantaranya sebagai berikut :
Konfigurasi elektron suatu unsur golongan A.
Sifat periodik unsur secara umum seperti jari-jari atom dalam satu golongan dan satu periode, kelektronegatifan atom dalam satu periode dan satu golongan.
Menentukan Proton, elektron, neutron.
Menghitung besarnya n,l,m,s yang sesuai dengan teori mekanika kuantum Mengelompokkan suatu unsur dalam satu golongan dan satu periode
berdasarkan kenaikan nomor atom
Kelompok kami juga menganalisis bagian-bagian dari materi Sistem Periodik Unsur didapatkan berdasarkan data Γ Tabel yang bersifat invalid, diantaranya sebagai berikut :
Konfigurasi elektron unsur golongan transisi Konfigurasi elektron unsur dalam bentuk ion
Menentukan pengisian orbital suatu unsur dalam bentuk ionnya. Menjelaskan teori-teori penyusunan Sistem Periodik Unsur
Mengaitkan sifat umum periodik unsur berdasarkan sifat dari masing-masing golongan
Menjelaskan secara teoritis submateri mekanika kuantum.
Menjelaskan sebab-akibat suatu unsur mengalami kestabilan duplet ataupun oktet.
6. Analisis Tingkat Kesukaran
dengan tingkat kesukaran sulit (10%). Hal ini tidak sesuai dengan proporsi tingkat kesukaran yang telah direncanakan. Berikut adalah presentasi tingkat kesukaran hasil tes uji.
Diagram 6.1. Presentasi Tingkat Kesukaran
Perbedaan hasil yang diperoleh dengan prediksi awal disebabkan oleh beberapa faktor, diantaranya :
1. Misunderstanding konsep Sistem Periodik Unsur karena adanya mutasi guru kimia ditengah proses pembelajaran pada materi ini.
2. Ketidaksesuaian dalam pemilihan bahasa sehingga soal yang dianggap sukar menjadi lebih mudah dipahami siswa.
3. Ketidaktepatan soal dengan aspek kognitif yang diprediksi di awal pembuatan soal.
7. Analisis Daya Pembeda
Untuk menganalisis daya pembeda, terlebih dahulu skor total disusun dari yang tertinggi hingga terendah. Diambil 17 testee sebagai kelompok atas (51%) dan 16 testee sebagai kelompok bawah (49%). Kemudian dihitung jumlah jawaban benar baik pada kelompok atas maupun kelompok bawah (terlampir). Variasi tingkat daya pembeda yang didapat dari perhitungan diantaranya sangat jelek, jelek dan baik. Berdasarkan tabel 4.2 sebanyak 15 butir soal masuk kedalam kategori sangat jelek, sebanyak 10 butir soal dalam kategori jelek dan 5 soal yang masuk kedalam kategori baik. Persentasi daya pembeda pada soal-soal tes uji yaitu 50% sangat jelek, 33% jelek dan 17% baik.
Berikut diagram presentase daya pembeda soal pilihan ganda.
Diagram 6.2 Presentase daya pembeda soal pilihan ganda
Jadi, sebanyak 83% soal pada tes pilihan ganda ini memiliki indeks daya pembeda yang jelek artinya soal tersebut tidak dapat membedakan antara testee yang menguasai materi dengan yang tidak. Hanya 17% soal yang mampu membedakan antara testee yang menguasai materi dengan yang tidak. Hal ini tidak sesuai dengan prediksi awal dimana soal sudah melalui tahap validasi sebanyak 2 kali oleh guru kimia yang bertanggungjawab di kelas X MIA 3. Validasi tersebut menghasilkan soal yang sudah disesuaikan dengan materi yang diajarkan sehingga meminimalisir adanya soal dengan daya pembeda yang jelek.
50%
33% 17%
Presentase Daya Pembeda
8. Distraktor
Setiap tes pilihan ganda memiliki satu pilihan benar dan pilihan yang lain merupakan pilihan yang salah. Pilihan salah inilah yang disebut distraktor yaitu pilihan yang dapat mengecoh peserta tes yang memang tidak mengetahui dengan tepat jawaban yang tersedia. Distraktor dapat berfungsi ketika dipilih minimal oleh 5% dari jumlah testee. Dimana pada uji soal ini diikuti oleh 33 peserta tes (testee) sehingga distraktor dapat berfungsi ketika dipilih minimal oleh 2 testee.
33 � 5
100= 1,65 ≈2
Analisis Distraktor
1. Pada soal nomor 1 merupakan soal untuk menentukan golongan dan periode dari �
17 35,5
yang mana jawaban benar adalah D. Golongan VII A Periode 3 dengan testee yang menjawab benar sebanyak 29. Pada soal ini diletakkan distraktor pada pilihan C. Golongan V A Periode 3 karena jika dilihat dari konfigurasi elektronnya 1 2 2 2 2�6 3 23�5 bagi siswa yang kurang paham dalam menentukan golongan ia akan mengira bahwa unsur tersebut terletak pada golongan V dilihat pada elektron sub kulit p akhir. Namun distraktor ini hanya dipilih oleh 1 testee sementara pada pilihan E. Golongan VIII A periode 3 terdapat 3 testee yang memilih. Hal tersebut kemungkinan karena mereka tidak mengetahui bagaimana konfigurasi elektronnya sehingga mereka menebak pilihan tersebut atau kemungkinan mereka tidak mengetahui cara menentukan golongan dengan benar sehingga mereka menjumlahkan angka 3 dan 5 pada sub kulit p.
2. Membahas tentang penentuan golongan dan periode dari suatu unsur Y yang diketahui jumlah elektron pada sub kulit s dan p, Y= [Ne] ↿ ↿⇂ ↿⇂ ↿
terkecoh dilihat dari 3 kolom elektron pada orbital p dengan 5 elektron yang mengisinya sehingga mereka mengira bahwa unsur tersebut terletak pada golongan IIIA periode 5.
3. Membahas sifat keperiodikan yaitu menentukan pilihan yang bukan sifat periodik unsur. 19 testee berhasil menjawab dengan benar pada pilihan E. Dari kiri ke kanan dalam satu periode titik didih semakin tinggi. Pada distractor A. Dari atas ke bawah dalam satu golongan energi ionisasi makin kecil, B. Dari kiri ke kanan dalam satu periode afinitas elektron makin besar, C. Dari atas ke bawah dalam satu golongan jari-jari atom semakin besar. Ke 3 distractor tersebut masing-masing dipilih oleh 7, 2 dan 5 testee. Pada soal ini meruapakan soal pengetahuan, dan siswa yang menjawab salah kemungkinan karena mereka tidak mengetahui dengan pasti sifat-sifat keperiodikan, atau bisa jadi mereka terkecoh karena kurang teliti dalam membaca soal sehingga jawaban yang merupakan sifat keperiodikan mereka pilih.
4. Membahas letak suatu unsur dan konfigurasi elektron pada 19X. Semua testee
menjawab dengan benar soal tersebut, yang berarti distractor pada soal ini sangat buruk sehingga testee tidak ada yang terkecoh untuk memilih distractor tersebut. Sehingga dapat dikatakan bahwa pada topik ini semua siswa telah mencapai standar kompetensi.
5. Membahas konfigurasi elektron pada suatu ion yaitu X2- pada unsur 16X . 22 testee
menjawab dengan benar pada pilihan C. 1 2 2 2 2�6 3 23�6. Sementara pada distractor A. 1 2 2 2 2�6 3 23�2 berhasil mengecoh 6 testee karena siswa berpikir bahwa ion 2- berarti unsur tersebut kekurangan 2 elektron sedangkan B. 1 2 2 2 2�6 3 23�4dipilih oleh 5 testee yang mana mereka tidak mengetahui perbedaan jumlah elektron pada unsur maupun ion.
7. Membahas unsur yang terletak dalam satu golongan yang terdiri dari unsur-unsur berikut : 12P, 16Q, 19R, 34S dan 53T. 29 testee menjawab dengan benar pada
pilihan D. Q dan S. Sedangkan pada distractor A. P dan Q, E. R dan T masing-masing dipiling oleh 1 testee. Pemilihan distractor ini karena unsur yang terletak dalam satu golongan sudah pasti memiliki kesamaan angka yaitu ganjil-ganji atau genap-genap sehingga testee memilih distractor tersebut walaupun distractor tersebut tidak berfungsi karena hanya dipilih oleh 1 testee.
8. Membahas konfigurasi elektron ion X2+ dengan nomor atom X adalah 27 dan pertanyaan ialah jumlah elektron yang tidak berpasangan dalam konfigurasi ion tersebut. 3 testee berhasil menjawab dengan benar pada pilihan C. 3 elektron tidak berpasangan. Distractor A. 1 dipilih oleh 10 testee karena mereka berfikir bahwa ion 2+ berarti nomor atom ditambahkan 2 yang berarti memiliki jumlah elektron 29 sehingga terdapat 1 elektron tunggal pada orbital d. Sedangkan pada distractor D. 5 tidak ada testee yang memilih padahal jika mereka mengetahui jumlah elektron dalan ion tersebut namun ada kekeliruan dalam susunan konfigurasinya (1 2 2 2 2�6 3 23�6 4 2 3 5) maka mereka akan menganggap bahwa elektron yang tidak berpasangan sebanyak 5 elektron. Namun distractor ini sangat tidak berfungsi karena tidak ada yang memilih. Sedangkan pada distractor E. 7 dipilih oleh 19 testee, hal ini dikarenakan mereka menganggap bahwa susunan konfigurasi elektron adalah 1 2 2 2 2�6 3 23�6 4 2 3 5 memiliki 7 elektron pada kulit terakhir s dan d dan mereka mengira elektron tersebut merupakan elektron tunggal.
10. Membahas jumlah proton, elektron dan neutron dalam suatu senyawa yang memiliki nomor atom 15 dan nomor massa 31 g/mol . 28 testee menjawab dengan benar pada pilihan C. Proton 15, elektron 15 dan neutron 16 . pada distractor A. P 15, e 15 dan n 31 dipilih oleh 3 testee karena menreka mengira bahwa neutron = nomor massa sedangkan pada distractor B. P 15, e 16 dan n 31 dipilih oleh 2 testee yang mana mereka mengira bahwa jumlah e diperoleh dari nomor massa – nomor atom dan jumlah neutron = nomor massa.
11. Membahas energi ionisasi dalam tabel periodik unsur. Bagaimana sifatnya dalam satu periodik dari kiri ke kanan. 22 testee menjawab dengan benar pilihan B. Cendrung naik. Distractor C. Cenderung turun dipilih oleh 8 testee dan distractor D. Dipilih oleh 2 testee . pertanyaan ini merupakan tipe soal pengetahuan sehingga siswa yang menjawab salah berarti mereka memang tidak mengetahui dengan pasti sifat energi ionisasi.
14. Membahas penyebab kecendrungan melepas elektron pada unsur logam dari atas ke bawah dalam tabel periodik. 6 testee menjawab dengan benar pada pilihan B. Jari-jari atomnya makin besar. Sedangkan pada distractor A. Energi ionisasi makin besar dipilih oleh 16 testee. Hal tersebut dikarenakan mereka berpikir bahwa elektron mudah terlepas karena adanya energi yang besar. Sementara energi ionisasi merupakan energi yang diperlukan untuk melepaskan elektron yang terletak pada kulit terluar, sehingga adanya kecendrungan elektron terlepas berarti energi yang dibutuhkan untuk melepaskan elektron semakin kecil.
B. Analisis Tes Uraian 1. Validitas Isi
Berdasarkan materi yang diujikan, yakni sistem periodik unsur kami membuat lima butir soal uraian. Sebagai alat untuk menunjang validitas isi maka dibuat kisi-kisi soal yang terlampir pada lampiran 1. Dalam menentukan atau mengetahui validitas isi maka dilakukan validitas konstruksi dengan cara meminta bantuan dosen pengampu, untuk menelaah apakah konsep materi yang diajukan telah memadai atau belum sebagai bahan tes uji.
2. Validitas Konstruksi
Berdasarkan evaluasi dari dosen pengampu, terdapat 3 soal yang tidak sesuai, terlihat pada lampiran 1 dengan kriteria dan perlu direvisi atau diperbaiki. Soal-soal tersebut diantaranya adalah :
Soal nomor 2 yaitu “Jelaskan apa yang dimaksud dengan: a. Jari-jari atom, b. Keelektronegatifan. c. Afinitas Elektron.”. Soal ini diganti karena tidak sesuai dengan tingkat pemahaman dalam soal uraian.
b. Satu periode dari kiri kekanan makin kecil
Soal nomor 3 yaitu “Bagaimana Niels Bohr mampu menjelaskan bahwa orbital unsur hidrogen bersifat kontinyu? Uraikan jawabanmu!”. Soal ini diganti karena terlalu sulit untuk tingkat 1 SMA dan tidak sesuai dengan kompetensi dasar.
Kami menggantinya dengan “Mengapa dalam sistem periodik unsur, golongan VIIIA merupakan golongan unsur-unsur yang stabil? Jelaskan !”
Soal nomor 4a, yaitu “Berikut ini adalah konfigurasi elektron beberapa unsur :
16X : 1s2 2s2 2p6 3s2 3p4
18Y : 1s2 2s2 2p6 3s2 3p6
11Z : 1s2 2s2 2p6 3s1
Berdasarkan konfigurasi elektron tersebut, tentukan :
a. letak masing-masing unsur dalam tabel periodik unsur
Soal ini diganti karena penggunaan bahasa yang kurang jelas. Kami menggantinya dengan “ a. golongan dan perioda masing-masing unsur”
3. Reliabilitas Tes Uraian
Berdasarkan ketetapan data dengan kondisi fakta test tersebut dalam suatu kelas observer, dapat dijelaskan bahwa test tersebut akan dilakukan analisa dari segi kualitatif maupun kuantitatif. Berdasarkan data pada tes tersebut, kami membandingkan data kuantitatif dengan kualitatif soal yang diberikan kepada testee. Secara kualitatif, dapat dismpulkan bahwa soal yang kami berikan sebagai alat observer memiliki pemilihan diksi yang sederhana serta keluwesan dalam pemilihan bahasa, selain itu tidak pleonasme dalam pemilihan kata-kata, sehingga dapat disimpulkan bahwa soal tersebut sangat mudah untuk dicerna serta dipahami oleh siswa. Dalam segi kualitatif, kelompok kami mampu mengorganisasikan sub-materi Sistem Periodik Unsur dikelas X MIA 3. Pengorganisasian ini didapatkan dari hasil konkret berdasarkan standart penilaian kelompok yang telah kami diskusikan bersama serta dikorelasi dengan pokok jawaban yang diberikan oleh siswa terhadap materi yang tertera didalam soal. Kelompok kami dapat menyimpulkan beberapa sub materi yang diorganisasikan menjadi 4 bagian, yaitu : sangat dipahami, dipahami, kurang dipahami dan yang sangat kurang untuk dipahami oleh siswa.
VI.
KESIMPULAN
1. Berdasarkan validitas konstruksi, terdapat 1 soal PG dan 3 soal uraian yang tidak sesuai.
2. Dalam soal pilihan ganda:
a. Soal memiliki nilai validitas bandingan sebesar 0,32. Korelasi signifikan dengan kriterium rendah.
b. Soal yang diujikan memiliki validitas item yang valid sebanyak 11 soal dan 19 soal invalid.
c. Terdapat 12 soal mudah, 15 soal sedang dan 3 soal sukar.
d. Berdasarkan perhitungan KR-20 soal Pilihan Ganda memiliki nilai reliabilitas sebesar 0,72 dengan kriteria baik (reliable).
e. Persentase tingkat kesukaran soal, mudah sebesar 40%, sedang 50% dan sukar 10%.
f. Daya pembeda soal memiliki presentase 17% baik, dan 83% jelek. g. Soal tidak dapat membedakan antara testee yang menguasai materi
dengan yang tidak menguasai.
3. Dalam soal uraian:
a. Soal memiliki reliabilitas rendah sebesar 0,35.
LAMPIRAN
Lampiran 1. Validitas Isi, Konstruksi dan Hasil Revisi Lampiran 2. Validitas Item dan Reliabilitas KR-20 Lampiran 3. Reliabilitas Uraian
Lampiran 1. Validitas Isi, Konstruksi dan Hasil Revisi
ASPEK KOGNITIF VALIDASI KETERANGAN YA TIDAK
1 Dua buah unsur memiliki notasi
27
13X dan 35,517Y. Unsur Y dalam
sistem periodik terletak pada ... A. golongan IV B, periode 5 B. golongan VIII B, periode 4 C. golongan V A, periode 3 D. golongan VII A, periode 3 E. golongan VIII A, periode 3
Mudah C2 : Pemahaman V
2 Diagram orbital 2 buah unsur sebagai berikut:
3 Manakah di antara penyataan di bawah ini yang bukan merupakan sifat periodik unsur-unsur… A. Dari atas ke bawah dalam satu
golongan energi ionisasi makin kecil.
B. Dari kiri ke kanan dalam satu periode afinitas elektron makin besar.
C. Dari atas ke bawah dalam satu golongan jari-jari atom makin besar.
D. Dari kiri ke kanan dalam satu periode keelektronegatifan makin besar.
E. Dari kiri ke kanan dalam satu periode titik didih makin tinggi.
Sedang C2 : Pemahaman V
4 Letak unsur dan konfigurasi elektron yang tepat untuk unsur 19X adalah...
A.Periode 4, golongan IA, [Ar] 4s1 B. Periode 1, golongan IB, [Ar] 4d1 C. Periode 1, golongan IIA, [Ar] 4s2 D. Periode 2, golongan IIB, [Ar] 4d2 E. Periode 3, golongan IVA, [Ar]
5 Konfigurasi elektron X
dari suatu unsur 16X adalah ...
A. 1s2 2s2 2p6 3s2 3p2 B. 1s2 2s2 2p6 3s2 3p4 C. 1s2 2s2 2p6 3s2 3p6 D. 1s2 2s2 2p6 3s2 3p6 3d2 E. 1s2 2s2 2p6 3s2 3p2 3d2
Sedang C2 : Pemahaman V
6 Konfigurasi elektron dari unsur X adalah
1s2 2s22p6 3s23p64s23d104p6 5s24d105 p3. Unsur tersebut terletak pada ...
A. golongan IIIA periode 5 B. golongan VA periode 5 C. golongan VA periode 3 D. golongan IIIA periode 4 E. golongan VIA periode 5
Mudah C2 : Pemahaman V
7 Di antara
unsur-unsur 12P, 16Q, 19R, 34S, dan 53T
yang terletak pada golongan yang sama dalam sistem periodik unsur adalah ...
A. P dan Q D. Q dan S B. S dan T E. R dan T C. P dan R
Mudah C2 : Pemahaman V
27. Jumlah elektron tidak
berpasangan dalam ion X+2 adalah ...
A. 1 B. 2 C. 3 D. 5 E. 7 9 Letak unsur X dengan nomor atom
26 dan nomor massa 56 dalam sistem periodik unsur terletak pada golongan dan periode ...
A. IIA dan 6 B. VIB dan 3 C. VIB dan 4 D. VIIIB dan 3 E. VIIIB dan 4
Sedang C2 : Pemahaman V
10 Atom X memiliki nomor atom 15 dan massa atom relatif 31
gram/mol . jumlah proton, elektron dan neutron berturut-turut adalah ... A. Proton : 15 Elektron: 15 Neutron: 31 B. Proton : 15 Elektron: 16 Neutron: 31 C. Proton : 15 Elektron: 15 Neutron: 16 D. Proton : 15 Elektron: 16 Neutron: 15 E. Proton : 15 Elektron: 31 Neutron: 16
Mudah C2 : Pemahaman V
12 Lima unsur A,B,C,D dan E masing-masing mempunyai susunan
a. 1s2 2s2 2p6 3s1 b. 1s2 2s2 2p6 3s2 c. 1s2 2s2 2p6 3s2 3p1
d. 1s2 2s2 2p6 3s2 3p6 3d10 4s1 e. 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p65s1 pasangan-pasangan di bawah ini yang merupakan unsur dari satu golongan yang sama adalah … A. a dan b D. d dan e B. a dan c E. a dan d C. a dan e
16 Konfigurasi atom 24Cr adalah…
A.1s2 2s2 2p6 3s2 3p6 4s2 3d4 B. 1s2 2s2 2p6 3s2 3p6 4s2 4p4 C.1s2 2s2 2p6 3s2 3p6 4s1 3d5 D.1s2 2s2 2p6 3s2 3p6 3d6 E. 1s2 2s2 2p6 3s2 3p6
Sedang C2 : Pemahaman V
17 Suatu unsur netral memiliki 2 elektron dalam kulit pertama, 8 elektron dalam kulit kedua, dan 7 elektron dalam kulit ketiga. Jumlah total elektron dalam orbital s adalah…
A. 6 B. 4
C. 17 D. 8 E. 7 19 Ion X2+
memiliki konfigurasi electron 1s2 2s2 2p6. Nilai keempat bilangan kuantum elektron valensi atom X2+ adalah …
A. n= 2, l= 0 m= 0 s= -1/2 B. n= 2, l= 1 m= +1 s= -1/2 C. n= 3, l= 0 m= 0 s= -1/2 D. n= 3, l= 1 m= -1 s= +1/2 E. n= 3, l= 1 m= 0 s= +1/2
Mudah C2 : Pemahaman V
20 Konfigurasi elektron suatu atom unsur sebagai berikut.
1s2 2s2 2p6 3s2 3P6 3d10 4s2 4p6 4d7 5s2. Unsur tersebut terletak pada golongan dan periode…
A. IIA/5 B. VA/7 C. VIIA/5 D. IIB/7 E. VIIIB/5
Sukar C2 : Pemahaman V
21 Orbital yang menempati elektron valensi unsur 23Mn adalah…
B. 3d C. 3d dan 4s D. 3p dan 3d E. 2s dan 3p
22 Konfigurasi elektron atom unsur A: 2 8 8 6. Unsur tersebut dalam sistem periodik terletak pada ....
A. golongan IA dan periode B. golongan IIA dan periode 4 C. golongan IVA periode 6 D. golongan VIA periode 4 E. golongan IVA periode 4
Sedang C2 : Penerapan V
25 Di antara unsur-unsur: 4P, 12Q, 16R, dan 18S, yang terletak dalam
golongan yang sama adalah .... A. P dan Q
B. P dan S C.P dan R D.Q dan R E. R dan S
Mudah C3 : Penerapan V
28 Anion S2–
memiliki konfigurasi elektron 2, 8, 8, atom unsur tersebut terletak pada golongan ….
A.IIA periode 8 B. IIIA periode 8
C.VIA periode 2 D.VIA periode 3 E. VIIIA periode 3
29 Apabila x dan y adalah pasangan unsur yang mempunyai elektron valensi sama, maka nomor atom x dan y adalah ….
besar.
Bagaimana Niels Bohr mampu menjelaskan bahwa orbital unsur
11 Kesimpulan yang benar tentang energi ionisasi dalam satu periode dari kiri ke kanan adalah … A.Tetap
13 Unsur X dengan konfigurasi elektron 1s2 2s2 2p6 3s1 mempunyai sifat …
A. mempunyai potensial ionisasi terbesar di antara unsur seperioda B. dapat membentuk oksida dengan
rumus XO2
C. dapat membentuk hidroksida yang sukar larut dalam air
D. dapat membentuk senyawa halida dengan klor dengan rumus XCl E. mempunyai jari-jari terkecil di antara unsur seperioda
14 Atom-atom unsur logam dalam satu golongan dari atas ke bawah
kecenderungan melepaskan elektron valensinya makin besar sebab… A. potensial ionisasinya makin besar B. jari-jari atomnya makin besar
C. afinitas elektronnya makin besar D. nomor massanya makin besar E. muatan intinya makin besar
Sedang C3 : Penerapan V
15 Unsur-unsur A,B, dan C terletak
pada periode 3 sistem periodik.
Oksida unsur A dalam air
menghasilkan larutan yang
mempunyai pH<7, sedangkan unsur
B dengan air bereaksi
menghasilkan gas hidrogen.
Percobaan lain menunjukkan bahwa
larutan asam maupun basa. Susunan
unsur-unsur tersebut dalam sistem periodik dari kiri ke kanan adalah … A. A,C,B D. A,B,C
18 Bilangan Kuantum magnetik menunjukan pernyataan bahwa …
A. Arah ruang orbital B. Tingkat energi kulit C. Subtingkat energi elektron D. Perbedaan arah rotasi elektron E. Kebolehjadian menemukan
elektron
Sukar C1 : Pengetahuan V
23 Unsur dengan nomor atom 15 memiliki sifat kimia sama dengan unsur bernomor atom... elektron. Atom unsur lain yang
sifatnya mirip adalah atom dengan nomor atom ....
A.10 B. 24 C.34 D.50 E. 64
26 Pernyataan berikut merupakan sifat-sifat gas mulia, kecuali ..
A. unsur paling stabil B. sukar melepaskan atau menangkap elektron
C. mudah bereaksi dengan unsur lain
D. terdapat di atmosfer dalam keadaan bebas
E. titik beku mendekati suhu 0 K
Sedang C2 : Pemahaman V
27 Pernyataan yang benar untuk unsur A dan B yang memiliki nomor atom 10 dan 18 adalah ….
A. jari-jari atom A > B B. jari-jari atom A = B C. A dan B terletak periode 3 D. A dan B satu golongan
4 (Esay)
Berikut ini adalah konfigurasi elektron beberapa unsur :
16X : 1s2 2s2 2p6 3s2 3p4 18Y : 1s2 2s2 2p6 3s2 3p6 11Z : 1s2 2s2 2p6 3s1
Berdasarkan konfigurasi elektron tersebut, tentukan :
a. letak masing-masing unsur
dalam tabel periodik unsur b. urutan afinitas elektron dan
keelektronegatifan dari tertinggi hingga terendah
C3 : Penerapan V Soal diganti dengan : a. golongan dan
perioda masing-masing unsur
5 (Esay)
Tentukan golongan dan periode atom X dan Y berdasarkan
konfigurasi elektron ion-ion berikut: X+ : 1s2 2s2 2p6 3s1
Y- : 1s2 2s2 2p6 3s2 3p5
44 Lampiran 5. Soal
SOAL SMA NEGERI 21 JAKARTA
MATA PELAJARAN : KIMIA
KELAS/SEMESTER : X MIA 3 / 1
MATERI POKOK : SISTEM PERIODIK UNSUR
WAKTU : 100 MENIT
PETUNJUK
PENGERJAAN SOAL:
1. Tulis nama dan kelas dengan jelas pada lembar jawaban 2. Periksa lembar soal sebelum mengerjakan soal
3. Soal berjumlah 35 yang terdiri dari 30 soal PG dan 5 soal uraian 4. Berilah tanda silang (x) untuk soal pilihan ganda pada lembar jawaban 5. Jawab soal uraian dengan benar dan jelas pada lembar jawaban
6. Periksa jawaban anda sebelum dikumpulkan
Pilihlah satu jawaban yang paling tepat di antara jawaban a, b, c, d, atau e!
1. Dua buah unsur memiliki notasi 2713X dan 35,517Y. Unsur Y dalam sistem periodik
terletak pada ...
A. golongan IV B, periode 5 B. golongan VIII B, periode 4 C. golongan V A, periode 3 D. golongan VII A, periode 3 E. golongan VIII A, periode 3
2. Diagram orbital 2 buah unsur sebagai berikut:
Letak unsur Y dalam tabel periodik terdapat pada golongan dan periode secara berurutan ...
3. Manakah di antara penyataan di bawah ini yang bukan merupakan sifat periodik unsur-unsur …
A. Dari atas ke bawah dalam satu golongan energi ionisasi makin kecil. B. Dari kiri ke kanan dalam satu periode afinitas elektron makin besar. C. Dari atas ke bawah dalam satu golongan jari-jari atom makin besar. D. Dari kiri ke kanan dalam satu periode keelektronegatifan makin besar. E. Dari kiri ke kanan dalam satu periode titik didih makin tinggi.
4. Letak unsur dan konfigurasi elektron yang tepat untuk unsur 19X adalah ... A.Periode 4, golongan IA, [Ar] 4s1
B. Periode 1, golongan IB, [Ar] 4d1 C. Periode 1, golongan IIA, [Ar] 4s2 D. Periode 2, golongan IIB, [Ar] 4d2 E. Periode 3, golongan IVA, [Ar] 4s2 3d2
5. Konfigurasi elektron X2- dari suatu unsur 16X adalah ...
A. 1s2 2s2 2p6 3s2 3p2 Unsur tersebut terletak pada ...
A. golongan IIIA periode 5 B. golongan VA periode 5 C. golongan VA periode 3 D. golongan IIIA periode 4 E. golongan VIA periode 5
7. Di antara unsur-unsur 12P, 16Q, 19R, 34S, dan 53T yang terletak pada golongan yang sama dalam sistem periodik unsur adalah ...
A. P dan Q C. P dan R E. R dan T B. S dan T D. Q dan S
8. Nomor atom unsur X sama dengan 27. Jumlah elektron tidak berpasangan dalam ion X+2 adalah ...
A. 1 B. 2 C. 3 D. 5 E. 7
9. Letak unsur X dengan nomor atom 26 dan nomor massa 56 dalam sistem periodik unsur terletak pada golongan dan periode ...
46
11.Kesimpulan yang benar tentang energi ionisasi dalam satu periode dari kiri ke kanan adalah …
12.Lima unsur A,B,C,D dan E masing-masing mempunyai susunan elektron sebagai berikut:
pasangan-pasangan di bawah ini yang merupakan unsur dari satu golongan yang sama
adalah …
A. a dan b C. a dan e E. a dan d B. a dan c D. d dan e
13.Unsur X dengan konfigurasi elektron 1s2 2s2 2p6 3s1 mempunyai sifat … A. mempunyai potensial ionisasi terbesar di antara unsur seperioda B. dapat membentuk oksida dengan rumus XO2
C. dapat membentuk hidroksida yang sukar larut dalam air
D. dapat membentuk senyawa halida dengan klor dengan rumus XCl E. mempunyai jari-jari terkecil di antara unsur seperioda
14.Atom-atom unsur logam dalam satu golongan dari atas ke bawah kecenderungan melepaskan elektron valensinya makin besar sebab…
A. potensial ionisasinya makin besar D. nomor massanya makin besar B. jari-jari atomnya makin besar E. muatan intinya makin besar C. afinitas elektronnya makin besar
15.Unsur-unsur dalam satu golongan yaitu F, Cl, Br, dan I mempunyai sifat-sifat yang benar dari atas ke bawah, kecuali….
16. Konfigurasi atom 24Cr adalah…
17. Suatu unsur netral memiliki 2 elektron dalam kulit pertama, 8 elektron dalam kulit kedua, dan 7 elektron dalam kulit ketiga. Jumlah total elektron dalam orbital s adalah…
18. Bilangan Kuantum magnetik menunjukan pernyataan bahwa … A.Arah ruang orbital kuantum elektron valensi atom X2+ adalah …
A.n= 2, l= 0 m= 0 s= -1/2 B.n= 2, l= 1 m= +1 s= -1/2 C.n= 3, l= 0 m= 0 s= -1/2 D.n= 3, l= 1 m= -1 s= +1/2 E.n= 3, l= 1 m= 0 s= +1/2
20. Konfigurasi elektron suatu atom unsur sebagai berikut.
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d7 5s2. Unsur tersebut terletak pada golongan dan
21. Orbital yang menempati electron valensi unsur 23Mn adalah…
A.4s B.3d
48 22. Konfigurasi elektron atom unsur A: 2 8 8 6. Unsur tersebut dalam sistem periodik
terletak pada ....
A. golongan IA dan periode B. golongan IIA dan periode 4 C. golongan IVA periode 6 D. golongan VIA periode 4 E. golongan IVA periode 4
23. Unsur dengan nomor atom 15 memiliki sifat kimia sama dengan unsur bernomor atom...
24. Atom suatu unsur memiliki 16 elektron. Atom unsur lain yang sifatnya mirip adalah atom dengan nomor atom ....
A.10
26. Pernyataan berikut merupakan sifat-sifat gas mulia, kecuali .. A. unsur paling stabil
B. sukar melepaskan atau menangkap elektron C. mudah bereaksi dengan unsur lain
D. terdapat di atmosfer dalam keadaan bebas E. titik beku mendekati suhu 0 K
27. Pernyataan yang benar untuk unsur A dan B yang memiliki nomor atom 10 dan 18 adalah ….
A. jari-jari atom A > B B. jari-jari atom A = B C. A dan B terletak periode 3 D. A dan B satu golongan E. terletak pada golongan VIIA
28. Anion S2– memiliki konfigurasi elektron 2, 8, 8, atom unsur tersebut terletak pada golongan ….
C.VIA periode 2 D.VIA periode 3 E.VIIIA periode 3
29. Apabila x dan y adalah pasangan unsur yang mempunyai elektron valensi sama, maka nomor atom x dan y adalah ….
30. Pasangan unsur yang terletak pada dalam sistem periodik adalah… A. 15P ; 19K D. 11Na ; 4Be
B. 13Al ; 3Li E. 6C ; 14Si
C. 15P ; 4Be
ESSAY
1. Jelaskan pengelompokan unsur menurut Dobereiner, dan berikan contohnya ! 2. Mengapa jari-jari atom dalam:
a. Satu golongan dari atas kebawah makin besar.
b. Satu periode dari kiri kekanan makin kecil.
3. Mengapa dalam sistem periodik unsur, golongan VIIIA merupakan golongan unsur-unsur yang stabil? Jelaskan !
4. Berikut ini adalah konfigurasi elektron beberapa unsur : 16X : 1s2 2s2 2p6 3s2 3p4
18Y : 1s2 2s2 2p6 3s2 3p6 11Z : 1s2 2s2 2p6 3s1
Berdasarkan konfigurasi elektron tersebut, tentukan : a. golongan dan perioda masing-masing unsur
b. urutan afinitas elektron dan keelektronegatifan dari tertinggi hingga terendah 5. Tentukan golongan dan periode atom X dan Y berdasarkan konfigurasi elektron
ion-ion berikut :