4 BAB II. TINJAUAN PU STA KA
TINJAUAN PUSTAKA A. Nyeri
1. Definisi
Nyeri merupakan gejala utama yang paling sering membuat seseorang mencari pertolongan dokter. Nyeri adalah rasa tidak menyenangkan, umumnya karena adanya perlukaan dalam tubuh, walaupun tidak sebatas itu. Nyeri dapat juga dianggap sebagai racun dalam tubuh, karena nyeri yang terjadi akibat adanya kerusakan jaringan atau saraf akan mengeluarkan berbagai mediator seperti H+, K+, ATP, prostaglandin, bradikinin, serotonin, substansia P, histamin dan sitokain.
Mediator kimiawi inilah yang menyebabkan rasa tidak nyaman dan karenanya mediator-meditor ini disebut sebagai mediator nyeri (Tanra, 2017).
International Association of the Study of Pain (IASP) mendefinisikan nyeri sebagai “an unpleasant sensory and emotional experience associated with actual or potential tissue damage or described in term of such damage”. Nyeri adalah rasa indrawi dan pengalaman emosional yang tidak menyenangkan akibat adanya kerusakan jaringan yang nyata atau berpotensi rusak atau tergambarkan seperti adanya kerusakan jaringan. Dari definisi ini dapat ditarik beberapa kesimpulan antara lain (Tanra, 2017):
Nyeri merupakan rasa indrawi yang tidak menyenangkan. Keluhan tanpa unsur tidak menyenangkan, tidak dapat dikategorikan sebagai nyeri.
Nyeri selain merupakan rasa indrawi (fisik) juga merupakan pengalaman emosional (psikologik) yang melibatkan efeksi jadi suatu nyeri mengandung paling sedikit dua dimensi yakni dimensi pisik dan psikologis.
commit to user
Nyeri terjadi sebagai akibat adanya kerusakan jaringan yang nyata, disebut sebagai nyeri nosiseptif atau nyeri akut.
Nyeri juga dapat timbul akibat adanya rangsangan yang berpotensi rusak, dan disebut sebagai nyeri fisiologis, misalnya cubitan atau terkena api rokok, hal itu akan membangkitkan refleks menghindar.
Selain itu nyeri dapat juga terjadi tanpa adanya kerusakan jaringan yang nyata, tapi penderita menggambarkannya sebagai suatu pengalaman seperti itu, hal ini disebut sebagai nyeri kronik.
2. Jalur Nyeri
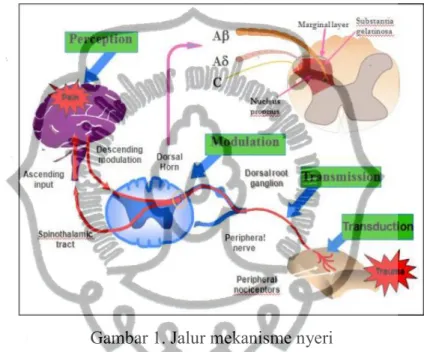
Kunci penatalaksanaan nyeri akut secara optimal adalah pemahaman mengenai anatomi lintasan nyeri dan mediator kimia yang terlibat dalam suatu rangsang noksius dan persepsi nyeri. Terdapat 5 peristiwa eletrofisiologik yang jelas antara suatu rangsang noksius sampai dirasakannya nyeri yakni transduksi, konduksi, modulasi, transmisi dan persepsi. Proses transduksi adalah rangsang noksius dapat berasal dari bahan kimia, seperti yang terjadi pada proses inflamasi yang menimbulkan sensitisasi dan mengaktifasi reseptor nyeri. Bisa juga diartikan sebagai pengubahan berbagai stimuli oleh reseptor menjadi impuls listrik yang mampu menimbulkan potensial aksi akhiran saraf. Selanjutnya proses transmisi adalah penyaluran impuls saraf sensorik dilakukan oleh serabut A delta bermyelin dan serabut C tak bermyelin sebagai neuron pertama, kemudian dilanjutkan traktus spinothalamikus sebagai neuron kedua dan selanjutnya di daerah thalamus disalurkan sebagai neuron ketiga sensorik pada area somatik primer di korteks serebri (Suwondo, 2017).
Modulasi adalah proses interaksi antara sistem analgesik endogen dengan input nyeri yang masuk di kornu posterior medulla spinalis. Proses modulasi tersebut terjadi ketika aktivasi nyeri dapat dihambat oleh analgesik endogen seperti endorphine, sistem inhibisi sentral serotonin dan noradrenalin, dan aktivitas serabut A beta.commit to user Sedangkan proses persepsi
merupakan hasil akhir proses interaksi yang kompleks, dimulai dari proses transduksi, transmisi, dan modulasi sepanjang aktivasi sensorik yang sampai pada area primer sensorik korteks serebri dan masukan lain bagian otak yang pada gilirannya menghasilkan suatu perasaan subyektif yang dikenal sebagai persepsi nyeri atau disebut dengan kesadaran akan adanya nyeri (Suwondo, 2017).
Gambar 1. Jalur mekanisme nyeri
(Yam, 2018. General Pathway of Pain Sensations and The Major Neurotransmitters Involved in Pain Regulation.)
3. Pengukuran Tingkat Nyeri
Ada beberapa cara untuk membantu mengetahui tingkat nyeri menggunakan skala assessment nyeri unidimensional (tunggal) atau multidimensi. Assessment nyeri unidimensional bersifat hanya mengukur intensitas nyeri, sesuai untuk nyeri akut, serta merupakan skala yang biasa digunakan untuk evaluasi pemberian analgetik. Visual Analog Scale (VAS) adalah cara yang paling banyak digunakan untuk menilai nyeri.
Gradasi tingkat nyeri yang mungkin dialami seorang pasien digambarkan secara visual melalui skala linier. Rentang nyeri diwakili sebagai garis sepanjang 10 cm, dengan atau tanpa tanda pada tiap sentimeter. Kemudian pada kedua ujung garis tersebut diberikan tanda berupa angka atau commit to user
pernyataan deskriptif. Ujung yang satu mewakili tidak ada nyeri, sedangkan ujung yang lain mewakili rasa nyeri terparah yang mungkin terjadi. Skala dapat dibuat vertikal atau horizontal. VAS juga dapat diadaptasi menjadi skala hilangnya/reda rasa nyeri. Skala ini dapat digunakan pada pasien anak >8 tahun dan dewasa. Manfaat utama VAS adalah penggunaannya sangat mudah dan sederhana (Suwondo, 2017).
Dalam sebuah penelitian, pasien diminta untuk mengukur nyeri yang dapat diterima serta yang tidak dapat diterima. Nyeri yang tidak dapat diterima berhubungan dengan skor VAS median 75 mm (kisaran, 40-100 mm). Kata-kata “nyeri sedang” dan “sakit parah” berhubungan dengan skor VAS median masing-masing 49 dan 91 mm. Selanjutnya, dalam studi nyeri pasca operasi, analgesik diperlukan secara subyektif pada intensitas nyeri (median) antara sekitar 50 dan 70 mm pada VAS 100 mm. Jika data ini diterapkan, nyeri yang tidak dapat diterima akan sesuai dengan kebutuhan untuk analgesik dan peringkat intensitas verbal antara "nyeri sedang" dan "nyeri parah” (Wahglen dan Quiding, 2000).
Gambar 2. Visual Analog Scale (Suwondo, 2017. Buku Ajar Nyeri)
Numeric Rating Scale (NRS) adalah skala lain yang dapat digunakan untuk menilai tingkat nyeri. Skala ini menggunakan rentang angka 1 - 10 untuk menilai tingkat nyeri yang dialami seseorang. Skala ini dianggap sederhana dan mudah dimengerti, serta lebih baik daripada VAS terutama untuk menilai nyeri akut. Namun, kekurangannya adalah keterbatasan pilihan kata untuk menggambarkan rasa nyeri, tidak memungkinkan untuk membedakan tingkat nyeri dengan lebih teliti dan dianggap terdapat jarak yang sama antar kata yang menggambarkan efek analgesic (Suwondo,
2017). commit to user
Gambar 3. Numeric Rating Scale (Suwondo, 2017. Buku Ajar Nyeri)
Pada pasien dewasa dan anak diatas usia 3 tahun yang tidak dapat menggambarkan intensitas nyerinya dengan angka, dapat digunakan Wong Baker Pain Rating Scale untuk menilai tingkat nyeri.
Gambar 4. Wong Baker Pain Rating Scale (Suwondo, 2017. Buku Ajar Nyeri)
4. Modulasi Manajemen Nyeri a. Analgesia Preemptif
Hiperalgesia merupakan gejala umum pada nyeri pascabedah, yakni suatu rangsang kuat yang normal terasa sakit, kini dirasakan lebih sakit dan allodinia, yakni suatu rangsang lemah yang normal tidak terasa sakit, kini terasa sakit. Pembedahan membuat terjadinya sensitisasi sentral dan perifer sehingga kedua gejala tersebut merupakan konsekuensi yang terjadi. Atas dasar itu maka prinsip dasar pengelolaan nyeri pascabedah adalah mencegah atau meminimalisasi terjadinya sensitisasi perifer maupun sensitisasi sentral yang dikenal sebagai plastisitas susunan saraf (plasticity of the nervous system). Sedangkan jika telah terjadi plastisitas susunan saraf, artinya sudah ditemukan adanya gejala hiperalgesia dan allodinia maka harus diberikan anti-commit to user
hiperalgesia dan anti-allodinia (misalnya ketamin) untuk mengembalikan fungsi saraf kembali normal. Istilah analgesia preemptif dan analgesia preventif muncul dari prinsip ini dengan tujuan mencegah atau memimalisir terjadinya sensitisasi sentral (Meliana, 2017).
Definisi analgesia preemptif adalah terapi antinosiseptif yang dimulai sebelum pembedahan. Dengan teknik ini diharapkan lebih efektif menghilangkan nyeri akut pascabedah dibandingkan dengan manajemen nyeri yang sama yang dilakukan pascabedah. Namun dari 80 RCT yang melibatkan 3761 pasien yang dipublikasi dari tahun 1983 – 2000 dengan menggunakan berbagai macam obat, misalnya NSAID, Epidural Analgesia, Infiltrasi dengan Lokal Anastetik, Analgesik Opioid dan Ketamin sebagai analgesia preemtif disimpulkan bahwa tak ada perbedaan yang bermakna antara intensitas nyeri setelah pemberian analgesia preemtif dibandingkan dengan pemberian obat pasca insisi atau pascabedah. Ini menunjukkan bahwa analgesia preemtif tidak lebih efektif dibandingkan dengan pemberian analgesia pascabedah (post insisinal treatment). Inilah yang membuat para ilmuwan berupaya mengetahui letak ketidakefektifan analgesia preemtif tersebut.
Akhirnya ditemukan bahwa analgesia preemptif bukan hanya terletak pada waktu pemberian (sebelum atau sesudah pembedahan) tetapi yang terpenting adalah durasi dari analgesia preemptif yang harus mencakup tidak saja fase kerusakan jaringan tetapi juga fase proses inflamasi, serta adanya blok nosiseptif yang komplit selama kedua fase tersebut (Meliana, 2017).
b. Analgesia Preventif
Dewasa ini konsep analgesia preemptif mengalami perubahan bukan lagi dititik beratkan pada mencegah input afferen nosiseptif sampai pada nyeri insisi saja tapi harus lebih dari itu. Untuk mendapatkan pengertian yang benar muncullah istilah analgesia commit to user
preventif, yang menekankan pada kenyataan bahwa terjadinya plastisisitas susunan syaraf yang di induksi oleh input nosiseptif mulai dari pre, intra dan pascabedah. Jadi tujuan utama analgesia preventif yakni mengurangi sensitisasi sentral yang muncul dari input nosiseptif selama keseluruhan periode perioperatif dan bukan hanya sampai selama insisi pembedahan. Dengan kata lain analgesia preventif adalah analgesia preemtif yang lebih luas meliputi pre-intra dan pascabedah (Meliana, 2017).
Yang perlu harus diingat bahwa dalam aplikasi klinik analgesia preventif, seyogyanya kitapun menggunakan analgesia multimodal yang menggunakan kombinasi dua obat atau lebih, dimana salah satu obat akan menekan sensitisasi perifer misalnya NSAID, utamanya yang selektif (celebrex atau precoxib) dan satu lagi yang menekan sensitisasi sentral misalnya opioid (morfin, pethidin atau fentanyl) utamanya epidural atau blok saraf. Dengan teknik preventif multimodal analgesia ini akan diperoleh selain analgesia yang optimal juga dapat mencegah terjadinya nyeri kronik pascabedah (Meliana, 2017).
B. Epidural Anestesi 1. Anatomi
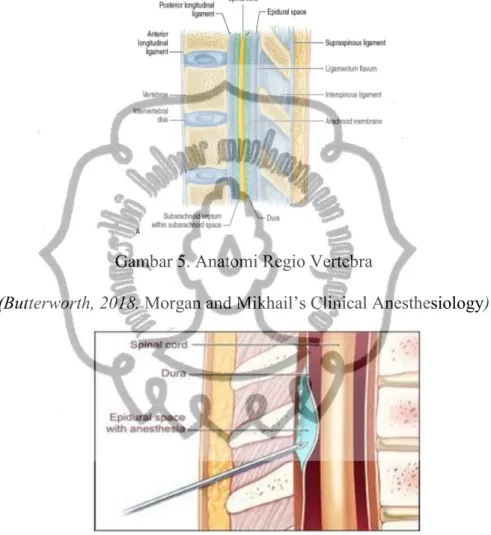
Anestesi epidural merupakan suatu prosedur teknik blok neuroaksial dengan cara memasukkan obat anestesi lokal ke dalam rongga potensial di luar duramater. Rongga tersebut dimulai pada perbatasan kranioservikal pada vertebra servikal 1 sampai dengan membrana sakrokoksigea, dan berada diantara ligamentum flavum dan lapisan duramater. Ruang ini mempunyai kedalaman maksimal pada daerah lumbal, terutama pada daerah vertebra lumbal 3 - 4 dimana rata-rata keseluruhan kedalaman ruang ini sekitar 5 mm. Secara teoritis, anestesi epidural dapat dilakukan pada level lumbal, torakal, dan servikal. Jika dibandingkan dengan anestesi spinal, maka anestesi epidural menawarkan suatu penerapan yang commit to user
lebih luas. Teknik ini digunakan antara lain untuk anestesia operatif, analgesia untuk kasus-kasus obstetri, analgesia post operatif dan untuk penanggulangan nyeri kronis (Butterworth, 2018).
Gambar 5. Anatomi Regio Vertebra
(Butterworth, 2018. Morgan and Mikhail’s Clinical Anesthesiology)
Gambar 6. Insersi Jarum pada Ruang Epidural
(Butterworth, 2018. Morgan and Mikhail’s Clinical Anesthesiology) 2. Jarum dan Teknik Epidural Anestesi
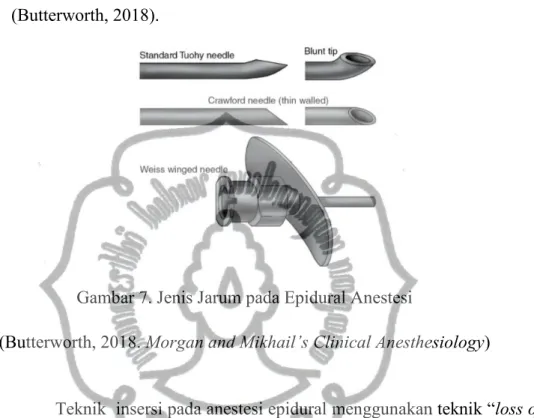
Pada prosedur anestesi epidural, jarum yang digunakan biasanya jarum 17-18 gauge, atau panjang 3-3,5 inci dan memiliki bevel tumpul dengan kurva 15-30 pada ujungnya. Jenis jarum yang digunakan biasanya jarum Tuohy. Hal ini dikarenakan ujungnya yang tumpul dapat berguna setelah melewati ligamentum flavum untuk menekan lapisan duramater menjauh. Kejadian tertusuknya duramater juga dapat dihindari karena commit to user
jarum langsung masuk tanpa ujung tajam seperti pada jarum Crawrod.
Ujung jarum yang melebar dan penempatan peralatan introduser sebagai petunjuk penempatan kateter termasuk dalam modifikasi jarum (Butterworth, 2018).
Gambar 7. Jenis Jarum pada Epidural Anestesi
(Butterworth, 2018. Morgan and Mikhail’s Clinical Anesthesiology)
Teknik insersi pada anestesi epidural menggunakan teknik “loss of resistence”, dimana sebuah jarum Touhy diinsersikan sampai ujungnya tertancap pada ligamentum flavum. Hal ini akan memblok jarum sehingga menimbulkan tahanan kuat terhadap injeksi udara maupun larutan NaCl 0,9%. Kemudian jarum didorong perlahan-lahan sambil tetap mencoba menginjeksikan udara ataupun NaCl 0,9%. Apabila tahanan hilang seketika dan injeksi udara atau NaCl 0,9% dapat dilakukan dengan mudah, maka ini artinya ujung jarum sudah berada pada ruang epidural sehingga obat anestesi lokal dapat disuntikkan atau kateter dapat diinsersikan (Butterworth, 2018).
3. Indikasi dan Kontraindikasi
Blok neuroaxial dapat digunakan sendiri atau bersama dengan anestesi umum untuk banyak prosedur. Sebagai anestesi primer, blok-blok neuroaxial terbukti paling berguna dalam operasi perut bagian bawah, commit to user
inguinal, urogenital, bagian dubur, dan ekstremitas bawah. Prosedur perut bagian atas (misalnya, gastrektomi) telah dilakukan dengan anestesi spinal atau epidural, tetapi karena bisa sulit untuk mencapai tingkat sensorik yang memadai untuk kenyamanan pasien dengan aman, teknik ini kurang umum digunakan (Twomey dan Tsui, 2007).
Jika anestesi neuroaxial dipertimbangkan, pasien harus siap secara mental untuk anestesi neuroaxial dimana sebelumnya sudah didiskusikan terlebih dahulu mengenai semua manfaat beserta risikonya. Pasien harus memahami bahwa mereka akan memiliki sedikit atau tidak ada fungsi motorik ekstremitas bawah sampai blok selesai. Prosedur yang memerlukan manuver yang dapat membahayakan fungsi pernapasan (misalnya, pneumoperitoneum atau pneumotoraks) atau operasi yang durasinya sangat lama biasanya dilakukan dengan anestesi umum, dengan atau tanpa blokade neuroaxial (Butterworth, 2018).
Kontraindikasi utama untuk anestesi neuroaxial termasuk kelainan koagulasi, hipovolemia berat, peningkatan tekanan intrakranial (terutama dengan massa intrakranial), dan infeksi pada tempat injeksi.
Kontraindikasi relatif lainnya termasuk stenosis aorta atau mitral yang berat dan obstruksi aliran keluar ventrikel kiri yang berat (kardiomiopati obstruktif hipertrofik); Namun, dengan pemantauan ketat dan kontrol tingkat anestesi, anestesi neuraksial dapat dilakukan dengan aman pada pasien dengan penyakit jantung katup stenotik, terutama jika penyebaran luas anestesi dermatom tidak diperlukan (misalnya, anestesi epidural blok sadel) (Butterworth, 2018).
Inspeksi dan palpasi punggung dapat mengungkapkan bekas luka bedah, skoliosis, lesi kulit, dan apakah proses spinosus dapat diidentifikasi atau tidak. Meskipun tes skrining pra operasi tidak diperlukan pada pasien sehat yang menjalani blokade neuroaxial, pengujian yang tepat harus dilakukan jika riwayat klinis menunjukkan kelainan koagulasi. Anestesi neuroaxial dengan adanya sepsis atau bakteremia secara teoritis dapat
commit to user
mempengaruhi pasien terhadap penyebaran agen infeksius secara hematogen ke ruang epidural atau subaraknoid (Butterworth, 2018).
Pasien dengan defisit neurologis yang sudah ada sebelumnya atau penyakit demielinasi dapat melaporkan gejala yang memburuk setelah blok neuroaxial. Untuk alasan ini, beberapa praktisi enggan mengambil risiko dengen menerapkan anestesi neuroaxial pada pasien tersebut.
Pemeriksaan neurologis sebelum operasi harus secara menyeluruh mendokumentasikan setiap defisit. Dalam sebuah penelitian retrospektif yang memeriksa catatan 567 pasien dengan neuropati yang sudah ada sebelumnya, 2 dari pasien mengembangkan neuropati baru atau memburuk setelah anestesi neuroaxial. Meskipun temuan ini menunjukkan risiko yang relatif rendah dari cedera lebih lanjut, peneliti penelitian menunjukkan bahwa saraf yang terluka rentan terhadap cedera tambahan, meningkatkan kemungkinan hasil neurologis yang buruk. Namun, riwayat defisit neurologis yang sudah ada sebelumnya atau penyakit demielinasi paling baik merupakan kontraindikasi relatif, dan keseimbangan risiko perioperatif dalam populasi pasien ini dapat mendukung anestesi neuroaxial pada pasien tertentu tertentu (Twomey dan Tsui, 2007).
Tabel 1. Kontraindikasi Anestesi Blok Neuroaksial
(Butterworth, 2018. Morgan and Mikhail’s Clinical Anesthesiology) Absolute
Infection at the site of injection Lack of consent
Coagulopathy of other bleeding diasthesis Severe hypovolemia
Increased intracranial pressure Relative
Sepsis
Uncooperative patient
Preexisiting neurological deficits Demyelinating lesions
Stenotic valvular heart lesions Left ventricular heart lesions
Left ventricular outflow obstruction (hypertrophic obstructive cardiomyopathy) commit to user
Controversial
Prior back surgery at the site of injection Complicated surgery
Prolonged operation Major blood loss
Maneuvers that compromise respiration
4. Komplikasi
Komplikasi anestesi spinal, epidural, atau caudal berkisar dari ringan hingga melumpuhkan dan mengancam jiwa. Secara umum, komplikasi dari teknik neuroaksial adalah efek sekunder dari efek fisiologis yang berlebihan dari obat yang disuntikkan dengan tepat, cedera akibat penempatan jarum atau kateter, dan toksisitas sistemik anestesi lokal. Berikut adalah beberapa komplikasi yang dapat terjadi (Twomey dan Tsui, 2007):
a. Respon fisiologis yang merugikan atau berlebihan:
1) Retensi urin 2) Blok tinggi
3) Total epidural anestesi 4) Henti jantung
5) Anterior epidural artery syndrome 6) Sindrom Horner
b. Komplikasi terkait penempatan jarum / kateter 1) Sakit punggung
2) Tusukan dural/kebocoran
Postdural puncture headache (PDPH) Diplopia
Tinnitus 3) Cedera saraf
Kerusakan nerve root Kerusakan epidural cord Sindrom Cauda equina commit to user
4) Perdarahan
Intraepidural/Epidural Hematoma 5) Kesalahan penempatan (Misplacement)
Tidak ada efek/anestesi yang tidak adekuat Blok subdural
Blok subarachnoid yang tidak disengaja Injeksi intravaskular yang tidak disengaja 6) Pemotongan / retensi kateter
7) Inflamasi
Arachnoiditis 8) Infeksi
Meningitis Abses epidural c. Toksisitas obat
1) Toksisitas sistemik obat anestesi lokal 2) Gejala neurologis sementara
3) Sindroma Cauda equina
C. Krim Estesia 1. Struktur Kimia
Krim estesia (EMLA) (lidokain 2.5% dan prilokain 2.5%) adalah emulsi di mana campuran minyak adalah campuran eutektik dari lidokain dan prilokain dalam perbandingan berat 1:1. Campuran eutektik ini memiliki titik lebur di bawah suhu ruangan dan oleh karena itu kedua anestesi lokal tersebut ada sebagai minyak cair daripada sebagai kristal.
Krim ini ada dalam sediaan tabung 5 gram dan 30 gram (Ralston dan Rapson, 1993).
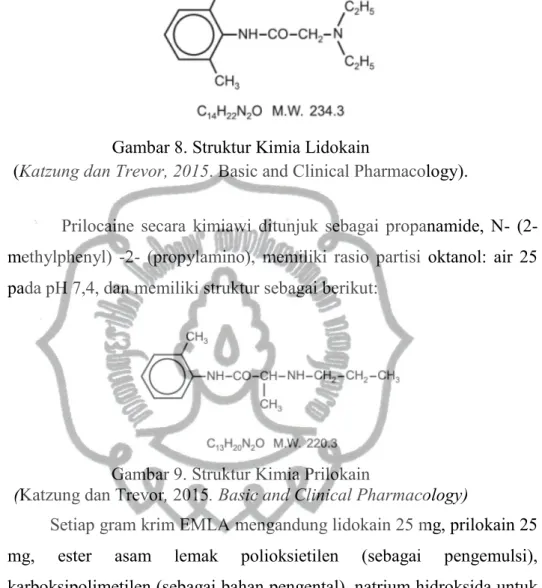
Lidocaine secara kimiawi ditunjuk sebagai acetamide, 2- (diethylamino) -N- (2,6-dimethylphenyl), memiliki oktanol: rasio partisi air 43 pada pH 7,4, dan memiliki struktur berikut: commit to user
Gambar 8. Struktur Kimia Lidokain
(Katzung dan Trevor, 2015. Basic and Clinical Pharmacology).
Prilocaine secara kimiawi ditunjuk sebagai propanamide, N- (2- methylphenyl) -2- (propylamino), memiliki rasio partisi oktanol: air 25 pada pH 7,4, dan memiliki struktur sebagai berikut:
Gambar 9. Struktur Kimia Prilokain
(Katzung dan Trevor, 2015. Basic and Clinical Pharmacology)
Setiap gram krim EMLA mengandung lidokain 25 mg, prilokain 25 mg, ester asam lemak polioksietilen (sebagai pengemulsi), karboksipolimetilen (sebagai bahan pengental), natrium hidroksida untuk menyesuaikan dengan pH yang mendekati 9, dan air murni hingga 1 gram.
Krim EMLA tidak mengandung bahan pengawet, namun melewati uji efektivitas antimikroba USP dikarenakan pH krim tersebut (Ralston dan Rapson, 1993).
2. Farmakologi Klinis
Krim estesia diaplikasikan secara topikal di bawah dressing oklusif, memberikan analgesia dermal dengan melepaskan lidokain dan prilokain dari krim ke lapisan epidermal dan dermal kulit dan dengan akumulasi lidokain dan prilokain di sekitar reseptor nyeri kulit dan ujung saraf.
Lidokain dan prilokain adalah agen anestesi lokal tipe amida. Baik commit to user
lidokain dan prilokain menstabilkan membran neuron dengan menghambat fluks ionik yang diperlukan untuk inisiasi dan konduksi impuls, sehingga menimbulkan efek anestesi local (Drasner, 2015).
Onset, kedalaman dan durasi analgesia dermal pada kulit yang diberikan oleh krim estesia tergantung terutama pada durasi aplikasi.
Untuk memberikan analgesia yang cukup untuk prosedur klinis seperti penempatan kateter intravena, krim estesia harus diaplikasikan di bawah pembalut oklusif selama setidaknya 1 jam. Untuk memberikan analgesia kulit untuk prosedur klinis seperti split skin graft, krim estesia harus dioleskan di bawah pembalut oklusif selama minimal 2 jam. Analgesia kulit yang memuaskan dicapai 1 jam setelah pemakaian, mencapai maksimum 2 hingga 3 jam, dan bertahan selama 1 hingga 2 jam setelah pengangkatan. Penyerapan dari mukosa genital lebih cepat dan waktu onset lebih pendek (5 hingga 10 menit) dibandingkan dengan pemakaian untuk kulit intak. Aplikasi dermal dari krim estesia dapat menyebabkan kemerahan yang terlokalisir di sekitar tempat pemakaian atau eritema (Drasner, 2015).
3. Farmakokinetik a. Absorpsi
Jumlah lidokain dan prilokain yang diserap secara sistemik dari krim estesia berhubungan langsung dengan durasi aplikasi dan area penggunaannya. Dalam dua studi farmakokinetik, 60 g krim estesia (1,5 g lidokain dan 1,5 g prilokain) diaplikasikan pada 400 cm2 kulit intak pada paha lateral dan kemudian ditutup dengan pembalut oklusif.
Subjek kemudian diacak sehingga setengah dari subjek dihentikan pemakaian krim estesia setelah 3 jam, sementara sisanya menggunakan krim estesia selama 24 jam. Ketika 60 g krim estesia diaplikasikan lebih dari 400 cm2 selama 24 jam, kadar lidokain darah puncak sekitar 1/20 tingkat toksik sistemik. Demikian juga, tingkat prilokain maksimum adalah sekitar 1/36 tingkat toksik. Penerapan krim estesia pada kulit commit to user
yang rusak atau terjadi inflamasi, atau dengan luas 2.000 cm2 atau lebih dari kulit di mana lebih banyak kedua anestesi diserap, dapat menghasilkan kadar plasma yang lebih tinggi yang pada individu yang rentan dapat menghasilkan respons farmakologis sistemik (Elson dan Paech, 1995).
b. Distribusi
Ketika setiap obat diberikan secara intravena, volume distribusi adalah 1,1 hingga 2,1 L / kg untuk lidokain dan 0,7 hingga 4,4 L / kg untuk prilocaine. Volume distribusi yang lebih besar untuk prilocaine menghasilkan konsentrasi plasma yang lebih rendah dari prilocaine yang diamati ketika jumlah yang sama dari prilocaine dan lidocaine diberikan. Pada konsentrasi yang dihasilkan oleh pemakaian krim estesia, lidocaine sekitar 70% terikat dengan protein plasma, terutama alfa-1 glikoprotein. Pada konsentrasi plasma yang jauh lebih tinggi (1 hingga 4 μg / mL basa bebas) pengikatan protein plasma lidokain bergantung pada konsentrasi. Prilocaine terikat 55% pada protein plasma. Baik lidokain dan prilokain melewati sawar darah otak dan plasenta, mungkin karena mekanisme difusi pasif (Elson dan Paech, 1995).
c. Metabolisme
Tidak diketahui apakah lidokain atau prilokain dimetabolisme di kulit. Lidocaine diketahui dimetabolisme dengan cepat oleh hati ke sejumlah metabolit termasuk monoethylglycinexylidide (MEGX) dan glycinexylidide (GX), keduanya memiliki aktivitas farmakologis yang serupa, tetapi kurang kuat dibandingkan dengan lidokain. Metabolit, 2,6-xylidine, memiliki aktivitas farmakologis yang tidak diketahui.
Setelah pemberian intravena, konsentrasi MEGX dan GX dalam kisaran serum dari 11 hingga 36% dan dari 5 hingga 11% dari konsentrasi lidokain, masing-masing. Prilocaine dimetabolisme di hati commit to user
dan ginjal oleh enzim amidase menjadi berbagai metabolit termasuk ortho-toluidine dan N-n-propylalanine. Prilokain tidak dimetabolisme oleh plasma esterase. Metabolit ortho-toluidine telah terbukti bersifat karsinogenik pada beberapa model hewan. Selain itu, ortho-toluidine dapat menghasilkan methemoglobinemia setelah dosis sistemik prilocaine kira-kira 8 mg/kg. Pasien yang sangat muda, pasien dengan defisiensi glukosa-6-fosfat dehidrogenase dan pasien yang menggunakan obat pengoksidasi seperti antimalaria dan sulfonamid lebih rentan terhadap methemoglobinemia (Elson dan Paech, 1995).
d. Eliminasi
Waktu paruh eliminasi lidokain dari plasma setelah pemberian intravena adalah sekitar 65 hingga 150 menit. Lebih dari 98% dosis lidokain yang diserap dapat diperoleh kembali dalam urin sebagai metabolit atau obat utuh. Systemic clearance adalah 10 hingga 20 mL / menit / kg. Waktu paruh eliminasi prilocaine adalah sekitar 10 hingga 150 menit. Systemic clearance adalah 18 hingga 64 mL / menit / kg.
Selama studi dengan pemberian intravena, waktu paruh eliminasi lidocaine secara statistik lebih lama secara signifikan pada pasien usia lanjut (2,5 jam) dibandingkan pada pasien yang lebih muda (1,5 jam).
Tidak ada penelitian yang tersedia pada farmakokinetik intravena prilocaine pada pasien usia lanjut (Elson dan Paech, 1995).
4. Aplikasi Klinis
Aplikasi krim estesia selama setidaknya 1 jam memberikan analgesia dermal yang lebih signifikan daripada krim plasebo atau etil klorida. Krim estesia sebanding dengan lidokain subkutan, tetapi kurang manjur dibandingkan lidokain intradermal. Sebagian besar pasien berpendapat pemberian krim estesia lebih disukai daripada infiltrasi lidokain atau semprotan etil klorida. Penggunaan krim estesia pada kulit diketahui dapat mengurangi persepsi nyeri dan suhu. Setelah 60 menit commit to user
pemakaian kulit di bawah oklusi, efek lokal estesia cukup untuk insersi jarum dan bedah minor pada kulit superfisial. Efikasi analgesik meningkat dengan waktu aplikasi yang lebih lama dan setelah 120 menit aplikasi, krim estesia menginduksi analgesia yang memadai untuk pemotongan cangkok kulit dengan dermatom (Nielsen, 1998).
Selain itu, krim estesia antara lain dapat digunakan pada pasien yang akan menjalani prosedur bedah mayor, dimana krim estesia digunakan untuk upaya meminimalkan ketidaknyamanan anestesi epidural. Hal ini dapat memberikan kontribusi penting untuk mengurangi kecemasan dan memberikan kepuasan pasien yang lebih besar. Saat ini diketahui penerapan estesia pada kulit punggung menghasilkan analgesia yang lebih cepat daripada di lokasi kulit lainnya. Untuk kedalamannya, penelitian Wahlgren dan Quiding menyebutkan bahwa analgesia yang disebabkan oleh estesia dapat mencapai kedalaman maksimal 5-6 mm (Wahlgren dan Quiding, 2000).
Penelitian tersebut menilai analgesia pada kulit dengan melakukan prosedur biopsy punch. Subjek penelitian dibagi kedalam dua kelompok, dimana kelompok satu mendapatkan aplikasi krim estesia (EMLA) selama 60-120 menit dan kelompok dua mendapatkan aplikasi krim EMLA selama 3-4 jam. Kira-kira 10 menit setelah pemakaian 60 dan 120 menit, sekitar 50% dari subyek masing-masing memiliki insersi punch biopsy 3 dan 5 mm, masing-masing, dengan rasa sakit yang dapat diterima. Insersi hingga kedalaman maksimum 6 mm dilakukan dengan nyeri yang dapat diterima di 9% dan 36% dari subyek setelah 60 dan 120 menit aplikasi krim EMLA. Tidak ada efek samping yang terkait dengan krimm EMLA yang dilaporkan. Pada kunjungan tindak lanjut setelah 2 bulan, salah satu dari 156 suntikan biopsi telah sembuh dengan hasil yang secara kosmetik tidak memuaskan karena jaringan parut yang terbentuk lebih tinggi sekitar 2 mm di atas permukaan kulit sekitarnya. Inspeksi pada 7 bulan setelah insersi biopsi mengungkapkan penyembuhan tanpa atau dengan sedikit jaringan parut pada semua subjek (Wahlgren dan Quiding, 2000). commit to user
Pada penelitian tersebut, nyeri dinilai oleh subyek menggunakan VAS. Selain itu, jika nyeri dirasakan (VAS> 0 mm), hal tersebut kemudian dinilai sebagai nyeri dapat diterima atau tidak dapat diterima. Kesimpulan dari hasil penelitian tersebut membuktikan bahwa prosedur biopsy punch dengan nyeri yang dapat diterima dapat dilakukan hingga kedalaman 1-2 mm pada aplikasi EMLA selama 60 menit, 2-3 mm pada aplikasi selama 120 menit, dan 6 mm pada pemakaian 3-4 jam (Wahlgren dan Quiding, 2000). Kedalaman analgesia kulit setelah aplikasi krim EMLA diteliti dengan penggunaan jarum intravena 18-gauge. Kedalaman maksimum analgesia kulit adalah sekitar 5 mm, diamati 30 menit setelah aplikasi selama 90 menit serta 60 menit setelah aplikasi krim EMLA selama 120 menit. Namun, kedalaman 5 mm mewakili kombinasi lekukan jarum pada permukaan kulit karena tekanan mekanis dan kedalaman penetrasi jarum yang sebenarnya ke dalam kulit. Tingkat indentasi yang tepat tidak ditunjukkan, tetapi jarum dapat dimasukkan kira-kira 1,8 mm secara tegak lurus ke kulit tanpa rasa sakit di daerah tanpa perawatan aktif. Oleh karena itu, kedalaman maksimal yang dinyatakan 5 mm dari analgesia kulit mungkin sebenarnya agak kurang (Wahlberg dan Quiding, 2000).
Kemanjuran analgesik dari EMLA juga diketahui meningkat dengan waktu aplikasi yang lebih lama, yang sesuai dengan penelitian sebelumnya. Sekitar 10 menit setelah pengangkatan krim EMLA, kedalaman rata-rata penyisipan punch biopsy dengan nyeri yang dapat diterima adalah 2,9 mm setelah 60 menit aplikasi dan 4,5 mm setelah 120 menit aplikasi. Insersi dengan kedalaman 6 mm menimbulkan rasa sakit yang dapat diterima setelah 3 sampai 4 jam aplikasi EMLA. Pemakaian dari krim EMLA juga dibatasi maksimal selama 5 jam (Wahlberg dan Quiding, 2000).
Penelitian lain juga menilai efektifitas pemakaian krim EMLA pada wanita yang akan diberikan anestesi epidural sebelum menjalani operasi Sectio Caesaria. Penelitian ini dilakukan pada wanita yang diberikan anestesi epidural tanpa sedasi sebelumnya, dimana ditemukan bahwa commit to user
aplikasi awal krim EMLA dikombinasikan dengan infiltrasi kulit menggunakan lignocaine 1% dapat mengoptimalkan kenyamanan pasien untuk insersi epidural. Hasil penelitian tersebut mengkonfirmasi bahwa nyeri sementara dengan tingkat keparahan sedang terjadi pada infiltrasi kulit dengan lignokain, dan bahwa ini dapat dikurangi secara signifikan dengan penggunaan EMLA. Teknik lain untuk meminimalkan rasa sakit tersebut termasuk alkalinisasi atau pemanasan lignokain atau penggunaan prokain sebagai anestesi lokal. Alkalinisasi lignokain dan penggunaan prokain telah terbukti secara signifikan mengurangi nyeri. (Elson dan Paech, 1995).
Krim EMLA memberikan analgesia kedalaman 5 mm pada lengan bawah, sebagaimana diketahui dengan jarum 18 gauge. Analgesia sampai 16 mm diamati dengan memasukkan jarum 25 gauge ke lengan atas, menunjukkan bahwa analgesia yang diberikan oleh EMLA meluas ke jaringan subkutan. Penelitian tersebut juga mendukung temuan ini, meskipun analgesia dermal yang baik diperoleh untuk infiltrasi dengan jarum gauge yang lebih kecil, EMLA saja tidak cukup untuk analgesia ketika menggunakan jarum Tuohy 16 gauge (Elson dan Paech, 1995).
Ralston dalam sebuah penelitian terbuka tentang rasa sakit selama pemasangan epidural, menggunakan waktu pemakaian rata-rata sekitar sepuluh menit dan mencatat bahwa dokter anestesi yang hadir merasa infiltrasi lignocaine lebih superior. Penelitian ini juga menemukan EMLA saja tidak memadai meskipun dengan penggunaan selama 90 menit.
Namun, telah disarankan bahwa ketebalan kulit yang lebih besar dari punggung mungkin dapat menyerap dan mendistribusikan volume EMLA yang lebih besar, sehingga dosis 2,5 g tidak cukup. Dengan demikian penelitian lebih lanjut menggunakan dosis yang lebih besar pada berbagai waktu pemakaian dapat dibenarkan (Ralston dan Rapson, 1993).
Penelitian berikutnya menunjukkan penurunan yang signifikan dalam skor nyeri ketika diberikan anestesi lokal berupa infiltrasi atau penggunaan EMLA dibandingkan dengan tidak ada anestesi lokal. commit to user
sebelum prosedur pungsi lumbal. Sebagian besar uji coba membandingkan infiltrasi lokal dengan aplikasi EMLA sebelum tusukan dermal menunjukkan pemakaian EMLA lebih manjur dibandingkan dengan infiltrasi lokal. Durasi aplikasi sangat penting untuk kemanjuran yang cukup dari EMLA karena analgesia maksimum akan didapatkan setelah pemakaian 90 menit, yang sering tidak dipertimbangkan dalam percobaan sebelumnya. Sebuah survei dari Ralston menunjukkan inferioritas EMLA terhadap infiltrasi lokal, tetapi durasi aplikasi sangat singkat (rata-rata 9 menit), oleh karena itu efek yang cukup tidak dapat diharapkan (Massoth, 2018).
Penelitian tersebut menunjukkan rata-rata skor VAS pada kelompok dengan penggunaan EMLA sedikit lebih rendah. Meskipun tidak mencapai signifikansi statistik, kemanjuran EMLA yang unggul konsisten dengan data dari sebagian besar survei yang sudah ada sebelumnya. Dalam penelitian tersebut, perbedaan dalam waktu paparan EMLA sebelum tusukan tidak dapat dihindari karena penelitian berlangsung dalam setting klinis, dimana ada variabilitas waktu di ruang operasi. Namun, mengingat farmakokinetik EMLA, waktu aplikasi minimum 60 menit harus dipenuhi dan ini tercapai pada semua pasien. Namun demikian, perbedaan waktu aplikasi total mungkin telah menyebabkan efek analgesik yang dilemahkan pada masing-masing pasien. Secara keseluruhan, penggunaan EMLA membutuhkan perencanaan lanjutan yang cermat dalam rutinitas klinis harian (Massoth, 2018).
Beberapa penelitian diatas adalah tindak lanjut terhadap temuan bahwa pada beberapa wanita dalam persalinan, landmark anatomi untuk prosedur anestesi sangat sulit diidentifikasi karena edema atau obesitas.
Penggunaan anestesi lokal infiltrasi lebih lanjut akan mengaburkan landmark apa pun yang mungkin telah teraba. Dalam hal ini krim EMLA memiliki keuntungan dimana tidak menyebabkan distorsi jaringan lunak, dan memang memberikan anestesi kulit setelah periode aplikasi singkat,
commit to user
sehingga menghasilkan anestesi kulit yang baik bagi banyak pasien (Massoth, 2018).
Penelitian lain juga dilakukan Nielsen pada tahun 1998 dimana dibahas efek pemberian krim EMLA pada prosedur anestesi spinal. Data penelitian tersebut mengandung tiga temuan yang pantas untuk dibahas lebih lanjut. Temuan penting pertama adalah bahwa penggunaan EMLA mengurangi rasa sakit yang terkait dengan tusukan jarum pada tulang belakang lebih dari 50% dibandingkan dengan kelompok lain. Temuan penting kedua adalah pemakaian EMLA membantu mengurangi kecemasan pasien, tetapi tidak memengaruhi pilihan anestesi mereka.
Temuan ketiga adalah bahwa analgesia infiltrasi sebelum anestesi spinal tidak memiliki keunggulan dibandingkan anestesi spinal langsung (Nielsen, 1998).
Analgesia yang didapatkan dari aplikasi krim EMLA mencapai kedalaman maksimum 5mm setelah 90-120 menit. Selain itu, aplikasi krim EMLA pada kulit punggung dibandingkan dengan dorsum tangan menghasilkan analgesia yang lebih cepat, yang cepat berkurang setelah pengangkatan krim. Namun, insersi jarum spinal, yang melibatkan struktur yang lebih dalam, menghasilkan nyeri yang lebih hebat daripada venipuncture. Aplikasi EMLA terbukti mengurangi nyeri tusukan di tulang belakang dibandingkan dengan plasebo dari 1,8 menjadi 0,75 pada VAS.
Ada beberapa penelitian yang memperlihatkan hasil VAS yang lebih rendah lagi. Namun, skor VAS yang lebih tinggi yang dilaporkan oleh para penulis ini dapat dijelaskan karena populasi yang berbeda yang dipelajari dan durasi aplikasi EMLA yang lebih lama pada penelitian sebelumnya.
Para pasien dalam penelitian tersebut lebih tua secara usia serta memiliki durasi pemakaian EMLA yang lebih singkat. Meskipun 1 jam aplikasi EMLA mengurangi rasa sakit tusukan lumbal pada anak-anak, efek analgesik dari krim meningkat dengan meningkatnya waktu aplikasi dan minimal waktu 100 menit diperlukan untuk mendapatkan blokade sensorik total pada kulit segera setelah pengangkatan EMLA (Nielsen, 1998). commit to user
Pasien-pasien yang akan diberikan anestesi spinal sering bertanya seberapa menyakitkan penusukan jarum spinal. Dua puluh empat persen dari pasien yang menolak anestesi regional melakukannya karena takut jarum. Pengurangan rasa takut ini dapat berkontribusi pada penerimaan anestesi yang lebih baik. Studi ini menunjukkan bahwa secara signifikan lebih banyak pasien dalam kelompok EMLA (73%) menggambarkan nyeri tusukan kurang dari yang diharapkan, dibandingkan dengan dua kelompok lainnya (infiltrasi 48%, plasebo 46%). Dengan kata lain, krim EMLA mengurangi kecemasan pasien untuk nyeri tusukan tulang belakang, jika mereka menerima anestesi neuroaxial lain di masa depan. Namun, kepuasan dengan anestesi neuroaxial dan keputusan untuk menerima bentuk anestesi ini di masa depan tidak hanya ditentukan oleh rasa takut jarum. Seperti dalam penelitian lain hanya tiga dari pasien penelitian tersebut (1,5%) yang akan memilih anestesi umum untuk operasi lain. Ini menunjukkan bahwa nyeri tusukan lumbal hanya merupakan penentu kecil dari keputusan pasien apakah akan menerima atau menolak anestesi neuroaxial. Meskipun demikian, krim EMLA tetap direkomendasikan untuk pasien yang menginginkan anestesi neuroaxial, tetapi khawatir terhadap nyeri tusukan jarum. Hal ini setelah ditarik kesimpulan bahwa krim EMLA adalah metode yang efektif untuk memberikan analgesia yang memadai untuk tusukan pada tulang belakang. Pemakaian dapat dilakukan dengan sederhana dan diterima dengan baik oleh pasien. Jika dibandingkan dengan pemberian analgesia lain, seperti infiltrasi kulit dan ligamen dengan 2 ml lignokain 2%, prosedur tersebut membutuhkan waktu ekstra dan tidak lebih baik daripada placebo, sehingga tidak direkomendasikan (Nielsen, 1998).
commit to user
D. Anestesi Lokal 1. Struktur Kimia
Sebagian besar agen anestesi lokal terdiri dari kelompok lipofilik yang dihubungkan oleh rantai perantara melalui ester atau amida ke kelompok terionisasi. Selain sifat fisik umum dari molekul, konfigurasi stereokimia spesifik dikaitkan dengan perbedaan dalam potensi stereoisomer (misalnya, levobupivacaine, ropivacaine). Karena rantai ester lebih rentan terhadap hidrolisis daripada rantai amida, obat golongan ester biasanya memiliki durasi aksi yang lebih pendek (Kumar., 2015).
Anestesi lokal adalah basa lemah dan biasanya tersedia secara klinis sebagai garam untuk meningkatkan kelarutan dan stabilitas. Di dalam tubuh, obat anestesi lokal beredar sebagai basa tidak bermuatan atau sebagai kation. Proporsi relatif dari kedua bentuk ini diatur oleh pKa obat dan pH cairan tubuh menurut persamaan Henderson-Hasselbalch (Drasner, 2015).
2. Mekanisme Aksi
Secara umum, mekanisme aksi dari obat anestesi lokal terbagi jadi 3, yaitu bekerja pada potensial membrane, pada isoform kanal natrium, serta blok kanal. Mekanisme utama aksi anestesi lokal adalah blokade kanal natrium. Selaput akson saraf yang dapat tereksitasi, seperti selaput otot jantung dan sel-sel sel saraf, mempertahankan potensi transmembran istirahat -90 hingga -60 mV. Selama eksitasi, saluran natrium terbuka, dan arus natrium ke dalam yang cepat mendepolarisasi membran menuju potensi keseimbangan natrium (+40 mV). Sebagai hasil dari proses depolarisasi ini, saluran natrium menutup (tidak aktif) dan saluran kalium terbuka. Aliran keluar kalium merepolarisasi membran menuju potensi kesetimbangan kalium (sekitar –95 mV); repolarisasi mengembalikan saluran natrium ke keadaan istirahat dengan waktu pemulihan yang khas yang menentukan periode refraktori. Gradien ion transmembran commit to user
dipertahankan oleh pompa natrium. Fluks ionik ini mirip dengan, tetapi lebih sederhana daripada, yang ada di otot jantung, dan anestesi lokal memiliki efek yang serupa di kedua jaringan (Drasner, 2015).
Setiap saluran natrium terdiri dari satu subunit alfa tunggal yang mengandung pori penghasil ion sentral yang terkait dengan subunit beta aksesori. Subunit alfa pembentuk pori sebenarnya cukup untuk fungsional, tetapi kinetika dan ketergantungan tegangan saluran dimodifikasi oleh subunit beta. Berbagai saluran natrium yang berbeda telah ditandai oleh rekaman elektrofisiologi, dan kemudian diisolasi dan dikloning, sementara analisis mutasi telah memungkinkan untuk mengidentifikasi komponen penting dari tempat pengikatan anestesi lokal. Sembilan saluran natrium mamalia telah dikarakterisasi dan diklasifikasikan sebagai Nav1.1 sampai dengan Nav1.9, di mana simbol kimia mewakili ion primer, subskrip tersebut menunjukkan regulator fisiologis (dalam hal ini voltase), angka awal menunjukkan gen, dan jumlah yang mengikuti periode menunjukkan isoform tertentu (Drasner, 2015).
Ketika konsentrasi anestesi lokal yang diberikan pada serat saraf semakin meningkat, maka ambang batas untuk eksitasi meningkat, konduksi impuls melambat, laju kenaikan potensial aksi menurun, amplitudo potensial aksi berkurang, dan, akhirnya, kemampuan untuk menghasilkan potensial aksi sepenuhnya dihapuskan. Efek progresif ini dihasilkan dari pengikatan anestesi lokal ke lebih banyak kanal natrium.
Jika arus natrium tersumbat di sepanjang panjang saraf yang kritis, perambatan impuls melintasi area yang tersumbat tidak lagi memungkinkan. Dalam saraf mielin, panjang kritis tampaknya dua sampai tiga node Ranvier. Pada dosis minimum yang diperlukan untuk memblokir perambatan impuls, potensi istirahat tidak berubah secara signifikan (Drasner, 2015).
commit to user
3. Anestesi Lokal pada Praktik Klinis
Anestesi lokal dapat memberikan analgesia yang sangat efektif di daerah tubuh yang teridentifikasi dengan baik. Rute pemberian yang biasa termasuk aplikasi topikal (misalnya, mukosa hidung, luka insisi), injeksi di sekitar ujung saraf tepi (infiltrasi perineural) dan batang saraf utama (blok), dan injeksi ke ruang epidural atau subarachnoid mengelilingi sumsum tulang belakang (Kumar, 2015).
Dalam praktik klinis, umumnya ada perubahan teratur komponen anestesi dimulai dengan transmisi simpatik dan berlanjut ke suhu, nyeri, sentuhan ringan, dan akhirnya blok motorik. Hal tersebut paling mudah dinilai selama onset anestesi spinal, di mana perbedaan spasial dapat dideteksi dalam modalitas, komponen yang paling rentan mencapai penyebaran dermatomal yang lebih besar. Dengan demikian, hilangnya sensasi dingin (sering dinilai oleh spons alkohol basah) akan kira-kira dua segmen di atas tingkat analgesik untuk pinprick, yang pada gilirannya akan menjadi sekitar dua segmen rostral hingga hilangnya pengenalan sentuhan ringan. Namun, karena pertimbangan anatomi untuk batang saraf perifer, onset dengan blok perifer lebih bervariasi, dan kelemahan motorik proksimal dapat mendahului timbulnya kehilangan sensorik yang lebih jauh. Selain itu, larutan anestesi umumnya tidak tersebar secara merata di sekitar ikatan saraf, dan penyebaran longitudinal serta penetrasi radial ke dalam batang saraf tidak sama di setiap bagiannya (Kumar, 2015).
Sehubungan dengan efek anestesi blok yang berbeda-beda, perlu dicatat bahwa anestesi pada prosedur bedah dapat dikatakan sukses apabila pasien kehilangan sentuhan, bukan hanya hilangnya rasa sakit, karena beberapa pasien bahkan akan merasakan sensasi sentuhan menjadi mengganggu selama operasi, dimana pasien seringkali takut bahwa prosedur tersebut dapat menjadi menyakitkan. Lebih lanjut, dengan perbedaan yang mungkin ada dalam modalitas, sementara ini tidak mungkin dengan teknik konvensional dapat menghasilkan anestesi pada prosedur bedah tanpa kehilangan fungsi motorik (Drasner, 2015). commit to user
Kemudian pada anestesi lokal dengan teknik infiltrasi, disinggung sebelumnya dimana salah satu kekurangannya adalah adanya kemungkinan landmark anatomi menjadi hilang tertutup oleh obat anestesi lokal. Kemungkinan penutupan struktur anatomi oleh infiltrasi anestesi lokal yang menyebabkan kesulitan untuk melakukan prosedur medis telah dibahas tetapi tidak pernah diselidiki. Namun, mengingat jumlah upaya yang diperlukan untuk berhasil menempatkan jarum intratekal, tidak ada perbedaan yang signifikan dalam jumlah upaya antar kelompok dengan anestesi infiltrasi dan yang tidak. Penelitian lebih lanjut diperlukan untuk mengevaluasi dampak infiltrasi anestesi lokal pada kondisi anestesi neuraxial. Tidak ada faktor lain yang terkait dengan kondisi yang lebih sulit yang diamati dalam populasi penelitian ini seperti obesitas ekstrem dan hanya satu pasien yang melaporkan operasi tulang belakang sebelumnya (Massoth, 2018).
commit to user
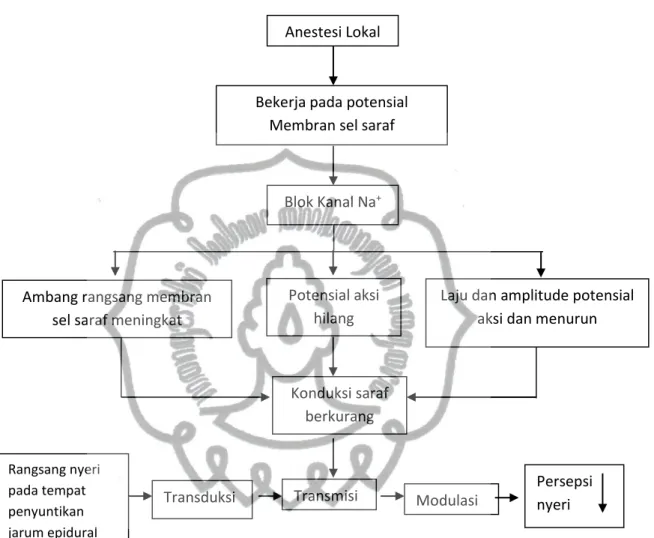
E. Kerangka Teori
Gambar 10. Kerangka Teori Anestesi Lokal
Bekerja pada potensial Membran sel saraf
Blok Kanal Na+
Laju dan amplitude potensial aksi dan menurun Ambang rangsang membran
sel saraf meningkat
Persepsi nyeri Rangsang nyeri
pada tempat penyuntikan jarum epidural
Transduksi Transmisi Modulasi Konduksi saraf
berkurang Potensial aksi
hilang
commit to user
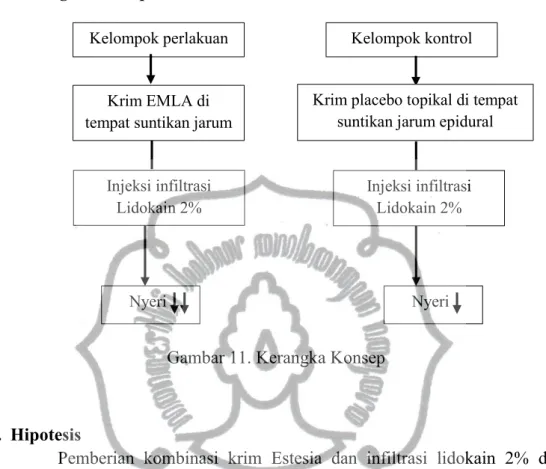
F. Kerangka Konsep
Gambar 11. Kerangka Konsep
G. Hipotesis
Pemberian kombinasi krim Estesia dan infiltrasi lidokain 2% dapat mengurangi nyeri pada suntikan jarum anestesi epidural.
Injeksi infiltrasi Lidokain 2%
Kelompok perlakuan Kelompok kontrol
Krim EMLA di tempat suntikan jarum
epidural
Krim placebo topikal di tempat suntikan jarum epidural
Nyeri Nyeri
Injeksi infiltrasi Lidokain 2%
commit to user