Sintesis TS-1 Mesopori Menggunakan Prekusor Nanocluster Dengan Variasi Waktu Hidrotermal
Zeni Rahmawati *, Didik Prasetyoko1
Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Teknologi Sepuluh Nopember Surabaya
ABSTRAK
Katalis TS-1 Mesopori telah disintesis menggunakan metode Eimer dkk dengan variasi waktu hidrotermal.Variasi waktu yang digunakan adalah 0,5 ; 1; 2 dan 3 hari. Cetil trimetil amonium bromida (CTAB) digunakan sebagai templat pengarah meso. Padatan hasil sintesis dikarakterisasi menggunakan XRD, Adsorpsi Desorpsi Nitrogen, dan FTIR. Difraktogram XRD menunjukkan bahwa semakin lama waktu hidrotermal menyebabkan peningkatan kristalinitas. Melalui analisa adsorpsi desorpsi nitrogen diperoleh data bahwa semua sampel mempunyai diameter pori sekitar 3,05 – 3,08 nm. Uji aktivitas katalitik dilakukan dengan mengaplikasikan sampel pada reaksi oksidasi fenol. Kromatrogram hasil produk oksidasi fenol mengindikasikan bahwa sampel katalis TS-1 selektif terhadap benzokuinon.
Kata Kunci: TS-1 Mesopori, Waktu hidrotermal , Hidroksilasi Fenol
ABSTRACT
Mesoporous TS-1 catalyst have been successfully synthesized with variation of hydrothermal time. The variation was 0.5, 1,2 and 3 days, while the temperatur for hydrothermal prosess was
800C. Mesoporous phase of TS-1 was synthesized using template cetyltrimethylammonium
bromide (CTAB). Various techniques including XRD, nitrogen adsorption-desorption, and FTIR were employed for the material characterization.The results of diffactogram peaks showed that crystalinity increased as the hydrothermal time increased, while nitrogen adsorption – desorption showed that all samples have pore size between 3.04-3.08 nm.The samples were catalytically tested in the hydroxylation of phenol.Chromatogram of the product indicated that the TS-1 sample were selective to benzoquinon.
Keywords:TS-1 Mesoporous, Hydrotermal Time , Hidroxilation of Phenol
*Corresponding author Phone : +6285732966498
e-mail : zeni@chem.its.ac.id
1 Alamat sekarang : Jur Kimia, Fak MIPA,
Institut Teknologi Sepuluh Nopember, Surabaya
I. PENDAHULUAN
Katalis adalah suatu zat yang dapat mempercepat reaksi dengan menurunkan energi aktivasi reaksi. Katalis telah digunakan secara luas untuk produksi berbagai macam produk seperti produk dalam industri perminyakan, farmasi, dan
fine chemicals, yang sukar didapat atau
mahal harganya. Katalis dibedakan menjadi dua golongan yaitu katalis homogen dan katalis heterogen. Pengembangan katalis
(Tang dkk, 2006). Salah satu contoh katalis heterogen adalah TS-1.
TS-1 adalah material katalis yang bersifat hidrofobik (Grieneisen dkk, 2000). Beberapa contoh penggunaan katalis TS-1
antara lain epoksidasi propilen,
meningkatkan aktivitas katalitik oksidasi α
-pinena dan hidroksilasi fenol (Wilkenhoner dkk, 2001). Lin dkk (2004) menyatakan bahwa katalis dengan ukuran mikropori tidak terlalu efektif mengkatalisis molekul dengan
ukuran besar (bulky molecules), sedangkan
katalis mesopori dengan ukuran pori yang
lebih besar dari mikropori, lebih
memungkinkan mengkatalisis material
dengan ukuran besar, sehingga dengan kata lain TS-1 mikropori kurang efektif untuk molekul ukuran besar. Beberapa katalis dikembangkan menjadi berukuran mesopori, antara lain MCM-41 dan MCM-48. Namun katalis–katalis tersebut tidak memiliki stabilitas hidrotermal yang tinggi, sehingga
dikembangkan TS-1 Mesopori yang
mempunyai stabilitas hidrotermal yang tinggi.
Sintesis TS-1 mesopori dilakukan secara hidrotermal yang melibatkan air sebagai pelarut, sumber silika, sumber titanium, agen pengarah struktur, dan substansi pengarah mesopori. Sintesis secara hidrotermal melibatkan air dan panas, dimana larutan prekursor dipanaskan pada temperatur relatif tinggi dalam wadah tertutup. Fasa mesopori dibentuk melalui pembentukan
silika dengan template misel diikuti
pemindahan template melalui kalsinasi (Vinu
dkk, 2006). Adanya template menyebabkan
volume pori menjadi lebih besar.
Widati (2009) telah melakukan sintesis TS-1 mesopori dengan variasi waktu hidrotermal 2, 4, dan 8 hari. Hasil yang didapatkan yaitu terbentuk fase mesopori pada waktu hidrotermal 2 hari, namun pada waktu hidrotermal 4 hari fase mesopori berkurang drastis dan berubah menjadi fase mikropori, sehingga diperlukan variasi waktu hidrotermal yang lebih kecil untuk mengamati fase mesopori pada sintesis TS-1. Oleh karena itu, dalam percobaan ini dipelajari pengaruh waktu hidrotermal terhadap pembentukan fase mesopori TS-1, yang dilakukan dengan waktu hidrotermal yang lebih pendek yaitu 0,5; 1, 2, dan 3 hari.
II. METODE
A. Sintesis ZSM-5 Mesopori
Katalis mesopori TS-1 disintesis dengan menggunakan metode yang dilakukan oleh Eimera dkk (2008). Bahan yang digunakan sebagai sumber silika adalah tetraetilortosilikat (TEOS) dan sumber
Titanium adalah tetrabutilortotitanat
(TBOT). Templat yang digunakan sebagai pengarah struktur MFI adalah TPAOH, sedangkan Cetil trimetil amonium bromida (CTAB) digunakan sebagai templat pengarah meso Sejumlah TEOS ditambah dengan TBOT dan diaduk selama 30 menit pada suhu kamar. Tetrapropilamonium hidroksida 40% dan natrium hidroksida ditambahkan ke dalam campuran, kemudian diaduk selama 15 jam, sehingga campuran yang diperoleh mempunyai perbandingan mol 1 TEOS : 0,017 TiO2 : 0,24 TPAOH : 21,2 H2O : 0,004 Na2O. Campuran yang terbentuk didiamkan pada suhu 80ºC selama 0,5; 1 ; 2 dan 3 hari. Sejumlah CTAB ditambahkan ke dalam campuran hingga diperoleh rasio molar CTAB/Si = 0,306. Selanjutnya, campuran didiamkan selama 3 jam. Padatan yang terbentuk kemudian disaring, dicuci dengan aquades, dikeringkan pada temperatur 60ºC selama 1 hari, dan dikalsinasi dengan dialiri N2 pada suhu 550ºC selama 1 jam, dilanjutkan kalsinasi tanpa N2 selama 6 jam.
B. Karakterisasi
Padatan yang dihasilkan
dikarakterisasi menggunakan teknik difraksi
sinar-X (X-Ray Diffraction Phillips Expert)
menggunakan radiasi CuKα pada panjang
gelombang λ = 1,541 Å, voltase 40 kV, dan
arus 30 mA dengan rentang sudut 2θ = 3-50°.
Selanjutnya, padatan yang dihasilkan
dikarakterisasi dengan spektroskopi
inframerah (SHIMADZU) untuk mengetahui ikatan yang terbentuk pada bilangan
gelombang 1400 cm-1 sampai 400 cm-1.
Katalis yang dihasilkan diuji aktivitasnya pada reaksi hidroksilasi phenol, menggunakan oksidator H2O2 dan pelarut air. Reaksi dilakukan selama 2 jam dan pada
suhu 70oC.
III. HASILPENELITIAN
A. Sintesis Katalis TS-1 Mesopori
TS-1 merupakan salah satu katalis heterogen yang biasanya disintesis dengan menggunakan metode sol gel, dalam penelitian ini TS- 1 mesopori dibuat menggunakan metode yang telah dilakukan oleh Eimer,dkk (2008). TS-1 tersusun atas rangkaian Si-O-Ti yang membentuk struktur MFI. Bahan baku yang digunakan sebagai sumber silika adalah silikon alkoksida (Si(OR)
4) yaitu tetraetilortosilikat (TEOS).
Alkoksida logam banyak dimanfaatkan karena adanya gugus OR yang sangat
elektronegatif, sehingga mampu
menstabilkan logam pada tingkat oksidasi paling tinggi. Tetra butil orto titanat (TBOT)
digunakan sebagai sumber titanium,
sedangkan untuk pengarah struktur MFI digunakan tetrapropilamonium hidroksida (TPAOH) dan surfaktan setiltrimetilamonium bromida (CTAB) digunakan sebagi agen pengarah struktur meso.
Tahap awal dari penelitian adalah dengan mencampurkan TEOS dengan TBOT. Tertra butil orto titanat dilarutkan ke dalam isopropanol sebelum dicampur dengan tetra etil orto silikat. Penambahan isopropanol bertujuan untuk mencegah hidrolisis TBOT menjadi TiO2, karena jika sudah terhidrolisis maka Ti tidak dapat lagi membentuk rangkaian bersama Si untuk membentuk struktur MFI. TBOT dimasukkan ke dalam beker glass yang berisi TEOS sambil diaduk. Campuran TEOS dan TBOT diaduk selama 30 menit, selanjutnya ditambah dengan
pengarah struktur TPAOH dan di aging
selama 15 jam.
Setelah pengadukan selesai, maka
campuran didiamkan dalam suhu 80oC agar
terjadi proses hidrotermal untuk membentuk kristal TS-1. Proses hidrotermal ini melibatkan prekusor, agen pengarah yang dipanaskan dalam ruang tertutup agar terjadi reaksi kondensasi yang memungkinkan adanya pemutusan dan pembentukan ikatan baru Si, T-O-Si Ti (Cundy dan Cox, 2005).
Variasi waktu hidrotermal dilakukan untuk mengetahui pengaruh waktu hidrotermal dalam membentuk mesopori pada TS-1, yaitu 0,5; 1; 2 dan 3 hari Tahap selanjutnya adalah pemberian surfaktan CTAB sebagai agen pengarah struktur meso. CTAB ditambahkan sampai mencapai rasio molar CTAB/Si 0,306 sehingga sistem surfaktan yang terjadi dalam penelitian ini adalah heksagonal sepertihalnya MCM-41.
Pendiaman selama 3 jam dilakukan untuk mengendapkan padatan yang terbentuk dan kemudian di sentifuge. Padatan dicuci dengan aquades hingga pH nya netral untuk menghilangkan sisa – sisa bahan yang tidak ikut bereaksi misalnya TPAOH. Sedangkan untuk menghilangkan kandungan airnya maka proses selanjutnya adalah padatan yang terbentuk dipanaskan pada 60ºC suhu selama 1 hari.
Tahap akhir dari sintesis TS-1 adalah
kalsinasi yang bertujuan untuk
menghilangkan template organik yang berada dalam pori – pori padatan. Metode kalsinasi umumnya dilakukan pada suhu ±550ºC dengan dialiri gas N2 selama 1 jam dan dilanjutkan kalsinasi dengan udara selama 6 jam (Kresge, 1992).
Selanjutnya TS-1 yang terbentuk dikarakterisasi dengan difraksi sinar X (XRD), spektroskopi inframerah, adsorpsi-desorpsi nitrogen dan diuji kaktivitasnya pada reaksi hidroksilasi fenol.
B. Karakterisasi Padatan 1. Difraksi Sinar X (XRD)
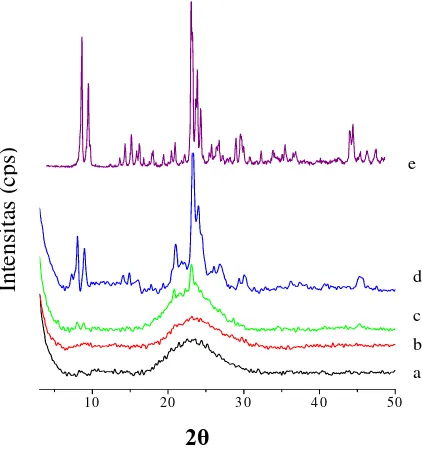
Difaktogram XRD digunakan untuk mengetahui fase dan struktur kristal, serta kristalinitas. Pada pengukuran difraksi sinar X dipelajari hubungan pertumbuhan kristal dengan lama waktu hidrotermal dengan menggunakan variasi waktu hidrotermal 0,5 hari, 1 hari, 2 hari dan 3 hari. Gambar 4.1 menunjukkan difaktogram dari sampel l dengan waktu hidrotermal (kode WH) yang berbeda – beda. Angka 0,5 menunjukkan lama waktu hidrotermal dalam satuan hari.
( Treacy dkk, 2001). Struktur MFI didapatkan karena menggunakan pengarah
struktur TPAOH. Penggunaan templat TPA+
memberikan pengaruh pada pembentukan ikatan Si,Ti-O-Si,Ti dan juga memberikan suasana basa yang membantu melarutkan silika. TPAOH mempengaruhi struktur produk akhir, sebagaimana biasanya ukuran
kristal bertambah dengan dimulainya
penambahan TPAOH pada gel prekusor.
Gambar 1 Pola difraksi sinar X sampel sampel a. WH-0.5, b. WH-1, c. WH-2, dan d. WH-3 e. Sampel TS-1 mikropori
Pada sudut 24,1o terdapat puncak
yang mengindikasikan perubahan struktur material dari simetri ortorombik (silikalit -1 ) menjadi simetri ortorombik (TS-1) seperti yang dilaporkan oleh Li Xu dkk (2002). Perubahan struktur material ini dikarenakan masuknya Ti ke dalam kerangka TS-1. Masuknya Ti ke dalam kerangka MFI memberikan efek yang signifikan pada struktur, (Marra, 2000).
Pengaruh waktu hidrotermal pada struktur TS-1 dapat dilihat pada gambar 4.1, semua sampel mempunyai puncak pada sudut
– sudut tersebut mengindikasikan
pembentukan dan pertumbuhan kristalinitas. Pada sampel WH-0,5 terlihat bahwa tidak terdapat garis difraksi yang jelas, tidak terdapat puncak namun terdapat gundukan
pada sudut 15-30o. Hal ini menunjukkan
bahwa sampel WH-0,5 merupakan padatan amorf, begitu juga dengan sampel WH-1. Untuk sampel WH-2 sudah mulai terbentuk
sedikit puncak kecil pada 7,9o; 8,9o, dan 23o ,
namun belum begitu jelas. Sedangkan pada sampel dengan variasi waktu hidrotermal 3 hari sudah mulai terlihat puncak yang jelas
dan tajam, yaitu pada 7,9o; 8,9o; 23,2o dan
24,1o. Hal ini mengindikasikan bahwa kristal
sudah terbentuk. Evolusi pola XRD mendukung transformasi dari amorf menjadi kristal. Sehingga dapat disimpulkan bahwa semakin lama waktu hidrotermal maka semakin tinggi kristalinitasnya. Hasil ini sesuai dengan hasil yang dilaporkan oleh Fraile dkk ( 2003) dan Parvulescu dkk, (2003). Hal ini disebabkan pada saat proses hidrotermal terjadi reaksi kondensasi yang memungkinkan terjadinya pemutusan dan pembentukan ikatan baru Si,Ti-O-Si,Ti (Cundy dan Cox, 2005), semakin lama waktu hidrotermal, semakin banyak ikatan yang terbentuk, jumlah bidang kristal menjadi lebih banyak dan teratur yang selanjutnya menyebabkan sinar X yang terdifraksikan secara teratur lebih banyak.
Gambar 1 juga memperlihatkan difraktogram TS-1 mikropori. Melalui data tersebut dapat dilihat bahwa terdapat perbedaan profil difraktogram antara TS-1 mikropori dan TS-1 mesopori. Perbedaan yang ditunjukkan dengan munculnya indikasi
puncak pada 2θ sekitar 3o yang tidak
terdapat pada TS-1 mikropori.Dengan demikian dapat disimpulkan bahwa indikasi
puncak pada 2θ sekitar 3o menunjukkan
adanya pori ukuran meso pada semua sampel.
Karena puncak karakteristik material
mesopori terletak pada 2θ 2,1-2,7º (Eimer
dkk, 2008).
2. Spektroskopi FTIR
Spektroskopi FTIR digunakan untuk
mengidentifikasi material, menentukan
komposisi dari campuran, dan membantu
memberikan informasi dalam
memperkirakan struktur molekul. Analisa dengan metode ini didasarkan pada fakta bahwa molekul memiliki frekuensi spesifik yang dihubungkan dengan vibrasi internal dari atom gugus. Gambar 4.2 menunjukkan spektra dari beberapa sampel dengan waktu hidrotermal yang berbeda – beda.
10 20 30 40 50
a b c d e
In
te
ns
ita
s
(c
ps
)
Titanium silikalit–1 mempunyai beberapa frekuensi spesifik yang disebabkan oleh vibrasi internal, yaitu pada 1230, 1100,
800, 550 dan 450 cm-1. Spektra tersebut
merupakan spektra vibrasi dari ikatan internal SiO4 atau AlO4 tetrahedral (Flanigen
dkk, 1973). Puncak pada 550 cm-1
menunjukkan adsorpsi spesifik yang
menunjukkan adanya vibrasi kerangka cincin ganda
lima Si-O-T (T=S atau Ti) yang menunjukkan bahwa strukturnya adalah tipe
MFI ( Fang, 2006). Puncak pada 960 cm-1
menunjukkan adanya vibrasi ikatan Si-O-Ti atau ikatan Si-O yang diganggu oleh kehadiran atom Ti dalam kerangka TS-1, puncak tersebut juga menunjukkan adanya titanium dalam kerangka zeolit (Fang, 2006). Namun tidak demikian untuk TS-1 mesopori. Fraile dkk melaporkan bahwa bilangan
gelombang pada 960 cm-1 tidak bisa
dijadikan sebagai acuan adanya Ti, karena kecenderungan material mesopori yang memiliki sifat amorf. Hal ini menunjukkan
bahwa puncak pada 960 cm-1 juga
mengindikasikan adanya vibrasi silanol dari jaringan amorf (Zhang, 2008). Seperti halnya
Zhang, Goncalves dkk 2008 juga
melaporkan bahwa panjang gelombang 960
cm-1 menunjukkan adanya gugus silanol yang
terdapat pada permukaan dinding mesopori. Puncak pada bilangan gelombang sekitar
1100 cm-1 menunjukkan adanya vibrasi
asimetri Si-O-Si dan pada 1200 cm-1
merupakan pita karakteristik dari kerangka zeolit MFI (Drago dkk, 1998).
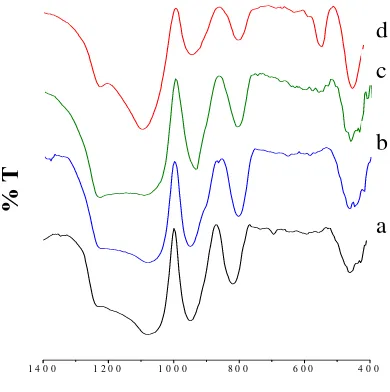
Sampel TS-1 dengan variasi waktu hidrotermal menunjukkan pola yang serupa pada bilangan serapan, namun mempunyai intensitas yantg berbeda – beda. Semua sampel TS–1 mempunyai puncak–puncak yang mengindikasikan gugus – gugus yang terdapat pada TS-1 , yaitu pada 1100, 1200,
960 dan 450 cm-1. Namun pada bilangan
serapan 550 cm-1 tidak semua sampel
mempunyai puncak di bilangan serapan tersebut. Intensitas pada panjang gelombang
550 cm-1 akan bertambah dengan
meningkatnya waktu hidrotermal.Hal ini dapat terlihat dari spektra yaitu sampel WH-1 belum terlihat adanya puncak pada
bilangan gelombang 550 cm-1, namun mulai
terlihat terbentuknya puncak pada WH-1 dan WH-2 dan benar –benar terdapat puncak
pada WH-3. Sampel WH-3 juga mempunyai intensitas paling tinggi pada bilangan serapan yang lain dibandingkan dengan sampel dengan waktu hidrotermal yang berbeda lainnya. Hal ini menunjukkan bahwa sampel WH-3 hari mempunyai struktur MFI yang paling sempurna dan fasanya bukan amorf.
Gambar 2 Spektra inframerah sampel a. WH-0.5, b. WH-1, c. WH-2, dan d. WH-3
Hubungan antara banyaknya struktur
MFI yang terbentuk dengan waktu
hidrotermal juga dapat dilihat dari rasio
intensitas luas area puncak pada 550 cm-1 dan
880 cm-1. Grafik 4.3 menunjukkan bahwa
semakin tinggi waktu hidrotermal rasio luas area semakin tinggi.
Terdapat korelasi antara data dari spektra FTIR dan difraktogram XRD yang menunjukkan bahwa semakin lama waktu hidrotermal maka semakin banyak struktur MFI yang terbentuk. Korelasi antara FTIR dan XRD diperlihatkan pada gambar 4.4. Pada gambar 4.4 menunjukkan perbandingan intensitas tiap sampel pada sudut 2 sekitar
23o dan perbandingan luas area puncak 550
cm-1/880 cm-1. Adanya puncak pada
bilangan gelombang 550 cm-1 dan 880 cm-1 menunjukkan banyaknya struktur MFI yang terbentuk. Sedangkan pada difraktogram banyaknya struktur MFI yang terbentuk ditunjukkan dengan adanya puncak pada
sudut 2θ sekitar 23o. Baik pada spektra IR
1 4 0 0 1 2 0 0 1 0 0 0 8 0 0 6 0 0 4 0 0
b
c
d
a
%
T
0.5 1.0 1.5 2.0 2.5 3.0 -0.2
0.0 0.2 0.4 0.6 0.8 1.0 1.2 1.4 1.6 1.8
-50 0 50 100 150 200 250 300 350
I
p
ad
a
2
θ
=2
3
o p
ad
a
di
fr
ak
to
gr
am
X
R
D
Waktu Hidrotermal
L
ua
s
A
re
a
550
cm
-1
/
880
cm
-1
pa
da
sp
ek
tr
a
FT
IR
maupun pada difraktogram menunjukkan pola yang sama, yaitu semakin lama waktu hidrotermal maka semakin banyak struktur MFI yang terbentuk
Gambar 4.4 korelasi data spektra FTIR dan difraktogram XRD pada TS-1 mesopori dengan variasi waktu hidrotermal
4.3.3 Adsorpsi Desorpsi Nitrogen
Adsorpsi desorpsi nitrogen
digunakan untuk menentukan luas
permukaan suatu padatan, yaitu fisisorbsi suatu gas inert seperti nitrogen atau argon, kemudian ditentukan berapa banyak molekul yang dibutuhkan untuk memenuhi seluruh permukaan membentuk lapisan tunggal. Luas suatu permukaan atau porositas dapat dicapai dengan mengetahui isoterm adsopsinya, ketika kuantitas dari adsorbat (bahan yang diserap) pada permukaan material dapat diukur dalam kisaran tekanan relatif yang lebar pada suhu konstan maka akan mengasilkan sebuah isotherm.
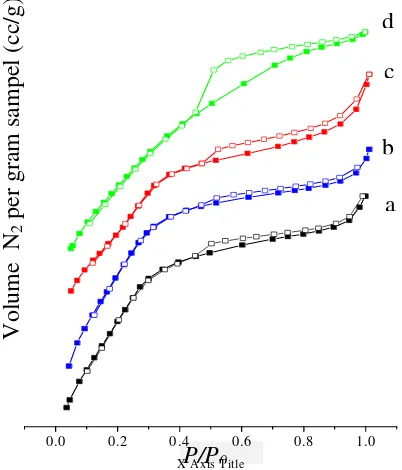
Isoterm adsorpsi desorpsi nitrogen ditunjukkan pada gambar 4.5. Grafik isoterm adsorpsi menggambarkan tipe IV yang merupakan sifat khas pada material mesopori dimana terdapat loop histerisis pada semua sampel yang berbeda variasi waktu hidrotermalnya. Dari grafik dapat dilihat
bahwa pada tekanan P/P0 = 0 gas yang
teradsorp sangat sedikit, dan daerah monolayer belum penuh kemudian pada saat
tekanan dinakkan lebih dari 0.1 mulai terjadi adsorpsi gas yang menjenuhi monolayer. Jumlah gas yang teradsorp adalah kecil, tetapi masih lebih besar dibandingkan dengan material non pori. Perubahan yang tajam
terjadi pada tekanan relatif (P/P0) sekitar 0.1
– 0.3 yang menunjukkan terjadinya pengisian mesopori, kemudian permukaan padatan akan tertutup oleh molekul nitrogen sehingga
membentuk lapisan tunggal (monolayer).
Perubahan ini merupakan karakteristik dari batas distribusi ukuran pori (Eimer, 2006). Semua sampel menunjukkan pola yang sama,
dengan kata lain semua sampel
mengindikasikan adanya mesopori.
Indikasi tersebut diperkuat dengan terjadinya loop histerisis yaitu ketika tekanan diturunkan untuk desorpsi gas di
Gambar 4 Grafik isoterm adsorpsi-desorpsi
N2 dari sampel a. WH-0.5, b.
WH-1, c. WH-2, dan d. WH-3
mana jumlah gas yang terdesorpsi tidak sama dengan jumlah yang teradsorpsi di awal. Pada tekanan yang sama, jumlah gas yang tertinggal di permukaan material ketika desorpsi masih lebih banyak dibandingkan ketika adsorpsi. Dengan kata lain, jumlah gas yang terdesorpsi lebih kecil daripada yang teradsorpsi. Hal ini disebabkan oleh kondensasi kapiler karena adanya pori dengan ukuran meso. Adanya pori pada permukaan padatan akan memberikan efek
a
b
c
d
V
ol
um
e
N
2p
er
g
ra
m
s
am
pe
l (
cc
/g
)
P/P
00.0 0.2 0.4 0.6 0.8 1.0
pembatasan jumlah lapisan pada adsorbat dan terjadi fenomena kondensasi kapiler ( Adamson,1990).
Isoterm adsorpsi desorpsi nitrogen semua sampel menunjukkan adanya loop
histerisis. Pada Gambar 4.5, Loop histerisis
teramati saat desorpsi pada tekanan relatif
P/P0 0,45-1 pada sampel WH 0.5 WH- 1 ,
WH-2 , WH-3. Loop histerisis yang paling besar terjadi pada sampel dengan waktu hidrotermal 3 hari, hal ini menunjukkan bahwa N2 yang tertingggal pada saat desorpsi paling besar. Sedangkan loop histerisis terkecil terjadi pada sampel dengan waktu hidrotermal 1 hari, hal ini menunjukkan bahwa N2 yang tertinggal pada saat desorpsi paling kecil, dalam arti jumlah materi ukuran mesopori nya paling kecil.
Karakteristik ukuran pori meso juga dapat dilihat dari data grafik distribusi ukuran pori yang menggunakan metode BJH (Barret, Joiner, Halenda). Distribusi ukuran pori masing - masing sampel dengan waktu hidrotermal yang berbeda ditunjukkan pada grafik 4.5.Material mesopori mempunyai distribusi ukuran pori yang bervariasi , dari grafik distribusi ukuran pori terlihat bahwa semua sampel mengalami kenaikan pada daerah 2- 5 nm, yaitu tepatnya pada 3,8 nm dan 3,054 nm. Bentuk grafik distribusi yang teramati merupakan karakteristik mesopori dengan diameter pori 3,8 nm, namun pada sampel dengan waktu hidrotermal 2 hari diameter porinya 3,054 nm.
Hasil analisis permukaan dan struktur pori dengan metode adsorpsi desorpsi nitrogen ditunjukkan pada tabel 1 Pada sampel WH-0,5 fase meso yang besar ditunjukkan dengan diameter yang cukup besar yaitu 3,835 nm dan volume porinya 0,21 cc/g. Sementara sampel WH-1 mempunyai volume 0,17 cc/g dan diameter porinya 3,05 nm. Sedangkan WH-2 memiliki volume pori 0,34 cc/g dan diameter pori 3,8 nm, serta untuk sampel WH-3 volume porinya sebesar 0.21 cc/g dan diameter porinya 3,8 nm. Hasil tersebut menunjukkan bahwa diameter pori setiap sampel hampir sama yaitu sekitar 3,8 nm kecuali pada WH-1 yaitu sebesar 3,054 nm.
Gambar 6 Distribusi ukuran pori sampel a. WH- 0.5, b. WH-1, c. WH-2, dan d. WH-3 dimana dV adalah perubahan volume
adsorbat pada tiap-tiap
diameter pori per gram sampel.
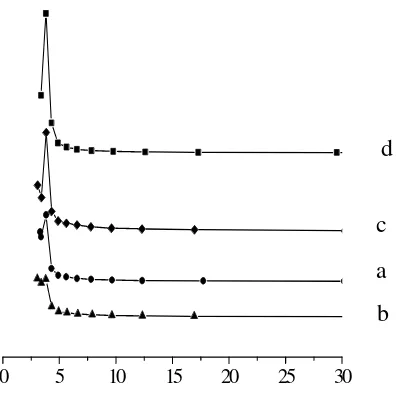
Analisis distribusi ukuran pori juga dapat dilakukan dengan metode t-plot. Metode ini didasarkan pada perbandingan data adsorpsi isoterm dari sampel berpori dan sampel nonpori (Storck dkk, 1998). Gambar 4.7 merupakan grafik t-plot dari sampel TS-1 Mesopori yang disintesis dengan variasi waktu hidrotermal. Pada grafik terlihat bahwa setiap sampel memiliki pola yang berbeda. Menurut Storck dkk (1998) plot garis linier yang identik dengan plot grafik sampel merupakan karakteristik dari bentuk padatan nonpori. Plot grafik yang horizontal terhadap plot garis linier adalah ciri dari padatan mikropori, sedangkan plot grafik yang vertikal terhadap plot garis linier merupakan bentuk khas dari padatan mesopori. Kombinasi dari plot horizontal dan vertikal menandakan adanya 2 tipe pori dalam sampel yaitu mikro dan mesopori. Seluruh sampel menunjukkan adanya garis vertikal maupun horizontal terhadap garis linear. Sehingga dapat disimpulkan bahwa semua sampel terdapat pori ukuran meso dan mikro atau dapat dikatakan bahwa ukuran porinya tidak seragam.
m
e
A
ds
or
ps
i
(m
L
/g
)
d
a
b
c
Gambar 4.7 Grafik t-plot untuk sampel a.
WH- 0.5, b. WH- 1, c. WH-2, dan d. WH-3
L
ua
s
ar
ea m
i-kr op o-ri (m 2 /g ) 98 9, 45 92 5, 55 99 7, 9 55 2, 77 L ua s ar ea m es o-po ri (m 2 /g ) 14 4, 17 10 6, 21 19 4, 5 19 2, 33 R at a-ra ta D ia -m et er Po ri (n m ) 2.
73 2.4
2,
65
2,
76
% Poro - sitas (Vm
e-so po ri / Vto ta l
x 100 %)
31 ,3 27 ,4 42 ,9 8 40 ,7 0 V ol u-m e T ot al Po ri pa da P/ P0 = 0, 99 (c c/ g) 0, 67 1 0, 62 4 0, 79 1 0, 51 6 D ia -m et er Po ri (B JH D e-so rp -si ) (n m ) 3, 83 5 3, 05 4 3, 84 3 3, 8 V ol u-m e M es o-po ri (B JH D e-so rp si ) (c c/ g) 0, 21 0, 17 0, 34 0, 21 V ol u-m e M ik ro -po ri ( t-Pl ot ) (c c/ g) 0, 36 7 0, 37 2 0, 34 6 0, 29 1 L ua s Pe r-m uk a -a n (B E T ) (m
2 /g )
11 33 , 62 10 31 , 76 11 92 , 40 74 5, 0 7 W
ak -tu
H id r ot er m al (h ar i
) 0.5 1 2 3
Sa m -pe l W H -0. 5 W H -1 W H -2 W H -3
2. Spektroskopi Inframerah
Spektra Inframerah dari sampel ditunjukkan pada Gambar 2. Pada gambar tersebut terlihat bahwa semua sampel menghasilkan spektra yang sama dengan spektra ZSM-5 komersial yaitu pada bilangan gelombang sekitar 1220, 1110, 800, 550, dan
450 cm-1. Hal ini menunjukkan bahwa pada
semua sampel tersebut terbentuk kristal ZSM-5. Pita absorpsi sekitar 1090, 790, dan
450 cm-1 menunjukkan adanya ikatan internal
dalam tetrahedral SiO4 (atau AlO4), dimana
puncak ini tidak sensitif terhadap perubahan struktur (Goncalves dkk, 2008). Gambar 2
menunjukkan semakin lama waktu aging,
intensitas pita yang terbentuk relatif semakin tinggi. Hal ini menunjukkan semakin terbentuknya Si-O-Si tetrahedral. Pita serapan pada bilangan gelombang sekitar
1100 cm-1 merupakan mode vibrasi asimetris
Si-O-Si, dan pita serapan pada bilangan
gelombang sekitar 800 cm-1 merupakan mode
vibrasi simetri. Sementara itu, pita absorpsi
pada daerah sekitar 1226, dan 544 cm-1
merupakan puncak karakteristik untuk zeolit dengan struktur MFI, yang berhubungan dengan struktur pembangun sekunder zeolit MFI dan sensitif terhadap perubahan struktur (Goncalves dkk, 2008). Pada umumnya, pita ini akan bergeser dengan perubahan rasio silikon terhadap alumunium. Oleh karena itu, puncak ini dijadikan dasar untuk mengetahui pembentukan ZSM-5. Pada pita absorpsi
sekitar 544 cm-1 menunujukkan adanya gugus
pentasil yang merupakan karakteristik dari ZSM-5.
Tabel 2. Bilangan gelombang dalam cm-1 dari
spektra inframerah sampel.
Gambar 2. Spektra FTIR ZSM-5 komersial mikropori (d) dan ZSM-5 mesopori dengan variasi
waktu aging 24 (a), 12 (b),
dan 6 jam (c)
Dari gambar 2 terlihat lebar pita yang semakin berkurang dengan bertambahnya
waktu aging pada bilangan gelombang antara
600-550 cm-1. Menurut Kirschhock dkk
(1999) lebar pita akan berkurang dengan meningkatnya kristalinitas pada bilangan
gelombang antara 600-550 cm-1, sehingga
dapat dikatakan bahwa kristalinitas sampel akan menurun dengan berkurangnya waktu
aging.
Intensitas pada bilangan gelombang
550 cm-1 mengindikasikan jumlah prekursor
zeolit (Goncalves dkk, 2008). Gambar 2
menunjukkan intensitas pada 550 cm-1 dari
sampel menurun dengan berkurangnya waktu
aging. Hal ini mengindikasikan bahwa
jumlah prekursor zeolit pada sampel semakin berkurang.
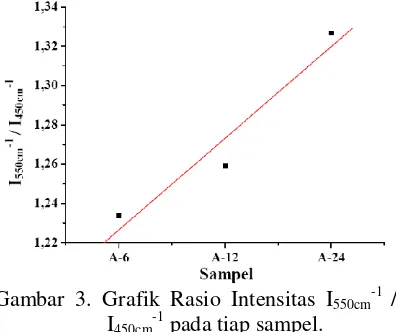
Gambar 3. Grafik Rasio Intensitas I550cm-1 /
I450cm-1 pada tiap sampel.
Pada grafik diatas dapat terlihat rasio
intensitas I550cm-1 / I450cm-1 yang semakin
bertambah dengan meningkatnya waktu
aging. Rasio intensitas I550cm-1 / I450cm-1 identik
dengan kristalinitas sampel (Goncalves dkk,
2008). Semakin besar rasio intensitas I560cm-1 /
I450cm-1 maka kristalinitasnya semakin
meningkat.
3. Adsorpsi – Desorpsi Nitrogen
Adsorpsi nitrogen merupakan
adsorpsi fisik yang digunakan dalam metode BET untuk menentukan total luas permukaan dan struktur pori suatu padatan (Haber dkk, 1995). Persamaan BET hanya dapat digunakan untuk adsorpsi isoterm yang mempunyai nilai P/P0 berkisar antara 0.05 sampai 0.3 (Adamson, 1990).
Isoterm linier dari sistem adsorpsi-desorpsi nitrogen untuk masing-masing sampel ditunjukkan pada Gambar 4. Gambar tersebut merupakan grafik jumlah adsorpsi nitrogen terhadap tekanan relatif P/P0. Pada Gambar 4.4 tersebut, dapat dilihat bahwa isoterm adsorpsi nitrogen semua sampel ZSM-5 menunjukkan pola yang serupa dimana terjadi kenaikan secara cepat pada tekanan relatif (P/P0) rendah, kemudian naik perlahan pada pertengahan dan naik lagi dengan cepat pada P/P0 mendekati satu. Kenaikan pertama terjadi karena molekul gas yang teradsorp berinteraksi dengan daerah yang berenergi pada permukaan padatan. Pada pengisian ini telah terbentuk lapisan tunggal, kemudian pada daerah P/P0 yang lebih tinggi, pertambahan molekul gas terjadi pada permukaan yang telah ditempati molekul gas dimana telah terbentuk lapisan tunggal. Pada pertambahan ini terbentuk lapisan berlapis (multilayer) dan pada akhir pengisian, terjadi kondensasi melekul gas yang teradsorp, selain itu juga terlihat adanya
loop histerisis pada daerah pertengahan.
Isoterm ini merupakan isoterm Tipe IV yaitu jenis adsorpsi dari padatan berpori meso, yang memiliki ukuran pori 2-50 nm (Gregg dan Sing, 1982).
Adanya pori pada permukaan
padatan akan memberikan efek pembatasan jumlah lapisan pada adsorbat dan terjadi fenomena kondensasi kapiler. Kondensasi kapiler ini menyebabkan terjadinya histerisis
tekanan relatif yang hampir sama dari 0,55 sampai 0,8, yang berarti distribusi ukuran porinya hampir identik pada kisaran 3 – 6 nm
(Choi, et al., 2008). Berdasarkan pola
adsorpsi awal ini telah dapat disimpulkan secara umum bahwa katalis ZSM-5 dengan
waktu aging 6, 12, maupun 24 jam
menunjukkan profil adsorpsi tipe IV
karakteristik padatan berpori meso.
Gambar 4. Grafik isoterm adsorpsi-desorpasi N2 dari ZSM-5 dengan
variasi waktu aging 6, 12,
dan 24 jam.
Selain itu, dari gambar 4 terlihat bahwa loop
histerisis paling besar pada sampel ZSM-5 A-6. Hal ini menunjukkan bahwa jumlah adsorbat (N2) yang tertinggal dalam pori saat
desorpsi paling banyak, yang
mengindikasikan bahwa jumlah mesopori pada ZSM-5 A-6 paling banyak.
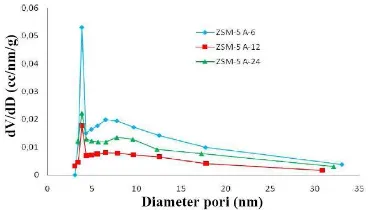
Pembuktian terhadap adanya pori meso pada permukaan padatan dapat dilihat dari data distribusi ukuran pori yang pada Gambar 5.
Gambar 5. Distribusi ukuran pori sampel
katalis ZSM-5 aging 6,12, dan
24 jam.
Berdasarkan Gambar 5, dapat disimpulkan bahwa adanya histeresis pada seluruh sampel ZSM-5 disebabkan adanya pori berukuran meso. Hal ini ditunjukkan oleh grafik
distribusi ukuran pori yang terus
menunjukkan kenaikan pada diameter pori lebih dari 2 nm (sekitar 3,8 nm), sehingga dapat disimpulkan bahwa katalis ZSM-5 A-6, ZSM-5 A-12, dan ZSM-5 A-24 memiliki pori berukuran meso.
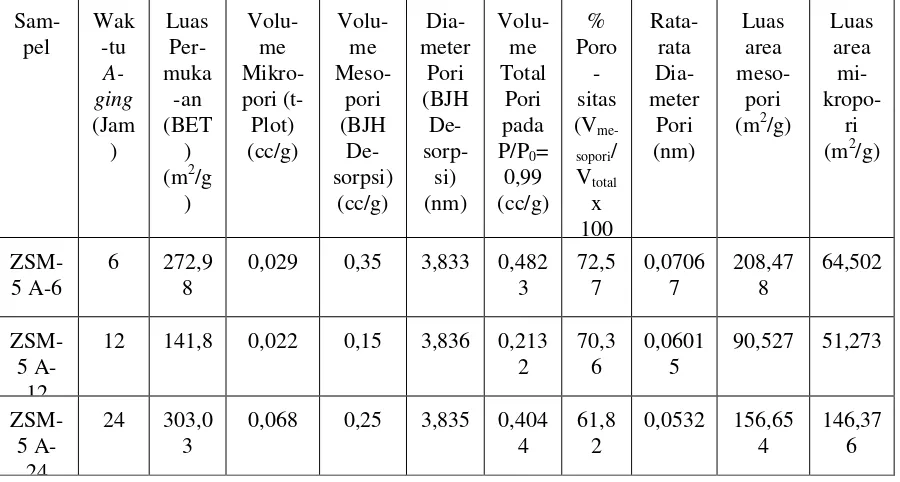
Hasil analisis permukaan dan struktur pori dengan adsorpsi-desorpsi nitrogen ditunjukkan pada tabel 3. Dari tabel
tersebut dapat dilihat bahwa waktu aging
berpengaruh pada porositas. Semakin lama
waktu aging maka porositasnya semakin
kecil. Goncalves (2008) menjelaskan
pengaruh waktu aging dalam sintesis ZSM-5
bahwa suatu peningkatan waktu aging akan
menghasilkan suatu perubahan yang cepat dari aluminosilikat mesopori menjadi ZSM-5,
hal ini mengindikasikan bahwa waktu aging
gel yang lebih lama meningkatkan jumlah prekursor ZSM-5 yang terbentuk sehingga
porositasnya berkurang. Waktu aging tidak
memberikan pengaruh pada ukuran diameter pori. Ukuran diameter pori dipengaruhi oleh ukuran templat yang digunakan dalam sintesis.
Evaluasi dstribusi ukuran pori pada
daerah mikropori dibutuhkan untuk
membuktikan adanya mikropori pada suatu katalis yang memiliki grafik isoterm tipe IV. Salah satu metode yang digunakan untuk analisa permukaan mikropori adalah t-plot. Metode ini didasarkan pada perbandingan data adsorpsi isoterm dari sampel berpori dan sampel nonpori (isoterm acuan = tipe II)
(Storck et.al., 1998). Grafik 6 merupakan
grafik t-plot untuk semua sampel. Dari grafik tersebut dapat dilihat bahwa semua sampel
ZSM-5 yang di-aging selama 6, 12, dan 24
jam memiliki pola yang sama. Garis horisontal dari garis linier mengindikasikan adanya mikropori, sedangkan garis vertikal
menunjukkan adanya mesopori (Storck et.al.,
ka
re
na
m
en
ga
nd
un
g
po
ri
ya
ng
be
ru
ku
ra
n
m
ik
ro
(<
2
n
m
) d
an
m
es
o (
2-5
0 n
m
).
Luas area mi-
kropo-ri (m2/g)
64,502
51,273
146,37 6 Luas
area meso-pori (m2/g)
208,47 8
90,527
156,65 4
Rata-rata Dia-meter
Pori (nm)
0,0706 7
0,0601 5
0,0532 %
Poro -sitas (V
me-sopori/ Vtotal x 100 72,5 7
70,3 6
61,8 2
Volu-me Total
Pori pada P/P0= 0,99 (cc/g)
0,482 3
0,213 2
0,404 4
Dia-meter Pori (BJH
De-
sorp-si) (nm)
3,833
3,836
3,835
Volu-me
Meso-pori (BJH
De-sorpsi)
(cc/g)
0,35
0,15
0,25
Volu-me Mikro-pori (t-Plot) (cc/g)
0,029
0,022
0,068 Luas
Per-muka
-an (BET
) (m2/g
)
272,9 8
141,8
303,0 3 Wak
-tu A-ging (Jam
)
6
12
24
Sam-pel
ZSM-5 A-6
ZSM-5
A-12
ZSM-5 A-24
Gambar 6 Grafik t-plot untuk semua sampel
ZSM-5 (aging 6, 12, dan 24
jam).
4. Scanning Electron Microscopy (SEM) Gambar 7 adalah morfologi dari
sampel ZSM-5 dengan variasi waktu aging 6,
12, dan 24 jam. Pada gambar tersebut dapat
dilihat bahwa sampel pada aging 12 jam
memiliki partikel yang lebih seragam dibandingkan dengan sampel pada waktu
aging 6 dan 24 jam.
Gambar 7. Morfologi SEM ZSM-5 mesopori
dengan variasi waktu aging
(a) Perbesaran 5000 kali dan (b) Perbesaran 20000 kali.
Selain itu, dari gambar diatas dapat dilihat bahwa ukuran partikel semakin besar dengan
adanya pengurangan waktu aging. Waktu
aging yang semakin lama mengakibatkan
ukuran partikel yang semakin kecil karena inti ZSM-5 yang terbentuk semakin banyak sehingga pada saat kristalisasi, inti tersebut menjadi kristal yang ukurannya kecil tetapi jumlahnya banyak. Salah satu ukuran partikel dari tiap-tiap sampel yang ditandai dengan lingkaran berwarna merah adalah 1,25 x 0,35
x 1 m (Aging 6 jam), 1,2 x 0,75 x 0,65 m
(Aging 12 jam), dan 1 x 0,85 x 0,5 m (Aging
Hasil analisa SEM mendukung data analisa XRD. Pada analisa XRD dikatakan bahwa ZSM-5 A-6 merupakan sampel yang paling amorf dibandingkan dengan ZSM-5 A-12 dan ZSM-5 A-24. Fasa amorf dari ZSM-5 A-6 dibuktikan dari gambar SEM. Pada gambar tersebut terlihat bahwa partikel yang terbentuk tidak seragam baik bentuk maupun ukurannya. Bentuk yang paling banyak pada ZSM-5 A-6 adalah lembaran. Banyaknya fasa amorf diakibatkan dari mesopori yang terbentuk. Berdasarkan data adsorpsi-desorpsi nitrogen, ZSM-5 A-6 memiliki mesopori yang paling banyak sehingga fasa amorf yang terbentuk juga semakin banyak.
IV. KESIMPULAN
ZSM-5 mesopori berhasil disintesis dari TEOS sebagai sumber silika, natrium
aluminat sebagai sumber aluminium,
TPAOH sebagai templat pengarah struktur ZSM-5 MFI, dan CTABr sebagai templat
mesopori pada waktu aging 6, 12, dan 24
jam. Hasil karakterisasi XRD menunjukkan bahwa ZSM-5 yang disintesis memiliki pori berukuran mesopori yang ditunjukkan
dengan adanya puncak pada area 2θ kurang
dari 5o. Selain itu kristalinitas ZSM-5
mesopori semakin menurun dengan
berkurangnya waktu aging yang terlihat dari
penurunan intensitas. Hal ini juga didukung oleh data hasil karakterisasi spektroskopi inframerah. Berdasarkan data adsorpsi-desorpsi nitrogen, semua sampel memiliki ukuran pori sekitar 3,8 nm, sedangkan porositas ZSM-5 mesopori berkurang dengan
meningkatnya waktu aging. ZSM-5 mesopori
dengan porositas terbesar dihasilkan pada
waktu aging 6 jam yaitu sebesar 72,57 %.
Selain itu, berdasarkan analisa SEM, waktu
aging juga berpengaruh pada ukuran partikel,
semakin lama waktu aging maka ukuran
partikelnya semakin kecil.
V. UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih kepada Penelitian Strategis ITS tahun anggaran 2009 yang dibiayai melalui DIPA ITS No : 0172.0/023-04.2/XV/2009 dan kepada Dr. Didik Prasetyoko, M.Sc atas
bimbingannya sampai terselesainya
penelitian ini.
VI. DAFTAR PUSTAKA
Adamson, A.W., (1990), Physical Chemistry
of Surfaces, John Wiley & Sons, Inc,
New York.
Choi, J., Kim, J., Yoo, K.S., Lee, T.G., (2008), “Synthesis of mesoporous
TiO2/γ-Al2O3 composite granules
with different sol composition and
calcination temperature”, Powder
Technology 181, hal. 83-88.
Cundy, C.S., Cox, P.A., (2003), “The
Hydrothermal Synthesis of Zeolites: History and Development from the Earliest Days to the Present Time”,
Chemical Review, 103, hal. 663-702.
Cundy, C.S., Cox, P.A., (2005), “The hydrothermal synthesis of zeolites:
Precursors, intermediates and
reaction mechanism”, Microporous
and Mesoporous Materials 82, hal.
1-78.
Goncalves, M.L., Dimitrov, L.D., Jorda,
M.H., Wallau, M.,
Urquieta-Gonzalez, E.A., (2008), ”Synthesis of mesoporous ZSM-5 by crystallization of aged gels in the presence of
cetyltrimethylammonium cations”,
Catalysis Today, Vol. 133-135, hal.
69-79.
Gontier, S. dan Tuel, A. (1996), “Synthesis
of Titanium Silicalite-1
UsingAmorphous SiO2 as Silicon
Source”, Zeolites, Vol. 16, hal.
184-195.
Gregg, S. J. and Sing, K. S. W. (1982), “Adsorption, Surface Area and Porosity”, 2nd Edition, London:
Academic Press.
Haber, J., Block, J. H., Delmon, B. (1995), “Manual of Methods and Procedures
for Catalyst Characterization”, Pure
and Applied Chemistry, Vol. 67, hal
1257-1306.
Huang, L., Guo, W., Deng, P., Xue, Z., Li,
Q., (2000), “Investigation of
Synthesizing MCM-41/ZSM-5
Composites”, Journal of Physical
Chemistry, 104 (13), hal. 2817-2823.
Ismail, A.A., Mohaned, R.M., Fouad, O.A., Ibrahim, I.A., (2006), “Synthesis of Nanosized ZSM-5 Using Different
Alumina Sources”, Crystal Research
Jacobs, P.A., Martens, J.A., (1991),
Introduction to Zeolite Science and Practice, Study Surface Science and
Catalysis, edited by Van Bekkum, H.; Flanigen, E.M.; Jansen, Elsevier J.C.; Amsterdam, Vol. 58, hal. 445-493.
Kresge, C.T., Leonowicz, M. E. , Roth, W. J. , Vartuli, J. C., Beck, J. S. , (1992), “Ordered mesoporous molecular sieves synthesized by a liquid-crystal
template mechanism”, Nature 359,
hal. 710-712.
Kirschhock, C.E.A., Ravishankar, R., Verspeurt, F., Grobet, P. J., Jacobs, P. A., Martens, J. A., (1999), “Identification of Precursor Species in the Formation of MFI Zeolite in the TPAOH−TEOS−H2O System”,
Journal of Physical Chemistry, 103,
hal. 4965-4971.
Liu, Y., Zhang, W., Pinnavaia, T. J., (2000),
“Steam-Stable Aluminosilicate
Mesostructures Assembled from
Zeolite Type Y Seeds”, Journal
American Chemical Society, 122
(36), hal. 8791-8792.
Liu, Y., Zhang, W., Pinnavaia, T. J., (2001),
“Steam-Stable MSU-S
Aluminosilicate Mesostructures
Assembled from Zeolite ZSM-5 and
Zeolite Beta Seeds”, Angewandte
Chemie 113(7), hal. 1295-1298.
Pérez, P.J., Díaz, I., Agúndez, J., (2005), “Strategies for ordering the network
of mesoporous materials”, C. R.
Chimie 8, 569–578.
Smitha, S., Shajesh, P., Aravind, P.R., Rajesh, K.S., Pillai, P. K., Warrier, K.G.K., (2006), “Effect Of Aging Time And Concentration Of Aging
Solution On The Porosity
Characteristics Of Subcritically
Dried Silica Aerogels”, Microporous
and Mesoporous Materials 91, hal.
286-292.
Storck, S., Bretinger, H., Maier, W. F., (1998), “Characterization of micro-
and mesoporous solids by
physisorption methods and pore-size
analysis”, Applied Catalysis A:
General, Vol 174, hal. 137-146.
Wang, H., Holmberg, B., Yan, Y., (2003), “Direct synthesis of template-free
zeolite nanocrystals within in-situ
thermoreversible polymer
hydrogels”, Journal American
Chemical Society, 125, hal.
9928-9929.
Wang, X.-S., Guo, X.-W., Li, G. (2002), “Synthesis of Titanium Silicalite (TS-1) from the TPABr System and
Its Catalytic Properties for
Epoxidation of Propylene”, Catalysis
Today, Vol. 74, hal. 65-75.
Zhu, H., Liu, Z., Kong, D., Wang, Y., Yuan, X., Xie, Z., (2009), “Synthesis of
ZSM-5 with intracrystal or
intercrystal mesopores by polyvinyl
butyral templating method”, Journal
of Colloid and Interface Science,