BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tanaman
Uraian tumbuhan meliputi morfologi tanaman, habitat, sistematika tanaman, sinonim, nama asing, nama daerah, kegunaan dan kandungan kimia dari tanaman.
2.1.1 Morfologi tanaman
Buah semangka berbentuk bola sampai bulat memanjang, besar bervariasi
dengan panjang 20-30 cm, diameter 15-20 cm, dengan berat mulai dari 3-7 kg, namun terkadang ada buah semangka yang mencapai 15-20 kg. Bagian dari buah semangka terdiri ataskulit buah, daging buah dan bijinya (Widyanigrum, 2011). Kulit buah semangka tebal dan berdaging, licin, warnanya bermacam-macam seperti hijau tua, kuning agak putih, atau hjiau muda bergaris-garis putih. Daging buah warnanya merah, merah muda (pink), jingga (orange), kuning sampai putih. Biji bentuk memanjang, pipih, warnanya hitam, putih, atau cokelat kemerahan. Ada juga yang tanpa biji (seedless) (Dalimartha, 2003).
Daun semangka lebar dan menjari, mempunyai batang kecil memanjang daun ditutupi oleh bulu-bulu yang halus dan tajam. Batang tanaman semangka adalah beruas-ruas dan disetiap ruas tumbuh daun-daun tanaman. Tanaman semangka tumbuh dengan cara menjalar. Bunga tanaman semangka termasuk monoecius (berumah satu) dan berkelamin satu (unisexual). Akar tanaman
2.1.2 Habitat
Tanaman semangka berasal dari daerah tropis dan subtropis Afrika. Tumbuh liar ditepi jalan, padang belukar, pantai laut, atau ditanam di kebun dan perkarangan sebagai tanaman buah. Tanaman ini tergolong cepat berproduksi yaitu sekitar 2-4 bulan. Semangka dapat berproduksi dengan baik pada ketinggian ±1000 meter diatas permukaan laut. Suhu udara yang baik untuk pertumbuhan semangka yaitu berkisar 25-30ºC. Di Indonesia tanaman ini banyak dikembangkan disekitar kota besar diantaranya Indramayu, Cirebon, Madiun, Lombok, Sumatera Utara dan sebagainya (Barus dan Syukri, 2008).
2.1.3 Sistematika tanaman
Menurut Rukmana (1994) sistematika tanaman semangka adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledonae Ordo : Cucurbitales Famili : Cucurbitaceae Genus : Citrullus
Species : Citrullus lanatus (Thunb.) Matsum. & Nakai 2.1.4 Sinonim
2.1.5 Nama asing
Buah semangka memiliki nama asing seperti Water Melon (Inggris), Xi Gua (Cina), Hamaka (Halmahera) (Dalimartha, 2003).
2.1.6 Nama daerah
Buah semangka memiliki nama lain seperti Samangka, Semongka, Watesan, Ghuleng-ghuleng (Jawa); Mandike, Karamboja, Kalambosa, Kamandriki (Sumatera); Mendikal, Pateka (Maluku); Lamuja, Karamujo, Ramujo, Samaka (Lampung) (Dalimartha, 2003).
2.1.7 Kegunaan
Daging buah semangka digunakan untuk pengobatan tekanan darah tinggi (hipertensi), demam, mulut kering, air kemih berwarna kuning tua, sakit tenggorok, sariawan, rasa lemah, napas berbau dan menghilangkan kerutan diwajah (Widyaningrum, 2011).
2.1.8 Kandungan kimia
Daging buah semangka bersifat rendah kalori dan mengandung air sebanyak 93,4%, protein 0,5%, karbohidrat 5,3%, lemak 0,1%, serat 0,2%dan vitamin (A, B dan C). Selain itu mengandung asam amino sitrulin (C6H13N3O3),
asam aminoasetat, asam malat, asam fosfat, arginin, betain, likopen (C40H56),
2.2 Freeze Drying
Freeze drying atau disebut juga lyophilization merupakan proses untuk
menghilangkan air tanpa pemanasan berlebih. Umumnya digunakan untuk memenuhi kebutuhan farmasetik dalam meningkatkan stabilitas dan waktu simpan obat-obatan yang tidak stabil, digunakan industri makanan untuk memperpanjang waktu simpan dengan mencegah pertumbuhan mikroorganisme dan memperlambat oksidasi lipida (Nireesha et al, 2013).
Metode pengeringan freeze drying hanya sedikit mengubah warna, rasa, tekstur, nutrisi, penampilan, komponen kimia dan aktivitas biologis dari sampel yang segar sehingga disebut sebagai metode pengeringan terbaik untuk makanan yang mengandung komponen sensitif panas dan komponen antioksidan seperti tokoferol, asam askorbat, karotenoid dan fenolik (Dirim dan Gulsah, 2012).
Freeze drying adalah proses dimana air dihilangkan dari suatu produk
dengan mengatur tekanan dan temperatur dalam keadaan vakum. Terdapat 2 komponen penting yang menyusun alat freeze dryer. Komponen pertama adalah ruang pengering untuk mengkontrol temperatur dan komponen kedua adalah ruang kondensor. Ruang pengering dihubungkan dengan sebuah katup ke ruang kondensor untuk mencapai temperatur -50 sampai -80ºC.
Tahapan yang terjadi pada saat freeze drying ada 3, yaitu : a. Freezing
b. Primary drying
Produk yang sudah beku dikondisikan dalam keadaan vakum dengan tekanan 10-4 sampai 10-5 atmosfer, sehingga pelarut dari produk menguap dari fase padat ke gas tanpa melewati fase cair atau disebut dengan sublimasi. Pada proses sublimasi perlu ditingkatkan temperatur sekitar -45º sampai -20º C untuk mempercepat penguapan. Peningkatan temperatur harus terus diperhatikan agar tetap di bawah critical process temperature (suhu dimana produk kembali mencair). Pada tahap ini, penguapan pelarut belum sempurna karena masih ada sisa-sisa embun hasil sublimasi yang masih tertinggal dalam produk.
c. Secondary drying
Ada sekitar 7-8% embun sisa primary drying yang harus dikeringkan pada temperatur yang lebih tinggi untuk mengurangi kandungan air dalam produk. Proses ini disebut dengan isothermal desorption. Pada tahap ini, temperatur produk harus lebih tinggi dari temperatur lingkungannya dan tekanan diturunkan sampai minimum. Tahap ini memerlukan waktu 1/3 atau 1/2 kali lebih lama dari tahap primary drying karena memerlukan energi yang lebih besar untuk menghilangkan sisa airnya (Nireesha et al, 2013).
2.3 Radikal Bebas
kondisi demikian mudah terbentuk radikal bebas, seperti anion superoksida, hidroksil dan lain-lain. Radikal bebas juga dapat terbentuk dari senyawa lain yang sebenarnya bukan radikal bebas, tetapi mudah berubah menjadi radikal bebas (Winarsi, 2007).
Sifat radikal bebas yang tidak stabil menyebabkan reaksi menerima atau memberikan elektron dengan molekul sekitarnya.Kebanyakan molekul ini bukan radikal bebas melainkan makromolekul biologi seperti lipid, protein, asam nukleat dan karbohidrat.Dengan reaksi ini timbullah reaksi radikal bebas beruntun yaitu terbentuknya radikal bebas baru yang bereaksi lagi dengan makromolekul lain (Kosasih dkk, 2004).
Secara umum sumber radikal bebas dapat dibedakan menjadi dua yaitu endogen dan eksogen. Radikal bebas endogen dihasilkan tubuh secara alami dari proses biokimia yang berlangsung didalam sel (intraselular) dan diluar sel (ekstraselular), proses ini terjadi terus menerus selama kehidupan. Keberadaannya dalam jumlah normal berguna untuk melawan peradangan, membunuh kuman penyebab penyakit, detoksifikasi racun xenobiotik, polimerisasi dinding sel serta untuk mengendalikan tonus otot polos pada pembuluh darah dan organ-organ dalam tubuh (Lingga, 2012). Radikal bebas eksogen berasal dari luar sistem tubuh misalnya sinar UV dan lingkungan seperti radiasi, polusi, asap rokok, makanan, minuman, ozon dan pestisida (Rohmatussolihat, 2009).
Senyawa oksigen reaktif (SOR)berperan dalam berbagai proses biologis alami didalam tubuh. SOR berasal dari oksigen (O2). Berbagai proses
Secara fisiologis tubuh menghasilkan SOR, namun apabila radikal bebas atau oksidan dihasilkan secara berlebihan oleh tubuh, maka bahan tersebut akanbersifat toksik dan merusak berbagai komponen dalam tubuh, seperti DNA, lipid dan enzim. Sel tubuh dapat rusak bahkan mati sebagai akibat dari keberadaan spesies oksigen reaktif yang tidak terkendali di dalam tubuh. Golongan senyawa oksigen reaktif antara lain adalah hidroksil (OH-), superoksida (O2-), peroksidal (RO2-),
asam hipoklorit (HOCl) dan hidrogen peroksida (H2O2) (Ionita, 2005).
Secara umum (Hamid, et al., 2010), reaksi pembentukan radikal bebas melalui 3 tahapan reaksiberikut :
a. Tahap inisiasi
RH + initiator → R˙ + H˙
R˙→ R˙ + O2→ ROO˙
b. Tahap propagasi R˙ + O2 → ROO˙
ROO˙ +RH → ROOH + R˙
c. Tahap terminasi R˙ + R˙ → RR
R˙ + ROO˙ → ROOR
2.4 Antioksidan
Antioksidan adalah zat yangdalam kadar rendah bila dibandingkan dengan bahan yang dapat dioksidasi, dapat memperlambat atau menghambat oksidasi bahan tersebut secara signifikan (Halliwell, 2002).
Senyawa ini memiliki berat molekul kecil, tetapi mampu menginaktivasi berkembangnya reaksi oksidasi, dengan cara mencegah terbentuknya radikal atau dengan mengikat radikal bebas dan molekul yang sangat reaktif (Winarsi, 2007).
Menurut Kumalaningsih (2006), antioksidan tubuh dikelompokkan menjadi 3 yakni:
1. Antioksidan primer yang berfungsi untuk mencegah pembentuk senyawa radikal baru karena dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi. Contohnya adalah enzim superoksida dismutase (SOD) yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh karena radikal bebas.
2. Antioksidan sekunder merupakan senyawa yang berfungsi menangkap senyawa serta mencegah terjadinya reaksi berantai. Contohnya adalah vitamin E, vitamin C dan betakaroten yang dapat diperoleh dari buah-buahan.
3. Antioksidan tersier merupakan senyawa yang memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas. Contohnya enzim metionin sulfoksidan reduktase untuk memperbaiki DNA pada inti sel.
efektif daripada suplemen antioksidan yang diisolasi. Hal ini mungkin dikarenakan oleh adanya komponen lain dan interaksinya dalam sayur-sayuran dan buah-buahan yang berperan secara positif (Silalahi, 2006).
Senyawa antioksidan alami tumbuhan umumnya adalah senyawa fenolik atau polifenolik yang dapat berupa golongan flavonoid, kumarin, tokoferol dan asam-asam organik.Senyawa polifenolik dapat bereaksi sebagai pereduksi, penangkap radikal bebas (Kumalaningsih, 2006).
2.4.1 Vitamin C
Vitamin C berhasil di isolasi untuk pertama kalinya pada tahun 1928 oleh Albert Szent-Györgyi. Penemuan ini terjadi dikarenakan keinginan dari Albert untuk mencoba mengidentifikasi suatu komponen yang mengikat oksigen dan dapat mencegah kerusakan buah (Iqbal, et al., 2004).
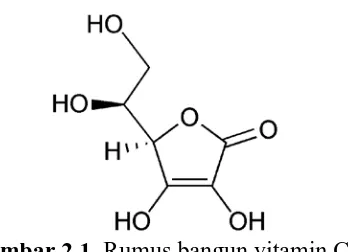
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan rumus bangun C6H8O6, dengan titik lebur 190-192°C. Asam askorbat
mengandung tidak kurang dari 99,0% C6H8O6. Pemerian: serbuk atau hablur
putih atau agak kuning, tidak berbau, rasa asam, oleh pengaruh cahaya lambat laun menjadi gelap, dalam larutan cepat teroksidasi. Kelarutan: mudah larut dalam air, agak sukar larut dalam etanol (95%) P, praktis tidak larut dalam kloroform P, dalam eter P dan dalam benzen P. Penyimpanan dalam wadah tertutup rapat, terlindung dari cahaya.Vitamin C mengandung khasiat sebagai antiskorbut (Depkes, 1979).
infeksi virus dan bakteri, berperan dalam pembentukan kolagen serta produksi neurotransmitter dan hormon tertentu dalam tubuh (Walingo, 2005).
Gambar 2.1. Rumus bangun vitamin C
(Iqbal, et al., 2004). Asam askorbat apabila terkena pengaruh oksigen, zat-zat pengoksidasi lemah, atau oleh pengaruh enzim asam askorbat oksidase, akan mempermudah senyawa ini mengalami oksidasi menjadi asam dehidroaskorbat, karena memiliki sifat mudah teroksidasi, asam askorbat digunakan sebagai antioksidan (Iqbal, et al., 2004).
2.4.2Beta karoten
Beta karoten bersifat larut dalam lemak sehingga melindungi sel dari kerusakan yang disebabkan oleh radikal bebas yang larut dalam lemak. Kemampuannya dalam menjaga integritas sel sangat baik sehingga dapat berperan sebagai antioksidan (Lingga, 2012). Rumus bangun betakaroten dapat dilihat pada Gambar 2.2.
Gambar 2.2 Rumus bangun betakaroten
(Hanson, 2005). 2.4.3 Flavonoid
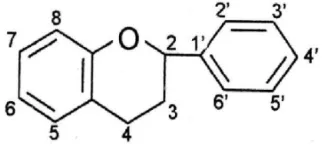
Golongan flavonoid dapat digambarkan sebagai deretan senyawa C6-C3
-C6. Kelompok terbesar flavonoid memiliki ciri adanya cincin piran yang
menghubungkan rantai tiga-karbon dengan salah satu dari cincin benzene. Senyawa ini merupakan pereduksi yang baik karena mampu menghambat reaksi oksidasi. Flavonoid pada tumbuhan berfungsi sebagai pelindung terhadap serangan jamur ataupun radiasi sinar UV yang dapat merusak tumbuhan. Selain itu, flavonoid juga terlibat dalam proses fotosintesis, transfer energi dan respirasi pada tumbuhan. Struktur umum untuk turunan flavonoid dapat dilihat pada gambar berikut:
Gambar 2.3 Rumus bangun flavonoid
2.4.4 Polifenol
Senyawa polifenol adalah senyawa yang paling sedikit memiliki satu cincin aromatik dan mengikat beberapa gugus hidroksil.Polifenol merupakan senyawa antioksidan alami yang paling banyak terdapat dalam buah-buahan dan sayuran. Sifat antioksidan yang dimiliki oleh polifenol dapat menghambat spesiesoksigen reaktif. Polifenol dapat menghambat senyawa-senyawa karsinogen dengan cara metilasi dan pembentukan glukoronid, serta pembukaan cincin, kebanyakan dari bagian katekol polifenol, akibat pengaruh dari enzim-azim dan bakteri pencernaan(Weisburger, 2004).
2.4.5 Sitrulin
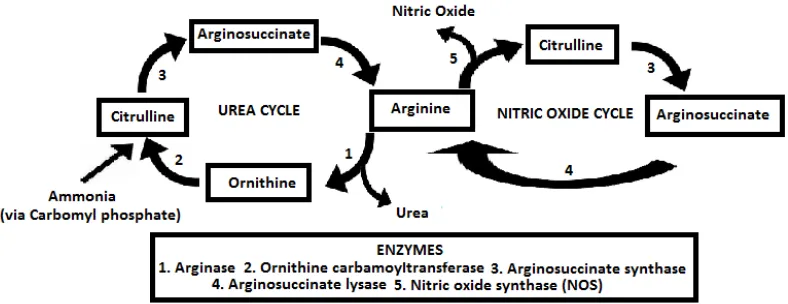
Sitrulin atau 2-amino-5-(carbamoylamino)pentanoic merupakan suatu asam amino.Sitrulindapat berubah menjadi arginin didalam ginjal serta dapat meningkakan produksi nitrogen monoksida.Proses metabolisme sitrulin didalam tubuh dapat dilihat pada gambar berikut :
Gambar 2.4 Metabolisme sitrulin didalam tubuh
didalam tubuh.Berdasarkan manfaat dan sifat dari sitrulin tersebut dapat digunakan sebagai antioksidan. Struktur umum sitrulin dapat dilihat pada gambar berikut :
Gambar 2.5 Rumus bangun sitrulin
(Cooke dan Oka, 2001)
2.5 Penentuan Aktivitas Antioksidan dengan Metode DPPH
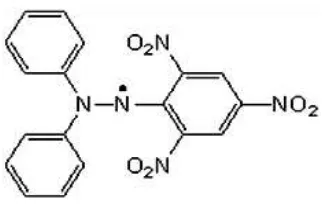
Pada tahun 1922, Goldschmidt dan Renn menemukan senyawa berwarna ungu radikal bebas stabil DPPH.DPPH berwarna sangat ungu seperti KMnO4 dan
tidak larut dalam air (Ionita, 2005).
Gambar 2.6 Rumus bangun DPPH
(Prakashet.al., 2001).
ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan. Perubahan warna ini berdasarkan reaksi kesetimbangan kimia (Prakashet.al., 2001).
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah harga konsentrasi efisien atau efficient concentration (EC50) atau Inhibition
Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan % penghambatan 50%. Zat yang mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah
(Molyneux, 2004). 2.5.1 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut metanol atau etanol dan kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.5.2 Pengukuran absorbansi – panjang gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam
pengukuran uji sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang maksimum untuk DPPH antara lain 515-520 nm, bagaimanapun dalam praktiknya hasil pengukuran yang memberikan peak maksimum itulah panjang gelombangnya yaitu sekitar panjang gelombang yang disebutkan diatas. (Molyneux, 2004).
2.5.3 Pengukuran waktu operasional (operating time)
operasional ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan (Rohman, 2007).
2.6 Spektrofotometri UV-Visible
Prinsip kerja spektrofotometer UV-Vis berdasarkan penyerapan cahaya atau energi radiasi oleh suatu larutan. Jumlah cahaya atau energi radiasi yang diserap memungkinkan pengukuran jumlah zat penyerap dalam larutan secara kuantitatif (Triyati, 1985).Panjang gelombang untuk sinar ultraviolet antara 200-400 nm sedangkan panjang gelombang untuk sinar tampak/visible antara 200-400-750 nm (Gandjar dan Rohman, 2007).