INTISARI
Penelitian ini bertujuan untuk mengetahui efek hepatoprotektif pemberian jangka panjang dekok herba Bidens pilosa L. pada tikus betina galur Wistar terinduksi karbon tetraklorida, beserta dosis efektifnya.
Penelitian ini menggunakan tikus betina galur Wistar, umur 2-3 bulan, dan berat 120-200 gram. Tikus dibagi secara acak ke dalam 6 kelompok, tiap kelompok 5 ekor tikus. Kelompok I (kontrol hepatotoksin) diberi karbon tetraklorida 2 ml/kg BB. Kelompok II (kontrol negatif) diberi olive oil 2 ml/kg BB. Kelompok III (kontrol dekok) diberi dekok herba Bidens pilosa L. 2 g/kgBB. Kelompok IV-VI (kelompok perlakuan) diberi dekok herba Bidens pilosa L. satu kali sehari selama enam hari dengan dosis 0,5; 1; dan 2 g/kgBB, kemudian pada hari ke-7 diinduksi karbon tetraklorida 2 ml/kgBB. Pada jam ke-24 setelah pemberian karbon tetraklorida dilakukan pemeriksaan aktivitas serum ALT dan AST pada semua kelompok perlakuan. Data aktivitas serum ALT dan AST dianalisis menggunakan one way ANOVA dengan taraf kepercayaan 95% dan dilanjutkan uji Scheffe atau uji T berpasangan.
Hasil penelitian ini menunjukkan bahwa pemberian dekok herba Bidens pilosa L. memiliki efek hepatoprotektif dengan menurunkan aktivitas serum ALT dan AST. Efek hepatoprotektif yang dihasilkan dari dosis terendah ke dosis tertinggi sebesar 71,5; 85,8; 44,0%. Dari data diperoleh dosis efektif pemberian dekok herba
Bidens pilosa L., yaitu 1 g/kgBB.
ABSTRACT
The aim of study research were to prove long-term administration of Bidens pilosa L. herb decoction in female Wistar rats induced carbon tetrachloride, and the effective dose.
This research use female Wistar rats, aged 2-3 months, and the weight 120-200 grams. Rats were randomly divided into six groups, each group had five rats. Group I (control hepatotoxins) induced by carbon tetrachoride 2 mL/kgBW. Group II (negative control) were given olive oil 2 ml/kgBW. Group III (control decoction) were given decoction of herbs Bidens pilosa L. 2 g/kg. Group IV-VI (treatment group) were given Bidens pilosa L. herb decoction once a day for six days with a dose started from 0.5; 1; and 2 g/kgBW, then in seventh day the group induced by carbon tetrachloride 2 ml/ kgBW. At the 24th hours after administrated of carbon tetrachloride, ALT and AST activities were examinated in all treatment groups. Data ALT and AST activities were analyzed using one-way ANOVA with 95% significancy level and continued with Scheffe test or paired t test.
The results showed that administration of Bidens pilosa L. herb decoction has a hepatoprotective effect by lowering ALT and AST activities. Hepatoprotective effects from the lowest to the highest doses were 71.5; 85.8; 44.0%. From the data, the effective dose of Bidens pilosa L. herb decoction were 1 g/kgBW.
EFEK HEPATOPROTEKTIF PEMBERIAN JANGKA PANJANG DEKOK
HERBA Bidens pilosa L. TERHADAP AKTIVITAS ALT-AST SERUM
PADA TIKUS BETINA TERINDUKSI KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Apriyanto Gomes
NIM : 118114127
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
EFEK HEPATOPROTEKTIF PEMBERIAN JANGKA PANJANG DEKOK
HERBA Bidens pilosa L. TERHADAP AKTIVITAS ALT-AST SERUM
PADA TIKUS BETINA TERINDUKSI KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Apriyanto Gomes
NIM : 118114127
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
iv
HALAMAN PERSEMBAHAN
Since everything is a reflection of your minds, everything can be changed by our minds
- Buddha -
If you are depressed, you are living in the past. If you are anxious, you are living in the future. If you are at peace you are living in the present
- Lao Tzu -
Bersama ini, saya persembahkan karya ini kepada: Tuhan Yang Maha Esa
Ayah, ibu sebagai ungkapan rasa hormat dan baktiku Kakak, adik serta keluarga besarku
Bapak/Ibu dosen Fakultas Farmasi Universitas Sanata Dharma Sahabat-sahabatku terkasih
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN JUDUL PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
PRAKATA ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
INTISARI ... xviii
ABSTRACT ... xix
BAB I. PENGANTAR ... 1
A. Latar Belakang... 1
1. Perumusan masalah ... 3
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 4
B. Tujuan Penelitian ... 5
BAB II. PENELAAHAN PUSTAKA... 6
x
1. Anatomi fisiologi hati ... 6
2. Jenis kerusakan hati ... 8
3. Hepatotoksin ... 9
4. ALT-AST ... 10
5. Evaluasi kerusakan hati ... 11
B. Karbon Tetraklorida... 13
C. Bidens pilosa Linn ... 16
1. Taksonomi ... 16
2. Nama daerah ... 17
3. Morfologi ... 17
4. Kandungan kimia dan kegunaan ... 18
D. Dekok ... 19
E. Landasan Teori... 20
F. Hipotesis ... 21
BAB III. METODE PENELITIAN... 22
A. Jenis dan Rancangan Penelitian... 22
B. Variabel dan Definisi Operasional... 22
1. Variabel utama ... 22
2. Variabel pengacau ... 22
3. Definisi operasional ... 23
C. Bahan Penelitian... 23
D. Alat Penelitian... 25
2. Alat pembuatan dekok herba Bidens pilosa L ... 25
3. Alat uji penetapan kadar air ... 25
4. Alat uji hepatoprotektif ... 25
E. Tata Cara Penelitian ... 26
1. Determinasi tanaman herba Bidens pilosa L ... 26
2. Pengumpulan bahan uji ... 26
3. Pembuatan serbuk herba Bidens pilosa L ... 26
4. Penetapan kadar air serbuk herba Bidens pilosa L ... 26
5. Pembuatan dekok herba Bidens pilosa L ... 26
6. Pembuatan hepatotoksin karbon tetraklorida konsentrasi 50% .. 27
7. Uji pendahuluan ... 27
8. Pengelompokkan dan perlakuan hewan uji ... 28
9. Pembuatan serum ... 29
10. Pengukuran aktivitas serum ALT dan AST ... 30
F. Tata Cara Analisis Hasil ... 30
BAB IV. HASIL DAN PEMBAHASAN ... 32
A. Penyiapan Bahan ... 32
1. Hasil determinasi tanaman ... 32
2. Penetapan kadar air serbuk herba Bidens pilosa L ... 32
B. Uji Pendahuluan... 33
1. Penentuan dosis hepatotoksin ... 33
2. Penentuan dosis herba Bidens pilosa L ... 33
xii
C. Hasil Uji Efek Hepatoprotektif Dekok Herba Bidens pilosa L ... 37
1. Kontrol hepatotoksin karbon tetraklorida dosis 2 mL/kgBB ... 41
2. Kontrol negatif olive oil dosis 2 mL/kgBB ... 42
3. Kontrol dekok herba Bidens pilosa L. dosis 2 g/kgBB ... 44
4. Kelompok perlakuan herba Bidens pilosa L. dosis 0,5;1;2 g/kgBB pada tikus betina galur Wistar terinduksi karbon tetraklorida ... 45
D. Rangkuman Pembahasan ... 49
BAB V. KESIMPULAN DAN SARAN ... 52
A. Kesimpulan ... 52
B. Saran ... 52
DAFTAR PUSTAKA ... 53
LAMPIRAN ... 57
DAFTAR TABEL
Tabel I. Peningkatan relatif dari beberapa serum enzim pada cedera hati .... 16
Tabel II. Komposisi dan konsentrasi reagen serum ALT ... 24
Tabel III. Komposisi dan konsentrasi reagen serum AST ... 25
Tabel IV. Purata aktivitas serum ALT ± pada selang waktu 0, 24, dan 48
jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB ... 34
Tabel V. Hasil uji Scheffe aktivitas serum ALT pada selang waktu 0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2
mL/kgBB ... 35
Tabel VI. Purata aktivitas serum AST ± SE pada selang waktu 0, 24, dan
48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB .... 35
Tabel VII. Hasil uji Scheffe aktivitas serum AST pada selang waktu 0, 24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2
mL/kgBB ... 36
Tabel VIII. Purata ± SE aktivitas serum ALT dan AST tikus betina galur
Wistar pada kelompok perlakuan ... 38
Tabel IX. Hasil uji Scheffe aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan... 40
Tabel X. Hasil uji Scheffe aktivitas serum AST tikus betina galur Wistar pada kelompok perlakuan... 41
Tabel XI. Purata ± SE aktivitas serum ALT dan AST setelah pemberian
xiv
Tabel XII. Hasil uji T berpasangan aktivitas serum ALT dan AST
DAFTAR GAMBAR
Gambar 1. Anatomi hati ... 6
Gambar 2. Mekanisme biotransformasi karbon tetraklorida ... 14
Gambar 3. Mekanisme peroksidasi lipid oleh radikal CCL3 ... 15
Gambar 4. Herba Bidens pilosa L. ... 17
Gambar 5. Struktur flavonoid herba Bidens pilosa L. ... 19
Gambar 6. Diagram batang purata aktivitas serum ALT pada selang waktu 0,24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mg/kgBB ... 34
Gambar 7. Diagram batang purata aktivitas serum AST pada selang waktu 0,24, dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mg/kgBB ... 36
Gambar 8. Diagram batang purata aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan ... 39
Gambar 9. Diagram batang purata aktivitas serum AST tikus betina galur Wistar pada kelompok perlakuan ... 39
Gambar 10. Diagram batang purata aktivitas serum ALT setelah pemberian olive oil dosis 2 mL/kgBB pada selang waktu 0 dan 24 jam ... 44
xvi
DAFTAR LAMPIRAN
Lampiran 1. Foto serbuk herba Bidens pilosa L. ... 57 Lampiran 2. Foto pembuatan dekok herba Bidens pilosa L. ... 57 Lampiran 3. Foto dekok herba Bidens pilosa L. ... 57 Lampiran 4. Surat pengesahan determinasi tanaman herba Bidens pilosa L. 58 Lampiran 5. Surat pengesahan Medical and Health Research Ethics
Committee (MHREC) ... 59 Lampiran 6. Analisis statistik aktivitas serum ALT pada uji pendahuluan
dosis hepatotoksin karbon tetraklorida 2 mL/kgBB ... 60
Lampiran 7. Analisis statistik aktivitas serum AST pada uji pendahuluan
dosis hepatotoksin karbon tetraklorida 2 mL/kgBB ... 62
Lampiran 8. Analisis statistik aktivitas serum ALT pada kelompok kontrol
olive oil 2 mL/kgBB ... 64 Lampiran 9. Analisis statistik aktivitas serum AST pada kelompok kontrol
olive oil 2 mL/kgBB ... 66 Lampiran 10. Analisis statistik aktivitas serum ALT pada perlakuan dekok
herba Bidens pilosa L. setelah induksi karbon tetraklorida 2 mL/kgBB ... 68
Lampiran 11. Analisis statistik aktivitas serum AST pada perlakuan dekok
herba Bidens pilosa L. setelah induksi karbon tetraklorida 2 mL/kgBB ... 72
Lampiran 13. Perhitungan konversi dosis herba Bidens pilosa L. untuk manusia ... 75
xviii INTISARI
Penelitian ini bertujuan untuk mengetahui efek hepatoprotektif pemberian jangka panjang dekok herba Bidens pilosa L. pada tikus betina galur Wistar terinduksi karbon tetraklorida, beserta dosis efektifnya.
Penelitian ini menggunakan tikus betina galur Wistar, umur 2-3 bulan, dan berat 120-200 gram. Tikus dibagi secara acak ke dalam 6 kelompok, tiap kelompok 5 ekor tikus. Kelompok I (kontrol hepatotoksin) diberi karbon tetraklorida 2 ml/kg BB. Kelompok II (kontrol negatif) diberi olive oil 2 ml/kg BB. Kelompok III (kontrol dekok) diberi dekok herba Bidens pilosa L. 2 g/kgBB. Kelompok IV-VI (kelompok perlakuan) diberi dekok herba Bidens pilosa L. satu kali sehari selama enam hari dengan dosis 0,5; 1; dan 2 g/kgBB, kemudian pada hari ke-7 diinduksi karbon tetraklorida 2 ml/kgBB. Pada jam ke-24 setelah pemberian karbon tetraklorida dilakukan pemeriksaan aktivitas serum ALT dan AST pada semua kelompok perlakuan. Data aktivitas serum ALT dan AST dianalisis menggunakan one way ANOVA dengan taraf kepercayaan 95% dan dilanjutkan uji Scheffe atau uji T berpasangan.
Hasil penelitian ini menunjukkan bahwa pemberian dekok herba Bidens pilosa L. memiliki efek hepatoprotektif dengan menurunkan aktivitas serum ALT dan AST. Efek hepatoprotektif yang dihasilkan dari dosis terendah ke dosis tertinggi sebesar 71,5; 85,8; 44,0%. Dari data diperoleh dosis efektif pemberian dekok herba Bidens pilosa L., yaitu 1 g/kgBB.
ABSTRACT
The aim of study research were to prove long-term administration of
Bidens pilosa L. herb decoction in female Wistar rats induced carbon tetrachloride, and the effective dose.
This research use female Wistar rats, aged 2-3 months, and the weight 120-200 grams. Rats were randomly divided into six groups, each group had five rats. Group I (control hepatotoxins) induced by carbon tetrachoride 2 mL/kgBW. Group II (negative control) were given olive oil 2 ml/kgBW. Group III (control decoction) were given decoction of herbs Bidens pilosa L. 2 g/kg. Group IV-VI (treatment group) were given Bidens pilosa L. herb decoction once a day for six days with a dose started from 0.5; 1; and 2 g/kgBW, then in seventh day the group induced by carbon tetrachloride 2 ml/ kgBW. At the 24th hours after administrated of carbon tetrachloride, ALT and AST activities were examinated in all treatment groups. Data ALT and AST activities were analyzed using one-way ANOVA with 95% significancy level and continued with Scheffe test or paired t test.
The results showed that administration of Bidens pilosa L. herb decoction has a hepatoprotective effect by lowering ALT and AST activities. Hepatoprotective effects from the lowest to the highest doses were 71.5; 85.8; 44.0%. From the data, the effective dose of Bidens pilosa L. herb decoction were 1 g/kgBW.
1 BAB I PENGANTAR
A. Latar Belakang
Hati merupakan organ terbesar yang memiliki peranan penting dalam
fungsi fisiologis tubuh. Hati dianggap sebagai organ metabolisme utama yang
memiliki berbagai fungsi, yaitu proses metabolisme karbohidrat, protein, lemak,
pengaturan koagulasi dan detoksifikasi dari substansi toksik (The Association of Physicians of India, 2012). Organ hati memiliki resiko yang cukup besar untuk mengalami kerusakan yang akan mengakibatkan terganggunya fungsi fisiologi
tubuh. Kerusakan tersebut dapat disebabkan oleh infeksi virus hepatitis, infeksi
bakteri, zat-zat toksik seperti alkohol (Roberts, 2010).
Perlemakan hati (steatosis) merupakan salah satu bentuk kerusakan hati. Pada perlemakan hati terjadi penumpukan trigliserida dalam bentuk droplet di
dalam sitoplasma sel hepatosit (Schattner and Knobler, 2008). Perlemakan hati
dapat disebabkan oleh penyakit hati alkoholik maupun penyakit hati non
alkoholik/non alcoholic fatty liver disease (NAFDL). Pada saat ini, perlemakan hati non alkoholik banyak ditemukan pada populasi masyarakat di negara
berkembang dan negara maju. Berdasarkan data epidemiologi, negara bagian barat
memiliki prevalensi NAFLD populasi dewasa sekitar 20-40%. Pada beberapa
negara Asia juga dilaporkan prevalensi NAFDL sekitar 5-40%, tergantung negara yang diteliti (Sari, 2012). Di Indonesia, prevalensi NAFDL diperkirakan sekitar
Indonesia memiliki keanekaragaman hayati yang berpotensi sebagai
tanaman obat. Di masyarakat penggunaan bahan alam untuk pengobatan
dipandang lebih ekonomis dan lebih aman dibandingkan pengobatan dengan
menggunakan bahan kimia. Salah satu tanaman yang berpotensi sebagai tanaman
obat adalah ketul (Bidens pilosa Linn.). Tanaman ini merupakan tanaman terna (berbatang lunak) yang berasal dari Amerika. Tanaman ini biasanya tumbuh di
dekat air, kebun atau ladang, halaman rumah, dan pinggiran jalan (Sugiarto dan
Putera, 2008). Penelitian yang dilakukan Kviencinski, et al. (2011) melaporkan bahwa penggunaan fraksi etil asetat herba Bidens pilosa L. selama sepuluh hari memiliki efek hepatoprotektif. Menurut Ariyanti (2007) herba Bidens pilosa L. mengandung senyawa flavonoid yang bersifat sebagai antioksidan. Senyawa
antioksidan diduga memiliki efek hepatoprotektif. Berdasarkan pemaparan di atas
peneliti tertarik untuk melakukan penelitian efek hepatoprotektif dengan
menggunakan dekok herba Bidens pilosa L. Pemilihan sediaan dekok, karena dekok mendekati cara pemakaian di masyarakat dengan cara direbus dengan air.
Selain itu, karena senyawa flavonoid bersifat polar sehingga dapat tersari
menggunakan pelarut air (Andersen and Markham, 2006).
Pada penelitian ini pemberian jangka panjang praperlakuan dilakukan
dengan jangka waktu enam hari berturut-turut mengacu kepada model penelitan
yang dilakukan oleh Rahmamurti (2013) mengenai “Efek Hepatoprotektif Ekstrak
Etanol-Air Daun Macaranga tanarius L. pada Tikus Terinduksi Karbon Tetraklorida : Kajian terhadap Praperlakuan Jangka Panjang. Karbon tetraklorida
kerusakan hati. Hepatotoksisitas karbon tetraklorida disebabkan oleh metabolit
triklorometil (•CCl3) yang merupakan radikal bebas yang dapat mengikat
lipoprotein dan menyebabkan peroksidasi lipid (Dongare, Dhande and Kadam,
2013). Adanya pengikatan lipoprotein dan peroksidasi lipid ini dapat
menyebabkan kerusakan hati berupa perlemakan hati (steatosis). Berdasarkan jenis kerusakan hati yang terjadi, karbon tetraklorida digunakan sebagai senyawa
model pada penelitian ini.
Ketoksikan karbon tetraklorida dapat menyebabkan perubahan sifat fisik
dan kimia dari membran sel yang akan mempengaruhi permeabilitas membran sel
sehingga dapat menyebabkan kebocoran enzim (Dongare, et al., 2013). Kerusakan hati ditandai dengan peningkatan kadar enzim ALT dan AST (Fleiser, 2009).
Berdasarkan pemaparan di atas, perlu dilakukan penelitian mengenai pengaruh
efek hepatoprotektif dekok herba Bidens pilosa L. pada tikus yang terinduksi karbon tetraklorida dengan melihat perubahan aktivitas ALT dan AST.
1. Perumusan masalah
a. Apakah pemberian jangka panjang dekok herba Bidens pilosa L. mempunyai efek hepatoprotektif dengan menurunkan aktivitas serum ALT
dan AST pada tikus betina galur Wistar terinduksi karbon tetraklorida?
2. Keaslian penelitian
Penelitian menggunakan herba Bidens pilosa L. pernah dilakukan oleh Ariyanti (2000) yang melaporkan mengenai aktivitas antioksidan fraksi air ekstrak
metanolik dengan mengunakan metode DPPH. Dari penelitan tersebut, dilaporkan
ekstrak metanol memiliki IC50 sebesar 44,77 µL/mL dan fraksi air sebesar 97,40
µg/mL. Penelitian lain melaporkan bahwa herba Bidens pilosa L. mengandung metabolit utama polyacetylene dan flavonoid yang berkhasiat dalam mengobati penyakit, seperti hiperglikemik, hipertensi, hepatoprotektif,
anti-inflamasi, dan lain-lain (Silva, et al., 2011). Penelitian Kviencinski, et al. (2011) mengenai aktivitas antioksidan dan efek hepatoprotektif dari fraksi etil asetat
herba Bidens pilosa L. di Brazil yang menunjukkan bahwa herba Bidens pilosa L. memiliki efek hepatoprotektif.
Sejauh penelusuran pustaka yang dilakukan peneliti, penelitian mengenai
“Efek Hepatoprotektif Pemberian Jangka Panjang Dekok Herba Bidens pilosa L.
terhadap Aktivitas Serum ALT-AST pada Tikus Betina Terinduksi Karbon
Tetraklorida” belum pernah dilakukan.
2. Manfaat penelitian
a. Manfaat teoritis
Hasil penelitian ini diharapkan mampu memberikan informasi terkait
ilmu pengetahuan khususnya bidang kefarmasian mengenai pengaruh
b. Manfaat praktis
Hasil penelitian ini diharapkan mampu memberikan informasi terkait
dosis efektif pemberian dekok herba Bidens pilosa L. bagi masyarakat khususnya sebagai hepatoprotektor jangka panjang.
B. Tujuan Penelitian 1. Tujuan umum
Untuk mengetahui efek hepatoprotektif pemberian dekok herba Bidens pilosa L. pada tikus betina galur Wistar.
2. Tujuan khusus
a. Mengetahui efek hepatoprotektif pemberian jangka panjang dekok herba
Bidens pilosa L.terhadap penurunan aktivitas serum ALT dan AST pada tikus betina galur Wistar terinduksi karbon tetraklorida.
b. Mengetahui dosis efektif pemberian jangka panjang dekok herba Bidens pilosa L.terhadap aktivitas serum ALT dan AST yang dapat memberikan efek hepatoprotektif optimal pada tikus betina galur Wistar terinduksi
BAB II
PENELAAHAN PUSTAKA
A. Hati 1. Anatomi fisiologi hati
Hati merupakan salah satu organ terbesar di dalam tubuh dengan berat
sekitar 1500 gram. Hati terletak dalam rongga perut sebelah kanan, berwarna
merah kecokelatan dengan konsistensi lunak (Wibowo, 2008). Bagian atas hati
berbentuk cembung, terletak di bawah kubah kanan diafragma. Bagian bawah hati
berbentuk cekung, di bawahnya terdapat ginjal kanan, lambung, pankreas, dan
usus (Baradero, Daydrit, dan Siswadi, 2008).
Gambar 1. Anatomi hati (Watson, 2014).
Hati dibagi menjadi dua lobus utama, kiri dan kanan (gambar 1).
Permukaan atas berbentung cembung dan terletak di bawah diafragma sedangkan
permukaan bawah tidak rata dan memperlihatkan lekukan fisura transversus.
longitudinal memisahkan lobus kanan dan kiri permukaan bawah, sedangkan
ligamen falsiformis memisahkan lobus kanan dan kiri permukaan atas. Hati dibagi
mejadi empat lobus (kanan, kiri, kaudata, dan kuadrata) yang terdiri atas lobulus.
Lobulus ini berbentuk polihedral (segi banyak) yang terdiri atas sel hati berbentuk
kubus, dan cabang-cabang pembuluh darah yang diikat bersama oleh jaringan hati
(Pearce, 2009).
Di dalam lobulus terdapat sel-sel hati (hepatosit) yang tersusun seperti
lapisan-lapisan plat. Pada setiap segi dari lobules terdapat cabang-cabang vena
porta, arteri hepatika, dan kanalikuli empedu. Di antara deretan sel-sel hati
terdapat sinusoid yang membawa darah dari cabang-cabang vena porta dan arteri
hepatika ke vena hepatika. Pada dinding sinusoid terdapat sel-sel fagosit yang
disebut sel Kupffer. Sel Kupffer ini memiliki fungsi utama menelan eristrosit, leukosit yang mati, mikroorganisme, dan benda asing yang masuk dalam hati
(Baradero, dkk., 2008).
Hati mempunyai peranan penting dan memiliki berbagai macam fungsi di
dalam tubuh. Fungsi-fungsi utama hati, yaitu membantu menjaga keseimbangan
glukosa darah (metabolisme karbohidrat), membantu pembentukan protein
terutama albumin, membantu metabolisme protein (tempat menyusun asam amino
menjadi protein, memproduksi sebagian besar protein plasma, memproduksi
faktor pembekuan darah, mengubah amonia menjadi urea), penyimpanan
vitamin/zat besi, memproduksi dan mensekresikan empedu, membantu
metabolisme lemak (memproduksi dan merombak kolesterol menjadi garam
2. Jenis kerusakan hati a. Steatosis
Steatosis merupakan akumulasi lemak pada hepatosit yang menunjukkan terjadinya kerusakan hati pada banyak kasus penyakit hati. Steatosis dikategorikan menjadi dua, yaitu makrovesikular dan microvesikular. Steatosis makrovesikular terjadi ketika satu atau beberapa droplet lemak hampir mengisi hepatosit
sedangkan mikrovesikular terjadi ketika ditemukan sejumlah droplet kecil yang
membuat hepatosit tampak berbusa. Steatosis pada orang dewasa umumnya terjadi karena penyakit hati alkoholik (Kelly, 2008). Selain itu, steatosis juga dapat disebabkan oleh hepatotoksin karbon tetraklorida. Hepatotoksin karbon
tetraklorida menyebabkan steatosis makrovesikular (Rubin, Strayer and Rubin, 2011).
b. Nekrosis
Nekrosis (kematian sel) dapat terjadi karena cedera sel langsung,
gangguan fungsi intraseluler, atau cedera langsung oleh sistem imun yang
dimediasi oleh kerusakan membran. Nekrosis hati dapat disebabkan oleh alkohol,
CCl4, brombenzena, dan berilium. Alkohol menyebabkan nekrosis periportal
(zona 1) karena alkohol dehidrogenase yang diangkut oleh darah kontak pada
daerah ini. Nekrosis mid zona (zona 2), disebabkan oleh berilium. Nekrosis zona 3
(nekrosis sentrilobular) disebabkan oleh aktivitas metabolisme senyawa toksin
c. Kolestasis
Kolestasis adalah penurunan atau penyumbatan aliran empedu yang
dapat menyebabkan kulit dan putih mata tampak berwarna kuning, kulit, urine
gelap, serta tinja dapat berwarna terang dan berbau busuk. Pada orang yang
mengalami kolestasis, aliran empedu (cairan pencernaan yang dihasilkan oleh
hati) terganggu di beberapa titik antara sel-sel hati dan usus dua belas jari (segmen
pertama dari usus kecil). Ketika aliran empedu terhenti, pigmen bilirubin (produk
limbah yang terbentuk ketika sel-sel darah merah tua atau rusak dipecah) lolos ke
dalam aliran darah dan menumpuk. Hal ini dapat terjadi karena gangguan hati,
saluran empedu, dan pankreas (Porter, 2009)
d. Sirosis
Sirosis adalah bentuk kerusakan akhir dari penyakit hati yang disebabkan
oleh berbagai penyebab. Penyebab yang paling umum adalah hepatotoksin seperti
alkohol, infeksi hepatitis virus, dan gangguan empedu primary sclerosing cholangitis (PSC). Kondisi ini ditandai dengan disfungsi hepatosit dengan pembentukan jaringan fibrosa, diikuti oleh nodul regeneratif (Mahkad, Hoey,
Lakkaraju and Bhuskute, 2012).
3. Hepatotoksin
Senyawa atau obat-obat yang dapat menyebabkan kerusakan hati
a. Hepatotoksin intrinsik
Senyawa yang memiliki efek hepatotoksik hampir pada seluruh populasi
yang terpejankan senyawa tersebut. Senyawa ini bergantung pada dosis
pemberian. Contohnya: parasetamol, karbon tetraklorida, dan alkohol.
b. Hepatotoksin idiosinkratik
Senyawa yang memiliki efek hepatotoksik pada sebagian kecil populasi
yang terpejankan senyawa tersebut. Beberapa bergantung pada dosis pemberian,
dan frekuensi kejadiannya sangat jarang. Contoh-contoh zat termasuk isoniazid, sulfonamida, valproat, dan fenitoin
(Friedman and Keeffe, 2012).
4. ALT-AST
Aminotransferase adalah enzim-enzim yang mengkatalisis konversi α -ketoacid menjadi asam amino melalui transfer dari satu residu amino. Aspartat aminotransferase (AST) mengkatalisis transfer residu 2-amino dari aspartat
menjadi 2-oksoglutarat, menghasilkan glutamat dan oksaloasetat. Alanin
aminotransferase (ALT) mengkatalisis transfer residu amino dari alanin
2-oksoglutarat, membentuk glutamat dan piruvat (Dancygier, 2010). Kisaran normal
AST adalah 0-40 IU/L, sedangkan ALT adalah 0-45 IU/L. Pemeriksaan kadar
ALT dan AST dapat digunakan sebagai indikator kerusakan atau kematian sel hati
yang sedang terjadi (Dickerson, 2006).
Serum normal aminotransferase mencerminkan pergantian sel fisiologis.
Pada penyakit hati peningkatan serum bukan terjadi karena peningkatan sintesis
oleh kematian sel hati atau kerusakan hati dengan peningkatan permeabilitas
membran hepatoseluler. Oleh karena itu, ALT dan AST dapat digunakan sebagai
indikator yang sensitif dari kerusakan hepatoselular. ALT dan AST digunakan
sebagai parameter diagnostik dasar untuk menilai dan memantau penyakit hati.
ALT adalah indikator yang relatif spesifik penyakit hati, yang hadir dalam cedera
sel bahkan kecil (Dancygier, 2010).
ALT sebagian besar ditemukan di hati, aktivitas ALT di hati lebih
spesifik, yaitu sepuluh kali lipat aktivitas di jantung atau otot rangka. Pada tingkat
selular, ALT di simpan dalam sitosol hepatosit sedangkan AST di dalam
mitokondria (70%) dan sitoplasma (30%) (Dancygier, 2010). Pada kasus
ekstrahepatik (infark miokard, gangguan otot, dan trauma) yang menyebabkan
peningkatan transaminase harus dikesampingkan, terutama AST. Rasio AST :
ALT > 1 biasanya menunjukkan kerusakan hati yang diinduksi alkohol dan rasio
AST : ALT < 1 menunjukkan kerusakan hati yang disebabkan virus. Tingkat
transaminase tertinggi ditemukan pada hepatitis akut (AST dan ALT> 10x upper limit of normal (ULN). Pada jaundice obstruktif, tingkat transaminase selalu naik, tetapi umumnya tetap pada tingkat <10 x ULN. Tingkat transaminase yang cukup
tinggi dapat menunjukkan berbagai penyakit hati yang disebabkan oleh alkohol,
obat yang menginduksi kerusakan hati, hepatitis kronis yang disebabkan virus,
sirosis hati, dan kongesti hati (Siegenthaler, 2007).
5. Evaluasi kerusakan hati
Evaluasi kerusakan hati dapat dilakukan dengan beberapa cara di
a. Uji aktivitas enzim serum
Evaluasi dilakukan dengan mengukur aktivitas enzim pada serum
aminotransferase, alkalin fosfatase, laktat dehidrogenase. Pengujian aktivitas
enzim menggambarkan fungsi hati. Serum aminotransferase merupakan indikator
yang sensitif dari cedera pada sel-sel hati dan berguna dalam mendeteksi penyakit
hati akut seperti hepatitis. Alanin aminotransferase (ALT), aspartat
aminotransferase (AST), dan gamma - glutamil transferase (GGT) adalah tes yang
paling sering digunakan dari kerusakan hati. Aktivitas ALT akan meningkat pada
gangguan hati dan dapat digunakan untuk memantau hepatitis, sirosis, dan efek
dari pengobatan yang mungkin beracun untuk hati. Serum AST ada dalam
jaringan yang memiliki aktivitas metabolik yang tinggi. Oleh karena itu, AST
akan meningkat saat terjadi kerusakan atau kematian jaringan organ seperti
jantung, hati, otot rangka, dan ginjal. Meskipun tidak spesifik untuk penyakit hati,
tingkat AST dapat meningkat pada sirosis, hepatitis, dan kanker hati. Peningkatan
kadar GGT berhubungan dengan kolestasis, tetapi juga dapat disebabkan oleh
penyakit hati alkoholik (Smeltzer, Bare, Hinkle and Cheever, 2009).
b. Ujiekskretori hepatik
Bilirubin adalah produk ekskretori hati yang dibentuk dari katabolisme
heme. Bilirubin diglukuronide dibentuk dengan bantuan konjugasi oleh hati yang
kemudian dieksresikan melalui kantong empedu (Vasudevan, Srekumari, and
Vaidyanathan, 2013). Pengukuran bilirubin dalam darah dan urin biasanya
digunakan untuk menilai transportasi anion hati, meskipun banyak anion lain,
c. Uji kadar protein serum
Hati mensintesis hampir semua protein plasma kecuali imunoglobulin.
Serum albumin secara kuantitatif merupakan protein penting yang disintesis oleh
hati, dan mencerminkan sejauh mana sel-sel hati masih berfungsi. Albumin
memiliki waktu paruh sekitar 20 hari, sehingga dalam semua penyakit kronis hati,
tingkat albumin akan menurun. Tingkat albumin normal dalam darah adalah 3,5
sampai 5 g/dL (Vasudevan, et al., 2013). d. Biopsi liver
Biopsi hati merupakan pengambilan sejumlah kecil jaringan hati yang
akan digunakan untuk pemeriksaan sel-sel hati di laboratorium. Biasanya yang
paling umum adalah untuk mengevaluasi gangguan menyebar dari parenkim dan
mendiagnosa ruang yang menempati lesi. Biopsi hati sangat berguna ketika
temuan klinis dan uji laboratorium tidak diagnostik (Smeltzer, et al., 2009).
B. Karbon Tetraklorida
Karbon tetraklorida (CCl4) merupakan pelarut yang digunakan secara luas
pada alat pemadam kebakaran, produk pembersih, dan produksi refrigeran
fluorocarbon. Pada tahun 1960 dan 1970-an penggunaan karbon tetraklorida
mengalami penurunan karena penemuan penyakit hati pada pekerja yang terpapar
(misalnya petugas toko dry cleaning), namun karbon tetraklorida masih digunakan di beberapa industri. CCl4 juga digunakan di laboratorium toksikologi karena
kemampuannya untuk menginduksi hepatotoksisitas intrinsik dan peroksidasi lipid
pada spesies yang beragam. Karbon tetraklorida juga merupakan polutan
sekitar. Sebagai zat yang sangat volatile, paparan sering terjadi melalui rute
inhalasi, walaupun kasus keracunan domestik kecelakaan juga terjadi dan
biasanya melibatkan karbon tetraklorida konsumsi melalui saluran gastrointestinal
(Burcham, 2014).
Karbon tetraklorida dapat menyebabkan nekrosi centrilobular hati dan
perlemakan hati. Senyawa ini memiliki efek utama toksik pada hati, terlepas dari
cara pemberian. Administrasi atau paparan kronis menyebabkan sirosis hati,
tumor hati dan juga kerusakan ginjal. Alasan untuk hati menjadi target utama
adalah bahwa toksisitas karbon tetraklorida tergantung pada aktivasi metabolik
oleh sitokrom P-450. Oleh karena itu, hati menjadi target karena mengandung
konsentrasi terbesar sitokrom P-450, terutama di wilayah centrilobular yang mana
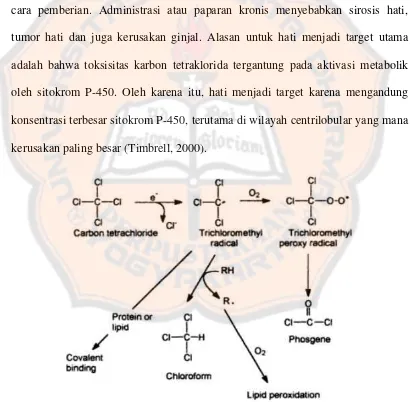
[image:36.595.102.512.276.678.2]kerusakan paling besar (Timbrell, 2000).
Gambar 2. Mekanisme biotransformasi karbon tetraklorida (Timbrell, 2000).
Bioaktivitas dari karbon tetraklorida tergantung dari dehalogenasi reduksi
metabolisme karbon tetraklorida menjadi triklorometil (•CCl3) yang bersifat
radikal bebas (Bateman, Jefferson, Thomas, Thompson, and Vale, 2014). Radikal
bebask triklorometil (gambar 2). dapat berikatan dengan komponen sel hati yang
berefek pada penghambatan sekresi lipoprotein. Hal ini menyebabkan menumpuk
lemak di hati (steatosis) (Manahan, 2002). Radikal bebas yang berinteraksi dengan lipid akan menyebabkan peroksidasi lipid yang dapat menganggu fungsi
sel dan integritas membran serta kematian sel. Triklorometil lalu akan bereaksi
dengan molekul oksigen membentuk radikal triklorometilperoksi (•OOCCL3)
yang lebih reaktif. Selain itu, radikal triklorometilperoksi dapat bereaksi lebih
lanjut untuk menghasilkan fosgen, yang dapat berinteraksi dengan jaringan
[image:37.595.104.510.287.642.2]makromolekul menghasilkan asam klorida dan karbondioksida (Bateman, et al., 2014).
Gambar 3. Mekanisme peroksidasi lipid oleh radikal CCl3 (Manahan, 2002).
Peroksidasi lipid merupakan proses oksidasi lemak tak jenuh melalui
reaksi radikal bebas membentuk lemak terperoksidasi (LOOH). Mekanisme
(gambar 3). Lemak terperoksidasi merupakan molekul tidak stabil yang dapat
terurai menghasilkan radikal bebas tambahan. Proses ini berakhir ketika radikal
bebas bereaksi dengan radikal bebas yang lain membentuk molekul yang stabil
[image:38.595.100.513.214.757.2](Manahan, 2002).
Tabel I. Peningkatan relatif dari beberapa serum enzim pada cedera hati
Senyawa toksik
Lesi Derajat peningkatan kadar enzim serum
Nekrosis Steatosis AST2 ALT2 OCT.SDH
CCl4 + + 4+ 3+ 4+
Tioacetamida + - 4+ 3+ 4+
Tetrasiklin - + 2 + 1+
Etionin - + + - +
Fosfor ± + 1-2+ 1-2+ 1-2+
Karbon tetraklorida dapat menyebabkan kerusakan hati berupa steatosis
(tabel I). Kerusakan hati yang disebabkan oleh karbon tetraklorida dapat dilihat
dari kenaikan aktivitas serum ALT dan AST. Pada saat terjadi steatosis terjadi peningkatan aktivitas serum ALT sebesar 3 kali normal dan aktivitas serum AST
sebesar 4 kali normal (Zimmerman, 1999).
C. Bidens pilosa Linn. 1. Taksonomi
Kingdom : Plantae
Sub Kingdom : Tracheobionta
Superdivisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Asteridae
Bangsa : Asterales
Marga : Bidens
Varietas : Bidens pilosa L.
(Bartolome, Villasenor and Yang, 2013).
2. Nama daerah
Ajeran, hareuga (Sunda), dan jaringan, ketul (Jawa) (Sugiarto dan Putera, 2008).
3. Morfologi
Tanaman Bidens pilosa Linn. merupakan tanaman terna (berbatang lunak) yang berasal dari amerika. Tanaman ini tumbuh di dekat air, kebun atau
ladang, halaman rumah, dan pinggiran jalan di ketinggian 250-2.500 meter dpl.
Tinggi tanaman ini dapat mencapai 150 cm dengan batang berbentuk segi empat
berwarna hijau. Daun terbagi tiga, berbentuk bulat telur dengan tepi bergerigi.
Bunga bertangkai panjang, mahkota bunga berwarna putih dengan putik berwarna
[image:39.595.97.515.86.703.2]kuning (gambar 4) (Sugiarto dan Putera, 2008).
4. Kandungan kimia dan kegunaan
Bidens pilosa L. memiliki berbagai macam kandungan kimia, seperti
polyacetylene, glikosida polyacetylene, auron, glikosida auron, turunan asam p-kumarat, turunan caffeoylquinic acid, flavonoid, glikosida flavonoid, seskuiterpen,
pheophytin, dan terpen (Bairwa, Kumar, Sharma, and Roy, 2010). Berdasarkan senyawa-senyawa yang dilaporkan, polyacetylene dan flavonoid merupakan golongan metabolit khas yang mendominasi pada genus Bidens. Tanaman Bidens pilosa L. telah dikenal luas sebagai obat tradisional di berbagai negara. Di Martinique, Cina dan Brazil, Bidens pilosa L. digunakan sebagai obat tradisional untuk mengobati berbagai penyakit, seperti diare, diabetes, peradangan, enteritis,
disentri basiler, dan faringitis (Silva, et al., 2011).
Beberapa ekstrak dan fraksi yang diperoleh dari Bidens pilosa L. memiliki aktivitas tertentu. Oleh karena itu, beberapa konstituen terisolasi dari
tanaman telah dipelajari mengacu pada efek anti-inflamasi, imunosupresif,
hepatoprotektif, anti-bakteri, anti-jamur, antioksidan, anti-malaria, dan anti-kanker
(Silva, et al., 2011). Senyawa bioaktif Bidens pilosa L. yang berperan untuk melindungi hati adalah flavonoid. Senyawa flavonoid pada Bidens pilosa L. dilaporkan memiliki aktivitas antioksidan yang berkorelasi terhadap efek
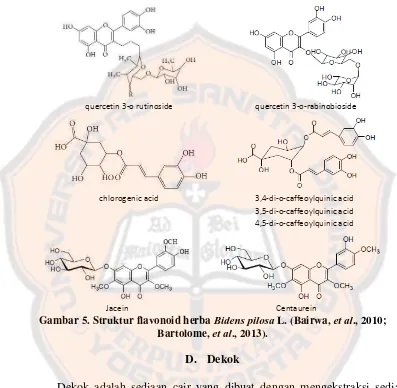
3,5-di-o-caffeoylquinic acid; 4,5-di-o-3,5-di-o-caffeoylquinic acid) (gambar5) (Bartolome, et al., 2013).
quercetin 3-o rutinoside quercetin 3-o-rabinobioside
chlorogenic acid 3,4-di-o-caffeoylquinic acid
3,5-di-o-caffeoylquinic acid
4,5-di-o-caffeoylquinic acid
[image:41.595.99.496.167.555.2]
Jacein Centaurein
Gambar 5. Struktur flavonoid herba Bidens pilosa L. (Bairwa, et al., 2010; Bartolome, et al., 2013).
D. Dekok
Dekok adalah sediaan cair yang dibuat dengan mengekstraksi sediaan
herbal dengan air pada suhu 90°C selama 30 menit. Dekok dapat dibuat dengan
cara mencampur simplisia dengan derajat halus yang sesuai dalam panci dengan
air secukupnya. Pemanasan dilakukan di atas penangas air selama 30 menit
terhitung sejak mencapai suhu 90°C yang disertai dengan pengadukan.
Penyerkaian dilakukan menggunakan kain flanel yang disertai dengan
menambahkan air panas secukupnya melalui ampas hingga diperoleh volume
E. Landasan Teori
Hati merupakan organ metabolisme yang memiliki peranan penting di
dalam tubuh manusia. Salah satu peranan penting hati di dalam tubuh adalah
mendetoksifikasi senyawa-senyawa toksik yang masuk ke dalam tubuh (Seifter,
Ratner and Sloane, 2005). Jika terjadi kerusakan pada organ hati maka fungsi di
dalam tubuh akan terganggu. Kerusakan pada sel-sel hati dapat disebabkan oleh
zat kimia toksik seperti alkohol, virus hepatitis, dan obat-obatan tertentu
(Kaplowitz and Deleve, 2013).
Herba Bidens pilosa L. memiliki berbagai macam kandungan kimia, bahkan tanaman ini telah dikenal luas dibeberapa negara sebagai obat tradisional.
Tanaman ini mengandung senyawa flavonoid yang diduga berperan dalam efek
hepatoprotektif. Pada penelitian ini digunakan sediaan dekok karena mudah
diaplikasikan di masyarakat dan senyawa flavonoid herba Bidens pilosa L. yang bersifat polar dapat tersari menggunakan air.
Karbon tetraklorida digunakan sebagai senyawa model untuk mengetahui
efek hepatoprotektif dekok herba Bidens pilosa L. Senyawa ini dipilih berdasarkan efek hepatotoksiknya yang dapat menyebabkan steatosis. Pada saat terjadi steatosis hati, aktivitas serum ALT dan AST akan meningkat (Kelly, 2008). Pemberian dekok herba Bidens pilosa L. yang mengandung senyawa flavonoid diharapkan dapat memiliki efek hepatoprotektif dengan menurunkan
F. Hipotesis
Dekok herba Bidens pilosa L. memiliki efek hepatoprotektif dengan menurunkan aktivitas ALT dan AST pada tikus betina galur Wistar terinduksi
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan
rancangan acak lengkap pola searah.
B. Variabel dan Definisi Operasional 1. Variabel utama
a. Variabel bebas
Variabel bebas penelitian ini adalah variasi dosis dalam pemberian
jangka panjang dekok herba Bidens pilosa L. b. Variabel tergantung
Variabel tergantung penelitian ini adalah efek hepatoprotektif.
2. Variabel pengacau
a. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah kondisi hewan
uji, yaitu tikus betina galur Wistar dengan berat badan 120-200 g; umur 2-3
bulan; cara pemberian hepatotoksin secara per oral; cara pemberian herba
Bidens pilosa L. secara per oral; frekuensi pemberian dekok herba Bidens pilosa L. satu kali sehari selama enam hari berturut-turut dengan waktu pemberian yang sama dan herba Bidens pilosa L. yang diperoleh dari Dusun Jenengan, Desa Maguwoharjo, Kecamatan Depok, Kabupaten Sleman,
b. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah kondisi
patologis tikus betina galur Wistar yang digunakan sebagai hewan uji.
3. Definisi operasional
a. Herba Bidens pilosa L.
Herba Bidens pilosa L. adalah semua bagian tumbuhan di atas tanah (batang, daun, bunga, dan buah herba Bidens pilosa L.).
b. Dekok herba Bidens pilosa L.
Dekok herba Bidens pilosa L. dengan konsentrasi 16% didapatkan dengan cara merebus 16,0 g serbuk kering herba Bidens pilosa L. dalam 100,0 ml aquadest pada suhu 90°C selama 30 menit.
c. Efek hepatoprotektif
Efek hepatoprotekif adalah kemampuan dekok herba Bidens pilosa L. pada dosis tertentu untuk menurunkan aktivitas serum ALT dan AST pada
tikus betina galur Wistar terinduksi karbon tetraklorida.
d. Jangka panjang
Jangka panjang adalah pemberian dekok herba Bidens pilosa L. satu kali sehari selama enam hari berturut-turut.
C. Bahan Penelitian 1. Bahan utama
a. Hewan uji yang digunakan dalam penelitian ini adalah tikus betina galur
diperoleh dari Laboratorium Hayati Imono, Fakultas Farmasi, Universitas
Sanata Dharma, Yogyakarta.
b. Bahan uji yang digunakan adalah herba Bidens pilosa L. yang diperoleh dari Dusun Jenengan, Desa Maguwoharjo, Kecamatan Depok, Kabupaten
Sleman, Daerah Istimewa Yogyakarta.
2. Bahan kimia
a. Bahan hepatotoksin yang digunakan adalah karbon tetraklorida (Merck®).
b. Pelarut hepatotoksin karbon tetraklorida dan kontrol negatif yang
digunakan adalah olive oil yang diperoleh dari PT. Brataco Chemika, Yogyakarta.
c. Pelarut untuk dekok digunakan aquadest yang diperoleh dari Laboratorium
Farmakognosi-Fitokimia, Fakultas Farmasi, Universitas Sanata Dharma,
Yogyakarta.
d. Blanko pengukuran aktivitas serum ALT dan AST menggunakan aqua
bidestilata yang diperoleh dari Laboratorium Kimia Analisis dan
Instrumental, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
e. Reagen ALT yang digunakan adalah reagen ALT DiaSys. Komposisi dan
[image:46.595.173.452.611.743.2]konsentrasi dari reagen ALT adalah sebagai berikut:
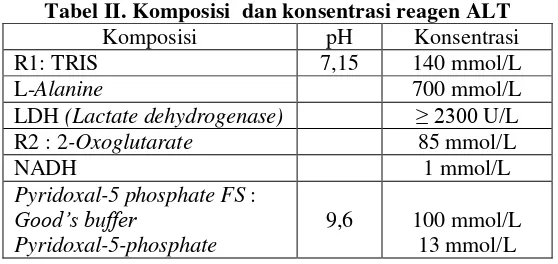
Tabel II. Komposisi dan konsentrasi reagen ALT
Komposisi pH Konsentrasi
R1: TRIS 7,15 140 mmol/L
L-Alanine 700 mmol/L
LDH (Lactate dehydrogenase) ≥ 2300 U/L
R2 : 2-Oxoglutarate 85 mmol/L
NADH 1 mmol/L
Pyridoxal-5 phosphate FS :
Good’s buffer
Pyridoxal-5-phosphate
9,6 100 mmol/L
f. Reagen AST yang digunakan adalah reagen AST DiaSys. Komposisi dan
[image:47.595.100.513.164.597.2]konsentrasi dari reagen AST adalah sebagai berikut:
Tabel III. Komposisi dan konsentrasi reagen AST
Komposisi pH Konsentrasi
R1: TRIS 7,65 110 mmol/L
L-Aspartate 320 mmol/L
MDH (Malate dehydrogenase) ≥ 800 U/L
LDH (Lactate dehydrogenase) ≥ 1200 U/L
R2 : 2-Oxoglutarate 65 mmol/L
NADH 1 mmol/L
Pyridoxal-5 phosphate FS :
Good’s buffer
Pyridoxal-5-phosphate
9,6 100 mmol/L
13 mmol/L
D. Alat Penelitian 1. Alat pembuatan serbuk herba Bidens pilosa L.
Alat-alat yang digunakan antara lain oven, mesin penyerbuk, dan ayakan.
2. Alat pembuatan dekok herba Bidens pilosa L.
Panci lapis alumunium, thermometer, stopwatch, beaker glass, gelas ukur, labu takar, corong, batang pengaduk, cawan porselen, penangas air,
timbangan analitik Mettler Toledo®, kain flannel.
3. Alat uji penetapan kadar air
Moisture balance, beaker glass, sendok.
4. Alat uji hepatoprotektif
Seperangkat alat gelas berupa beaker glass, gelas ukur, tabung reaksi, pipet tetes, labu takar, batang pengaduk Pyrex Iwaki Glass®, timbangan analitik Mettler Toledo®, sentrifuge Centurion Scientific®, vortex Genie Wilten®, spuit injeksi per oral, spuit injeksi i.p., pipa kapiler, micropipette,
E. Tata Cara Penelitian 1. Determinasi tanaman herba Bidens pilosa L.
Determinasi dilakukan dengan mencocokkan morfologi tanaman herba
Bidens pilosa L. dengan menggunakan buku acuan (Backer, 1963).
2. Pengumpulan bahan uji
Bahan uji yang digunakan adalah herba Bidens pilosa L. yang meliputi semua bagian tumbuhan di atas tanah (batang, daun, bunga, dan buah), dipilih
yang masih bagus dan terhindar dari penyakit pada bulan Juli 2014.
3. Pembuatan serbuk herba Bidens pilosa L.
Herba Bidens pilosa L. dicuci bersih, dipotong-potong, dan dikeringkan. Setelah itu oven pada suhu 50°C selama 48 jam. Setelah benar-benar kering,
herba diserbuk dan diayak menggunakan ayakan nomor mesh 40.
4. Penetapan kadar air serbuk herba Bidens pilosa L.
Serbuk herba Bidens pilosa L. dimasukkan ke dalam alat moisture balance sebanyak 5 g, lalu diratakan. Bobot serbuk tersebut ditetapkan sebagai bobot sebelum pemanasan, setelah itu dipanaskan pada suhu 1050C.
Serbuk yang telah dipanaskan ditimbang kembali lalu dihitung sebagai bobot
setelah pemanasan. Kadar air serbuk diperoleh menggunakan rumus:
5. Pembuatan dekok herba Bidens pilosa L.
di atas heater pada suhu 90°C selama 30 menit, dihitung ketika suhu campuran mencapai 90°C. Dekok lalu disaring menggunakan kain flanel,
tambahkan aquadest panas melalui ampas rebusan hingga volume 100,0 mL
pada labu takar.
6. Pembuatan hepatotoksin karbon tetraklorida 50%
Hepatotoksin karbon tetraklorida 50% dibuat dengan cara mencampur
larutan karbon tetraklorida dan olive oil dengan perbandingan volume 1:1.
7. Uji pendahuluan
a. Penetapan dosis hepatotoksin karbon tetraklorida
Berdasarkan penelitian Al-Olayan, et al., (2014) ditetapkan dosis hepatotoksin karbon tetraklorida sebesar 2 mL/kgBB yang diberikan secara
intraperitoneal. Pemilihan dosis hepatotoksik ini karena pada dosis tersebut telah menyebabkan kerusakan sel-sel hati pada tikus galur Wistar yang
ditunjukkan dengan peningkatan aktivitas serum ALT dan AST, namun
belum menyebabkan kematian. Hal ini juga didukung oleh penelitian
Wijayanti (2013) yang melaporkan induksi karbon tetraklorida 2 mL/kgBB
mampu meningkatkan ALT dan AST tiga kali dari aktivitas serum awal.
b. Penetapan dosis dekok herba Bidens pilosa L.
Penetapan dosis dekok herba Bidens pilosa L. dihitung berdasarkan berat badan tertinggi hewan uji tikus, ½ volume maksimal secara per oral pada
D x BB = C x V
D x BB tertinggi tikus (kgBB) = C dekok (g/mL) x ½ Vmaks
D x 200 g/kgBB = 0,16 g/mL x 2,5 mL
D = 2 g/kgBB
Dosis tertinggi 2 g/kgBB digunakan sebagai dosis III. Peringkat dosis
lainnya dihitung dengan menggunakan faktor kelipatan 2, sehingga
didapatkan dosis I sebesar 0,5 g/kgBB dan dosis II sebesar 1 g/kgBB.
c. Penetapan waktu pencuplikan darah
Penetapan waktu pencuplikan darah ditentukan melalui orientasi pada
jam ke - 0, 24, dan 48, dibuat kelompok orientasi masing-masing 5 ekor tikus.
Setiap ekor tikus diambil darahnya melalui sinus orbitalis mata menggunakan pipa kapiler pada jam ke-0, 24, dan 48 setelah pemejanan hepatotoksin
karbon tetraklorida. Kemudian diukur aktivitas serum ALT dan AST.
8. Pengelompokkan dan perlakuan hewan uji
Sejumlah 30 ekor tikus dibagi secara acak ke dalam 6 kelompok
perlakuan, masing-masing sejumlah lima ekor tikus. Pengelompokkan dan
perlakuan hewan uji, yaitu sebagai berikut :
a. Kelompok I (kontrol hepatotoksin) diberi hepatotoksin karbon tetraklorida
b. Kelompok II (kontrol negatif) diberi olive oil dengan dosis 2 mL/kgBB secara intraperitoneal. Setelah 24 jam darah hewan uji diambil melalui
sinus orbitalis mata, lalu diukur aktivitas serum ALT dan AST.
c. Kelompok III (kontrol dekok) diberi dekok herba Bidens pilosa L. dosis tertinggi, yaitu 2 g/kg BB selama enam hari berturut-turut secara p.o.
Setelah 24 jam darah hewan uji diambil melalui sinus orbitalis mata, lalu diukur aktivitas serum ALT dan AST.
d. Kelompok IV (dosis I) diberi dekok herba Bidens pilosa L. dosis 0,5 g/kgBB selama enam hari berturut-turut secara p.o.
e. Kelompok V (dosis II) diberi dekok herba Bidens pilosa L. dosis 1 g/kgBB selama enam hari berturut-turut secara p.o.
f. Kelompok VI (dosis III) diberi dekok herba Bidens pilosa L. dosis 2 g/kgBB selama enam hari berturut-turut secara p.o.
Pada hari ke tujuh kelompok IV, V, dan VI diberi hepatotoksin karbon
tetraklorida 2 mL/kgBB secara intraperitoneal dengan waktu yang sama dengan pemberian dekok. Setelah 24 jam darah hewan uji diambil melalui
sinus orbitalis mata, lalu diukur aktivitas serum ALT dan AST.
9. Pembuatan serum
Setiap tikus diambil darahnya melalui sinus orbitalis mata menggunakan pipa kapiler, ditampung dalam tabung Eppendorf. Darah yang telah diambil didiamkan selama 15 menit, lalu disentrifugasi pada kecepatan 8000 rpm
disentrifugasi kembali pada kecepatan 8000 rpm selama 10 menit. Bagian
supernatan diambil menggunakan micropipette.
10. Pengukuran aktivitas serum ALT dan AST
Pengukuran aktivitas serum ALT-AST dilakukan menggunakan
Microlab-200 Merck® di Laboratorium Biokimia Fisiologi Manusia, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta. Aktivitas serum ALT-AST
diukur pada panjang gelombang 340 nm, dan dinyatakan dengan satuan U/L.
Pengukuran serum ALT dilakukan dengan cara mencampur 100 µL
serum dengan 1000 µL reagen 1, lalu divortex dan didiamkan selama
operating time 2 menit. Reagen 2 ditambahkan sebanyak 250 µL, lalu divortex dan diukur setelah didiamkan selama operating time 1 menit. Pengukuran serum AST dilakukan dengan cara mencampur 100 µL serum
dengan 1000 µL reagen 1, lalu divortex dan didiamkan selama operating time
2 menit. Reagen 2 ditambahkan sebanyak 250 µL, lalu divortex dan diukur
setelah didiamkan selama operating time 1 menit.
F. Tata Cara Analisis Hasil
Data aktivitas serum ALT dan AST diuji dengan Saphiro-Wilk untuk mengetahui distribusi data dan analisis varian (uji Levene’s) untuk mengetahui homogenitas varian antar kelompok hewan uji. Jika data terdistribusi normal dan
bermakna (p>0,05). Pada satu kelompok yang memiliki dua data berhubungan,
kebermaknaan dilakukan dengan uji T berpasangan dengan taraf kepercayaan
95%.
Perhitungan efek hepatoprotektif terhadap hepatotoksin karbon
BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini bertujuan untuk mengetahui pengaruh pemberian dan besar
dosis efektif hepatoprotektif dari dekok herba Bidens pilosa L. pada tikus betina galur Wistar terinduksi karbon tetraklorida, yaitu dengan melihat aktivitas serum
ALT dan AST. Efek hepatoprotektif ditunjukkan dengan adanya penurunan
aktivitas serum ALT dan AST setelah pemberian herba Bidens pilosa L. pada tikus betina galur Wistar yang terinduksi karbon tetraklorida.
A. Penyiapan Bahan 1. Hasil determinasi tanaman
Determinasi tanaman bertujuan untuk memastikan bahwa tanaman yang
digunakan dalam penelitian adalah herba Bidens pilosa L., sehingga tidak terjadi kesalahan dalam penyiapan bahan. Determinasi dilakukan di Laboratorium
Farmakognosi-Fitokimia, Fakultas Farmasi, Universitas Sanata Dharma,
Yogyakarta. Determinasi tanaman dilakukan hingga tingkat spesies dengan cara
mencocokan kesamaan makroskopis tanaman dengan menggunakan buku acuan
Backer (1963). Bagian tanaman yang dideterminasi, yaitu batang, daun, bunga,
dan buah. Dari hasil determinasi, dipastikan bahwa batang, daun, bunga, dan buah
yang digunakan adalah benar dari tanaman Bidens pilosa L. (lampiran 4).
2. Penetapan kadar air serbuk herba Bidens pilosa L.
Penetapan kadar air bertujuan untuk mengetahui apakah serbuk herba
1995). Penetapan kadar air dilakukan dengan metode gravimetri dengan menggunakan alat moisture balance. Serbuk dipanaskan di dalam alat pada suhu 105oC selama 15 menit, setelah itu dilakukan perhitungan terhadap kadar air
serbuk herba Bidens pilosa L. Hasil perhitungan menunjukkan bahwa serbuk herba Bidens pilosa L. memiliki kadar air sebesar 8,614%, maka serbuk herba
Bidens pilosa L. memenuhi syarat kadar air serbuk simplisia yang baik.
B. Uji Pendahuluan 1. Penentuan dosis hepatotoksin
Pada penelitian ini senyawa model hepatotoksin yang digunakan adalah
karbon tetraklorida. Penentuan dosis karbon tetraklorida bertujuan untuk
mengetahui berapa dosis karbon tetraklorida yang dapat menyebabkan kerusakan
hati pada tikus yang ditunjukkan dengan peningkatan aktivitas serum ALT dan
AST. Kenaikan serum ALT sebanyak 3 kali dan AST 4 kali lipat menjukkan
terjadinya steatosis (Zimmerman, 1999). Dosis karbon tetraklorida yang digunakan pada penelitian ini mengacu pada penelitian Al-Olayan, et al., (2014) yang melaporkan pada dosis 2 mL/kgBB telah dapat menginduksi hepatotoksik
pada tikus tanpa menyebabkan kematian.
2. Penentuan dosis herba Bidens pilosa L.
Penentuan dosis dekok dihitung berdasarkan konsentrasi tertinggi herba
Bidens pilosa L. yang dapat dibuat, yaitu 16%. Berdasarkan konsentrasi tersebut,
dosis tertinggi yang dapat dibuat yaitu 2 g/kgBB. Pada penelitian ini digunakan 3
peringkat dosis dengan faktor kelipatan 2 sehingga dosis rendah 0,5 g/kgBB, dosis
3. Penentuan waktu pencuplikan darah hewan uji
Penentuan waktu pencuplikan bertujuan untuk mengetahui waktu karbon
tetraklorida dosis 2 mL/kgBB menimbulkan ketoksikan yang maksimal,
ditunjukkan dengan peningkatan aktivitas serum ALT dan AST tertinggi pada
selang waktu tertentu. Karbon tetraklorida dosis 2 mL/kgBB diberikan secara i.p
pada tikus, kemudian dilakukan pencuplikan darah pada selang waktu 0, 24, dan
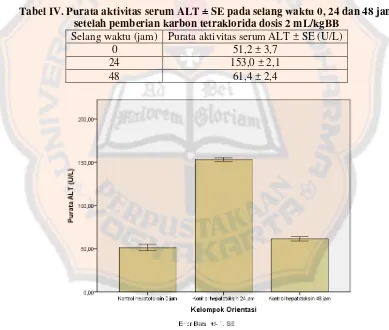
[image:56.595.105.494.302.632.2]48 jam. Hasil uji aktivitas serum ALT ditampilkan pada tabel IV dan gambar 6.
Tabel IV. Purata aktivitas serum ALT ± SE pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB
Selang waktu (jam) Purata aktivitas serum ALT ± SE (U/L)
0 51,2 ± 3,7
24 153,0 ± 2,1
48 61,4 ± 2,4
Gambar 6. Diagram batang purata aktivitas serum ALT pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mg/kgBB
Hasil analisis statistik serum ALT menunjukkan distribusi data normal
dan variansi data homogen, sehingga data dapat dianalisis menggunakan analisis
menunjukkan nilai signifikansi sebesar 0,000 (p<0,05), yang berarti bahwa
terdapat perbedaan bermakna antar kelompok. Oleh karena itu, untuk melihat
perbedaan antar kelompok dilanjutkan dengan uji Scheffe. Hasil uji Scheffe
[image:57.595.99.514.231.579.2]aktivitas serum ALT ditampilkan pada tabel V.
Tabel V. Hasil uji Scheffe aktivitas serum ALT pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB
Selang waktu (jam) Jam ke-0 Jam ke-24 Jam ke-48
0 BB BTB
24 BB BB
48 BTB BB
Keterangan:
BB = Berbeda bermakna (p<0,05), BTB = Berbeda tidak bermakna (p>0,05)
Dari tabel IV dan gambar 6 terlihat bahwa aktivitas serum ALT yang
paling tinggi ditunjukkan pada jam ke-24 (153,0 ± 2,1 U/L). Jika dibandingkan
dengan jam ke-0 (51,2 ± 3,7 U/L) aktivitas serum ALT mengalami kenaikan
sekitar 3 kali, sedangkan pada pencuplikan darah ke-48 (61,4 ± 2,4 U/L) aktivitas
serum ALT telah mengalami penurunan. Hal ini juga ditunjukkan pada tabel V,
aktivitas serum ALT pada jam ke-0 memiliki perbedaan yang tidak bermakna
terhadap jam ke-48, yang berarti bahwa aktivitas serum ALT pada jam ke-48 telah
kembali normal seperti pada jam ke-0.
Tabel VI. Purata aktivitas serum AST ± SE pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB
Selang waktu (jam) Purata aktivitas serum AST ± SE (U/L)
0 109,0 ± 4,6
24 425,6 ± 10,4
Gambar 7. Diagram batang purata aktivitas serum AST pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mg/kgBB
Hasil analisis statistik serum AST menunjukkan distribusi data normal
dan variansi data homogen, sehingga data dapat dianalisis menggunakan analisis
variansi satu arah. Hasil analisis variansi satu arah dari data aktivitas serum AST
menunjukkan nilai signifikansi sebesar 0,000 (p<0,05), yang berarti bahwa
terdapat perbedaan bermakna antar kelompok. Oleh karena itu, untuk melihat
perbedaan antar kelompok dilanjutkan dengan uji Scheffe. Hasil uji Scheffe
aktivitas serum ALT ditampilkan pada tabel VII.
Tabel VII. Hasil uji Scheffe aktivitas serum AST pada selang waktu 0, 24 dan 48 jam setelah pemberian karbon tetraklorida dosis 2 mL/kgBB
Selang waktu (jam) Jam ke-0 Jam ke-24 Jam ke-48
0 BB BB
24 BB BB
48 BB BB
Keterangan:
BB = Berbeda bermakna (p<0,05)
Dari tabel VI dan gambar 7 terlihat bahwa aktivitas serum AST yang
dengan jam ke-0 (109,0 ± 4,6 U/L) aktivitas serum AST mengalami kenaikan
sekitar 4 kali, sedangkan pada pencuplikan darah ke-48 (150,6 ± 7,0 U/L)
aktivitas serum AST telah mengalami penurunan.
Berdasarkan hasil aktivitas serum ALT dan AST pada penelitian ini,
karbon tetraklorida memiliki efek hepatotoksik yang paling tinggi pada jam ke-24,
sehingga waktu pencuplikan darah yang digunakan dalam penelitian ini adalah
jam ke-24 setelah pemberian karbon tetraklorida 2 mL/kgBB secara
intraperitoneal.
C. Hasil Uji Efek Hepatoprotektif Dekok Herba Bidens pilosa L.
Pada penelitian ini dilihat efek hepatoprotektif dari dekok herba Bidens pilosa L. pada tiga peringkat dosis, yaitu peringkat dosis terkecil sebesar 0,5 g/kgBB, dosis tengah sebesar 1 g/kgBB, dan dosis tertinggi sebesar 2 g/kgBB.
Pemberian dekok herba Bidens pilosa L. dilakukan secara peroral selama enam hari turut-turut, kemudian pada hari ke tujuh diberikan hepatotoksin karbon
tetraklorida dosis 2 ml/kgBB secara intraperitoneal. Efek hepatoprotektif ditunjukkan dengan penurunan aktivitas serum ALT dan AST. Data aktivitas
[image:59.595.96.515.264.623.2]serum ALT dan AST ditampilkan dalam bentuk purata ± SE pada tabel VIII,
Tabel VIII. Purata ± SE aktivitas serum ALT dan AST tikus betina galur Wistar pada kelompok perlakuan
Kelompok Perlakuan
Purata aktivitas serum ALT ± SE (U/L)
Purata aktivitas serum AST ± SE (U/L)
Efek hepato-protektif (ALT) Efek hepato-protektif (AST) I Kontrol hepatotoksin karbon tetraklorida 2 mL/kgBB
174,4 ± 2,9 409,6 ± 7,8 0% 0%
II
Kontrol negatif olive oil 2 ml/kgBB
57,2 ± 3,1 101,8 ± 3,8 100% 100%
III
Kontrol DHBP 2 g/kgBB
55,4 ± 2,3 98,2 ± 4,2 - -
IV DHBP 0,5 g/kgBB + karbon tetraklorida 2 mL/kgBB
90,6 ± 3,2 164,8 ± 5,0 71,5% 79,5%
V DHBP 1 g/kgBB + karbon tetraklorida 2 mL/kgBB
73,8 ± 2,5 132,6 ± 4,2 85,8% 90%
VI DHBP 2 g/kgBB + karbon tetraklorida 2 mL/kgBB
122,8 ± 3,6 213,0 ± 5,5 44,0% 63,9%
Gambar 8. Diagram batang purata aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan
Gambar 9. Diagram batang purata aktivitas serum AST tikus betina galur Wistar pada kelompok perlakuan
Data aktivitas serum ALT dan AST dianalisis dengan uji Shapiro-Wilk
menunjukkan bahwa distribusi data normal dengan signifikansi (p>0,05). Data
aktivitas serum ALT dan AST juga menunjukkan tidak adanya variansi data antar
sehingga data dilanjutkan dengan analisis variansi satu arah. Hasil analisis
variansi satu arah aktivitas ALT dan AST menunjukkan nilai signifikansi 0,000
(p<0,005), yang berarti bahwa terdapat perbedaan bermakna antar kelompok
perlakuan. Oleh karena itu, untuk melihat perbedaan antar kelompok dilanjutkan
[image:62.595.101.528.253.635.2]dengan uji Scheffe. Hasil uji Scheffe ditampilkan pada tabel IX dan tabel X.
Tabel IX. Hasil uji Scheffe aktivitas serum ALT tikus betina galur Wistar pada kelompok perlakuan
Kelompok Perlakuan
Kontrol hepatotoksin
CCl4 2
mL/kgBB
Kontrol negatif
olive oil 2 mL/kgBB Kontrol DHBP 2 g/kgBB DHBP 0,5 g/kgBB + CCl4 2
mL/kgBB
DHBP 1 g/kgBB +
CCl4 2
mL/kgBB
DHBP 2 g/kgBB +
CCl4 2
mL/kgBB Kontrol
hepatotoksin CCl4 2
mL/kgBB
BB BB BB BB BB
Kontrol negatif olive
oil 2 mL/kgBB
BB BTB BB BB BB
Kontrol DHBP 2 g/kgBB
BB BTB BB BB BB
DHBP 0,5 g/kgBB + CCl4 2
mL/kgBB
BB BB BB BB BB
DHBP 1 g/kgBB +
CCl4 2
mL/kgBB
BB BB BB BB BB
DHBP 2 g/kgBB +
CCl4 2
mL/kgBB
BB BB BB BB BB
Keterangan:
DHBP = Dekok herba Bidens pilosa L.
Tabel X. Hasil uji Scheffe aktivitas serum AST tikus betina galur Wistar pada kelompok perlakuan Kelompok Perlakuan Kontrol hepatotoksin
CCl4 2
mL/kgBB
Kontrol negatif
olive oil 2 mL/kgBB Kontrol DHBP 2 g/kgBB DHBP 0,5 g/kgBB + CCl4 2
mL/kgBB
DHBP 1 g/kgBB +
CCl4 2
mL/kgBB
DHBP 2 g/kgBB +
CCl4 2
mL/kgBB Kontrol
hepatotoksin CCl4 2
mL/kgBB
BB BB BB BB BB
Kontrol negatif olive
oil 2 mL/kgBB
BB BTB BB BB BB
Kontrol DHBP 2 g/kgBB
BB BTB BB BB BB
DHBP 0,5 g/kgBB + CCl4 2
mL/kgBB
BB BB BB BB BB
DHBP 1 g/kgBB +
CCl4 2
mL/kgBB
BB BB BB BB BB
DHBP 2 g/kgBB +
CCl4 2
mL/kgBB
BB BB BB BB BB
Keterangan:
DHBP = Dekok herba Bidens pilosa L.
BB = Berbeda bermakna (p<0,05), BTB = Berbeda tidak bermakna (p>0,05)
1. Kontrol hepatotoksin karbon tetraklorida dosis 2 mL/kgBB
Kontrol hepatotoksin bertujuan untuk melihat kerusakan hati yang
ditimbulkan oleh hepatotoksin karbon tetraklorida dosis 2 mL/kgBB yang
diberikan secara intraperitoneal. Parameter kerusakan hati yang terjadi dilakukan dengan pengukuran aktivitas serum ALT dan AST pada jam ke-24.
Pengukuran aktivitas serum ALT dan AST pada jam ke-24 setelah
pemberian karbon tetraklorida pada jam ke-24 sebesar 174,4 ± 2,9 U/L dan 409,6
serum sebesar 3 kali dari kontrol negatif (57,2 ± 3,1 U/L) dan aktivitas AST
serum sebesar 4 kali aktivitas serum AST pada kontrol negatif (101,8 ± 3,8 U/L).
Peningkatakan aktivitas ALT serum sebesar 3 kali lipat dan AST serum sebesar 4
kali lipat terhadap nilai normal menandakan terjadinya kerusakan hati berupa
steatosis (Zimmerman, 1999).
Hasil uji Scheffe yang ditampilkan pada tabel IX dan X, menunjukkan bahwa aktivitas serum ALT dan AST kontrol hepatotoksin berbeda signifikan
dengan aktivitas ser